湖北省施恩州巴东县第三高级中学2022-2023学年高二下学期6月第四次月考化学试题(含答案)
文档属性
| 名称 | 湖北省施恩州巴东县第三高级中学2022-2023学年高二下学期6月第四次月考化学试题(含答案) |

|
|
| 格式 | doc | ||
| 文件大小 | 987.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-06-06 00:00:00 | ||
图片预览



文档简介
巴东县第三高级中学2022-2023学年高二下学期6月第四次月考
化学
考生注意:
1.本试卷分选择题和非选择题两部分。满分100分,考试时间75分钟。
2.答题前,考生务必用直径0.5毫米黑色墨水签字笔将密封线内项目填写清楚。
3.考生作答时,请将答案答在答题卡上。选择题每小题选出答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑;非选择题请用直径0.5毫米黑色墨水签字笔在答题卡上各题的答题区域内作答,超出答题区域书写的答案无效,在试题卷、草稿纸上作答无效。
4.本卷命题范围:人教版高考内容。
5.可能用到的相对原子质量:H 1 C 12 O 16 Na 23 S 32 Cu 64
一、选择题(本题共15小题,每小题3分,共计45分。在每小题列出的四个选项中,只有一项是符合题目要求的)
1.“霾尘积聚难见路人”,雾霾[含有]的形成除了与有关外,还有的参与,才能将转化为硫酸盐。下列说法不正确的是( )
A.雾霾的分散剂是空气 B.雾霾能产生丁达尔效应
C.均属于酸性氧化物 D.雾霾生成过程发生氧化还原反应
2.制造5G芯片的材料有高纯硅、等半导体材料、线型酚醛树脂等光刻胶以及用于硅材料的清洗剂——超高纯等。下列说法正确的是( )
A.线型酚醛树脂属于无机材料
B.制取反应:中,是氧化剂
C.制取高纯硅反应:属于置换反应
D.清洗硅材料表面反应为,说明是碱性氧化性
3.已知三角雉形分子a和直线形分子b反应,生成两种直线形分子c和d(组成a、b、c、d分子的元素原子序数均小于10),其结构如图所示,则下列判断错误的是( )
A.a是极性分子 B.b是最活泼的非金属单质
C.c能使紫色石蕊溶液变红色 D.d化学性质比较活泼
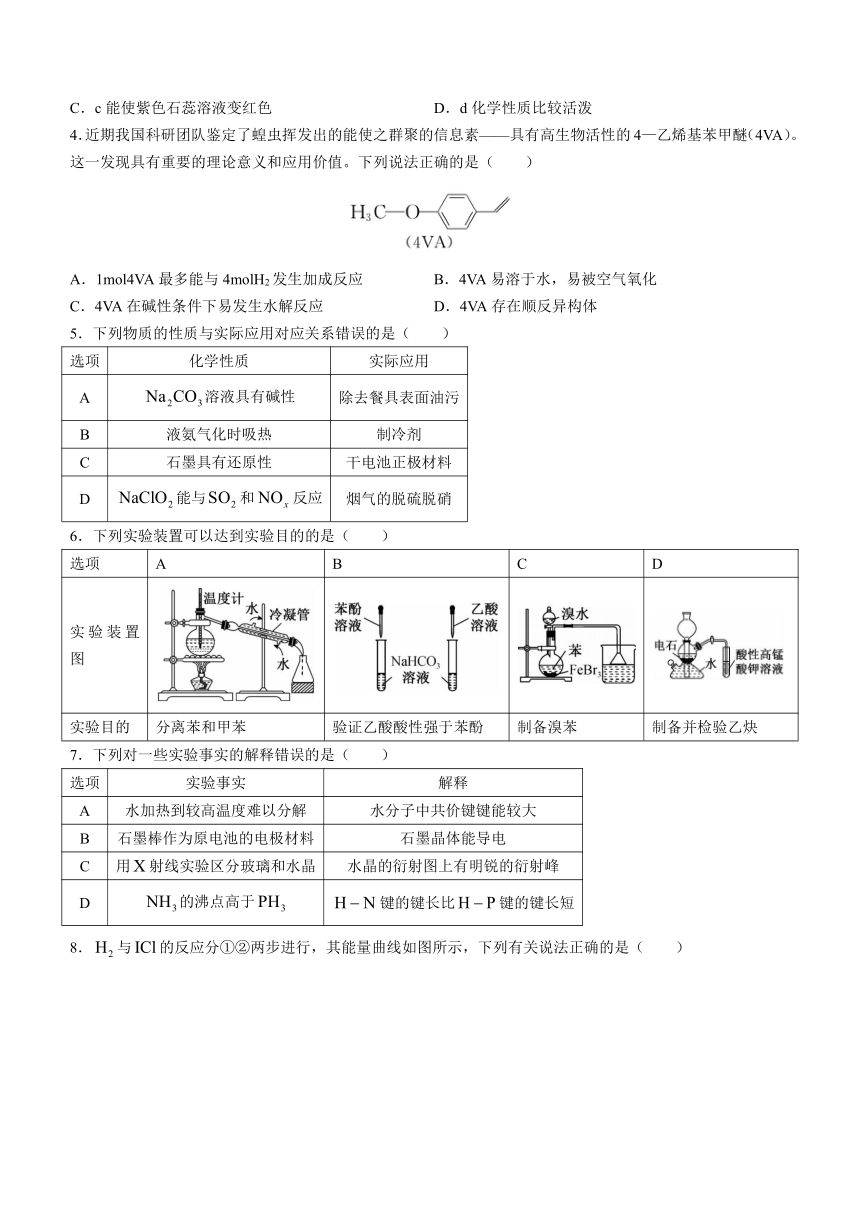
4.近期我国科研团队鉴定了蝗虫挥发出的能使之群聚的信息素——具有高生物活性的4—乙烯基苯甲醚(4VA)。这一发现具有重要的理论意义和应用价值。下列说法正确的是( )
A.1mol4VA最多能与4molH2发生加成反应 B.4VA易溶于水,易被空气氧化
C.4VA在碱性条件下易发生水解反应 D.4VA存在顺反异构体
5.下列物质的性质与实际应用对应关系错误的是( )
选项 化学性质 实际应用
A 溶液具有碱性 除去餐具表面油污
B 液氨气化时吸热 制冷剂
C 石墨具有还原性 干电池正极材料
D 能与和反应 烟气的脱硫脱硝
6.下列实验装置可以达到实验目的的是( )
选项 A B C D
实验装置图
实验目的 分离苯和甲苯 验证乙酸酸性强于苯酚 制备溴苯 制备并检验乙炔
7.下列对一些实验事实的解释错误的是( )
选项 实验事实 解释
A 水加热到较高温度难以分解 水分子中共价键键能较大
B 石墨棒作为原电池的电极材料 石墨晶体能导电
C 用射线实验区分玻璃和水晶 水晶的衍射图上有明锐的衍射峰
D 的沸点高于 键的键长比键的键长短
8.与的反应分①②两步进行,其能量曲线如图所示,下列有关说法正确的是( )
A.反应①、反应②均为吸热反应
B.活化能:反应①<反应②
C.反应速率:反应①>反应②
D.
9.常温下,将浓度均为的一元酸和分别与的溶液等体积混合,混合后溶液的依次为9、7。下列说法错误的是( )
A.HX为弱酸 B.常温下,的溶液的为1
C.前者混合液中 D.后者混合液中
10.为阿伏加德罗常数的值。下列说法正确的是( )
A.由和组成的混合物中含阴、阳离子总数为
B.乙酸与乙醇在浓硫酸作用下,生成乙酸乙酯分子数为
C.反应,每生成转移电子数
D.体积均为(标准状况下)的乙烷与苯含氢原子数均为
11.化合物丙是制备解痉药奥昔布宁的中间体,其合成路线如下。下列说法正确的是( )
A.化合物甲易溶于水 B.甲→乙的反应类型为加成反应
C.化合物乙和丙互为同系物 D.等物质的量的甲、丙消耗的物质的量不同
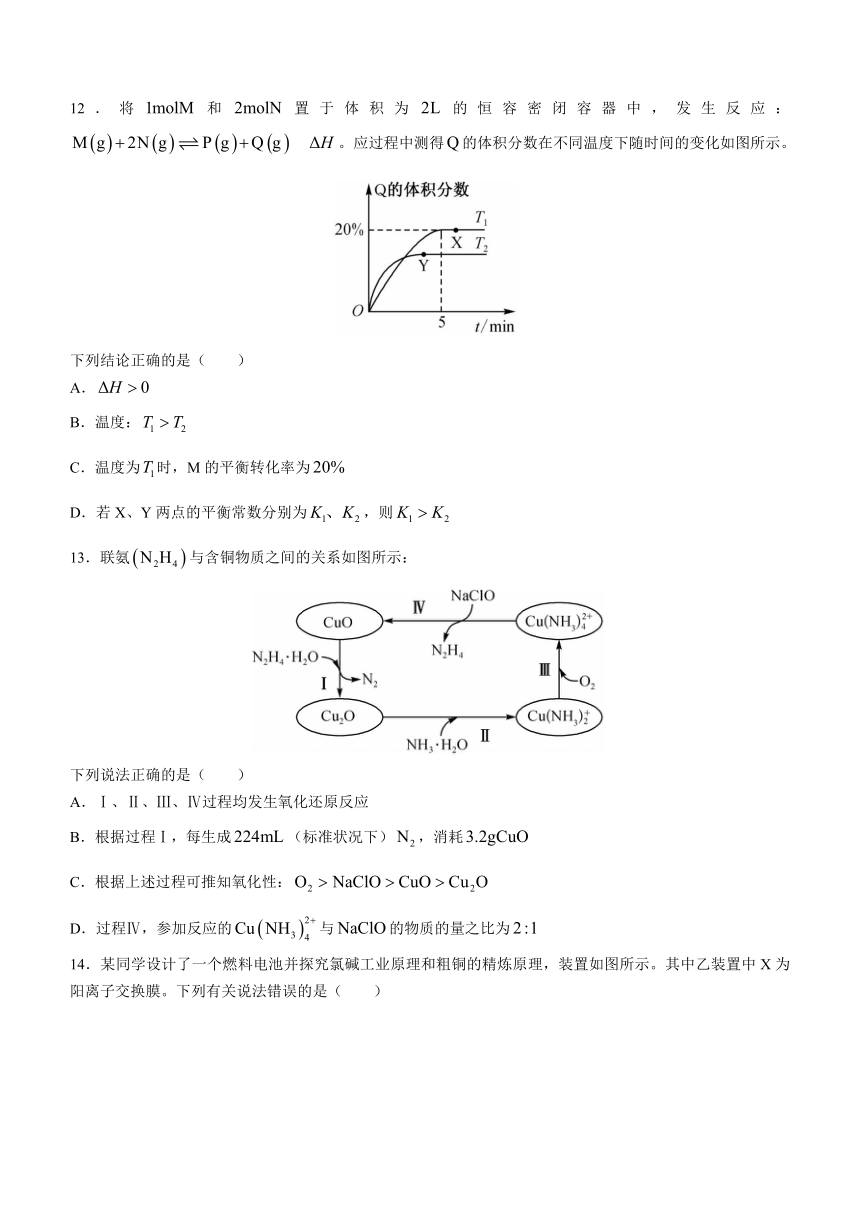
12.将和置于体积为的恒容密闭容器中,发生反应:。应过程中测得的体积分数在不同温度下随时间的变化如图所示。
下列结论正确的是( )
A.
B.温度:
C.温度为时,M的平衡转化率为
D.若X、Y两点的平衡常数分别为,则
13.联氨与含铜物质之间的关系如图所示:
下列说法正确的是( )
A.Ⅰ、Ⅱ、Ⅲ、Ⅳ过程均发生氧化还原反应
B.根据过程Ⅰ,每生成(标准状况下),消耗
C.根据上述过程可推知氧化性:
D.过程Ⅳ,参加反应的与的物质的量之比为
14.某同学设计了一个燃料电池并探究氯碱工业原理和粗铜的精炼原理,装置如图所示。其中乙装置中X为阳离子交换膜。下列有关说法错误的是( )
A.通入的极为正极,该电极反应式为
B.乙装置中铁电极为阴极,电极反应式为
C.反应一段时间后,乙装置中在铁电极区生成氢氧化钠溶液
D.反应一段时间后,丙装置中硫酸铜溶液浓度可能减小
15.乙二胺四乙酸又叫EDTA,是一种良好的配合剂,常用于测定金属离子的含量。已知:ED-TA的结构如图。下列叙述正确的是( )
A.EDTA中氮原子杂化方式为
B.EDTA与金属离子形成配合物时,碳原子提供孤电子对
C.EDTA分子中既含有键又含有键
D.EDTA是共价化合物,属于共价晶体
二、非选择题(本题共4小题,共55分)
16.(16分)氮的许多重要化合物在半导体材料及炸药等方面用途非常广泛。回答下列问题:
(1)是一种半导体材料。基态原子的核外电子排布式为________;基态原子电子占据的最高能级符号为________,其电子云轮廓图为________形。
(2)是一种炸药,可通过下列方法合成:。
(1)属于________晶体,其中阴离子中氮原子的杂化方式是________,该阴离子的空间构型为________。
(2)和中原子的杂化方式________(填“相同”或“不同”);键角:________(填“大于”“小于”或“等于”)。
17.(11分)新冠病毒已经给人类带来巨大灾难。研究表明,过氧乙酸能有效地杀灭病毒。一种制备过氧乙酸工艺流程如下:
回答下列问题:
(1)“电解”发生反应为。在电解过程中,理论上电路中转移电子,将生成________(标准状况下)。
(2)“水解”时又生成了,写出该反应的化学方程式:________________。
(3)分离溶液时,采取“减圧蒸馏”,目的是________________。
(4)“合成”反应为可逆反应,写出该反应的化学方程式:________________。
(5)过氧乙酸浓度测定
取过氧乙酸溶液,用硫酸使溶液酸化,再用浓度为的标准溶液滴定其中的(),耗用的标准溶液的体积为(滴定过程中不与过氧乙酸反应)。
另取待测液,加入过量的,并用硫酸使溶液酸化,此时过氧乙酸和残留的都能跟反应生成(;)。再用浓度为的标准溶液滴定生成的(),耗用的体积为。过氧乙酸的浓度为________(用含的代数式表示)。
18.(14分)的排放是形成酸雨的重要原因之一,工业上可采用多种方法减少的排放。回答下列问题:
(1)还原法:
已知:;
。
则和反应生成和的热化学方程式为________________。
(2)碘循环法:其循环过程如图所示。反应①的化学方程式为________________,在整个循环系统中做催化剂的物质是________(填化学式)。
(3)钠碱循环法:用的溶液吸收尾气中的。
①上述溶液中:________;________。
(2)室温下,当溶液的约为6时,溶液吸收能力显著下降,此时溶液中的浓度是,则此时溶液中各离子浓度由大到小的顺序为________。
(4)氨石灰水法:
第一步:用过量的浓氨水吸收,并在空气中氧化;
第二步:加入澄清石灰水。
已知:室温下,,,则室温下,第二步反应:的平衡常数________。
19.(14分)有机物Ⅰ是合成药物的重要中间体,Ⅰ的一种合成路线如下:
已知:ⅰ.;
ⅱ.。
回答下列问题:
(1)C的结构简式是________;B中官能团的名称是________;C生成D的反应类型为________。
(2)下列说法正确的是________(填字母)。
a.C可发生消去反应
b.最多能与反应
c.与反应类型相同
(3)写出反应的化学方程式:________________。
(4)写出一种同时符合下列条件的化合物的同分异构体的结构简式:________________。
①能与氯化铁溶液发生显色反应;②核磁共振氢谱显示4组吸收峰。
(5)参照上述合成路线,设计以为原料制备A的合成路线:________________(其他无机试剂任选)。
巴东县第三高级中学2022-2023学年高二下学期6月第四次月考
化学
参考答案、提示及评分细则
1.C 雾霾的分散剂是空气,A项正确;雾霾是气凝胶,能产生丁达尔效应,项正确;不属于酸性氧化物,C项错误;由生成发生氧化还原反应,D项正确。
2.C 线型酚醛树脂属于合成有机高分子,A项错误;既不是氧化剂又不是还原剂,B项错误;根据置换反应特点知,C项正确;是酸性氧化物,D项错误。
3.D 由组成a、b、c、d分子的元素原子序数均小于10及a为三角雉形分子可知a为,组成c的元素除氢外另一元素为价的氟,故为,c为,d为,属于极性分子,A项正确;是最活泼的非金属单质,B项正确;水溶液呈酸性,C项正确;分子中含有氮氮三键,化学性质稳定,D项错误。
4.A 最多能与发生加成反应,A项正确;4-乙烯基苯甲醚(4VA)是蝗虫挥发出的能使之群聚的信息素,不易溶于水且不易被空气氧化,B项错误;4-乙烯基苯甲醚(4VA)含有碳碳双键和醚键,不能发生水解反应,C项错误;中的碳碳双键一端碳原子上连接两个氢原子,不存在顺反异构体,D项错误。
5.C 溶于水,水解产生的与油脂发生皂化反应,项正确;液氨气化吸热,可作制冷剂,B项正确;干电池中石墨棒起导电作用,C项错误;利用的强氧化性将氧化为和除去,D项正确。
6.B 分离苯和甲苯的混合溶液应选择蒸馏,蒸馏时,温度计水银球应在蒸馏烧瓶支管口下沿处,A项错误;乙酸可以与碳酸氢钠溶液发生反应,而苯酚不能与碳酸氢钠溶液发生反应,则可以验证乙酸酸性强于苯酚,B项正确;溴苯应用苯与液溴在催化下反应制备,而不是用溴水,C项错误;制备乙炔应用饱和食盐水与电石反应且不能使用启普发生器,并且反应产物中有等杂质,检验前应先用硫酸铜溶液除去杂质,D项错误。
7.D 水加热到较高温度难以分解,说明水中存在的化学键较强,键能较大,A项正确;石墨晶体能导电,可作电极材料,B项正确;晶体的X射线衍射图中有明锐的衍射峰,C项正确;非金属氢化物的熔沸点与分子间作用力和氢键有关,与键长无关,分子间能形成氢键,分子间不能形成氢键,故的沸点高于,D项错误。
8.D 根据图像,反应①②中反应物的总能量大于生成物的总能量,均是放热反应,A项错误;反应①正反应的活化能大于反应②的,反应速率:反应①<反应②,B、C两项错误;根据盖斯定律知,反应①、反应②的焓变之和,D项正确。
9.C 等浓度、等体积的和溶液混合后,混合溶液的为9,溶液呈碱性,说明为弱酸,A项正确;后者混合溶液的,说明为强酸,即的溶液的为1,B项正确;前者混合溶液中,因为,故,C项错误;后者混合溶液中,因为,故,D项正确。
10.A 和摩尔质量相等,且阴阳离子数之比为,所以由和组成的混合物中含阴、阳离子总数为,A项正确;乙酸与乙醇发生酯化反应是可逆反应,B项错误;由反应中化合价的变化可知,每生成转移电子数,C项错误;标准状况下,乙烷为气态,苯为液态,D项错误。
11.B 由结构简式可知,化合物甲含有酯基,不易溶于水,A项错误;由流程可知,甲→乙的反应产物只有乙,没有小分子生成,反应类型为加成反应,B项正确;乙中含有酯基,丙中含有羧基,C项错误;化合物甲分子中含有的酯基和化合物丙分子中含有的羧基能与氢氧化钠溶液反应,所以等物质的量的甲、丙消耗的氢氧化钠的物质的量相同,D项错误。
12.D 先拐先平数值大,,温度升高,的体积分数减小,平衡逆向移动,说明,A、B两项错误;温度为时,设的变化量为,根据反应:
初始: 1 2 0 0
变化:
平衡:
温度为,平衡时的体积分数
解得
的平衡转化率为,C项错误;对于放热反应,温度越低平衡常数越大,则,D项正确。
13.B 过程Ⅱ无化合价的变化,A项错误;反应Ⅰ:,由方程可知,,,B项正确;上述过程中,无法推知与的氧化性强弱,C项错误;过程Ⅳ反应:,D项错误。
14.A 甲装置为燃料电池,通的极为正极,电解质为,电极反应式为,A项错误;通的极为负极,即电极为阴极,电极反应式为,B项正确;根据B项的分析及为阳离子交换膜,允许通过知,反应一段时间后,乙装置中铁电极区生成溶液,C项正确;根据上述分析,精铜作阴极,电极反应式为,粗铜作阳极,电极反应式为,但粗铜中含有比活泼的金属,这些金属先失电子,使溶液的浓度减小,D项正确。
15.C 根据EDTA结构,氮原子杂化方式为,A项错误;EDTA与金属离子形成配合物时,或提供孤电子对,B项错误;EDTA分子中存在羧基,故既含有键又含有键,C项正确;EDTA是共价化合物,属于分子晶体,D项错误。
16.(1)或;;哑铃
(2)①离子;;平面三角形 ②相同;小于
17.(1)22.4
(2)
(3)降低蒸馏温度,防止分解
(4)
(5)
18.(1)
(2);
(3)①2.4; ②
(4)
19.(1);碳溴键、酯基;取代反应(酯化反应)
(2)b
(3)
(4)、或
(5)
化学
考生注意:
1.本试卷分选择题和非选择题两部分。满分100分,考试时间75分钟。
2.答题前,考生务必用直径0.5毫米黑色墨水签字笔将密封线内项目填写清楚。
3.考生作答时,请将答案答在答题卡上。选择题每小题选出答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑;非选择题请用直径0.5毫米黑色墨水签字笔在答题卡上各题的答题区域内作答,超出答题区域书写的答案无效,在试题卷、草稿纸上作答无效。
4.本卷命题范围:人教版高考内容。
5.可能用到的相对原子质量:H 1 C 12 O 16 Na 23 S 32 Cu 64
一、选择题(本题共15小题,每小题3分,共计45分。在每小题列出的四个选项中,只有一项是符合题目要求的)
1.“霾尘积聚难见路人”,雾霾[含有]的形成除了与有关外,还有的参与,才能将转化为硫酸盐。下列说法不正确的是( )
A.雾霾的分散剂是空气 B.雾霾能产生丁达尔效应
C.均属于酸性氧化物 D.雾霾生成过程发生氧化还原反应
2.制造5G芯片的材料有高纯硅、等半导体材料、线型酚醛树脂等光刻胶以及用于硅材料的清洗剂——超高纯等。下列说法正确的是( )
A.线型酚醛树脂属于无机材料
B.制取反应:中,是氧化剂
C.制取高纯硅反应:属于置换反应
D.清洗硅材料表面反应为,说明是碱性氧化性
3.已知三角雉形分子a和直线形分子b反应,生成两种直线形分子c和d(组成a、b、c、d分子的元素原子序数均小于10),其结构如图所示,则下列判断错误的是( )
A.a是极性分子 B.b是最活泼的非金属单质
C.c能使紫色石蕊溶液变红色 D.d化学性质比较活泼
4.近期我国科研团队鉴定了蝗虫挥发出的能使之群聚的信息素——具有高生物活性的4—乙烯基苯甲醚(4VA)。这一发现具有重要的理论意义和应用价值。下列说法正确的是( )
A.1mol4VA最多能与4molH2发生加成反应 B.4VA易溶于水,易被空气氧化
C.4VA在碱性条件下易发生水解反应 D.4VA存在顺反异构体
5.下列物质的性质与实际应用对应关系错误的是( )
选项 化学性质 实际应用
A 溶液具有碱性 除去餐具表面油污
B 液氨气化时吸热 制冷剂
C 石墨具有还原性 干电池正极材料
D 能与和反应 烟气的脱硫脱硝
6.下列实验装置可以达到实验目的的是( )
选项 A B C D
实验装置图
实验目的 分离苯和甲苯 验证乙酸酸性强于苯酚 制备溴苯 制备并检验乙炔
7.下列对一些实验事实的解释错误的是( )
选项 实验事实 解释
A 水加热到较高温度难以分解 水分子中共价键键能较大
B 石墨棒作为原电池的电极材料 石墨晶体能导电
C 用射线实验区分玻璃和水晶 水晶的衍射图上有明锐的衍射峰
D 的沸点高于 键的键长比键的键长短
8.与的反应分①②两步进行,其能量曲线如图所示,下列有关说法正确的是( )
A.反应①、反应②均为吸热反应
B.活化能:反应①<反应②
C.反应速率:反应①>反应②
D.
9.常温下,将浓度均为的一元酸和分别与的溶液等体积混合,混合后溶液的依次为9、7。下列说法错误的是( )
A.HX为弱酸 B.常温下,的溶液的为1
C.前者混合液中 D.后者混合液中
10.为阿伏加德罗常数的值。下列说法正确的是( )
A.由和组成的混合物中含阴、阳离子总数为
B.乙酸与乙醇在浓硫酸作用下,生成乙酸乙酯分子数为
C.反应,每生成转移电子数
D.体积均为(标准状况下)的乙烷与苯含氢原子数均为
11.化合物丙是制备解痉药奥昔布宁的中间体,其合成路线如下。下列说法正确的是( )
A.化合物甲易溶于水 B.甲→乙的反应类型为加成反应
C.化合物乙和丙互为同系物 D.等物质的量的甲、丙消耗的物质的量不同
12.将和置于体积为的恒容密闭容器中,发生反应:。应过程中测得的体积分数在不同温度下随时间的变化如图所示。
下列结论正确的是( )
A.
B.温度:
C.温度为时,M的平衡转化率为
D.若X、Y两点的平衡常数分别为,则
13.联氨与含铜物质之间的关系如图所示:
下列说法正确的是( )
A.Ⅰ、Ⅱ、Ⅲ、Ⅳ过程均发生氧化还原反应
B.根据过程Ⅰ,每生成(标准状况下),消耗
C.根据上述过程可推知氧化性:
D.过程Ⅳ,参加反应的与的物质的量之比为
14.某同学设计了一个燃料电池并探究氯碱工业原理和粗铜的精炼原理,装置如图所示。其中乙装置中X为阳离子交换膜。下列有关说法错误的是( )
A.通入的极为正极,该电极反应式为
B.乙装置中铁电极为阴极,电极反应式为
C.反应一段时间后,乙装置中在铁电极区生成氢氧化钠溶液
D.反应一段时间后,丙装置中硫酸铜溶液浓度可能减小
15.乙二胺四乙酸又叫EDTA,是一种良好的配合剂,常用于测定金属离子的含量。已知:ED-TA的结构如图。下列叙述正确的是( )
A.EDTA中氮原子杂化方式为
B.EDTA与金属离子形成配合物时,碳原子提供孤电子对
C.EDTA分子中既含有键又含有键
D.EDTA是共价化合物,属于共价晶体
二、非选择题(本题共4小题,共55分)
16.(16分)氮的许多重要化合物在半导体材料及炸药等方面用途非常广泛。回答下列问题:
(1)是一种半导体材料。基态原子的核外电子排布式为________;基态原子电子占据的最高能级符号为________,其电子云轮廓图为________形。
(2)是一种炸药,可通过下列方法合成:。
(1)属于________晶体,其中阴离子中氮原子的杂化方式是________,该阴离子的空间构型为________。
(2)和中原子的杂化方式________(填“相同”或“不同”);键角:________(填“大于”“小于”或“等于”)。
17.(11分)新冠病毒已经给人类带来巨大灾难。研究表明,过氧乙酸能有效地杀灭病毒。一种制备过氧乙酸工艺流程如下:
回答下列问题:
(1)“电解”发生反应为。在电解过程中,理论上电路中转移电子,将生成________(标准状况下)。
(2)“水解”时又生成了,写出该反应的化学方程式:________________。
(3)分离溶液时,采取“减圧蒸馏”,目的是________________。
(4)“合成”反应为可逆反应,写出该反应的化学方程式:________________。
(5)过氧乙酸浓度测定
取过氧乙酸溶液,用硫酸使溶液酸化,再用浓度为的标准溶液滴定其中的(),耗用的标准溶液的体积为(滴定过程中不与过氧乙酸反应)。
另取待测液,加入过量的,并用硫酸使溶液酸化,此时过氧乙酸和残留的都能跟反应生成(;)。再用浓度为的标准溶液滴定生成的(),耗用的体积为。过氧乙酸的浓度为________(用含的代数式表示)。
18.(14分)的排放是形成酸雨的重要原因之一,工业上可采用多种方法减少的排放。回答下列问题:
(1)还原法:
已知:;
。
则和反应生成和的热化学方程式为________________。
(2)碘循环法:其循环过程如图所示。反应①的化学方程式为________________,在整个循环系统中做催化剂的物质是________(填化学式)。
(3)钠碱循环法:用的溶液吸收尾气中的。
①上述溶液中:________;________。
(2)室温下,当溶液的约为6时,溶液吸收能力显著下降,此时溶液中的浓度是,则此时溶液中各离子浓度由大到小的顺序为________。
(4)氨石灰水法:
第一步:用过量的浓氨水吸收,并在空气中氧化;
第二步:加入澄清石灰水。
已知:室温下,,,则室温下,第二步反应:的平衡常数________。
19.(14分)有机物Ⅰ是合成药物的重要中间体,Ⅰ的一种合成路线如下:
已知:ⅰ.;
ⅱ.。
回答下列问题:
(1)C的结构简式是________;B中官能团的名称是________;C生成D的反应类型为________。
(2)下列说法正确的是________(填字母)。
a.C可发生消去反应
b.最多能与反应
c.与反应类型相同
(3)写出反应的化学方程式:________________。
(4)写出一种同时符合下列条件的化合物的同分异构体的结构简式:________________。
①能与氯化铁溶液发生显色反应;②核磁共振氢谱显示4组吸收峰。
(5)参照上述合成路线,设计以为原料制备A的合成路线:________________(其他无机试剂任选)。
巴东县第三高级中学2022-2023学年高二下学期6月第四次月考
化学
参考答案、提示及评分细则
1.C 雾霾的分散剂是空气,A项正确;雾霾是气凝胶,能产生丁达尔效应,项正确;不属于酸性氧化物,C项错误;由生成发生氧化还原反应,D项正确。
2.C 线型酚醛树脂属于合成有机高分子,A项错误;既不是氧化剂又不是还原剂,B项错误;根据置换反应特点知,C项正确;是酸性氧化物,D项错误。
3.D 由组成a、b、c、d分子的元素原子序数均小于10及a为三角雉形分子可知a为,组成c的元素除氢外另一元素为价的氟,故为,c为,d为,属于极性分子,A项正确;是最活泼的非金属单质,B项正确;水溶液呈酸性,C项正确;分子中含有氮氮三键,化学性质稳定,D项错误。
4.A 最多能与发生加成反应,A项正确;4-乙烯基苯甲醚(4VA)是蝗虫挥发出的能使之群聚的信息素,不易溶于水且不易被空气氧化,B项错误;4-乙烯基苯甲醚(4VA)含有碳碳双键和醚键,不能发生水解反应,C项错误;中的碳碳双键一端碳原子上连接两个氢原子,不存在顺反异构体,D项错误。
5.C 溶于水,水解产生的与油脂发生皂化反应,项正确;液氨气化吸热,可作制冷剂,B项正确;干电池中石墨棒起导电作用,C项错误;利用的强氧化性将氧化为和除去,D项正确。
6.B 分离苯和甲苯的混合溶液应选择蒸馏,蒸馏时,温度计水银球应在蒸馏烧瓶支管口下沿处,A项错误;乙酸可以与碳酸氢钠溶液发生反应,而苯酚不能与碳酸氢钠溶液发生反应,则可以验证乙酸酸性强于苯酚,B项正确;溴苯应用苯与液溴在催化下反应制备,而不是用溴水,C项错误;制备乙炔应用饱和食盐水与电石反应且不能使用启普发生器,并且反应产物中有等杂质,检验前应先用硫酸铜溶液除去杂质,D项错误。
7.D 水加热到较高温度难以分解,说明水中存在的化学键较强,键能较大,A项正确;石墨晶体能导电,可作电极材料,B项正确;晶体的X射线衍射图中有明锐的衍射峰,C项正确;非金属氢化物的熔沸点与分子间作用力和氢键有关,与键长无关,分子间能形成氢键,分子间不能形成氢键,故的沸点高于,D项错误。
8.D 根据图像,反应①②中反应物的总能量大于生成物的总能量,均是放热反应,A项错误;反应①正反应的活化能大于反应②的,反应速率:反应①<反应②,B、C两项错误;根据盖斯定律知,反应①、反应②的焓变之和,D项正确。
9.C 等浓度、等体积的和溶液混合后,混合溶液的为9,溶液呈碱性,说明为弱酸,A项正确;后者混合溶液的,说明为强酸,即的溶液的为1,B项正确;前者混合溶液中,因为,故,C项错误;后者混合溶液中,因为,故,D项正确。
10.A 和摩尔质量相等,且阴阳离子数之比为,所以由和组成的混合物中含阴、阳离子总数为,A项正确;乙酸与乙醇发生酯化反应是可逆反应,B项错误;由反应中化合价的变化可知,每生成转移电子数,C项错误;标准状况下,乙烷为气态,苯为液态,D项错误。
11.B 由结构简式可知,化合物甲含有酯基,不易溶于水,A项错误;由流程可知,甲→乙的反应产物只有乙,没有小分子生成,反应类型为加成反应,B项正确;乙中含有酯基,丙中含有羧基,C项错误;化合物甲分子中含有的酯基和化合物丙分子中含有的羧基能与氢氧化钠溶液反应,所以等物质的量的甲、丙消耗的氢氧化钠的物质的量相同,D项错误。
12.D 先拐先平数值大,,温度升高,的体积分数减小,平衡逆向移动,说明,A、B两项错误;温度为时,设的变化量为,根据反应:
初始: 1 2 0 0
变化:
平衡:
温度为,平衡时的体积分数
解得
的平衡转化率为,C项错误;对于放热反应,温度越低平衡常数越大,则,D项正确。
13.B 过程Ⅱ无化合价的变化,A项错误;反应Ⅰ:,由方程可知,,,B项正确;上述过程中,无法推知与的氧化性强弱,C项错误;过程Ⅳ反应:,D项错误。
14.A 甲装置为燃料电池,通的极为正极,电解质为,电极反应式为,A项错误;通的极为负极,即电极为阴极,电极反应式为,B项正确;根据B项的分析及为阳离子交换膜,允许通过知,反应一段时间后,乙装置中铁电极区生成溶液,C项正确;根据上述分析,精铜作阴极,电极反应式为,粗铜作阳极,电极反应式为,但粗铜中含有比活泼的金属,这些金属先失电子,使溶液的浓度减小,D项正确。
15.C 根据EDTA结构,氮原子杂化方式为,A项错误;EDTA与金属离子形成配合物时,或提供孤电子对,B项错误;EDTA分子中存在羧基,故既含有键又含有键,C项正确;EDTA是共价化合物,属于分子晶体,D项错误。
16.(1)或;;哑铃
(2)①离子;;平面三角形 ②相同;小于
17.(1)22.4
(2)
(3)降低蒸馏温度,防止分解
(4)
(5)
18.(1)
(2);
(3)①2.4; ②
(4)
19.(1);碳溴键、酯基;取代反应(酯化反应)
(2)b
(3)
(4)、或
(5)
同课章节目录
