2023年中考化学重难点突破——构成物质的微粒(含解析)
文档属性
| 名称 | 2023年中考化学重难点突破——构成物质的微粒(含解析) |  | |
| 格式 | docx | ||
| 文件大小 | 117.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-06-06 20:38:21 | ||
图片预览



文档简介
2023年中考化学重难点突破——构成物质的微粒
一、单选题
1.微粒观是认识和研究物质的基本观念。下列有关粒子结构示意图的说法不正确的是
A.①②属于不同种元素 B.③是一种具有稳定结构的原子
C.④可以用化学符号表示为Na+ D.⑤在化学反应中容易失去电子
2.化学符号“ 2H2”可以用下列微观图示表示的是
A.B.
C. D.
3.某化学反应的微观过程如图所示,下列说法错误的是
A.该反应属于化合反应
B.该反应的化学方程式为:2AB2+B2=2AB3
C.该反应尚未完全进行
D.该反应属于还原反应
4.下列关于物质结构的说法错误的是
A.金属原子的最外层电子一般少于4个,因而在化学反应中易失去电子
B.金刚石与石墨烯的性质存在明显差异是因为碳原子排列方式不同
C.金属很难被压缩,说明物质的微粒间不存在间隙
D.不同的碱却存在一些相似的化学性质,是因为它们在水溶液中都能解离出OH-
5.对原子序数为9的元素,下列说法正确的是
A.其原子结构示意图可表示为:
B.该元素的原子在化学反应中易失电子
C.该元素原子的核外电子总数为10
D.该元素的相对原子质量为9
6.原子结构示意图能简明地表示原子核外电子的排布。小云从如图微粒结构示意图中获得相关信息,你认为正确的是
A.②③属于同一种原子 B.①②属于同一种元素
C.①③表示的都是原子 D.②③表示质子数相同
7.在公园里行走,常能闻到各种花的香味,主要原因是
A.分子总在不断运动 B.分子的体积变大
C.分子的数目变多 D.分子之间的间隔变小
8.如图为四种原子的结构示意图,其中化学性质相似的一组是
A.①和② B.①和③ C.②和③ D.③和④
9.用水壶烧开水,水沸腾后壶盖被顶起,说明
A.分子是由原子构成的 B.分子的质量很小
C.分子的体积变大 D.分子间的间隔变大
10.下列化学用语书写正确的是
A.三个氮分子3N2 B.铝离子Al+3
C.两个氧原子O2 D.硫酸钠NaSO4
二、填空题
11.用化学符号表示
(1)3个钙原子______;
(2)空气中含量最多的元素______;
(3)硫酸根离子______;
(4)显正三价的铝元素______。
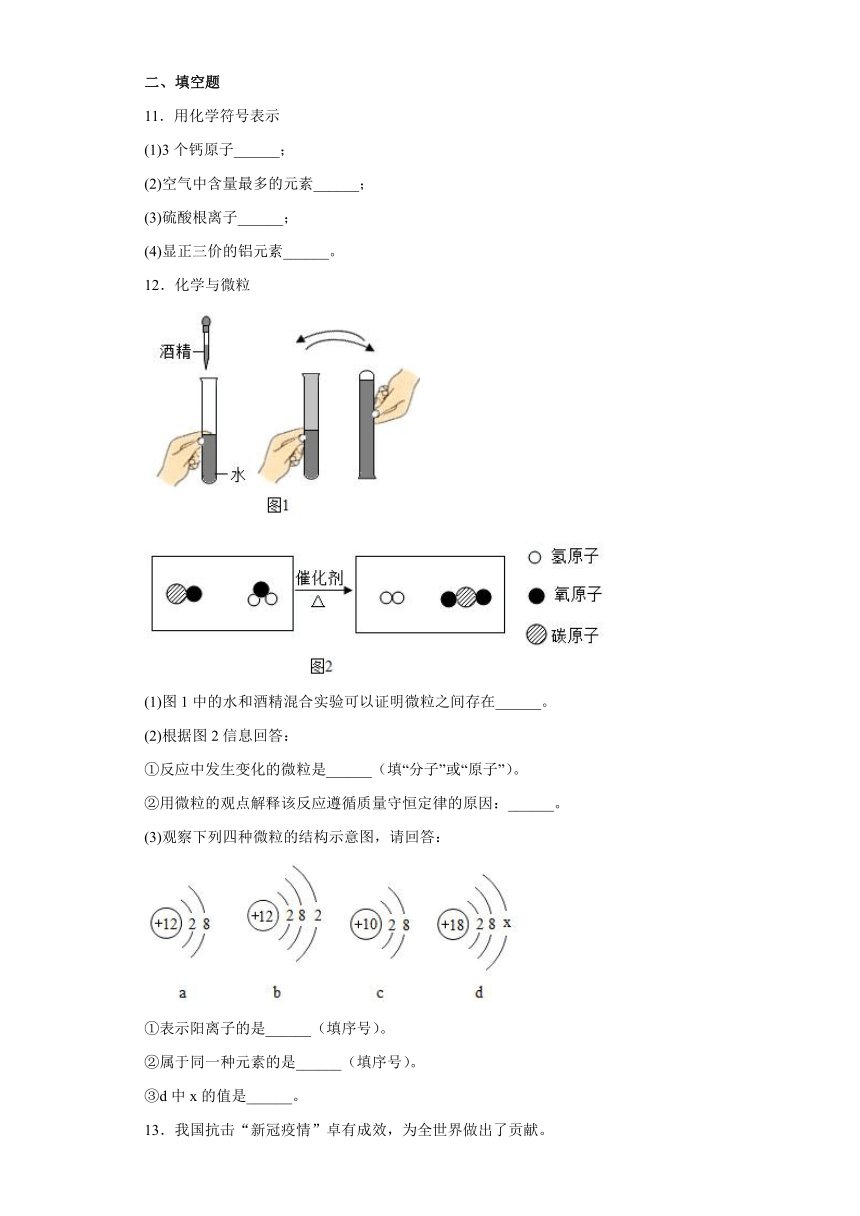
12.化学与微粒
(1)图1中的水和酒精混合实验可以证明微粒之间存在______。
(2)根据图2信息回答:
①反应中发生变化的微粒是______(填“分子”或“原子”)。
②用微粒的观点解释该反应遵循质量守恒定律的原因:______。
(3)观察下列四种微粒的结构示意图,请回答:
①表示阳离子的是______(填序号)。
②属于同一种元素的是______(填序号)。
③d中x的值是______。
13.我国抗击“新冠疫情”卓有成效,为全世界做出了贡献。
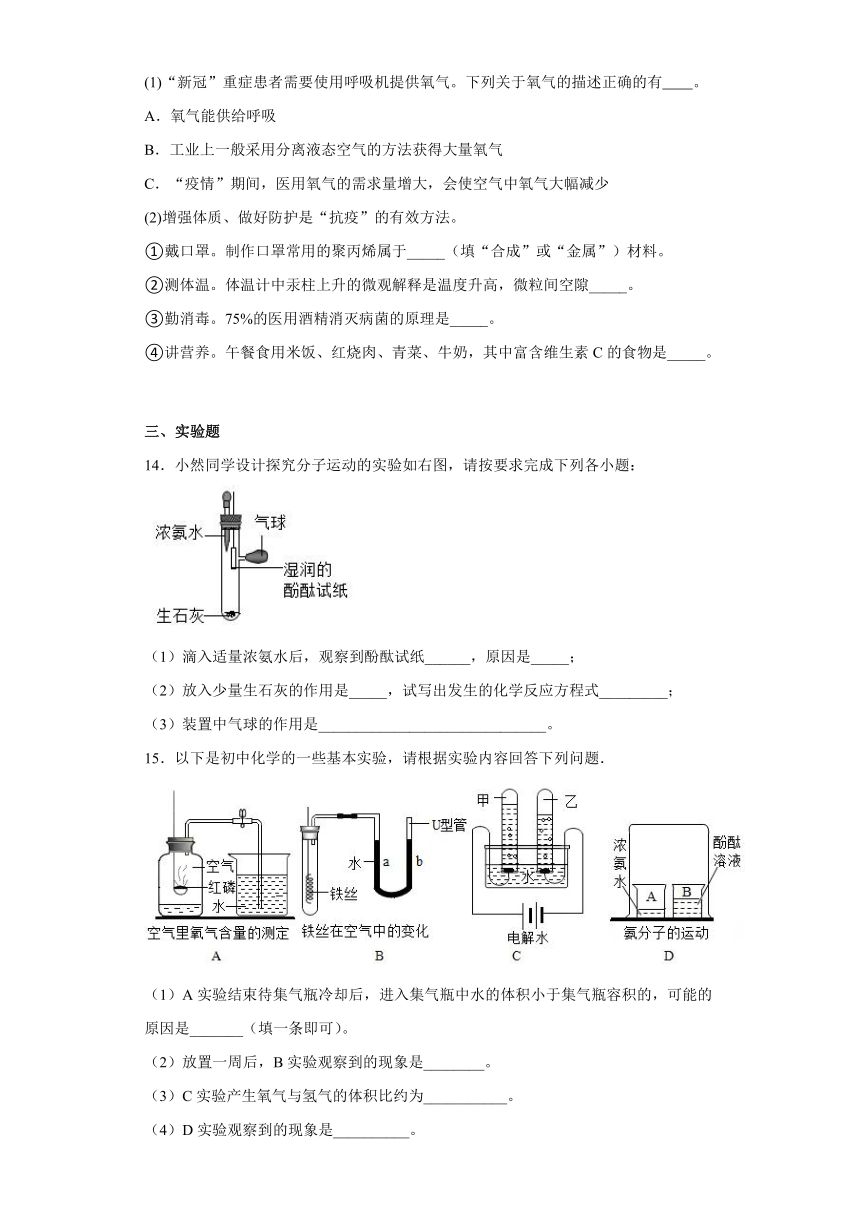
(1)“新冠”重症患者需要使用呼吸机提供氧气。下列关于氧气的描述正确的有 。
A.氧气能供给呼吸
B.工业上一般采用分离液态空气的方法获得大量氧气
C.“疫情”期间,医用氧气的需求量增大,会使空气中氧气大幅减少
(2)增强体质、做好防护是“抗疫”的有效方法。
①戴口罩。制作口罩常用的聚丙烯属于_____(填“合成”或“金属”)材料。
②测体温。体温计中汞柱上升的微观解释是温度升高,微粒间空隙_____。
③勤消毒。75%的医用酒精消灭病菌的原理是_____。
④讲营养。午餐食用米饭、红烧肉、青菜、牛奶,其中富含维生素C的食物是_____。
三、实验题
14.小然同学设计探究分子运动的实验如右图,请按要求完成下列各小题:
(1)滴入适量浓氨水后,观察到酚酞试纸______,原因是_____;
(2)放入少量生石灰的作用是_____,试写出发生的化学反应方程式_________;
(3)装置中气球的作用是______________________________。
15.以下是初中化学的一些基本实验,请根据实验内容回答下列问题.
(1)A实验结束待集气瓶冷却后,进入集气瓶中水的体积小于集气瓶容积的,可能的原因是_______(填一条即可)。
(2)放置一周后,B实验观察到的现象是________。
(3)C实验产生氧气与氢气的体积比约为___________。
(4)D实验观察到的现象是__________。
四、科学探究题
16.同学们学习了分子、原子、离子是构成物质常见的基本粒子,它们的质量和体积都很小。某化学兴趣小组的同学对粒子体积大小有没有差异进行了如下探究:
【查阅资料】
鸡蛋膜有极其微小的孔隙。
【实验探究】
如图所示:向5个鸡蛋壳内分别加入下表中的物质,放入盛有蒸馏水的小烧杯中,一段时间后取出鸡蛋壳,再向小烧杯中分别加入下表中的物质进行实验。
实验编号 ① ② ③ ④ ⑤
鸡蛋壳内加入的物质 NaCl溶液 Na2CO3溶液 NaOH溶液 淀粉溶液 鸡蛋清
小烧杯中加入的物质 AgNO3溶液 CaCl2溶液 FeCl3溶液 碘水 浓硝酸
小烧杯中的现象 白色沉淀 ______ 红褐色沉淀 无现象 无现象
【实验分析】
(1)实验①小烧杯中产生的白色沉淀是_______;实验③小烧杯中产生红褐色沉淀,反应的化学方程式为______。
(2)通过实验①②③得出的结论是_______。
【实验结论】
综上实验探究可知:构成物质的基本粒子的体积_______。
【反思交流】
小明同学认为上述实验④⑤不能比较分子体积大小差异,还应增加下列对比实验进行完善:将实验④鸡蛋壳内和小烧杯中物质互换,重复上述实验操作,小烧杯中的现象是_________。
【拓展延伸】
科学家设计制造出孔径大小不同的“小筛子”,让体积大小不同的粒子通过,从而分离提纯物质。如天然水的净化、海水淡化。
参考答案:
1.A
【详解】A、元素是质子数相同的一类原子的总称,①②质子数相同,属于同种元素,符合题意;
B、③质子数=核外电子数,表示原子,且其最外层电子数为8,达到了相对稳定结构,不符合题意;
C、④质子数大于核外电子数,表示阳离子,质子数=原子序数,11号元素是钠元素,故④为钠离子,表示为:Na+,不符合题意;
D、⑤的最外层电子数为2,小于4,在化学反应中容易失去电子,不符合题意。
故选A。
2.C
【分析】化学式前面的数字表示分子个数,故2H2表示2个氢分子,每个氢分子由2个氢原子构成。
【详解】A、该图可表示4个原子,不符合题意;
B、该图存在两种原子,不符合题意;
C、该图存在两个相同分子,且该分子由同种原子构成,可表示“2H2”,符合题意;
D、该图存在两个相同分子,但是该分子由两种原子构成,不符合题意。
故选C。
3.D
【分析】由图可知,反应为4个AB2分子和2个B2分子反应生成4个AB3分子;
【详解】由分析可知;
A、反应符合多变一特点,属于化合反应,正确;
B、该反应的化学方程式为:2AB2+B2=2AB3,正确;
C、该反应反应后仍有反应物分子剩余,故尚未完全进行,正确;
D、不确定AB原子种类,不能判断该反应是否属于还原反应,错误。
故选D。
4.C
【详解】A、金属原子的最外层电子一般少于4个,因而在化学反应中易失去电子,形成稳定结构,正确;
B、物质结构决定物质性质,金刚石与石墨烯的性质存在明显差异是因为碳原子排列方式不同,正确;
C、金属很难被压缩,是因为固体微粒之间间隔很小,很难被压缩,错误;
D、不同的碱却存在一些相似的化学性质,是因为它们在水溶液中都能解离出OH-,正确;
故选C。
5.A
【详解】A、原子序数=核外电子数=质子数=9,所以原子结构示意图可表示为:,故说法正确;
B、该原子最外层电子数大于4,原子在化学反应中易得电子,故说法错误;
C、原子序数=核外电子数=9,故说法错误;
D、相对原子质量≈质子数+中子数,不知道其中子数,无法得知其相对原子质量,故说法错误。
故选A。
6.B
【分析】A、根据原子中,质子数 核外电子数;当质子数 核外电子数,为阳离子;当质子数 核外电子数,为阴离子;进行分析判断;
B、根据元素是质子数 即核电荷数 相同的一类原子的总称,进行分析判断;
C、根据原子中,质子数 核外电子数;当质子数 核外电子数,为阳离子;当质子数 核外电子数,为阴离子;进行分析判断;
D、根据粒子结构示意图中,圆圈内数字表示核内质子数,进行分析判断。
【详解】A、②质子数=17,核外电子数=18,质子数<核外电子数,为阴离子;③质子数=19,核外电子数=18,质子数>核外电子数,为阳离子;②③的核内质子数不同,属于不同种的元素的离子,故选项说法错误;
B、①②的核内质子数相同,属于同一种元素,故选项说法正确;
C、①质子数 核外电子数=17,为原子;①质子数=19,核外电子数=18,质子数>核外电子数,为阳离子,故选项说法错误;
D、粒子结构示意图中,圆圈内数字表示核内质子数,②③的核内质子数分别是17、19,核内质子数不同,故选项说法错误。
故选:B。
7.A
【详解】在公园里行走,常能闻到各种花的香味,是花内含有的芳香性化合物(香精油)的分子不断运动,扩散到周围空间造成的,在此过程中分子的体积大小不变,分子的数目不变,分子之间的间隔变大。故选A。
8.B
【详解】原子最外层电子数相同,化学性质相似。最外层8个电子是相对稳定结构。但第一层就是最外层的,2个电子就是相对稳定结构。图中①③都是相对稳定结构。
综上所述:选择B。
9.D
【详解】A、用水壶烧开水,水沸腾后壶盖被顶起,是因为温度升高,分子间的间隔变大,与分子是由原子构成的无关,故选项错误;
B、用水壶烧开水,水沸腾后壶盖被顶起,是因为温度升高,分子间的间隔变大,与分子的质量很小无关,故选项错误;
C、用水壶烧开水,水沸腾后壶盖被顶起,是因为温度升高,分子间的间隔变大,而分子的体积不变,故选项错误;
D、用水壶烧开水,水沸腾后壶盖被顶起,是因为温度升高,分子间的间隔变大,故选项正确。
故选D。
10.A
【详解】A、表示微粒的个数在微粒前面加对应数字,三个氮分子3N2,正确;
B、离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略;铝离子Al3+,错误;
C、原子的表示方法用元素符号表示,表示微粒的个数在微粒前面加对应数字;两个氧原子2O,错误;
D、硫酸钠中钠元素化合价为+1,硫酸根化合价为-2,化合物中正负化合价代数和为零,则为Na2SO4,错误。
故选A。
11.(1)3Ca
(2)N
(3)
(4)
【详解】(1)原子的表示方法用元素符号表示,3个钙原子3Ca;
(2)空气中含量最多的元素为氮元素N;
(3)离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略;硫酸根离子为;
(4)化合价的表示方法,在该元素的上方用正负号和数字表示,正负号在前,数字在后;显正三价的铝元素为。
12.(1)空隙
(2) 分子 在化学反应中,反应前后原子的种类和数目不变、原子质量不变
(3) a ab 8
【分析】(1)
由实验中水与酒精等体积混合后总体积减小可知,微粒之间有空隙,故填:空隙。
(2)
①由微粒的变化可知,反应中发生变化的微粒是分子,故填:分子。
②由化学反应的实质是分子的破裂原子的重新组合可知,化学反应遵循质量守恒定律的原因:反应前后原子的种类和数目不变、原子质量不变,故填:在化学反应中,反应前后原子的种类和数目不变、原子质量不变。
(3)
①在a中,核外电子数少于质子数,表示的是阳离子,故填:a。
②元素是具有相同核电荷数 (即质子数) 的同一类原子的总称,由微粒结构示意图可知,a和b的质子数相同,属于同一种元素,故填:ab。
③由微粒的结构示意图可知,d的质子数是18,是氩元素,为稳定结构,即不容易得电子失电子,所以x为8,故填:8。
13.(1)AB
(2) 合成 变大 75%的医用酒精能使病菌的蛋白质变性 青菜
【解析】(1)
A.氧气能供给呼吸,该选项说法正确;
B.工业上一般采用分离液态空气的方法获得大量氧气,该选项说法正确;
C.“疫情”期间,医用氧气的需求量增大,不会使空气中氧气大幅减少,该选项说法不正确。故选AB
(2)
制作口罩常用的聚丙烯属于合成材料;
体温计中汞柱上升的微观解释是温度升高,微粒之间间隔变大;
75%的医用酒精消灭病菌的原理是75%的医用酒精能使病菌的蛋白质变性;
午餐食用米饭、红烧肉、青菜、牛奶,其中富含维生素C的食物是青菜。
14. 变红 氨分子在不断运动 提供热量,加快分子的运动速率 防止氨气扩散到空气中污染环境,调节装置内的压强平衡
【详解】(1)浓氨水具有挥发性,挥发出的氨分子不断运动,当氨分子不断运动到湿润的酚酞试纸上,氨气溶于水形成氨水,氨水显碱性,能使酚酞试液变红,故填:变红,氨分子在不断运动;
(2)生石灰能与水反应生成氢氧化钙,该反应放出大量的热,温度升高,可加快氨分子的运动速率,该反应的化学方程式为:;
(3)生石灰与水反应放出大量的热,可使装置内温度升高,压强增大,装置中气球的作用是缓冲,调节装置内的压强平衡,同时防止氨气扩散到空气中污染环境。
15. 红磷量不足 U型管内a端液面上升,b端液面下降 1:2 无色的酚酞试液变红色
【详解】(1)测量的结果发现进入集气瓶中水的体积小于原瓶中空气体积的五分之一,是因为反应的红磷量不足导致氧气未被完全消耗或装置漏气或未等集气瓶彻底冷却就打开止水夹等;
(2)铁在空气中锈蚀需消耗空气中的氧气,造成试管内的气体压强减小,所以看到U型管内a端液面上升,b端液面下降;
(3)通电电解水,一段时间后,正极生成的气体是氧气,负极生成的气体是氢气,二者的体积之比约为1:2;
(4)分子在不断的运动,氨分子与酚酞试液中的水分子结合成氨水,氨水显碱性,能使酚酞试液变红色。
考点:常见化学实验
16. 白色沉淀 氯化银##AgCl 离子可以透过鸡蛋膜进入到烧杯中。 很小 淀粉溶液变蓝
【详解】[实验分析]
(1)由于构成物质的微粒不断运动,且质量和体积都很小,则构成氯化钠的钠离子和氯离子通过运动透过鸡蛋膜进入到烧杯中,其中氯离子与烧杯中的银离子结合生成了氯化银白色沉淀。故实验①小烧杯中产生的白色沉淀是氯化银;实验③小烧杯中产生红褐色沉淀是氢氧化钠与氯化铁反应生成的氢氧化铁红褐色沉淀和氯化钠,化学方程式为。
(2)实验①②③鸡蛋壳内的物质(三种物质都是离子化合物)都能透过鸡蛋膜进入到烧杯中与烧杯中的物质发生反应,故通过实验①②③得出的结论是离子可以透过鸡蛋膜进入到烧杯中。
[实验结论]
综上实验探究可知:构成物质的基本粒子的体积都很小。
[反思交流]
实验④鸡蛋壳中加入的是淀粉溶液,实验⑤鸡蛋壳中加入的是鸡蛋清(主要成分是蛋白质),这两种物质都是大分子物质,故不能透过鸡蛋膜进入到烧杯中,所以没有明显现象。小明同学认为上述实验④⑤不能比较分子体积大小差异,还应增加下列对比实验进行完善:将实验④鸡蛋壳内和小烧杯中物质互换,重复上述实验操作,由于碘的分子体积很小,可以透过鸡蛋膜进入到烧杯中,此时小烧杯中碘与淀粉发生反应,现象是溶液变为蓝色。
一、单选题
1.微粒观是认识和研究物质的基本观念。下列有关粒子结构示意图的说法不正确的是
A.①②属于不同种元素 B.③是一种具有稳定结构的原子
C.④可以用化学符号表示为Na+ D.⑤在化学反应中容易失去电子
2.化学符号“ 2H2”可以用下列微观图示表示的是
A.B.
C. D.
3.某化学反应的微观过程如图所示,下列说法错误的是
A.该反应属于化合反应
B.该反应的化学方程式为:2AB2+B2=2AB3
C.该反应尚未完全进行
D.该反应属于还原反应
4.下列关于物质结构的说法错误的是
A.金属原子的最外层电子一般少于4个,因而在化学反应中易失去电子
B.金刚石与石墨烯的性质存在明显差异是因为碳原子排列方式不同
C.金属很难被压缩,说明物质的微粒间不存在间隙
D.不同的碱却存在一些相似的化学性质,是因为它们在水溶液中都能解离出OH-
5.对原子序数为9的元素,下列说法正确的是
A.其原子结构示意图可表示为:
B.该元素的原子在化学反应中易失电子
C.该元素原子的核外电子总数为10
D.该元素的相对原子质量为9
6.原子结构示意图能简明地表示原子核外电子的排布。小云从如图微粒结构示意图中获得相关信息,你认为正确的是
A.②③属于同一种原子 B.①②属于同一种元素
C.①③表示的都是原子 D.②③表示质子数相同
7.在公园里行走,常能闻到各种花的香味,主要原因是
A.分子总在不断运动 B.分子的体积变大
C.分子的数目变多 D.分子之间的间隔变小
8.如图为四种原子的结构示意图,其中化学性质相似的一组是
A.①和② B.①和③ C.②和③ D.③和④
9.用水壶烧开水,水沸腾后壶盖被顶起,说明
A.分子是由原子构成的 B.分子的质量很小
C.分子的体积变大 D.分子间的间隔变大
10.下列化学用语书写正确的是
A.三个氮分子3N2 B.铝离子Al+3
C.两个氧原子O2 D.硫酸钠NaSO4
二、填空题
11.用化学符号表示
(1)3个钙原子______;
(2)空气中含量最多的元素______;
(3)硫酸根离子______;
(4)显正三价的铝元素______。
12.化学与微粒
(1)图1中的水和酒精混合实验可以证明微粒之间存在______。
(2)根据图2信息回答:
①反应中发生变化的微粒是______(填“分子”或“原子”)。
②用微粒的观点解释该反应遵循质量守恒定律的原因:______。
(3)观察下列四种微粒的结构示意图,请回答:
①表示阳离子的是______(填序号)。
②属于同一种元素的是______(填序号)。
③d中x的值是______。
13.我国抗击“新冠疫情”卓有成效,为全世界做出了贡献。
(1)“新冠”重症患者需要使用呼吸机提供氧气。下列关于氧气的描述正确的有 。
A.氧气能供给呼吸
B.工业上一般采用分离液态空气的方法获得大量氧气
C.“疫情”期间,医用氧气的需求量增大,会使空气中氧气大幅减少
(2)增强体质、做好防护是“抗疫”的有效方法。
①戴口罩。制作口罩常用的聚丙烯属于_____(填“合成”或“金属”)材料。
②测体温。体温计中汞柱上升的微观解释是温度升高,微粒间空隙_____。
③勤消毒。75%的医用酒精消灭病菌的原理是_____。
④讲营养。午餐食用米饭、红烧肉、青菜、牛奶,其中富含维生素C的食物是_____。
三、实验题
14.小然同学设计探究分子运动的实验如右图,请按要求完成下列各小题:
(1)滴入适量浓氨水后,观察到酚酞试纸______,原因是_____;
(2)放入少量生石灰的作用是_____,试写出发生的化学反应方程式_________;
(3)装置中气球的作用是______________________________。
15.以下是初中化学的一些基本实验,请根据实验内容回答下列问题.
(1)A实验结束待集气瓶冷却后,进入集气瓶中水的体积小于集气瓶容积的,可能的原因是_______(填一条即可)。
(2)放置一周后,B实验观察到的现象是________。
(3)C实验产生氧气与氢气的体积比约为___________。
(4)D实验观察到的现象是__________。
四、科学探究题
16.同学们学习了分子、原子、离子是构成物质常见的基本粒子,它们的质量和体积都很小。某化学兴趣小组的同学对粒子体积大小有没有差异进行了如下探究:
【查阅资料】
鸡蛋膜有极其微小的孔隙。
【实验探究】
如图所示:向5个鸡蛋壳内分别加入下表中的物质,放入盛有蒸馏水的小烧杯中,一段时间后取出鸡蛋壳,再向小烧杯中分别加入下表中的物质进行实验。
实验编号 ① ② ③ ④ ⑤
鸡蛋壳内加入的物质 NaCl溶液 Na2CO3溶液 NaOH溶液 淀粉溶液 鸡蛋清
小烧杯中加入的物质 AgNO3溶液 CaCl2溶液 FeCl3溶液 碘水 浓硝酸
小烧杯中的现象 白色沉淀 ______ 红褐色沉淀 无现象 无现象
【实验分析】
(1)实验①小烧杯中产生的白色沉淀是_______;实验③小烧杯中产生红褐色沉淀,反应的化学方程式为______。
(2)通过实验①②③得出的结论是_______。
【实验结论】
综上实验探究可知:构成物质的基本粒子的体积_______。
【反思交流】
小明同学认为上述实验④⑤不能比较分子体积大小差异,还应增加下列对比实验进行完善:将实验④鸡蛋壳内和小烧杯中物质互换,重复上述实验操作,小烧杯中的现象是_________。
【拓展延伸】
科学家设计制造出孔径大小不同的“小筛子”,让体积大小不同的粒子通过,从而分离提纯物质。如天然水的净化、海水淡化。
参考答案:
1.A
【详解】A、元素是质子数相同的一类原子的总称,①②质子数相同,属于同种元素,符合题意;
B、③质子数=核外电子数,表示原子,且其最外层电子数为8,达到了相对稳定结构,不符合题意;
C、④质子数大于核外电子数,表示阳离子,质子数=原子序数,11号元素是钠元素,故④为钠离子,表示为:Na+,不符合题意;
D、⑤的最外层电子数为2,小于4,在化学反应中容易失去电子,不符合题意。
故选A。
2.C
【分析】化学式前面的数字表示分子个数,故2H2表示2个氢分子,每个氢分子由2个氢原子构成。
【详解】A、该图可表示4个原子,不符合题意;
B、该图存在两种原子,不符合题意;
C、该图存在两个相同分子,且该分子由同种原子构成,可表示“2H2”,符合题意;
D、该图存在两个相同分子,但是该分子由两种原子构成,不符合题意。
故选C。
3.D
【分析】由图可知,反应为4个AB2分子和2个B2分子反应生成4个AB3分子;
【详解】由分析可知;
A、反应符合多变一特点,属于化合反应,正确;
B、该反应的化学方程式为:2AB2+B2=2AB3,正确;
C、该反应反应后仍有反应物分子剩余,故尚未完全进行,正确;
D、不确定AB原子种类,不能判断该反应是否属于还原反应,错误。
故选D。
4.C
【详解】A、金属原子的最外层电子一般少于4个,因而在化学反应中易失去电子,形成稳定结构,正确;
B、物质结构决定物质性质,金刚石与石墨烯的性质存在明显差异是因为碳原子排列方式不同,正确;
C、金属很难被压缩,是因为固体微粒之间间隔很小,很难被压缩,错误;
D、不同的碱却存在一些相似的化学性质,是因为它们在水溶液中都能解离出OH-,正确;
故选C。
5.A
【详解】A、原子序数=核外电子数=质子数=9,所以原子结构示意图可表示为:,故说法正确;
B、该原子最外层电子数大于4,原子在化学反应中易得电子,故说法错误;
C、原子序数=核外电子数=9,故说法错误;
D、相对原子质量≈质子数+中子数,不知道其中子数,无法得知其相对原子质量,故说法错误。
故选A。
6.B
【分析】A、根据原子中,质子数 核外电子数;当质子数 核外电子数,为阳离子;当质子数 核外电子数,为阴离子;进行分析判断;
B、根据元素是质子数 即核电荷数 相同的一类原子的总称,进行分析判断;
C、根据原子中,质子数 核外电子数;当质子数 核外电子数,为阳离子;当质子数 核外电子数,为阴离子;进行分析判断;
D、根据粒子结构示意图中,圆圈内数字表示核内质子数,进行分析判断。
【详解】A、②质子数=17,核外电子数=18,质子数<核外电子数,为阴离子;③质子数=19,核外电子数=18,质子数>核外电子数,为阳离子;②③的核内质子数不同,属于不同种的元素的离子,故选项说法错误;
B、①②的核内质子数相同,属于同一种元素,故选项说法正确;
C、①质子数 核外电子数=17,为原子;①质子数=19,核外电子数=18,质子数>核外电子数,为阳离子,故选项说法错误;
D、粒子结构示意图中,圆圈内数字表示核内质子数,②③的核内质子数分别是17、19,核内质子数不同,故选项说法错误。
故选:B。
7.A
【详解】在公园里行走,常能闻到各种花的香味,是花内含有的芳香性化合物(香精油)的分子不断运动,扩散到周围空间造成的,在此过程中分子的体积大小不变,分子的数目不变,分子之间的间隔变大。故选A。
8.B
【详解】原子最外层电子数相同,化学性质相似。最外层8个电子是相对稳定结构。但第一层就是最外层的,2个电子就是相对稳定结构。图中①③都是相对稳定结构。
综上所述:选择B。
9.D
【详解】A、用水壶烧开水,水沸腾后壶盖被顶起,是因为温度升高,分子间的间隔变大,与分子是由原子构成的无关,故选项错误;
B、用水壶烧开水,水沸腾后壶盖被顶起,是因为温度升高,分子间的间隔变大,与分子的质量很小无关,故选项错误;
C、用水壶烧开水,水沸腾后壶盖被顶起,是因为温度升高,分子间的间隔变大,而分子的体积不变,故选项错误;
D、用水壶烧开水,水沸腾后壶盖被顶起,是因为温度升高,分子间的间隔变大,故选项正确。
故选D。
10.A
【详解】A、表示微粒的个数在微粒前面加对应数字,三个氮分子3N2,正确;
B、离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略;铝离子Al3+,错误;
C、原子的表示方法用元素符号表示,表示微粒的个数在微粒前面加对应数字;两个氧原子2O,错误;
D、硫酸钠中钠元素化合价为+1,硫酸根化合价为-2,化合物中正负化合价代数和为零,则为Na2SO4,错误。
故选A。
11.(1)3Ca
(2)N
(3)
(4)
【详解】(1)原子的表示方法用元素符号表示,3个钙原子3Ca;
(2)空气中含量最多的元素为氮元素N;
(3)离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略;硫酸根离子为;
(4)化合价的表示方法,在该元素的上方用正负号和数字表示,正负号在前,数字在后;显正三价的铝元素为。
12.(1)空隙
(2) 分子 在化学反应中,反应前后原子的种类和数目不变、原子质量不变
(3) a ab 8
【分析】(1)
由实验中水与酒精等体积混合后总体积减小可知,微粒之间有空隙,故填:空隙。
(2)
①由微粒的变化可知,反应中发生变化的微粒是分子,故填:分子。
②由化学反应的实质是分子的破裂原子的重新组合可知,化学反应遵循质量守恒定律的原因:反应前后原子的种类和数目不变、原子质量不变,故填:在化学反应中,反应前后原子的种类和数目不变、原子质量不变。
(3)
①在a中,核外电子数少于质子数,表示的是阳离子,故填:a。
②元素是具有相同核电荷数 (即质子数) 的同一类原子的总称,由微粒结构示意图可知,a和b的质子数相同,属于同一种元素,故填:ab。
③由微粒的结构示意图可知,d的质子数是18,是氩元素,为稳定结构,即不容易得电子失电子,所以x为8,故填:8。
13.(1)AB
(2) 合成 变大 75%的医用酒精能使病菌的蛋白质变性 青菜
【解析】(1)
A.氧气能供给呼吸,该选项说法正确;
B.工业上一般采用分离液态空气的方法获得大量氧气,该选项说法正确;
C.“疫情”期间,医用氧气的需求量增大,不会使空气中氧气大幅减少,该选项说法不正确。故选AB
(2)
制作口罩常用的聚丙烯属于合成材料;
体温计中汞柱上升的微观解释是温度升高,微粒之间间隔变大;
75%的医用酒精消灭病菌的原理是75%的医用酒精能使病菌的蛋白质变性;
午餐食用米饭、红烧肉、青菜、牛奶,其中富含维生素C的食物是青菜。
14. 变红 氨分子在不断运动 提供热量,加快分子的运动速率 防止氨气扩散到空气中污染环境,调节装置内的压强平衡
【详解】(1)浓氨水具有挥发性,挥发出的氨分子不断运动,当氨分子不断运动到湿润的酚酞试纸上,氨气溶于水形成氨水,氨水显碱性,能使酚酞试液变红,故填:变红,氨分子在不断运动;
(2)生石灰能与水反应生成氢氧化钙,该反应放出大量的热,温度升高,可加快氨分子的运动速率,该反应的化学方程式为:;
(3)生石灰与水反应放出大量的热,可使装置内温度升高,压强增大,装置中气球的作用是缓冲,调节装置内的压强平衡,同时防止氨气扩散到空气中污染环境。
15. 红磷量不足 U型管内a端液面上升,b端液面下降 1:2 无色的酚酞试液变红色
【详解】(1)测量的结果发现进入集气瓶中水的体积小于原瓶中空气体积的五分之一,是因为反应的红磷量不足导致氧气未被完全消耗或装置漏气或未等集气瓶彻底冷却就打开止水夹等;
(2)铁在空气中锈蚀需消耗空气中的氧气,造成试管内的气体压强减小,所以看到U型管内a端液面上升,b端液面下降;
(3)通电电解水,一段时间后,正极生成的气体是氧气,负极生成的气体是氢气,二者的体积之比约为1:2;
(4)分子在不断的运动,氨分子与酚酞试液中的水分子结合成氨水,氨水显碱性,能使酚酞试液变红色。
考点:常见化学实验
16. 白色沉淀 氯化银##AgCl 离子可以透过鸡蛋膜进入到烧杯中。 很小 淀粉溶液变蓝
【详解】[实验分析]
(1)由于构成物质的微粒不断运动,且质量和体积都很小,则构成氯化钠的钠离子和氯离子通过运动透过鸡蛋膜进入到烧杯中,其中氯离子与烧杯中的银离子结合生成了氯化银白色沉淀。故实验①小烧杯中产生的白色沉淀是氯化银;实验③小烧杯中产生红褐色沉淀是氢氧化钠与氯化铁反应生成的氢氧化铁红褐色沉淀和氯化钠,化学方程式为。
(2)实验①②③鸡蛋壳内的物质(三种物质都是离子化合物)都能透过鸡蛋膜进入到烧杯中与烧杯中的物质发生反应,故通过实验①②③得出的结论是离子可以透过鸡蛋膜进入到烧杯中。
[实验结论]
综上实验探究可知:构成物质的基本粒子的体积都很小。
[反思交流]
实验④鸡蛋壳中加入的是淀粉溶液,实验⑤鸡蛋壳中加入的是鸡蛋清(主要成分是蛋白质),这两种物质都是大分子物质,故不能透过鸡蛋膜进入到烧杯中,所以没有明显现象。小明同学认为上述实验④⑤不能比较分子体积大小差异,还应增加下列对比实验进行完善:将实验④鸡蛋壳内和小烧杯中物质互换,重复上述实验操作,由于碘的分子体积很小,可以透过鸡蛋膜进入到烧杯中,此时小烧杯中碘与淀粉发生反应,现象是溶液变为蓝色。
同课章节目录
