第3章 有机合成及其应用 合成高分子化合物 检测题(含答案) 高二化学鲁科版(2019)选择性必修3
文档属性
| 名称 | 第3章 有机合成及其应用 合成高分子化合物 检测题(含答案) 高二化学鲁科版(2019)选择性必修3 |

|
|
| 格式 | docx | ||
| 文件大小 | 1.3MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-06-09 00:00:00 | ||
图片预览




文档简介
第三章《有机合成及其应用 合成高分子化合物》检测题
一、单选题(共13题)
1.下列说法正确的是
A.等质量的乙炔和乙醛完全燃烧时消耗氧气的质量相等
B.等质量的乙炔和乙醛完全燃烧时生成二氧化碳的质量相等
C.等物质的量的乙炔和乙醛完全燃烧时消耗氧气的物质的量相等
D.等物质的量的乙炔和乙醛完全燃烧时生成水的物质的量相等
2.从柑橘中可提炼得1,8-萜二烯(()。下列有关它的说法正确的是
A.分子式为C10H14
B.难溶于水,可用某些有机溶剂提取1,8-萜二烯
C.与酸性高锰酸钾溶液、溴水均可发生氧化反应
D.它的一种同分异构体的结构中可能含有苯环
3.设表示阿伏加德罗常数的值。下列说法正确的是
A.聚丙烯中含键总数目为
B.常温下,的溶液中含有的数目为
C.的溶液中,阴离子总数大于
D.含有个胶粒的氢氧化铁胶体中,铁元素的质量为
4.有A、B两种烃,它们碳的物质的量的分数相同,关于A和B关系的叙述中正确的是
A.一定是同分异构体 B.最简式一定相同
C.不可能是同系物 D.各1 mol烃完全燃烧后生成的水的质量一定不相等
5.对羟基肉桂酸甲酯具有高光敏性等优良的特点,用于制作触摸屏和光纤材料,该物质的结构简式如图所示。关于该有机化合物说法不正确的是
A.可与溶液发生显色反应
B.1mol该有机化合物最多可与发生反应
C.分子中的含氧官能团是羟基和酯基
D.可以发生聚合反应
6.中成药连花清瘟胶囊在对抗病毒中发挥重大作用,其有效成分绿原酸的结构简式如图所示,下列有关说法错误的是
A.绿原酸属于芳香化合物
B.绿原酸能使溴的四氯化碳溶液褪色
C.绿原酸最多可消耗
D.与绿原酸苯环上取代基种类及个数均相同的有机物有5种
7.现在大量使用的塑料,如聚苯乙烯,因难以分解而造成严重的“白色污染”,为此,铁道部下令全国铁路餐车停止使用聚苯乙烯制造的餐具,改用一种可降解塑料,其结构简式为,该可降解塑料在乳酸菌作用下迅速分解为无毒物质。则下列有关该可降解塑料的叙述正确的是
A.该可降解塑料是一种纯净物 B.其能发生银镜反应
C.经加聚反应生成 D.其单体是
8.有机物M是合成治疗癌症的药物中间体,其结构简式如图所示,下列说法正确的是
A.M不能使酸性高锰酸钾溶液褪色
B.M在一定条件下能发生加聚反应和酯化反应
C.在一定条件下,1molM最多只能与3molH2发生加成反应
D.1mol有机物M与足量Na反应可以生成1molH2
9.蓖麻油酸(结构简式如图所示)是工业上制备高分子材料锦纶常使用的一种原料。下列关于蓖麻油酸的说法错误的是
A.分子式为C18H34O3 B.分子中含有两种含氧官能团
C.可发生氧化、加成和取代反应 D.1mol蓖麻油酸可与足量金属钠反应生成2molH2
10.在抗击新冠病毒肺炎中瑞德西韦是主要药物之一 ,瑞德西韦的结构如图所示,下列说法正确的是
A.瑞德西韦中N、O、P元素的电负性:N>O> P
B.瑞德西韦分子可以发生水解反应、加成反应、氧化反应和还原反应
C.瑞德西韦中所有的N都为sp3杂化
D.瑞德西韦结构中存在σ键、π键、不存在大π键
11.和是重要的化工原料,下列说法不正确的是
A.两者均能发生加成反应
B.两者均能发生酯化反应
C.两者均能与NaOH溶液反应
D.两者均能被氧化为醛
12.阿司匹林的化学名称为乙酰水杨酸,具有解热镇痛作用,其结构如图所示。下列说法正确的是
A.乙酰水杨酸属于芳香烃 B.乙酰水杨酸分子中所有原子可能共面
C.乙酰水杨酸能发生水解反应 D.乙酰水杨酸的分子式为C9H10O4
13.结构为的有机物可以通过不同的反应得到下列四种物质:
① ② ③ ④
生成这四种有机物的反应类型依次为( )
A.酯化、加成、取代、缩聚 B.取代、酯化、消去、缩聚
C.取代、加成、消去、加聚 D.取代、酯化、加成、加聚
二、非选择题(共10题)
14.按要求回答下列问题:
(1)常温下,与混合后光照,反应产物中属于气体的是_______。(填化学式)。
(2)键线式 表示的有机物的分子式为_______。
(3)有机物 的系统命名法名称为_______。
(4)2-甲基丙烯的核磁共振氢谱图中,不同化学环境的氢原子的个数比为_______。
(5)实验室制乙炔的化学方程式为_______。反应产生的气体需先通过溶液,是为了除去气体中的_______等杂质。
15.按要求写出下列烷烃:
(1)相对分子质量为44的烷烃的结构简式___________。
(2)碳、氢原子个数比为2∶5的烷烃的分子式___________。
(3)分子中含50个电子的烷烃的分子式___________。
16.E是合成某药物的中间体,其一种合成路线如下:
(1)A的分子式为_______。
(2)的化学方程式是_______。
(3)的反应类型是_______。
(4)D的官能团的名称是_______。
(5)的反应条件是_______。
三、实验题
17.青蒿素是烃的含氧衍生物,为无色针状晶体,可溶于乙醇、乙醚,在水中几乎不溶,熔点为156~157℃,是高效的抗疟药。已知:乙醚的沸点为34.5℃。从青蒿中提取青蒿素的方法之一是以萃取原理为基础的,主要有乙醚浸取法和汽油浸取法。
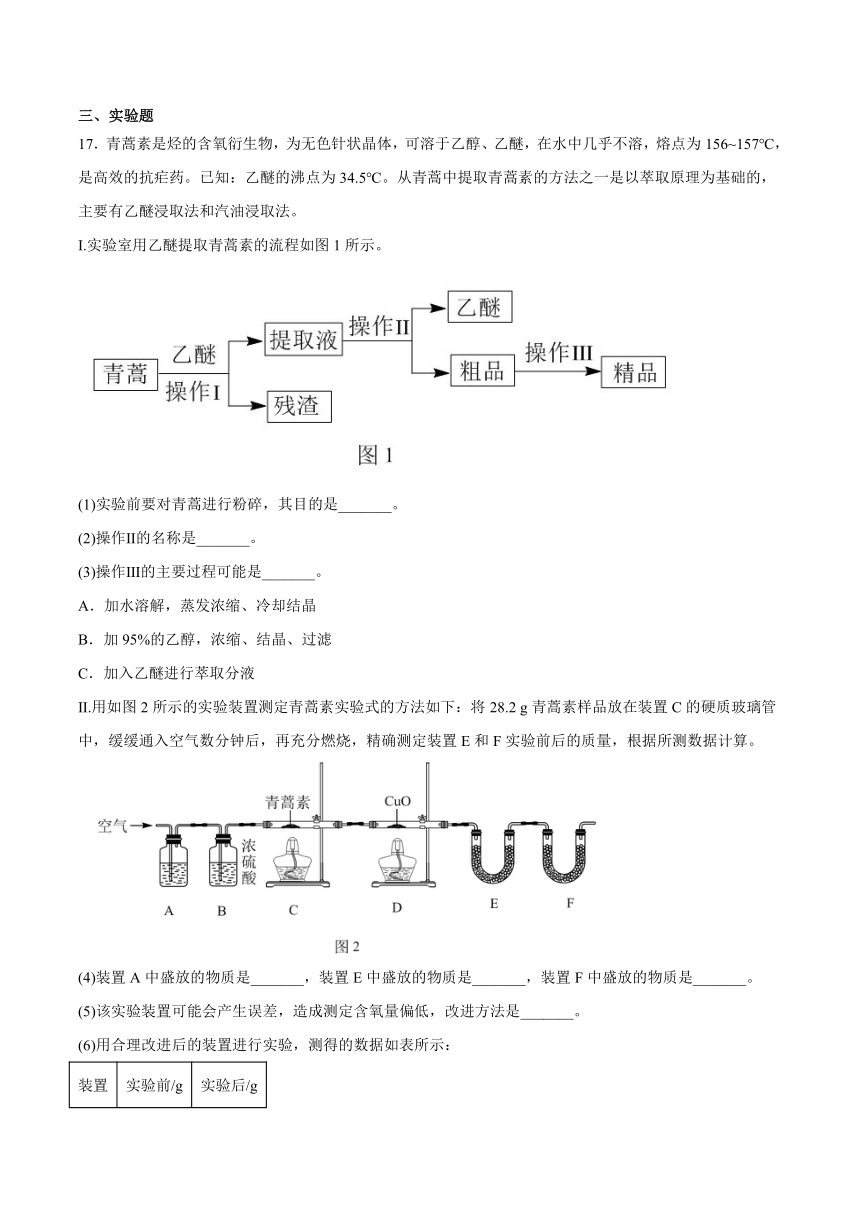
Ⅰ.实验室用乙醚提取青蒿素的流程如图1所示。
(1)实验前要对青蒿进行粉碎,其目的是_______。
(2)操作Ⅱ的名称是_______。
(3)操作Ⅲ的主要过程可能是_______。
A.加水溶解,蒸发浓缩、冷却结晶
B.加95%的乙醇,浓缩、结晶、过滤
C.加入乙醚进行萃取分液
Ⅱ.用如图2所示的实验装置测定青蒿素实验式的方法如下:将28.2 g青蒿素样品放在装置C的硬质玻璃管中,缓缓通入空气数分钟后,再充分燃烧,精确测定装置E和F实验前后的质量,根据所测数据计算。
(4)装置A中盛放的物质是_______,装置E中盛放的物质是_______,装置F中盛放的物质是_______。
(5)该实验装置可能会产生误差,造成测定含氧量偏低,改进方法是_______。
(6)用合理改进后的装置进行实验,测得的数据如表所示:
装置 实验前/g 实验后/g
E 22.6 42.4
F 80.2 146.2
则青蒿素的实验式是_______。
18.青蒿素是烃的含氧衍生物,为无色针状晶体。
(1)用如图所示实验装置测定青蒿素的分子式,将青蒿素放在硬质玻璃管C中充分燃烧:
①装置E中盛放的物质是_______,装置F中盛放的物质是_______。
②用该实验装置测定可能产生误差,造成测定的含氧量偏低,改进方法是_______。
③已知青蒿素是烃的含氧衍生物,用合理改进后的装置进行实验,所得实验数据如表所示:
装置 实验前装置的质量/g 实验后装置的质量/g
E
F
青蒿素的最简式是_______。
(2)将青蒿素加入含有、酚酞的水溶液中,青蒿素的溶解度较小,加热并搅拌,青蒿素的溶解度增大,且溶液红色变浅,说明青蒿素与_______(填标号)具有相似的性质。
A.乙醇 B.乙酸 C.乙酸乙酯 D.葡萄糖
四、计算题
19.有一元羧酸和一元醇形成的酯A。燃烧7.4gA,可得5.4g水和6.72L(标准状况)CO2。3.7gA与100mL0.8mol·L-1NaOH溶液共热,当完全水解后,为中和剩余的碱液,耗去0.5mol·L-1盐酸60mL。
(1)A的分子式为_______
(2)符合条件的A有_______种同分异构体,其可能的结构简式为_______。
20.苹果酸广泛存在于水果肉中,是一种常用的食品添加剂。物理分析测得苹果酸的相对分子质量为134,存在5种不同环境的H原子,ω(C)=35.82%、ω(H)=4.48%、ω(O)=59.70%。取2.68g苹果酸溶于水配成溶液,用0.80mol/LNaOH溶液滴定耗去50.00mL恰好中和,1mol苹果酸与足量的Na反应生成1.5mol的H2。试求:
(1)苹果酸的分子式;
(2)苹果酸分子中含羧基的个数;
(3)请写出苹果酸的结构简式。
21.某气态链烃能使溴水褪色,经测定该烃存在支链,并且0.1 mol该烃充分燃烧可以生成7.2 g水,请据此回答下列问题。
(1)通过计算确定该烃具有的分子式____________和结构简式____________。
(2)请对(1)中所确定的烃进行系统命名____________。
22.近年来,由于石油价格不断上涨,以煤为原料制备一些化工产品的前景又被看好。以煤为原料在不同条件下可合成下列物质(部分条件未标出),C是一种植物生长调节剂,用它可以催熟果实。根据以下化学反应框图填空:
(1)①写出A的电子式____;C的空间构型为平面结构,键角约为____。
②B中所含官能团的名称是____。
(2)①若分别完全燃烧等质量的HC≡C—CH=CH2和乙炔,所需氧气的量____(选填“前者多”“后者多”“一样多”)。
②写出与环辛四烯互为同分异构体的芳香烃发生聚合反应的化学方程式____。
③异丙苯是苯的同系物。由苯与2—丙醇反应制备异丙苯属于____反应;由异丙苯制备对溴异丙苯的反应试剂和反应条件为____。
(3)异丙苯有多种同分异构体,其中一溴代物最少的芳香烃的结构简式是____。
23.(1)互为同分异构体的四种有机物A、B、C、D,相对分子质量为74,完全燃烧只生成CO2和H2O,经分析其含氧元素的质量分数为43.3%,则这些有机物的分子式为__________,
(2)已知A、B、C、D分子结构中均含甲基,把它们分别进行下列实验以鉴别之,其实验记录如下:
NaOH溶液 银氨溶液 新制Cu(OH)2 金属钠
A 中和反应 —— 溶解 产生氢气
B —— 有银镜 加热后有红色沉淀 产生氢气
C 水解反应 有银镜 加热后有红色沉淀 ——
D 水解反应 —— —— ——
①写出由稀氨水和硝酸银稀溶液制备银氨溶液的化学方程式__________________________
②写出B与新制Cu(OH)2悬浊液反应的化学方程式_____________________________________
③B在浓硫酸存在的条件下能反应生成E,写出以E作原料在一定条件下制备高分子化合物的化学方程式__。
参考答案:
1.C 2.B 3.C 4.B 5.B 6.C 7.D 8.B 9.D 10.B 11.C 12.C 13.B
14.(1)HCl、
(2)
(3)2-甲基-1,3-丁二烯
(4)1∶3(或3∶1)
(5) 、
15.(1)
(2)
(3)
16. ClCl 取代(水解)反应 羧基、羰基 浓硫酸、加热、
17. 增大青蒿与乙醚的接触面积,提高青蒿素的浸出速率 蒸馏 B NaOH溶液 碱石灰 装置F后连接一个防止空气中和进入F的装置
18.(1) 无水(或) 碱石灰(或其他合理答案) 除去装置左侧通入的空气中的和水蒸气,在装置F后加一个防止空气中的和水蒸气进入装置F的装置
(2)C
19. C3H6O2 2 HCOOCH2CH3、CH3COOCH3
20.(1)C4H6O5
(2)2
(3)HOOC-CH(OH)CH2COOH 或
21. C4H8 CH2=C(CH3)2 2-甲基丙烯
22.(1) 120° 碳碳双键、氯原子
(2) 一样多 n 取代 Br2 /FeBr3或Br2 / Fe
(3)
23. C3H6O2 AgNO3+3NH3·H2O=Ag(NH3)2OH+NH4NO3+2H2O CH3CH(OH)CHO+2Cu(OH)2+NaOHCH3CH(OH)COONa+Cu2O↓+3H2O nCH2=CHCOOH
一、单选题(共13题)
1.下列说法正确的是
A.等质量的乙炔和乙醛完全燃烧时消耗氧气的质量相等
B.等质量的乙炔和乙醛完全燃烧时生成二氧化碳的质量相等
C.等物质的量的乙炔和乙醛完全燃烧时消耗氧气的物质的量相等
D.等物质的量的乙炔和乙醛完全燃烧时生成水的物质的量相等
2.从柑橘中可提炼得1,8-萜二烯(()。下列有关它的说法正确的是
A.分子式为C10H14
B.难溶于水,可用某些有机溶剂提取1,8-萜二烯
C.与酸性高锰酸钾溶液、溴水均可发生氧化反应
D.它的一种同分异构体的结构中可能含有苯环
3.设表示阿伏加德罗常数的值。下列说法正确的是
A.聚丙烯中含键总数目为
B.常温下,的溶液中含有的数目为
C.的溶液中,阴离子总数大于
D.含有个胶粒的氢氧化铁胶体中,铁元素的质量为
4.有A、B两种烃,它们碳的物质的量的分数相同,关于A和B关系的叙述中正确的是
A.一定是同分异构体 B.最简式一定相同
C.不可能是同系物 D.各1 mol烃完全燃烧后生成的水的质量一定不相等
5.对羟基肉桂酸甲酯具有高光敏性等优良的特点,用于制作触摸屏和光纤材料,该物质的结构简式如图所示。关于该有机化合物说法不正确的是
A.可与溶液发生显色反应
B.1mol该有机化合物最多可与发生反应
C.分子中的含氧官能团是羟基和酯基
D.可以发生聚合反应
6.中成药连花清瘟胶囊在对抗病毒中发挥重大作用,其有效成分绿原酸的结构简式如图所示,下列有关说法错误的是
A.绿原酸属于芳香化合物
B.绿原酸能使溴的四氯化碳溶液褪色
C.绿原酸最多可消耗
D.与绿原酸苯环上取代基种类及个数均相同的有机物有5种
7.现在大量使用的塑料,如聚苯乙烯,因难以分解而造成严重的“白色污染”,为此,铁道部下令全国铁路餐车停止使用聚苯乙烯制造的餐具,改用一种可降解塑料,其结构简式为,该可降解塑料在乳酸菌作用下迅速分解为无毒物质。则下列有关该可降解塑料的叙述正确的是
A.该可降解塑料是一种纯净物 B.其能发生银镜反应
C.经加聚反应生成 D.其单体是
8.有机物M是合成治疗癌症的药物中间体,其结构简式如图所示,下列说法正确的是
A.M不能使酸性高锰酸钾溶液褪色
B.M在一定条件下能发生加聚反应和酯化反应
C.在一定条件下,1molM最多只能与3molH2发生加成反应
D.1mol有机物M与足量Na反应可以生成1molH2
9.蓖麻油酸(结构简式如图所示)是工业上制备高分子材料锦纶常使用的一种原料。下列关于蓖麻油酸的说法错误的是
A.分子式为C18H34O3 B.分子中含有两种含氧官能团
C.可发生氧化、加成和取代反应 D.1mol蓖麻油酸可与足量金属钠反应生成2molH2
10.在抗击新冠病毒肺炎中瑞德西韦是主要药物之一 ,瑞德西韦的结构如图所示,下列说法正确的是
A.瑞德西韦中N、O、P元素的电负性:N>O> P
B.瑞德西韦分子可以发生水解反应、加成反应、氧化反应和还原反应
C.瑞德西韦中所有的N都为sp3杂化
D.瑞德西韦结构中存在σ键、π键、不存在大π键
11.和是重要的化工原料,下列说法不正确的是
A.两者均能发生加成反应
B.两者均能发生酯化反应
C.两者均能与NaOH溶液反应
D.两者均能被氧化为醛
12.阿司匹林的化学名称为乙酰水杨酸,具有解热镇痛作用,其结构如图所示。下列说法正确的是
A.乙酰水杨酸属于芳香烃 B.乙酰水杨酸分子中所有原子可能共面
C.乙酰水杨酸能发生水解反应 D.乙酰水杨酸的分子式为C9H10O4
13.结构为的有机物可以通过不同的反应得到下列四种物质:
① ② ③ ④
生成这四种有机物的反应类型依次为( )
A.酯化、加成、取代、缩聚 B.取代、酯化、消去、缩聚
C.取代、加成、消去、加聚 D.取代、酯化、加成、加聚
二、非选择题(共10题)
14.按要求回答下列问题:
(1)常温下,与混合后光照,反应产物中属于气体的是_______。(填化学式)。
(2)键线式 表示的有机物的分子式为_______。
(3)有机物 的系统命名法名称为_______。
(4)2-甲基丙烯的核磁共振氢谱图中,不同化学环境的氢原子的个数比为_______。
(5)实验室制乙炔的化学方程式为_______。反应产生的气体需先通过溶液,是为了除去气体中的_______等杂质。
15.按要求写出下列烷烃:
(1)相对分子质量为44的烷烃的结构简式___________。
(2)碳、氢原子个数比为2∶5的烷烃的分子式___________。
(3)分子中含50个电子的烷烃的分子式___________。
16.E是合成某药物的中间体,其一种合成路线如下:
(1)A的分子式为_______。
(2)的化学方程式是_______。
(3)的反应类型是_______。
(4)D的官能团的名称是_______。
(5)的反应条件是_______。
三、实验题
17.青蒿素是烃的含氧衍生物,为无色针状晶体,可溶于乙醇、乙醚,在水中几乎不溶,熔点为156~157℃,是高效的抗疟药。已知:乙醚的沸点为34.5℃。从青蒿中提取青蒿素的方法之一是以萃取原理为基础的,主要有乙醚浸取法和汽油浸取法。
Ⅰ.实验室用乙醚提取青蒿素的流程如图1所示。
(1)实验前要对青蒿进行粉碎,其目的是_______。
(2)操作Ⅱ的名称是_______。
(3)操作Ⅲ的主要过程可能是_______。
A.加水溶解,蒸发浓缩、冷却结晶
B.加95%的乙醇,浓缩、结晶、过滤
C.加入乙醚进行萃取分液
Ⅱ.用如图2所示的实验装置测定青蒿素实验式的方法如下:将28.2 g青蒿素样品放在装置C的硬质玻璃管中,缓缓通入空气数分钟后,再充分燃烧,精确测定装置E和F实验前后的质量,根据所测数据计算。
(4)装置A中盛放的物质是_______,装置E中盛放的物质是_______,装置F中盛放的物质是_______。
(5)该实验装置可能会产生误差,造成测定含氧量偏低,改进方法是_______。
(6)用合理改进后的装置进行实验,测得的数据如表所示:
装置 实验前/g 实验后/g
E 22.6 42.4
F 80.2 146.2
则青蒿素的实验式是_______。
18.青蒿素是烃的含氧衍生物,为无色针状晶体。
(1)用如图所示实验装置测定青蒿素的分子式,将青蒿素放在硬质玻璃管C中充分燃烧:
①装置E中盛放的物质是_______,装置F中盛放的物质是_______。
②用该实验装置测定可能产生误差,造成测定的含氧量偏低,改进方法是_______。
③已知青蒿素是烃的含氧衍生物,用合理改进后的装置进行实验,所得实验数据如表所示:
装置 实验前装置的质量/g 实验后装置的质量/g
E
F
青蒿素的最简式是_______。
(2)将青蒿素加入含有、酚酞的水溶液中,青蒿素的溶解度较小,加热并搅拌,青蒿素的溶解度增大,且溶液红色变浅,说明青蒿素与_______(填标号)具有相似的性质。
A.乙醇 B.乙酸 C.乙酸乙酯 D.葡萄糖
四、计算题
19.有一元羧酸和一元醇形成的酯A。燃烧7.4gA,可得5.4g水和6.72L(标准状况)CO2。3.7gA与100mL0.8mol·L-1NaOH溶液共热,当完全水解后,为中和剩余的碱液,耗去0.5mol·L-1盐酸60mL。
(1)A的分子式为_______
(2)符合条件的A有_______种同分异构体,其可能的结构简式为_______。
20.苹果酸广泛存在于水果肉中,是一种常用的食品添加剂。物理分析测得苹果酸的相对分子质量为134,存在5种不同环境的H原子,ω(C)=35.82%、ω(H)=4.48%、ω(O)=59.70%。取2.68g苹果酸溶于水配成溶液,用0.80mol/LNaOH溶液滴定耗去50.00mL恰好中和,1mol苹果酸与足量的Na反应生成1.5mol的H2。试求:
(1)苹果酸的分子式;
(2)苹果酸分子中含羧基的个数;
(3)请写出苹果酸的结构简式。
21.某气态链烃能使溴水褪色,经测定该烃存在支链,并且0.1 mol该烃充分燃烧可以生成7.2 g水,请据此回答下列问题。
(1)通过计算确定该烃具有的分子式____________和结构简式____________。
(2)请对(1)中所确定的烃进行系统命名____________。
22.近年来,由于石油价格不断上涨,以煤为原料制备一些化工产品的前景又被看好。以煤为原料在不同条件下可合成下列物质(部分条件未标出),C是一种植物生长调节剂,用它可以催熟果实。根据以下化学反应框图填空:
(1)①写出A的电子式____;C的空间构型为平面结构,键角约为____。
②B中所含官能团的名称是____。
(2)①若分别完全燃烧等质量的HC≡C—CH=CH2和乙炔,所需氧气的量____(选填“前者多”“后者多”“一样多”)。
②写出与环辛四烯互为同分异构体的芳香烃发生聚合反应的化学方程式____。
③异丙苯是苯的同系物。由苯与2—丙醇反应制备异丙苯属于____反应;由异丙苯制备对溴异丙苯的反应试剂和反应条件为____。
(3)异丙苯有多种同分异构体,其中一溴代物最少的芳香烃的结构简式是____。
23.(1)互为同分异构体的四种有机物A、B、C、D,相对分子质量为74,完全燃烧只生成CO2和H2O,经分析其含氧元素的质量分数为43.3%,则这些有机物的分子式为__________,
(2)已知A、B、C、D分子结构中均含甲基,把它们分别进行下列实验以鉴别之,其实验记录如下:
NaOH溶液 银氨溶液 新制Cu(OH)2 金属钠
A 中和反应 —— 溶解 产生氢气
B —— 有银镜 加热后有红色沉淀 产生氢气
C 水解反应 有银镜 加热后有红色沉淀 ——
D 水解反应 —— —— ——
①写出由稀氨水和硝酸银稀溶液制备银氨溶液的化学方程式__________________________
②写出B与新制Cu(OH)2悬浊液反应的化学方程式_____________________________________
③B在浓硫酸存在的条件下能反应生成E,写出以E作原料在一定条件下制备高分子化合物的化学方程式__。
参考答案:
1.C 2.B 3.C 4.B 5.B 6.C 7.D 8.B 9.D 10.B 11.C 12.C 13.B
14.(1)HCl、
(2)
(3)2-甲基-1,3-丁二烯
(4)1∶3(或3∶1)
(5) 、
15.(1)
(2)
(3)
16. ClCl 取代(水解)反应 羧基、羰基 浓硫酸、加热、
17. 增大青蒿与乙醚的接触面积,提高青蒿素的浸出速率 蒸馏 B NaOH溶液 碱石灰 装置F后连接一个防止空气中和进入F的装置
18.(1) 无水(或) 碱石灰(或其他合理答案) 除去装置左侧通入的空气中的和水蒸气,在装置F后加一个防止空气中的和水蒸气进入装置F的装置
(2)C
19. C3H6O2 2 HCOOCH2CH3、CH3COOCH3
20.(1)C4H6O5
(2)2
(3)HOOC-CH(OH)CH2COOH 或
21. C4H8 CH2=C(CH3)2 2-甲基丙烯
22.(1) 120° 碳碳双键、氯原子
(2) 一样多 n 取代 Br2 /FeBr3或Br2 / Fe
(3)
23. C3H6O2 AgNO3+3NH3·H2O=Ag(NH3)2OH+NH4NO3+2H2O CH3CH(OH)CHO+2Cu(OH)2+NaOHCH3CH(OH)COONa+Cu2O↓+3H2O nCH2=CHCOOH
