黑龙江省绥化市第八中学2022-2023学年八年级(五四学制)下学期期中考试化学试题(含答案)
文档属性
| 名称 | 黑龙江省绥化市第八中学2022-2023学年八年级(五四学制)下学期期中考试化学试题(含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 225.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-06-10 00:00:00 | ||
图片预览



文档简介
初三期中考试化学试题
可能用到的相对原子质量:H:1、C:12、O:16、Cl:35.5、K:39、Mn:55、K:40
一、选择题(1-15小题每题只有一个选项符合题意,16-20小题每题有一个或两个选项符合题意)
1.下列有关内容用质量守恒定律解释正确的是 ( )
A.10mL水和10mL酒精混合后,总体积一定是20mL
B.某化合物在氧气中燃烧生成了水和二氧化碳,则该化合物一定含碳元素和氢元素
C.煤燃烧后产生的煤渣的质量一定等于所用煤的质量
D.将5gA和5gB混合后发生化合反应,一定能生成10gC
2.氯碱工业的反应原理是电解饱和食盐水(主要成分为NaCl和H2O),下列物质不可能是氯碱工业产品的是 ( )
A.H2 B.Cl2 C.Na2CO3 D.NaOH
3.下列实验能够直接用于验证质量守恒定律的是 ( )
A.B.C. D.
4.今年2月美国俄亥俄州的氯乙烯泄漏事件给当地居民的健康造成严重损害。氯乙烯(C2H3C1)有致癌性,是易燃气体,完全燃烧的反应方程式为,其中X的化学式为( )
A.H2 B.CO C.HCl D.Cl2
5.下列反应的化学方程式书写正确的是( )
A. B.
C. D.
6.在A+3B=2C+2D的反应中,14gA和48gB恰好完全反应生成44gC和一定质量的D,若D的相对分子质量为18,则B的相对分子质量是( )
A.16 B.32 C.48 D.96
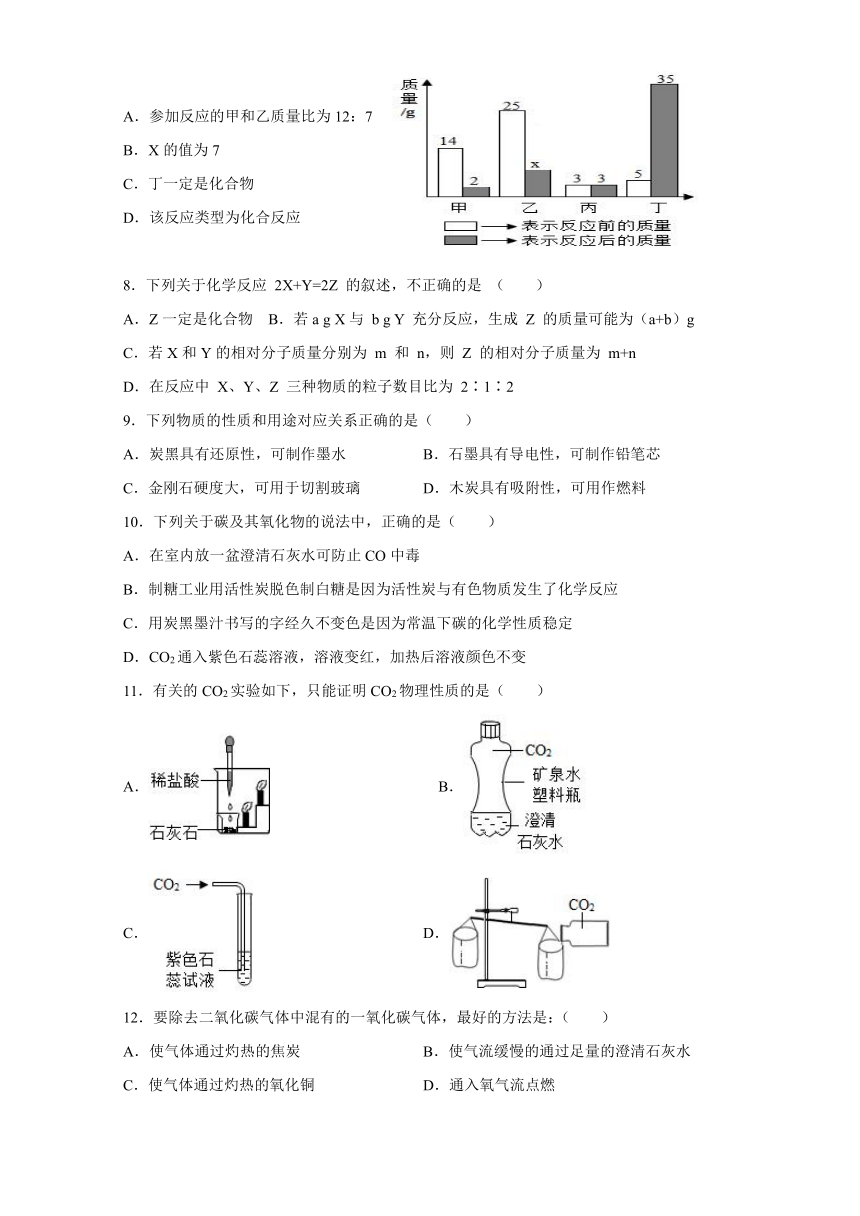
7.甲、乙、丙、丁四种物质在反应前后的质量关系如图所示,下列有关说法不正确的是
A.参加反应的甲和乙质量比为12:7 B.X的值为7
C.丁一定是化合物 D.该反应类型为化合反应
8.下列关于化学反应 2X+Y=2Z 的叙述,不正确的是 ( )
A.Z一定是化合物 B.若a g X与 b g Y 充分反应,生成 Z 的质量可能为(a+b)g
C.若X和Y的相对分子质量分别为 m 和 n,则 Z 的相对分子质量为 m+n
D.在反应中 X、Y、Z 三种物质的粒子数目比为 2∶1∶2
9.下列物质的性质和用途对应关系正确的是( )
A.炭黑具有还原性,可制作墨水 B.石墨具有导电性,可制作铅笔芯
C.金刚石硬度大,可用于切割玻璃 D.木炭具有吸附性,可用作燃料
10.下列关于碳及其氧化物的说法中,正确的是( )
A.在室内放一盆澄清石灰水可防止CO中毒
B.制糖工业用活性炭脱色制白糖是因为活性炭与有色物质发生了化学反应
C.用炭黑墨汁书写的字经久不变色是因为常温下碳的化学性质稳定
D.CO2通入紫色石蕊溶液,溶液变红,加热后溶液颜色不变
11.有关的CO2实验如下,只能证明CO2物理性质的是( )
A. B.
C. D.
12.要除去二氧化碳气体中混有的一氧化碳气体,最好的方法是:( )
A.使气体通过灼热的焦炭 B.使气流缓慢的通过足量的澄清石灰水
C.使气体通过灼热的氧化铜 D.通入氧气流点燃
13.构建模型是化学学习常用的方法,如图为某化学反应的微观模拟示意图,请判断下列说法,正确的是( )
A.反应前后分子个数不变 B.该反应中生成C和D的质量比为14:1
C.若有16g的A参加反应,则生成D的质量为6g D.该反应不符合质量守恒定律
14.氢气在氧气中燃烧的化学方程式是:从这个化学方程式获得信息错误的是( )
A.氢气与氧气在点燃的条件下反应生成水
B.每2个氢分子与1个氧分子完全反应,生成2个水分子
C.常温下,每2体积的氢气与1体积的氧气完全反应,生成2体积的水
D.每4份质量的氢气与32份质量的氧气完全反应,生成36份质量的水
15.在反应2CO+O22CO2中,各物质间的质量比为( )
A.2:1:2 B.56:32:88 C.28:32:44 D.1:1:2
16.下列方法中,可用来鉴别CO和CO2的有( )
①通入紫色的石蕊试液;②通入澄清的石灰水;③点燃;④通过灼热的CuO.
A.②③ B.②④ C.①②④ D.①②③④
17.实验室用15.8g高锰酸钾放在试管里加热制氧气,反应一段时间后,称得剩余物质的质量为14.3g则剩余物是( )
A.MnO2 K2MnO4 B.K2MnO4
C.MnO2 K2MnO4 KMnO4 D.K2MnO4 KMnO4
18.某物质4.6g在空气中完全燃烧生成8.8g二氧化碳和5.4g水,则关于这种物质的组成描述正确的是( )
A.该物质只含有碳元素和氢元素
B.该物质中碳元素与氢元素的质量比为12︰1
C.该物质一定含有碳元素、氢元素和氧元素
D.该物质的分子中碳原子与氢原子的个数比为1︰3
19.将N2、CO2、H2O(气体)、CO的混合气体依次通过澄清的石灰水、灼热的氧化铜和浓硫酸(干燥剂)(每步都是充分反应),最终得到的气体成分是( )
A.氮气 B.氮气和水蒸气
C.氮气和一氧化碳 D.氮气和二氧化碳
20.把20g氢气和氧气的混合气体充入一密闭容器中(密闭容器里无其他杂质)经火花点火充分反应后,有18g水生成,原混合气体中氢气与氧气的质量比可能为( )
A.1:4 B.1:8 C.9:1 D. 1:9
二、填空题(每空一分共 28分)
21.从氧气、一氧化碳、二氧化碳等气体中,选择合适的气体用化学式填空:
(1)具有可燃性的气体是______ (2) 能使紫色石蕊溶液变红的气体是 ____
(3) 有毒的气体是_ ____ (4)能使带火星的木条复燃的气体是_______
22.质量守恒定律是自然科学的基本定律之一,化学反应遵循质量守恒定律。
(1)化学反应前后,肯定不会变化的是______(填序号)
①元素的种类 ②原子的数目 ③分子的数目 ④物质的种类 ⑤原子的种类 ⑥物质的体积总和 ⑦反应前后物质的质量总和
(2)在化学反应中,已知7gA与20gB恰好完全反应,生成8gC和______gD,要制得3.8gD,则参加反应的A的质量为______g。
23.下面是某化学反应前后的微观模拟图,请根据图示回答:
(1)该化学反应中,参加反应的“”和“”与反应后生成的“”各粒子间的个数比为______________。(2)该反应的基本反应类型为______________。
(3)根据图所示,写出一个符合该反应的化学方程式______________。
24.如图所示,向盛有红棕色二氧化氮气体的集气瓶里投入几小块木炭,最终观察到红棕色______(填“变深”、“消失”或“不变”),漏斗中液面______(填“上升”、“下降”或“不变”).其原因为:木炭具有______作用,使瓶中气体压强______外界大气压.(填“大于”、“小于”或“等于”)
25.如图是金刚石、石墨、C60、碳纳米管结构示意图。请回答下列问题:
(1)金刚石是立体网状结构,金刚石是自然界存在的最___________的物质
(2)石墨为层状结构,层与层之间能滑动,因此石墨有润滑性,可以用作___________
(3)一定条件下,石墨转化成金刚石,该变化是___________变化,碳纳米管的物理性质与金刚石、石墨不同是因为 。
26.实验室制取二氧化碳时,不能用浓盐酸代替稀盐酸的原因是
一氧化碳和二氧化碳化学性质不同的原因是
27.早在1979年在瑞士日内瓦召开的第一次世界气候大会上,科学家警告说,大气中二氧化碳气体浓度的增加将导致地球呈“病态”。而且近年来,空气质量问题频发,引起了世界各国人民的关注。
(1)固态的二氧化碳俗称_______________。菜农定期会向蔬菜大棚中补充二氧化碳,这样做有利于植物进行___________作用。
(2)二氧化碳气体浓度的增加将导致地球呈现出哪些“病态”?任写一条。 (3)洁净的空气对人类非常重要.下列做法有利于净化空气的是___________(填序号)。
①使用清洁能源 ②工业废气处理后达标排放 ③积极植树造林
28.如图是二氧化碳的性质探究实验:
(1)图1中观察到的现象是: ,
此实验说明二氧化碳的化学性质是
(2)图2中,向盛有CO2的软塑料瓶中加入约1/3的水,立即拧紧瓶盖振荡,观察到的现象是:___________,由此得出的结论是:____________。
三、实验题(每空1分共24分)
29.某校化学兴趣小组在老师的引导下进行“化学反应中,反应物与生成物的质量关系”的实验探究。他们使用的实验装置和选用药品如图所示,现分别以A、B、C表示如下:
A、B、C三个实验分别由甲、 乙、丙三个组 的同学来完成,他们都进行了规范的操作、准确的称量和细致的观察。回答下列问题
(1) A实验:引燃白磷待反应结束锥形瓶冷却后,重新放到托盘天平上称量,天平平衡。甲组同学得出的结论是:质量守恒。该实验过程中小气球的变化是 。
锥形瓶底沙子的作用是
(2)乙组同学用B实验验证了质量守恒定律;反应的化学方程式是_____。
(3)丙组同学得到的错误结论是“C实验说明质量不守恒”。你认为C实验天平不平衡的原因是 。若用该反应验证质量守恒定律,则需将该反应置于 ____容器中进行。
30.实验室制取气体的部分装置如图所示,请回答下列问题:
(1) 实验室制取二氧化碳的药品是 和稀盐酸(填名称),
(2)反应的化学方程式为 ,
(3 )用装置C收集二氧化碳理由是
若用装置F收集二氧化碳,气体应从导管______(选填“b”或“c”)口处通入,检验二氧化碳已收集满的方法是__ ________。
(4)通常状况下,硫化氢(H2S)是一种密度比空气大且能溶于水的气体,实验室常用块状硫化亚铁(FeS)和稀硫酸在常温下反应制取硫化氢气体,则制取硫化氢气体可选用的装置组合是______(填字母)。
31.如图所示是木炭还原氧化铜的实验,回答
(1)酒精灯加网罩的目的是:_______
(2)观察到试管A 中的现象
反应的化学方程式为
(3)B试管澄清石灰水变浑浊,反应的化学方程式为 。
32.兴趣小组为探究一氧化碳具有还原性,设计了如下实验装置。请回答以下有关问题:
(1) 实验开始时,先通入CO一段时间后再加热,其原因是___________。
(2)实验中图A处玻璃管中发生的现象是_________,其化学反应方程式为________。
(3) 该装置中有一个明显的缺陷是 。
33.某同学设计了如下一组实验。取4朵用石蕊溶液染成紫色的干燥纸花,分别按图进行实验。试回答下列问题:
(1)观察到纸花的颜色变化是:
Ⅰ 纸花变红, Ⅱ ___ _____, Ⅲ 纸花不变色, Ⅳ _________;
(2)该同学进行的Ⅰ、Ⅱ两项实验说明了酸能使紫色石蕊溶液变红; 该同学进行的Ⅲ、Ⅳ两项实验说明了_____ ________。
(3)将第四朵小花取出,小心烘烤,出现的现象是________________,原因是(用化学方程式解释) 。
四、计算题(8分)
34.把一定质量的氯酸钾和二氧化锰混合物放入大试管中加热至质量不再变化为止。实验测得固体混合物质量随加热时间变化的相关数据如图所示。
请计算:
(1)产生氧气的质量是___________g。
(2)原混合物中氯酸钾的质量
35.化学兴趣小组的同学为了测定某大理石中碳酸钙的含量,进行了如下实验:取12.5g大理石样品于烧杯中,逐渐加入稀盐酸(杂质不与稀盐酸反应),产生二氧化碳的质量与所加稀盐酸的质量关系如图所示。请计算:
(1)生成二氧化碳的质量是_______g
(2)该大理石中碳酸钙的质量分数
参考答案:
1.B2.C3.B4.C5.B6.B 7.A8.C9.C10.C11.D12.C13.C14.C15.B
16.D 17.C 18.C D 19.D 20.A D
21. CO CO2 CO O2 22.(1)①②⑤⑦(2) 19 1.4
23. 2:1:2 化合反应
24. 消失 上升 吸附 小于
25.(1)硬 (2)润滑剂 (3) 化学 碳原子的排列方式不同
26. 浓盐酸具有挥发性,挥发出的氯化氢气体使制得的二氧化碳不纯
分子的构成不同
27. 干冰 光合 冰川融化,海平面上升等 ① ② ③
28. 下层蜡烛先熄灭,上层蜡烛后熄灭 二氧化碳不燃烧,不支持燃烧
软塑料瓶变瘪 二氧化碳能溶于水
29. 先变大后变小 防止锥形瓶受热不均而炸裂 过氧化氢在二氧化锰催化作用下分解生成水和氧气,氧气逸出装置外导致天平不平衡 密闭
30. 石灰石(或大理石)
(3)密度比空气大 c 将燃着的木条放在b导管口处,燃着木条熄灭,二氧化碳集满
(4) B C 31.(1)集中火焰,提高温度(2) 黑色固体逐渐变红 (3) CO2+Ca(OH)2=CaCO3↓+H2O
32.(1)排尽装置内的空气,防止加热时发生爆炸
(2) 黑色粉末逐渐变成红色 CuO+COCu+CO2 (3) 没有处理尾气
33. 纸花不变色(或仍为紫色) 纸花变红 二氧化碳与水反应生成酸性物质
纸花由红色又变成紫色 H2CO3 =CO2↑+H2O
34.(1)9.6 (2) 24.5g 35.(1)4.4 (2) 80%
答案第2页,共2页
可能用到的相对原子质量:H:1、C:12、O:16、Cl:35.5、K:39、Mn:55、K:40
一、选择题(1-15小题每题只有一个选项符合题意,16-20小题每题有一个或两个选项符合题意)
1.下列有关内容用质量守恒定律解释正确的是 ( )
A.10mL水和10mL酒精混合后,总体积一定是20mL
B.某化合物在氧气中燃烧生成了水和二氧化碳,则该化合物一定含碳元素和氢元素
C.煤燃烧后产生的煤渣的质量一定等于所用煤的质量
D.将5gA和5gB混合后发生化合反应,一定能生成10gC
2.氯碱工业的反应原理是电解饱和食盐水(主要成分为NaCl和H2O),下列物质不可能是氯碱工业产品的是 ( )
A.H2 B.Cl2 C.Na2CO3 D.NaOH
3.下列实验能够直接用于验证质量守恒定律的是 ( )
A.B.C. D.
4.今年2月美国俄亥俄州的氯乙烯泄漏事件给当地居民的健康造成严重损害。氯乙烯(C2H3C1)有致癌性,是易燃气体,完全燃烧的反应方程式为,其中X的化学式为( )
A.H2 B.CO C.HCl D.Cl2
5.下列反应的化学方程式书写正确的是( )
A. B.
C. D.
6.在A+3B=2C+2D的反应中,14gA和48gB恰好完全反应生成44gC和一定质量的D,若D的相对分子质量为18,则B的相对分子质量是( )
A.16 B.32 C.48 D.96
7.甲、乙、丙、丁四种物质在反应前后的质量关系如图所示,下列有关说法不正确的是
A.参加反应的甲和乙质量比为12:7 B.X的值为7
C.丁一定是化合物 D.该反应类型为化合反应
8.下列关于化学反应 2X+Y=2Z 的叙述,不正确的是 ( )
A.Z一定是化合物 B.若a g X与 b g Y 充分反应,生成 Z 的质量可能为(a+b)g
C.若X和Y的相对分子质量分别为 m 和 n,则 Z 的相对分子质量为 m+n
D.在反应中 X、Y、Z 三种物质的粒子数目比为 2∶1∶2
9.下列物质的性质和用途对应关系正确的是( )
A.炭黑具有还原性,可制作墨水 B.石墨具有导电性,可制作铅笔芯
C.金刚石硬度大,可用于切割玻璃 D.木炭具有吸附性,可用作燃料
10.下列关于碳及其氧化物的说法中,正确的是( )
A.在室内放一盆澄清石灰水可防止CO中毒
B.制糖工业用活性炭脱色制白糖是因为活性炭与有色物质发生了化学反应
C.用炭黑墨汁书写的字经久不变色是因为常温下碳的化学性质稳定
D.CO2通入紫色石蕊溶液,溶液变红,加热后溶液颜色不变
11.有关的CO2实验如下,只能证明CO2物理性质的是( )
A. B.
C. D.
12.要除去二氧化碳气体中混有的一氧化碳气体,最好的方法是:( )
A.使气体通过灼热的焦炭 B.使气流缓慢的通过足量的澄清石灰水
C.使气体通过灼热的氧化铜 D.通入氧气流点燃
13.构建模型是化学学习常用的方法,如图为某化学反应的微观模拟示意图,请判断下列说法,正确的是( )
A.反应前后分子个数不变 B.该反应中生成C和D的质量比为14:1
C.若有16g的A参加反应,则生成D的质量为6g D.该反应不符合质量守恒定律
14.氢气在氧气中燃烧的化学方程式是:从这个化学方程式获得信息错误的是( )
A.氢气与氧气在点燃的条件下反应生成水
B.每2个氢分子与1个氧分子完全反应,生成2个水分子
C.常温下,每2体积的氢气与1体积的氧气完全反应,生成2体积的水
D.每4份质量的氢气与32份质量的氧气完全反应,生成36份质量的水
15.在反应2CO+O22CO2中,各物质间的质量比为( )
A.2:1:2 B.56:32:88 C.28:32:44 D.1:1:2
16.下列方法中,可用来鉴别CO和CO2的有( )
①通入紫色的石蕊试液;②通入澄清的石灰水;③点燃;④通过灼热的CuO.
A.②③ B.②④ C.①②④ D.①②③④
17.实验室用15.8g高锰酸钾放在试管里加热制氧气,反应一段时间后,称得剩余物质的质量为14.3g则剩余物是( )
A.MnO2 K2MnO4 B.K2MnO4
C.MnO2 K2MnO4 KMnO4 D.K2MnO4 KMnO4
18.某物质4.6g在空气中完全燃烧生成8.8g二氧化碳和5.4g水,则关于这种物质的组成描述正确的是( )
A.该物质只含有碳元素和氢元素
B.该物质中碳元素与氢元素的质量比为12︰1
C.该物质一定含有碳元素、氢元素和氧元素
D.该物质的分子中碳原子与氢原子的个数比为1︰3
19.将N2、CO2、H2O(气体)、CO的混合气体依次通过澄清的石灰水、灼热的氧化铜和浓硫酸(干燥剂)(每步都是充分反应),最终得到的气体成分是( )
A.氮气 B.氮气和水蒸气
C.氮气和一氧化碳 D.氮气和二氧化碳
20.把20g氢气和氧气的混合气体充入一密闭容器中(密闭容器里无其他杂质)经火花点火充分反应后,有18g水生成,原混合气体中氢气与氧气的质量比可能为( )
A.1:4 B.1:8 C.9:1 D. 1:9
二、填空题(每空一分共 28分)
21.从氧气、一氧化碳、二氧化碳等气体中,选择合适的气体用化学式填空:
(1)具有可燃性的气体是______ (2) 能使紫色石蕊溶液变红的气体是 ____
(3) 有毒的气体是_ ____ (4)能使带火星的木条复燃的气体是_______
22.质量守恒定律是自然科学的基本定律之一,化学反应遵循质量守恒定律。
(1)化学反应前后,肯定不会变化的是______(填序号)
①元素的种类 ②原子的数目 ③分子的数目 ④物质的种类 ⑤原子的种类 ⑥物质的体积总和 ⑦反应前后物质的质量总和
(2)在化学反应中,已知7gA与20gB恰好完全反应,生成8gC和______gD,要制得3.8gD,则参加反应的A的质量为______g。
23.下面是某化学反应前后的微观模拟图,请根据图示回答:
(1)该化学反应中,参加反应的“”和“”与反应后生成的“”各粒子间的个数比为______________。(2)该反应的基本反应类型为______________。
(3)根据图所示,写出一个符合该反应的化学方程式______________。
24.如图所示,向盛有红棕色二氧化氮气体的集气瓶里投入几小块木炭,最终观察到红棕色______(填“变深”、“消失”或“不变”),漏斗中液面______(填“上升”、“下降”或“不变”).其原因为:木炭具有______作用,使瓶中气体压强______外界大气压.(填“大于”、“小于”或“等于”)
25.如图是金刚石、石墨、C60、碳纳米管结构示意图。请回答下列问题:
(1)金刚石是立体网状结构,金刚石是自然界存在的最___________的物质
(2)石墨为层状结构,层与层之间能滑动,因此石墨有润滑性,可以用作___________
(3)一定条件下,石墨转化成金刚石,该变化是___________变化,碳纳米管的物理性质与金刚石、石墨不同是因为 。
26.实验室制取二氧化碳时,不能用浓盐酸代替稀盐酸的原因是
一氧化碳和二氧化碳化学性质不同的原因是
27.早在1979年在瑞士日内瓦召开的第一次世界气候大会上,科学家警告说,大气中二氧化碳气体浓度的增加将导致地球呈“病态”。而且近年来,空气质量问题频发,引起了世界各国人民的关注。
(1)固态的二氧化碳俗称_______________。菜农定期会向蔬菜大棚中补充二氧化碳,这样做有利于植物进行___________作用。
(2)二氧化碳气体浓度的增加将导致地球呈现出哪些“病态”?任写一条。 (3)洁净的空气对人类非常重要.下列做法有利于净化空气的是___________(填序号)。
①使用清洁能源 ②工业废气处理后达标排放 ③积极植树造林
28.如图是二氧化碳的性质探究实验:
(1)图1中观察到的现象是: ,
此实验说明二氧化碳的化学性质是
(2)图2中,向盛有CO2的软塑料瓶中加入约1/3的水,立即拧紧瓶盖振荡,观察到的现象是:___________,由此得出的结论是:____________。
三、实验题(每空1分共24分)
29.某校化学兴趣小组在老师的引导下进行“化学反应中,反应物与生成物的质量关系”的实验探究。他们使用的实验装置和选用药品如图所示,现分别以A、B、C表示如下:
A、B、C三个实验分别由甲、 乙、丙三个组 的同学来完成,他们都进行了规范的操作、准确的称量和细致的观察。回答下列问题
(1) A实验:引燃白磷待反应结束锥形瓶冷却后,重新放到托盘天平上称量,天平平衡。甲组同学得出的结论是:质量守恒。该实验过程中小气球的变化是 。
锥形瓶底沙子的作用是
(2)乙组同学用B实验验证了质量守恒定律;反应的化学方程式是_____。
(3)丙组同学得到的错误结论是“C实验说明质量不守恒”。你认为C实验天平不平衡的原因是 。若用该反应验证质量守恒定律,则需将该反应置于 ____容器中进行。
30.实验室制取气体的部分装置如图所示,请回答下列问题:
(1) 实验室制取二氧化碳的药品是 和稀盐酸(填名称),
(2)反应的化学方程式为 ,
(3 )用装置C收集二氧化碳理由是
若用装置F收集二氧化碳,气体应从导管______(选填“b”或“c”)口处通入,检验二氧化碳已收集满的方法是__ ________。
(4)通常状况下,硫化氢(H2S)是一种密度比空气大且能溶于水的气体,实验室常用块状硫化亚铁(FeS)和稀硫酸在常温下反应制取硫化氢气体,则制取硫化氢气体可选用的装置组合是______(填字母)。
31.如图所示是木炭还原氧化铜的实验,回答
(1)酒精灯加网罩的目的是:_______
(2)观察到试管A 中的现象
反应的化学方程式为
(3)B试管澄清石灰水变浑浊,反应的化学方程式为 。
32.兴趣小组为探究一氧化碳具有还原性,设计了如下实验装置。请回答以下有关问题:
(1) 实验开始时,先通入CO一段时间后再加热,其原因是___________。
(2)实验中图A处玻璃管中发生的现象是_________,其化学反应方程式为________。
(3) 该装置中有一个明显的缺陷是 。
33.某同学设计了如下一组实验。取4朵用石蕊溶液染成紫色的干燥纸花,分别按图进行实验。试回答下列问题:
(1)观察到纸花的颜色变化是:
Ⅰ 纸花变红, Ⅱ ___ _____, Ⅲ 纸花不变色, Ⅳ _________;
(2)该同学进行的Ⅰ、Ⅱ两项实验说明了酸能使紫色石蕊溶液变红; 该同学进行的Ⅲ、Ⅳ两项实验说明了_____ ________。
(3)将第四朵小花取出,小心烘烤,出现的现象是________________,原因是(用化学方程式解释) 。
四、计算题(8分)
34.把一定质量的氯酸钾和二氧化锰混合物放入大试管中加热至质量不再变化为止。实验测得固体混合物质量随加热时间变化的相关数据如图所示。
请计算:
(1)产生氧气的质量是___________g。
(2)原混合物中氯酸钾的质量
35.化学兴趣小组的同学为了测定某大理石中碳酸钙的含量,进行了如下实验:取12.5g大理石样品于烧杯中,逐渐加入稀盐酸(杂质不与稀盐酸反应),产生二氧化碳的质量与所加稀盐酸的质量关系如图所示。请计算:
(1)生成二氧化碳的质量是_______g
(2)该大理石中碳酸钙的质量分数
参考答案:
1.B2.C3.B4.C5.B6.B 7.A8.C9.C10.C11.D12.C13.C14.C15.B
16.D 17.C 18.C D 19.D 20.A D
21. CO CO2 CO O2 22.(1)①②⑤⑦(2) 19 1.4
23. 2:1:2 化合反应
24. 消失 上升 吸附 小于
25.(1)硬 (2)润滑剂 (3) 化学 碳原子的排列方式不同
26. 浓盐酸具有挥发性,挥发出的氯化氢气体使制得的二氧化碳不纯
分子的构成不同
27. 干冰 光合 冰川融化,海平面上升等 ① ② ③
28. 下层蜡烛先熄灭,上层蜡烛后熄灭 二氧化碳不燃烧,不支持燃烧
软塑料瓶变瘪 二氧化碳能溶于水
29. 先变大后变小 防止锥形瓶受热不均而炸裂 过氧化氢在二氧化锰催化作用下分解生成水和氧气,氧气逸出装置外导致天平不平衡 密闭
30. 石灰石(或大理石)
(3)密度比空气大 c 将燃着的木条放在b导管口处,燃着木条熄灭,二氧化碳集满
(4) B C 31.(1)集中火焰,提高温度(2) 黑色固体逐渐变红 (3) CO2+Ca(OH)2=CaCO3↓+H2O
32.(1)排尽装置内的空气,防止加热时发生爆炸
(2) 黑色粉末逐渐变成红色 CuO+COCu+CO2 (3) 没有处理尾气
33. 纸花不变色(或仍为紫色) 纸花变红 二氧化碳与水反应生成酸性物质
纸花由红色又变成紫色 H2CO3 =CO2↑+H2O
34.(1)9.6 (2) 24.5g 35.(1)4.4 (2) 80%
答案第2页,共2页
同课章节目录
