第三章铁 金属材料单元测试(含解析) 高一上学期化学人教版(2019)必修第一册
文档属性
| 名称 | 第三章铁 金属材料单元测试(含解析) 高一上学期化学人教版(2019)必修第一册 |

|
|
| 格式 | docx | ||
| 文件大小 | 481.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-06-10 00:00:00 | ||
图片预览




文档简介
第三章 铁 金属材料 单元测试
一、单选题
1.利用铜矿石(主要成分为,还含少量,,制备晶体的流程如下图所示。已知在酸性条件下不稳定,易生成金属和,下列说法错误的是
A.“滤渣1”的成分为、
B.“氧化”过程中的离子方程式:
C.“调”所用的试剂a可选用
D.操作X为蒸发浓缩、冷却结晶、过滤、洗涤、干燥
2.向含有c(FeCl3)=0.2mol L﹣1、c(FeCl2)=0.1mol L﹣1的混合溶液中滴加稀NaOH溶液可得到一种黑色分散系,其中分散质粒子是直径约为9.3nm的金属氧化物,下列有关说法中正确的是
A.该分散系的分散质为Fe2O3
B.可用过滤的方法将黑色金属氧化物与NaCl分离开
C.在电场作用下,阴极附近分散系黑色变深,则说明该分散系带正电荷
D.当光束通过该分散系时,可以看到一条光亮的“通路”
3.下列关于铁及其化合物的说法正确的是
A.红热的铁能与水蒸气反应,生成和
B.在空气中充分灼烧得到FeO
C.FeO是一种黑色粉末,不稳定,在空气中受热,迅速转化成红棕色粉末
D.过量铁与氯气或者稀盐酸反应均可制得
4.下列分子或离子在指定的分散系中一定能大量共存的一组是
A.空气:
B.氢氧化铁胶体:
C.使酚酞变红的溶液:
D.与反应放出的溶液:
5.下列除去杂质的实验方法正确的是(括号里为少量杂质)
A.CO2( CO):用酒精灯点燃
B.K2CO3( NaHCO3):置于坩埚中加热
C.FeCl2( FeCl3):加入足量铜粉,过滤
D.Fe2O3(Al2O3):氢氧化钠溶液,过滤、洗涤
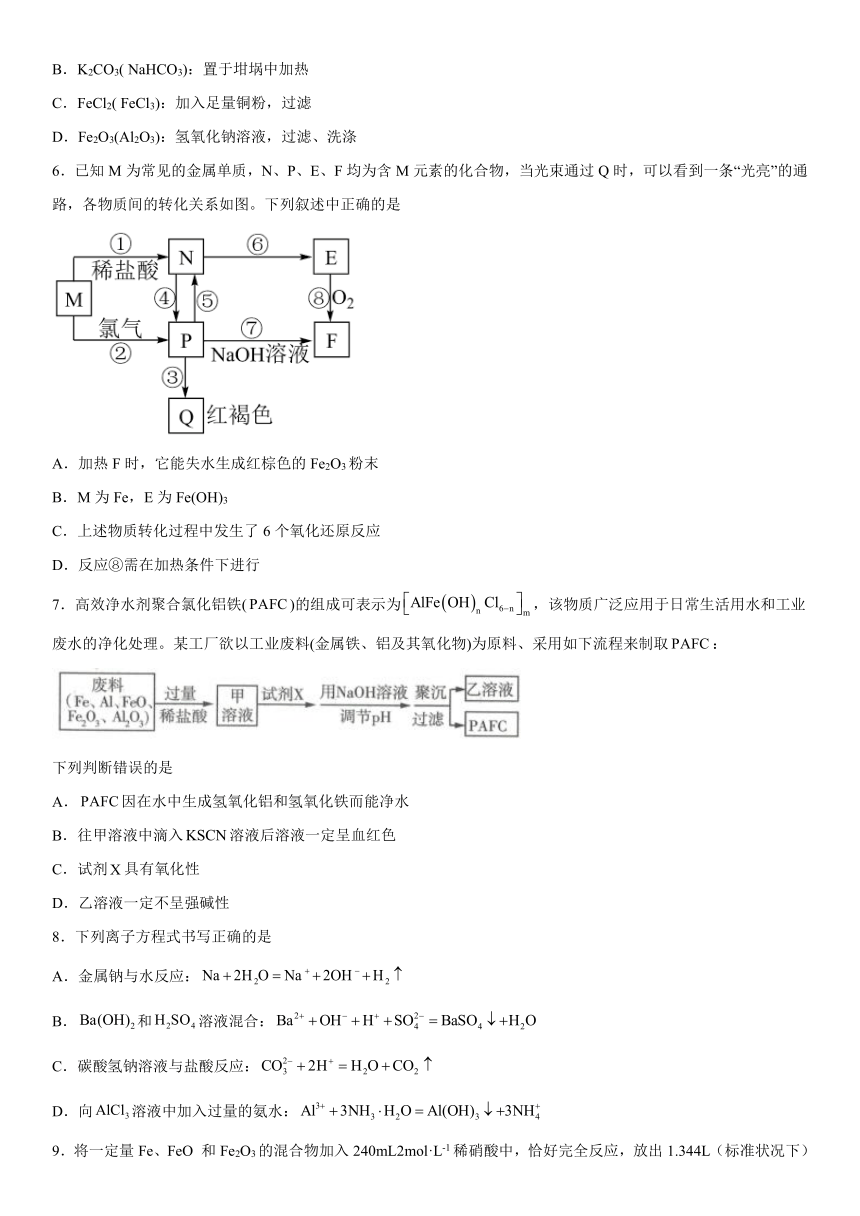
6.已知M为常见的金属单质,N、P、E、F均为含M元素的化合物,当光束通过Q时,可以看到一条“光亮”的通路,各物质间的转化关系如图。下列叙述中正确的是
A.加热F时,它能失水生成红棕色的Fe2O3粉末
B.M为Fe,E为Fe(OH)3
C.上述物质转化过程中发生了6个氧化还原反应
D.反应⑧需在加热条件下进行
7.高效净水剂聚合氯化铝铁()的组成可表示为,该物质广泛应用于日常生活用水和工业废水的净化处理。某工厂欲以工业废料(金属铁、铝及其氧化物)为原料、采用如下流程来制取:
下列判断错误的是
A.因在水中生成氢氧化铝和氢氧化铁而能净水
B.往甲溶液中滴入溶液后溶液一定呈血红色
C.试剂具有氧化性
D.乙溶液一定不呈强碱性
8.下列离子方程式书写正确的是
A.金属钠与水反应:
B.和溶液混合:
C.碳酸氢钠溶液与盐酸反应:
D.向溶液中加入过量的氨水:
9.将一定量Fe、FeO 和Fe2O3的混合物加入240mL2mol·L-1稀硝酸中,恰好完全反应,放出1.344L(标准状况下)NO 气体,往所得溶液中加入酸性KMnO4溶液,无明显现象。若用足量的H2在加热条件下与相同质量的上述混合物充分反应,能得到铁的质量为
A.6.72g B.7.84g C.8.96g D.13.4g
10.下列关于铁单质的说法中不正确的是
A.3 mol单质Fe完全转变为Fe3O4,失去8NA个电子
B.装月饼的袋子里常放有干燥剂和铁粉,这是利用了铁粉的还原性
C.常温下,Fe与H2O不反应,但在空气中O2、H2O的共同作用下能发生氧化反应
D.56 g铁和71 g氯气完全反应,转移的电子数为3NA
二、填空题
11.NaNO2外观和食盐相似,又有咸味,容易使人误食中毒。已知NaNO2能发生如下反应:
2NaNO2+4HI=2NO↑+I2+2NaI+2H2O。
(1)NaNO2中N的化合价为___。
(2)为了获取反应后溶液中的I2,可采用_______方法
(3)将上述化学方程式改写为离子方程式并用双线桥标明电子转移的方向和数目:______
(4)根据上述离子反应,鉴别NaNO2和NaCl。可选用的物质有:①碘化钾淀粉试纸 (试纸上含KI和淀粉) ②淀粉 ③白酒 ④食醋,你认为应选用的物质有_________(填序号)。
(5)若产生的气体在标准状况下体积为2.24L,则反应过程中转移电子的数目为___NA,(NA表示阿伏伽德罗常数的值),被氧化的HI的物质的量为____,发生反应的NaNO2的质量为____ g.
12.请设计尽可能多的实验方案,在实验室中制备____________。
13.铁及其重要化合物的“价类二维图”如下图所示。
(1)该“价类二维图”中缺失的类别A应为_______。
(2)生活中的钢铁制品如废旧铁锅,使用时间长久后若要丢弃,应归为_______。
A.干垃圾 B.湿垃圾 C.有毒有害垃圾 D.可回收垃圾
(3)在烧制砖瓦时,用黏土做成的坯经过烘烧后,铁的化合物转化成_______(填字母,下同)而制得红色砖瓦;若烘烧后期从窑顶向下慢慢浇水,窑内会产生大量CO、H2气体,它们把该红色物质还原成黑色的_______,同时还有未燃烧的碳的颗粒,而制得了青色砖瓦。
A.Fe2O3 B.Fe3O4 C.FeO D.Fe(OH)3
(4)要实现Fe转化为Fe2+,可选用足量的_______(填字母)
A.稀盐酸 B.溶液 C.稀硝酸 D.浓硫酸
(5)要实现Fe转化为,除了将Fe与氧气点燃外,另外的方法是(写出化学方程式)_______。
14.将xgFe、FeO和Fe2O3混合物分成两等份,向其中一份中滴加500mL稀硝酸,固体恰好完全溶解并产生标准状况下NO气体aL,溶液中Fe元素均以+3价形式存在,另一份固体与足量H2反应质量减少yg。根据以上数据计算稀硝酸的浓度为___mol·L-1(写出计算过程)。
15.实验室常用加热高锰酸钾的方法制备少量氧气。
(1)请写出该反应的化学方程式___________。
(2)现欲制备3.36L(标准状况)氧气,理论上需要________克高锰酸钾?
(3)用制备的3.36L(标准状况)氧气与H2完全反应生成水,理论上需要________升H2的体积(标准状况)?
三、计算题
16.将45.0gFeC2O4 2H2O隔绝空气加热使之分解,最终可得到19. 6g某种铁的氧化物,请通过计算推测该铁的氧化物的组成:_______(写出化学式)。并写出计算过程:_______
17.蛋白质在一定条件下与浓硫酸反应可转化为硫酸铵,后者在浓氢氧化钠溶液和水蒸气作用下,其中的氮元素可转化为氨放出。现用30.0mL牛奶进行上述实验,将牛奶中蛋白质里的氮元素完全转化成氨,再用50.0mL硫酸溶液吸收放出的氨,剩余的酸用38.0mL氢氧化钠溶液可恰好完全中和。
(1)30.0mL牛奶中共含有_______克氮?
(2)如果牛奶中蛋白质含氮16%(质量分数),则牛奶中蛋白质的质量分数是______?(已知牛奶的密度是)
四、实验题
18.易被空气中的氧气氧化,故制备时主要是避免氧气的介入。某学生利用稀硫酸A、铁粉B和某碱溶液C在实验室设计了如图装置制备白色固体。
(1)写出易被空气中的氧气氧化的方程式_______。
(2)装置Ⅱ盛放的溶液C是_______(a.NaOH b.);配置该溶液时,为除去蒸馏水中溶解的常采用的方法是_______。
(3)铁粉与稀硫酸制备的离子方程式为_______,的作用有_______(填编号)。
a.驱赶装置内的空气
b.把物质B压入Ⅱ中
c.保护白色不被空气氧化
(4)实验过程中,用针管吸取锥形瓶Ⅰ中的溶液,检验其中是否含有。方法为:用该针管吸取_______溶液,用力振荡几次,溶液不变色,把针管中的混合物全部注入干净试管,振荡几次,溶液慢慢变红色。依据现象得出的结论有_______、_______。
(5)白色沉淀在_____(填“锥形瓶Ⅰ”或“锥形瓶Ⅱ”)内生成,经在无氧环境中干燥处理,得到的白色粉末是很好的化工_______(填“除酸剂”或“除氧剂”)。
19.化学实验兴趣小组探究不同氛围、不同温度下草酸亚铁晶体(FeC2O4·2H2O)的分解产物。
I.甲同学在空气氛围中加热草酸亚铁晶体,分析在400℃左右完全分解得到的固体,可能含有FeO、Fe2O3、Fe3O4中的一-种或多种。
已知:a.Fe3O4能与高浓度盐酸反应,与低浓度盐酸不反应;
b.实验中所用溶液均已做除O2处理。
(1)甲同学对固体成分进行了如下实验探究,请填空:
实验操作 实验现象 实验结论
实验1:取少量固体于试管中,向其中加入足量稀1mol/L盐酸,充分振荡,静置 固体部分溶解 结论一:____
实验2:取少许固体于试管中,向其中加入足量12mol/L浓盐酸,充分振荡 固体部分溶解
实验3:取少量实验1试管中的上层清液于试管中,滴入几滴____ ____ 结论二:固体含有FeO
实验4:____ 无明显现象 结论三:_____
(2)上述实验3对应的离子反应方程式为___________。
II.乙同学将54.0g草酸亚铁晶体(FeC2O4·2H2O,M=180g/mol)在氮气的氛围中加热分解,得到分解产物的热重曲线(样品质量随温度的变化情况)如图所示。
(3)A点时,固体物质的化学式为___________
(4)B点时,固体只含有一种铁的氧化物,则FeC2O4·2H2O晶体400℃时受热分解的化学方程式为___________
参考答案:
1.B
【解析】由流程可知,原料(含Cu2O、Fe3O4、SiO2)与足量稀硫酸作用后得CuSO4、FeSO4虑液和SiO2、Cu滤渣。在滤液中加过氧化氢将Fe2+氧化为Fe3+,然后调节溶液的pH使Fe3+沉淀而得CuSO4溶液,再将CuSO4溶液蒸发浓缩、降温结晶、过滤洗涤即得晶体CuSO4 5H2O。
【解析】A.因Cu+在酸性条件下不稳定,易生成金属Cu和Cu2+,所以硫酸与氧化亚铜反应方程式为:H2SO4+Cu2O=CuSO4+Cu+H2O,四氧化三铁可溶于硫酸,反应方程式为:Fe3O4+4H2SO4=Fe2(SO4)3+FeSO4+4H2O,部分Cu与硫酸铁反应生成硫酸铜和硫酸亚铁,二氧化硅与硫酸不反应,故“滤渣1”的成分为:SiO2、Cu,A正确;
B.滤液中含Cu2+、Fe2+,Fe2+可被过氧化氢氧化为Fe3+,反应的离子方程式为:2Fe2++H2O2+2H+=2Fe3++2H2O,B错误;
C.调节溶液的pH使Fe3+沉淀,为了不引入杂质,试剂a可选用CuO消耗H+来增大pH,C正确;
D.从CuSO4溶液溶液得到带有结晶水的晶体,可以采用蒸发浓缩、冷却结晶、过滤、洗涤、干燥即得晶体CuSO4 5H2O,D正确;
故选B。
2.D
【解析】A.氧化铁是红棕色固体,不是黑色,所以该分散系的分散质不可能是氧化铁,故错误;
B. 分散质粒子是直径约为9.3nm能通过滤纸,故不能用过滤的方法分离黑色固体和氯化钠溶液,故错误;
C. 在电场作用下,阴极附近分散系黑色变深,则说明黑色的微粒带正电荷,但不能说明分散系带正电荷,故错误;
D.该分散系属于胶体,有丁达尔效应,故正确。
故选D。
3.A
【解析】A.铁与水蒸气在高温下生成Fe3O4和H2,故A正确;
B.氢氧化亚铁具有还原性,在空气中灼烧氧气将+2价Fe氧化+3价Fe,最终不能得到FeO,故B错误;
C.FeO是一种黑色粉末,不稳定,在空气里加热,最终被氧化成黑色的Fe3O4,故C错误;
D.铁无论过量还是不足,与氯气在加热条件下反应,均生成FeCl3,故D错误;
答案为A。
4.C
【解析】A.一氧化氮能与空气中的氧气反应,不能大量共存,A错误;
B.氢氧化铁胶体、硫离子均能与氢离子反应,不能大量共存,B错误;
C.使酚酞变红的溶液呈碱性,四种离子都能大量共存,C正确;
D.与反应放出的溶液,可能为酸溶液或碱溶液,铵根离子和氢氧根离子不能大量共存,D错误;
答案选C。
5.D
【解析】根据除杂的基本原则“不减、不增、不污、易分”来分析.也就是,除去杂质的同时,要保证不能使所需物质的量减少,但可以增加,更不能引入新的杂质,生成物还不能造成环境污染,并且,生成物、所选试剂与所需物质要容易分离。
【解析】A.应将气体通过加热的氧化铜,将CO转化成CO2,故A错误;
B.利用碳酸氢钠受热易分解的性质,可将其转换为碳酸钠,碳酸钠仍为杂质,故B错误;
C.FeCl3加入足量铜粉生成FeCl2和CuCl2,引入CuCl2杂质,故C错误;
D.Al2O3与氢氧化钠溶液反应生成NaAlO2,Fe2O3不溶于NaOH溶液,过滤、洗涤,能达到除去Al2O3目的,故D正确;
故选D。
【点睛】解答此类题型不但要明确除杂的基本原则“不减、不增、不污、易分”,而且对课本上常见的物质的性质必须熟悉,易错点B,注意碳酸氢钠受热分解转换为碳酸钠,碳酸钠仍为杂质。
6.A
【解析】由M为常见的金属单质,能与稀盐酸和氯气生成不同化合物可知,M为变价金属,由光束通过红褐色Q时,可以看到一条“光亮”的通路可知,Q为氢氧化铁胶体,则M为铁、N为氯化亚铁、P为氯化铁、E为氢氧化亚铁、F为氢氧化铁。
【解析】A.由分析可知,F为氢氧化铁,氢氧化铁受热会发生分解反应生成氧化铁和水,故A正确;
B.由分析可知,M为铁、E为氢氧化亚铁,故B错误;
C.由物质间的转化关系可知,反应中有化合价变化的反应为①②④⑤⑧,则物质转化过程中发生了5个氧化还原反应,故C错误;
D.氢氧化亚铁的还原性强,反应⑧为常温下氢氧化亚铁与空气中的氧气发生氧化还原反应生成氢氧化铁,故D错误;
故选A。
7.B
【解析】A.在水中可生成具有吸附性的氢氧化铝和氢氧化铁,可用于净水,A不符合题意;
B.由于、以及的物质的量的关系无法确定,故不能确定甲溶液中元素的存在形式,即不能确定溶液中是否存在,则加入溶液后溶液不一定呈血红色,B符合题意;
C.因中为价,故试剂X应为氧化剂,将氧化成,C不符合题意;
D.若乙溶液呈强碱性,因氢氧化铝与氢氧化钠反应生成偏铝酸钠,则不可能生成,故意溶液不一定呈强碱性,D不符合题意。
故选:B。
8.D
【解析】A.金属钠与水反应:,故A错误;
B.和溶液混合,没有按照比例拆分,因此离子方程式为:,故B错误;
C.碳酸氢钠溶液与盐酸反应,碳酸氢根不能拆:,故C错误;
D.向溶液中加入过量的氨水:,故D正确。
综上所述,答案为D。
9.B
【解析】因一定量的Fe、FeO和Fe2O3的混合物中加入240mL 2mol L-1的稀硝酸,恰好使混合物完全溶解,往所得溶液中加入KMnO4的酸性溶液,无明显现象,说明溶液中的溶质为硝酸铁,1.344LNO(标准状况)的物质的量为:=0.06mol,根据氮元素守恒,硝酸铁中的硝酸根离子的物质的量为:0.24L×2mol/L-0.06mol=0.42mol,所以硝酸铁的物质的量为:×0.42mol=0.14mol,由铁元素守恒可知,得到铁的物质的量为n(Fe)=0.14mol,质量为0.14mol×56g/mol=7.84g,答案选B。
【点睛】氮元素守恒在本题中应用比较简便,元素守恒的应用也很关键。
10.D
【解析】A.3 mol单质Fe完全转变为Fe3O4,失去8NA个电子,故A正确;
B.装月饼的袋子里常放有干燥剂和铁粉,铁粉做脱氧剂,利用了铁粉的还原性,故B正确;
C.常温下,Fe与H2O不反应,但在空气中O2、H2O的共同作用下铁能发生氧化反应被锈蚀,故C正确;
D.56 g铁和71 g氯气完全反应,铁有剩余,氯气完全反应生成FeCl3,转移的电子数为2NA,故D错误;
选D。
11.(1)+3
(2)萃取
(3)
(4)①④
(5) 1 1mol 69
【解析】(1)
NaNO2中各元素化合价代数和为0,Na显+1价,O显-2价,设N的化合价为x,1+x+2 (-2)=0,解得x=+3,即N的化合价为+3;
(2)
I2易溶于有机溶剂,可利用CCl4或苯对反应后的碘溶液进行萃取后再蒸馏获得I2,故答案为:萃取;
(3)
N的化合价降低,得到1个电子,I元素的化合价升高生成碘单质失去2个电子,根据氧化还原反应的规律用双线桥标明电子转移的方向和数目如下:;
(4)
根据已知反应可推知,碘化钾在酸性条件下可与亚硝酸钠溶液反应生成碘单质,碘单质遇淀粉变为蓝色,而氯化钠则无此现象,所以选择鉴别得试剂为:碘化钾淀粉试纸、食醋,故答案为:①④;
(5)
对于反应2NaNO2+4HI=2NO↑+I2+2NaI+2H2O,若产生的气体在标准状况下体积为2.24L,即NO的物质的量为1mol,根据关系式2e-2NO可知,反应过程中转移电子的物质的量为1mol,其数目为1NA,(NA表示阿伏伽德罗常数的值),2molNO生成时,4molHI被消耗,只有2molHI被氧化为碘单质,所以当有1molNO生成时,被氧化的HI的物质的量为1mol,发生反应的NaNO2的物质的量为1mol,其质量为=69g,故答案为:1;1mol;69。
12.⑴向铁粉中加入适量稀硫酸溶液;⑵向硫酸铜溶液中加入足量铁粉,过滤;⑶向硫酸铁中加入足量铁粉,过滤;⑷向氧化亚铁中加入适量硫酸溶液。
【解析】硫酸亚铁是盐类,金属与酸反应,金属与盐反应,金属氧化物与酸反应都能得到硫酸亚铁,在实验室中制备有四种方法:⑴向铁粉中加入适量稀硫酸溶液;⑵向硫酸铜溶液中加入足量铁粉,过滤;⑶向硫酸铁中加入足量铁粉,过滤;⑷氧化亚铁中加入适量硫酸溶液;故答案为:⑴向铁粉中加入适量稀硫酸溶液;⑵向硫酸铜溶液中加入足量铁粉,过滤;⑶向硫酸铁中加入足量铁粉,过滤;⑷向氧化亚铁中加入适量硫酸溶液。
13.(1)盐
(2)D
(3) A B
(4)AB
(5)
【解析】(1)
该“价类二维图”中缺失的类别A为Fe2+、Fe3+,亚铁盐、铁盐,应为盐类;
(2)
生活中的钢铁制品如废旧铁锅,使用时间长久后若要丢弃,为金属合金可回收利用,应归为可回收垃圾;答案选D;
(3)
在烧制砖瓦时,用黏土作成的坯经过烘烧后,铁的化合物转化成Fe2O3而制得红色砖瓦,若烘烧后期从窑顶慢慢浇水,发生C+H2O H2+CO,生成还原性气体,与Fe2O3反应生成黑色的化合物F'e3O4,同时还有未燃烧的碳的颗粒,而制得了青色砖瓦;
答案选A;B;
(4)
要实现Fe转化为Fe2+,应选择弱氧化剂,稀盐酸、溶液符合,稀硝酸及浓硫酸氧化性较强不合适,答案选AB;
(5)
要实现Fe转化为,除了将Fe与氧气点燃外,也可将铁粉在高温下与水蒸气反应,反应的化学方程式为。
14.mol·L-1
【解析】根据反应3H2+Fe2O32Fe+3H2O,H2+FeOFe+H2O质量减少yg,减少的质量为氧的质量,所以m(Fe)=(x-y)g,故n(Fe)=mol,再根据 Fe2O3+6HNO3=2Fe(NO3)3+3H2O,3FeO+10HNO3 =3Fe(NO3)3+NO+5H2O,Fe+4HNO3=Fe(NO3)3+NO+2H2O,可得 n(HNO3)= n(Fe)×3+ n(NO),已知n(Fe)=mol=,n(NO)=mol=mol,n(HNO3)=3×+,c(HNO3)===mol/L;
15.(1)2KMnO4K2MnO4+MnO2+O2↑
(2)47.4
(3)6.72
【解析】(1)加热高锰酸钾反应生成锰酸钾、二氧化锰和氧气,化学方程式为2KMnO4 K2MnO4+MnO2+O2↑;
(2)3.36L(标准状况)氧气的物质的量为 ,根据化学反应方程式可知,n(KMnO4)=2n(O2)=0.30mol,需要高锰酸钾的质量为 ;
(3)根据化学反应方程式2H2+O2 2H2O,3.36L(标准状况)氧气的物质的量为 ,需要n(H2)=0.30mol,需要H2的体积(标准状况)为 。
16. Fe5O7 或Fe3O4 Fe2O3或2Fe2O3 FeO ,
【解析】45.0gFeC2O4 2H2O的物质的量为:,则所含Fe的质量为:m(Fe)=0.25mol×56g/mol=14g,最终可得到19. 6g某种铁的氧化物,其中铁的质量14g,则O的质量为:19.6g-14g=5.6g,n(O)=,n(Fe):n(O)=0.25:0.35=5:7,则氧化物的化学式为:Fe5O7 或Fe3O4 Fe2O3或2Fe2O3 FeO,故答案为:Fe5O7 或Fe3O4 Fe2O3或2Fe2O3 FeO;,;
17.(1)0.168
(2)3.4%
【解析】(1)令38mL 1.00mol L-1的 NaOH溶液中和硫酸的物质的量为n,则,解得:n=0.038L×1mol/L×0.5=0.019mol,故吸收氨气的硫酸的物质的量为:0.500mol L-1×0.05mL-0.019mol=0.006mol,令30.0mL牛奶中氮元素的质量是m,则:,所以m=28g×=0.168g,故答案为:0.168;
(2)30mL牛奶的质量为:30mL×1.03g mL-1=30.9g,所以30.9g×ω(蛋白质)×16.0%=0.168g,解得:ω(蛋白质)=3.4%,故答案为:该牛奶中蛋白质的质量分数为3.4%。
18.(1)
(2) a 加热煮沸
(3) abc
(4) KSCN 锥形瓶Ⅰ中溶液不含 溶液注入试管后,空气中的氧气氧化得到,遇变红
(5) 锥形瓶Ⅱ 除氧剂
【解析】装置Ⅰ中,稀硫酸和铁粉反应,生成氢气和硫酸亚铁,产生的氢气能排除装置中的氧气;反应一段时间后,关闭止水夹,则产生的硫酸亚铁会进入装置Ⅱ中,与碱发生反应,生成,据此分析作答。
(1)
易被空气中的氧气氧化,生成氢氧化铁,化学方程式为:,故答案为:;
(2)
硫酸亚铁会进入装置Ⅱ中,与碱发生反应,生成,可知该碱为NaOH;配置该溶液时,为除去蒸馏水中溶解的常采用的方法是加热煮沸,故答案为:a;加热煮沸;
(3)
稀硫酸和铁粉反应,生成氢气和硫酸亚铁,离子方程式为;产生的氢气能驱赶装置内的空气、关闭止水夹,能把物质B压入Ⅱ中、同时防止空气进入装置Ⅱ,保护白色不被空气氧化,故答案为:;abc;
(4)
KSCN遇,溶液会变红色,则用该针管吸取KSCN溶液,用力振荡几次,溶液不变色,说明锥形瓶Ⅰ中溶液不含;把针管中的混合物全部注入干净试管,振荡几次,溶液慢慢变红色,说明溶液注入试管后,空气中的氧气氧化得到,遇变红,故答案为:KSCN;锥形瓶Ⅰ中溶液不含;溶液注入试管后,空气中的氧气氧化得到,遇变红;
(5)
由分析可知,白色沉淀在锥形瓶Ⅱ内生成;易被空气中的氧气氧化,经在无氧环境中干燥处理,得到的白色粉末是很好的化工除氧剂,故答案为:锥形瓶Ⅱ;除氧剂。
19.(1) 固体含有Fe3O4 K3Fe(CN)6溶液 生成蓝色沉淀 取少量实验1试管上层清液于试管中,滴入几滴KSN溶液 固体不含有Fe2O3
(2)3Fe2++2Fe(CN)=Fe3[Fe(CN)6]2↓
(3)FeC2O4
(4)3FeC2O4+2H2O=Fe3O4+4CO↑+2CO2↑+6H2O
【解析】(1)
根据已知信息:Fe3O4能与高浓度盐酸反应,与低浓度盐酸不反应,结合实验1和实验2的现象,可知原固体含有能溶于浓盐酸而不溶于稀盐酸的Fe3O4,则结论一:固体含有Fe3O4;根据实验3,只要证明实验1试管的上层清液含有Fe2+,就可得出固体含有FeO的结论,则可加入几滴K3Fe(CN)6溶液,生成蓝色沉淀,发生反应的离子方程式为3Fe2++2Fe(CN)=Fe3[Fe(CN)6]2↓;根据结论三固体不含有,需要证明实验1试管中的上层清液不含Fe3+,则应加入几滴KSCN溶液,观察无明显现象;
(2)
实验3中Fe2+与K3Fe(CN)6溶液反应生成蓝色沉淀,发生反应的离子方程式为3Fe2++2Fe(CN)=Fe3[Fe(CN)6]2↓;
(3)
n(FeC2O4·2H2O)=,0.3mol FeC2O4的固体质量刚好为43.2g,即热重曲线上A点刚好为FeC2O4;
(4)
B点时,固体只有一种铁的氧化物,m(Fe)=nM=0.3mol×56g/mol=16.8g,则m(O)=23.2g-16.8g=6.4g,n(O)=,n(Fe):n(O)=0.3:04=3:4,则该含铁氧化物的化学式为Fe3O4,则FeC2O4·2H2O晶体400℃时受热分解的化学方程式为3FeC2O4+2H2O=Fe3O4+4CO↑+2CO2↑+6H2O。
一、单选题
1.利用铜矿石(主要成分为,还含少量,,制备晶体的流程如下图所示。已知在酸性条件下不稳定,易生成金属和,下列说法错误的是
A.“滤渣1”的成分为、
B.“氧化”过程中的离子方程式:
C.“调”所用的试剂a可选用
D.操作X为蒸发浓缩、冷却结晶、过滤、洗涤、干燥
2.向含有c(FeCl3)=0.2mol L﹣1、c(FeCl2)=0.1mol L﹣1的混合溶液中滴加稀NaOH溶液可得到一种黑色分散系,其中分散质粒子是直径约为9.3nm的金属氧化物,下列有关说法中正确的是
A.该分散系的分散质为Fe2O3
B.可用过滤的方法将黑色金属氧化物与NaCl分离开
C.在电场作用下,阴极附近分散系黑色变深,则说明该分散系带正电荷
D.当光束通过该分散系时,可以看到一条光亮的“通路”
3.下列关于铁及其化合物的说法正确的是
A.红热的铁能与水蒸气反应,生成和
B.在空气中充分灼烧得到FeO
C.FeO是一种黑色粉末,不稳定,在空气中受热,迅速转化成红棕色粉末
D.过量铁与氯气或者稀盐酸反应均可制得
4.下列分子或离子在指定的分散系中一定能大量共存的一组是
A.空气:
B.氢氧化铁胶体:
C.使酚酞变红的溶液:
D.与反应放出的溶液:
5.下列除去杂质的实验方法正确的是(括号里为少量杂质)
A.CO2( CO):用酒精灯点燃
B.K2CO3( NaHCO3):置于坩埚中加热
C.FeCl2( FeCl3):加入足量铜粉,过滤
D.Fe2O3(Al2O3):氢氧化钠溶液,过滤、洗涤
6.已知M为常见的金属单质,N、P、E、F均为含M元素的化合物,当光束通过Q时,可以看到一条“光亮”的通路,各物质间的转化关系如图。下列叙述中正确的是
A.加热F时,它能失水生成红棕色的Fe2O3粉末
B.M为Fe,E为Fe(OH)3
C.上述物质转化过程中发生了6个氧化还原反应
D.反应⑧需在加热条件下进行
7.高效净水剂聚合氯化铝铁()的组成可表示为,该物质广泛应用于日常生活用水和工业废水的净化处理。某工厂欲以工业废料(金属铁、铝及其氧化物)为原料、采用如下流程来制取:
下列判断错误的是
A.因在水中生成氢氧化铝和氢氧化铁而能净水
B.往甲溶液中滴入溶液后溶液一定呈血红色
C.试剂具有氧化性
D.乙溶液一定不呈强碱性
8.下列离子方程式书写正确的是
A.金属钠与水反应:
B.和溶液混合:
C.碳酸氢钠溶液与盐酸反应:
D.向溶液中加入过量的氨水:
9.将一定量Fe、FeO 和Fe2O3的混合物加入240mL2mol·L-1稀硝酸中,恰好完全反应,放出1.344L(标准状况下)NO 气体,往所得溶液中加入酸性KMnO4溶液,无明显现象。若用足量的H2在加热条件下与相同质量的上述混合物充分反应,能得到铁的质量为
A.6.72g B.7.84g C.8.96g D.13.4g
10.下列关于铁单质的说法中不正确的是
A.3 mol单质Fe完全转变为Fe3O4,失去8NA个电子
B.装月饼的袋子里常放有干燥剂和铁粉,这是利用了铁粉的还原性
C.常温下,Fe与H2O不反应,但在空气中O2、H2O的共同作用下能发生氧化反应
D.56 g铁和71 g氯气完全反应,转移的电子数为3NA
二、填空题
11.NaNO2外观和食盐相似,又有咸味,容易使人误食中毒。已知NaNO2能发生如下反应:
2NaNO2+4HI=2NO↑+I2+2NaI+2H2O。
(1)NaNO2中N的化合价为___。
(2)为了获取反应后溶液中的I2,可采用_______方法
(3)将上述化学方程式改写为离子方程式并用双线桥标明电子转移的方向和数目:______
(4)根据上述离子反应,鉴别NaNO2和NaCl。可选用的物质有:①碘化钾淀粉试纸 (试纸上含KI和淀粉) ②淀粉 ③白酒 ④食醋,你认为应选用的物质有_________(填序号)。
(5)若产生的气体在标准状况下体积为2.24L,则反应过程中转移电子的数目为___NA,(NA表示阿伏伽德罗常数的值),被氧化的HI的物质的量为____,发生反应的NaNO2的质量为____ g.
12.请设计尽可能多的实验方案,在实验室中制备____________。
13.铁及其重要化合物的“价类二维图”如下图所示。
(1)该“价类二维图”中缺失的类别A应为_______。
(2)生活中的钢铁制品如废旧铁锅,使用时间长久后若要丢弃,应归为_______。
A.干垃圾 B.湿垃圾 C.有毒有害垃圾 D.可回收垃圾
(3)在烧制砖瓦时,用黏土做成的坯经过烘烧后,铁的化合物转化成_______(填字母,下同)而制得红色砖瓦;若烘烧后期从窑顶向下慢慢浇水,窑内会产生大量CO、H2气体,它们把该红色物质还原成黑色的_______,同时还有未燃烧的碳的颗粒,而制得了青色砖瓦。
A.Fe2O3 B.Fe3O4 C.FeO D.Fe(OH)3
(4)要实现Fe转化为Fe2+,可选用足量的_______(填字母)
A.稀盐酸 B.溶液 C.稀硝酸 D.浓硫酸
(5)要实现Fe转化为,除了将Fe与氧气点燃外,另外的方法是(写出化学方程式)_______。
14.将xgFe、FeO和Fe2O3混合物分成两等份,向其中一份中滴加500mL稀硝酸,固体恰好完全溶解并产生标准状况下NO气体aL,溶液中Fe元素均以+3价形式存在,另一份固体与足量H2反应质量减少yg。根据以上数据计算稀硝酸的浓度为___mol·L-1(写出计算过程)。
15.实验室常用加热高锰酸钾的方法制备少量氧气。
(1)请写出该反应的化学方程式___________。
(2)现欲制备3.36L(标准状况)氧气,理论上需要________克高锰酸钾?
(3)用制备的3.36L(标准状况)氧气与H2完全反应生成水,理论上需要________升H2的体积(标准状况)?
三、计算题
16.将45.0gFeC2O4 2H2O隔绝空气加热使之分解,最终可得到19. 6g某种铁的氧化物,请通过计算推测该铁的氧化物的组成:_______(写出化学式)。并写出计算过程:_______
17.蛋白质在一定条件下与浓硫酸反应可转化为硫酸铵,后者在浓氢氧化钠溶液和水蒸气作用下,其中的氮元素可转化为氨放出。现用30.0mL牛奶进行上述实验,将牛奶中蛋白质里的氮元素完全转化成氨,再用50.0mL硫酸溶液吸收放出的氨,剩余的酸用38.0mL氢氧化钠溶液可恰好完全中和。
(1)30.0mL牛奶中共含有_______克氮?
(2)如果牛奶中蛋白质含氮16%(质量分数),则牛奶中蛋白质的质量分数是______?(已知牛奶的密度是)
四、实验题
18.易被空气中的氧气氧化,故制备时主要是避免氧气的介入。某学生利用稀硫酸A、铁粉B和某碱溶液C在实验室设计了如图装置制备白色固体。
(1)写出易被空气中的氧气氧化的方程式_______。
(2)装置Ⅱ盛放的溶液C是_______(a.NaOH b.);配置该溶液时,为除去蒸馏水中溶解的常采用的方法是_______。
(3)铁粉与稀硫酸制备的离子方程式为_______,的作用有_______(填编号)。
a.驱赶装置内的空气
b.把物质B压入Ⅱ中
c.保护白色不被空气氧化
(4)实验过程中,用针管吸取锥形瓶Ⅰ中的溶液,检验其中是否含有。方法为:用该针管吸取_______溶液,用力振荡几次,溶液不变色,把针管中的混合物全部注入干净试管,振荡几次,溶液慢慢变红色。依据现象得出的结论有_______、_______。
(5)白色沉淀在_____(填“锥形瓶Ⅰ”或“锥形瓶Ⅱ”)内生成,经在无氧环境中干燥处理,得到的白色粉末是很好的化工_______(填“除酸剂”或“除氧剂”)。
19.化学实验兴趣小组探究不同氛围、不同温度下草酸亚铁晶体(FeC2O4·2H2O)的分解产物。
I.甲同学在空气氛围中加热草酸亚铁晶体,分析在400℃左右完全分解得到的固体,可能含有FeO、Fe2O3、Fe3O4中的一-种或多种。
已知:a.Fe3O4能与高浓度盐酸反应,与低浓度盐酸不反应;
b.实验中所用溶液均已做除O2处理。
(1)甲同学对固体成分进行了如下实验探究,请填空:
实验操作 实验现象 实验结论
实验1:取少量固体于试管中,向其中加入足量稀1mol/L盐酸,充分振荡,静置 固体部分溶解 结论一:____
实验2:取少许固体于试管中,向其中加入足量12mol/L浓盐酸,充分振荡 固体部分溶解
实验3:取少量实验1试管中的上层清液于试管中,滴入几滴____ ____ 结论二:固体含有FeO
实验4:____ 无明显现象 结论三:_____
(2)上述实验3对应的离子反应方程式为___________。
II.乙同学将54.0g草酸亚铁晶体(FeC2O4·2H2O,M=180g/mol)在氮气的氛围中加热分解,得到分解产物的热重曲线(样品质量随温度的变化情况)如图所示。
(3)A点时,固体物质的化学式为___________
(4)B点时,固体只含有一种铁的氧化物,则FeC2O4·2H2O晶体400℃时受热分解的化学方程式为___________
参考答案:
1.B
【解析】由流程可知,原料(含Cu2O、Fe3O4、SiO2)与足量稀硫酸作用后得CuSO4、FeSO4虑液和SiO2、Cu滤渣。在滤液中加过氧化氢将Fe2+氧化为Fe3+,然后调节溶液的pH使Fe3+沉淀而得CuSO4溶液,再将CuSO4溶液蒸发浓缩、降温结晶、过滤洗涤即得晶体CuSO4 5H2O。
【解析】A.因Cu+在酸性条件下不稳定,易生成金属Cu和Cu2+,所以硫酸与氧化亚铜反应方程式为:H2SO4+Cu2O=CuSO4+Cu+H2O,四氧化三铁可溶于硫酸,反应方程式为:Fe3O4+4H2SO4=Fe2(SO4)3+FeSO4+4H2O,部分Cu与硫酸铁反应生成硫酸铜和硫酸亚铁,二氧化硅与硫酸不反应,故“滤渣1”的成分为:SiO2、Cu,A正确;
B.滤液中含Cu2+、Fe2+,Fe2+可被过氧化氢氧化为Fe3+,反应的离子方程式为:2Fe2++H2O2+2H+=2Fe3++2H2O,B错误;
C.调节溶液的pH使Fe3+沉淀,为了不引入杂质,试剂a可选用CuO消耗H+来增大pH,C正确;
D.从CuSO4溶液溶液得到带有结晶水的晶体,可以采用蒸发浓缩、冷却结晶、过滤、洗涤、干燥即得晶体CuSO4 5H2O,D正确;
故选B。
2.D
【解析】A.氧化铁是红棕色固体,不是黑色,所以该分散系的分散质不可能是氧化铁,故错误;
B. 分散质粒子是直径约为9.3nm能通过滤纸,故不能用过滤的方法分离黑色固体和氯化钠溶液,故错误;
C. 在电场作用下,阴极附近分散系黑色变深,则说明黑色的微粒带正电荷,但不能说明分散系带正电荷,故错误;
D.该分散系属于胶体,有丁达尔效应,故正确。
故选D。
3.A
【解析】A.铁与水蒸气在高温下生成Fe3O4和H2,故A正确;
B.氢氧化亚铁具有还原性,在空气中灼烧氧气将+2价Fe氧化+3价Fe,最终不能得到FeO,故B错误;
C.FeO是一种黑色粉末,不稳定,在空气里加热,最终被氧化成黑色的Fe3O4,故C错误;
D.铁无论过量还是不足,与氯气在加热条件下反应,均生成FeCl3,故D错误;
答案为A。
4.C
【解析】A.一氧化氮能与空气中的氧气反应,不能大量共存,A错误;
B.氢氧化铁胶体、硫离子均能与氢离子反应,不能大量共存,B错误;
C.使酚酞变红的溶液呈碱性,四种离子都能大量共存,C正确;
D.与反应放出的溶液,可能为酸溶液或碱溶液,铵根离子和氢氧根离子不能大量共存,D错误;
答案选C。
5.D
【解析】根据除杂的基本原则“不减、不增、不污、易分”来分析.也就是,除去杂质的同时,要保证不能使所需物质的量减少,但可以增加,更不能引入新的杂质,生成物还不能造成环境污染,并且,生成物、所选试剂与所需物质要容易分离。
【解析】A.应将气体通过加热的氧化铜,将CO转化成CO2,故A错误;
B.利用碳酸氢钠受热易分解的性质,可将其转换为碳酸钠,碳酸钠仍为杂质,故B错误;
C.FeCl3加入足量铜粉生成FeCl2和CuCl2,引入CuCl2杂质,故C错误;
D.Al2O3与氢氧化钠溶液反应生成NaAlO2,Fe2O3不溶于NaOH溶液,过滤、洗涤,能达到除去Al2O3目的,故D正确;
故选D。
【点睛】解答此类题型不但要明确除杂的基本原则“不减、不增、不污、易分”,而且对课本上常见的物质的性质必须熟悉,易错点B,注意碳酸氢钠受热分解转换为碳酸钠,碳酸钠仍为杂质。
6.A
【解析】由M为常见的金属单质,能与稀盐酸和氯气生成不同化合物可知,M为变价金属,由光束通过红褐色Q时,可以看到一条“光亮”的通路可知,Q为氢氧化铁胶体,则M为铁、N为氯化亚铁、P为氯化铁、E为氢氧化亚铁、F为氢氧化铁。
【解析】A.由分析可知,F为氢氧化铁,氢氧化铁受热会发生分解反应生成氧化铁和水,故A正确;
B.由分析可知,M为铁、E为氢氧化亚铁,故B错误;
C.由物质间的转化关系可知,反应中有化合价变化的反应为①②④⑤⑧,则物质转化过程中发生了5个氧化还原反应,故C错误;
D.氢氧化亚铁的还原性强,反应⑧为常温下氢氧化亚铁与空气中的氧气发生氧化还原反应生成氢氧化铁,故D错误;
故选A。
7.B
【解析】A.在水中可生成具有吸附性的氢氧化铝和氢氧化铁,可用于净水,A不符合题意;
B.由于、以及的物质的量的关系无法确定,故不能确定甲溶液中元素的存在形式,即不能确定溶液中是否存在,则加入溶液后溶液不一定呈血红色,B符合题意;
C.因中为价,故试剂X应为氧化剂,将氧化成,C不符合题意;
D.若乙溶液呈强碱性,因氢氧化铝与氢氧化钠反应生成偏铝酸钠,则不可能生成,故意溶液不一定呈强碱性,D不符合题意。
故选:B。
8.D
【解析】A.金属钠与水反应:,故A错误;
B.和溶液混合,没有按照比例拆分,因此离子方程式为:,故B错误;
C.碳酸氢钠溶液与盐酸反应,碳酸氢根不能拆:,故C错误;
D.向溶液中加入过量的氨水:,故D正确。
综上所述,答案为D。
9.B
【解析】因一定量的Fe、FeO和Fe2O3的混合物中加入240mL 2mol L-1的稀硝酸,恰好使混合物完全溶解,往所得溶液中加入KMnO4的酸性溶液,无明显现象,说明溶液中的溶质为硝酸铁,1.344LNO(标准状况)的物质的量为:=0.06mol,根据氮元素守恒,硝酸铁中的硝酸根离子的物质的量为:0.24L×2mol/L-0.06mol=0.42mol,所以硝酸铁的物质的量为:×0.42mol=0.14mol,由铁元素守恒可知,得到铁的物质的量为n(Fe)=0.14mol,质量为0.14mol×56g/mol=7.84g,答案选B。
【点睛】氮元素守恒在本题中应用比较简便,元素守恒的应用也很关键。
10.D
【解析】A.3 mol单质Fe完全转变为Fe3O4,失去8NA个电子,故A正确;
B.装月饼的袋子里常放有干燥剂和铁粉,铁粉做脱氧剂,利用了铁粉的还原性,故B正确;
C.常温下,Fe与H2O不反应,但在空气中O2、H2O的共同作用下铁能发生氧化反应被锈蚀,故C正确;
D.56 g铁和71 g氯气完全反应,铁有剩余,氯气完全反应生成FeCl3,转移的电子数为2NA,故D错误;
选D。
11.(1)+3
(2)萃取
(3)
(4)①④
(5) 1 1mol 69
【解析】(1)
NaNO2中各元素化合价代数和为0,Na显+1价,O显-2价,设N的化合价为x,1+x+2 (-2)=0,解得x=+3,即N的化合价为+3;
(2)
I2易溶于有机溶剂,可利用CCl4或苯对反应后的碘溶液进行萃取后再蒸馏获得I2,故答案为:萃取;
(3)
N的化合价降低,得到1个电子,I元素的化合价升高生成碘单质失去2个电子,根据氧化还原反应的规律用双线桥标明电子转移的方向和数目如下:;
(4)
根据已知反应可推知,碘化钾在酸性条件下可与亚硝酸钠溶液反应生成碘单质,碘单质遇淀粉变为蓝色,而氯化钠则无此现象,所以选择鉴别得试剂为:碘化钾淀粉试纸、食醋,故答案为:①④;
(5)
对于反应2NaNO2+4HI=2NO↑+I2+2NaI+2H2O,若产生的气体在标准状况下体积为2.24L,即NO的物质的量为1mol,根据关系式2e-2NO可知,反应过程中转移电子的物质的量为1mol,其数目为1NA,(NA表示阿伏伽德罗常数的值),2molNO生成时,4molHI被消耗,只有2molHI被氧化为碘单质,所以当有1molNO生成时,被氧化的HI的物质的量为1mol,发生反应的NaNO2的物质的量为1mol,其质量为=69g,故答案为:1;1mol;69。
12.⑴向铁粉中加入适量稀硫酸溶液;⑵向硫酸铜溶液中加入足量铁粉,过滤;⑶向硫酸铁中加入足量铁粉,过滤;⑷向氧化亚铁中加入适量硫酸溶液。
【解析】硫酸亚铁是盐类,金属与酸反应,金属与盐反应,金属氧化物与酸反应都能得到硫酸亚铁,在实验室中制备有四种方法:⑴向铁粉中加入适量稀硫酸溶液;⑵向硫酸铜溶液中加入足量铁粉,过滤;⑶向硫酸铁中加入足量铁粉,过滤;⑷氧化亚铁中加入适量硫酸溶液;故答案为:⑴向铁粉中加入适量稀硫酸溶液;⑵向硫酸铜溶液中加入足量铁粉,过滤;⑶向硫酸铁中加入足量铁粉,过滤;⑷向氧化亚铁中加入适量硫酸溶液。
13.(1)盐
(2)D
(3) A B
(4)AB
(5)
【解析】(1)
该“价类二维图”中缺失的类别A为Fe2+、Fe3+,亚铁盐、铁盐,应为盐类;
(2)
生活中的钢铁制品如废旧铁锅,使用时间长久后若要丢弃,为金属合金可回收利用,应归为可回收垃圾;答案选D;
(3)
在烧制砖瓦时,用黏土作成的坯经过烘烧后,铁的化合物转化成Fe2O3而制得红色砖瓦,若烘烧后期从窑顶慢慢浇水,发生C+H2O H2+CO,生成还原性气体,与Fe2O3反应生成黑色的化合物F'e3O4,同时还有未燃烧的碳的颗粒,而制得了青色砖瓦;
答案选A;B;
(4)
要实现Fe转化为Fe2+,应选择弱氧化剂,稀盐酸、溶液符合,稀硝酸及浓硫酸氧化性较强不合适,答案选AB;
(5)
要实现Fe转化为,除了将Fe与氧气点燃外,也可将铁粉在高温下与水蒸气反应,反应的化学方程式为。
14.mol·L-1
【解析】根据反应3H2+Fe2O32Fe+3H2O,H2+FeOFe+H2O质量减少yg,减少的质量为氧的质量,所以m(Fe)=(x-y)g,故n(Fe)=mol,再根据 Fe2O3+6HNO3=2Fe(NO3)3+3H2O,3FeO+10HNO3 =3Fe(NO3)3+NO+5H2O,Fe+4HNO3=Fe(NO3)3+NO+2H2O,可得 n(HNO3)= n(Fe)×3+ n(NO),已知n(Fe)=mol=,n(NO)=mol=mol,n(HNO3)=3×+,c(HNO3)===mol/L;
15.(1)2KMnO4K2MnO4+MnO2+O2↑
(2)47.4
(3)6.72
【解析】(1)加热高锰酸钾反应生成锰酸钾、二氧化锰和氧气,化学方程式为2KMnO4 K2MnO4+MnO2+O2↑;
(2)3.36L(标准状况)氧气的物质的量为 ,根据化学反应方程式可知,n(KMnO4)=2n(O2)=0.30mol,需要高锰酸钾的质量为 ;
(3)根据化学反应方程式2H2+O2 2H2O,3.36L(标准状况)氧气的物质的量为 ,需要n(H2)=0.30mol,需要H2的体积(标准状况)为 。
16. Fe5O7 或Fe3O4 Fe2O3或2Fe2O3 FeO ,
【解析】45.0gFeC2O4 2H2O的物质的量为:,则所含Fe的质量为:m(Fe)=0.25mol×56g/mol=14g,最终可得到19. 6g某种铁的氧化物,其中铁的质量14g,则O的质量为:19.6g-14g=5.6g,n(O)=,n(Fe):n(O)=0.25:0.35=5:7,则氧化物的化学式为:Fe5O7 或Fe3O4 Fe2O3或2Fe2O3 FeO,故答案为:Fe5O7 或Fe3O4 Fe2O3或2Fe2O3 FeO;,;
17.(1)0.168
(2)3.4%
【解析】(1)令38mL 1.00mol L-1的 NaOH溶液中和硫酸的物质的量为n,则,解得:n=0.038L×1mol/L×0.5=0.019mol,故吸收氨气的硫酸的物质的量为:0.500mol L-1×0.05mL-0.019mol=0.006mol,令30.0mL牛奶中氮元素的质量是m,则:,所以m=28g×=0.168g,故答案为:0.168;
(2)30mL牛奶的质量为:30mL×1.03g mL-1=30.9g,所以30.9g×ω(蛋白质)×16.0%=0.168g,解得:ω(蛋白质)=3.4%,故答案为:该牛奶中蛋白质的质量分数为3.4%。
18.(1)
(2) a 加热煮沸
(3) abc
(4) KSCN 锥形瓶Ⅰ中溶液不含 溶液注入试管后,空气中的氧气氧化得到,遇变红
(5) 锥形瓶Ⅱ 除氧剂
【解析】装置Ⅰ中,稀硫酸和铁粉反应,生成氢气和硫酸亚铁,产生的氢气能排除装置中的氧气;反应一段时间后,关闭止水夹,则产生的硫酸亚铁会进入装置Ⅱ中,与碱发生反应,生成,据此分析作答。
(1)
易被空气中的氧气氧化,生成氢氧化铁,化学方程式为:,故答案为:;
(2)
硫酸亚铁会进入装置Ⅱ中,与碱发生反应,生成,可知该碱为NaOH;配置该溶液时,为除去蒸馏水中溶解的常采用的方法是加热煮沸,故答案为:a;加热煮沸;
(3)
稀硫酸和铁粉反应,生成氢气和硫酸亚铁,离子方程式为;产生的氢气能驱赶装置内的空气、关闭止水夹,能把物质B压入Ⅱ中、同时防止空气进入装置Ⅱ,保护白色不被空气氧化,故答案为:;abc;
(4)
KSCN遇,溶液会变红色,则用该针管吸取KSCN溶液,用力振荡几次,溶液不变色,说明锥形瓶Ⅰ中溶液不含;把针管中的混合物全部注入干净试管,振荡几次,溶液慢慢变红色,说明溶液注入试管后,空气中的氧气氧化得到,遇变红,故答案为:KSCN;锥形瓶Ⅰ中溶液不含;溶液注入试管后,空气中的氧气氧化得到,遇变红;
(5)
由分析可知,白色沉淀在锥形瓶Ⅱ内生成;易被空气中的氧气氧化,经在无氧环境中干燥处理,得到的白色粉末是很好的化工除氧剂,故答案为:锥形瓶Ⅱ;除氧剂。
19.(1) 固体含有Fe3O4 K3Fe(CN)6溶液 生成蓝色沉淀 取少量实验1试管上层清液于试管中,滴入几滴KSN溶液 固体不含有Fe2O3
(2)3Fe2++2Fe(CN)=Fe3[Fe(CN)6]2↓
(3)FeC2O4
(4)3FeC2O4+2H2O=Fe3O4+4CO↑+2CO2↑+6H2O
【解析】(1)
根据已知信息:Fe3O4能与高浓度盐酸反应,与低浓度盐酸不反应,结合实验1和实验2的现象,可知原固体含有能溶于浓盐酸而不溶于稀盐酸的Fe3O4,则结论一:固体含有Fe3O4;根据实验3,只要证明实验1试管的上层清液含有Fe2+,就可得出固体含有FeO的结论,则可加入几滴K3Fe(CN)6溶液,生成蓝色沉淀,发生反应的离子方程式为3Fe2++2Fe(CN)=Fe3[Fe(CN)6]2↓;根据结论三固体不含有,需要证明实验1试管中的上层清液不含Fe3+,则应加入几滴KSCN溶液,观察无明显现象;
(2)
实验3中Fe2+与K3Fe(CN)6溶液反应生成蓝色沉淀,发生反应的离子方程式为3Fe2++2Fe(CN)=Fe3[Fe(CN)6]2↓;
(3)
n(FeC2O4·2H2O)=,0.3mol FeC2O4的固体质量刚好为43.2g,即热重曲线上A点刚好为FeC2O4;
(4)
B点时,固体只有一种铁的氧化物,m(Fe)=nM=0.3mol×56g/mol=16.8g,则m(O)=23.2g-16.8g=6.4g,n(O)=,n(Fe):n(O)=0.3:04=3:4,则该含铁氧化物的化学式为Fe3O4,则FeC2O4·2H2O晶体400℃时受热分解的化学方程式为3FeC2O4+2H2O=Fe3O4+4CO↑+2CO2↑+6H2O。
