2023年中考化学复习 主题三 物质的性质与应用第14讲 常见的酸和碱课件(共40张PPT)
文档属性
| 名称 | 2023年中考化学复习 主题三 物质的性质与应用第14讲 常见的酸和碱课件(共40张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 4.0MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-06-11 00:00:00 | ||
图片预览








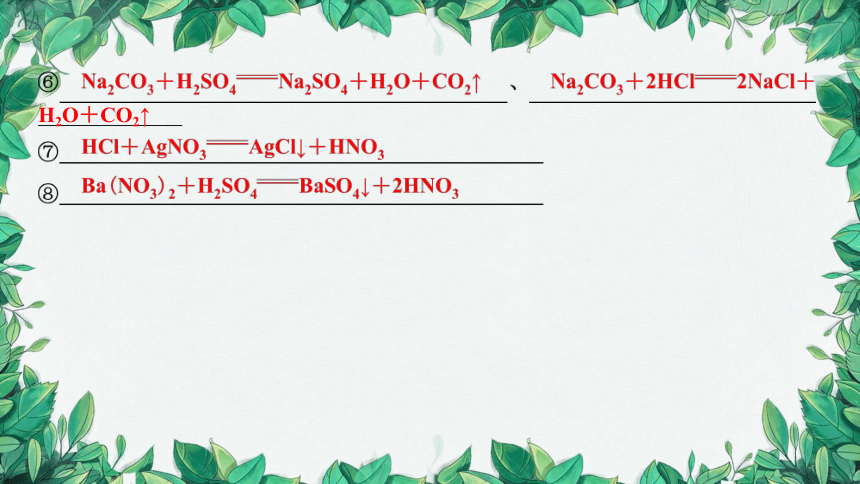

文档简介
(共40张PPT)
主题三 物质的性质与应用
第14讲 常见的酸和碱
以盐酸、硫酸、氢氧化钠和氢氧化钙为例,通过实验探究认识酸、碱的主要性质和用途。
一、常见的酸
二、常见的碱
易错易混提醒:
1.碱溶液使酚酞变红,使酚酞变红的不一定是碱,如碳酸钠溶液。
2.酚酞遇某溶液不变色,该溶液不一定是酸,也可能是中性溶液。
3.敞口放置在空气中一段时间的浓硫酸和浓盐酸,溶质质量分数都变小,都是物理变化。
4.盐酸是氯化氢气体的水溶液,属于混合物。
5.敞口放置的烧碱固体质量会增加,原因是吸收了空气中的二氧化碳,是化学变化。
6.敞口放置的烧碱固体会吸收空气中的水蒸气而潮解,是物理变化。
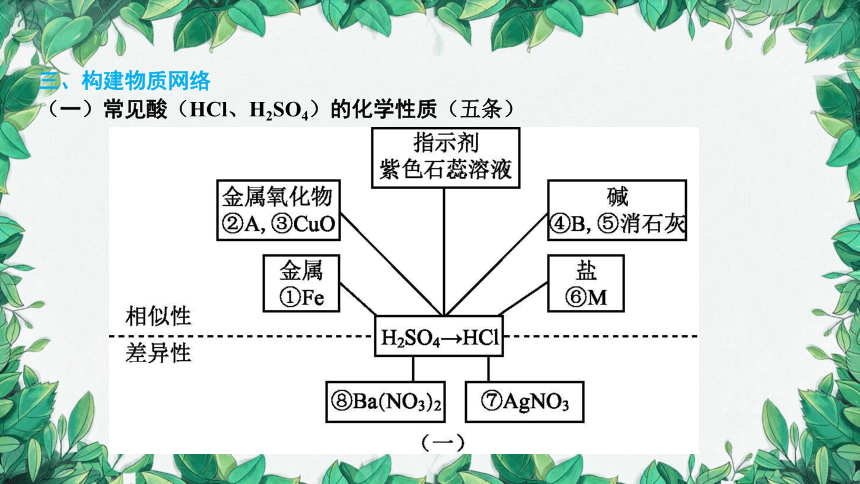
三、构建物质网络
(一)常见酸(HCl、H2SO4)的化学性质(五条)
已知:物质A是铁锈的主要成分;B俗称烧碱、苛性钠;M俗称苏打、纯碱。
1.写出对应物质的化学式:
A: Fe2O3 B: NaOH M: Na2CO3
2.按序号写出对应的化学方程式:
Fe2O3
NaOH
Na2CO3
3H2O
2H2O
H2O+CO2↑
(二)常见碱[NaOH、Ca(OH)2]的化学性质
已知:物质甲的浓溶液可使木条炭化;乙是胃液的主要成分;丙的固体俗称干冰,丁遇碱溶液变红;戊的溶液呈蓝色,反应生成氯化物。
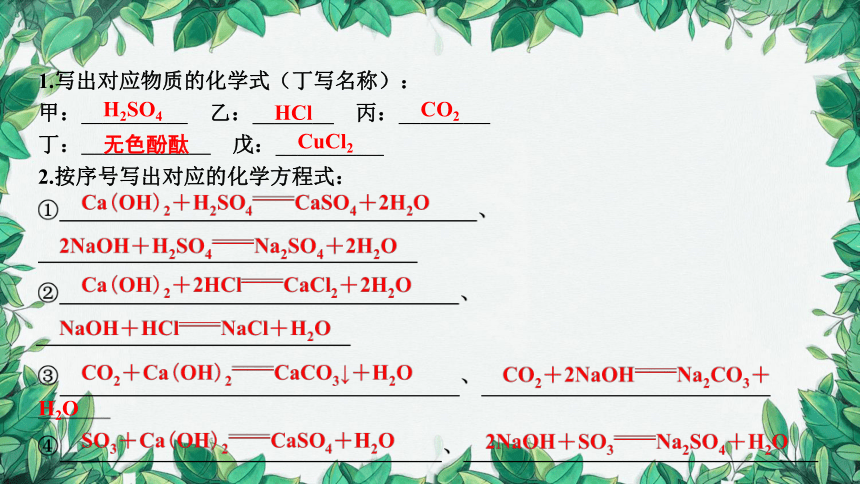
1.写出对应物质的化学式(丁写名称):
甲: H2SO4 乙: HCl 丙: CO2
丁: 无色酚酞 戊: CuCl2
2.按序号写出对应的化学方程式:
H2SO4
HCl
CO2
无色酚酞
CuCl2
H2O
Cu(OH)2↓+2NaCl
一、验证二氧化碳能与氢氧化钠溶液发生反应
1.设计思路
二氧化碳和氢氧化钠反应无明显现象,可通过检验反应物的减少或有新物质生成两种思路探究反应是否发生。
2.方案一:检验反应物的减少
(1)实验原理:利用二者在密闭容器中反应的压强变化来判断反应是否发生。由于NaOH溶液中有水,为排除水对实验的干扰,需要进行对比实验。
(2)实验装置
(3)实验现象和结论
实验 编号 现象 结论
甲 U形管左侧液面 高于 右侧液面 CO2能与NaOH反应
乙 倒扣在NaOH溶液中的试管内液柱 更高
丙 盛NaOH溶液的塑料瓶 更瘪
高于
更高
更瘪
3.方案二:检验生成物
(1)实验原理:反应后生成的碳酸盐能与可溶性钙盐或钡盐反应生成沉淀。
(2)操作与结论:取少量反应后的溶液,往其中滴入几滴氯化钙或氯化钡溶液,观察到有沉淀生成。
二、NaOH变质的探究实验
实验方案
实验试剂 实验现象 化学方程式 实验结论
酸 HCl(或H2SO4) 有气泡生成 氢氧化钠已
变质
碱 Ca(OH)2[或Ba(OH)2] 生成白色沉淀
HCl(或
H2SO4)
CO2↑
H2O+CO2↑)
Ca(OH)2[或
Ba(OH)2]
+2NaOH
[或Na2CO3+Ba(OH) 2
实验试剂 实验现象 化学方程式 实验结论
盐 CaCl2溶液 (或BaCl2溶液) 生成白色沉淀 氢氧化钠已
变质
生成白色沉
淀
CaCO3↓
BaCO3↓)
3.探究变质的程度
实验方案
实验目的 实验操作 实验现象 实验结论
检验并除去NaOH中的Na2CO3 取样溶于水,滴入过量的CaCl2(或BaCl2)溶液 有白色沉淀生成 NaOH已变质
检验是否存在NaOH 取上述步骤中所得的上层清液, 滴加无色酚酞溶液 溶液变红 部分变质
溶液不变红 完全变质
有白色沉淀生
成
部分变质
溶液不变红
4.反思提升
(1)小张在检验氢氧化钠是否变质时,向样品溶液中滴入几滴稀盐酸,观察到无气泡生成,认为氢氧化钠没有变质,你认为他的结论 不准确 (填“准确”或“不准确”),原因是 滴入的稀盐酸太少,若氢氧化钠部分变质,加入的酸先与氢氧化钠反应,无明显现象,无法观察到气泡 。
(2) 不能 (填“能”或“不能”)用Ca(OH)2或Ba(OH)2溶液替代CaCl2或BaCl2溶液除去碳酸钠后再检验是否有NaOH,原因是 氢氧化钙或氢氧化钡会与碳酸钠反应生成氢氧化钠,干扰氢氧化钠的检验 。
(3)除去碳酸钠后检验是否存在NaOH,除了用酚酞溶液,还可以选用的试剂有: 紫色石蕊溶液(或“硫酸铜溶液”或“氯化铁溶液”或“氯化镁溶液”) 。
不准确
滴入的稀盐酸太少,若氢氧化钠部分变质,加入的酸先与
氢氧化钠反应,无明显现象,无法观察到气泡
不能
氢氧化钙或氢氧化钡会与
碳酸钠反应生成氢氧化钠,干扰氢氧化钠的检验
紫色石蕊溶液(或“硫酸铜溶液”或“氯化铁溶液”或“氯化镁溶
液”)
典例1:小明同学归纳总结了有关酸和碱的化学性质的知识网络如图所示。其中A是一种生活中最常见的金属,B是一种常见的化合物,图中短线表示两种物质在一定条件下可以发生化学反应。请根据图示回答有关问题:
(1)写出烧碱的化学式: NaOH 。
(2)B可能是 Na2CO3(合理即可) (填化学式);若反应⑧的现象是溶液变红,则反应⑦的现象是 无明显现象 。
NaOH
Na2CO3(合理即可)
无明显现象
(3)请写出有关反应的化学方程式:
(4)请你用文字描述反应⑤的实验现象: 黑色粉末溶解,溶液变蓝色 。
(5)图中所标的9个反应中,属于中和反应的是 ⑥⑨ (填代号,下同),属于置换反应的是 ① 。
CO2+Ca(OH) 2
黑色粉末溶解,溶液变蓝色
⑥⑨
①
典例2:某同学用如图所示装置探究二氧化碳与氢氧化钠的反应。请结合信息回答下列问题:
(1)甲同学观察到瘪气球胀大,依此现象判断二氧化碳与氢氧化钠发生了反应,乙同学认为不严谨,原因是 CO2与溶液中的水反应也能观察到气球胀大 。
CO2与溶液中的水反应也能观察到气球胀大
H2O
(3)同学们对反应后溶液中的溶质成分采用了不同方案进行探究。
【作出猜想】猜想1:Na2CO3; 猜想2:Na2CO3和NaOH的混合物。
【实验验证】
方案 操作 现象 结论
一 用玻璃棒蘸取溶液滴在pH试纸上 pH>7 猜想2成立
二 取反应后的溶液逐滴滴入稀盐酸 先无明显现象后有气泡
三 取反应后的溶液逐滴滴入足量的 CaCl2 溶液,然后再滴入 无色酚酞 有白色沉淀生成, 溶液变红
pH>7
先无明显现象后有气
泡
CaCl2
无色酚酞
溶
液变红
【反思提高】
(4)在老师的建议下,同学们再利用图1装置研究NaOH与CO2的反应。用等体积的氢氧化钠溶液、水分别进行实验,将注射器内液体快速全部推入,测得一段时间内温度和压强的变化如图2、图3所示。
①图2可说明NaOH与CO2发生了化学反应,其依据是 加入水,压强无明显变化,加入氢氧化钠溶液,压强明显减小 。
②等到锥形瓶中气压不再改变时,测得注入水的锥形瓶中的气压与0s时的气压相同,说明在该条件下1体积的水最多能溶解 1 体积的二氧化碳。
③由图3可得到的结论是 氢氧化钠和二氧化碳反应放热 。
④图2中0~30s时间内,气压略有升高,原因是 推入液体时,瓶内气压升高 。
加入水,压强无明显变化,
加入氢氧化钠溶液,压强明显减小
1
氢氧化钠和二氧化碳反应放热
推入液体时,瓶内气压升高
考点1 酸碱指示剂
1.(2022·聊城)下列图示是几种常见物质溶于水后发生解离的微观示意图,其中能使紫色石蕊溶液变红的是( D )
A
B
C
D
D
2.(2022·柳州)化学课上老师给同学们变“魔术”:往浸过酚酞溶液的白色纸花上喷了某种无色溶液后,白花瞬间变成了红花,老师喷的溶液可能是( C )
A.水 B.稀盐酸
C.氨水 D.氯化钠溶液
C
考点2 常见的酸及其性质
3.(2017.3)下列试剂瓶应有 标志的是( C )
A.氯化钠 B.蒸馏水
C.浓硫酸 D.葡萄糖
4.(2022·株洲)下列物质中,不.能.与稀硫酸反应的是( B )
A.BaCl2溶液 B.Cu丝
C.CuO粉末 D.Cu(OH)2固体
C
B
5.(各地中考真题汇编)判断下列说法的正误。
(1)打开装有浓盐酸的试剂瓶瓶盖,瓶口出现白烟 ( × )
(2)浓硫酸有吸水性,在实验室中可干燥H2、O2和CO2 ( √ )
(3)浓硫酸与浓盐酸长期露置在空气中,溶质质量分数均减小的原因相同 ( × )
(4)盐酸具有挥发性,因此可用于除铁锈 ( × )
(5)实验室可用块状石灰石与稀硫酸制备CO2 ( × )
×
√
×
×
×
6.(2022·陕西)如图所示,稀硫酸能与相连的物质发生化学反应。
(1)稀硫酸与BaCl2溶液反应的现象是 产生白色沉淀 。
(3)若X可用作钾肥,其化学式为 K2CO3(或KHCO3) 。
产生白色沉淀
H2O
K2CO3(或KHCO3)
7.(2022·北京)如图所示,向井穴板的孔穴1~3中滴加稀盐酸,4~6中滴加无色酚酞溶液。
(1)1中所得溶液的颜色为 黄色 。
黄色
2HCl+
(3)4、5、6中无明显现象的是 4、5 (填序号)。
4、5
考点3 常见的碱及其性质
8.(广东省真题组合)判断下列说法的正误。
(1)氢氧化钠具有碱性,常用于改良酸性土壤(2019.8D) ( × )
(2)向盛有NaOH溶液的试管中滴加几滴酚酞溶液,溶液变红色,说明NaOH溶液没有变质(2019.13C) ( × )
(3)除去NaOH中混有的少量Na2CO3,滴加稀盐酸至不再产生气泡为止(2018.12 C) ( × )
(4)向NaOH溶液中加入稀盐酸,没有明显现象,说明NaOH和盐酸不反应(2017.11B) ( × )
×
×
×
×
(5)往久置于空气中的氢氧化钠溶液滴加稀硫酸,有气泡生成,说明氢氧化钠溶液已变质(2015.12B) ( √ )
(6)用水区分NH4NO3和NaOH两种固体(2013.9C) ( √ )
√
√
9.(2021·邵阳)下列关于氢氧化钠的描述中错.误.的是( B )
A.对皮肤有强烈的腐蚀作用 B.其水溶液能使石蕊溶液变红
C.能去除油污,可作炉具清洁剂 D.易溶于水,溶解时放出热量
10.(2020·郴州)下列关于Ca(OH)2的说法错.误.的是( B )
A.微溶于水,水溶液呈碱性
B.能与酸反应,可用于治疗胃酸过多
C.与CuSO4溶液按一定比例混合,可配制波尔多液
D.澄清溶液可用来检验CO2
11.(2022·乐山)向某无色溶液中加入NaOH后能产生沉淀,则该溶液可能是( A )
A.MgCl2溶液 B.Ba(NO3)2溶液
C.稀盐酸 D.CuSO4溶液
B
B
A
12.(2021·丽水)物质结构决定性质,物质性质决定用途,反应本质决定变化现象。如图是小科构建的氢氧化钙部分知识网络,其中“—”表示相连物质能发生化学反应,X与图中所给物质的类别不同。请回答:
(1)酚酞试液在Ca(OH)2溶液中显红色,能使酚酞试液变红的离子是 OH- 。
(2)列举熟石灰[Ca(OH)2]在工农业上的一种用途: 中和酸性土壤 。
OH
-
中和酸性土壤
13.(2021·恩施州)图1是关于氢氧化钠化学性质的思维导图,请据图回答问题。
(1)性质①,将无色酚酞溶液滴入氢氧化钠溶液中,溶液呈 红 色。
(2)性质②,将氢氧化钠溶液滴入稀盐酸中,图2表示该反应过程中溶液pH的变化曲线,n点溶液中的溶质是 NaCl、NaOH (填化学式)。
红
NaCl、NaOH
14.(2021·陕西)学习小组同学用如图装置进行实验。打开分液漏斗的活塞,将NaOH浓溶液加入锥形瓶A中,关闭活塞,打开弹簧夹,观察到烧杯B中液面降低,A中产生白色沉淀。
+H2O
(2)若X是一种碱,其化学式可能是 Ba(OH)2[或Ca(OH)2] (写一种)。
(3)学习小组同学用的X是CaCl2(CaCl2溶液呈中性),实验结束后,同学们又分别做了以下三组实验:
①取少量A中溶液,测其pH,pH>7;
②取少量A中溶液,向其中加入CaCl2溶液,无明显现象,再测其pH,pH>7;
③取少量A中溶液,测其pH,pH>7,再向其中加入K2CO3溶液,产生白色沉淀。
以上三组实验事实中,能说明A中溶液一定含有NaOH的是 ②③ (填序号)。
Ba(OH)2[或Ca(OH)2]
②③
主题三 物质的性质与应用
第14讲 常见的酸和碱
以盐酸、硫酸、氢氧化钠和氢氧化钙为例,通过实验探究认识酸、碱的主要性质和用途。
一、常见的酸
二、常见的碱
易错易混提醒:
1.碱溶液使酚酞变红,使酚酞变红的不一定是碱,如碳酸钠溶液。
2.酚酞遇某溶液不变色,该溶液不一定是酸,也可能是中性溶液。
3.敞口放置在空气中一段时间的浓硫酸和浓盐酸,溶质质量分数都变小,都是物理变化。
4.盐酸是氯化氢气体的水溶液,属于混合物。
5.敞口放置的烧碱固体质量会增加,原因是吸收了空气中的二氧化碳,是化学变化。
6.敞口放置的烧碱固体会吸收空气中的水蒸气而潮解,是物理变化。
三、构建物质网络
(一)常见酸(HCl、H2SO4)的化学性质(五条)
已知:物质A是铁锈的主要成分;B俗称烧碱、苛性钠;M俗称苏打、纯碱。
1.写出对应物质的化学式:
A: Fe2O3 B: NaOH M: Na2CO3
2.按序号写出对应的化学方程式:
Fe2O3
NaOH
Na2CO3
3H2O
2H2O
H2O+CO2↑
(二)常见碱[NaOH、Ca(OH)2]的化学性质
已知:物质甲的浓溶液可使木条炭化;乙是胃液的主要成分;丙的固体俗称干冰,丁遇碱溶液变红;戊的溶液呈蓝色,反应生成氯化物。
1.写出对应物质的化学式(丁写名称):
甲: H2SO4 乙: HCl 丙: CO2
丁: 无色酚酞 戊: CuCl2
2.按序号写出对应的化学方程式:
H2SO4
HCl
CO2
无色酚酞
CuCl2
H2O
Cu(OH)2↓+2NaCl
一、验证二氧化碳能与氢氧化钠溶液发生反应
1.设计思路
二氧化碳和氢氧化钠反应无明显现象,可通过检验反应物的减少或有新物质生成两种思路探究反应是否发生。
2.方案一:检验反应物的减少
(1)实验原理:利用二者在密闭容器中反应的压强变化来判断反应是否发生。由于NaOH溶液中有水,为排除水对实验的干扰,需要进行对比实验。
(2)实验装置
(3)实验现象和结论
实验 编号 现象 结论
甲 U形管左侧液面 高于 右侧液面 CO2能与NaOH反应
乙 倒扣在NaOH溶液中的试管内液柱 更高
丙 盛NaOH溶液的塑料瓶 更瘪
高于
更高
更瘪
3.方案二:检验生成物
(1)实验原理:反应后生成的碳酸盐能与可溶性钙盐或钡盐反应生成沉淀。
(2)操作与结论:取少量反应后的溶液,往其中滴入几滴氯化钙或氯化钡溶液,观察到有沉淀生成。
二、NaOH变质的探究实验
实验方案
实验试剂 实验现象 化学方程式 实验结论
酸 HCl(或H2SO4) 有气泡生成 氢氧化钠已
变质
碱 Ca(OH)2[或Ba(OH)2] 生成白色沉淀
HCl(或
H2SO4)
CO2↑
H2O+CO2↑)
Ca(OH)2[或
Ba(OH)2]
+2NaOH
[或Na2CO3+Ba(OH) 2
实验试剂 实验现象 化学方程式 实验结论
盐 CaCl2溶液 (或BaCl2溶液) 生成白色沉淀 氢氧化钠已
变质
生成白色沉
淀
CaCO3↓
BaCO3↓)
3.探究变质的程度
实验方案
实验目的 实验操作 实验现象 实验结论
检验并除去NaOH中的Na2CO3 取样溶于水,滴入过量的CaCl2(或BaCl2)溶液 有白色沉淀生成 NaOH已变质
检验是否存在NaOH 取上述步骤中所得的上层清液, 滴加无色酚酞溶液 溶液变红 部分变质
溶液不变红 完全变质
有白色沉淀生
成
部分变质
溶液不变红
4.反思提升
(1)小张在检验氢氧化钠是否变质时,向样品溶液中滴入几滴稀盐酸,观察到无气泡生成,认为氢氧化钠没有变质,你认为他的结论 不准确 (填“准确”或“不准确”),原因是 滴入的稀盐酸太少,若氢氧化钠部分变质,加入的酸先与氢氧化钠反应,无明显现象,无法观察到气泡 。
(2) 不能 (填“能”或“不能”)用Ca(OH)2或Ba(OH)2溶液替代CaCl2或BaCl2溶液除去碳酸钠后再检验是否有NaOH,原因是 氢氧化钙或氢氧化钡会与碳酸钠反应生成氢氧化钠,干扰氢氧化钠的检验 。
(3)除去碳酸钠后检验是否存在NaOH,除了用酚酞溶液,还可以选用的试剂有: 紫色石蕊溶液(或“硫酸铜溶液”或“氯化铁溶液”或“氯化镁溶液”) 。
不准确
滴入的稀盐酸太少,若氢氧化钠部分变质,加入的酸先与
氢氧化钠反应,无明显现象,无法观察到气泡
不能
氢氧化钙或氢氧化钡会与
碳酸钠反应生成氢氧化钠,干扰氢氧化钠的检验
紫色石蕊溶液(或“硫酸铜溶液”或“氯化铁溶液”或“氯化镁溶
液”)
典例1:小明同学归纳总结了有关酸和碱的化学性质的知识网络如图所示。其中A是一种生活中最常见的金属,B是一种常见的化合物,图中短线表示两种物质在一定条件下可以发生化学反应。请根据图示回答有关问题:
(1)写出烧碱的化学式: NaOH 。
(2)B可能是 Na2CO3(合理即可) (填化学式);若反应⑧的现象是溶液变红,则反应⑦的现象是 无明显现象 。
NaOH
Na2CO3(合理即可)
无明显现象
(3)请写出有关反应的化学方程式:
(4)请你用文字描述反应⑤的实验现象: 黑色粉末溶解,溶液变蓝色 。
(5)图中所标的9个反应中,属于中和反应的是 ⑥⑨ (填代号,下同),属于置换反应的是 ① 。
CO2+Ca(OH) 2
黑色粉末溶解,溶液变蓝色
⑥⑨
①
典例2:某同学用如图所示装置探究二氧化碳与氢氧化钠的反应。请结合信息回答下列问题:
(1)甲同学观察到瘪气球胀大,依此现象判断二氧化碳与氢氧化钠发生了反应,乙同学认为不严谨,原因是 CO2与溶液中的水反应也能观察到气球胀大 。
CO2与溶液中的水反应也能观察到气球胀大
H2O
(3)同学们对反应后溶液中的溶质成分采用了不同方案进行探究。
【作出猜想】猜想1:Na2CO3; 猜想2:Na2CO3和NaOH的混合物。
【实验验证】
方案 操作 现象 结论
一 用玻璃棒蘸取溶液滴在pH试纸上 pH>7 猜想2成立
二 取反应后的溶液逐滴滴入稀盐酸 先无明显现象后有气泡
三 取反应后的溶液逐滴滴入足量的 CaCl2 溶液,然后再滴入 无色酚酞 有白色沉淀生成, 溶液变红
pH>7
先无明显现象后有气
泡
CaCl2
无色酚酞
溶
液变红
【反思提高】
(4)在老师的建议下,同学们再利用图1装置研究NaOH与CO2的反应。用等体积的氢氧化钠溶液、水分别进行实验,将注射器内液体快速全部推入,测得一段时间内温度和压强的变化如图2、图3所示。
①图2可说明NaOH与CO2发生了化学反应,其依据是 加入水,压强无明显变化,加入氢氧化钠溶液,压强明显减小 。
②等到锥形瓶中气压不再改变时,测得注入水的锥形瓶中的气压与0s时的气压相同,说明在该条件下1体积的水最多能溶解 1 体积的二氧化碳。
③由图3可得到的结论是 氢氧化钠和二氧化碳反应放热 。
④图2中0~30s时间内,气压略有升高,原因是 推入液体时,瓶内气压升高 。
加入水,压强无明显变化,
加入氢氧化钠溶液,压强明显减小
1
氢氧化钠和二氧化碳反应放热
推入液体时,瓶内气压升高
考点1 酸碱指示剂
1.(2022·聊城)下列图示是几种常见物质溶于水后发生解离的微观示意图,其中能使紫色石蕊溶液变红的是( D )
A
B
C
D
D
2.(2022·柳州)化学课上老师给同学们变“魔术”:往浸过酚酞溶液的白色纸花上喷了某种无色溶液后,白花瞬间变成了红花,老师喷的溶液可能是( C )
A.水 B.稀盐酸
C.氨水 D.氯化钠溶液
C
考点2 常见的酸及其性质
3.(2017.3)下列试剂瓶应有 标志的是( C )
A.氯化钠 B.蒸馏水
C.浓硫酸 D.葡萄糖
4.(2022·株洲)下列物质中,不.能.与稀硫酸反应的是( B )
A.BaCl2溶液 B.Cu丝
C.CuO粉末 D.Cu(OH)2固体
C
B
5.(各地中考真题汇编)判断下列说法的正误。
(1)打开装有浓盐酸的试剂瓶瓶盖,瓶口出现白烟 ( × )
(2)浓硫酸有吸水性,在实验室中可干燥H2、O2和CO2 ( √ )
(3)浓硫酸与浓盐酸长期露置在空气中,溶质质量分数均减小的原因相同 ( × )
(4)盐酸具有挥发性,因此可用于除铁锈 ( × )
(5)实验室可用块状石灰石与稀硫酸制备CO2 ( × )
×
√
×
×
×
6.(2022·陕西)如图所示,稀硫酸能与相连的物质发生化学反应。
(1)稀硫酸与BaCl2溶液反应的现象是 产生白色沉淀 。
(3)若X可用作钾肥,其化学式为 K2CO3(或KHCO3) 。
产生白色沉淀
H2O
K2CO3(或KHCO3)
7.(2022·北京)如图所示,向井穴板的孔穴1~3中滴加稀盐酸,4~6中滴加无色酚酞溶液。
(1)1中所得溶液的颜色为 黄色 。
黄色
2HCl+
(3)4、5、6中无明显现象的是 4、5 (填序号)。
4、5
考点3 常见的碱及其性质
8.(广东省真题组合)判断下列说法的正误。
(1)氢氧化钠具有碱性,常用于改良酸性土壤(2019.8D) ( × )
(2)向盛有NaOH溶液的试管中滴加几滴酚酞溶液,溶液变红色,说明NaOH溶液没有变质(2019.13C) ( × )
(3)除去NaOH中混有的少量Na2CO3,滴加稀盐酸至不再产生气泡为止(2018.12 C) ( × )
(4)向NaOH溶液中加入稀盐酸,没有明显现象,说明NaOH和盐酸不反应(2017.11B) ( × )
×
×
×
×
(5)往久置于空气中的氢氧化钠溶液滴加稀硫酸,有气泡生成,说明氢氧化钠溶液已变质(2015.12B) ( √ )
(6)用水区分NH4NO3和NaOH两种固体(2013.9C) ( √ )
√
√
9.(2021·邵阳)下列关于氢氧化钠的描述中错.误.的是( B )
A.对皮肤有强烈的腐蚀作用 B.其水溶液能使石蕊溶液变红
C.能去除油污,可作炉具清洁剂 D.易溶于水,溶解时放出热量
10.(2020·郴州)下列关于Ca(OH)2的说法错.误.的是( B )
A.微溶于水,水溶液呈碱性
B.能与酸反应,可用于治疗胃酸过多
C.与CuSO4溶液按一定比例混合,可配制波尔多液
D.澄清溶液可用来检验CO2
11.(2022·乐山)向某无色溶液中加入NaOH后能产生沉淀,则该溶液可能是( A )
A.MgCl2溶液 B.Ba(NO3)2溶液
C.稀盐酸 D.CuSO4溶液
B
B
A
12.(2021·丽水)物质结构决定性质,物质性质决定用途,反应本质决定变化现象。如图是小科构建的氢氧化钙部分知识网络,其中“—”表示相连物质能发生化学反应,X与图中所给物质的类别不同。请回答:
(1)酚酞试液在Ca(OH)2溶液中显红色,能使酚酞试液变红的离子是 OH- 。
(2)列举熟石灰[Ca(OH)2]在工农业上的一种用途: 中和酸性土壤 。
OH
-
中和酸性土壤
13.(2021·恩施州)图1是关于氢氧化钠化学性质的思维导图,请据图回答问题。
(1)性质①,将无色酚酞溶液滴入氢氧化钠溶液中,溶液呈 红 色。
(2)性质②,将氢氧化钠溶液滴入稀盐酸中,图2表示该反应过程中溶液pH的变化曲线,n点溶液中的溶质是 NaCl、NaOH (填化学式)。
红
NaCl、NaOH
14.(2021·陕西)学习小组同学用如图装置进行实验。打开分液漏斗的活塞,将NaOH浓溶液加入锥形瓶A中,关闭活塞,打开弹簧夹,观察到烧杯B中液面降低,A中产生白色沉淀。
+H2O
(2)若X是一种碱,其化学式可能是 Ba(OH)2[或Ca(OH)2] (写一种)。
(3)学习小组同学用的X是CaCl2(CaCl2溶液呈中性),实验结束后,同学们又分别做了以下三组实验:
①取少量A中溶液,测其pH,pH>7;
②取少量A中溶液,向其中加入CaCl2溶液,无明显现象,再测其pH,pH>7;
③取少量A中溶液,测其pH,pH>7,再向其中加入K2CO3溶液,产生白色沉淀。
以上三组实验事实中,能说明A中溶液一定含有NaOH的是 ②③ (填序号)。
Ba(OH)2[或Ca(OH)2]
②③
同课章节目录
