化学人教版(2019)选择性必修3 4.1糖类 课件(共35张ppt)
文档属性
| 名称 | 化学人教版(2019)选择性必修3 4.1糖类 课件(共35张ppt) |

|
|
| 格式 | pptx | ||
| 文件大小 | 7.4MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-06-11 00:00:00 | ||
图片预览







文档简介
(共35张PPT)
第四章 生物大分子
第一节 糖类
一、糖类的组成和分类
1、组成
糖类化合物一般由C、H、O三种元素组成。很多糖类分子中氢原子和氧原子数目比恰好为2:1,组成可以用通式Cm(H2O)n表示,故糖类也被称为碳水化合物。如:葡萄糖(C6H12O6)、蔗糖(C12H22O11)、淀粉[(C6H10O5)n]等,
注意:1.并非所有糖类符合这个通式,例如脱氧核糖C5H10O4。
2.符合该通式的也不一定是糖类,例如乙酸C2H4O2
2、定义
从结构上看,糖类是多羟基醛(如葡萄糖)、多羟基酮(如果糖)和它们的脱水缩合物
3、分类:
1)根据糖类能否水解以及水解后的产物,糖类可分为
单糖 寡糖(低聚糖) 多糖
概念 ______水解的糖 1 mol糖水解后能产生________mol单糖的糖 1 mol糖水解后能产生 __________单糖的糖
代表物 _______、______ ______、________ ______、________
分子式 ________ __________ (C6H10O5)n
不能
2~10
葡萄糖
果糖
蔗糖
麦芽糖
C6H12O6
C12H22O11
10 mol以上
淀粉
纤维素
4、糖类间相互转化
二、单糖
(一)葡萄糖——还原性糖
1、存在:水果、蜂蜜等;动物的血液和淋巴液中。
2、物理性质:易溶于水的无色晶体,有甜味,但甜度 不如蔗糖。
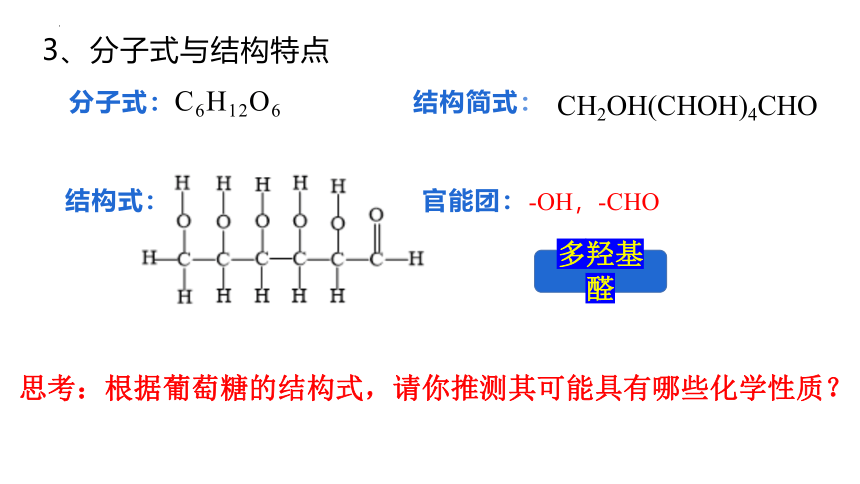
3、分子式与结构特点
分子式:C6H12O6 结构简式:
结构式: 官能团:
思考:根据葡萄糖的结构式,请你推测其可能具有哪些化学性质?
多羟基醛
CH2OH(CHOH)4CHO
-OH,-CHO
(1)与H2发生加成反应
CH2OH(CHOH)4CHO+H2→ CH2OH(CHOH)4CH2OH
(2)银镜反应
4、化学性质
CH2OH(CHOH)4CHO+2Ag(NH3)2OH → CH2OH(CHOH)4COONH4+2Ag↓+3NH3+H2O
(3)与新制Cu(OH)2反应
CH2OH(CHOH)4CHO+2Cu(OH)2 +NaOH → CH2OH(CHOH)4COONa+Cu2O↓+ 3H2O
△
△
属于还原糖
另外:葡萄糖也可以使溴水、酸性高锰酸钾褪色
醛基的性质
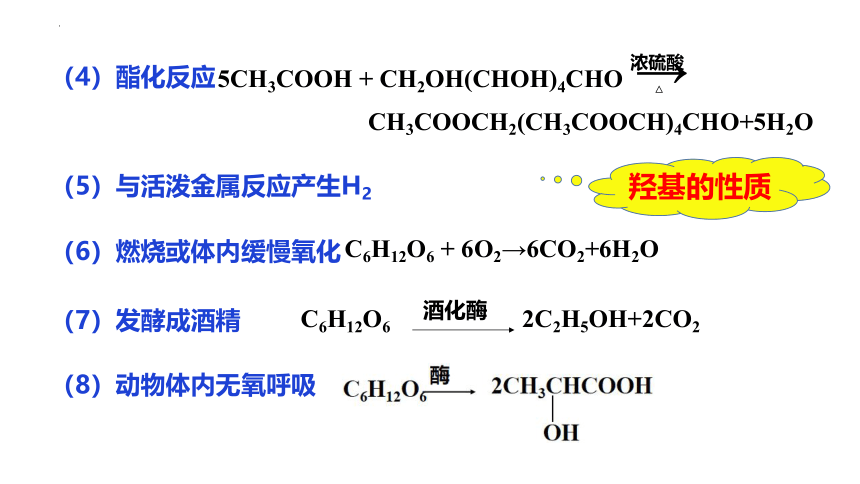
(6)燃烧或体内缓慢氧化
C6H12O6 + 6O2→6CO2+6H2O
C6H12O6 2C2H5OH+2CO2
酒化酶
(7)发酵成酒精
(5)与活泼金属反应产生H2
(4)酯化反应
5CH3COOH + CH2OH(CHOH)4CHO →
CH3COOCH2(CH3COOCH)4CHO+5H2O
△
浓硫酸
羟基的性质
(8)动物体内无氧呼吸
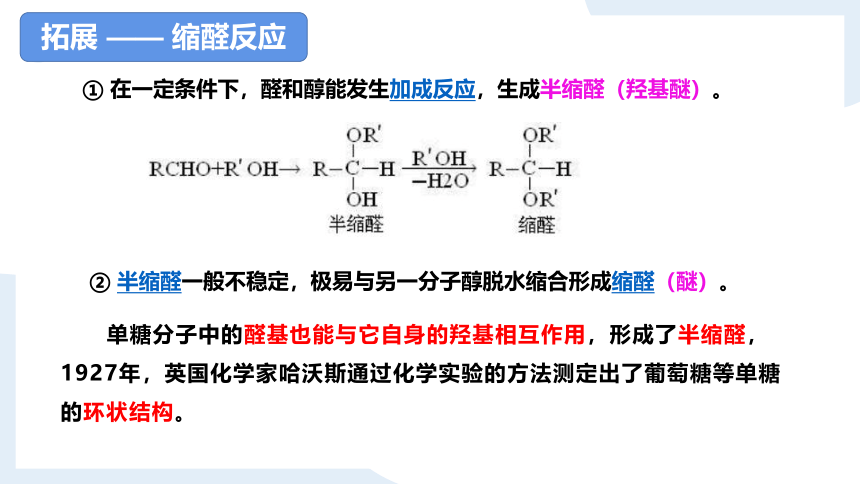
单糖分子中的醛基也能与它自身的羟基相互作用,形成了半缩醛,1927年,英国化学家哈沃斯通过化学实验的方法测定出了葡萄糖等单糖的环状结构。
拓展 —— 缩醛反应
① 在一定条件下,醛和醇能发生加成反应,生成半缩醛(羟基醚)。
② 半缩醛一般不稳定,极易与另一分子醇脱水缩合形成缩醛(醚)。
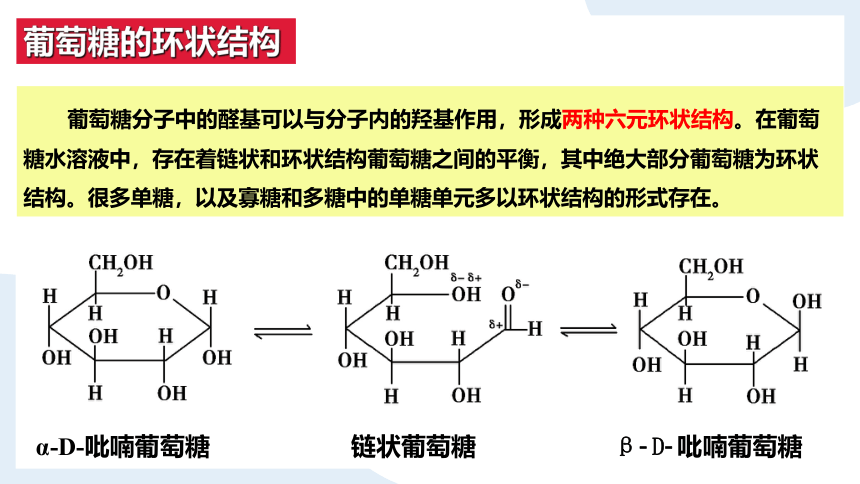
α D 吡喃葡萄糖
链状葡萄糖
β D 吡喃葡萄糖
葡萄糖分子中的醛基可以与分子内的羟基作用,形成两种六元环状结构。在葡萄糖水溶液中,存在着链状和环状结构葡萄糖之间的平衡,其中绝大部分葡萄糖为环状结构。很多单糖,以及寡糖和多糖中的单糖单元多以环状结构的形式存在。
葡萄糖的环状结构
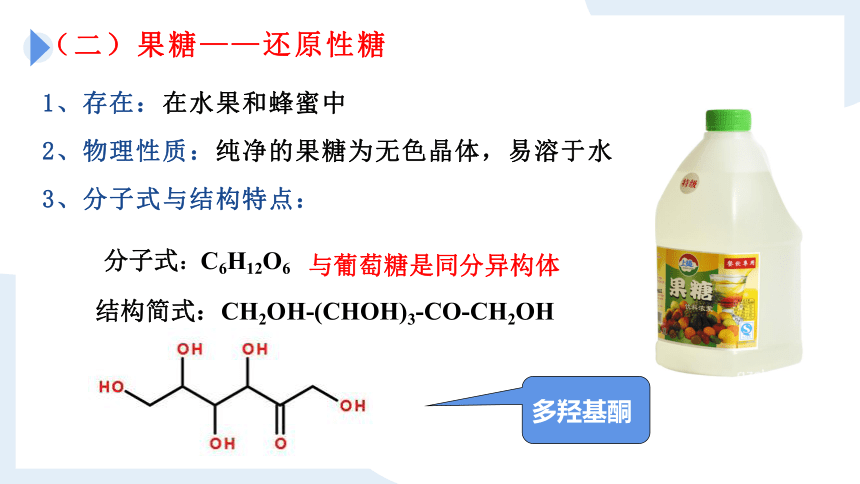
(二)果糖——还原性糖
1、存在:在水果和蜂蜜中
2、物理性质:纯净的果糖为无色晶体,易溶于水
3、分子式与结构特点:
分子式:C6H12O6
结构简式:CH2OH-(CHOH)3-CO-CH2OH
多羟基酮
与葡萄糖是同分异构体
思考:怎么鉴别葡萄糖和果糖?
葡萄糖
果糖
【实验】在试管中加入2 mL 10%NaOH溶液,滴加5%CuSO4溶液5滴,再加入2mL10%果糖溶液,加热,________________产生。
有砖红色沉淀
酮糖具有酮羰基,但在碱性条件下易转化为烯醇中间体,它可异构化为醛式,所以酮糖也易被银氨溶液、新制氢氧化铜氧化(碱性条件)。因此,果糖也是还原性糖。
思考:那究竟该如何鉴别葡萄糖和果糖?
可用溴水鉴别葡萄糖和果糖。
(了解)
4、果糖与葡萄糖的比较
分子式 结构简式 官能团 类别 关系
葡萄糖 C6H12O6 CH2OH(CHOH)4CHO 羟基、醛基 单糖 互为同分异构体
果糖 C6H12O6 羟基、酮羰基 单糖
(三)核糖与脱氧核糖
生物体的遗传物质核糖核酸(RNA)与脱氧核糖核酸(DNA)的重要组成部分
含有5个碳原子的单糖——戊糖。均为醛糖,具有还原性。
核糖
脱氧核糖
(四)最简单的醛糖 —— 丙醛糖,又称甘油醛
结构简式:HOCH2CHOHCHO
分子式:C3H6O3
对映异构
镜面
在分子中连有4个不同的原子或原子团的碳原子叫做不对称碳原子,也叫手性碳原子。
糖类分子与手性
三、二糖——蔗糖与麦芽糖(C12H22O11)
(一)蔗糖
1、存在:大多数植物体内(甜菜、甘蔗中含量最高), 白糖、红糖、冰糖等主要成分都是蔗糖。
2、物理性质:无色晶体,易溶于水,甜味仅次于果糖。
3、分子式:C12H22O11
4、化学性质:
无醛基,无还原性,不发生银镜反应,也不和新制氢氧化铜反应。
水解反应:但水解产物有还原性。
1、存在:发芽的谷粒和麦芽中。
2、物理性质:无色晶体,易溶于水,有甜味,但甜味不如蔗糖。
3、分子式:C12H22O11 (与蔗糖互为同分异构体)。
麦芽糖是由两分子葡萄糖脱水形成的。
(二)麦芽糖(C12H22O11)
对比实验
实验 步骤
实验 现象
实验 结论 蔗糖_______还原糖,麦芽糖_______还原糖 无明显现象
出现砖红色沉淀
不属于
属于
有醛基,有还原性,水解产物也有还原性。
①还原性:能发生银镜反应(分子中含有醛基),是还原性糖。
②水解反应:产物为葡萄糖
4、麦芽糖的化学性质:
蔗糖 麦芽糖
相似点 不 同 点 是否具有还原性
化学 性质
水解 产物
蔗糖和麦芽糖的比较
无-CHO
无还原性
①组成相同,分子式均为C12H22O11,互为同分异构体;
②都属于二糖,1 mol二糖水解后生成2 mol单糖
有-CHO
有还原性
能发生银镜反应,能被新
制的Cu(OH)2氧化
不能发生银镜反应,也不能
被新制的Cu(OH)2氧化
葡萄糖和果糖
葡萄糖
四、多糖——淀粉与纤维素
(C6H10O5)n
土豆:淀粉
棉花:纤维素
四、多糖—淀粉与纤维素(C6H10O5)n
1、淀粉和纤维素的组成与结构
(1)淀粉和纤维素都是由大量葡萄糖单元相互连接组成,属于天然有机高分子; 淀粉的相对分子质量可达到几十万,纤维素可达到几百万;
(2)分子式(C6H10O5)n
(3)淀粉和纤维素分子中所包含的葡萄糖单元数目,即n值不同,二者的结构和组成不同,不是同分异构体。
(4)结构示意图
(一)淀粉
1、存在
在种子、块根和块茎中含量丰富,谷类和薯类含淀粉较多。
2、物理性质
白色固体,无气味、无味道,不溶于冷水,在热水中糊化。
3、 分类
天然淀粉由直链淀粉和支链淀粉组成。支链淀粉含量很高的一些谷物,如糯米、糯玉米等有比较黏的口感
直链淀粉:含有几百个葡萄糖单元,分子量几万~十几万
支链淀粉:含有几千个葡萄糖单元,分子量几十万。
4、淀粉的化学性质
① 遇到碘单质——变蓝
② 非还原糖,不与新制氢氧化铜和银氨溶液反应
(用于检验淀粉或I2的存在)
③ 水解反应:
由于其分子中葡萄糖单元醇羟基的存在,淀粉可以发生酯化反应,可用于生产食品添加剂、表面活性剂和可降解塑料等。
④ 酯化反应:
淀粉液
稀硫酸
加热
水解液
碘水
现象A
NaOH
溶液
中和液
银氨溶液
水浴加热
现象B
现象 结论
现象A 现象B
溶液变蓝
无银镜生成
淀粉没有水解
溶液变蓝
有银镜生成
淀粉部分水解
溶液无现象
有银镜生成
淀粉完全水解
【思 考1】 如何设计实验证明淀粉是没有水解、部分水解,还是完全水解?
酸中水解,
碱中检验!
用I2检验淀粉时,应直接取水解后的混合液加碘水。若取中和液加碘水,因I2与NaOH溶液反应,影响淀粉的检验。
【思 考2】上述实验,能否在加碘水之前,也加入氢氧化钠溶液?
纤维素自然界中分布最广泛的一种多糖,参与构成了植物的细胞壁,起着保护和支持作用。其中:棉花含纤维素92%~95%
亚麻含纤维素约80%
木材含纤维素约50%
(二)纤维素
1. 物理性质
白色纤维状物质,没有甜味,不溶于水,也不溶于一般的有机溶剂。
2. 化学性质
① 不显还原性
② 可发生水解,但比淀粉水解困难
(C6H10O5)n + nH2O nC6H12O6
纤维素
葡萄糖
③ 可以发生酯化反应
如:与硝酸反应,生成纤维素硝酸酯
俗名:硝酸纤维
俗名:醋酸纤维
与醋酸反应,生成纤维素乙酸酯
(二)纤维素
淀粉和纤维素的比较
淀粉 纤维素
分子结构 分子通式 (C6H10O5)n 相对分子质量 几万到几十万 几十万到几百万
分子结构关系 都是由葡萄糖结构单元(C6H10O5)构成的天然有机高分子,但分子内n的数目不同,分子结构不同,不是同分异构体。 都是混合物,没有固定的熔沸点。 化学 性质 共性 无还原性 水解最终生成葡萄糖 主要性质 遇单质碘变蓝 与醋酸、硝酸等发生酯化反应
糖类小结
第四章 生物大分子
第一节 糖类
一、糖类的组成和分类
1、组成
糖类化合物一般由C、H、O三种元素组成。很多糖类分子中氢原子和氧原子数目比恰好为2:1,组成可以用通式Cm(H2O)n表示,故糖类也被称为碳水化合物。如:葡萄糖(C6H12O6)、蔗糖(C12H22O11)、淀粉[(C6H10O5)n]等,
注意:1.并非所有糖类符合这个通式,例如脱氧核糖C5H10O4。
2.符合该通式的也不一定是糖类,例如乙酸C2H4O2
2、定义
从结构上看,糖类是多羟基醛(如葡萄糖)、多羟基酮(如果糖)和它们的脱水缩合物
3、分类:
1)根据糖类能否水解以及水解后的产物,糖类可分为
单糖 寡糖(低聚糖) 多糖
概念 ______水解的糖 1 mol糖水解后能产生________mol单糖的糖 1 mol糖水解后能产生 __________单糖的糖
代表物 _______、______ ______、________ ______、________
分子式 ________ __________ (C6H10O5)n
不能
2~10
葡萄糖
果糖
蔗糖
麦芽糖
C6H12O6
C12H22O11
10 mol以上
淀粉
纤维素
4、糖类间相互转化
二、单糖
(一)葡萄糖——还原性糖
1、存在:水果、蜂蜜等;动物的血液和淋巴液中。
2、物理性质:易溶于水的无色晶体,有甜味,但甜度 不如蔗糖。
3、分子式与结构特点
分子式:C6H12O6 结构简式:
结构式: 官能团:
思考:根据葡萄糖的结构式,请你推测其可能具有哪些化学性质?
多羟基醛
CH2OH(CHOH)4CHO
-OH,-CHO
(1)与H2发生加成反应
CH2OH(CHOH)4CHO+H2→ CH2OH(CHOH)4CH2OH
(2)银镜反应
4、化学性质
CH2OH(CHOH)4CHO+2Ag(NH3)2OH → CH2OH(CHOH)4COONH4+2Ag↓+3NH3+H2O
(3)与新制Cu(OH)2反应
CH2OH(CHOH)4CHO+2Cu(OH)2 +NaOH → CH2OH(CHOH)4COONa+Cu2O↓+ 3H2O
△
△
属于还原糖
另外:葡萄糖也可以使溴水、酸性高锰酸钾褪色
醛基的性质
(6)燃烧或体内缓慢氧化
C6H12O6 + 6O2→6CO2+6H2O
C6H12O6 2C2H5OH+2CO2
酒化酶
(7)发酵成酒精
(5)与活泼金属反应产生H2
(4)酯化反应
5CH3COOH + CH2OH(CHOH)4CHO →
CH3COOCH2(CH3COOCH)4CHO+5H2O
△
浓硫酸
羟基的性质
(8)动物体内无氧呼吸
单糖分子中的醛基也能与它自身的羟基相互作用,形成了半缩醛,1927年,英国化学家哈沃斯通过化学实验的方法测定出了葡萄糖等单糖的环状结构。
拓展 —— 缩醛反应
① 在一定条件下,醛和醇能发生加成反应,生成半缩醛(羟基醚)。
② 半缩醛一般不稳定,极易与另一分子醇脱水缩合形成缩醛(醚)。
α D 吡喃葡萄糖
链状葡萄糖
β D 吡喃葡萄糖
葡萄糖分子中的醛基可以与分子内的羟基作用,形成两种六元环状结构。在葡萄糖水溶液中,存在着链状和环状结构葡萄糖之间的平衡,其中绝大部分葡萄糖为环状结构。很多单糖,以及寡糖和多糖中的单糖单元多以环状结构的形式存在。
葡萄糖的环状结构
(二)果糖——还原性糖
1、存在:在水果和蜂蜜中
2、物理性质:纯净的果糖为无色晶体,易溶于水
3、分子式与结构特点:
分子式:C6H12O6
结构简式:CH2OH-(CHOH)3-CO-CH2OH
多羟基酮
与葡萄糖是同分异构体
思考:怎么鉴别葡萄糖和果糖?
葡萄糖
果糖
【实验】在试管中加入2 mL 10%NaOH溶液,滴加5%CuSO4溶液5滴,再加入2mL10%果糖溶液,加热,________________产生。
有砖红色沉淀
酮糖具有酮羰基,但在碱性条件下易转化为烯醇中间体,它可异构化为醛式,所以酮糖也易被银氨溶液、新制氢氧化铜氧化(碱性条件)。因此,果糖也是还原性糖。
思考:那究竟该如何鉴别葡萄糖和果糖?
可用溴水鉴别葡萄糖和果糖。
(了解)
4、果糖与葡萄糖的比较
分子式 结构简式 官能团 类别 关系
葡萄糖 C6H12O6 CH2OH(CHOH)4CHO 羟基、醛基 单糖 互为同分异构体
果糖 C6H12O6 羟基、酮羰基 单糖
(三)核糖与脱氧核糖
生物体的遗传物质核糖核酸(RNA)与脱氧核糖核酸(DNA)的重要组成部分
含有5个碳原子的单糖——戊糖。均为醛糖,具有还原性。
核糖
脱氧核糖
(四)最简单的醛糖 —— 丙醛糖,又称甘油醛
结构简式:HOCH2CHOHCHO
分子式:C3H6O3
对映异构
镜面
在分子中连有4个不同的原子或原子团的碳原子叫做不对称碳原子,也叫手性碳原子。
糖类分子与手性
三、二糖——蔗糖与麦芽糖(C12H22O11)
(一)蔗糖
1、存在:大多数植物体内(甜菜、甘蔗中含量最高), 白糖、红糖、冰糖等主要成分都是蔗糖。
2、物理性质:无色晶体,易溶于水,甜味仅次于果糖。
3、分子式:C12H22O11
4、化学性质:
无醛基,无还原性,不发生银镜反应,也不和新制氢氧化铜反应。
水解反应:但水解产物有还原性。
1、存在:发芽的谷粒和麦芽中。
2、物理性质:无色晶体,易溶于水,有甜味,但甜味不如蔗糖。
3、分子式:C12H22O11 (与蔗糖互为同分异构体)。
麦芽糖是由两分子葡萄糖脱水形成的。
(二)麦芽糖(C12H22O11)
对比实验
实验 步骤
实验 现象
实验 结论 蔗糖_______还原糖,麦芽糖_______还原糖 无明显现象
出现砖红色沉淀
不属于
属于
有醛基,有还原性,水解产物也有还原性。
①还原性:能发生银镜反应(分子中含有醛基),是还原性糖。
②水解反应:产物为葡萄糖
4、麦芽糖的化学性质:
蔗糖 麦芽糖
相似点 不 同 点 是否具有还原性
化学 性质
水解 产物
蔗糖和麦芽糖的比较
无-CHO
无还原性
①组成相同,分子式均为C12H22O11,互为同分异构体;
②都属于二糖,1 mol二糖水解后生成2 mol单糖
有-CHO
有还原性
能发生银镜反应,能被新
制的Cu(OH)2氧化
不能发生银镜反应,也不能
被新制的Cu(OH)2氧化
葡萄糖和果糖
葡萄糖
四、多糖——淀粉与纤维素
(C6H10O5)n
土豆:淀粉
棉花:纤维素
四、多糖—淀粉与纤维素(C6H10O5)n
1、淀粉和纤维素的组成与结构
(1)淀粉和纤维素都是由大量葡萄糖单元相互连接组成,属于天然有机高分子; 淀粉的相对分子质量可达到几十万,纤维素可达到几百万;
(2)分子式(C6H10O5)n
(3)淀粉和纤维素分子中所包含的葡萄糖单元数目,即n值不同,二者的结构和组成不同,不是同分异构体。
(4)结构示意图
(一)淀粉
1、存在
在种子、块根和块茎中含量丰富,谷类和薯类含淀粉较多。
2、物理性质
白色固体,无气味、无味道,不溶于冷水,在热水中糊化。
3、 分类
天然淀粉由直链淀粉和支链淀粉组成。支链淀粉含量很高的一些谷物,如糯米、糯玉米等有比较黏的口感
直链淀粉:含有几百个葡萄糖单元,分子量几万~十几万
支链淀粉:含有几千个葡萄糖单元,分子量几十万。
4、淀粉的化学性质
① 遇到碘单质——变蓝
② 非还原糖,不与新制氢氧化铜和银氨溶液反应
(用于检验淀粉或I2的存在)
③ 水解反应:
由于其分子中葡萄糖单元醇羟基的存在,淀粉可以发生酯化反应,可用于生产食品添加剂、表面活性剂和可降解塑料等。
④ 酯化反应:
淀粉液
稀硫酸
加热
水解液
碘水
现象A
NaOH
溶液
中和液
银氨溶液
水浴加热
现象B
现象 结论
现象A 现象B
溶液变蓝
无银镜生成
淀粉没有水解
溶液变蓝
有银镜生成
淀粉部分水解
溶液无现象
有银镜生成
淀粉完全水解
【思 考1】 如何设计实验证明淀粉是没有水解、部分水解,还是完全水解?
酸中水解,
碱中检验!
用I2检验淀粉时,应直接取水解后的混合液加碘水。若取中和液加碘水,因I2与NaOH溶液反应,影响淀粉的检验。
【思 考2】上述实验,能否在加碘水之前,也加入氢氧化钠溶液?
纤维素自然界中分布最广泛的一种多糖,参与构成了植物的细胞壁,起着保护和支持作用。其中:棉花含纤维素92%~95%
亚麻含纤维素约80%
木材含纤维素约50%
(二)纤维素
1. 物理性质
白色纤维状物质,没有甜味,不溶于水,也不溶于一般的有机溶剂。
2. 化学性质
① 不显还原性
② 可发生水解,但比淀粉水解困难
(C6H10O5)n + nH2O nC6H12O6
纤维素
葡萄糖
③ 可以发生酯化反应
如:与硝酸反应,生成纤维素硝酸酯
俗名:硝酸纤维
俗名:醋酸纤维
与醋酸反应,生成纤维素乙酸酯
(二)纤维素
淀粉和纤维素的比较
淀粉 纤维素
分子结构 分子通式 (C6H10O5)n 相对分子质量 几万到几十万 几十万到几百万
分子结构关系 都是由葡萄糖结构单元(C6H10O5)构成的天然有机高分子,但分子内n的数目不同,分子结构不同,不是同分异构体。 都是混合物,没有固定的熔沸点。 化学 性质 共性 无还原性 水解最终生成葡萄糖 主要性质 遇单质碘变蓝 与醋酸、硝酸等发生酯化反应
糖类小结
