第1章有机化合物的结构与性质烃测试卷(含解析)高二下学期化学鲁科版(2019)选择性必修3
文档属性
| 名称 | 第1章有机化合物的结构与性质烃测试卷(含解析)高二下学期化学鲁科版(2019)选择性必修3 |
|
|
| 格式 | docx | ||
| 文件大小 | 1.4MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-06-12 00:00:00 | ||
图片预览




文档简介
第1章《有机化合物的结构与性质 烃》测试卷
一、单选题
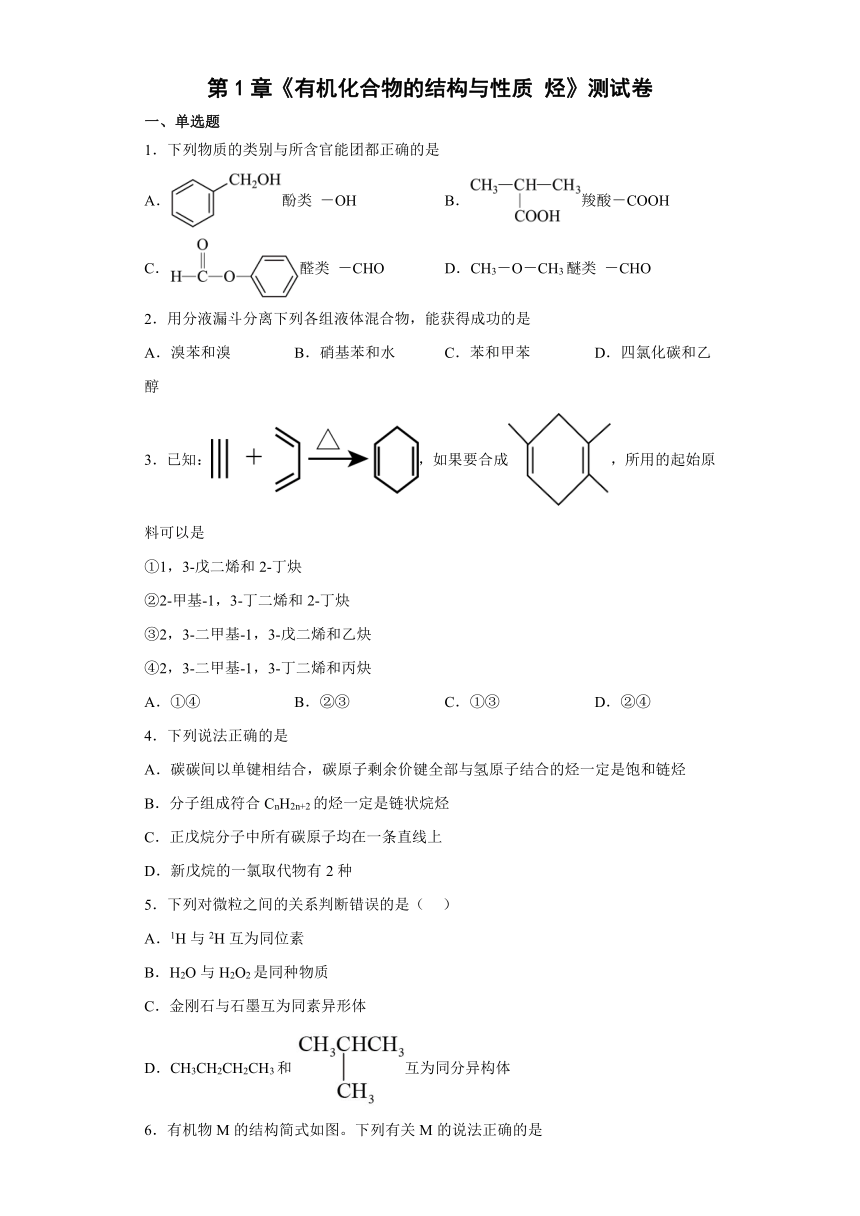
1.下列物质的类别与所含官能团都正确的是
A.酚类 -OH B.羧酸-COOH
C.醛类 -CHO D.CH3-O-CH3醚类 -CHO
2.用分液漏斗分离下列各组液体混合物,能获得成功的是
A.溴苯和溴 B.硝基苯和水 C.苯和甲苯 D.四氯化碳和乙醇
3.已知:,如果要合成,所用的起始原料可以是
①1,3-戊二烯和2-丁炔
②2-甲基-1,3-丁二烯和2-丁炔
③2,3-二甲基-1,3-戊二烯和乙炔
④2,3-二甲基-1,3-丁二烯和丙炔
A.①④ B.②③ C.①③ D.②④
4.下列说法正确的是
A.碳碳间以单键相结合,碳原子剩余价键全部与氢原子结合的烃一定是饱和链烃
B.分子组成符合CnH2n+2的烃一定是链状烷烃
C.正戊烷分子中所有碳原子均在一条直线上
D.新戊烷的一氯取代物有2种
5.下列对微粒之间的关系判断错误的是( )
A.1H与2H互为同位素
B.H2O与H2O2是同种物质
C.金刚石与石墨互为同素异形体
D.CH3CH2CH2CH3和互为同分异构体
6.有机物M的结构简式如图。下列有关M的说法正确的是
A.分子式为C15H12O3
B.苯环上的一氯代物有7种
C.M不能使酸性KMnO4溶液褪色
D.1molM与足量的Na反应,生成22.4LH2
7.下列物质中,不属于酯类的是
A.硬脂酸钠 B.醋酸纤维 C.乙酸乙酯 D.牛油
8.下列关于有机化合物的说法,正确的是
A.图该烃中含有4个碳原子
B.不能用溴水鉴别己烯、乙醇
C.乙烷、乙烯分子内所有原子均可能在同一平面上
D.分子式为与的有机物不一定互为同系物
9.傅克反应是合成芳香族化合物的一种重要方法。有机物a(—R为烃基)和苯通过傅克反应合成b的过程如下(无机小分子产物略去):
下列说法错误的是
A.一定条件下苯与氢气反应的产物之一环己烯与螺[2.3]己烷()互为同分异构体
B.b苯环上的二氯代物超过三种
C.R为C5H11时,a的结构有九种
D.R为C4H9时,1molb加成生成C10H20至少需要3molH2
10.下列分子式只能表示一种物质的是
A.C3H7Cl B.C3H6 C.C3H8 D.C2H6O
11.某单炔烃加氢后产物的结构简式为CH3CH2CH2CH(CH3)CH(C2H5)2,此炔烃可能的结构有
A.1种 B.2.种 C.3种 D.4种
12.苏轼的《格物粗谈》有这样的记载:“红柿摘下未熟,每篮用木瓜三枚放入,得气即发,并无涩味。”按照现代科技观点,该文中的“气”是指
A.二氧化硫 B.乙烯 C.生长素 D.甲烷
13.科学家利用降冰片烯和二氢呋喃共聚合成可降解烯醇醚,如图所示,下列说法错误的是
n(二氢呋喃)+m(降冰片烯)(可降解烯醇醚)
A.二氢呋喃和降冰片烯分子中均含有手性碳
B.二氢呋喃、降冰片烯、可降解烯醇醚均能使酸性高锰酸钾溶液褪色
C.二氢呋喃和可降解烯醇醚中所含的官能团完全相同
D.该反应的原子利用率为100%,符合绿色化学要求
14.下列物质不属于有机物的是
A.碳化硅(SiC) B.甲烷(CH4) C.醋酸(CH3COOH) D.乙炔(C2H2)
15.下列物质:①甲烷②乙烯③乙炔④苯⑤甲苯,既能使酸性高锰酸钾溶液褪色,又能使溴的四氯化碳溶液褪色的是
A.①② B.②③ C.②③⑤ D.②③④
二、填空题
16.苯的某些同系物可被酸性高锰酸钾溶液氧化,例如:
(1)以上反应说明苯的这些同系物分子中的烷基受到了什么影响_________?
(2)若苯的同系物侧链的烷基中,直接与苯连接的碳原子上没有,则该物质一般不能被酸性高锰酸钾溶液氧化成苯甲酸。某分子式为的单烷基取代苯,已知它可以被氧化成苯甲酸的同分异构体共有7种,其中的3种是:
、。
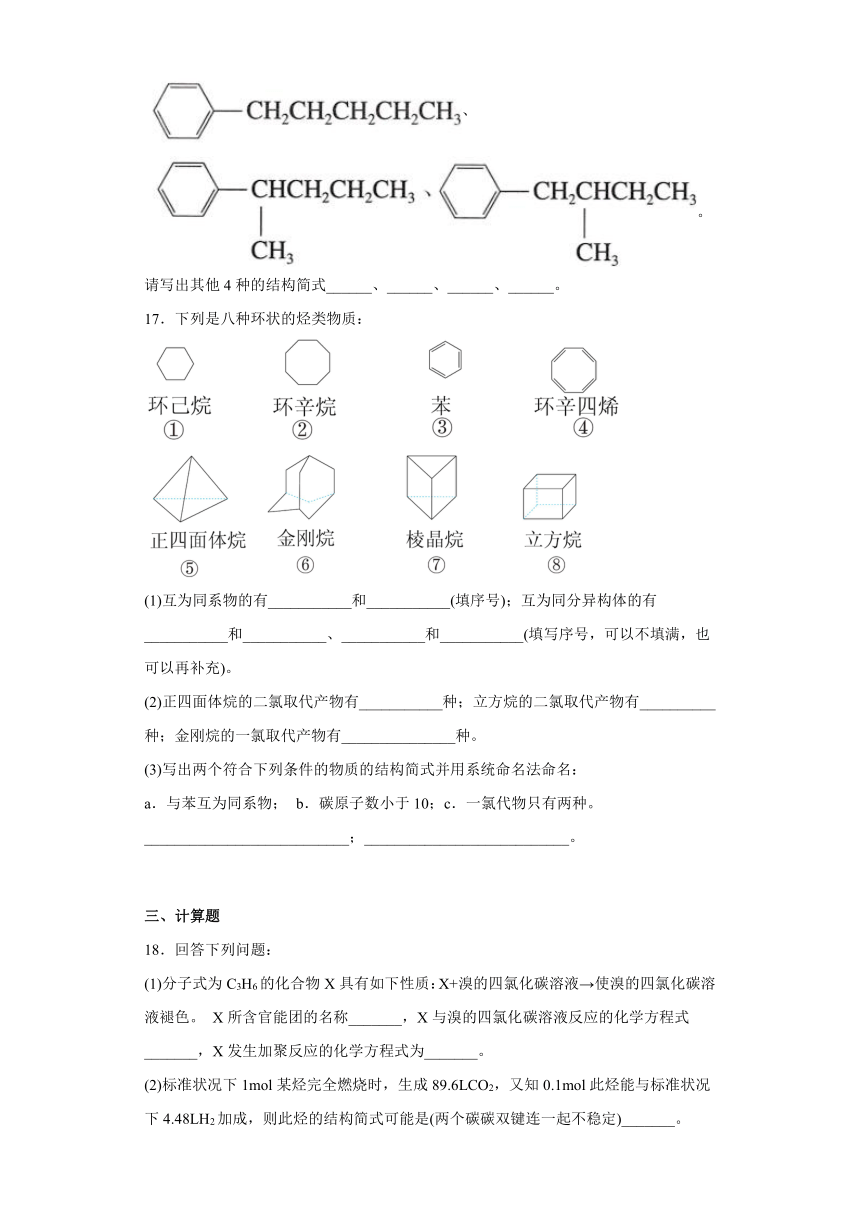
请写出其他4种的结构简式______、______、______、______。
17.下列是八种环状的烃类物质:
(1)互为同系物的有___________和___________(填序号);互为同分异构体的有___________和___________、___________和___________(填写序号,可以不填满,也可以再补充)。
(2)正四面体烷的二氯取代产物有___________种;立方烷的二氯取代产物有__________种;金刚烷的一氯取代产物有_______________种。
(3)写出两个符合下列条件的物质的结构简式并用系统命名法命名:
a.与苯互为同系物; b.碳原子数小于10;c.一氯代物只有两种。___________________________;___________________________。
三、计算题
18.回答下列问题:
(1)分子式为C3H6的化合物X具有如下性质:X+溴的四氯化碳溶液→使溴的四氯化碳溶液褪色。 X所含官能团的名称_______,X与溴的四氯化碳溶液反应的化学方程式_______,X发生加聚反应的化学方程式为_______。
(2)标准状况下1mol某烃完全燃烧时,生成89.6LCO2,又知0.1mol此烃能与标准状况下4.48LH2加成,则此烃的结构简式可能是(两个碳碳双键连一起不稳定)_______。
(3)一种能使溴水褪色的烃,标准状况下5.6 L 完全燃烧时生成28L二氧化碳和22.5g水。则该烃的结构简式有_______种(不考虑顺反异构)。
(4)分子式为C6H14的化合物的同分异构体中,写出其中含有四个甲基的物质的结构简式为_______。
19.将11.2L(标准状况)乙烯和乙烷的混合气体通入足量溴水中,充分反应后,溴水的质量增加了5.6g。求原气体混合物中乙烯与乙烷的物质的量之比和质量比。
四、实验题
20.化学实验小组同学设计的苯与溴反应制取溴苯的实验方案和装置如下:
①把苯和少量液态溴放在烧瓶里,同时加入少量铁。
②用带导管的瓶塞寒紧瓶口,跟瓶口垂直的一段导管可以兼起冷凝的作用。
③观察并记录实验现象。
请回答相关问题:
(1)铁屑的本反应中的作用是________________。实验开始后,可以看到的现象是______________________。
(2)能说明该反应是取代反应而不是加成反应的现象是_______________。
(3)纯净的溴苯是无色的,但本实验中得到的溴苯是褐色的,原因是____________________。
21.已知碳化铝(Al4C3)与水反应生成氢氧化铝和甲烷。为了探究甲烷性质,某同学设计如下两组实验方案:甲方案探究甲烷与氧化剂反应(如图1所示);乙方案探究甲烷与氯气反应的条件(如图2所示)。
甲方案实验现象:溴水无颜色变化,无水硫酸铜变蓝色,澄清石灰水变浑浊。
乙方案实验操作过程:通过排饱和食盐水的方法收集两瓶甲烷与氯气(体积比为1∶4)的混合气体,I瓶放在光亮处,II瓶用预先准备好的黑色纸套套上,按图2安装好装置,并加紧弹簧夹a和b。
(1)碳化铝与稀硫酸反应的化学方程式为_________________________。
(2)写出甲方案实验中硬质试管里可能发生的化学方程式_______________(实验测得消耗甲烷与氧化铜物质的量之比2∶7)。
(3)实验甲中浓硫酸的作用是___________,集气瓶中收集到的气体__________(填“能”或“不能”)直接排入空气中?
(4)下列对甲方案实验中的有关现象与结论的叙述都正确的是( )
A.酸性高锰酸钾溶液不褪色,结论是通常条件下,甲烷不能与强氧化剂反应
B.硬质试管里黑色粉末变红色,说明氧化铜发生了氧化反应
C.硬质试管里黑色粉末变红色,推断氧化铜与甲烷反应只生成水和二氧化碳
D.甲烷不能与溴水反应,推知甲烷不能与卤素单质反应
(5)乙方案中烧杯里放入足量的水,打开弹簧夹a、b,一段时间后,观察到有水倒吸到I瓶中,但水并不能充满I瓶,请写出该实验现象所涉及的一个化学方程式_______________。除了上述现象外,该实验中还可能观察到的现象有____________(填序号)。
A.I瓶中气体颜色变浅 B.I瓶中出现白雾
C.I瓶瓶内壁出现油状物质 D.II瓶中与I瓶现象相同
参考答案:
1.B
【详解】A. 属于酚类,官能团为-OH,故A错误;
B. 属于羧酸,官能团为-COOH,故B正确;
C. 属于酯类,官能团为-COOC-,故C错误;
D.CH3-O-CH3属于醚类,官能团为-C-O-C-,故D错误。
综上所述,答案为B。
2.B
【分析】根据分液漏斗可以将互不相溶的两层液体分开,则分析选项中物质的溶解性即可解答。
【详解】A.溴和溴苯互溶,不能用分液漏斗进行分离,故A不符合;
B.硝基苯和水不溶,能用分液漏斗进行分离,故B符合;
C.苯和甲苯互溶,不能用分液漏斗进行分离,故C不符合;
D.四氯化碳和乙醇互溶,不能用分液漏斗进行分离,故D不符合。
故选B。
3.D
【详解】由已知可得, 或 ,则合成 的原料可以为2,3-二甲基-1,3-丁二烯和丙炔或者2-甲基-1,3-丁二烯和2-丁炔,综上所述D符合题意,故D正确;
答案选D。
4.B
【详解】A.碳碳间以单键相结合,碳原子剩余价键全部与氢原子结合的烃为饱和烃,可为链状烷烃,也可为环烷烃,A错误,
B.碳碳间以单键相结合,碳原子剩余价键全部与氢原子结合的烃为饱和烃,可为链状烷烃,也可为环烷烃,但分子组成符合CnH2n+2的烃一定为链状烷烃,B正确;
C.在烷烃分子中与碳原子紧邻的四个原子构成四面体形,所以正戊烷分子中所有碳原子呈锯齿形,而非直线形,C错误;
D.新戊烷分子完全对称,分子中只有一种氢原子,故一氯代物只有一种,D错误;
故答案为B。
5.B
【详解】A.1H与2H是氢的不同核素,互为同位素,A正确;
B.H2O与H2O2是不同物质,B错误;
C.金刚石与石墨是碳的不同单质,互为同素异形体,C正确;
D.CH3CH2CH2CH3和的分子式均是C4H10,结构不同,互为同分异构体,D正确;
答案选B。
6.B
【详解】A.由物质M的结构简式可知,分子式为,选项A错误;
B.由物质M的结构简式可知其苯环上有7种等效氢,故苯环上的一氯代物有7种,选项B正确;
C.M含醇羟基,能使酸性KMnO4溶液褪色,选项C错误;
D.M含有羟基和羧基都可以与Na反应,生成1mol H2,标准状况下为22.4 L,选项D错误。
答案选B。
7.A
【详解】A.硬脂酸钠属于盐,A符合题意;
B.醋酸纤维是醋酸和纤维素形成的酯类,B不符合题意;
C.乙酸乙酯属于酯类,C不符合题意;
D.牛油属于酯类,D不符合题意;
故选A。
8.D
【详解】A.烃是只含碳氢两种元素的有机物,而该有机物含有O元素,不属于烃,故A错误;
B.乙烯和溴水发生加成反应,乙醇与溴水不反应,因此能用溴水鉴别己烯、乙醇,故B错误
C.乙烯分子内所有原子均可能在同一平面上,而乙烷中含有碳连四个价键,所有原子不能在同一平面上,故C错误;
D.是乙烯,可以是丁烯或环丁烷,因此分子式为与的有机物不一定互为同系物,故D正确。
综上所述,答案为D。
9.C
【详解】A.环己烯与螺[2.3]己烷的分子式相同、结构不同,二者互为同分异构体,故A正确;
B.b的苯环上含3种H原子,固定1个Cl在R的邻位,移动另一个Cl有4种,再固定1个Cl在R的间位,移动另一个Cl有2种,共6种,故B正确;
C.CH3CH2CH2CH2CH3、、中含H原子数分别为3、4、1,则R为C5H11时,a的结构有8种,故C错误;
D.R为C4H9时,为饱和烃基,b中只有苯环与氢气发生加成反应,则1molb加成生成C10H20至少需要3molH2,故D正确;
故选:C。
10.C
【分析】只能表示一种物质,说明不存在同分异构体。
【详解】A.可以是1—氯丙烷,也可以是2—氯丙烷,A错误;
B.可以是丙烯,也可以是环丙烷,B错误;
C.只能是丙烷,不存在同分异构体,C正确;
D.可以是乙醇,也可以是二甲醚,D错误,
答案选C。
11.C
【详解】加成反应指有机物分子中的不饱和键断裂,断键原子与其他原子或原子团相结合,生成新的化合物的反应。根据加成原理采取逆推法还原C≡C,烷烃分子中相邻碳原子上均带2个氢原子的碳原子间是对应炔存在C≡C的位置,则根据CH3CH2CH2CH(CH3)CH(C2H5)2可知左侧有两种三键,右侧乙基中有一种三键,共计是3种。答案选C。
12.B
【详解】A.“气”起了催熟作用,二氧化硫没有相应作用,故A不选;
B.乙烯的主要作用是促进果实成熟,故B选;
C.生长素具有两重性既能促进生长也能抑制生长,既能促进发芽也能抑制发芽,与催熟无关,故C不选;
D.甲烷不具有催熟作用,故D不选;
故选:B。
13.A
【详解】A.手性碳指的是碳原子连接的是四个不同的原子或原子团,二氢呋喃中不含有这样子的碳原子,即二氢呋喃不含手性碳,A错误,符合题意;
B.二氢呋喃、降冰片烯、可降解烯醇醚均含有不饱和碳碳双键,能使酸性高锰酸钾溶液褪色,B正确,不符合题意;
C.二氢呋喃和可降解烯醇醚中含有的官能团都为醚键和碳碳双键,所含的官能团完全相同,C正确,不符合题意;
D.该反应只有一种产物,表明该反应的原子利用率为100%,符合绿色化学要求,D正确,不符合题意;
故选A。
14.A
【详解】A.碳化硅(SiC)是含碳元素的无机化合物,不属于有机物,选项A符合题意;
B.甲烷(CH4)分子中含有C、H两种元素,属于烃,是有机化合物,选项B不符合题意;
C.醋酸(CH3COOH)分子中含有C、H、O三种元素,是烃的衍生物,是有机化合物,选项C不符合题意;
D.乙炔(C2H2)是含碳、氢两元素的化合物,是烃,属于有机物,选项D不符合题意;
答案选A。
15.B
【详解】乙烯、乙炔和甲苯都能被酸性高锰酸钾溶液氧化而使酸性高锰酸钾溶液褪色,乙烯和乙炔中均含有碳碳不饱和键,二者均能和溴发生加成反应而使溴的四氯化碳溶液褪色,故选:B。
16.(1)说明苯的这些同系物分子中的烷基受到了苯环的影响
(2)
【解析】(1)
烷烃稳定,不能与酸性的高锰酸钾溶液发生氧化还原反应,但是苯的一些同系物可以与酸性的高锰酸钾溶液发生氧化还原反应,说明苯的这些同系物分子中的烷基受到了苯环的影响,故答案为:说明苯的这些同系物分子中的烷基受到了苯环的影响;
(2)
根据题意,这些异构体的侧链烷基中,与苯环直接相连的碳原子必须有C-H,才能被氧化成苯甲酸,所以其他四种的结构简式分别为:、、、,故答案为:;;;。
17.(1) ① ② ⑤ ⑦ ④ ⑧
(2) 1 3 2
(3) (1,4-二甲苯) (1,3,5-三甲苯)
【详解】(1)同系物:结构相似,分子组成上相差一个或若干个CH2原子团的化合物,则环己烷(C6H12)与环辛烷(C8H16)均为环烷烃,分子组成上相差2个CH2,互为同系物;同分异构体:分子式相同,结构不同的化合物,则苯与棱晶烷(分子式均为C6H6),环辛四烯与立方烷(分子式均为C8H8)互为同分异构体;
(2)正四面体烷完全对称,只有一种氢原子,一氯代物只有1种,一氯代物中氢原子也只有1种,所以故二氯代物只有1种;金刚烷分子中有两种氢原子,一种是次甲基氢,一种亚甲基氢,所以其一氯代物有2种;立方烷分子中只有一种氢原子,其一氯代物有1种,而一氯代物有3种氢原子,分为在,则立方烷的二氯代物有3种;
(3)苯的同系物含有1个苯环,侧链为烷基,一氯代物只有两种的物质,说明只有2种氢原子,则与苯互为同系物且一氯代物只有两种的物质的结构简式为,名称为1,4-二甲苯;,名称为1,3,5-三甲苯。
【点睛】注意限制条件下同分异构体的书写,根据正四面体烷的结构写出分子式;正四面体烷二氯代物的种类取决于一氯代物中氢原子的种类;金刚烷的一氯代物取决于氢原子的种类;立方烷的二氯代物取决于一氯代物中氢原子的种类;苯的同系物含有1个苯环,侧链为烷基,一氯代物只有两种的物质,说明只有2种氢原子,然后根据苯的同系物命名方法命名。
18.(1) 碳碳双键 CH3CH=CH2+Br2 n CH3CH=CH2
(2)HC≡CCH2CH3、CH3 C≡CCH3、CH2=CHCH=CH2
(3)5
(4)
【详解】(1)分子式为C3H6的烃X能使溴的四氯化碳溶液褪色说明分子中含有碳碳双键,属于烯烃,则X的结构简式为CH3CH=CH2,官能团为碳碳双键;CH3CH=CH2与溴的四氯化碳溶液发生加成反应生成1,2—二溴乙烷,反应的化学方程式为CH3CH=CH2+Br2;催化剂作用下丙烯能发生加聚反应生成聚丙烯,反应的化学方程式为n CH3CH=CH2,故答案为:碳碳双键;CH3CH=CH2+Br2;n CH3CH=CH2;
(2)标准状况下89.6L二氧化碳的物质的量为=4mol,则标准状况下1mol某烃完全燃烧时,生成89.6L二氧化碳说明烃分子中含有4个碳原子,标准状况下4.48L氢气的物质的量为=0.2mol,0.1mol此烃能与标准状况下4.48L氢气加成说明烃分子中含有2个碳碳双键或1个三键,由两个碳碳双键连一起不稳定可知,符合条件的炔烃、二烯烃的结构简式为HC≡CCH2CH3、CH3 C≡CCH3、CH2=CHCH=CH2,故答案为:HC≡CCH2CH3、CH3 C≡CCH3、CH2=CHCH=CH2;
(3)标准状况下,5.6 L烃的物质的量为=0.25mol、28 L二氧化碳的物质的量为=1.25mol,22.5g水的物质的量为=1.25mol,则烃分子和分子中碳原子、氢原子的物质的量比为0.25mol:1.25mol:1.25mol×2=1:5:10,分子式为C5H10,该烃能使溴水褪色说明烃分子中含有碳碳双键,属于烯烃,不考虑顺反异构的戊烯共有5种,分别是1—戊烯、2—戊烯、2—甲基—1—丁烯、3—甲基—1—丁烯、2—甲基—2—丁烯,故答案为:5;
(4)分子式为C6H14的烃为烷烃,分子中含有四个甲基的烃为2,3—二甲基丁烷,结构简式为,故答案为:。
19.(1)物质的量之比2:3
(2)质量之比28:45
【详解】11.2L混合气体的物质的量为n===0.5mol,
乙烯含有双键,能与溴水发生加成反应,乙烯和乙烷的混合气体通入足量溴水中,充分反应后,溴水的质量增加了5.6g,即为乙烯的质量,
所以乙烯的物质的量为n===0.2mol,
则乙烷的物质的量为:0.5mol-0.2mol=0.3mol,质量为:0.3mol×30g/mol=9g,
所以,乙烯与乙烷的物质的量之比为0.2mol:0.3mol=2:3,
质量之比为5.6g:9g=28:45,
答:原气体混合物中乙烯与乙烷的物质的量之比为:2:3;质量比分别为28:45。
20.(1) 与液溴反应生成催化剂 液体轻微翻腾,有气体逸出,导管口有白雾产生,锥形瓶溶液中有浅黄色沉淀生成,烧瓶底部有褐色不溶于水的液体生成
(2)锥形瓶内有淡黄色沉淀生成
(3)未发生反应的溴和反应中的催化剂FeBr3,溶解在生成的溴苯中
【分析】铁与单质溴发生反应产生FeBr3,苯与液溴在FeBr3催化下发生取代反应产生溴苯和HBr,HBr通过导气管进入锥形瓶中,与溶液中的AgNO3发生取代反应产生AgBr浅黄色沉淀,垂直于烧瓶口的长的导气管作用是导气和冷凝,减少苯及液溴的挥发。
【详解】(1)铁屑与液溴在常温下反应生成溴化铁,溴化铁在苯与液溴发生取代反应生成溴苯时作催化剂,故铁屑在本反应中的作用是与液溴反应生成催化剂;实验开始后,苯与液溴发生取代反应产生溴苯和HBr,反应放出大量的热量,可以看到的现象是液体轻微翻腾,有气体逸出,导管口有白雾产生,HBr气体进入锥形瓶溶液中,与AgNO3溶液反应产生AgBr浅黄色沉淀,故还可以看到在锥形瓶中有浅黄色沉淀生成,反应产生的溴苯密度比苯大,未反应的溴溶解在溴苯中,故还可以看到烧瓶底部有褐色不溶于水的液体生成;
(2)若发生取代反应,反应产生溴苯和HBr,HBr气体不溶于有机物中,通过导气管进入锥形瓶中,与AgNO3溶液发生复分解反应产生AgBr浅黄色沉淀;若发生加成反应,挥发的液溴通过垂直于烧瓶口的长的导气管冷凝作用,回流到烧瓶中,因此锥形瓶中不会产生淡黄色沉淀。故能说明该反应是取代反应而不是加成反应的现象是锥形瓶内有淡黄色沉淀生成;
(3)纯净的溴苯是无色的,但反应物不能完全转化为生成物,未发生反应的溴溶解在生成的溴苯中,使本实验中得到的溴苯是褐色的。
21. Al4C3+6H2SO4=2Al2(SO4)3+3CH4↑ 2CH4+7CuO7Cu+CO2+CO+4H2O 干燥甲烷 不能 A CH4+Cl2CH3Cl+HCl ABC
【详解】(1)已知碳化铝(Al4C3)与水反应生成氢氧化铝和甲烷,用假设Al4C3 的系数为1的方法配平可得:Al4C3 + 6 H2SO4 =2Al2(SO4)3 + 3CH4↑;
(2甲方案的目的是探究甲烷与氧化剂反应,实验测得消耗甲烷与氧化铜物质的量之比2∶7可知,设甲烷的系数为2,先后依据铜、氢、氧、碳原子个数守恒可得:硬质试管里可能发生的化学方程式为2 CH4 + 7 CuO7 Cu + CO2 + CO + 4 H2O;
(3)浓硫酸具有吸水性,且不能与甲烷反应,因此实验甲中浓硫酸起干燥甲烷的作用;集气瓶是尾气处理装置,其中收集到的不溶于水的气体主要是CO,CO气体有毒,不能直接排入空气;
(4)A.酸性高锰酸钾溶液不褪色,结论是通常条件下,甲烷不能与强氧化剂反应,A正确;
B.硬质试管里黑色粉末变红色,说明氧化铜发生了还原反应,因为铜元素由+2价降低到0价,B错误;
C.硬质试管里黑色粉末变红色,推断氧化铜与甲烷反应不仅仅生成水和二氧化碳,还生成了具有还原性的CO,C错误;
D.甲烷不能与溴水反应,推知甲烷不能与卤素单质的水溶液反应,但是甲烷能与纯净的卤素单质在光照或高温下发生取代反应,D错误;
答案选A;
(5)乙方案中烧杯里放入足量的水,打开弹簧夹a、b,一段时间后,观察到有水倒吸到I瓶中,但水并不能充满I瓶,说明甲烷与氯气在光照下生成了易溶于水的氯化氢气体,因此推断发生了取代反应,如CH4 + Cl2 CH3Cl + HCl;
A.I瓶中气体颜色变浅,因为黄绿色的氯气逐渐消耗完全,A正确;
B.I瓶中出现白雾,因为生成的氯化氢气体容易与水蒸气结合为盐酸小液滴,B正确;
C.I瓶瓶内壁出现油状物质,因为甲烷与氯气发生取代反应,生成的一氯甲烷是气体,二氯甲烷、三氯甲烷、四氯化碳是油状液体,C正确;
D.II瓶中与I瓶现象不相同,因为I有光照条件,能发生取代反应,II缺少光照条件,不能发生取代反应,D错误;
答案选ABC。
【点晴】控制变量思想方法,探究实验异常现象成为近几年实验探究命题的热点,突出对实验能力的考查。该题为实验探究题,装置图、流程图很简单,但探究过程较复杂,准确全面获取信息、通过控制变量思想进行逻辑分析是解题的关键,凭感觉做题,不容易准确获取题中信息。该类试题的解题策略为:(1)确定变量:解答这类题目时首先要认真审题,理清影响实验探究结果的因素有哪些。(2)定多变: 在探究时,应该先确定其他的因素不变,只变化一种因素,看这种因素与探究的问题存在怎样的关系;这样确定一种以后,再确定另一种,通过分析每种因素与所探究问题之间的关系,得出所有影响因素与所探究问题之间的关系。(3)数据有效;解答时注意选择数据(或设置实验)要有效,且变量统一,否则无法做出正确判断。
一、单选题
1.下列物质的类别与所含官能团都正确的是
A.酚类 -OH B.羧酸-COOH
C.醛类 -CHO D.CH3-O-CH3醚类 -CHO
2.用分液漏斗分离下列各组液体混合物,能获得成功的是
A.溴苯和溴 B.硝基苯和水 C.苯和甲苯 D.四氯化碳和乙醇
3.已知:,如果要合成,所用的起始原料可以是
①1,3-戊二烯和2-丁炔
②2-甲基-1,3-丁二烯和2-丁炔
③2,3-二甲基-1,3-戊二烯和乙炔
④2,3-二甲基-1,3-丁二烯和丙炔
A.①④ B.②③ C.①③ D.②④
4.下列说法正确的是
A.碳碳间以单键相结合,碳原子剩余价键全部与氢原子结合的烃一定是饱和链烃
B.分子组成符合CnH2n+2的烃一定是链状烷烃
C.正戊烷分子中所有碳原子均在一条直线上
D.新戊烷的一氯取代物有2种
5.下列对微粒之间的关系判断错误的是( )
A.1H与2H互为同位素
B.H2O与H2O2是同种物质
C.金刚石与石墨互为同素异形体
D.CH3CH2CH2CH3和互为同分异构体
6.有机物M的结构简式如图。下列有关M的说法正确的是
A.分子式为C15H12O3
B.苯环上的一氯代物有7种
C.M不能使酸性KMnO4溶液褪色
D.1molM与足量的Na反应,生成22.4LH2
7.下列物质中,不属于酯类的是
A.硬脂酸钠 B.醋酸纤维 C.乙酸乙酯 D.牛油
8.下列关于有机化合物的说法,正确的是
A.图该烃中含有4个碳原子
B.不能用溴水鉴别己烯、乙醇
C.乙烷、乙烯分子内所有原子均可能在同一平面上
D.分子式为与的有机物不一定互为同系物
9.傅克反应是合成芳香族化合物的一种重要方法。有机物a(—R为烃基)和苯通过傅克反应合成b的过程如下(无机小分子产物略去):
下列说法错误的是
A.一定条件下苯与氢气反应的产物之一环己烯与螺[2.3]己烷()互为同分异构体
B.b苯环上的二氯代物超过三种
C.R为C5H11时,a的结构有九种
D.R为C4H9时,1molb加成生成C10H20至少需要3molH2
10.下列分子式只能表示一种物质的是
A.C3H7Cl B.C3H6 C.C3H8 D.C2H6O
11.某单炔烃加氢后产物的结构简式为CH3CH2CH2CH(CH3)CH(C2H5)2,此炔烃可能的结构有
A.1种 B.2.种 C.3种 D.4种
12.苏轼的《格物粗谈》有这样的记载:“红柿摘下未熟,每篮用木瓜三枚放入,得气即发,并无涩味。”按照现代科技观点,该文中的“气”是指
A.二氧化硫 B.乙烯 C.生长素 D.甲烷
13.科学家利用降冰片烯和二氢呋喃共聚合成可降解烯醇醚,如图所示,下列说法错误的是
n(二氢呋喃)+m(降冰片烯)(可降解烯醇醚)
A.二氢呋喃和降冰片烯分子中均含有手性碳
B.二氢呋喃、降冰片烯、可降解烯醇醚均能使酸性高锰酸钾溶液褪色
C.二氢呋喃和可降解烯醇醚中所含的官能团完全相同
D.该反应的原子利用率为100%,符合绿色化学要求
14.下列物质不属于有机物的是
A.碳化硅(SiC) B.甲烷(CH4) C.醋酸(CH3COOH) D.乙炔(C2H2)
15.下列物质:①甲烷②乙烯③乙炔④苯⑤甲苯,既能使酸性高锰酸钾溶液褪色,又能使溴的四氯化碳溶液褪色的是
A.①② B.②③ C.②③⑤ D.②③④
二、填空题
16.苯的某些同系物可被酸性高锰酸钾溶液氧化,例如:
(1)以上反应说明苯的这些同系物分子中的烷基受到了什么影响_________?
(2)若苯的同系物侧链的烷基中,直接与苯连接的碳原子上没有,则该物质一般不能被酸性高锰酸钾溶液氧化成苯甲酸。某分子式为的单烷基取代苯,已知它可以被氧化成苯甲酸的同分异构体共有7种,其中的3种是:
、。
请写出其他4种的结构简式______、______、______、______。
17.下列是八种环状的烃类物质:
(1)互为同系物的有___________和___________(填序号);互为同分异构体的有___________和___________、___________和___________(填写序号,可以不填满,也可以再补充)。
(2)正四面体烷的二氯取代产物有___________种;立方烷的二氯取代产物有__________种;金刚烷的一氯取代产物有_______________种。
(3)写出两个符合下列条件的物质的结构简式并用系统命名法命名:
a.与苯互为同系物; b.碳原子数小于10;c.一氯代物只有两种。___________________________;___________________________。
三、计算题
18.回答下列问题:
(1)分子式为C3H6的化合物X具有如下性质:X+溴的四氯化碳溶液→使溴的四氯化碳溶液褪色。 X所含官能团的名称_______,X与溴的四氯化碳溶液反应的化学方程式_______,X发生加聚反应的化学方程式为_______。
(2)标准状况下1mol某烃完全燃烧时,生成89.6LCO2,又知0.1mol此烃能与标准状况下4.48LH2加成,则此烃的结构简式可能是(两个碳碳双键连一起不稳定)_______。
(3)一种能使溴水褪色的烃,标准状况下5.6 L 完全燃烧时生成28L二氧化碳和22.5g水。则该烃的结构简式有_______种(不考虑顺反异构)。
(4)分子式为C6H14的化合物的同分异构体中,写出其中含有四个甲基的物质的结构简式为_______。
19.将11.2L(标准状况)乙烯和乙烷的混合气体通入足量溴水中,充分反应后,溴水的质量增加了5.6g。求原气体混合物中乙烯与乙烷的物质的量之比和质量比。
四、实验题
20.化学实验小组同学设计的苯与溴反应制取溴苯的实验方案和装置如下:
①把苯和少量液态溴放在烧瓶里,同时加入少量铁。
②用带导管的瓶塞寒紧瓶口,跟瓶口垂直的一段导管可以兼起冷凝的作用。
③观察并记录实验现象。
请回答相关问题:
(1)铁屑的本反应中的作用是________________。实验开始后,可以看到的现象是______________________。
(2)能说明该反应是取代反应而不是加成反应的现象是_______________。
(3)纯净的溴苯是无色的,但本实验中得到的溴苯是褐色的,原因是____________________。
21.已知碳化铝(Al4C3)与水反应生成氢氧化铝和甲烷。为了探究甲烷性质,某同学设计如下两组实验方案:甲方案探究甲烷与氧化剂反应(如图1所示);乙方案探究甲烷与氯气反应的条件(如图2所示)。
甲方案实验现象:溴水无颜色变化,无水硫酸铜变蓝色,澄清石灰水变浑浊。
乙方案实验操作过程:通过排饱和食盐水的方法收集两瓶甲烷与氯气(体积比为1∶4)的混合气体,I瓶放在光亮处,II瓶用预先准备好的黑色纸套套上,按图2安装好装置,并加紧弹簧夹a和b。
(1)碳化铝与稀硫酸反应的化学方程式为_________________________。
(2)写出甲方案实验中硬质试管里可能发生的化学方程式_______________(实验测得消耗甲烷与氧化铜物质的量之比2∶7)。
(3)实验甲中浓硫酸的作用是___________,集气瓶中收集到的气体__________(填“能”或“不能”)直接排入空气中?
(4)下列对甲方案实验中的有关现象与结论的叙述都正确的是( )
A.酸性高锰酸钾溶液不褪色,结论是通常条件下,甲烷不能与强氧化剂反应
B.硬质试管里黑色粉末变红色,说明氧化铜发生了氧化反应
C.硬质试管里黑色粉末变红色,推断氧化铜与甲烷反应只生成水和二氧化碳
D.甲烷不能与溴水反应,推知甲烷不能与卤素单质反应
(5)乙方案中烧杯里放入足量的水,打开弹簧夹a、b,一段时间后,观察到有水倒吸到I瓶中,但水并不能充满I瓶,请写出该实验现象所涉及的一个化学方程式_______________。除了上述现象外,该实验中还可能观察到的现象有____________(填序号)。
A.I瓶中气体颜色变浅 B.I瓶中出现白雾
C.I瓶瓶内壁出现油状物质 D.II瓶中与I瓶现象相同
参考答案:
1.B
【详解】A. 属于酚类,官能团为-OH,故A错误;
B. 属于羧酸,官能团为-COOH,故B正确;
C. 属于酯类,官能团为-COOC-,故C错误;
D.CH3-O-CH3属于醚类,官能团为-C-O-C-,故D错误。
综上所述,答案为B。
2.B
【分析】根据分液漏斗可以将互不相溶的两层液体分开,则分析选项中物质的溶解性即可解答。
【详解】A.溴和溴苯互溶,不能用分液漏斗进行分离,故A不符合;
B.硝基苯和水不溶,能用分液漏斗进行分离,故B符合;
C.苯和甲苯互溶,不能用分液漏斗进行分离,故C不符合;
D.四氯化碳和乙醇互溶,不能用分液漏斗进行分离,故D不符合。
故选B。
3.D
【详解】由已知可得, 或 ,则合成 的原料可以为2,3-二甲基-1,3-丁二烯和丙炔或者2-甲基-1,3-丁二烯和2-丁炔,综上所述D符合题意,故D正确;
答案选D。
4.B
【详解】A.碳碳间以单键相结合,碳原子剩余价键全部与氢原子结合的烃为饱和烃,可为链状烷烃,也可为环烷烃,A错误,
B.碳碳间以单键相结合,碳原子剩余价键全部与氢原子结合的烃为饱和烃,可为链状烷烃,也可为环烷烃,但分子组成符合CnH2n+2的烃一定为链状烷烃,B正确;
C.在烷烃分子中与碳原子紧邻的四个原子构成四面体形,所以正戊烷分子中所有碳原子呈锯齿形,而非直线形,C错误;
D.新戊烷分子完全对称,分子中只有一种氢原子,故一氯代物只有一种,D错误;
故答案为B。
5.B
【详解】A.1H与2H是氢的不同核素,互为同位素,A正确;
B.H2O与H2O2是不同物质,B错误;
C.金刚石与石墨是碳的不同单质,互为同素异形体,C正确;
D.CH3CH2CH2CH3和的分子式均是C4H10,结构不同,互为同分异构体,D正确;
答案选B。
6.B
【详解】A.由物质M的结构简式可知,分子式为,选项A错误;
B.由物质M的结构简式可知其苯环上有7种等效氢,故苯环上的一氯代物有7种,选项B正确;
C.M含醇羟基,能使酸性KMnO4溶液褪色,选项C错误;
D.M含有羟基和羧基都可以与Na反应,生成1mol H2,标准状况下为22.4 L,选项D错误。
答案选B。
7.A
【详解】A.硬脂酸钠属于盐,A符合题意;
B.醋酸纤维是醋酸和纤维素形成的酯类,B不符合题意;
C.乙酸乙酯属于酯类,C不符合题意;
D.牛油属于酯类,D不符合题意;
故选A。
8.D
【详解】A.烃是只含碳氢两种元素的有机物,而该有机物含有O元素,不属于烃,故A错误;
B.乙烯和溴水发生加成反应,乙醇与溴水不反应,因此能用溴水鉴别己烯、乙醇,故B错误
C.乙烯分子内所有原子均可能在同一平面上,而乙烷中含有碳连四个价键,所有原子不能在同一平面上,故C错误;
D.是乙烯,可以是丁烯或环丁烷,因此分子式为与的有机物不一定互为同系物,故D正确。
综上所述,答案为D。
9.C
【详解】A.环己烯与螺[2.3]己烷的分子式相同、结构不同,二者互为同分异构体,故A正确;
B.b的苯环上含3种H原子,固定1个Cl在R的邻位,移动另一个Cl有4种,再固定1个Cl在R的间位,移动另一个Cl有2种,共6种,故B正确;
C.CH3CH2CH2CH2CH3、、中含H原子数分别为3、4、1,则R为C5H11时,a的结构有8种,故C错误;
D.R为C4H9时,为饱和烃基,b中只有苯环与氢气发生加成反应,则1molb加成生成C10H20至少需要3molH2,故D正确;
故选:C。
10.C
【分析】只能表示一种物质,说明不存在同分异构体。
【详解】A.可以是1—氯丙烷,也可以是2—氯丙烷,A错误;
B.可以是丙烯,也可以是环丙烷,B错误;
C.只能是丙烷,不存在同分异构体,C正确;
D.可以是乙醇,也可以是二甲醚,D错误,
答案选C。
11.C
【详解】加成反应指有机物分子中的不饱和键断裂,断键原子与其他原子或原子团相结合,生成新的化合物的反应。根据加成原理采取逆推法还原C≡C,烷烃分子中相邻碳原子上均带2个氢原子的碳原子间是对应炔存在C≡C的位置,则根据CH3CH2CH2CH(CH3)CH(C2H5)2可知左侧有两种三键,右侧乙基中有一种三键,共计是3种。答案选C。
12.B
【详解】A.“气”起了催熟作用,二氧化硫没有相应作用,故A不选;
B.乙烯的主要作用是促进果实成熟,故B选;
C.生长素具有两重性既能促进生长也能抑制生长,既能促进发芽也能抑制发芽,与催熟无关,故C不选;
D.甲烷不具有催熟作用,故D不选;
故选:B。
13.A
【详解】A.手性碳指的是碳原子连接的是四个不同的原子或原子团,二氢呋喃中不含有这样子的碳原子,即二氢呋喃不含手性碳,A错误,符合题意;
B.二氢呋喃、降冰片烯、可降解烯醇醚均含有不饱和碳碳双键,能使酸性高锰酸钾溶液褪色,B正确,不符合题意;
C.二氢呋喃和可降解烯醇醚中含有的官能团都为醚键和碳碳双键,所含的官能团完全相同,C正确,不符合题意;
D.该反应只有一种产物,表明该反应的原子利用率为100%,符合绿色化学要求,D正确,不符合题意;
故选A。
14.A
【详解】A.碳化硅(SiC)是含碳元素的无机化合物,不属于有机物,选项A符合题意;
B.甲烷(CH4)分子中含有C、H两种元素,属于烃,是有机化合物,选项B不符合题意;
C.醋酸(CH3COOH)分子中含有C、H、O三种元素,是烃的衍生物,是有机化合物,选项C不符合题意;
D.乙炔(C2H2)是含碳、氢两元素的化合物,是烃,属于有机物,选项D不符合题意;
答案选A。
15.B
【详解】乙烯、乙炔和甲苯都能被酸性高锰酸钾溶液氧化而使酸性高锰酸钾溶液褪色,乙烯和乙炔中均含有碳碳不饱和键,二者均能和溴发生加成反应而使溴的四氯化碳溶液褪色,故选:B。
16.(1)说明苯的这些同系物分子中的烷基受到了苯环的影响
(2)
【解析】(1)
烷烃稳定,不能与酸性的高锰酸钾溶液发生氧化还原反应,但是苯的一些同系物可以与酸性的高锰酸钾溶液发生氧化还原反应,说明苯的这些同系物分子中的烷基受到了苯环的影响,故答案为:说明苯的这些同系物分子中的烷基受到了苯环的影响;
(2)
根据题意,这些异构体的侧链烷基中,与苯环直接相连的碳原子必须有C-H,才能被氧化成苯甲酸,所以其他四种的结构简式分别为:、、、,故答案为:;;;。
17.(1) ① ② ⑤ ⑦ ④ ⑧
(2) 1 3 2
(3) (1,4-二甲苯) (1,3,5-三甲苯)
【详解】(1)同系物:结构相似,分子组成上相差一个或若干个CH2原子团的化合物,则环己烷(C6H12)与环辛烷(C8H16)均为环烷烃,分子组成上相差2个CH2,互为同系物;同分异构体:分子式相同,结构不同的化合物,则苯与棱晶烷(分子式均为C6H6),环辛四烯与立方烷(分子式均为C8H8)互为同分异构体;
(2)正四面体烷完全对称,只有一种氢原子,一氯代物只有1种,一氯代物中氢原子也只有1种,所以故二氯代物只有1种;金刚烷分子中有两种氢原子,一种是次甲基氢,一种亚甲基氢,所以其一氯代物有2种;立方烷分子中只有一种氢原子,其一氯代物有1种,而一氯代物有3种氢原子,分为在,则立方烷的二氯代物有3种;
(3)苯的同系物含有1个苯环,侧链为烷基,一氯代物只有两种的物质,说明只有2种氢原子,则与苯互为同系物且一氯代物只有两种的物质的结构简式为,名称为1,4-二甲苯;,名称为1,3,5-三甲苯。
【点睛】注意限制条件下同分异构体的书写,根据正四面体烷的结构写出分子式;正四面体烷二氯代物的种类取决于一氯代物中氢原子的种类;金刚烷的一氯代物取决于氢原子的种类;立方烷的二氯代物取决于一氯代物中氢原子的种类;苯的同系物含有1个苯环,侧链为烷基,一氯代物只有两种的物质,说明只有2种氢原子,然后根据苯的同系物命名方法命名。
18.(1) 碳碳双键 CH3CH=CH2+Br2 n CH3CH=CH2
(2)HC≡CCH2CH3、CH3 C≡CCH3、CH2=CHCH=CH2
(3)5
(4)
【详解】(1)分子式为C3H6的烃X能使溴的四氯化碳溶液褪色说明分子中含有碳碳双键,属于烯烃,则X的结构简式为CH3CH=CH2,官能团为碳碳双键;CH3CH=CH2与溴的四氯化碳溶液发生加成反应生成1,2—二溴乙烷,反应的化学方程式为CH3CH=CH2+Br2;催化剂作用下丙烯能发生加聚反应生成聚丙烯,反应的化学方程式为n CH3CH=CH2,故答案为:碳碳双键;CH3CH=CH2+Br2;n CH3CH=CH2;
(2)标准状况下89.6L二氧化碳的物质的量为=4mol,则标准状况下1mol某烃完全燃烧时,生成89.6L二氧化碳说明烃分子中含有4个碳原子,标准状况下4.48L氢气的物质的量为=0.2mol,0.1mol此烃能与标准状况下4.48L氢气加成说明烃分子中含有2个碳碳双键或1个三键,由两个碳碳双键连一起不稳定可知,符合条件的炔烃、二烯烃的结构简式为HC≡CCH2CH3、CH3 C≡CCH3、CH2=CHCH=CH2,故答案为:HC≡CCH2CH3、CH3 C≡CCH3、CH2=CHCH=CH2;
(3)标准状况下,5.6 L烃的物质的量为=0.25mol、28 L二氧化碳的物质的量为=1.25mol,22.5g水的物质的量为=1.25mol,则烃分子和分子中碳原子、氢原子的物质的量比为0.25mol:1.25mol:1.25mol×2=1:5:10,分子式为C5H10,该烃能使溴水褪色说明烃分子中含有碳碳双键,属于烯烃,不考虑顺反异构的戊烯共有5种,分别是1—戊烯、2—戊烯、2—甲基—1—丁烯、3—甲基—1—丁烯、2—甲基—2—丁烯,故答案为:5;
(4)分子式为C6H14的烃为烷烃,分子中含有四个甲基的烃为2,3—二甲基丁烷,结构简式为,故答案为:。
19.(1)物质的量之比2:3
(2)质量之比28:45
【详解】11.2L混合气体的物质的量为n===0.5mol,
乙烯含有双键,能与溴水发生加成反应,乙烯和乙烷的混合气体通入足量溴水中,充分反应后,溴水的质量增加了5.6g,即为乙烯的质量,
所以乙烯的物质的量为n===0.2mol,
则乙烷的物质的量为:0.5mol-0.2mol=0.3mol,质量为:0.3mol×30g/mol=9g,
所以,乙烯与乙烷的物质的量之比为0.2mol:0.3mol=2:3,
质量之比为5.6g:9g=28:45,
答:原气体混合物中乙烯与乙烷的物质的量之比为:2:3;质量比分别为28:45。
20.(1) 与液溴反应生成催化剂 液体轻微翻腾,有气体逸出,导管口有白雾产生,锥形瓶溶液中有浅黄色沉淀生成,烧瓶底部有褐色不溶于水的液体生成
(2)锥形瓶内有淡黄色沉淀生成
(3)未发生反应的溴和反应中的催化剂FeBr3,溶解在生成的溴苯中
【分析】铁与单质溴发生反应产生FeBr3,苯与液溴在FeBr3催化下发生取代反应产生溴苯和HBr,HBr通过导气管进入锥形瓶中,与溶液中的AgNO3发生取代反应产生AgBr浅黄色沉淀,垂直于烧瓶口的长的导气管作用是导气和冷凝,减少苯及液溴的挥发。
【详解】(1)铁屑与液溴在常温下反应生成溴化铁,溴化铁在苯与液溴发生取代反应生成溴苯时作催化剂,故铁屑在本反应中的作用是与液溴反应生成催化剂;实验开始后,苯与液溴发生取代反应产生溴苯和HBr,反应放出大量的热量,可以看到的现象是液体轻微翻腾,有气体逸出,导管口有白雾产生,HBr气体进入锥形瓶溶液中,与AgNO3溶液反应产生AgBr浅黄色沉淀,故还可以看到在锥形瓶中有浅黄色沉淀生成,反应产生的溴苯密度比苯大,未反应的溴溶解在溴苯中,故还可以看到烧瓶底部有褐色不溶于水的液体生成;
(2)若发生取代反应,反应产生溴苯和HBr,HBr气体不溶于有机物中,通过导气管进入锥形瓶中,与AgNO3溶液发生复分解反应产生AgBr浅黄色沉淀;若发生加成反应,挥发的液溴通过垂直于烧瓶口的长的导气管冷凝作用,回流到烧瓶中,因此锥形瓶中不会产生淡黄色沉淀。故能说明该反应是取代反应而不是加成反应的现象是锥形瓶内有淡黄色沉淀生成;
(3)纯净的溴苯是无色的,但反应物不能完全转化为生成物,未发生反应的溴溶解在生成的溴苯中,使本实验中得到的溴苯是褐色的。
21. Al4C3+6H2SO4=2Al2(SO4)3+3CH4↑ 2CH4+7CuO7Cu+CO2+CO+4H2O 干燥甲烷 不能 A CH4+Cl2CH3Cl+HCl ABC
【详解】(1)已知碳化铝(Al4C3)与水反应生成氢氧化铝和甲烷,用假设Al4C3 的系数为1的方法配平可得:Al4C3 + 6 H2SO4 =2Al2(SO4)3 + 3CH4↑;
(2甲方案的目的是探究甲烷与氧化剂反应,实验测得消耗甲烷与氧化铜物质的量之比2∶7可知,设甲烷的系数为2,先后依据铜、氢、氧、碳原子个数守恒可得:硬质试管里可能发生的化学方程式为2 CH4 + 7 CuO7 Cu + CO2 + CO + 4 H2O;
(3)浓硫酸具有吸水性,且不能与甲烷反应,因此实验甲中浓硫酸起干燥甲烷的作用;集气瓶是尾气处理装置,其中收集到的不溶于水的气体主要是CO,CO气体有毒,不能直接排入空气;
(4)A.酸性高锰酸钾溶液不褪色,结论是通常条件下,甲烷不能与强氧化剂反应,A正确;
B.硬质试管里黑色粉末变红色,说明氧化铜发生了还原反应,因为铜元素由+2价降低到0价,B错误;
C.硬质试管里黑色粉末变红色,推断氧化铜与甲烷反应不仅仅生成水和二氧化碳,还生成了具有还原性的CO,C错误;
D.甲烷不能与溴水反应,推知甲烷不能与卤素单质的水溶液反应,但是甲烷能与纯净的卤素单质在光照或高温下发生取代反应,D错误;
答案选A;
(5)乙方案中烧杯里放入足量的水,打开弹簧夹a、b,一段时间后,观察到有水倒吸到I瓶中,但水并不能充满I瓶,说明甲烷与氯气在光照下生成了易溶于水的氯化氢气体,因此推断发生了取代反应,如CH4 + Cl2 CH3Cl + HCl;
A.I瓶中气体颜色变浅,因为黄绿色的氯气逐渐消耗完全,A正确;
B.I瓶中出现白雾,因为生成的氯化氢气体容易与水蒸气结合为盐酸小液滴,B正确;
C.I瓶瓶内壁出现油状物质,因为甲烷与氯气发生取代反应,生成的一氯甲烷是气体,二氯甲烷、三氯甲烷、四氯化碳是油状液体,C正确;
D.II瓶中与I瓶现象不相同,因为I有光照条件,能发生取代反应,II缺少光照条件,不能发生取代反应,D错误;
答案选ABC。
【点晴】控制变量思想方法,探究实验异常现象成为近几年实验探究命题的热点,突出对实验能力的考查。该题为实验探究题,装置图、流程图很简单,但探究过程较复杂,准确全面获取信息、通过控制变量思想进行逻辑分析是解题的关键,凭感觉做题,不容易准确获取题中信息。该类试题的解题策略为:(1)确定变量:解答这类题目时首先要认真审题,理清影响实验探究结果的因素有哪些。(2)定多变: 在探究时,应该先确定其他的因素不变,只变化一种因素,看这种因素与探究的问题存在怎样的关系;这样确定一种以后,再确定另一种,通过分析每种因素与所探究问题之间的关系,得出所有影响因素与所探究问题之间的关系。(3)数据有效;解答时注意选择数据(或设置实验)要有效,且变量统一,否则无法做出正确判断。
