4.2蛋白质和酶 课件(共32张PPT)高二化学人教版(2019)选择性必修3
文档属性
| 名称 | 4.2蛋白质和酶 课件(共32张PPT)高二化学人教版(2019)选择性必修3 |

|
|
| 格式 | pptx | ||
| 文件大小 | 2.8MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-06-12 00:00:00 | ||
图片预览








文档简介
(共32张PPT)
第二节 蛋白质和酶
第四章 生物大分子
我们身边的蛋白质都有哪些?
蛋白质是动植物组织中的主要物质,是生命活动的物质基础:
1、酶的催化功能;
2、激素的代谢调节功能;
3、血红蛋白和脂蛋白的运输功能;
4、肌纤维蛋白的运到功能;
5、机体的免疫功能和胶原蛋白的支架功能。
我们身边的蛋白质都有哪些?
蛋白质的基石——氨基酸
蛋白质种类为何如此丰富 (从结构方面)
几乎一切生命活动过程都与蛋白质有关,没有蛋白质就没有生命
氨基酸就是构成蛋白质这个“万里长城”的基石
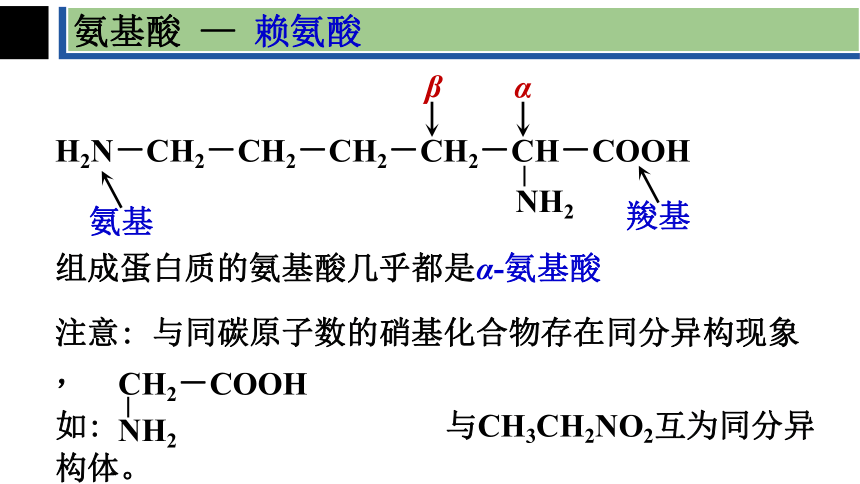
氨基酸 — 赖氨酸
H2N-CH2-CH2-CH2-CH2-CH-COOH
NH2
氨基
羧基
α
β
组成蛋白质的氨基酸几乎都是α-氨基酸
注意: 与同碳原子数的硝基化合物存在同分异构现象,
如: 与CH3CH2NO2互为同分异构体。
CH2-COOH
NH2
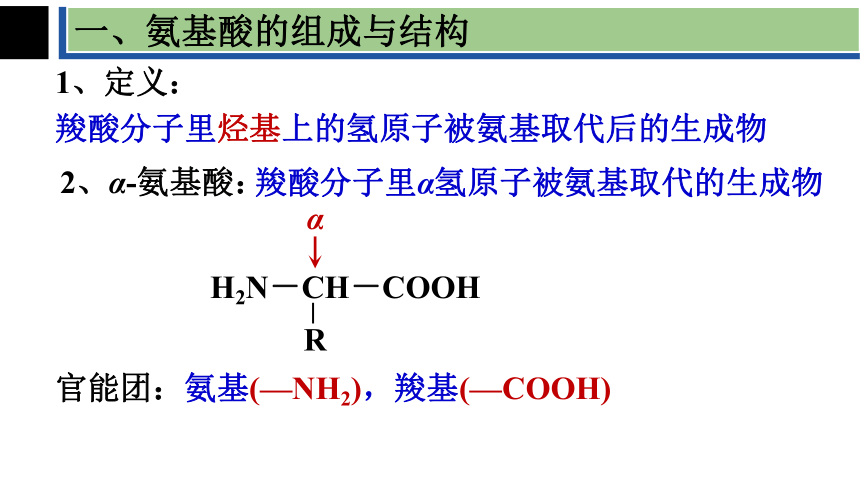
一、氨基酸的组成与结构
1、定义:
羧酸分子里烃基上的氢原子被氨基取代后的生成物
2、α-氨基酸:
羧酸分子里α氢原子被氨基取代的生成物
官能团:氨基(—NH2),羧基(—COOH)
α
H2N-CH-COOH
R
一、氨基酸的组成与结构
2、几种常见的氨基酸:
(1)甘氨酸(α-氨基乙酸)
(2)丙氨酸(α-氨基丙酸)
(3)谷氨酸(α-氨基戊二酸)
(4)苯丙氨酸(α-氨基-β-苯基丙酸)
CH2—COOH
NH2
CH3—CH—COOH
NH2
HOOC—(CH2)2—CH—COOH
NH2
—CH2—CH—COOH
NH2
二、氨基酸的性质 — 物理性质
1、氨基酸的物理性质
天然氨基酸是无色晶体,熔点较高,在200~300℃时熔化分解,一般能溶于水而难溶于乙醇、乙醚。
H2N—CH—COOH
R
氨基典型反应
羧基典型反应
想一想:从氨基酸的结构分析,氨基酸可能具有怎样的化学性质?
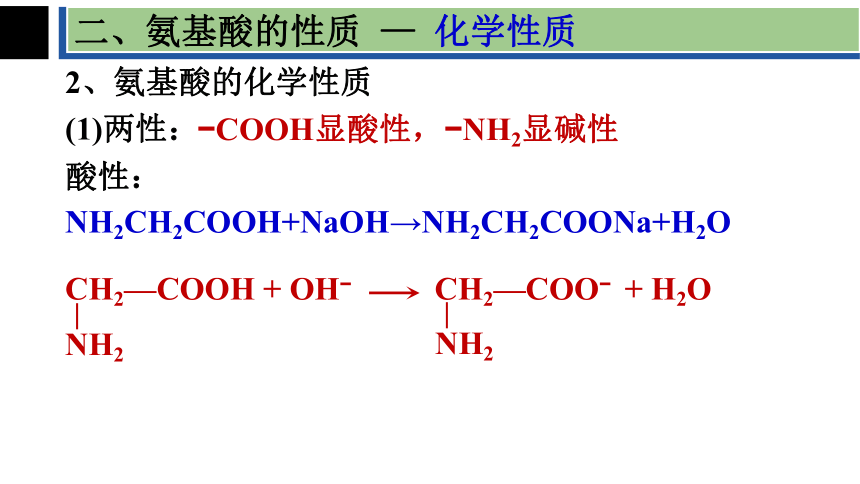
二、氨基酸的性质 — 化学性质
2、氨基酸的化学性质
(1)两性:
COOH显酸性, NH2显碱性
酸性:
NH2CH2COOH+NaOH→NH2CH2COONa+H2O
CH2—COOH + OH
NH2
CH2—COO + H2O
NH2
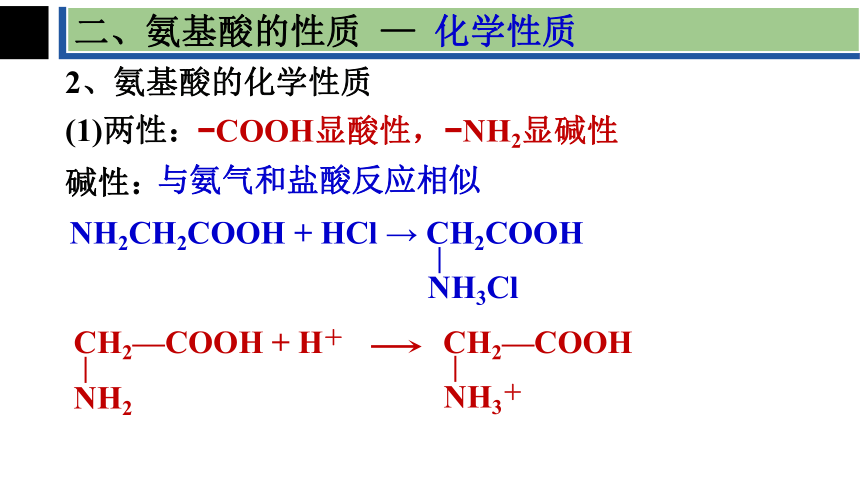
二、氨基酸的性质 — 化学性质
2、氨基酸的化学性质
(1)两性:
COOH显酸性, NH2显碱性
碱性:
CH2—COOH + H+
NH2
CH2—COOH
NH3+
NH2CH2COOH + HCl → CH2COOH
NH3Cl
与氨气和盐酸反应相似
拓展:既能与酸又能与碱反应的物质
①单质,如:Al等
②两性氧化物,如:Al2O3等
③两性氢氧化物,如:Al(OH)3等
④弱酸的铵盐,如:(NH4)2CO3、NH4HCO3等
⑤多元弱酸的酸式盐;如:NH4HCO3、NaHCO3等
⑥具有双官能团的某些有机物,如:氨基酸、蛋白质等
常见的既能与酸又能与碱反应的物质
二、氨基酸的性质 — 化学性质
2、氨基酸的化学性质
(2)成肽反应
一个氨基酸分子中的羧基可以跟另一个氨基酸分子中的氨基反应,按羧基脱羟基、氨基脱氢的反应原理,脱去一个水分子而形成酰胺基( ),即肽键,此反应称为成肽反应。
—C—N—
O H
二、氨基酸的性质 — 化学性质
(2)成肽反应
O
H
H—N—CH2—C—OH +
O
H
H—N—CH2—C—OH
酶或酸或碱
O
H
H—N—CH2—C—N—CH2—C—OH
O
H
+H2O
肽键
(取代反应)
两个氨基酸分子消去水分子而形成二肽多个氨基酸分子消去水分子而形成多肽
二、氨基酸的性质 — 化学性质
练1.由甘氨酸和丙氨酸形成的链状二肽可能有几种?写出相应的产物。
CH2—COOH
NH2
CH3—CH—COOH
NH2
4种
三、蛋白质的结构及在人体内的作用 — 结构
相对分子质量大于1万,具有一定空间结构的多肽叫蛋白质。蛋白质分子中含有C、O、H、N、S等元素。
三、蛋白质的结构及在人体内的作用 — 结构
一级结构:
蛋白质分子中各种氨基酸的连接方式和排列顺序叫蛋白质的一级结构。
二级结构:
多肽链卷曲盘旋和折叠的空间结构称为蛋白质的二级结构。
三级结构:
蛋白质分子在二级结构的基础上进一步盘曲折叠形成的三维结构。
具有三级结构的多肽链叫亚基
三、蛋白质的结构及在人体内的作用 — 结构
四级结构:
蛋白质分子中亚基的立体排布、亚基间的相互作用与布局称为蛋白质的四级结构。
三、蛋白质的结构及在人体内的作用 — 作用
蛋白质在人体内的作用
(1)对生物反应起催化作用的酶
(2)运输作用的血红蛋白
(3)保护作用的毛发、皮肤、甲、壳等
(4)抵抗病毒、细菌作用的高度特异性蛋白:抗体
(5)构成动物大部分结构的纤维物质软骨、肌肉
四、蛋白质的性质
1、具有两性:
酸性( COOH)和碱性( NH2)
2、水解:
蛋白质
酸、碱或酶作用
多种氨基酸
原理:
HO
H
O
H—N—CH2—C—
O
H
—N—CH2—C—OH
H
注意:不同的蛋白质水解最终生成各种氨基酸,天然蛋白质水解均生成α-氨基酸
四、蛋白质的性质 — 演示实验一
演示实验一:蛋白质的盐析
鸡蛋白溶液
浓无机盐
蛋白质凝聚
水
蛋白质重新溶解
四、蛋白质的性质 — 演示实验一
演示实验一:蛋白质的盐析
实验结论:
1、浓的无机盐溶液[如Na2SO4、(NH4) 2SO4等],可使蛋白质的溶解度减小,而从溶液中析出—盐析。
2、盐析是一个可逆的过程,故不影响蛋白质的性质
应用:利用多次盐析,可以分离、提纯蛋白质
四、蛋白质的性质 — 演示实验二
演示实验二:蛋白质的变性
鸡蛋白溶液
加热或加
入醋酸铅
蛋白质凝结
水
蛋白质不再溶解
四、蛋白质的性质 — 演示实验二
演示实验二:蛋白质的变性
实验结论:
在热、酸、碱、重金属盐、甲醛、酒精、紫外线等作用下,蛋白质失去原有的可溶性而凝结,同时丧失了生理活性。这种过程是不可逆的。
应用:消毒杀菌
蛋白质的盐析与变性对比
盐析 变性
变化条件
变化性质
变化过程
用途
浓的无机盐溶液
受热、紫外线、酸、碱、
重金属盐和某些有机物
物理变化
(溶解度降低)
化学变化
(蛋白质性质改变)
可逆
不可逆
分离提纯
杀菌消毒
练1.欲将蛋白质从水中析出而又不改变它的性质
应加入( )
A. 甲醛溶液 B. 饱和Na2SO4溶液
C. CuSO4溶液 D. 浓硫酸
B
四、蛋白质的性质
想一想、议一议
1、为什么医院里用高温蒸煮、照射紫外线、喷洒苯酚溶液、在伤口处涂抹酒精溶液等方法来消毒杀菌?
2、钡盐也属于重金属盐,医院在做胃透视时要服用“钡餐”BaSO4为何不会中毒?能否改服BaCO3?
四、蛋白质的性质 — 演示实验三
演示实验三:蛋白质的颜色反应
鸡蛋白溶液
浓硝酸
变成黄色
四、蛋白质的性质 — 演示实验三
演示实验三:蛋白质的颜色反应
实验结论:
蛋白质可以跟许多试剂发生特殊的颜色反应。如某些蛋白质跟浓硝酸作用,加热会产生黄色沉淀,也称“黄蛋白反应”。
应用:用于鉴别蛋白质的存在
3
2
四、蛋白质的性质 — 演示实验四
演示实验四:蛋白质的灼烧实验
1
应用:区别合成纤维与蛋白质
练2.为鉴别某白色纺织品的成分是蚕丝还是“人造丝”,可选用的方法是( )
A.滴加浓硝酸 B.滴加浓硫酸
C.滴加酒精 D.灼烧
A D
四、蛋白质的性质
五、酶 — 具有催化作用的蛋白质
1、酶的概念
酶是一类由活细胞产生的对生物体内的化学反应具有催化作用的蛋白质。
过氧化氢酶
五、酶 — 具有催化作用的蛋白质
2、酶的催化特点
条件温和、不需加热:在接近体温和接近中性的条件下
具有高度专一性:如蛋白酶只能催化蛋白质的水解,如同一把药匙开一把锁一样
具有高效催化作用:比普通催化剂高107~1013倍
五、酶 — 具有催化作用的蛋白质
3、酶的应用
(4)酶还可用于疾病的诊断。
(1)淀粉酶应用于食品、发酵、纺织、制药等工业;
(2)蛋白酶应用于医药、制革等工业;
(3)脂肪酶应用于脂肪水解、羊毛脱脂等;
蛋白酶
脂肪酶
第二节 蛋白质和酶
第四章 生物大分子
我们身边的蛋白质都有哪些?
蛋白质是动植物组织中的主要物质,是生命活动的物质基础:
1、酶的催化功能;
2、激素的代谢调节功能;
3、血红蛋白和脂蛋白的运输功能;
4、肌纤维蛋白的运到功能;
5、机体的免疫功能和胶原蛋白的支架功能。
我们身边的蛋白质都有哪些?
蛋白质的基石——氨基酸
蛋白质种类为何如此丰富 (从结构方面)
几乎一切生命活动过程都与蛋白质有关,没有蛋白质就没有生命
氨基酸就是构成蛋白质这个“万里长城”的基石
氨基酸 — 赖氨酸
H2N-CH2-CH2-CH2-CH2-CH-COOH
NH2
氨基
羧基
α
β
组成蛋白质的氨基酸几乎都是α-氨基酸
注意: 与同碳原子数的硝基化合物存在同分异构现象,
如: 与CH3CH2NO2互为同分异构体。
CH2-COOH
NH2
一、氨基酸的组成与结构
1、定义:
羧酸分子里烃基上的氢原子被氨基取代后的生成物
2、α-氨基酸:
羧酸分子里α氢原子被氨基取代的生成物
官能团:氨基(—NH2),羧基(—COOH)
α
H2N-CH-COOH
R
一、氨基酸的组成与结构
2、几种常见的氨基酸:
(1)甘氨酸(α-氨基乙酸)
(2)丙氨酸(α-氨基丙酸)
(3)谷氨酸(α-氨基戊二酸)
(4)苯丙氨酸(α-氨基-β-苯基丙酸)
CH2—COOH
NH2
CH3—CH—COOH
NH2
HOOC—(CH2)2—CH—COOH
NH2
—CH2—CH—COOH
NH2
二、氨基酸的性质 — 物理性质
1、氨基酸的物理性质
天然氨基酸是无色晶体,熔点较高,在200~300℃时熔化分解,一般能溶于水而难溶于乙醇、乙醚。
H2N—CH—COOH
R
氨基典型反应
羧基典型反应
想一想:从氨基酸的结构分析,氨基酸可能具有怎样的化学性质?
二、氨基酸的性质 — 化学性质
2、氨基酸的化学性质
(1)两性:
COOH显酸性, NH2显碱性
酸性:
NH2CH2COOH+NaOH→NH2CH2COONa+H2O
CH2—COOH + OH
NH2
CH2—COO + H2O
NH2
二、氨基酸的性质 — 化学性质
2、氨基酸的化学性质
(1)两性:
COOH显酸性, NH2显碱性
碱性:
CH2—COOH + H+
NH2
CH2—COOH
NH3+
NH2CH2COOH + HCl → CH2COOH
NH3Cl
与氨气和盐酸反应相似
拓展:既能与酸又能与碱反应的物质
①单质,如:Al等
②两性氧化物,如:Al2O3等
③两性氢氧化物,如:Al(OH)3等
④弱酸的铵盐,如:(NH4)2CO3、NH4HCO3等
⑤多元弱酸的酸式盐;如:NH4HCO3、NaHCO3等
⑥具有双官能团的某些有机物,如:氨基酸、蛋白质等
常见的既能与酸又能与碱反应的物质
二、氨基酸的性质 — 化学性质
2、氨基酸的化学性质
(2)成肽反应
一个氨基酸分子中的羧基可以跟另一个氨基酸分子中的氨基反应,按羧基脱羟基、氨基脱氢的反应原理,脱去一个水分子而形成酰胺基( ),即肽键,此反应称为成肽反应。
—C—N—
O H
二、氨基酸的性质 — 化学性质
(2)成肽反应
O
H
H—N—CH2—C—OH +
O
H
H—N—CH2—C—OH
酶或酸或碱
O
H
H—N—CH2—C—N—CH2—C—OH
O
H
+H2O
肽键
(取代反应)
两个氨基酸分子消去水分子而形成二肽多个氨基酸分子消去水分子而形成多肽
二、氨基酸的性质 — 化学性质
练1.由甘氨酸和丙氨酸形成的链状二肽可能有几种?写出相应的产物。
CH2—COOH
NH2
CH3—CH—COOH
NH2
4种
三、蛋白质的结构及在人体内的作用 — 结构
相对分子质量大于1万,具有一定空间结构的多肽叫蛋白质。蛋白质分子中含有C、O、H、N、S等元素。
三、蛋白质的结构及在人体内的作用 — 结构
一级结构:
蛋白质分子中各种氨基酸的连接方式和排列顺序叫蛋白质的一级结构。
二级结构:
多肽链卷曲盘旋和折叠的空间结构称为蛋白质的二级结构。
三级结构:
蛋白质分子在二级结构的基础上进一步盘曲折叠形成的三维结构。
具有三级结构的多肽链叫亚基
三、蛋白质的结构及在人体内的作用 — 结构
四级结构:
蛋白质分子中亚基的立体排布、亚基间的相互作用与布局称为蛋白质的四级结构。
三、蛋白质的结构及在人体内的作用 — 作用
蛋白质在人体内的作用
(1)对生物反应起催化作用的酶
(2)运输作用的血红蛋白
(3)保护作用的毛发、皮肤、甲、壳等
(4)抵抗病毒、细菌作用的高度特异性蛋白:抗体
(5)构成动物大部分结构的纤维物质软骨、肌肉
四、蛋白质的性质
1、具有两性:
酸性( COOH)和碱性( NH2)
2、水解:
蛋白质
酸、碱或酶作用
多种氨基酸
原理:
HO
H
O
H—N—CH2—C—
O
H
—N—CH2—C—OH
H
注意:不同的蛋白质水解最终生成各种氨基酸,天然蛋白质水解均生成α-氨基酸
四、蛋白质的性质 — 演示实验一
演示实验一:蛋白质的盐析
鸡蛋白溶液
浓无机盐
蛋白质凝聚
水
蛋白质重新溶解
四、蛋白质的性质 — 演示实验一
演示实验一:蛋白质的盐析
实验结论:
1、浓的无机盐溶液[如Na2SO4、(NH4) 2SO4等],可使蛋白质的溶解度减小,而从溶液中析出—盐析。
2、盐析是一个可逆的过程,故不影响蛋白质的性质
应用:利用多次盐析,可以分离、提纯蛋白质
四、蛋白质的性质 — 演示实验二
演示实验二:蛋白质的变性
鸡蛋白溶液
加热或加
入醋酸铅
蛋白质凝结
水
蛋白质不再溶解
四、蛋白质的性质 — 演示实验二
演示实验二:蛋白质的变性
实验结论:
在热、酸、碱、重金属盐、甲醛、酒精、紫外线等作用下,蛋白质失去原有的可溶性而凝结,同时丧失了生理活性。这种过程是不可逆的。
应用:消毒杀菌
蛋白质的盐析与变性对比
盐析 变性
变化条件
变化性质
变化过程
用途
浓的无机盐溶液
受热、紫外线、酸、碱、
重金属盐和某些有机物
物理变化
(溶解度降低)
化学变化
(蛋白质性质改变)
可逆
不可逆
分离提纯
杀菌消毒
练1.欲将蛋白质从水中析出而又不改变它的性质
应加入( )
A. 甲醛溶液 B. 饱和Na2SO4溶液
C. CuSO4溶液 D. 浓硫酸
B
四、蛋白质的性质
想一想、议一议
1、为什么医院里用高温蒸煮、照射紫外线、喷洒苯酚溶液、在伤口处涂抹酒精溶液等方法来消毒杀菌?
2、钡盐也属于重金属盐,医院在做胃透视时要服用“钡餐”BaSO4为何不会中毒?能否改服BaCO3?
四、蛋白质的性质 — 演示实验三
演示实验三:蛋白质的颜色反应
鸡蛋白溶液
浓硝酸
变成黄色
四、蛋白质的性质 — 演示实验三
演示实验三:蛋白质的颜色反应
实验结论:
蛋白质可以跟许多试剂发生特殊的颜色反应。如某些蛋白质跟浓硝酸作用,加热会产生黄色沉淀,也称“黄蛋白反应”。
应用:用于鉴别蛋白质的存在
3
2
四、蛋白质的性质 — 演示实验四
演示实验四:蛋白质的灼烧实验
1
应用:区别合成纤维与蛋白质
练2.为鉴别某白色纺织品的成分是蚕丝还是“人造丝”,可选用的方法是( )
A.滴加浓硝酸 B.滴加浓硫酸
C.滴加酒精 D.灼烧
A D
四、蛋白质的性质
五、酶 — 具有催化作用的蛋白质
1、酶的概念
酶是一类由活细胞产生的对生物体内的化学反应具有催化作用的蛋白质。
过氧化氢酶
五、酶 — 具有催化作用的蛋白质
2、酶的催化特点
条件温和、不需加热:在接近体温和接近中性的条件下
具有高度专一性:如蛋白酶只能催化蛋白质的水解,如同一把药匙开一把锁一样
具有高效催化作用:比普通催化剂高107~1013倍
五、酶 — 具有催化作用的蛋白质
3、酶的应用
(4)酶还可用于疾病的诊断。
(1)淀粉酶应用于食品、发酵、纺织、制药等工业;
(2)蛋白酶应用于医药、制革等工业;
(3)脂肪酶应用于脂肪水解、羊毛脱脂等;
蛋白酶
脂肪酶
