化学人教版(2019)选择性必修3 4.2蛋白质 课件(共28张ppt)
文档属性
| 名称 | 化学人教版(2019)选择性必修3 4.2蛋白质 课件(共28张ppt) |  | |
| 格式 | pptx | ||
| 文件大小 | 113.9MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-06-12 22:38:27 | ||
图片预览





文档简介
(共28张PPT)
网
科
第二节 蛋白质
第四章 生物大分子
4.2 蛋白质
学习目标
1.通过结构分析认识氨基酸的组成、结构特点和主要化学性质,能判断氨基酸的缩合产物。
2.了解蛋白质的组成、结构和性质,知道氨基酸、多肽和蛋白质之间的关系。学会用蛋白质的性质解释生活中的相关现象。
3.了解酶催化反应的特点。
新课导入
羧酸分子烃基上的氢原子被氨基(-NH2)取代的化合物(属于取代羧酸)
1.概念:
例如:
烃基上一个H被-NH2取代
α-氨基丁酸
CH3CH2CH2COOH
CH3CH2CH COOH
NH2
γ β α
自然界中存在的氨基酸
组成生物体内
人体内不能合成
只有21种
8种氨基酸
几百种
必需氨基酸
→为了人体的健康,应注意合理膳食、科学营养,保证人体必需氨基酸的摄取。
2-氨基丁酸
食物供给
天然的蛋白质都是由α-氨基酸构成!
(氨基和羧基连在同一C上)
一、氨基酸
俗名 结构简式 系统命名
甘氨酸 H2N—CH2COOH
丙氨酸
谷氨酸
苯丙氨酸
半胱氨酸
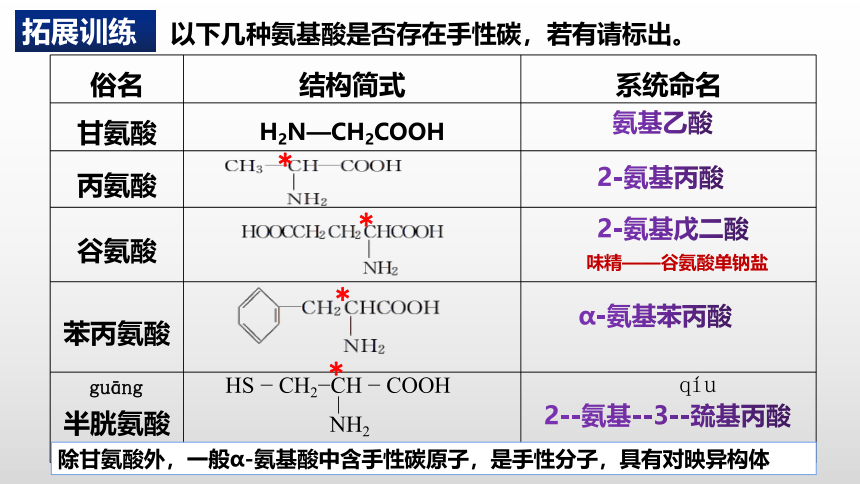
以下几种氨基酸是否存在手性碳,若有请标出。
氨基乙酸
2-氨基丙酸
2-氨基戊二酸
α-氨基苯丙酸
2 -氨基 -3 -巯基丙酸
*
HS CH2 CH COOH
NH2
*
*
*
除甘氨酸外,一般α 氨基酸中含手性碳原子,是手性分子,具有对映异构体
味精——谷氨酸单钠盐
qíu
guāng
拓展训练
R CH COOH
NH2
酯化
酸性
羧基
氨基
碱性
还原性
CH2COOH+HCl CH2COOH
NH2
NH3Cl
R-CH-COOH + NaOH
NH2
R-CH-COONa + H2O
NH2
(1) 两性:能与酸、碱反应
(参照:NH3 + HCl = NH4Cl)
2.物理性质
天然氨基酸均为无色晶体,熔点较高,在200~3000C时熔化分解,
一般能溶于水而难溶于乙醇、乙醚等有机溶剂
3.化学性质
盐酸(氯化)氨基羧酸
氨基羧酸钠
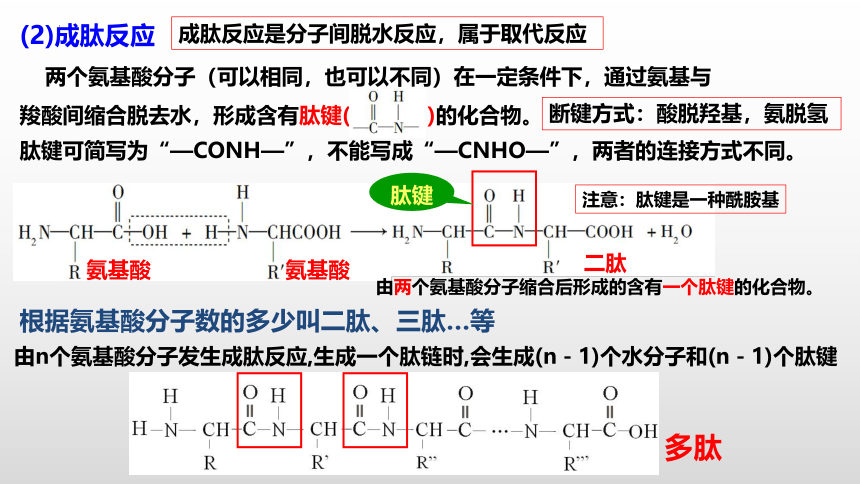
(2)成肽反应
两个氨基酸分子(可以相同,也可以不同)在一定条件下,通过氨基与 羧酸间缩合脱去水,形成含有肽键( )的化合物。
氨基酸
氨基酸
成肽反应是分子间脱水反应,属于取代反应
断键方式:酸脱羟基,氨脱氢
注意:肽键是一种酰胺基
肽键
多肽
根据氨基酸分子数的多少叫二肽、三肽…等
二肽
由两个氨基酸分子缩合后形成的含有一个肽键的化合物。
由n个氨基酸分子发生成肽反应,生成一个肽链时,会生成(n-1)个水分子和(n-1)个肽键
肽键可简写为“—CONH—”,不能写成“—CNHO—”,两者的连接方式不同。
两分子氨基酸
缩合
二肽
三肽
缩合
+氨基酸
缩合
+氨基酸
四肽
缩合
+氨基酸
多肽
· · · · · ·
呈链状
肽链
又称
相互结合形成
盘曲、折叠
蛋白质
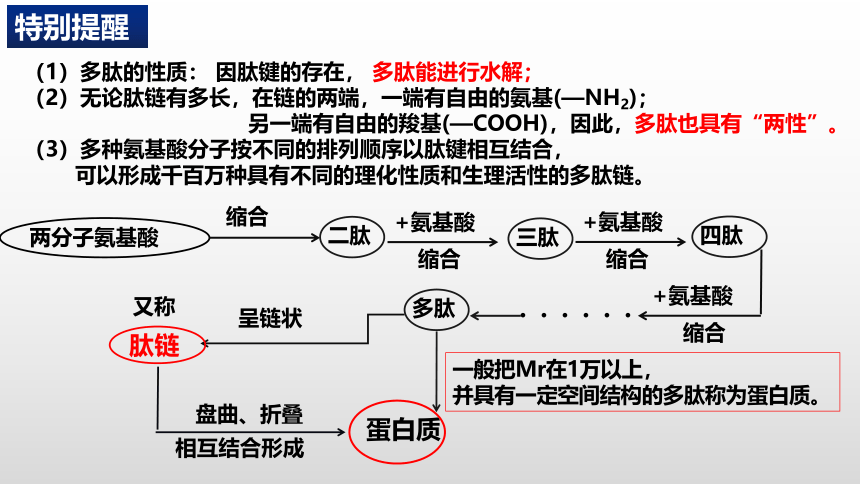
(1)多肽的性质: 因肽键的存在, 多肽能进行水解;
(2)无论肽链有多长,在链的两端,一端有自由的氨基(—NH2);
另一端有自由的羧基(—COOH),因此,多肽也具有“两性”。
(3)多种氨基酸分子按不同的排列顺序以肽键相互结合,
可以形成千百万种具有不同的理化性质和生理活性的多肽链。
一般把Mr在1万以上,
并具有一定空间结构的多肽称为蛋白质。
特别提醒
R O R′ O
-HN-CH-C-NH-CH-C-
=
=
[ ]n
R O R′ O
H-HN-CH-C-OH + H-NH-CH-C-OH
=
=
H
OH
多肽
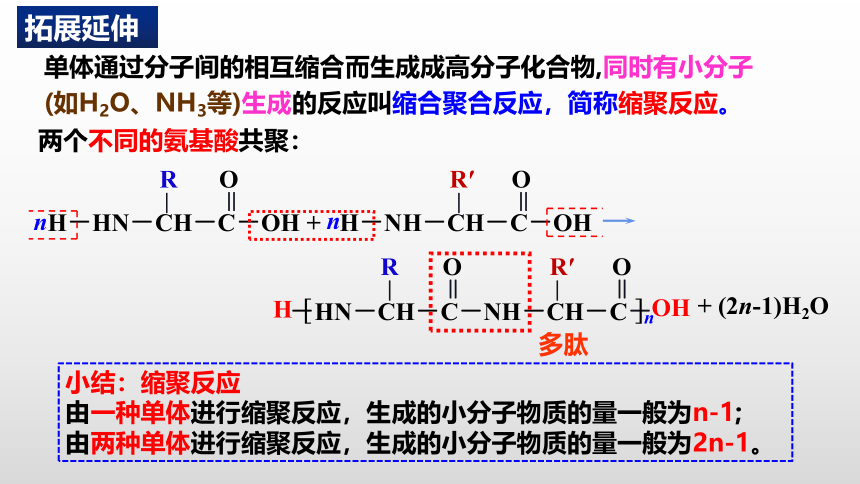
两个不同的氨基酸共聚:
单体通过分子间的相互缩合而生成成高分子化合物,同时有小分子(如H2O、NH3等)生成的反应叫缩合聚合反应,简称缩聚反应。
小结:缩聚反应
由一种单体进行缩聚反应,生成的小分子物质的量一般为n-1;
由两种单体进行缩聚反应,生成的小分子物质的量一般为2n-1。
n
n
+ (2n-1)H2O
拓展延伸
2.氨基酸的缩合反应也可能成环,试写出下列反应方程式
①NH2-CH2-COOH的分子间脱水成环
②NH2-CH2-CH2-CH2-CH2-COOH的分子内脱水成环
O=C
C=O
NH—CH2
CH2—NH
1.由甘氨酸和丙氨酸形成的链状二肽可能有几种?
4种
催化剂
2H2O
H2C-CO-OH
NH-H
HO-OC-CH2
H-HN
+
+
+
H2O
催化剂
CH2 —CH2—CO—OH
CH2—CH2—NH—H
H2C
C=O
CH2—CH2
CH2—NH
对点训练
3. 书写下列氨基酸的缩聚反应
苯丙氨酸与甘氨酸发生成肽反应生成多肽
①
②
R-CH-COOH
NH2
对点训练
4. 已知-NH2连在苯环上显碱性, 连在苯环上显中性,现有有机物C7H7O2N,分子结构中有一个苯环和两个取代基,且两取代基在苯环上处于相对位置,请写出符合下列要求的结构简式。
(1)该有机物只具有酸性:
(2)该有机物只具有碱性:
(3)该有机物具有两性:
(4)该有机物既无酸性又无碱性:
HO-
-C-NH2
O
O
-C-NH2
H2N-
-C-OH
O
H2N-
-O-C-H
O
O2N-
-CH3
同分异构:氨基酸、氨基酯、硝基化合物三者异构
对点训练
胶原蛋白
鸡蛋清
银耳
桃胶
鸡蛋清和胶原蛋白溶液中含有蛋白质,而银耳和桃胶中不含蛋白质。其实银耳和桃胶煮出来的东西看上去粘稠有弹性,像是一种胶,但并不是胶原蛋白,从化学的角度来看,他们是我们前面学过的多糖。
化学与生活
注意:
(2)组成: 蛋白质中主要含有C、H、O、N、S等元素,有些蛋白质还含有
P、Fe、Zn、Cu等元素。属于天然有机高分子。其溶液具有胶体的某些性质。
(1)定义:蛋白质是由多种氨基酸通过肽键等相互连接形成的一类生物大分子。
1.蛋白质的定义与组成
(3)存在:
1839年,荷兰化学家穆尔德提出蛋白质(protein)这个名词,源于希腊文“proteios”,意为原始的,引申为第一位的,最重要的意思。
光亮的通路
动物的肌肉、皮肤、血液、蚕丝、 毛、发、蹄、角;
酶、激素、血红蛋白、细菌、病毒、抗体、阿胶含有蛋白质;
许多植物的种子(大豆、花生、小麦、稻谷)里也富含蛋白质。
新冠病毒
是一般细胞中含量最多的有机分子,约占细胞干重的一半以上。
几乎一切生命活动过程都与蛋白质有关,没有蛋白质就没有生命。
二、蛋白质
一级结构
二级结构
三级结构
四级结构
2.蛋白质的结构
结构多样性
功能多样性
脱水缩合
空间结构肽链
三聚氰胺含氮量为66.7%,是牛奶的151倍,是奶粉的23倍。
每100g牛奶中添加
0.1克三聚氰胺,
就能提高0.4%蛋白质!
蛋白质含量的测定:由于生物组织中绝大部分氮元素来自蛋白质,而且各种来源不同的蛋白质的含氮量都比较接近,平均为16%。因此生物样品中的1 g氮元素大致相当于6.25 g蛋白质,由此可以通过测定样品中氮元素的质量分数计算出其中蛋白质的含量。
资料卡片
【思考】蛋白质结构中一定含有哪些官能团?
3.蛋白质的化学性质
(1)蛋白质的两性:
氨基
羧基
肽键
肽键
蛋白质的多肽是由多个氨基酸缩合形成的,
在多肽链的两端必然存在着自由的氨基与羧基,
同时侧链中也往往存在酸性或碱性基团。
蛋白质与氨基酸类似,也是两性分子,
既能与酸反应,又能与碱反应。
氨基
羧基
肽键
(2)水解反应
蛋白质 多肽 氨基酸
酶或酸或碱
水解
酶或酸或碱
水解
HO
H
能发生水解的有机物
酯、油脂、
归纳总结:
蛋白质等
蔗糖、麦芽糖、淀粉、纤维素、
卤代烃、
天然蛋白质→ 多肽 →二肽 →α-氨基酸(最终产物)
食物中的蛋白质在人体内各种蛋白酶的作用下水解成氨基酸,
氨基酸被肠壁吸收进入血液,再在体内重新合成人体所需要的
蛋白质。
(3)盐析
注意:
①盐析是一个可逆的过程,属于物理变化过程。不影响蛋白质的性质。 ②应用:利用多次盐析的方法分离、提纯蛋白质。
可溶性盐
硫酸铵、
硫酸钠、
氯化钠等
蛋白质溶液
加水
盐溶液少量:
促进蛋白质的溶解
盐溶液达到一定浓度:
使蛋白质的溶解度降低而从溶液中析出
加热
白色沉淀
加水
沉淀不溶解
概 念
影响因素 物理
化学
特 点 变性会使蛋白质的结构发生变化,使其失去原有的__________,
在水中不能重新溶解,是 过程
应 用
在某些物理或化学因素的影响下,蛋白质的性质和生理功能发生改变的现象
加热、加压、搅拌、振荡、紫外线和放射线、超声波等
强酸、强碱、重金属盐(Pb2+、Cu2+、Ba2+、Ag+、Hg2+等)、乙醇、甲醛、丙酮等
不可逆
生理活性
杀菌、消毒、防中毒
(4)蛋白质的变性
思考:关于怎么吃鸡蛋,网上众说纷纭,有些主张生吃,有些觉得熟的更好,大家更倾向于哪一种呢?
科普:鸡蛋加热后,蛋白质的空间结构被破坏,原有的生物活性会丧失,溶解度降低,黏度增大,肽链松散,更易被水解消化。所以更多的人会选择将鸡蛋煮熟了再吃,这是有一定科学依据的(这样更利于消化吸收)。
鸡蛋清溶液
在日常生活中有时需要利用蛋白质变性:
食物加热后,其中的蛋白质发生了变性,有利于人体消化吸收。
乙醇、苯酚和碘等作为消毒防腐药可以使微生物的蛋白质变性,
导致其死亡,达到消毒的目的。
紫外线可用于杀菌消毒。
常用福尔马林(40%的甲醛溶液)保存动物标本
波尔多液(硫酸铜、生石灰和水制成)防治农作物病害
疫苗等生物制剂需要在低温下保存。
攀登高山时为防止强紫外线引起皮肤和眼睛的蛋白质变性灼伤,
需要防晒护目。
因误服铅、汞等重金属盐中毒的患者在急救时,可口服牛奶、蛋清 或豆浆,让铅、汞等重金属盐使他们变性,减少对人体伤害。
有时也要注意防止蛋白质变性。
化学与生活
(5)显色反应
含有苯环的蛋白质遇浓硝酸会有白色沉淀产生,加热后沉淀变黄色。
皮肤、指甲不慎沾上浓硝酸会出现黄色就是由此造成的。
除了硝酸,其他一些试剂也可以与蛋白质作用,
呈现特定颜色,可用于蛋白质的分析检测。
(6)灼烧:蛋白质在灼烧时有类似烧焦羽毛的气味。可用于蛋白质的鉴别。
浓硝酸
—鸡蛋清溶液
振荡
白色沉淀
加热
沉淀变黄色
颜(显)色反应:一般指有明显颜色变化的化学反应。
如:Fe3+(aq)与苯酚或SCN-(aq);
I2(aq)遇淀粉溶液;
浓HNO3(aq)和某些蛋白质,微热等。
焰色反应:某些金属单质或其化合物被灼烧时火焰呈现特殊的颜色。属于物理变化。
例:用于区分“毛线与棉线”,“人造丝与蚕丝”
(4)蛋白质的用途
蛋白质
蛋白质存在于一切细胞中,是人类必需的营养物质
毛和蚕丝的成分都为蛋白质,可以制作服装。
动物的皮革是衣服的原料
从动物皮、骨中提取的明胶可作食品增稠剂,阿胶可作中药材等。
从大豆、牛奶中提取的酪素用来制作食品和涂料。
绝大多数酶也是蛋白质,是重要的催化剂。
人工合成结晶牛胰岛素
胰岛素是由胰腺分泌的一种激素,具有调节体内糖类、蛋白质和脂肪代谢等功能。胰岛素是最先被确定氨基酸序列的蛋白质,其结构由桑格①等于1955年测定。它由两条肽链组成,分别是由21个氨基酸形成的 A 链和30个氨基酸形成的 B 链,两条链通过二硫键(- S - S -)连接。
烫发的原理
头发主要由角蛋白组成,其中的含硫氨基酸形成的二硫键(-S-S-)是维持头发弹性和形状的一个重要结构。一般烫发时使用的还原剂可以使头发中的二硫键断裂,产生游离的巯基(-SH )。再用一定的工具将头发卷曲或拉直成需要的形状。然后用氧化剂使巯基之间发生反应,生成新的二硫键,使头发的形状得以固定。频繁烫发会对头发造成一定程度的损害。
资料卡片
科学史话
酶是一类由_____产生的、对生物体内的化学反应具有_____作用的有机化合物,其中绝大多数是________。
在酶的作用下,生物才能进行新陈代谢,完成消化、呼吸、运动、生长、发育、繁殖等生命活动。
细胞
催化
蛋白质
(1)高度的专一性. (一种酶只催化一种反应)
(2)高效性. (比普通催化剂高107)
(3)条件温和, 不需加热.
(一般在接近体温和中性的条件下进行,此时酶的
活性最高。超过适宜的温度时,酶将失去活性)
新冠病毒主要蛋白酶结构
3.酶催化作用的特点
目前,酶已经得到了广泛的应用,如蛋白酶用于医药、制革等工业,
淀粉酶用于食品、发酵、纺织等工业,有的酶还可用于疾病的诊断。
1.定义:
2.功能:
4.酶的应用:
三、酶
1.市场上有一种加酶洗衣粉,即在洗衣粉中加入少量的碱性蛋白酶,它的催化活性很强,衣服上的汗渍、血迹及人体排出的蛋白质、油渍遇到它,皆能水解而除去。下列衣料不能用加酶洗衣粉洗涤的是
①棉织品 ②羊毛织品 ③腈纶织品 ④蚕丝织品 ⑤涤纶织品 ⑥锦纶织品
A.①②③ B.②④ C.③④⑤ D.③⑤⑥
B
2.绝大多数的酶是蛋白质,能催化多种化学反应。下列表示温度与化学反应速率的关系曲线中,以酶作催化剂的是( )
C
对点训练
缩合
组成、结构
性质
胶体
盐析
变性
颜色反应
灼烧反应
水解
两性
鉴别蛋白质
分离提纯蛋白质
消毒杀菌
蛋白质
α-氨基酸
水解
R—C—COOH
NH2
H
α-氨基酸通式:
化学性质
分子结构
两性
成肽反应
概念、存在、物性
酶
概念
应用
特点
功能
高效性
专一性
温和性
课堂小结
(1)氨基酸是一种既能与强碱反应又能与强酸反应的有机高分子。 ( )
(2)酶的催化作用是温度越高越好。( )
(3)蛋白质遇浓硝酸都会显黄色。( )
(4)硫酸铵溶液会使蛋白质发生变性。( )
(5)氨基酸分子、烃分子中的氢原子数均为偶数。( )
(6)氨基酸能发生酯化反应、成肽反应和水解反应。( )
(7)向两份蛋白质溶液中分别加入饱和NaCl溶液和CuSO4溶液,均有固体析出,两者原理相同。 ( )
(8)酶均是蛋白质,是体内反应的催化剂。( )
(9)蛋白质在酶的作用下,可直接水解生成各种氨基酸。( )
1.判断正误
×
×
×
×
×
×
×
×
×
达标训练
2.新型冠状病毒的主要成分是蛋白质、核酸、脂肪及糖类物质,下列说法正确的是( )
A.蛋白质、核酸、脂肪及糖类在一定条件下都能水解,其中蛋白质水解的产物是氨基酸
B.医院可能采取高温或者紫外线照射的方法能使蛋白质变性,杀死病毒
C.蛋白质、核酸、脂肪及糖类都是高分子化合物
D.浓的K2SO4溶液能使溶液中的蛋白质析出,加水后析出的蛋白质不再溶解
B
3.“春蚕到死丝方尽,蜡烛成灰泪始干”中的“泪” 和“丝”分别指( )
A.纤维素、脂肪 B.烃、蛋白质
C.淀粉、油脂 D.蛋白质、植物油
B
4.把①蔗糖 ②淀粉 ③纤维素 ④蛋白质在稀硫酸存在下分别进行水解,
最终产物只有1种是( )
A.①和② B.只有③
C.只有④ D.只有②和③
D
达标训练
网
科
第二节 蛋白质
第四章 生物大分子
4.2 蛋白质
学习目标
1.通过结构分析认识氨基酸的组成、结构特点和主要化学性质,能判断氨基酸的缩合产物。
2.了解蛋白质的组成、结构和性质,知道氨基酸、多肽和蛋白质之间的关系。学会用蛋白质的性质解释生活中的相关现象。
3.了解酶催化反应的特点。
新课导入
羧酸分子烃基上的氢原子被氨基(-NH2)取代的化合物(属于取代羧酸)
1.概念:
例如:
烃基上一个H被-NH2取代
α-氨基丁酸
CH3CH2CH2COOH
CH3CH2CH COOH
NH2
γ β α
自然界中存在的氨基酸
组成生物体内
人体内不能合成
只有21种
8种氨基酸
几百种
必需氨基酸
→为了人体的健康,应注意合理膳食、科学营养,保证人体必需氨基酸的摄取。
2-氨基丁酸
食物供给
天然的蛋白质都是由α-氨基酸构成!
(氨基和羧基连在同一C上)
一、氨基酸
俗名 结构简式 系统命名
甘氨酸 H2N—CH2COOH
丙氨酸
谷氨酸
苯丙氨酸
半胱氨酸
以下几种氨基酸是否存在手性碳,若有请标出。
氨基乙酸
2-氨基丙酸
2-氨基戊二酸
α-氨基苯丙酸
2 -氨基 -3 -巯基丙酸
*
HS CH2 CH COOH
NH2
*
*
*
除甘氨酸外,一般α 氨基酸中含手性碳原子,是手性分子,具有对映异构体
味精——谷氨酸单钠盐
qíu
guāng
拓展训练
R CH COOH
NH2
酯化
酸性
羧基
氨基
碱性
还原性
CH2COOH+HCl CH2COOH
NH2
NH3Cl
R-CH-COOH + NaOH
NH2
R-CH-COONa + H2O
NH2
(1) 两性:能与酸、碱反应
(参照:NH3 + HCl = NH4Cl)
2.物理性质
天然氨基酸均为无色晶体,熔点较高,在200~3000C时熔化分解,
一般能溶于水而难溶于乙醇、乙醚等有机溶剂
3.化学性质
盐酸(氯化)氨基羧酸
氨基羧酸钠
(2)成肽反应
两个氨基酸分子(可以相同,也可以不同)在一定条件下,通过氨基与 羧酸间缩合脱去水,形成含有肽键( )的化合物。
氨基酸
氨基酸
成肽反应是分子间脱水反应,属于取代反应
断键方式:酸脱羟基,氨脱氢
注意:肽键是一种酰胺基
肽键
多肽
根据氨基酸分子数的多少叫二肽、三肽…等
二肽
由两个氨基酸分子缩合后形成的含有一个肽键的化合物。
由n个氨基酸分子发生成肽反应,生成一个肽链时,会生成(n-1)个水分子和(n-1)个肽键
肽键可简写为“—CONH—”,不能写成“—CNHO—”,两者的连接方式不同。
两分子氨基酸
缩合
二肽
三肽
缩合
+氨基酸
缩合
+氨基酸
四肽
缩合
+氨基酸
多肽
· · · · · ·
呈链状
肽链
又称
相互结合形成
盘曲、折叠
蛋白质
(1)多肽的性质: 因肽键的存在, 多肽能进行水解;
(2)无论肽链有多长,在链的两端,一端有自由的氨基(—NH2);
另一端有自由的羧基(—COOH),因此,多肽也具有“两性”。
(3)多种氨基酸分子按不同的排列顺序以肽键相互结合,
可以形成千百万种具有不同的理化性质和生理活性的多肽链。
一般把Mr在1万以上,
并具有一定空间结构的多肽称为蛋白质。
特别提醒
R O R′ O
-HN-CH-C-NH-CH-C-
=
=
[ ]n
R O R′ O
H-HN-CH-C-OH + H-NH-CH-C-OH
=
=
H
OH
多肽
两个不同的氨基酸共聚:
单体通过分子间的相互缩合而生成成高分子化合物,同时有小分子(如H2O、NH3等)生成的反应叫缩合聚合反应,简称缩聚反应。
小结:缩聚反应
由一种单体进行缩聚反应,生成的小分子物质的量一般为n-1;
由两种单体进行缩聚反应,生成的小分子物质的量一般为2n-1。
n
n
+ (2n-1)H2O
拓展延伸
2.氨基酸的缩合反应也可能成环,试写出下列反应方程式
①NH2-CH2-COOH的分子间脱水成环
②NH2-CH2-CH2-CH2-CH2-COOH的分子内脱水成环
O=C
C=O
NH—CH2
CH2—NH
1.由甘氨酸和丙氨酸形成的链状二肽可能有几种?
4种
催化剂
2H2O
H2C-CO-OH
NH-H
HO-OC-CH2
H-HN
+
+
+
H2O
催化剂
CH2 —CH2—CO—OH
CH2—CH2—NH—H
H2C
C=O
CH2—CH2
CH2—NH
对点训练
3. 书写下列氨基酸的缩聚反应
苯丙氨酸与甘氨酸发生成肽反应生成多肽
①
②
R-CH-COOH
NH2
对点训练
4. 已知-NH2连在苯环上显碱性, 连在苯环上显中性,现有有机物C7H7O2N,分子结构中有一个苯环和两个取代基,且两取代基在苯环上处于相对位置,请写出符合下列要求的结构简式。
(1)该有机物只具有酸性:
(2)该有机物只具有碱性:
(3)该有机物具有两性:
(4)该有机物既无酸性又无碱性:
HO-
-C-NH2
O
O
-C-NH2
H2N-
-C-OH
O
H2N-
-O-C-H
O
O2N-
-CH3
同分异构:氨基酸、氨基酯、硝基化合物三者异构
对点训练
胶原蛋白
鸡蛋清
银耳
桃胶
鸡蛋清和胶原蛋白溶液中含有蛋白质,而银耳和桃胶中不含蛋白质。其实银耳和桃胶煮出来的东西看上去粘稠有弹性,像是一种胶,但并不是胶原蛋白,从化学的角度来看,他们是我们前面学过的多糖。
化学与生活
注意:
(2)组成: 蛋白质中主要含有C、H、O、N、S等元素,有些蛋白质还含有
P、Fe、Zn、Cu等元素。属于天然有机高分子。其溶液具有胶体的某些性质。
(1)定义:蛋白质是由多种氨基酸通过肽键等相互连接形成的一类生物大分子。
1.蛋白质的定义与组成
(3)存在:
1839年,荷兰化学家穆尔德提出蛋白质(protein)这个名词,源于希腊文“proteios”,意为原始的,引申为第一位的,最重要的意思。
光亮的通路
动物的肌肉、皮肤、血液、蚕丝、 毛、发、蹄、角;
酶、激素、血红蛋白、细菌、病毒、抗体、阿胶含有蛋白质;
许多植物的种子(大豆、花生、小麦、稻谷)里也富含蛋白质。
新冠病毒
是一般细胞中含量最多的有机分子,约占细胞干重的一半以上。
几乎一切生命活动过程都与蛋白质有关,没有蛋白质就没有生命。
二、蛋白质
一级结构
二级结构
三级结构
四级结构
2.蛋白质的结构
结构多样性
功能多样性
脱水缩合
空间结构肽链
三聚氰胺含氮量为66.7%,是牛奶的151倍,是奶粉的23倍。
每100g牛奶中添加
0.1克三聚氰胺,
就能提高0.4%蛋白质!
蛋白质含量的测定:由于生物组织中绝大部分氮元素来自蛋白质,而且各种来源不同的蛋白质的含氮量都比较接近,平均为16%。因此生物样品中的1 g氮元素大致相当于6.25 g蛋白质,由此可以通过测定样品中氮元素的质量分数计算出其中蛋白质的含量。
资料卡片
【思考】蛋白质结构中一定含有哪些官能团?
3.蛋白质的化学性质
(1)蛋白质的两性:
氨基
羧基
肽键
肽键
蛋白质的多肽是由多个氨基酸缩合形成的,
在多肽链的两端必然存在着自由的氨基与羧基,
同时侧链中也往往存在酸性或碱性基团。
蛋白质与氨基酸类似,也是两性分子,
既能与酸反应,又能与碱反应。
氨基
羧基
肽键
(2)水解反应
蛋白质 多肽 氨基酸
酶或酸或碱
水解
酶或酸或碱
水解
HO
H
能发生水解的有机物
酯、油脂、
归纳总结:
蛋白质等
蔗糖、麦芽糖、淀粉、纤维素、
卤代烃、
天然蛋白质→ 多肽 →二肽 →α-氨基酸(最终产物)
食物中的蛋白质在人体内各种蛋白酶的作用下水解成氨基酸,
氨基酸被肠壁吸收进入血液,再在体内重新合成人体所需要的
蛋白质。
(3)盐析
注意:
①盐析是一个可逆的过程,属于物理变化过程。不影响蛋白质的性质。 ②应用:利用多次盐析的方法分离、提纯蛋白质。
可溶性盐
硫酸铵、
硫酸钠、
氯化钠等
蛋白质溶液
加水
盐溶液少量:
促进蛋白质的溶解
盐溶液达到一定浓度:
使蛋白质的溶解度降低而从溶液中析出
加热
白色沉淀
加水
沉淀不溶解
概 念
影响因素 物理
化学
特 点 变性会使蛋白质的结构发生变化,使其失去原有的__________,
在水中不能重新溶解,是 过程
应 用
在某些物理或化学因素的影响下,蛋白质的性质和生理功能发生改变的现象
加热、加压、搅拌、振荡、紫外线和放射线、超声波等
强酸、强碱、重金属盐(Pb2+、Cu2+、Ba2+、Ag+、Hg2+等)、乙醇、甲醛、丙酮等
不可逆
生理活性
杀菌、消毒、防中毒
(4)蛋白质的变性
思考:关于怎么吃鸡蛋,网上众说纷纭,有些主张生吃,有些觉得熟的更好,大家更倾向于哪一种呢?
科普:鸡蛋加热后,蛋白质的空间结构被破坏,原有的生物活性会丧失,溶解度降低,黏度增大,肽链松散,更易被水解消化。所以更多的人会选择将鸡蛋煮熟了再吃,这是有一定科学依据的(这样更利于消化吸收)。
鸡蛋清溶液
在日常生活中有时需要利用蛋白质变性:
食物加热后,其中的蛋白质发生了变性,有利于人体消化吸收。
乙醇、苯酚和碘等作为消毒防腐药可以使微生物的蛋白质变性,
导致其死亡,达到消毒的目的。
紫外线可用于杀菌消毒。
常用福尔马林(40%的甲醛溶液)保存动物标本
波尔多液(硫酸铜、生石灰和水制成)防治农作物病害
疫苗等生物制剂需要在低温下保存。
攀登高山时为防止强紫外线引起皮肤和眼睛的蛋白质变性灼伤,
需要防晒护目。
因误服铅、汞等重金属盐中毒的患者在急救时,可口服牛奶、蛋清 或豆浆,让铅、汞等重金属盐使他们变性,减少对人体伤害。
有时也要注意防止蛋白质变性。
化学与生活
(5)显色反应
含有苯环的蛋白质遇浓硝酸会有白色沉淀产生,加热后沉淀变黄色。
皮肤、指甲不慎沾上浓硝酸会出现黄色就是由此造成的。
除了硝酸,其他一些试剂也可以与蛋白质作用,
呈现特定颜色,可用于蛋白质的分析检测。
(6)灼烧:蛋白质在灼烧时有类似烧焦羽毛的气味。可用于蛋白质的鉴别。
浓硝酸
—鸡蛋清溶液
振荡
白色沉淀
加热
沉淀变黄色
颜(显)色反应:一般指有明显颜色变化的化学反应。
如:Fe3+(aq)与苯酚或SCN-(aq);
I2(aq)遇淀粉溶液;
浓HNO3(aq)和某些蛋白质,微热等。
焰色反应:某些金属单质或其化合物被灼烧时火焰呈现特殊的颜色。属于物理变化。
例:用于区分“毛线与棉线”,“人造丝与蚕丝”
(4)蛋白质的用途
蛋白质
蛋白质存在于一切细胞中,是人类必需的营养物质
毛和蚕丝的成分都为蛋白质,可以制作服装。
动物的皮革是衣服的原料
从动物皮、骨中提取的明胶可作食品增稠剂,阿胶可作中药材等。
从大豆、牛奶中提取的酪素用来制作食品和涂料。
绝大多数酶也是蛋白质,是重要的催化剂。
人工合成结晶牛胰岛素
胰岛素是由胰腺分泌的一种激素,具有调节体内糖类、蛋白质和脂肪代谢等功能。胰岛素是最先被确定氨基酸序列的蛋白质,其结构由桑格①等于1955年测定。它由两条肽链组成,分别是由21个氨基酸形成的 A 链和30个氨基酸形成的 B 链,两条链通过二硫键(- S - S -)连接。
烫发的原理
头发主要由角蛋白组成,其中的含硫氨基酸形成的二硫键(-S-S-)是维持头发弹性和形状的一个重要结构。一般烫发时使用的还原剂可以使头发中的二硫键断裂,产生游离的巯基(-SH )。再用一定的工具将头发卷曲或拉直成需要的形状。然后用氧化剂使巯基之间发生反应,生成新的二硫键,使头发的形状得以固定。频繁烫发会对头发造成一定程度的损害。
资料卡片
科学史话
酶是一类由_____产生的、对生物体内的化学反应具有_____作用的有机化合物,其中绝大多数是________。
在酶的作用下,生物才能进行新陈代谢,完成消化、呼吸、运动、生长、发育、繁殖等生命活动。
细胞
催化
蛋白质
(1)高度的专一性. (一种酶只催化一种反应)
(2)高效性. (比普通催化剂高107)
(3)条件温和, 不需加热.
(一般在接近体温和中性的条件下进行,此时酶的
活性最高。超过适宜的温度时,酶将失去活性)
新冠病毒主要蛋白酶结构
3.酶催化作用的特点
目前,酶已经得到了广泛的应用,如蛋白酶用于医药、制革等工业,
淀粉酶用于食品、发酵、纺织等工业,有的酶还可用于疾病的诊断。
1.定义:
2.功能:
4.酶的应用:
三、酶
1.市场上有一种加酶洗衣粉,即在洗衣粉中加入少量的碱性蛋白酶,它的催化活性很强,衣服上的汗渍、血迹及人体排出的蛋白质、油渍遇到它,皆能水解而除去。下列衣料不能用加酶洗衣粉洗涤的是
①棉织品 ②羊毛织品 ③腈纶织品 ④蚕丝织品 ⑤涤纶织品 ⑥锦纶织品
A.①②③ B.②④ C.③④⑤ D.③⑤⑥
B
2.绝大多数的酶是蛋白质,能催化多种化学反应。下列表示温度与化学反应速率的关系曲线中,以酶作催化剂的是( )
C
对点训练
缩合
组成、结构
性质
胶体
盐析
变性
颜色反应
灼烧反应
水解
两性
鉴别蛋白质
分离提纯蛋白质
消毒杀菌
蛋白质
α-氨基酸
水解
R—C—COOH
NH2
H
α-氨基酸通式:
化学性质
分子结构
两性
成肽反应
概念、存在、物性
酶
概念
应用
特点
功能
高效性
专一性
温和性
课堂小结
(1)氨基酸是一种既能与强碱反应又能与强酸反应的有机高分子。 ( )
(2)酶的催化作用是温度越高越好。( )
(3)蛋白质遇浓硝酸都会显黄色。( )
(4)硫酸铵溶液会使蛋白质发生变性。( )
(5)氨基酸分子、烃分子中的氢原子数均为偶数。( )
(6)氨基酸能发生酯化反应、成肽反应和水解反应。( )
(7)向两份蛋白质溶液中分别加入饱和NaCl溶液和CuSO4溶液,均有固体析出,两者原理相同。 ( )
(8)酶均是蛋白质,是体内反应的催化剂。( )
(9)蛋白质在酶的作用下,可直接水解生成各种氨基酸。( )
1.判断正误
×
×
×
×
×
×
×
×
×
达标训练
2.新型冠状病毒的主要成分是蛋白质、核酸、脂肪及糖类物质,下列说法正确的是( )
A.蛋白质、核酸、脂肪及糖类在一定条件下都能水解,其中蛋白质水解的产物是氨基酸
B.医院可能采取高温或者紫外线照射的方法能使蛋白质变性,杀死病毒
C.蛋白质、核酸、脂肪及糖类都是高分子化合物
D.浓的K2SO4溶液能使溶液中的蛋白质析出,加水后析出的蛋白质不再溶解
B
3.“春蚕到死丝方尽,蜡烛成灰泪始干”中的“泪” 和“丝”分别指( )
A.纤维素、脂肪 B.烃、蛋白质
C.淀粉、油脂 D.蛋白质、植物油
B
4.把①蔗糖 ②淀粉 ③纤维素 ④蛋白质在稀硫酸存在下分别进行水解,
最终产物只有1种是( )
A.①和② B.只有③
C.只有④ D.只有②和③
D
达标训练
