2023年中考化学复习 实验专攻五 金属活动顺序课件(共17张PPT)
文档属性
| 名称 | 2023年中考化学复习 实验专攻五 金属活动顺序课件(共17张PPT) |

|
|
| 格式 | ppt | ||
| 文件大小 | 2.0MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-06-13 00:00:00 | ||
图片预览





文档简介
(共17张PPT)
第一部分
基础知识复习
第三板块 身边的化学物质
1
必备知识
2
精例精析
3
突破训练
实验专攻五 金属活动顺序
金属活动顺序探究的原理
默写金属活动性顺序表:___________________________________________________________
1.金属与酸的反应:能与酸反应的金属在 前,反应越剧烈,则金属活动性越强,不能与酸反应的金属位于氢后。
2.金属与盐溶液反应:能发生反应,则该金属的活动性大于组成该盐的金属。
K Ca Na Mg Al Zn Fe Sn Pb(H) Cu Hg Ag Pt Au
氢
注意:①实验前必须用砂纸打磨,目的是除去金属表面的氧化膜。②实验不能采用浓硫酸或者硝酸,同时必须选择质量、大小、形状相同的金属和相同浓度的酸。③验证三种金属活动性强弱时,先按照金属活动顺序表把金属排序,然后再采取“两金夹一盐”方案即活动性最强与活动性最弱的金属用单质与活动性居中的金属的盐溶液进行反应,或者“两盐夹一金”的方案即活动性最强与最弱的金属用其盐溶液与活动性居中的金属单质进行反应。
(2022·陕西)白铜是铜、镍(Ni)合金,某小组同学欲利用废弃的白铜回收铜、镍两种金属。
(1)先向盛有等量镍粉和锌粉的两支试管中分别加入溶质质量分数相同的稀硫酸,观察到都有气泡产生,且锌粉与稀硫酸反应更剧烈,镍粉与稀硫酸反应后的溶液为绿色,说明镍的金属活动性比锌
(填“强”或“弱”)。
弱
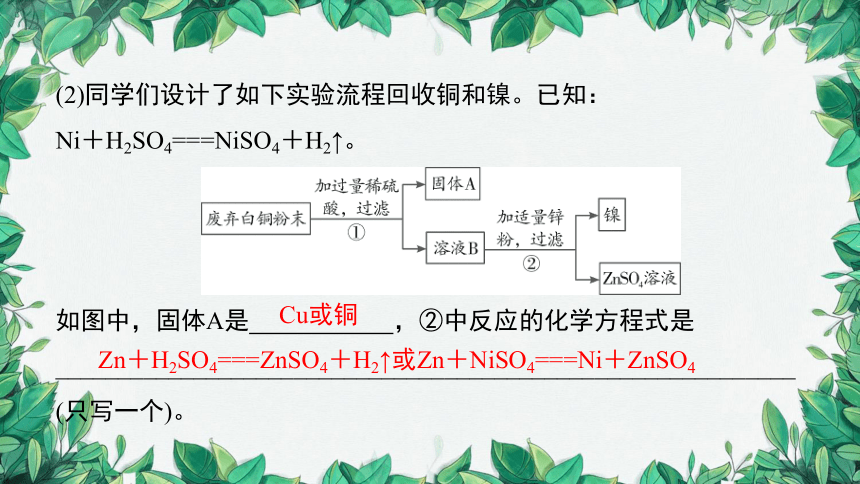
(2)同学们设计了如下实验流程回收铜和镍。已知:
Ni+H2SO4===NiSO4+H2↑。
如图中,固体A是 ,②中反应的化学方程式是___________________________________________________________
(只写一个)。
Cu或铜
Zn+H2SO4===ZnSO4+H2↑或Zn+NiSO4===Ni+ZnSO4
(3)要验证Ni、Zn、Cu的金属活动性顺序,下列各组药品不能达到目的的是 (填字母)。
A.Ni、Zn、Cu、稀盐酸 B.Ni、Cu、ZnSO4溶液
C.Zn、Cu、NiSO4溶液 D.Ni、ZnSO4溶液、CuSO4溶液
B
【思路点拨】 (1)由实验现象可知,锌粉与稀硫酸反应更剧烈,则Zn>Ni;(2)根据金属活动性顺序,铜排在氢的后面,与酸不反应,因此固体A为铜;硫酸过量,因此滤液B中含有硫酸和硫酸镍,锌与硫酸反应生成硫酸锌和氢气,锌比镍活泼,可以将镍置换出来;(3)A.锌和稀盐酸反应速率比镍快,铜不能和稀盐酸反应,说明活动性锌>镍>铜;B.镍、铜都不能和硫酸锌反应,说明锌最活泼,不能比较镍和铜的活泼性;C.锌能和硫酸镍反应,铜不能和硫酸镍反应,说明活动性锌>镍>铜;D.镍不能和硫酸锌反应,说明锌比镍活泼,镍能和硫酸铜反应,说明镍比铜活泼。
1.(2022·娄底模拟)下面对金属的利用,不能用金属活动性顺序解释的是( )
A.用铁回收含铜废液中的铜
B.用锌与稀硫酸反应制取氢气
C.古代金银制品能保存至今
D.利用涂刷铝粉来保护铁质暖气片
D
2.(2022·鸡西)现有X、Y、Z三种金属。如果把X和Y分别放入稀硫酸中,X溶解并产生氢气,Y不反应。如果Y和Z分别放入硝酸银溶液中,过一会儿,在Y表面有银析出,而Z没有变化。根据以上实验事实,金属活泼性由强到弱( )
A.X>Y>Z B.Z>X>Y
C.X>Z>Y D.Y>X>Z
A
3.(2022·湘西州)为验证铁、铜、银的金属活动性
顺序,某同学设计了以下四组实验。下列说法错
误的是( )
A.通过实验①、②,能验证金属活动性:Fe>
Cu
B.通过实验①、②、③,能验证金属活动性:Fe>Cu>Ag
C.实验④中X为Cu,Y为FeSO4,能验证金属活动性:Fe>Cu
D.实验④中X为Cu,Y为AgNO3,能验证金属活动性:Cu>Ag
B
4.(2022·邵阳)在硝酸铜、硝酸银的混合溶液中加入一定量的锌粉,充分反应后过滤。下列说法正确的是( )
A.若滤液为无色,则滤渣中一定有银和锌,可能有铜
B.若滤液为蓝色,则滤液中一定有Cu2+、Zn2+,可能有Ag+
C.若往滤渣中加入稀盐酸有气泡产生,则滤液中一定有Zn2+、Ag+,可能有Cu2+
D.若往滤液中加入稀盐酸有白色沉淀产生,则滤渣中一定有银和铜,可能有锌
B
5.(2022·朝阳)在人类社会的发展进程中,金属起着重要的作用,结合所学知识回答下列问题:
(1)铝合金与铝片相互刻画,在铝片表面会留下划痕,说明铝合金比铝硬度 (选填“大”或“小”)。
(2)汽车表面的烤漆,不仅美观还能防锈,其防锈的原理是 。
(3)工人师傅切割铁板时,用硫酸铜溶液在铁板上画线,可以留下红色痕迹,产生这种现象的原因是 . (用化学方程式表示)。
大
隔绝氧气和水
Fe+CuSO4===FeSO4+Cu
(4)在含有硝酸银、硝酸亚铁和硝酸铝的混合溶液中,加入一定量的锌,充分反应后,过滤,滤液仍为浅绿色,则此时滤液中一定含有的溶质是___________________________________(用化学式表示)。
(5)为探究Fe、Zn、Cu三种金属的活动性强弱,下列选项中能达到实验目的的是 。
A. 铁、氯化锌溶液、氯化铜溶液 B.铜、锌、氯化亚铁溶液
C.铜、氯化锌溶液、氯化亚铁溶液
Al(NO3)3、Zn(NO3)2、Fe(NO3)2
AB
6.(2022·云南)金属及金属材料广泛应用于生产、生活及科学实验,其应用推动了社会的发展。
(1)下列实验中,铜片上的白磷燃烧,说明铜具有 导热性;黄铜片和纯铜片相互刻画,纯铜片上留下刻痕,说明黄铜的硬度比纯铜的硬度 (填“大”或“小”)。
大
(2)铁在潮湿的空气中易生锈,写出一种防止铁制品生锈的方法 。
(3)春秋战国时期,我国就开始生产和使用铁器。工业上用赤铁矿(主要成分Fe2O3)和一氧化碳反应炼铁的化学方程式为______________________________________。
铁制品表面涂油或刷油漆(合理即可)
3CO+Fe2O3 2Fe+3CO2
高温
(4)某同学对含Cu(NO3)2、
AgNO3、M(NO3)2的混合溶液
进行探究,已知M表示一种金
属元素。
①气体X的化学式为 ;
②金属Fe、Cu、Ag、M的活动性由强到弱的顺序是 。
③滤液D中所含溶质的成分可能有 种情况。
H2
M>Fe>Cu>Ag
3
第一部分
基础知识复习
第三板块 身边的化学物质
1
必备知识
2
精例精析
3
突破训练
实验专攻五 金属活动顺序
金属活动顺序探究的原理
默写金属活动性顺序表:___________________________________________________________
1.金属与酸的反应:能与酸反应的金属在 前,反应越剧烈,则金属活动性越强,不能与酸反应的金属位于氢后。
2.金属与盐溶液反应:能发生反应,则该金属的活动性大于组成该盐的金属。
K Ca Na Mg Al Zn Fe Sn Pb(H) Cu Hg Ag Pt Au
氢
注意:①实验前必须用砂纸打磨,目的是除去金属表面的氧化膜。②实验不能采用浓硫酸或者硝酸,同时必须选择质量、大小、形状相同的金属和相同浓度的酸。③验证三种金属活动性强弱时,先按照金属活动顺序表把金属排序,然后再采取“两金夹一盐”方案即活动性最强与活动性最弱的金属用单质与活动性居中的金属的盐溶液进行反应,或者“两盐夹一金”的方案即活动性最强与最弱的金属用其盐溶液与活动性居中的金属单质进行反应。
(2022·陕西)白铜是铜、镍(Ni)合金,某小组同学欲利用废弃的白铜回收铜、镍两种金属。
(1)先向盛有等量镍粉和锌粉的两支试管中分别加入溶质质量分数相同的稀硫酸,观察到都有气泡产生,且锌粉与稀硫酸反应更剧烈,镍粉与稀硫酸反应后的溶液为绿色,说明镍的金属活动性比锌
(填“强”或“弱”)。
弱
(2)同学们设计了如下实验流程回收铜和镍。已知:
Ni+H2SO4===NiSO4+H2↑。
如图中,固体A是 ,②中反应的化学方程式是___________________________________________________________
(只写一个)。
Cu或铜
Zn+H2SO4===ZnSO4+H2↑或Zn+NiSO4===Ni+ZnSO4
(3)要验证Ni、Zn、Cu的金属活动性顺序,下列各组药品不能达到目的的是 (填字母)。
A.Ni、Zn、Cu、稀盐酸 B.Ni、Cu、ZnSO4溶液
C.Zn、Cu、NiSO4溶液 D.Ni、ZnSO4溶液、CuSO4溶液
B
【思路点拨】 (1)由实验现象可知,锌粉与稀硫酸反应更剧烈,则Zn>Ni;(2)根据金属活动性顺序,铜排在氢的后面,与酸不反应,因此固体A为铜;硫酸过量,因此滤液B中含有硫酸和硫酸镍,锌与硫酸反应生成硫酸锌和氢气,锌比镍活泼,可以将镍置换出来;(3)A.锌和稀盐酸反应速率比镍快,铜不能和稀盐酸反应,说明活动性锌>镍>铜;B.镍、铜都不能和硫酸锌反应,说明锌最活泼,不能比较镍和铜的活泼性;C.锌能和硫酸镍反应,铜不能和硫酸镍反应,说明活动性锌>镍>铜;D.镍不能和硫酸锌反应,说明锌比镍活泼,镍能和硫酸铜反应,说明镍比铜活泼。
1.(2022·娄底模拟)下面对金属的利用,不能用金属活动性顺序解释的是( )
A.用铁回收含铜废液中的铜
B.用锌与稀硫酸反应制取氢气
C.古代金银制品能保存至今
D.利用涂刷铝粉来保护铁质暖气片
D
2.(2022·鸡西)现有X、Y、Z三种金属。如果把X和Y分别放入稀硫酸中,X溶解并产生氢气,Y不反应。如果Y和Z分别放入硝酸银溶液中,过一会儿,在Y表面有银析出,而Z没有变化。根据以上实验事实,金属活泼性由强到弱( )
A.X>Y>Z B.Z>X>Y
C.X>Z>Y D.Y>X>Z
A
3.(2022·湘西州)为验证铁、铜、银的金属活动性
顺序,某同学设计了以下四组实验。下列说法错
误的是( )
A.通过实验①、②,能验证金属活动性:Fe>
Cu
B.通过实验①、②、③,能验证金属活动性:Fe>Cu>Ag
C.实验④中X为Cu,Y为FeSO4,能验证金属活动性:Fe>Cu
D.实验④中X为Cu,Y为AgNO3,能验证金属活动性:Cu>Ag
B
4.(2022·邵阳)在硝酸铜、硝酸银的混合溶液中加入一定量的锌粉,充分反应后过滤。下列说法正确的是( )
A.若滤液为无色,则滤渣中一定有银和锌,可能有铜
B.若滤液为蓝色,则滤液中一定有Cu2+、Zn2+,可能有Ag+
C.若往滤渣中加入稀盐酸有气泡产生,则滤液中一定有Zn2+、Ag+,可能有Cu2+
D.若往滤液中加入稀盐酸有白色沉淀产生,则滤渣中一定有银和铜,可能有锌
B
5.(2022·朝阳)在人类社会的发展进程中,金属起着重要的作用,结合所学知识回答下列问题:
(1)铝合金与铝片相互刻画,在铝片表面会留下划痕,说明铝合金比铝硬度 (选填“大”或“小”)。
(2)汽车表面的烤漆,不仅美观还能防锈,其防锈的原理是 。
(3)工人师傅切割铁板时,用硫酸铜溶液在铁板上画线,可以留下红色痕迹,产生这种现象的原因是 . (用化学方程式表示)。
大
隔绝氧气和水
Fe+CuSO4===FeSO4+Cu
(4)在含有硝酸银、硝酸亚铁和硝酸铝的混合溶液中,加入一定量的锌,充分反应后,过滤,滤液仍为浅绿色,则此时滤液中一定含有的溶质是___________________________________(用化学式表示)。
(5)为探究Fe、Zn、Cu三种金属的活动性强弱,下列选项中能达到实验目的的是 。
A. 铁、氯化锌溶液、氯化铜溶液 B.铜、锌、氯化亚铁溶液
C.铜、氯化锌溶液、氯化亚铁溶液
Al(NO3)3、Zn(NO3)2、Fe(NO3)2
AB
6.(2022·云南)金属及金属材料广泛应用于生产、生活及科学实验,其应用推动了社会的发展。
(1)下列实验中,铜片上的白磷燃烧,说明铜具有 导热性;黄铜片和纯铜片相互刻画,纯铜片上留下刻痕,说明黄铜的硬度比纯铜的硬度 (填“大”或“小”)。
大
(2)铁在潮湿的空气中易生锈,写出一种防止铁制品生锈的方法 。
(3)春秋战国时期,我国就开始生产和使用铁器。工业上用赤铁矿(主要成分Fe2O3)和一氧化碳反应炼铁的化学方程式为______________________________________。
铁制品表面涂油或刷油漆(合理即可)
3CO+Fe2O3 2Fe+3CO2
高温
(4)某同学对含Cu(NO3)2、
AgNO3、M(NO3)2的混合溶液
进行探究,已知M表示一种金
属元素。
①气体X的化学式为 ;
②金属Fe、Cu、Ag、M的活动性由强到弱的顺序是 。
③滤液D中所含溶质的成分可能有 种情况。
H2
M>Fe>Cu>Ag
3
同课章节目录
