第三章《有机合成及其应用合成高分子化合物》检测题(含答案)下学期高二化学鲁科版(2019)选择性必修3
文档属性
| 名称 | 第三章《有机合成及其应用合成高分子化合物》检测题(含答案)下学期高二化学鲁科版(2019)选择性必修3 |
|
|
| 格式 | docx | ||
| 文件大小 | 1.6MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-06-13 00:00:00 | ||
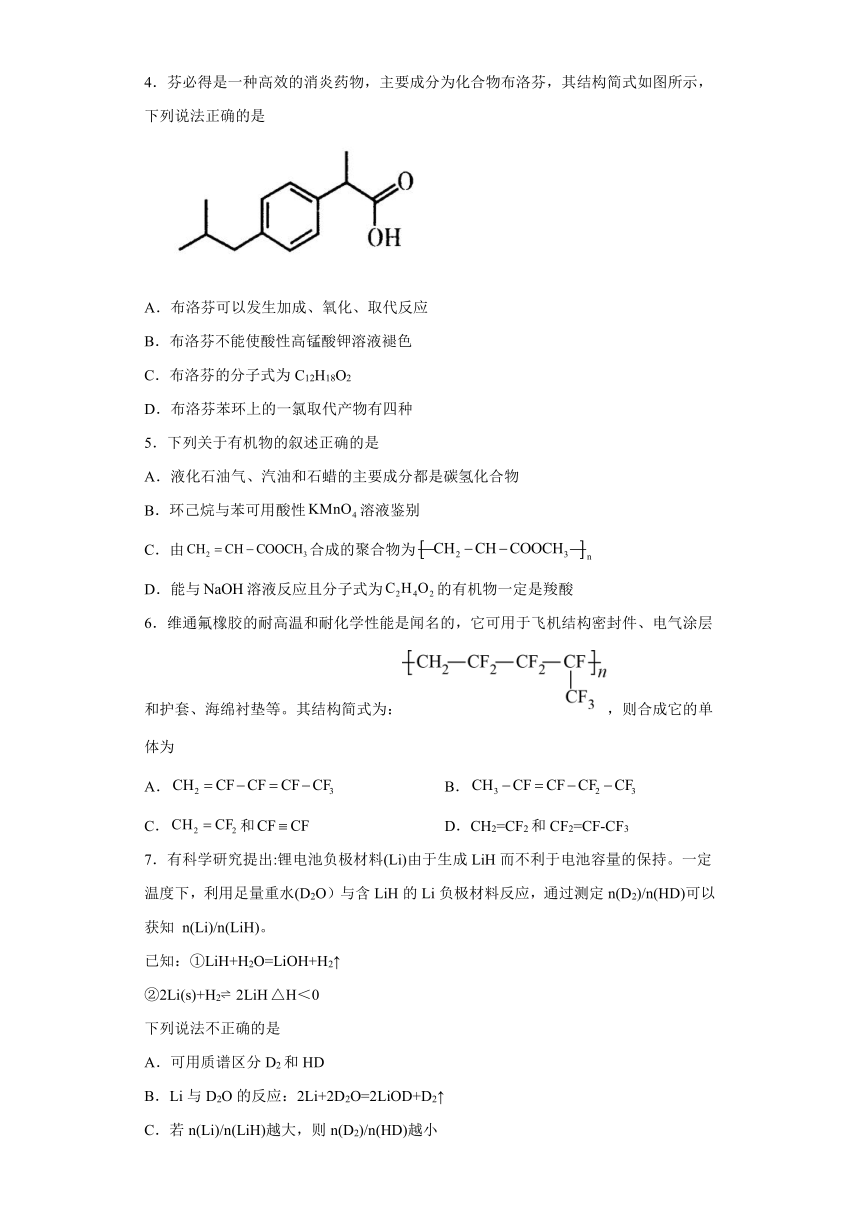
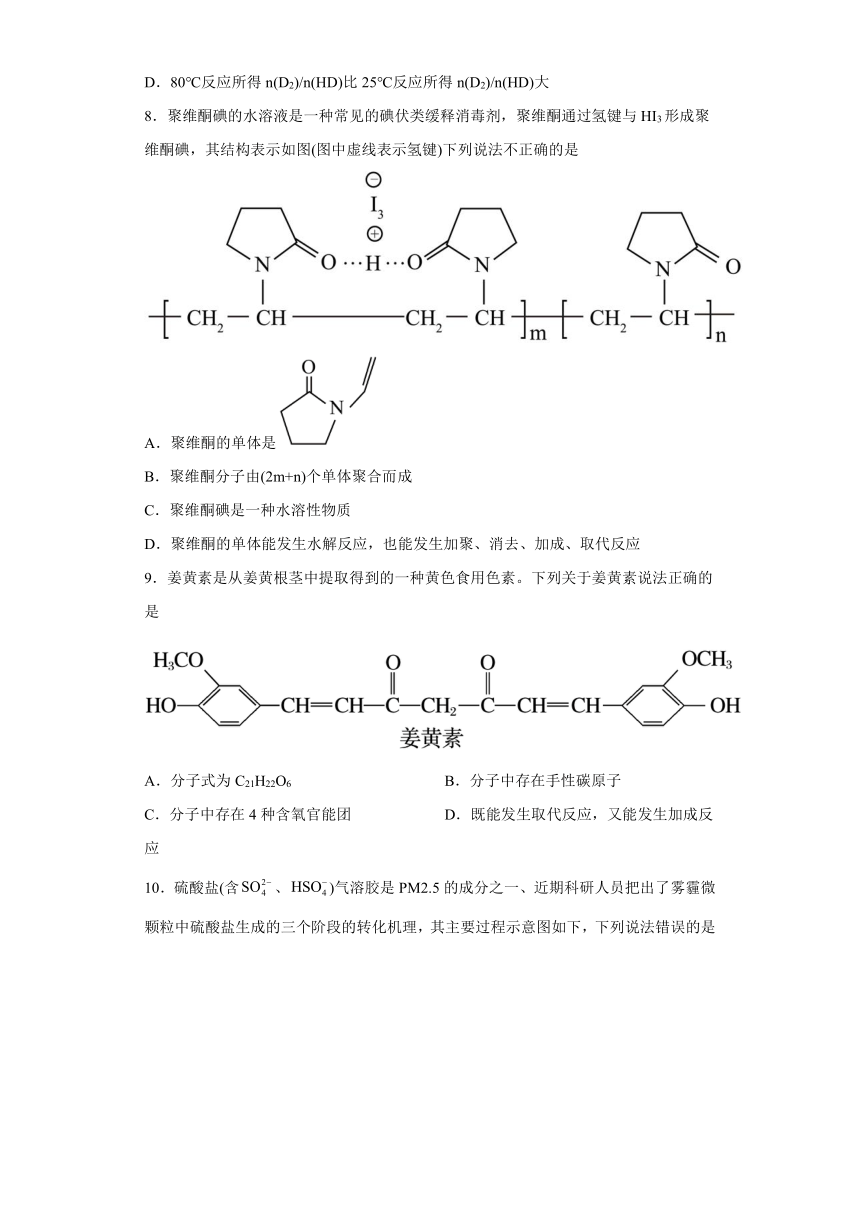
图片预览



文档简介
第三章《有机合成及其应用 合成高分子化合物》检测题
一、单选题(共13题)
1.我国科研人员发现中药成分黄芩素能明显抑制新冠病毒的活性。下列有关黄芩素的说法不正确的是
A.分子中有3种官能团 B.能与溶液反应
C.可发生氧化反应 D.能与发生加成反应
2.将有机物完全燃烧,生成CO2和H2O。将12.4 g该有机物的完全燃烧产物通过浓硫酸,浓硫酸增重10.8 g,再通过碱石灰,碱石灰又增重了17.6 g。下列说法不正确的是
A.该有机物的最简式为CH3O
B.该有机物的分子式可能为CH3O
C.该有机物的分子式一定为C2H6O2
D.该有机物核磁共振氢谱中可能有两个吸收峰
3.某化合物的结构(键线式)、球棍模型以及该有机分子的核磁共振氢谱图如图:
下列关于该有机化合物的叙述正确的是
A.该有机化合物中不同化学环境的氢原子有3种
B.该有机化合物属于芳香族化合物
C.键线式中的Et代表的基团为
D.1mol该有机化合物完全燃烧可以产生9molCO2和7molH2O
4.芬必得是一种高效的消炎药物,主要成分为化合物布洛芬,其结构简式如图所示,下列说法正确的是
A.布洛芬可以发生加成、氧化、取代反应
B.布洛芬不能使酸性高锰酸钾溶液褪色
C.布洛芬的分子式为C12H18O2
D.布洛芬苯环上的一氯取代产物有四种
5.下列关于有机物的叙述正确的是
A.液化石油气、汽油和石蜡的主要成分都是碳氢化合物
B.环己烷与苯可用酸性溶液鉴别
C.由合成的聚合物为
D.能与溶液反应且分子式为的有机物一定是羧酸
6.维通氟橡胶的耐高温和耐化学性能是闻名的,它可用于飞机结构密封件、电气涂层和护套、海绵衬垫等。其结构简式为:,则合成它的单体为
A. B.
C.和 D.CH2=CF2和CF2=CF-CF3
7.有科学研究提出:锂电池负极材料(Li)由于生成LiH而不利于电池容量的保持。一定温度下,利用足量重水(D2O)与含LiH的Li负极材料反应,通过测定n(D2)/n(HD)可以获知 n(Li)/n(LiH)。
已知:①LiH+H2O=LiOH+H2↑
②2Li(s)+H2 2LiH △H<0
下列说法不正确的是
A.可用质谱区分D2和HD
B.Li与D2O的反应:2Li+2D2O=2LiOD+D2↑
C.若n(Li)/n(LiH)越大,则n(D2)/n(HD)越小
D.80℃反应所得n(D2)/n(HD)比25℃反应所得n(D2)/n(HD)大
8.聚维酮碘的水溶液是一种常见的碘伏类缓释消毒剂,聚维酮通过氢键与HI3形成聚维酮碘,其结构表示如图(图中虚线表示氢键)下列说法不正确的是
A.聚维酮的单体是
B.聚维酮分子由(2m+n)个单体聚合而成
C.聚维酮碘是一种水溶性物质
D.聚维酮的单体能发生水解反应,也能发生加聚、消去、加成、取代反应
9.姜黄素是从姜黄根茎中提取得到的一种黄色食用色素。下列关于姜黄素说法正确的是
A.分子式为C21H22O6 B.分子中存在手性碳原子
C.分子中存在4种含氧官能团 D.既能发生取代反应,又能发生加成反应
10.硫酸盐(含、)气溶胶是PM2.5的成分之一、近期科研人员把出了雾霾微颗粒中硫酸盐生成的三个阶段的转化机理,其主要过程示意图如下,下列说法错误的是
A.第I阶段的化学方程式为:+NO2=+
B.该过程中NO2为催化剂
C.1mol在第II、III两个阶段共失去电子数目为NA
D.氧化性NO2>HNO2
11.下列说法正确的是
A.某有机物燃烧只生成CO2和H2O,且二者物质的量相等,则此有机物的组成为CnH2n
B.相同物质的量的乙烯和乙醇完全燃烧,乙醇消耗的氧气多
C.CH4和C2H4的混合气体与足量O2完全反应,反应前后气体体积一定不变(气体体积在同一温度和压强下测量)
D.相同质量的烃完全燃烧,烃中氢的百分含量越高,消耗O2越多
12.下列说法正确的是
A.丙烷分子的空间填充模型为:
B.羟基中氢原子的活泼性:乙酸>水>乙醇
C.聚丙烯的结构简式:
D.丙烯中所有原子可能共平面
13.如图所示物质是某药物的中间体。关于该化合物的说法错误的是
A.该物质既能发生加成反应又能发生消去反应
B.该物质存在顺反异构体
C.分子中含有3种含氧官能团
D.1mol该物质最多能与4molNaOH反应
二、非选择题(共10题)
14.某有机化合物经李比希法测得其中含碳的质量分数为54.5%、含氢的质量分数为9.1%,其余为氧。用质谱法分析知该有机物的相对分子质量为88.请回答下列有关问题:
(1)该有机物的分子式为_______。
(2)若该有机物的水溶液呈酸性,且结构中不含支链,则其核磁共振氢谱图中的峰面积之比为_______。
(3)若实验测得该有机物中不含结构,利用红外光谱仪测得该有机物的红外光谱如图所示。则该有机物的结构简式可能是_______、_______(写出两种即可)。
15.卤代烃在不同溶液中会发生不同类型的反应。请回答下列问题:
(1)向盛有1mL溴乙烷的试管中加入2mL 5%的NaOH溶液,加热,发生反应的化学方程式为_______。某同学取少量反应后的混合溶液,向其中滴加溶液,产生少量沉淀。该同学由此得出溴乙烷与NaOH水溶液反应生成了溴化钠,你认为他的结论_______(填“合理”或“不合理”),理由是_______。
(2)某同学在圆底烧瓶中加入2.0g NaOH和15mL无水乙醇,搅拌,再加入5mL 1-溴丁烷和几片碎瓷片,微热(液体沸腾后,移开酒精灯)。产生的气体通过盛有水的试管后,再通入盛有酸性溶液的试管中,观察到溶液紫红色逐渐褪去。
已知:溴乙烷的沸点:38.4℃,1-溴丁烷的沸点:101.6℃。
①该同学用溴乙烷代替1-溴丁烷进行实验时,发现酸性溶液不褪色。由已知沸点差异分析实验失败的原因可能是_______。
②实验后检验出反应产物中含有丁烯,但不能说明该条件下没有发生取代反应。若进一步检验是否生成1-丁醇,可采用的方法是_______(填字母)。
a.对产物进行红外光谱分析
b.对产物进行核磁共振氢谱分析
c.使反应混合物与金属钠反应
(3)写出2-溴-2-甲基丙烷发生消去反应的化学方程式:_______。
16.以乙烯为基本原料,合成六元环状化合物D的反应如下所示(部分试剂、产物及反应条件略去):
请写出各步反应的化学方程式和反应类型___________。
17.现有某有机化合物样品,对其进行如下操作:
i.充分燃烧6.51g该样品,得到20.47g二氧化碳和8.36g水。
ii.质谱分析得该物质的相对分子质量为84,
(1)该有机化合物的分子式为_______。
(2)向该有机化合物中加入少量溴的四氯化碳溶液,溶液褪色,用酸性溶液氧化该物质只能得到丙酸,该有机化合物的结构简式为_______。
18.(1)有两种有机物都含有碳92.3%,含有氢7.7%,第一种有机物对氢气的相对密度为13,第二种有机物的密度为3.49g/L(标准状况下),则第一种有机物的结构简式为___,第二种有机物的分子式为___。
(2)某仅由C、H、O三种元素组成的有机化合物,经测定相对分子质量为90,取该有机化合物样品1.8g,在纯氧中完全燃烧将产物先后通过浓硫酸和碱石灰,两者分别增重1.08g和2.64g,则该有机化合物分子式为___。
19.苯酚、甲醛溶液、浓盐酸在沸水浴条件下可制得酚醛树脂,实验室制取酚醛树脂的装置如图所示:
(1)试管上方长玻璃管的作用是___________。
(2)浓盐酸的作用是___________。
(3)此反应需水浴加热,不用温度计控制水浴温度的原因是___________。
(4)实验完毕后,若试管不易用水洗净,可以加入少量___________浸泡几分钟后,再洗净。
(5)写出实验室制取酚醛树脂的化学方程式___________,该有机反应类型是___________。
20.已知反应:,实验室用如图所示装置制备溴乙烷(沸点为38.4℃,密度为)。实验前先向仪器a中加入10g乙醇和足量浓硫酸,然后加入研细的20.6gNaBr。
(1)加入碎瓷片的作用是_______。
(2)试管d中出现的实验现象是_______。
(3)反应结束后,试管d中含少量杂质,为了除去粗产品中的杂质,可选用的试剂是_______(填字母)。
A.苯 B. C.溶液 D.
(4)经过分离、提纯、干燥后,该实验最终得到10.9g溴乙烷,则本实验中溴乙烷的产率为_______。
(5)通过以下实验步骤可检验溴乙烷中的溴元素,其正确的操作顺序是_______(填序号)。
①加热 ②加入溶液 ③加入稀酸化 ④加入溶液 ⑤冷却 ⑥取少量溴乙烷
21.某同学为确定某分子式为C2H6O2的液态有机物X的结构,准备按下列程序进行:
(1)查阅资料。已知:一个碳原子上连两个羟基()的物质不稳定。
(2)预测。若分子中不存在过氧键(-O-O-),则X的结构简式可能是:_____。
(3)设计实验方案验证X的结构。取一定量X与足量钠反应,通过测定生成氢气的体积来确定X分子中能与金属钠反应的氢原子数目,进而确定X的结构。若取6.2gX与足量金属钠反应,测得在标准状况下生成H22.24L,对应X的名称为:_____。
(4)根据实验方案讲行实验.
①选取如图仪器(胶管和固定装置略去,必要试剂自选),接口连接顺序为:_____。
②如何检验整套装置气密性 _____
③请指出能使实验比较安全、准确进行的关键实验步骤_____(至少指出两个关键步骤)。
22.某相对分子质量为40的链状不饱和烃A,能发生如图转化:
已知:①羟基所连接的碳原子上无氢原子时,难以发生催化氧化;②E能与NaHCO3溶液反应产生气体;③F为酯类化合物。
(1)A的分子式为____,A转化为B的反应类型为____,C转化为D的反应条件为____。
(2)B中所含有的官能团的名称为____,B中共平面的原子最多有____个。
(3)写出D转化为E的化学方程式:____。
(4)与E互为同分异构体的芳香族化合物K,已知:①K与E具有相同的官能团;②K不能与FeCl3溶液发生显色反应;③K有二个取代基,则符合上述条件的K共有___种。
(5)F的结构简式为_____。
23.物质F是一种芳香酯,常用作调香剂,其合成路线如下图所示:
已知E中含有两个甲基,请回答下列问题:
(1)物质A的名称是_______。
(2)各取1 mol物质D分别与足量Na、NaOH溶液、NaHCO3溶液反应,消耗的Na、NaOH、NaHCO3的物质的量之比为_______。
(3)物质A到F中除D以外含有手性碳原子的物质是_______(填标号)。
(4)B→C的反应方程式是_______。
(5)E的同分异构体中与其含有相同种类官能团的有_______种(不含E本身)。
参考答案:
1.A 2.B 3.C 4.A 5.A 6.D 7.C 8.D 9.D 10.B 11.D 12.B
13.D
14. 3:2:2:1
15.(1) 不合理 没有用硝酸进行酸化,排除的干扰
(2) 溴乙烷沸点低,加热时没有充分反应就挥发出去 ab
(3)
16.A→B:CH2=CH2+Br2CH2BrCH2Br,加成反应;B→C:CH2BrCH2Br+2 H2O CH2OHCH2OH+2HBr,取代反应;C→D:2 CH2OHCH2OH +H2O,取代反应
17.(1)C6H12
(2)CH3CH2CH=CHCH2CH3
18. CH≡CH C6H6 C3H6O3
19. 导气、冷凝回流 作催化剂 该反应的条件是沸水浴加热 乙醇 n+n +(n-1)H2O 缩聚反应
20.(1)防止液体暴沸
(2)液体分层,下层为油状液体
(3)C
(4)50%
(5)⑥④①⑤③②
21. CH3-O-CH2-OH、CH2OH-CH2OH 乙二醇 a、c、b、d、e、f 连接好仪器,关闭分液漏斗活塞,在量筒(水槽)中加水至浸没导管口,微热烧瓶,导管口有气泡产生,停止加热,导管内有一段水柱产生,说明气密性良好 检查实验装置的气密性;加入稍过量的金属钠;从漏斗中缓慢滴加X;待实验装置冷却后再读数;上下移动量筒,使其中液面与广口瓶中液面相平;视线与凹液面的最低点水平,读取量筒中水的体积
22.(1) C3H4 加成反应 NaOH的水溶液/加热
(2) 碳碳双键 17
(3)+O2+H2O
(4)12
(5)
23. 2-甲基-1-丁烯 2:1:1 BC 7
一、单选题(共13题)
1.我国科研人员发现中药成分黄芩素能明显抑制新冠病毒的活性。下列有关黄芩素的说法不正确的是
A.分子中有3种官能团 B.能与溶液反应
C.可发生氧化反应 D.能与发生加成反应
2.将有机物完全燃烧,生成CO2和H2O。将12.4 g该有机物的完全燃烧产物通过浓硫酸,浓硫酸增重10.8 g,再通过碱石灰,碱石灰又增重了17.6 g。下列说法不正确的是
A.该有机物的最简式为CH3O
B.该有机物的分子式可能为CH3O
C.该有机物的分子式一定为C2H6O2
D.该有机物核磁共振氢谱中可能有两个吸收峰
3.某化合物的结构(键线式)、球棍模型以及该有机分子的核磁共振氢谱图如图:
下列关于该有机化合物的叙述正确的是
A.该有机化合物中不同化学环境的氢原子有3种
B.该有机化合物属于芳香族化合物
C.键线式中的Et代表的基团为
D.1mol该有机化合物完全燃烧可以产生9molCO2和7molH2O
4.芬必得是一种高效的消炎药物,主要成分为化合物布洛芬,其结构简式如图所示,下列说法正确的是
A.布洛芬可以发生加成、氧化、取代反应
B.布洛芬不能使酸性高锰酸钾溶液褪色
C.布洛芬的分子式为C12H18O2
D.布洛芬苯环上的一氯取代产物有四种
5.下列关于有机物的叙述正确的是
A.液化石油气、汽油和石蜡的主要成分都是碳氢化合物
B.环己烷与苯可用酸性溶液鉴别
C.由合成的聚合物为
D.能与溶液反应且分子式为的有机物一定是羧酸
6.维通氟橡胶的耐高温和耐化学性能是闻名的,它可用于飞机结构密封件、电气涂层和护套、海绵衬垫等。其结构简式为:,则合成它的单体为
A. B.
C.和 D.CH2=CF2和CF2=CF-CF3
7.有科学研究提出:锂电池负极材料(Li)由于生成LiH而不利于电池容量的保持。一定温度下,利用足量重水(D2O)与含LiH的Li负极材料反应,通过测定n(D2)/n(HD)可以获知 n(Li)/n(LiH)。
已知:①LiH+H2O=LiOH+H2↑
②2Li(s)+H2 2LiH △H<0
下列说法不正确的是
A.可用质谱区分D2和HD
B.Li与D2O的反应:2Li+2D2O=2LiOD+D2↑
C.若n(Li)/n(LiH)越大,则n(D2)/n(HD)越小
D.80℃反应所得n(D2)/n(HD)比25℃反应所得n(D2)/n(HD)大
8.聚维酮碘的水溶液是一种常见的碘伏类缓释消毒剂,聚维酮通过氢键与HI3形成聚维酮碘,其结构表示如图(图中虚线表示氢键)下列说法不正确的是
A.聚维酮的单体是
B.聚维酮分子由(2m+n)个单体聚合而成
C.聚维酮碘是一种水溶性物质
D.聚维酮的单体能发生水解反应,也能发生加聚、消去、加成、取代反应
9.姜黄素是从姜黄根茎中提取得到的一种黄色食用色素。下列关于姜黄素说法正确的是
A.分子式为C21H22O6 B.分子中存在手性碳原子
C.分子中存在4种含氧官能团 D.既能发生取代反应,又能发生加成反应
10.硫酸盐(含、)气溶胶是PM2.5的成分之一、近期科研人员把出了雾霾微颗粒中硫酸盐生成的三个阶段的转化机理,其主要过程示意图如下,下列说法错误的是
A.第I阶段的化学方程式为:+NO2=+
B.该过程中NO2为催化剂
C.1mol在第II、III两个阶段共失去电子数目为NA
D.氧化性NO2>HNO2
11.下列说法正确的是
A.某有机物燃烧只生成CO2和H2O,且二者物质的量相等,则此有机物的组成为CnH2n
B.相同物质的量的乙烯和乙醇完全燃烧,乙醇消耗的氧气多
C.CH4和C2H4的混合气体与足量O2完全反应,反应前后气体体积一定不变(气体体积在同一温度和压强下测量)
D.相同质量的烃完全燃烧,烃中氢的百分含量越高,消耗O2越多
12.下列说法正确的是
A.丙烷分子的空间填充模型为:
B.羟基中氢原子的活泼性:乙酸>水>乙醇
C.聚丙烯的结构简式:
D.丙烯中所有原子可能共平面
13.如图所示物质是某药物的中间体。关于该化合物的说法错误的是
A.该物质既能发生加成反应又能发生消去反应
B.该物质存在顺反异构体
C.分子中含有3种含氧官能团
D.1mol该物质最多能与4molNaOH反应
二、非选择题(共10题)
14.某有机化合物经李比希法测得其中含碳的质量分数为54.5%、含氢的质量分数为9.1%,其余为氧。用质谱法分析知该有机物的相对分子质量为88.请回答下列有关问题:
(1)该有机物的分子式为_______。
(2)若该有机物的水溶液呈酸性,且结构中不含支链,则其核磁共振氢谱图中的峰面积之比为_______。
(3)若实验测得该有机物中不含结构,利用红外光谱仪测得该有机物的红外光谱如图所示。则该有机物的结构简式可能是_______、_______(写出两种即可)。
15.卤代烃在不同溶液中会发生不同类型的反应。请回答下列问题:
(1)向盛有1mL溴乙烷的试管中加入2mL 5%的NaOH溶液,加热,发生反应的化学方程式为_______。某同学取少量反应后的混合溶液,向其中滴加溶液,产生少量沉淀。该同学由此得出溴乙烷与NaOH水溶液反应生成了溴化钠,你认为他的结论_______(填“合理”或“不合理”),理由是_______。
(2)某同学在圆底烧瓶中加入2.0g NaOH和15mL无水乙醇,搅拌,再加入5mL 1-溴丁烷和几片碎瓷片,微热(液体沸腾后,移开酒精灯)。产生的气体通过盛有水的试管后,再通入盛有酸性溶液的试管中,观察到溶液紫红色逐渐褪去。
已知:溴乙烷的沸点:38.4℃,1-溴丁烷的沸点:101.6℃。
①该同学用溴乙烷代替1-溴丁烷进行实验时,发现酸性溶液不褪色。由已知沸点差异分析实验失败的原因可能是_______。
②实验后检验出反应产物中含有丁烯,但不能说明该条件下没有发生取代反应。若进一步检验是否生成1-丁醇,可采用的方法是_______(填字母)。
a.对产物进行红外光谱分析
b.对产物进行核磁共振氢谱分析
c.使反应混合物与金属钠反应
(3)写出2-溴-2-甲基丙烷发生消去反应的化学方程式:_______。
16.以乙烯为基本原料,合成六元环状化合物D的反应如下所示(部分试剂、产物及反应条件略去):
请写出各步反应的化学方程式和反应类型___________。
17.现有某有机化合物样品,对其进行如下操作:
i.充分燃烧6.51g该样品,得到20.47g二氧化碳和8.36g水。
ii.质谱分析得该物质的相对分子质量为84,
(1)该有机化合物的分子式为_______。
(2)向该有机化合物中加入少量溴的四氯化碳溶液,溶液褪色,用酸性溶液氧化该物质只能得到丙酸,该有机化合物的结构简式为_______。
18.(1)有两种有机物都含有碳92.3%,含有氢7.7%,第一种有机物对氢气的相对密度为13,第二种有机物的密度为3.49g/L(标准状况下),则第一种有机物的结构简式为___,第二种有机物的分子式为___。
(2)某仅由C、H、O三种元素组成的有机化合物,经测定相对分子质量为90,取该有机化合物样品1.8g,在纯氧中完全燃烧将产物先后通过浓硫酸和碱石灰,两者分别增重1.08g和2.64g,则该有机化合物分子式为___。
19.苯酚、甲醛溶液、浓盐酸在沸水浴条件下可制得酚醛树脂,实验室制取酚醛树脂的装置如图所示:
(1)试管上方长玻璃管的作用是___________。
(2)浓盐酸的作用是___________。
(3)此反应需水浴加热,不用温度计控制水浴温度的原因是___________。
(4)实验完毕后,若试管不易用水洗净,可以加入少量___________浸泡几分钟后,再洗净。
(5)写出实验室制取酚醛树脂的化学方程式___________,该有机反应类型是___________。
20.已知反应:,实验室用如图所示装置制备溴乙烷(沸点为38.4℃,密度为)。实验前先向仪器a中加入10g乙醇和足量浓硫酸,然后加入研细的20.6gNaBr。
(1)加入碎瓷片的作用是_______。
(2)试管d中出现的实验现象是_______。
(3)反应结束后,试管d中含少量杂质,为了除去粗产品中的杂质,可选用的试剂是_______(填字母)。
A.苯 B. C.溶液 D.
(4)经过分离、提纯、干燥后,该实验最终得到10.9g溴乙烷,则本实验中溴乙烷的产率为_______。
(5)通过以下实验步骤可检验溴乙烷中的溴元素,其正确的操作顺序是_______(填序号)。
①加热 ②加入溶液 ③加入稀酸化 ④加入溶液 ⑤冷却 ⑥取少量溴乙烷
21.某同学为确定某分子式为C2H6O2的液态有机物X的结构,准备按下列程序进行:
(1)查阅资料。已知:一个碳原子上连两个羟基()的物质不稳定。
(2)预测。若分子中不存在过氧键(-O-O-),则X的结构简式可能是:_____。
(3)设计实验方案验证X的结构。取一定量X与足量钠反应,通过测定生成氢气的体积来确定X分子中能与金属钠反应的氢原子数目,进而确定X的结构。若取6.2gX与足量金属钠反应,测得在标准状况下生成H22.24L,对应X的名称为:_____。
(4)根据实验方案讲行实验.
①选取如图仪器(胶管和固定装置略去,必要试剂自选),接口连接顺序为:_____。
②如何检验整套装置气密性 _____
③请指出能使实验比较安全、准确进行的关键实验步骤_____(至少指出两个关键步骤)。
22.某相对分子质量为40的链状不饱和烃A,能发生如图转化:
已知:①羟基所连接的碳原子上无氢原子时,难以发生催化氧化;②E能与NaHCO3溶液反应产生气体;③F为酯类化合物。
(1)A的分子式为____,A转化为B的反应类型为____,C转化为D的反应条件为____。
(2)B中所含有的官能团的名称为____,B中共平面的原子最多有____个。
(3)写出D转化为E的化学方程式:____。
(4)与E互为同分异构体的芳香族化合物K,已知:①K与E具有相同的官能团;②K不能与FeCl3溶液发生显色反应;③K有二个取代基,则符合上述条件的K共有___种。
(5)F的结构简式为_____。
23.物质F是一种芳香酯,常用作调香剂,其合成路线如下图所示:
已知E中含有两个甲基,请回答下列问题:
(1)物质A的名称是_______。
(2)各取1 mol物质D分别与足量Na、NaOH溶液、NaHCO3溶液反应,消耗的Na、NaOH、NaHCO3的物质的量之比为_______。
(3)物质A到F中除D以外含有手性碳原子的物质是_______(填标号)。
(4)B→C的反应方程式是_______。
(5)E的同分异构体中与其含有相同种类官能团的有_______种(不含E本身)。
参考答案:
1.A 2.B 3.C 4.A 5.A 6.D 7.C 8.D 9.D 10.B 11.D 12.B
13.D
14. 3:2:2:1
15.(1) 不合理 没有用硝酸进行酸化,排除的干扰
(2) 溴乙烷沸点低,加热时没有充分反应就挥发出去 ab
(3)
16.A→B:CH2=CH2+Br2CH2BrCH2Br,加成反应;B→C:CH2BrCH2Br+2 H2O CH2OHCH2OH+2HBr,取代反应;C→D:2 CH2OHCH2OH +H2O,取代反应
17.(1)C6H12
(2)CH3CH2CH=CHCH2CH3
18. CH≡CH C6H6 C3H6O3
19. 导气、冷凝回流 作催化剂 该反应的条件是沸水浴加热 乙醇 n+n +(n-1)H2O 缩聚反应
20.(1)防止液体暴沸
(2)液体分层,下层为油状液体
(3)C
(4)50%
(5)⑥④①⑤③②
21. CH3-O-CH2-OH、CH2OH-CH2OH 乙二醇 a、c、b、d、e、f 连接好仪器,关闭分液漏斗活塞,在量筒(水槽)中加水至浸没导管口,微热烧瓶,导管口有气泡产生,停止加热,导管内有一段水柱产生,说明气密性良好 检查实验装置的气密性;加入稍过量的金属钠;从漏斗中缓慢滴加X;待实验装置冷却后再读数;上下移动量筒,使其中液面与广口瓶中液面相平;视线与凹液面的最低点水平,读取量筒中水的体积
22.(1) C3H4 加成反应 NaOH的水溶液/加热
(2) 碳碳双键 17
(3)+O2+H2O
(4)12
(5)
23. 2-甲基-1-丁烯 2:1:1 BC 7
