人教版(2019)必修二 7.3.2 乙酸 课件(共27张PPT)
文档属性
| 名称 | 人教版(2019)必修二 7.3.2 乙酸 课件(共27张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 2.5MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-06-15 00:00:00 | ||
图片预览







文档简介
(共27张PPT)
第七章 有机化合物
乙酸
第二课时
乙酸
学习目标
1. 掌握乙酸的结构及其主要性质与应用,
2.认识有机化合物中的羧基与其性质的关系。
食醋中含有3%~5%的乙酸
任务一:简述乙酸的物理性质
乙酸俗称醋酸,是一种有强烈刺激性气味的无色液体,易溶于水和乙醇。
熔点:16.6 ℃,温度低于熔点时,乙酸凝结成晶体,所以纯净的乙酸又称冰醋酸。
C2H4O2
CH3COOH
—COOH
任务二:探究乙酸的组成和结构
1、下列说法正确的是( )
A.乙酸中含有双键,因此属于不饱和烃
B.在标准状况下醋酸是一种无色有强烈刺激性气味的液体C.乙酸分子中含有 和—OH两种官能团
D.乙酸的结构简式可以写成CH3COOH
D
课堂练习
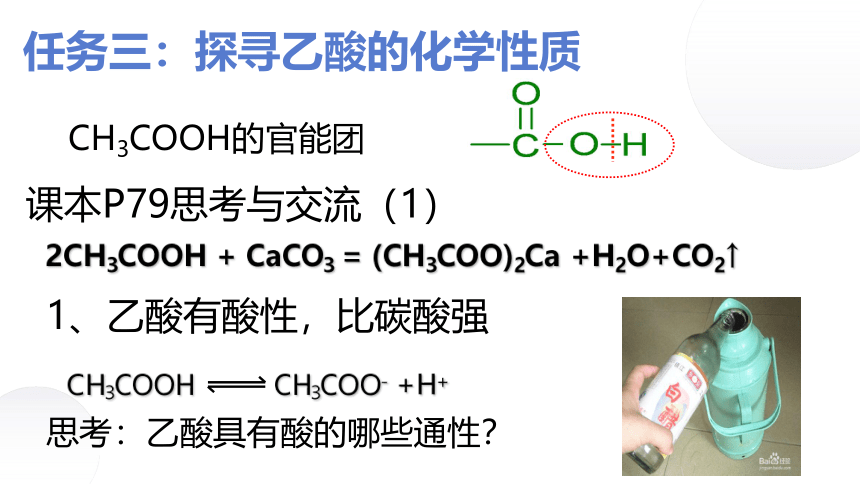
任务三:探寻乙酸的化学性质
CH3COOH的官能团
课本P79思考与交流(1)
2CH3COOH + CaCO3 = (CH3COO)2Ca +H2O+CO2↑
1、乙酸有酸性,比碳酸强
CH3COOH CH3COO- +H+
思考:乙酸具有酸的哪些通性?
乙酸能使紫色石蕊溶液变红
①与指示剂反应
②与金属反应(Na)
③与碱性氧化物反应(CuO)
④与碱反应(NaOH)
⑤与盐反应(Na2CO3)
2Na + 2CH3COOH → 2CH3COONa + H2↑
CuO + 2CH3COOH → (CH3COO)2Cu + H2O
NaOH+ CH3COOH → CH3COONa + H2O
Na2CO3 + 2CH3COOH → 2CH3COONa + CO2↑+ H2O
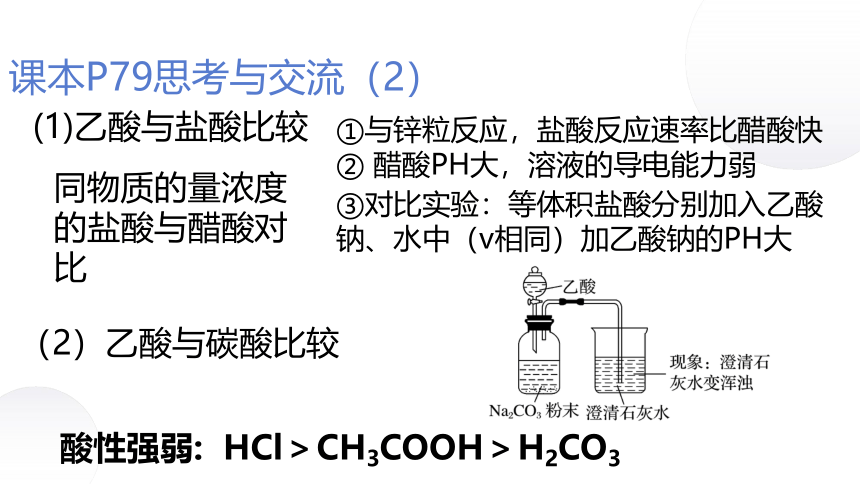
课本P79思考与交流(2)
(2)乙酸与碳酸比较
(1)乙酸与盐酸比较
①与锌粒反应,盐酸反应速率比醋酸快
② 醋酸PH大,溶液的导电能力弱
同物质的量浓度的盐酸与醋酸对比
③对比实验:等体积盐酸分别加入乙酸钠、水中(v相同)加乙酸钠的PH大
酸性强弱: HCl>CH3COOH>H2CO3
2.下列物质中,能与醋酸发生反应的是( )
①乙醇 ②金属铝 ③甲烷④碳酸钙 ⑤氢氧化钠⑥ 氧化镁
A.①③④⑤⑥ B.②③④⑤
C. ①②④⑤⑥ D.全部
C
课堂练习
3.下列物质都能与金属钠反应放出H2,产生H2的速率由大到小的顺序正确的是( )
①C2H5OH ②水 ③醋酸溶液
A.①>②>③ B.②>①>③
C.③>②>① D.③>①>②
C
羟基氢的活泼性:CH3COOH>H2O>C2H5OH
课堂练习
“酒是陈的香”
“美味佳肴”
有腥味的鱼
无腥、香醇,特别鲜美
任务四:探寻乙酸在生活中的应用
酯化反应(取代反应):酸和醇起作用,生成酯和水的反应。
酯化反应是可逆反应,乙酸乙酯会与水反应生成酸和醇。
酸 + 醇 酯 + 水
注意:可逆反应
CH3COOH+HOC2H5
CH3COOC2H5+H2O
2.乙酸的酯化反应
酯化反应的可能的两种脱水方式
1、
2、
同位素示踪法:
----研究有机反应机理常用的方法
酸脱羟基、醇脱氢(羟基上的)
实质:
4.Na2CO3溶液试管中导管不能插入溶液中
酯化反应注意的问题:
3.碎瓷片的作用
防暴沸
防倒吸
1.药品的装入顺序如何?试管倾斜加热的目的是什么
乙醇→浓硫酸→(冷却后)乙酸
增大受热面积
2.浓硫酸的作用是什么?
催化剂、吸水剂
5.得到的反应产物主要杂质有哪些?
6.用饱和Na2CO3溶液接收的作用
乙酸、乙醇
① 中和乙酸
② 吸收乙醇
③ 降低酯在水中的溶解度
4.白酒密封储存在地窖里,时间越长越香,形成这种香味效果的主要物质是( )
A.醇类物质 B.酯类物质
C.酸类物质 D.盐类物质
B
课堂练习
5.某研究小组用如图所示装置制取乙酸乙酯,请回答下列问题:
(1)为防止试管a中液体实验时发生暴沸,加热前应采取的措施为___________________。
加入碎瓷片(或沸石)
(2)装置中的球形漏斗除起冷凝作用外,它的另一重要作用是__________。
防止倒吸
(3)试管b中饱和碳酸钠溶液的作用除了溶解乙醇,还有_______________,_____________________。
中和乙酸
降低乙酸乙酯的溶解度
课堂练习
(4)待试管b收集到一定量产物后停止加热,撤去试管b并用力振荡试管b,静置后试管b中所观察到的实验现象:_________________________________,要分离试管中的液体混合物,采用的方法为_____。
分层,上层为无色有香味的油状液体
分液
(5)如果用含示踪原子18O的乙醇参与反应,生成的产物中,只有乙酸乙酯中含有18O,则酯化反应中,乙酸和乙醇分子中断裂的各是什么键,在方
程式中表示出其断键部位:_______________________________________。
含酯的物质
四、酯
草莓中含有乙酸乙酯和乙酸异戊酯,苹果中含有戊酸戊酯等
1. 酯的官能团是_________________
酯基
2. 酯一般密度比水小,难溶于水,易溶于乙醇、乙醚等有机溶剂,低级酯是具有芳香气味的液体。
—COOR
3.酯的用途:用作饮料、糖果、香水、化妆品中的香料;也可以用作指甲油、胶水的溶剂。
乙酸
乙醇
乙酸乙酯
某酸
某醇
某酸某酯
羧酸 + 醇 酯 + 水
举例
推广
4.命名
5.化学性质——水解反应
甲酸甲酯
请说出下列酯的名称及水解产物:
HCOOCH3
CH3COOCH3
CH3CH2COOC2H5
丙酸乙酯
乙酸甲酯
任务五:理解官能团及有机化合物的分类
有机化合物类别 官能团 代表物
烃 烷烃 - CH4甲烷
烯烃 ___________________ ___________乙烯
炔烃 __________________ ________乙炔
芳香烃 - 苯
碳碳双键
CH2==CH2
—C≡C—碳碳三键
CH≡CH
烃的 衍生物 卤代烃 ________________ (X表示卤素原子) __________溴乙烷
醇 __________ CH3CH2OH乙醇
醛 _____________
____________乙醛
羧酸 _______________
______________乙酸
酯 _________________
乙酸乙酯
碳卤键
CH3CH2Br
—OH羟基
醛基
羧基
酯基
(12)
(13)
(14)
(15)
烷烃
烷烃
烯烃
烯烃
炔烃
炔烃
卤代烃
卤代烃
醇
醇
羧酸
芳香烃
芳香烃
环烷烃
环烷烃
(1)CH4
CH3
(2)CH3CHCH2CH3
(3)CH2=CH2
CH3
(4)CH3-C=CHCH3
(5)CH≡CH
(6)CH3C≡CH
(7)CH3-Cl
(8)CH3CH2Br
(9)CH3OH
(10)CH3CH2OH
CH3
(11)CH3COH
O
按官能团对这些化合物进行分类:
6.脱落酸是一种抑制生长
的植物激素,因能促使叶
子脱落而得名,其结构简式
如图所示,试回答下列问题。
(1)脱落酸的分子式为________,分子中所含官能团
除羰基( )外还有_____________________(写名称)。
C15H20O4
碳碳双键、羟基、羧基
课堂练习
(2)根据脱落酸的结构简式,下列关于
脱落酸的性质说法正确的是______。
A.脱落酸既可以和乙醇,也可以和乙酸发生酯化反应
B.1 mol脱落酸和足量的钠反应生成2 mol H2
C.脱落酸可以使溴的四氯化碳溶液褪色
D.1 mol脱落酸最多可以和2 mol Br2发生加成反应
E.脱落酸可以和NaOH发生中和反应,且1 mol脱落酸最多需要消耗2 mol NaOH
AC
一、乙酸的结构
二、乙酸的物理性质
三、乙酸的化学性质
1.酸的通性
2.酯化反应
课堂小结
四、酯
五、根据官能团对有机物进行分类
第七章 有机化合物
乙酸
第二课时
乙酸
学习目标
1. 掌握乙酸的结构及其主要性质与应用,
2.认识有机化合物中的羧基与其性质的关系。
食醋中含有3%~5%的乙酸
任务一:简述乙酸的物理性质
乙酸俗称醋酸,是一种有强烈刺激性气味的无色液体,易溶于水和乙醇。
熔点:16.6 ℃,温度低于熔点时,乙酸凝结成晶体,所以纯净的乙酸又称冰醋酸。
C2H4O2
CH3COOH
—COOH
任务二:探究乙酸的组成和结构
1、下列说法正确的是( )
A.乙酸中含有双键,因此属于不饱和烃
B.在标准状况下醋酸是一种无色有强烈刺激性气味的液体C.乙酸分子中含有 和—OH两种官能团
D.乙酸的结构简式可以写成CH3COOH
D
课堂练习
任务三:探寻乙酸的化学性质
CH3COOH的官能团
课本P79思考与交流(1)
2CH3COOH + CaCO3 = (CH3COO)2Ca +H2O+CO2↑
1、乙酸有酸性,比碳酸强
CH3COOH CH3COO- +H+
思考:乙酸具有酸的哪些通性?
乙酸能使紫色石蕊溶液变红
①与指示剂反应
②与金属反应(Na)
③与碱性氧化物反应(CuO)
④与碱反应(NaOH)
⑤与盐反应(Na2CO3)
2Na + 2CH3COOH → 2CH3COONa + H2↑
CuO + 2CH3COOH → (CH3COO)2Cu + H2O
NaOH+ CH3COOH → CH3COONa + H2O
Na2CO3 + 2CH3COOH → 2CH3COONa + CO2↑+ H2O
课本P79思考与交流(2)
(2)乙酸与碳酸比较
(1)乙酸与盐酸比较
①与锌粒反应,盐酸反应速率比醋酸快
② 醋酸PH大,溶液的导电能力弱
同物质的量浓度的盐酸与醋酸对比
③对比实验:等体积盐酸分别加入乙酸钠、水中(v相同)加乙酸钠的PH大
酸性强弱: HCl>CH3COOH>H2CO3
2.下列物质中,能与醋酸发生反应的是( )
①乙醇 ②金属铝 ③甲烷④碳酸钙 ⑤氢氧化钠⑥ 氧化镁
A.①③④⑤⑥ B.②③④⑤
C. ①②④⑤⑥ D.全部
C
课堂练习
3.下列物质都能与金属钠反应放出H2,产生H2的速率由大到小的顺序正确的是( )
①C2H5OH ②水 ③醋酸溶液
A.①>②>③ B.②>①>③
C.③>②>① D.③>①>②
C
羟基氢的活泼性:CH3COOH>H2O>C2H5OH
课堂练习
“酒是陈的香”
“美味佳肴”
有腥味的鱼
无腥、香醇,特别鲜美
任务四:探寻乙酸在生活中的应用
酯化反应(取代反应):酸和醇起作用,生成酯和水的反应。
酯化反应是可逆反应,乙酸乙酯会与水反应生成酸和醇。
酸 + 醇 酯 + 水
注意:可逆反应
CH3COOH+HOC2H5
CH3COOC2H5+H2O
2.乙酸的酯化反应
酯化反应的可能的两种脱水方式
1、
2、
同位素示踪法:
----研究有机反应机理常用的方法
酸脱羟基、醇脱氢(羟基上的)
实质:
4.Na2CO3溶液试管中导管不能插入溶液中
酯化反应注意的问题:
3.碎瓷片的作用
防暴沸
防倒吸
1.药品的装入顺序如何?试管倾斜加热的目的是什么
乙醇→浓硫酸→(冷却后)乙酸
增大受热面积
2.浓硫酸的作用是什么?
催化剂、吸水剂
5.得到的反应产物主要杂质有哪些?
6.用饱和Na2CO3溶液接收的作用
乙酸、乙醇
① 中和乙酸
② 吸收乙醇
③ 降低酯在水中的溶解度
4.白酒密封储存在地窖里,时间越长越香,形成这种香味效果的主要物质是( )
A.醇类物质 B.酯类物质
C.酸类物质 D.盐类物质
B
课堂练习
5.某研究小组用如图所示装置制取乙酸乙酯,请回答下列问题:
(1)为防止试管a中液体实验时发生暴沸,加热前应采取的措施为___________________。
加入碎瓷片(或沸石)
(2)装置中的球形漏斗除起冷凝作用外,它的另一重要作用是__________。
防止倒吸
(3)试管b中饱和碳酸钠溶液的作用除了溶解乙醇,还有_______________,_____________________。
中和乙酸
降低乙酸乙酯的溶解度
课堂练习
(4)待试管b收集到一定量产物后停止加热,撤去试管b并用力振荡试管b,静置后试管b中所观察到的实验现象:_________________________________,要分离试管中的液体混合物,采用的方法为_____。
分层,上层为无色有香味的油状液体
分液
(5)如果用含示踪原子18O的乙醇参与反应,生成的产物中,只有乙酸乙酯中含有18O,则酯化反应中,乙酸和乙醇分子中断裂的各是什么键,在方
程式中表示出其断键部位:_______________________________________。
含酯的物质
四、酯
草莓中含有乙酸乙酯和乙酸异戊酯,苹果中含有戊酸戊酯等
1. 酯的官能团是_________________
酯基
2. 酯一般密度比水小,难溶于水,易溶于乙醇、乙醚等有机溶剂,低级酯是具有芳香气味的液体。
—COOR
3.酯的用途:用作饮料、糖果、香水、化妆品中的香料;也可以用作指甲油、胶水的溶剂。
乙酸
乙醇
乙酸乙酯
某酸
某醇
某酸某酯
羧酸 + 醇 酯 + 水
举例
推广
4.命名
5.化学性质——水解反应
甲酸甲酯
请说出下列酯的名称及水解产物:
HCOOCH3
CH3COOCH3
CH3CH2COOC2H5
丙酸乙酯
乙酸甲酯
任务五:理解官能团及有机化合物的分类
有机化合物类别 官能团 代表物
烃 烷烃 - CH4甲烷
烯烃 ___________________ ___________乙烯
炔烃 __________________ ________乙炔
芳香烃 - 苯
碳碳双键
CH2==CH2
—C≡C—碳碳三键
CH≡CH
烃的 衍生物 卤代烃 ________________ (X表示卤素原子) __________溴乙烷
醇 __________ CH3CH2OH乙醇
醛 _____________
____________乙醛
羧酸 _______________
______________乙酸
酯 _________________
乙酸乙酯
碳卤键
CH3CH2Br
—OH羟基
醛基
羧基
酯基
(12)
(13)
(14)
(15)
烷烃
烷烃
烯烃
烯烃
炔烃
炔烃
卤代烃
卤代烃
醇
醇
羧酸
芳香烃
芳香烃
环烷烃
环烷烃
(1)CH4
CH3
(2)CH3CHCH2CH3
(3)CH2=CH2
CH3
(4)CH3-C=CHCH3
(5)CH≡CH
(6)CH3C≡CH
(7)CH3-Cl
(8)CH3CH2Br
(9)CH3OH
(10)CH3CH2OH
CH3
(11)CH3COH
O
按官能团对这些化合物进行分类:
6.脱落酸是一种抑制生长
的植物激素,因能促使叶
子脱落而得名,其结构简式
如图所示,试回答下列问题。
(1)脱落酸的分子式为________,分子中所含官能团
除羰基( )外还有_____________________(写名称)。
C15H20O4
碳碳双键、羟基、羧基
课堂练习
(2)根据脱落酸的结构简式,下列关于
脱落酸的性质说法正确的是______。
A.脱落酸既可以和乙醇,也可以和乙酸发生酯化反应
B.1 mol脱落酸和足量的钠反应生成2 mol H2
C.脱落酸可以使溴的四氯化碳溶液褪色
D.1 mol脱落酸最多可以和2 mol Br2发生加成反应
E.脱落酸可以和NaOH发生中和反应,且1 mol脱落酸最多需要消耗2 mol NaOH
AC
一、乙酸的结构
二、乙酸的物理性质
三、乙酸的化学性质
1.酸的通性
2.酯化反应
课堂小结
四、酯
五、根据官能团对有机物进行分类
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
