8.1.1海水资源的综合利用 课件(共22张ppt)化学人教版(2019)必修第二册
文档属性
| 名称 | 8.1.1海水资源的综合利用 课件(共22张ppt)化学人教版(2019)必修第二册 |  | |
| 格式 | pptx | ||
| 文件大小 | 11.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-06-15 23:24:26 | ||
图片预览





文档简介
(共22张PPT)
第2课时 海水资源的综合利用
第八章 化学与可持续发展 第一节 自然资源的开发利用
金属矿物
海水资源
化石燃料
学习目标
学习重点
海水中化学资源的开发利用。
.掌握海水中化学资源的开发利用。
学习难点
掌握海水提溴、提镁等工艺流程。
引言
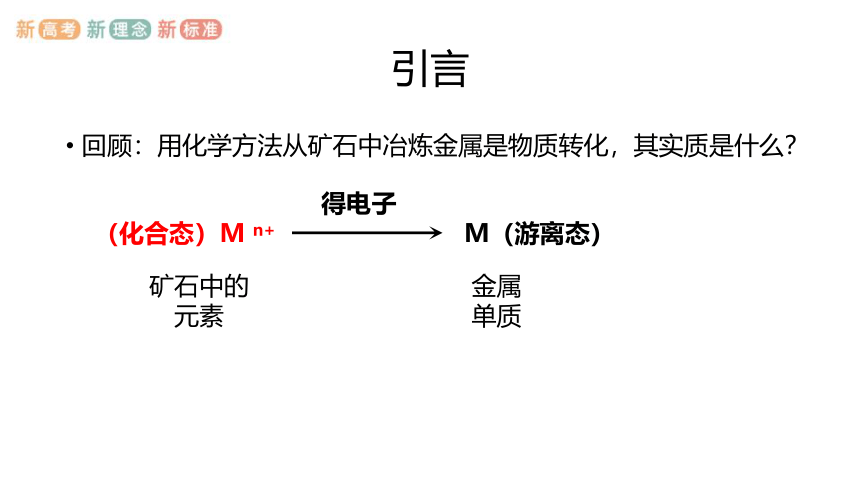
回顾:用化学方法从矿石中冶炼金属是物质转化,其实质是什么?
(化合态)M n+
得电子
M(游离态)
矿石中的
元素
金属单质
引言
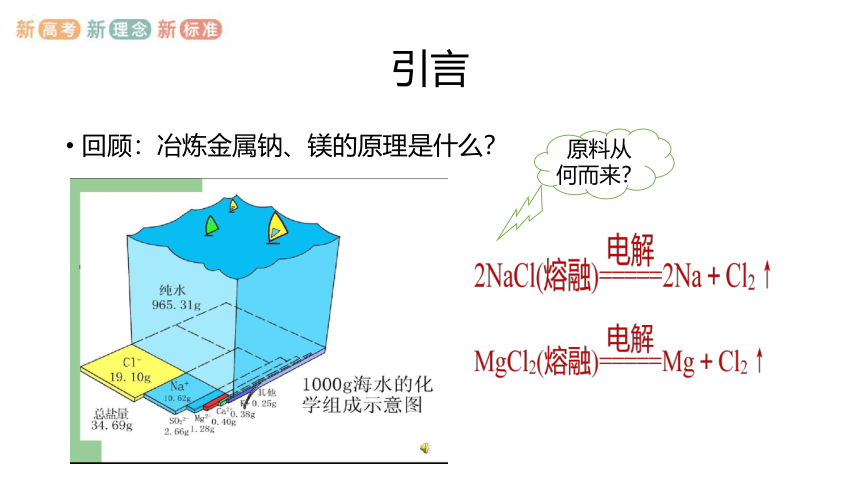
回顾:冶炼金属钠、镁的原理是什么?
原料从何而来?
(1)海水制盐
盐田
海水
饱和食盐水
引入
日晒风吹
析出
粗盐
食用盐
氯碱工业
精制
海水资源与化工生产
母液
“母液”也叫“苦卤”,含有高浓度的K+、Mg2+、Br-和SO42-等,可从中提取多种化工原料。
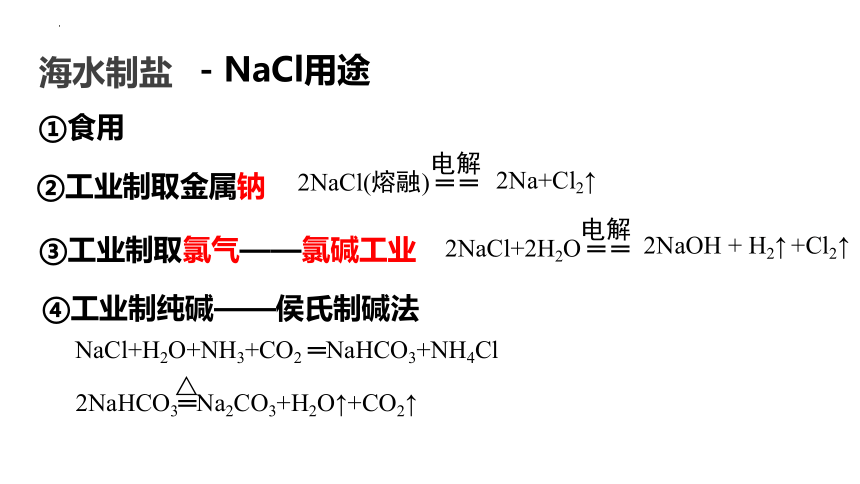
- NaCl用途
海水制盐
2NaCl(熔融) ═ ═
电解
2Na+Cl2↑
2NaCl+2H2O ═ ═
电解
2NaOH + H2↑ +Cl2↑
②工业制取金属钠
③工业制取氯气——氯碱工业
④工业制纯碱——侯氏制碱法
2NaHCO3═Na2CO3+H2O↑+CO2↑
△
①食用
NaCl+H2O+NH3+CO2 ═NaHCO3+NH4Cl
典例2.
海水是一个巨大的化学资源宝库,下列有关海水综合利用的说法正确的是( )
A.海水中含有钾元素,只需经过物理变化就可以得到钾单质
B.海水蒸发制海盐的过程中只发生了化学变化
C.从海水中可以得到NaCl,电解熔融NaCl可制备Cl2
D.利用潮汐发电是将化学能转化为电能
【答案】C
【解析】海水中的钾元素是以化合态形式存在,要求化合态转化为游离态,一定发生氧化还原反应,A不正确;海水蒸发制海盐,是发生了物理变化,B错误;电解熔融NaCl可以制得Na和Cl2,C正确;潮汐发电是将机械能转化为电能,因此D也不正确。
课堂练习
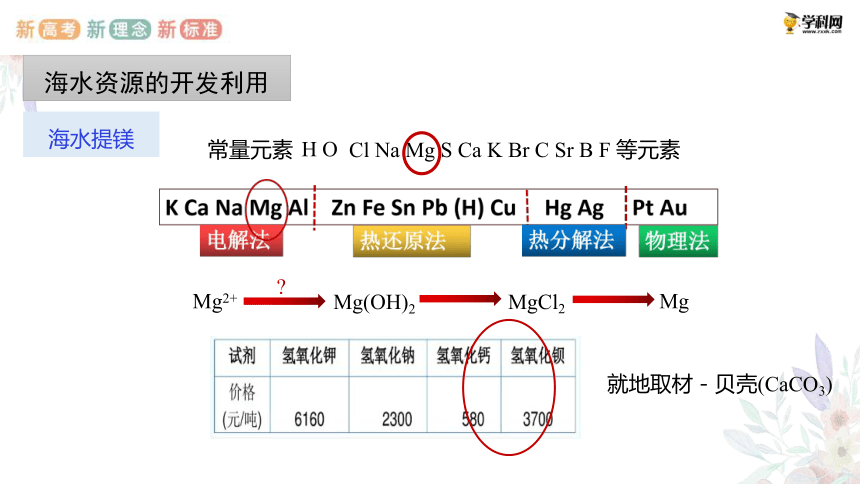
海水资源的开发利用
海水提镁
H O
Cl Na Mg S Ca K Br C Sr B F 等元素
常量元素
Mg2+
Mg
MgCl2
Mg(OH)2
就地取材-贝壳(CaCO3)
二.海水资源的开发利用
(1)海水提镁
写出有关方程式?
?
二.海水资源的开发利用
①
高温
CaCO3 CaO+CO2↑
CaO+H2O===Ca(OH)2
②
③ MgCl2+Ca(OH)2===Mg(OH)2+CaCl2
④ Mg(OH)2+2HCl===MgCl2+2H2O
⑤
高温
MgCl2·6H2O MgCl2+6H2O
MgCl2 (熔融) Mg + Cl2 ↑
电解
⑥
典例5.
下表是氧化镁和氯化镁的熔、沸点数据:
请参考以上数据分析,从海水中提取镁,正确的方法是( )
【答案】D
课堂练习
物质 氧化镁 氯化镁
熔点/℃ 2 852 714
沸点/℃ 3 600 1 412
酸和Cl2
海水Br-
Br2
氧化室
1
2
3
4
空气
SO2和H2O
Cl2
吹出塔
吸收塔
蒸馏塔
工业生产流程图
海水中溴元素以Br-形式存在,工业上用空气吹出法从海水中提取溴的工艺流程图如下所示:
(1)步骤①反应的离子方程式是_____________________________________。
(2)步骤③反应的化学方程式是______________________________________。
(3)步骤②中,用热空气将Br2吹出,利用溴的性质为______________,从步骤②到步骤④的目的是____________________________________。
2Br-+Cl2=Br2+2Cl-
SO2+Br2+2H2O=H2SO4+2HBr
易挥发
将溴浓缩,提高Br2的提取率
(4)从理论上考虑,下列物质也能充分吸收Br2的是________(填字母)。
A.NaOH B.FeCl2 C.Na2SO3 D.H2O
(5)步骤⑤蒸馏过程中,温度应控制在80~90 ℃。温度过高或过低都不利于生产,若温度过高,大量水蒸气随溴排出,溴蒸气中水分增加;若温度过低,则___________________________________。
ABC
溴不能完全蒸出,产率太低
二、海水资源的开发利用
观看实验视频,回答下列问题
实验现象:
加入H2O2溶液后,溶液由无色变为黄色;
( I2的水溶液为深黄色)
加入淀粉溶液后,溶液又变为蓝色。
实验原理:
(离子方程式表示)
2I-+H2O2+2H+= I2+2H2O
实验结论:
海带中有碘元素
海水资源的开发利用
海带提碘
晒干
灼烧
①加水
②加热
滴入H2O2
(H+,aq)
淀粉
海带灰
海带
含I-水溶液
变蓝色
I2、H2O
提取碘
I2的CCl4溶液
单质I2
典例4.
从海带中提取碘的实验过程中,涉及到下列操作,其中正确的是( )
【答案】D
【解析】物质的灼烧应该选用耐高温的坩埚,A错;过滤操作时,向漏斗中加液要用玻璃棒引流,B错;碘的苯溶液在上层,应由分液漏斗的上口倒出,C错;固液分离可以用蒸馏法分离,D对。
课堂练习
3、海水资源的其他利用
(1)从海水中提取铀和重水,用于核能开发。
(2)开发潮汐能、波浪能等新型能源。
海水资源
海水化学资源的开发利用
海水提镁
海水提溴
海带提碘
海水制盐
浓缩海水
课堂小结
谢谢观看
第2课时 海水资源的综合利用
第八章 化学与可持续发展 第一节 自然资源的开发利用
金属矿物
海水资源
化石燃料
学习目标
学习重点
海水中化学资源的开发利用。
.掌握海水中化学资源的开发利用。
学习难点
掌握海水提溴、提镁等工艺流程。
引言
回顾:用化学方法从矿石中冶炼金属是物质转化,其实质是什么?
(化合态)M n+
得电子
M(游离态)
矿石中的
元素
金属单质
引言
回顾:冶炼金属钠、镁的原理是什么?
原料从何而来?
(1)海水制盐
盐田
海水
饱和食盐水
引入
日晒风吹
析出
粗盐
食用盐
氯碱工业
精制
海水资源与化工生产
母液
“母液”也叫“苦卤”,含有高浓度的K+、Mg2+、Br-和SO42-等,可从中提取多种化工原料。
- NaCl用途
海水制盐
2NaCl(熔融) ═ ═
电解
2Na+Cl2↑
2NaCl+2H2O ═ ═
电解
2NaOH + H2↑ +Cl2↑
②工业制取金属钠
③工业制取氯气——氯碱工业
④工业制纯碱——侯氏制碱法
2NaHCO3═Na2CO3+H2O↑+CO2↑
△
①食用
NaCl+H2O+NH3+CO2 ═NaHCO3+NH4Cl
典例2.
海水是一个巨大的化学资源宝库,下列有关海水综合利用的说法正确的是( )
A.海水中含有钾元素,只需经过物理变化就可以得到钾单质
B.海水蒸发制海盐的过程中只发生了化学变化
C.从海水中可以得到NaCl,电解熔融NaCl可制备Cl2
D.利用潮汐发电是将化学能转化为电能
【答案】C
【解析】海水中的钾元素是以化合态形式存在,要求化合态转化为游离态,一定发生氧化还原反应,A不正确;海水蒸发制海盐,是发生了物理变化,B错误;电解熔融NaCl可以制得Na和Cl2,C正确;潮汐发电是将机械能转化为电能,因此D也不正确。
课堂练习
海水资源的开发利用
海水提镁
H O
Cl Na Mg S Ca K Br C Sr B F 等元素
常量元素
Mg2+
Mg
MgCl2
Mg(OH)2
就地取材-贝壳(CaCO3)
二.海水资源的开发利用
(1)海水提镁
写出有关方程式?
?
二.海水资源的开发利用
①
高温
CaCO3 CaO+CO2↑
CaO+H2O===Ca(OH)2
②
③ MgCl2+Ca(OH)2===Mg(OH)2+CaCl2
④ Mg(OH)2+2HCl===MgCl2+2H2O
⑤
高温
MgCl2·6H2O MgCl2+6H2O
MgCl2 (熔融) Mg + Cl2 ↑
电解
⑥
典例5.
下表是氧化镁和氯化镁的熔、沸点数据:
请参考以上数据分析,从海水中提取镁,正确的方法是( )
【答案】D
课堂练习
物质 氧化镁 氯化镁
熔点/℃ 2 852 714
沸点/℃ 3 600 1 412
酸和Cl2
海水Br-
Br2
氧化室
1
2
3
4
空气
SO2和H2O
Cl2
吹出塔
吸收塔
蒸馏塔
工业生产流程图
海水中溴元素以Br-形式存在,工业上用空气吹出法从海水中提取溴的工艺流程图如下所示:
(1)步骤①反应的离子方程式是_____________________________________。
(2)步骤③反应的化学方程式是______________________________________。
(3)步骤②中,用热空气将Br2吹出,利用溴的性质为______________,从步骤②到步骤④的目的是____________________________________。
2Br-+Cl2=Br2+2Cl-
SO2+Br2+2H2O=H2SO4+2HBr
易挥发
将溴浓缩,提高Br2的提取率
(4)从理论上考虑,下列物质也能充分吸收Br2的是________(填字母)。
A.NaOH B.FeCl2 C.Na2SO3 D.H2O
(5)步骤⑤蒸馏过程中,温度应控制在80~90 ℃。温度过高或过低都不利于生产,若温度过高,大量水蒸气随溴排出,溴蒸气中水分增加;若温度过低,则___________________________________。
ABC
溴不能完全蒸出,产率太低
二、海水资源的开发利用
观看实验视频,回答下列问题
实验现象:
加入H2O2溶液后,溶液由无色变为黄色;
( I2的水溶液为深黄色)
加入淀粉溶液后,溶液又变为蓝色。
实验原理:
(离子方程式表示)
2I-+H2O2+2H+= I2+2H2O
实验结论:
海带中有碘元素
海水资源的开发利用
海带提碘
晒干
灼烧
①加水
②加热
滴入H2O2
(H+,aq)
淀粉
海带灰
海带
含I-水溶液
变蓝色
I2、H2O
提取碘
I2的CCl4溶液
单质I2
典例4.
从海带中提取碘的实验过程中,涉及到下列操作,其中正确的是( )
【答案】D
【解析】物质的灼烧应该选用耐高温的坩埚,A错;过滤操作时,向漏斗中加液要用玻璃棒引流,B错;碘的苯溶液在上层,应由分液漏斗的上口倒出,C错;固液分离可以用蒸馏法分离,D对。
课堂练习
3、海水资源的其他利用
(1)从海水中提取铀和重水,用于核能开发。
(2)开发潮汐能、波浪能等新型能源。
海水资源
海水化学资源的开发利用
海水提镁
海水提溴
海带提碘
海水制盐
浓缩海水
课堂小结
谢谢观看
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
