辽宁省凌源市2022-2023学年高二下学期6月联考化学试题(含答案)
文档属性
| 名称 | 辽宁省凌源市2022-2023学年高二下学期6月联考化学试题(含答案) |

|
|
| 格式 | doc | ||
| 文件大小 | 1.4MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-06-16 00:00:00 | ||
图片预览



文档简介
凌源市2022-2023学年高二下学期6月联考
化学
考生注意:
1.本试卷分选择题和非选择题两部分。满分100分,考试时间75分钟。
2.答题前,考生务必用直径0.5毫米黑色墨水签字笔将密封线内项目填写清楚。
3.考生作答时,请将答案答在答题卡上。选择题每小题选出答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑;非选择题请用直径0.5毫米黑色墨水签字笔在答题卡上各题的答题区城内作答,超出答题区域书写的答案无效,在试题卷、草稿纸上作答无效。
4.本卷命题范围:人教版必修一、必修二、选修1、选修2、选修3第一章一第三章第三节。
5.可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23
一、选择题(本题共15小题,每小题3分,共计45分。在每小题列出的四个选项中,只有一项是符合题目要求的)
1.下列化学用语不正确的是( )
A.甲基的电子式为 B.乙炔的结构式:
C.苯的空间填充模型: D.乙烯的结构简式:
2.化学与生活密切相关。下列说法正确的是( )
A.冬奥会使用的石墨烯材料属于烯烃
B.制作陶制品秦陵兵马俑的主要原料为黏土和石灰石
C.王水是由浓硝酸和浓硫酸按一定比例组成的混合物
D.“司南之杓,投之于地,其柢指南”,“司南”的主要成分为
3.下列说法正确的是( )
A.基态原子中的末成对电子数为6
B.在基态多电子原子中,轨道电子能量一定高于轨道电子能量
C.电负性甲大于乙,则第一电离能甲一定大于乙
D.根据原子核外电子排布的特点,元素在周期表中属于区
4.可通过反应制得。下列有关该反应的说法正确的是( )
A.为非电解质 B.反应类型为置换反应
C.均属于盐 D.中硫元素的化合价为
5.恒温下气体反应达到化学平衡,平衡常数。晅容时,若降低温度,D的浓度增大。下列说法错误的是( )
A.该反应的化学方程式为
B.增大减小
C.恒容时,向容器中充入,反应速率不变
D.正反应为放热反应
6.设为阿伏加德罗常数的值。下列叙述正确的是( )
A.标准状况下,中含有分子的数目为
B.常温常压下,中含有共价键的数目为
C.常温下,的溶液中,水电离出的数目为
D.常温常压下,与足量溶液反应,转移电子的数目为
7.下列对一些实验事实的解释错误的是( )
选项 实验事实 解释
A 水加热到较高温度难以分解 水分子中共价键键能较大
B 石墨棒作为原电池的电极材料 石墨晶体能导电
C 用射线实验区分玻璃和水晶 水晶的衍射图上有明锐的衍射峰
D 的沸点高于 键的键长比键的键长短
8.下列化学反应的离子方程式书写正确的是( )
A.向盐酸中滴加少量纯碱溶液:
B.向溶液中滴加少量溶液:
C.向溶液中滴加过量氯水:
D.向胶体中滴加足量的溶液:(胶体)
9.下列关于的叙述,正确的是( )
A.不存在顺反异构体
B.与互为同分异构体
C.分子中所有碳原子可能在同一平面上
D.用系统命名法命名,其名称是3,5-二甲基-2-已烯
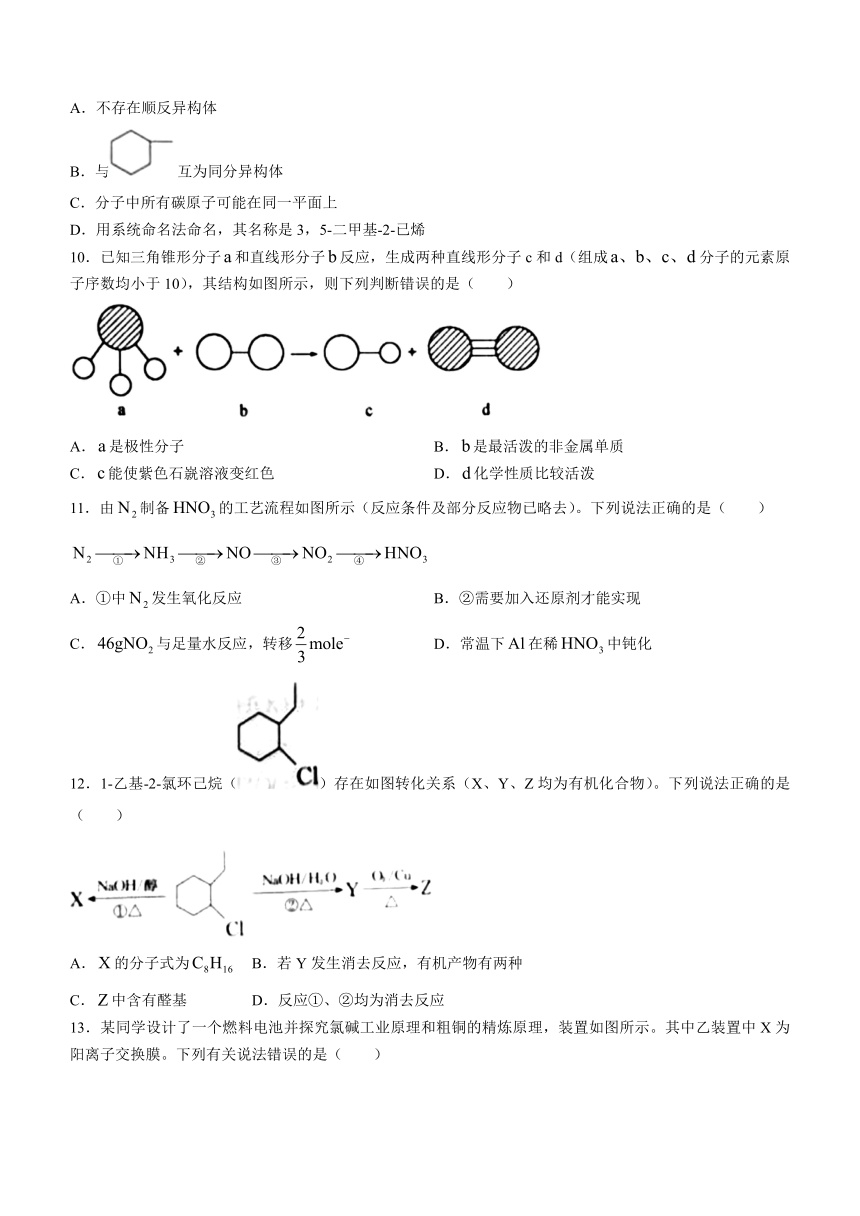
10.已知三角锥形分子和直线形分子反应,生成两种直线形分子c和d(组成分子的元素原子序数均小于10),其结构如图所示,则下列判断错误的是( )
A.是极性分子 B.是最活泼的非金属单质
C.能使紫色石 溶液变红色 D.化学性质比较活泼
11.由制备的工艺流程如图所示(反应条件及部分反应物已略去)。下列说法正确的是( )
A.①中发生氧化反应 B.②需要加入还原剂才能实现
C.与足量水反应,转移 D.常温下在稀中钝化
12.1-乙基-2-氯环己烷()存在如图转化关系(X、Y、Z均为有机化合物)。下列说法正确的是( )
A.的分子式为 B.若Y发生消去反应,有机产物有两种
C.中含有醛基 D.反应①、②均为消去反应
13.某同学设计了一个燃料电池并探究氯碱工业原理和粗铜的精炼原理,装置如图所示。其中乙装置中X为阳离子交换膜。下列有关说法错误的是( )
A.通入的极为正极,该电极反应式为
B.乙装置中铁电极为阴极,电极反应式为
C.反应一段时间后,乙装置中在铁电极区生成氢氧化钠溶液
D.反应一段时间后,丙装置中硫酸铜溶液浓度可能减小
14.有机化合物的结构简式如图所示。下列有关的说法正确的是( )
A.分子式为 B.可以与溶液反应
C.最多与反应 D.不可以发生加聚反应
15.乙二胺四乙酸又叫,是一种良好的配合剂,常用于测定金属离子的含量。已知:的结构如图。下列叙述正确的是( )
A.中氮原子杂化方式为
B.与金属离子形成配合物时,碳原子提供孤电子对
C.分子中既含有键又含有键
D.是共价化合物,属于共价晶体
二、非选择题(本题共4小题,共55分)
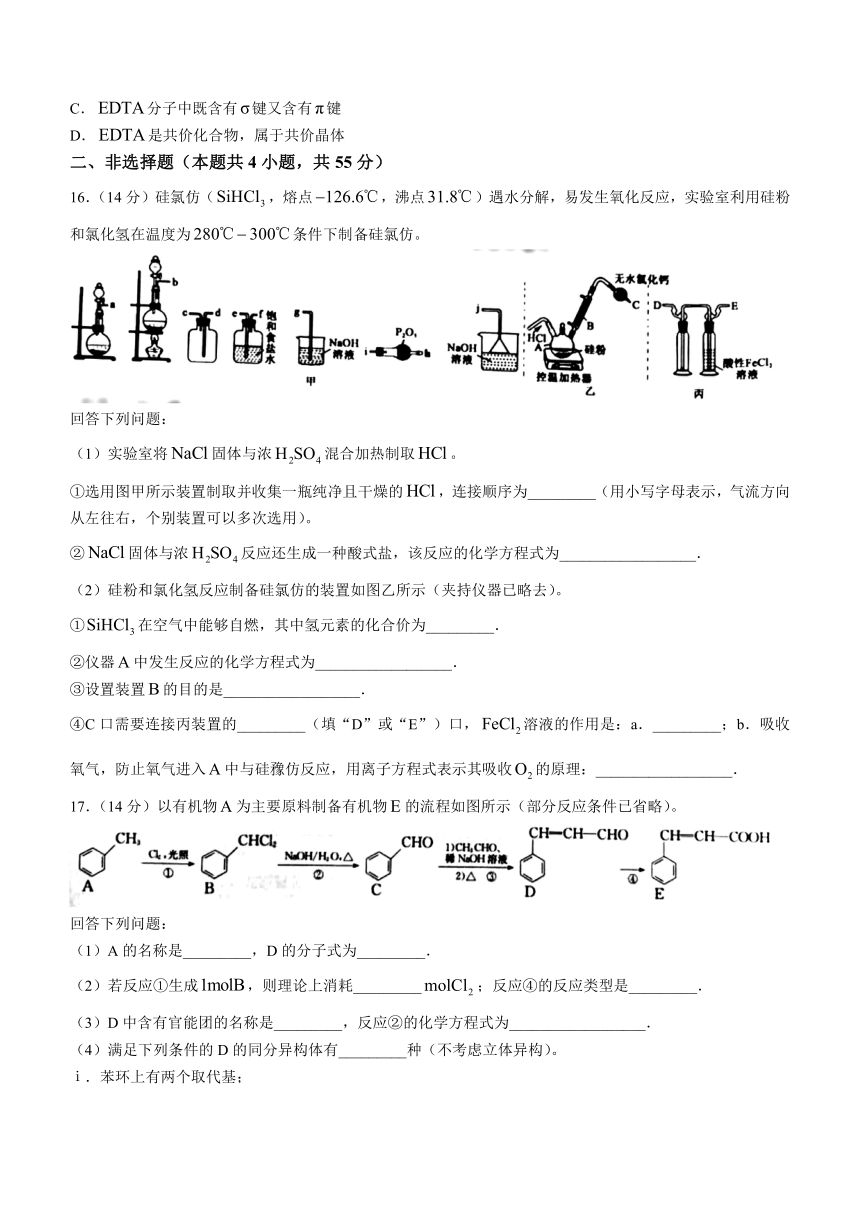
16.(14分)硅氯仿(,熔点,沸点)遇水分解,易发生氧化反应,实验室利用硅粉和氯化氢在温度为条件下制备硅氯仿。
回答下列问题:
(1)实验室将固体与浓混合加热制取。
①选用图甲所示装置制取并收集一瓶纯净且干燥的,连接顺序为_________(用小写字母表示,气流方向从左往右,个别装置可以多次选用)。
②固体与浓反应还生成一种酸式盐,该反应的化学方程式为__________________.
(2)硅粉和氯化氢反应制备硅氯仿的装置如图乙所示(夹持仪器已略去)。
①在空气中能够自燃,其中氢元素的化合价为_________.
②仪器中发生反应的化学方程式为__________________.
③设置装置的目的是__________________.
④C口需要连接丙装置的_________(填“D”或“E”)口,溶液的作用是:a._________;b.吸收氧气,防止氧气进入中与硅 仿反应,用离子方程式表示其吸收的原理:__________________.
17.(14分)以有机物为主要原料制备有机物的流程如图所示(部分反应条件已省略)。
回答下列问题:
(1)A的名称是_________,D的分子式为_________.
(2)若反应①生成,则理论上消耗_________;反应④的反应类型是_________.
(3)D中含有官能团的名称是_________,反应②的化学方程式为__________________.
(4)满足下列条件的D的同分异构体有_________种(不考虑立体异构)。
ⅰ.苯环上有两个取代基;
ⅱ.能与溶液发生显色反应;
ⅲ.除苯环外不含有其他环,也不含有“”
(5)请参照上述合成路线,设计以为原料制备的合成路线:__________________(无机试剂任选)。
18.(13分)甲醇既是重要的化工原料,又可作为燃料。利用合成气(主要成分为、和)在催化剂作用下可合成甲醇,发生的主要反应如下:
Ⅰ.;
Ⅱ.;
Ⅲ.。
(1)_________.
(2)将和通入容积为的恒容密闭容器中,在一定条件下发生反应Ⅱ,测得的平衡转化率与温度的关系如图1所示。
①时反应达到平衡所需的时间为,则反应从起始至内,用表示该反应的平均反应速率为__________________;平衡后向容器中再通入,平衡_________(填“正向”“逆向”或“不”)移动。
(2)时,反应Ⅱ的平衡常数_________.
(3)甲醇会对水质造成一定的污染,有一种电化学法可消除这种污染,其原理如下:通电后,将氧化成,然后以作氧化剂,将水中的甲醇氧化成而净化。实验室用如图2装置模拟上述过程。
①写出阳极的电极反应式:___________________________.
②写出除去甲醇的离子方程式:___________________________.
19.(14分)氮的许多重要化合物在半导体材料及炸药等方面用途非常广泛。回答下列问题:
(1)是一种半导体材料。基态原子的核外电子排布式为_________;基态原子电子占据的最高能级符号为_________,其电子云轮廓图为_________形。
(2)是一种炸药,可通过下列方法合成:。
①属于_________晶体,其中阴离子中氮原子的杂化方式是_________,该阴离子的空间构型为_________.
②和中原子的杂化方式_________(填“相同”或“不同”);键角:_________(填“大于”“小于”或“等于”)。
凌源市2022-2023学年高二下学期6月联考
化学
参考答案、提示及评分细则
1.B 甲基的电子式为,A项正确;乙炔的结构式为,B项错误;苯的空间填充模型为,C项正确;乙烯的结构简式为,D项正确。
2.D 石墨烯是碳元素的一种单质,A项错误;制作陶制品的主要原料为黏土,B项错误;王水由浓硝酸和浓盐酸混合而成,C项错误;司南就是古代的指南针,由天然磁石制作,其主要成分为,D项正确。
3.A 基态原子的核外电子排布式为,A项正确;原子中电子的能量小于电子,B项错误;电负性:,但,C项错误;元素在区,D项错误。
4.C 为电解质,A项错误;只有单质参加反应,没有单质生成,反应类型不是置换反应,B项错误;、均属于盐,C项正确;中硫元素的化合价为,D项错误。
5.B 根据平衡常数的计算式得出该反应的化学方程式为,A项正确;增大,平衡正向移动,但只与温度有关,温度没变,因此不变,B项错误;恒容时,向容器中充入稀有气体,各物质的浓度不变,反应速率不变,C项正确;降低温度,D的浓度增大,平衡正向移动,正反应是放热反应,D项正确。
6.B 在标准状况下为液体,不能用气体摩尔体积计算,A项错误;为,含有个,B项正确;时溶液中,因无溶液体积,无法计算水电离出的数目,C项错误;与反应转移的电子数为,D项错误。
7.D 水加热到较高温度难以分解,说明水中存在的化学键较强,键能较大,A项正确;石墨晶体能导电,可作电极材料,B项正确;晶体的X射线衍射图中有明锐的衍射峰,C项正确;非金属氢化物的熔沸点与分子间作用力和氢键有关,与键长无关,分子间能形成氢键,分子间不能形成氢键,故的沸点高于,D项错误。
8.C 盐酸过量,滴入少量溶液,发生的反应为,A项错误;向溶液中滴加少量溶液生成,B项错误;氯水过量,能够反应完,离子方程式为,C项正确;会被还原为,离子方程式为,D项错误。
9.D 有机物中双键碳原子两侧若均连有不同的原子,则存在顺反异构,A项错误;它与分子式不相同,不互为同分异构体,B项错误;其结构中有一个碳原子同与其直接相连的两个碳原子构成四面体,所有碳原子不可能在同一平面上,C项错误;用系统命名法命名,其名称是3,5-二甲基-2-已烯,D项正确。
10.D 由组成分子的元素原子序数均小于10及为三角锥形分子可知为,组成的元素除氢外另一元素为价的氟,故为为为属于极性分子,A项正确;是最活泼的非金属单质,B项正确;水溶液呈酸性,C项正确;分子中含有氮氮三键,化学性质稳定,D项错误。
11.C 氮元素化合价降低,①为还原反应,A项错误;氮元素化合价升高,②为氧化反应,需要加入氧化剂才能实现,B项错误;物质的量为,其与足量水反应,转移,C项正确;常温下与浓发生钝化反应,D项错误。
12.B X的分子式为,A项错误;发生消去反应,有机产物有两种,B项正确;中含有羰基,不含有醛基,C项错误;反应①、②分别为消去反应、取代反应,D项错误。
13.A 甲装置为燃料电池,通的极为正极,电解质为,电极反应式为,A项错误;通的极为负极,即电极为阴极,电极反应式为,B项正确;根据B项的分析及为阳离子交换膜,充许通过知,反应一段时间后,乙装置中铁电极区生成溶液,C项正确;根据上述分析,精铜作阴极,电极反应式为,粗铜作阳极,电极反应式为,但粗铜中含有比活泼的金属,这些金属先失电子,使溶液的浓度减小,D项正确。
14.B 其不饱和度为6,分子式为,A项错误;其含有酚羟基,可以与溶液反应,B项正确;最多与反应,C项错误;中含有,可以发生加聚反应,D项错误。
15.C 根据EDTA结构,氮原子杂化方式为,A项错误;EDTA与金属离子形成配合物时,或提供孤电子对,B项错误;EDTA分子中存在羧基,故既含有键又含有键,C项正确;EDTA是共价化合物,属于分子晶体,D项错误。
16.(1)①bihdcihj ②
(2)①-1
②
(3)使冷凝回流、导气
(4)D;吸收,防止污染环境;
17.(1)甲苯;
(2)2;氧化反应
(3)碳碳双键、醛基;
(4)6
(5)
18.(1)
(2)①;不 ②3
(3)①
②
19.(1)或;;亚铃
(2)①离子;;平面三角形 ②相同;小于
化学
考生注意:
1.本试卷分选择题和非选择题两部分。满分100分,考试时间75分钟。
2.答题前,考生务必用直径0.5毫米黑色墨水签字笔将密封线内项目填写清楚。
3.考生作答时,请将答案答在答题卡上。选择题每小题选出答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑;非选择题请用直径0.5毫米黑色墨水签字笔在答题卡上各题的答题区城内作答,超出答题区域书写的答案无效,在试题卷、草稿纸上作答无效。
4.本卷命题范围:人教版必修一、必修二、选修1、选修2、选修3第一章一第三章第三节。
5.可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23
一、选择题(本题共15小题,每小题3分,共计45分。在每小题列出的四个选项中,只有一项是符合题目要求的)
1.下列化学用语不正确的是( )
A.甲基的电子式为 B.乙炔的结构式:
C.苯的空间填充模型: D.乙烯的结构简式:
2.化学与生活密切相关。下列说法正确的是( )
A.冬奥会使用的石墨烯材料属于烯烃
B.制作陶制品秦陵兵马俑的主要原料为黏土和石灰石
C.王水是由浓硝酸和浓硫酸按一定比例组成的混合物
D.“司南之杓,投之于地,其柢指南”,“司南”的主要成分为
3.下列说法正确的是( )
A.基态原子中的末成对电子数为6
B.在基态多电子原子中,轨道电子能量一定高于轨道电子能量
C.电负性甲大于乙,则第一电离能甲一定大于乙
D.根据原子核外电子排布的特点,元素在周期表中属于区
4.可通过反应制得。下列有关该反应的说法正确的是( )
A.为非电解质 B.反应类型为置换反应
C.均属于盐 D.中硫元素的化合价为
5.恒温下气体反应达到化学平衡,平衡常数。晅容时,若降低温度,D的浓度增大。下列说法错误的是( )
A.该反应的化学方程式为
B.增大减小
C.恒容时,向容器中充入,反应速率不变
D.正反应为放热反应
6.设为阿伏加德罗常数的值。下列叙述正确的是( )
A.标准状况下,中含有分子的数目为
B.常温常压下,中含有共价键的数目为
C.常温下,的溶液中,水电离出的数目为
D.常温常压下,与足量溶液反应,转移电子的数目为
7.下列对一些实验事实的解释错误的是( )
选项 实验事实 解释
A 水加热到较高温度难以分解 水分子中共价键键能较大
B 石墨棒作为原电池的电极材料 石墨晶体能导电
C 用射线实验区分玻璃和水晶 水晶的衍射图上有明锐的衍射峰
D 的沸点高于 键的键长比键的键长短
8.下列化学反应的离子方程式书写正确的是( )
A.向盐酸中滴加少量纯碱溶液:
B.向溶液中滴加少量溶液:
C.向溶液中滴加过量氯水:
D.向胶体中滴加足量的溶液:(胶体)
9.下列关于的叙述,正确的是( )
A.不存在顺反异构体
B.与互为同分异构体
C.分子中所有碳原子可能在同一平面上
D.用系统命名法命名,其名称是3,5-二甲基-2-已烯
10.已知三角锥形分子和直线形分子反应,生成两种直线形分子c和d(组成分子的元素原子序数均小于10),其结构如图所示,则下列判断错误的是( )
A.是极性分子 B.是最活泼的非金属单质
C.能使紫色石 溶液变红色 D.化学性质比较活泼
11.由制备的工艺流程如图所示(反应条件及部分反应物已略去)。下列说法正确的是( )
A.①中发生氧化反应 B.②需要加入还原剂才能实现
C.与足量水反应,转移 D.常温下在稀中钝化
12.1-乙基-2-氯环己烷()存在如图转化关系(X、Y、Z均为有机化合物)。下列说法正确的是( )
A.的分子式为 B.若Y发生消去反应,有机产物有两种
C.中含有醛基 D.反应①、②均为消去反应
13.某同学设计了一个燃料电池并探究氯碱工业原理和粗铜的精炼原理,装置如图所示。其中乙装置中X为阳离子交换膜。下列有关说法错误的是( )
A.通入的极为正极,该电极反应式为
B.乙装置中铁电极为阴极,电极反应式为
C.反应一段时间后,乙装置中在铁电极区生成氢氧化钠溶液
D.反应一段时间后,丙装置中硫酸铜溶液浓度可能减小
14.有机化合物的结构简式如图所示。下列有关的说法正确的是( )
A.分子式为 B.可以与溶液反应
C.最多与反应 D.不可以发生加聚反应
15.乙二胺四乙酸又叫,是一种良好的配合剂,常用于测定金属离子的含量。已知:的结构如图。下列叙述正确的是( )
A.中氮原子杂化方式为
B.与金属离子形成配合物时,碳原子提供孤电子对
C.分子中既含有键又含有键
D.是共价化合物,属于共价晶体
二、非选择题(本题共4小题,共55分)
16.(14分)硅氯仿(,熔点,沸点)遇水分解,易发生氧化反应,实验室利用硅粉和氯化氢在温度为条件下制备硅氯仿。
回答下列问题:
(1)实验室将固体与浓混合加热制取。
①选用图甲所示装置制取并收集一瓶纯净且干燥的,连接顺序为_________(用小写字母表示,气流方向从左往右,个别装置可以多次选用)。
②固体与浓反应还生成一种酸式盐,该反应的化学方程式为__________________.
(2)硅粉和氯化氢反应制备硅氯仿的装置如图乙所示(夹持仪器已略去)。
①在空气中能够自燃,其中氢元素的化合价为_________.
②仪器中发生反应的化学方程式为__________________.
③设置装置的目的是__________________.
④C口需要连接丙装置的_________(填“D”或“E”)口,溶液的作用是:a._________;b.吸收氧气,防止氧气进入中与硅 仿反应,用离子方程式表示其吸收的原理:__________________.
17.(14分)以有机物为主要原料制备有机物的流程如图所示(部分反应条件已省略)。
回答下列问题:
(1)A的名称是_________,D的分子式为_________.
(2)若反应①生成,则理论上消耗_________;反应④的反应类型是_________.
(3)D中含有官能团的名称是_________,反应②的化学方程式为__________________.
(4)满足下列条件的D的同分异构体有_________种(不考虑立体异构)。
ⅰ.苯环上有两个取代基;
ⅱ.能与溶液发生显色反应;
ⅲ.除苯环外不含有其他环,也不含有“”
(5)请参照上述合成路线,设计以为原料制备的合成路线:__________________(无机试剂任选)。
18.(13分)甲醇既是重要的化工原料,又可作为燃料。利用合成气(主要成分为、和)在催化剂作用下可合成甲醇,发生的主要反应如下:
Ⅰ.;
Ⅱ.;
Ⅲ.。
(1)_________.
(2)将和通入容积为的恒容密闭容器中,在一定条件下发生反应Ⅱ,测得的平衡转化率与温度的关系如图1所示。
①时反应达到平衡所需的时间为,则反应从起始至内,用表示该反应的平均反应速率为__________________;平衡后向容器中再通入,平衡_________(填“正向”“逆向”或“不”)移动。
(2)时,反应Ⅱ的平衡常数_________.
(3)甲醇会对水质造成一定的污染,有一种电化学法可消除这种污染,其原理如下:通电后,将氧化成,然后以作氧化剂,将水中的甲醇氧化成而净化。实验室用如图2装置模拟上述过程。
①写出阳极的电极反应式:___________________________.
②写出除去甲醇的离子方程式:___________________________.
19.(14分)氮的许多重要化合物在半导体材料及炸药等方面用途非常广泛。回答下列问题:
(1)是一种半导体材料。基态原子的核外电子排布式为_________;基态原子电子占据的最高能级符号为_________,其电子云轮廓图为_________形。
(2)是一种炸药,可通过下列方法合成:。
①属于_________晶体,其中阴离子中氮原子的杂化方式是_________,该阴离子的空间构型为_________.
②和中原子的杂化方式_________(填“相同”或“不同”);键角:_________(填“大于”“小于”或“等于”)。
凌源市2022-2023学年高二下学期6月联考
化学
参考答案、提示及评分细则
1.B 甲基的电子式为,A项正确;乙炔的结构式为,B项错误;苯的空间填充模型为,C项正确;乙烯的结构简式为,D项正确。
2.D 石墨烯是碳元素的一种单质,A项错误;制作陶制品的主要原料为黏土,B项错误;王水由浓硝酸和浓盐酸混合而成,C项错误;司南就是古代的指南针,由天然磁石制作,其主要成分为,D项正确。
3.A 基态原子的核外电子排布式为,A项正确;原子中电子的能量小于电子,B项错误;电负性:,但,C项错误;元素在区,D项错误。
4.C 为电解质,A项错误;只有单质参加反应,没有单质生成,反应类型不是置换反应,B项错误;、均属于盐,C项正确;中硫元素的化合价为,D项错误。
5.B 根据平衡常数的计算式得出该反应的化学方程式为,A项正确;增大,平衡正向移动,但只与温度有关,温度没变,因此不变,B项错误;恒容时,向容器中充入稀有气体,各物质的浓度不变,反应速率不变,C项正确;降低温度,D的浓度增大,平衡正向移动,正反应是放热反应,D项正确。
6.B 在标准状况下为液体,不能用气体摩尔体积计算,A项错误;为,含有个,B项正确;时溶液中,因无溶液体积,无法计算水电离出的数目,C项错误;与反应转移的电子数为,D项错误。
7.D 水加热到较高温度难以分解,说明水中存在的化学键较强,键能较大,A项正确;石墨晶体能导电,可作电极材料,B项正确;晶体的X射线衍射图中有明锐的衍射峰,C项正确;非金属氢化物的熔沸点与分子间作用力和氢键有关,与键长无关,分子间能形成氢键,分子间不能形成氢键,故的沸点高于,D项错误。
8.C 盐酸过量,滴入少量溶液,发生的反应为,A项错误;向溶液中滴加少量溶液生成,B项错误;氯水过量,能够反应完,离子方程式为,C项正确;会被还原为,离子方程式为,D项错误。
9.D 有机物中双键碳原子两侧若均连有不同的原子,则存在顺反异构,A项错误;它与分子式不相同,不互为同分异构体,B项错误;其结构中有一个碳原子同与其直接相连的两个碳原子构成四面体,所有碳原子不可能在同一平面上,C项错误;用系统命名法命名,其名称是3,5-二甲基-2-已烯,D项正确。
10.D 由组成分子的元素原子序数均小于10及为三角锥形分子可知为,组成的元素除氢外另一元素为价的氟,故为为为属于极性分子,A项正确;是最活泼的非金属单质,B项正确;水溶液呈酸性,C项正确;分子中含有氮氮三键,化学性质稳定,D项错误。
11.C 氮元素化合价降低,①为还原反应,A项错误;氮元素化合价升高,②为氧化反应,需要加入氧化剂才能实现,B项错误;物质的量为,其与足量水反应,转移,C项正确;常温下与浓发生钝化反应,D项错误。
12.B X的分子式为,A项错误;发生消去反应,有机产物有两种,B项正确;中含有羰基,不含有醛基,C项错误;反应①、②分别为消去反应、取代反应,D项错误。
13.A 甲装置为燃料电池,通的极为正极,电解质为,电极反应式为,A项错误;通的极为负极,即电极为阴极,电极反应式为,B项正确;根据B项的分析及为阳离子交换膜,充许通过知,反应一段时间后,乙装置中铁电极区生成溶液,C项正确;根据上述分析,精铜作阴极,电极反应式为,粗铜作阳极,电极反应式为,但粗铜中含有比活泼的金属,这些金属先失电子,使溶液的浓度减小,D项正确。
14.B 其不饱和度为6,分子式为,A项错误;其含有酚羟基,可以与溶液反应,B项正确;最多与反应,C项错误;中含有,可以发生加聚反应,D项错误。
15.C 根据EDTA结构,氮原子杂化方式为,A项错误;EDTA与金属离子形成配合物时,或提供孤电子对,B项错误;EDTA分子中存在羧基,故既含有键又含有键,C项正确;EDTA是共价化合物,属于分子晶体,D项错误。
16.(1)①bihdcihj ②
(2)①-1
②
(3)使冷凝回流、导气
(4)D;吸收,防止污染环境;
17.(1)甲苯;
(2)2;氧化反应
(3)碳碳双键、醛基;
(4)6
(5)
18.(1)
(2)①;不 ②3
(3)①
②
19.(1)或;;亚铃
(2)①离子;;平面三角形 ②相同;小于
同课章节目录
