第九单元金属测试题(含答案)---2022-2023学年九年级化学鲁教版下册
文档属性
| 名称 | 第九单元金属测试题(含答案)---2022-2023学年九年级化学鲁教版下册 | 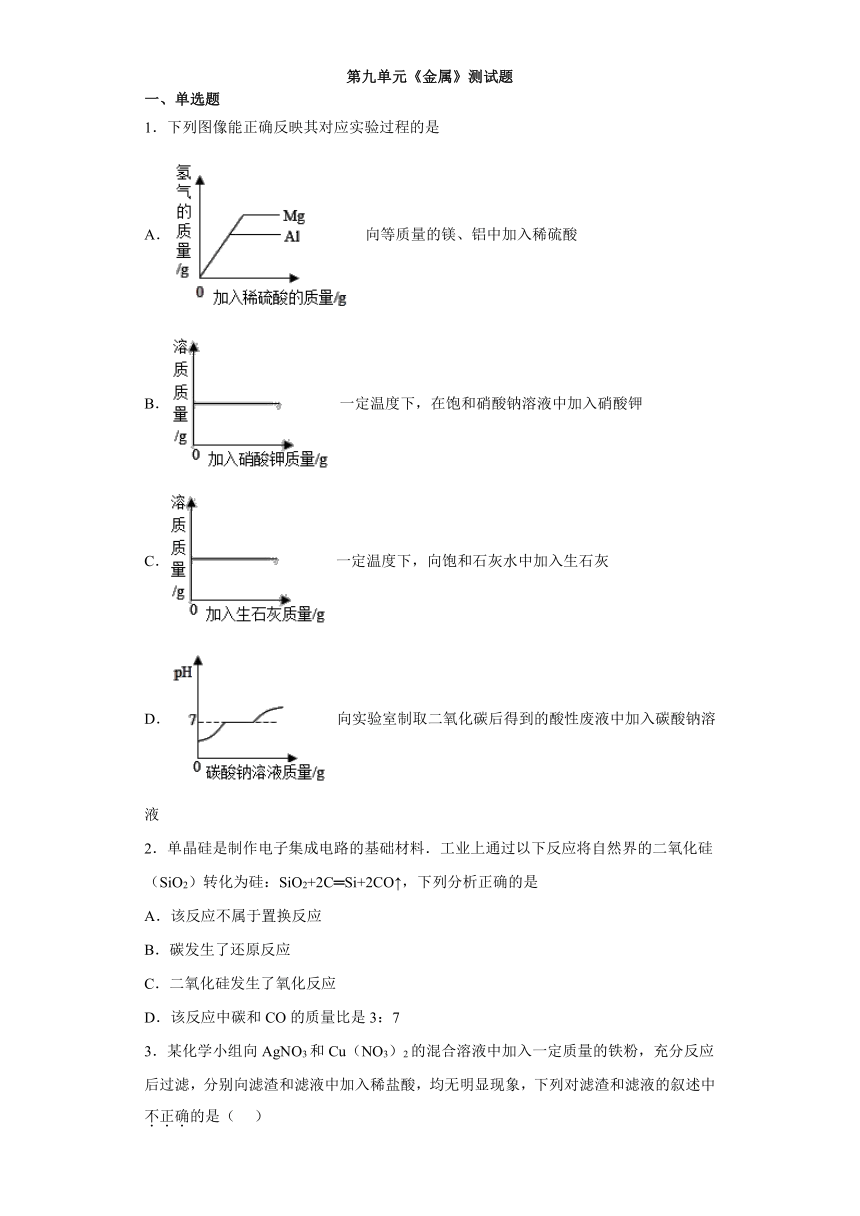 | |
| 格式 | docx | ||
| 文件大小 | 116.4KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-06-16 20:44:41 | ||
图片预览




文档简介
第九单元《金属》测试题
一、单选题
1.下列图像能正确反映其对应实验过程的是
A. 向等质量的镁、铝中加入稀硫酸
B. 一定温度下,在饱和硝酸钠溶液中加入硝酸钾
C. 一定温度下,向饱和石灰水中加入生石灰
D. 向实验室制取二氧化碳后得到的酸性废液中加入碳酸钠溶液
2.单晶硅是制作电子集成电路的基础材料.工业上通过以下反应将自然界的二氧化硅(SiO2)转化为硅:SiO2+2C═Si+2CO↑,下列分析正确的是
A.该反应不属于置换反应
B.碳发生了还原反应
C.二氧化硅发生了氧化反应
D.该反应中碳和CO的质量比是3:7
3.某化学小组向AgNO3和Cu(NO3)2的混合溶液中加入一定质量的铁粉,充分反应后过滤,分别向滤渣和滤液中加入稀盐酸,均无明显现象,下列对滤渣和滤液的叙述中不正确的是( )
A.滤渣中一定含有Ag B.滤渣中一定不含Fe
C.滤液中可能含有Fe(NO3)2 D.滤液中可能含有Cu(NO3)2
4.将一定量的锌粉放入氯化亚铁稀溶液中,充分反应后过滤,再向滤渣中加盐酸有气泡产生。下列说法不正确的是
A.滤出的固体中一定有铁,可能有锌
B.滤液中一定有氯化锌,可能有氯化亚铁
C.反应后溶液的质量一定增大
D.若反应后溶液为浅绿色,则反应后溶液中溶质只为氯化亚铁
5.下列有关实验现象的描述,正确的是
A.红磷在空气中燃烧产生白雾
B.硫在空气中燃烧生成无色无味的气体
C.一氧化碳在空气中燃烧产生蓝色火焰
D.将铁钉投入硫酸铜溶液中,有黑色的铜析出
6.下列图像能正确反映其对应关系的是
A.①表示高温下一定质量的碳与足量的二氧化碳反应
B.②表示向氢氧化钠溶液中加水稀释
C.③表示电解水生成氢气与氧气的质量关系
D.④表示分别向等质量足量的铁粉、锌粉中加入一定量等质量,等质量分数的稀盐酸
7.下列实验现象描述正确的是
A.铁钉与硫酸铜溶液反应:银白色固体表面有紫红色的铜生成,溶液由浅绿色变为蓝色
B.镁带在空气中燃烧:银白色固体燃烧,发出耀眼白光,放热,产生白烟
C.电解水实验:两个电极表面产生气泡,一段时间,正、负极产生气体体积比约为2:1
D.木炭在氧气中燃烧:黑色固体燃烧,发出黄白色火焰,放出大量热
8.下列依据实验目的所设计的实验操作中,不正确的是
选项 实验目的 实验操作
A 除去CO2中的CO 通入澄清石灰水中
B 除去铜粉中的铁粉 滴加适量稀盐酸
C 鉴别纯水和矿泉水 滴加适量肥皂水
D 鉴别真黄金和假黄金(铜锌合金) 滴加稀盐酸
A.A B.B C.C D.D
9.下列实验现象描述正确的是( )
A.生石灰与水反应:水沸腾,白色固体变白色浆液,吸收大量的热
B.硫在氧气中燃烧:发出明亮的蓝紫色火焰,产生有刺激性气味的气体
C.一氧化碳还原氧化铁粉末:红棕色粉末变为银白色,澄清石灰水变浑浊
D.铁丝插入硫酸铜溶液中:银白色固体表面有紫红色固体生成,溶液由蓝色变成无色
10.下列实验操作能达到实验目的是( )
选项 实验目的 实验操作
A 鉴别木炭粉和铁粉 加稀盐酸,观察有无气泡产生
B 鉴别氮气和二氧化碳 将燃着的木条分别伸入盛气体的集气瓶中
C 除去一氧化碳中的氧气 将气体缓慢通过灼热的铜网
D 除去FeSO4溶液中少量的CuSO4 加入足量锌粉,充分反应后过滤
A.A B.B C.C D.D
11.除去下列物质中混有的少量杂质(括号内为杂质),所用方法正确的是
A.O2气体(N2)——通过灼热的铜网
B.KCl固体(KClO3)——加入少量的二氧化锰,加热
C.CaCl2溶液(HCl)——加入过量的碳酸钙,过滤
D.Fe固体(Cu)——加入过量CuCl2溶液,过滤、洗涤、干燥
12.除去下表中各物质(A~C为溶液)中的少量杂质,所选用的试剂、方法正确的是
编号 物质 杂质(少量) 试剂 除杂操作方法
A NaCl CaCl2 适量K2CO3溶液 过滤
B Fe粉 Cu粉 硫酸 过滤
C KNO3 NaCl / 冷却热饱和溶液,过滤
D CO2 CO / 点燃
A.A B.B C.C D.D
二、填空题
13.金属及金属材料在生产、生活中有广泛的应用。
(1)近年来,我市多地纷开展文明城创建工作,垃圾分类回收是其中一项重要举措。某街道垃圾桶如图所示,请回答下列问题:
①图中标识的物质,属于金属材料的是______(写出一种即可);
②使用铝合金做内筒的优点是______(写出一点即可)。某品牌饮料的空易拉罐应放入______(选填“可回收”或“不可回收”)桶中;
③铁制品锈蚀的过程,实际上是铁制品跟空气中的______发生化学反应的过程。
(2)将甲、乙、丙三种金属分别投入稀硫酸中,甲、丙表面有气泡产生,乙无明显现象;若将甲放入丙的硫酸盐溶液中,一段时间后,甲的表面有丙析出。由此推断这三种金属的活动性由强到弱的顺序是______。
14.在Pb、Hg、Fe、Cu、Ag五种金属中,按金属活动性顺序由强到弱排列的是:______,在稀H2SO4中最容易变为金属离子的是______,不能从盐酸中置换出氢的金属是______。
15.回答下列与金属有关的问题:
(1)生铁和纯铁,硬度较大的是______。
(2)铝制品其有很好的抗腐蚀性能,原因是铝在空气中与氧气反应,其表面生成一层致密的______(用名称或化学式填空)薄膜。
(3)向AgNO3、Cu(NO3)2、NaNO3的混合溶液中,加入一定量的锌粉,充分反应后过滤,得到金属滤渣和无色滤液。则所得滤液中一定含有的溶质是______。
三、实验题
16.如图是实验室制取并收集气体的实验装置图。请回答下列问题:
(1)写出仪器的名称②_______。
(2)实验室用固体混合物制取并收集干燥的氧气应选择的装置组合是A和_______(填序号),发生反应的化学方程式为_______。
(3)B装置用于实验室制取氢气,发生反应的化学方程式为_______,仪器a在实验中起的作用是方便添加液体药品和_______。
(4)用F装置收集氧气,应从_______(填“b”或“c”)端通入氧气。
四、计算题
17.2021年5月15日我国首次火星探测任务天问一号探测器在火星着落。为测定天问一号的某电子元件材料的黄铜合金(假设合金中仅含铜、锌)中铜的质量分数,兴趣小组同学称取10g黄铜粉末于烧杯中,将40g稀盐酸平均分四次加入,充分反应,测得实验数据如表:
第一次 第二次 第三次 第四次
加入稀盐酸的质量(g) 10 10 10 10
烧杯剩余物的质量(g) 19.96 29.92 39.89 m
(1)m的值为_______ g,完全反应后生产氢气的质量为_______ g。
(2)该黄铜中铜的质量分数是多少?(计算结果精确到0.1%)
18.为了测定某黄铜(铜锌合金)中铜的质量分数,某化学小组进行了如下实验:
(1)发生反应的化学方程式为___________________;
(2)根据已知条件列出求解100g该黄铜中锌的质量(x)的比例式为__________;
(3)该黄铜样品中铜的质量分数是__________;
(4)实验中所用的稀盐酸中氯化氢的质量为__________;
(5)过滤后所得滤液中氯化锌与水的最简整数质量比为__________。
试卷第4页,共6页
参考答案:
1.D
2.D
3.C
4.D
5.C
6.A
7.B
8.A
9.B
10.A
11.C
12.C
13. 铁质外筒(或铝合金内筒) 抗腐蚀性强(合理均可) 可回收 水和氧气 甲>丙>乙
14. Fe、Pb、Cu、Hg、Ag Fe Cu、Hg、Ag
15. 生铁 氧化铝或Al2O3 NaNO3、Zn(NO3)2
16.(1)锥形瓶
(2) C 2KClO32KCl+3O2↑
(3) Zn+H2SO4=ZnSO4+H2↑ 控制反应速率
(4)c
17.(1) 49.89 0.11
(2)解:设黄铜中锌的质量为x
所以该黄铜中铜的质量分数是
答:该黄铜中铜的质量分数是64.3%。
18.(1)Zn+2HCl=ZnCl2+H2↑
(2)
(3)87%
(4)解:设氯化氢的质量为y,氯化锌的质量为z。
答:实验中所用的稀盐酸中氯化氢的质量为14.6g。
(5)滤液中水的质量为199.6g-(100g×87%)-27.2g=85.4g。
所以滤液中氯化锌与水的质量比为27.2g:85.4g=136:427。
答:滤液中氯化锌与水的质量比为136:427
一、单选题
1.下列图像能正确反映其对应实验过程的是
A. 向等质量的镁、铝中加入稀硫酸
B. 一定温度下,在饱和硝酸钠溶液中加入硝酸钾
C. 一定温度下,向饱和石灰水中加入生石灰
D. 向实验室制取二氧化碳后得到的酸性废液中加入碳酸钠溶液
2.单晶硅是制作电子集成电路的基础材料.工业上通过以下反应将自然界的二氧化硅(SiO2)转化为硅:SiO2+2C═Si+2CO↑,下列分析正确的是
A.该反应不属于置换反应
B.碳发生了还原反应
C.二氧化硅发生了氧化反应
D.该反应中碳和CO的质量比是3:7
3.某化学小组向AgNO3和Cu(NO3)2的混合溶液中加入一定质量的铁粉,充分反应后过滤,分别向滤渣和滤液中加入稀盐酸,均无明显现象,下列对滤渣和滤液的叙述中不正确的是( )
A.滤渣中一定含有Ag B.滤渣中一定不含Fe
C.滤液中可能含有Fe(NO3)2 D.滤液中可能含有Cu(NO3)2
4.将一定量的锌粉放入氯化亚铁稀溶液中,充分反应后过滤,再向滤渣中加盐酸有气泡产生。下列说法不正确的是
A.滤出的固体中一定有铁,可能有锌
B.滤液中一定有氯化锌,可能有氯化亚铁
C.反应后溶液的质量一定增大
D.若反应后溶液为浅绿色,则反应后溶液中溶质只为氯化亚铁
5.下列有关实验现象的描述,正确的是
A.红磷在空气中燃烧产生白雾
B.硫在空气中燃烧生成无色无味的气体
C.一氧化碳在空气中燃烧产生蓝色火焰
D.将铁钉投入硫酸铜溶液中,有黑色的铜析出
6.下列图像能正确反映其对应关系的是
A.①表示高温下一定质量的碳与足量的二氧化碳反应
B.②表示向氢氧化钠溶液中加水稀释
C.③表示电解水生成氢气与氧气的质量关系
D.④表示分别向等质量足量的铁粉、锌粉中加入一定量等质量,等质量分数的稀盐酸
7.下列实验现象描述正确的是
A.铁钉与硫酸铜溶液反应:银白色固体表面有紫红色的铜生成,溶液由浅绿色变为蓝色
B.镁带在空气中燃烧:银白色固体燃烧,发出耀眼白光,放热,产生白烟
C.电解水实验:两个电极表面产生气泡,一段时间,正、负极产生气体体积比约为2:1
D.木炭在氧气中燃烧:黑色固体燃烧,发出黄白色火焰,放出大量热
8.下列依据实验目的所设计的实验操作中,不正确的是
选项 实验目的 实验操作
A 除去CO2中的CO 通入澄清石灰水中
B 除去铜粉中的铁粉 滴加适量稀盐酸
C 鉴别纯水和矿泉水 滴加适量肥皂水
D 鉴别真黄金和假黄金(铜锌合金) 滴加稀盐酸
A.A B.B C.C D.D
9.下列实验现象描述正确的是( )
A.生石灰与水反应:水沸腾,白色固体变白色浆液,吸收大量的热
B.硫在氧气中燃烧:发出明亮的蓝紫色火焰,产生有刺激性气味的气体
C.一氧化碳还原氧化铁粉末:红棕色粉末变为银白色,澄清石灰水变浑浊
D.铁丝插入硫酸铜溶液中:银白色固体表面有紫红色固体生成,溶液由蓝色变成无色
10.下列实验操作能达到实验目的是( )
选项 实验目的 实验操作
A 鉴别木炭粉和铁粉 加稀盐酸,观察有无气泡产生
B 鉴别氮气和二氧化碳 将燃着的木条分别伸入盛气体的集气瓶中
C 除去一氧化碳中的氧气 将气体缓慢通过灼热的铜网
D 除去FeSO4溶液中少量的CuSO4 加入足量锌粉,充分反应后过滤
A.A B.B C.C D.D
11.除去下列物质中混有的少量杂质(括号内为杂质),所用方法正确的是
A.O2气体(N2)——通过灼热的铜网
B.KCl固体(KClO3)——加入少量的二氧化锰,加热
C.CaCl2溶液(HCl)——加入过量的碳酸钙,过滤
D.Fe固体(Cu)——加入过量CuCl2溶液,过滤、洗涤、干燥
12.除去下表中各物质(A~C为溶液)中的少量杂质,所选用的试剂、方法正确的是
编号 物质 杂质(少量) 试剂 除杂操作方法
A NaCl CaCl2 适量K2CO3溶液 过滤
B Fe粉 Cu粉 硫酸 过滤
C KNO3 NaCl / 冷却热饱和溶液,过滤
D CO2 CO / 点燃
A.A B.B C.C D.D
二、填空题
13.金属及金属材料在生产、生活中有广泛的应用。
(1)近年来,我市多地纷开展文明城创建工作,垃圾分类回收是其中一项重要举措。某街道垃圾桶如图所示,请回答下列问题:
①图中标识的物质,属于金属材料的是______(写出一种即可);
②使用铝合金做内筒的优点是______(写出一点即可)。某品牌饮料的空易拉罐应放入______(选填“可回收”或“不可回收”)桶中;
③铁制品锈蚀的过程,实际上是铁制品跟空气中的______发生化学反应的过程。
(2)将甲、乙、丙三种金属分别投入稀硫酸中,甲、丙表面有气泡产生,乙无明显现象;若将甲放入丙的硫酸盐溶液中,一段时间后,甲的表面有丙析出。由此推断这三种金属的活动性由强到弱的顺序是______。
14.在Pb、Hg、Fe、Cu、Ag五种金属中,按金属活动性顺序由强到弱排列的是:______,在稀H2SO4中最容易变为金属离子的是______,不能从盐酸中置换出氢的金属是______。
15.回答下列与金属有关的问题:
(1)生铁和纯铁,硬度较大的是______。
(2)铝制品其有很好的抗腐蚀性能,原因是铝在空气中与氧气反应,其表面生成一层致密的______(用名称或化学式填空)薄膜。
(3)向AgNO3、Cu(NO3)2、NaNO3的混合溶液中,加入一定量的锌粉,充分反应后过滤,得到金属滤渣和无色滤液。则所得滤液中一定含有的溶质是______。
三、实验题
16.如图是实验室制取并收集气体的实验装置图。请回答下列问题:
(1)写出仪器的名称②_______。
(2)实验室用固体混合物制取并收集干燥的氧气应选择的装置组合是A和_______(填序号),发生反应的化学方程式为_______。
(3)B装置用于实验室制取氢气,发生反应的化学方程式为_______,仪器a在实验中起的作用是方便添加液体药品和_______。
(4)用F装置收集氧气,应从_______(填“b”或“c”)端通入氧气。
四、计算题
17.2021年5月15日我国首次火星探测任务天问一号探测器在火星着落。为测定天问一号的某电子元件材料的黄铜合金(假设合金中仅含铜、锌)中铜的质量分数,兴趣小组同学称取10g黄铜粉末于烧杯中,将40g稀盐酸平均分四次加入,充分反应,测得实验数据如表:
第一次 第二次 第三次 第四次
加入稀盐酸的质量(g) 10 10 10 10
烧杯剩余物的质量(g) 19.96 29.92 39.89 m
(1)m的值为_______ g,完全反应后生产氢气的质量为_______ g。
(2)该黄铜中铜的质量分数是多少?(计算结果精确到0.1%)
18.为了测定某黄铜(铜锌合金)中铜的质量分数,某化学小组进行了如下实验:
(1)发生反应的化学方程式为___________________;
(2)根据已知条件列出求解100g该黄铜中锌的质量(x)的比例式为__________;
(3)该黄铜样品中铜的质量分数是__________;
(4)实验中所用的稀盐酸中氯化氢的质量为__________;
(5)过滤后所得滤液中氯化锌与水的最简整数质量比为__________。
试卷第4页,共6页
参考答案:
1.D
2.D
3.C
4.D
5.C
6.A
7.B
8.A
9.B
10.A
11.C
12.C
13. 铁质外筒(或铝合金内筒) 抗腐蚀性强(合理均可) 可回收 水和氧气 甲>丙>乙
14. Fe、Pb、Cu、Hg、Ag Fe Cu、Hg、Ag
15. 生铁 氧化铝或Al2O3 NaNO3、Zn(NO3)2
16.(1)锥形瓶
(2) C 2KClO32KCl+3O2↑
(3) Zn+H2SO4=ZnSO4+H2↑ 控制反应速率
(4)c
17.(1) 49.89 0.11
(2)解:设黄铜中锌的质量为x
所以该黄铜中铜的质量分数是
答:该黄铜中铜的质量分数是64.3%。
18.(1)Zn+2HCl=ZnCl2+H2↑
(2)
(3)87%
(4)解:设氯化氢的质量为y,氯化锌的质量为z。
答:实验中所用的稀盐酸中氯化氢的质量为14.6g。
(5)滤液中水的质量为199.6g-(100g×87%)-27.2g=85.4g。
所以滤液中氯化锌与水的质量比为27.2g:85.4g=136:427。
答:滤液中氯化锌与水的质量比为136:427
同课章节目录
- 第七单元 常见的酸和碱
- 第一节 酸及其性质
- 第二节 碱及其性质
- 第三节 溶液的酸碱性
- 第四节 酸碱中和反应
- 到实验室去:探究酸和碱的化学性质
- 第八单元 海水中的化学
- 第一节 海洋化学资源
- 第二节 海水“晒盐“
- 第三节 海水“制碱“
- 到实验室去:粗盐中难溶性杂质的去除
- 第九单元 金属
- 第一节 常见的金属材料
- 第二节 金属的化学性质
- 第三节 钢铁的锈蚀与防护
- 到实验室去 探究金属的性质
- 第十单元 化学与健康
- 第一节 食物中的有机物
- 第二节 化学元素与人体健康
- 第三节 远离有毒物质
- 第十一单元 化学与社会发展
- 第一节 化学与能源开发
- 第二节 化学与材料研制
- 第三节 化学与农业生产
- 第四节 化学与环境保护
