1.1物质的分类及转化同步练习题 高一上学期化学人教版(2019)必修第一册(含解析)
文档属性
| 名称 | 1.1物质的分类及转化同步练习题 高一上学期化学人教版(2019)必修第一册(含解析) |

|
|
| 格式 | docx | ||
| 文件大小 | 1.8MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-06-17 00:00:00 | ||
图片预览




文档简介
1.1 物质的分类及转化 同步练习题
一、选择题
1.下列有关物质的分类正确的是
A.混合物:稀硫酸 B.碱:Cu2(OH)2CO3 C.盐:NH3.H2O D.氧化物:HCOOH
2.下列物质下列物质间的每一个转化都能通过一步反应实现的是
A.Fe2O3FeFeCl3 B.H2O2H2H2O
C.CaCl2溶液CaCO3CO2 D.CuSO4溶液CuCuO
3.下列广州博物馆馆藏文物中,不属于由金属材料制成的是
文物
选项 A.广彩人物纹大碗 B.明代铁锚 C.海兽葡萄纹铜镜 D.鎏金转鸭广钟
A.A B.B C.C D.D
4.将FeCl3饱和溶液逐滴滴入到沸水中,再加热至红褐色即得到Fe(OH)3胶体。下列说法错误的是
A.光束照射Fe(OH)3胶体时会产生丁达尔现象
B.将所得胶体过滤,滤纸上无残留固体
C.通直流电时,Fe(OH)3胶体粒子会定向移动
D.Fe(OH)3胶体粒子有吸附性,可用于水的消毒
5.下列各组物质,前者属于电解质,后者属于非电解质的是
A.Na2SO4、CO2 B.Cu、SO2 C.NaCl、BaSO4 D.稀盐酸、NH3
6.下列各物质的分类、名称(或俗名)、化学式都正确的是
选项 分类 名称(或俗名) 化学式
A 正盐 小苏打 NaHCO3
B 酸 氯酸 HClO3
C 盐 苛性钠 NaOH
D 碱 纯碱 Na2CO3
A.A B.B C.C D.D
7.有人设想将碳酸钙通过特殊的加工方法使之变为纳米碳酸钙(即碳酸钙粒子直径是纳米级),这将引起建筑材料的性能发生巨变。下列关于纳米碳酸钙的推测可能正确的是
A.纳米碳酸钙是与胶体相似的分散系
B.纳米碳酸钙会产生丁达尔效应
C.纳米碳酸钙化学性质已与原来碳酸钙完全不同
D.纳米碳酸钙的粒子能透过滤纸
8.用特殊方法把固体物质加工到纳米级(1~100nm,)的超细粉末粒子,然后制得纳米材料,下列分散系中的分散质的微粒直径和这种粒子具有相同数量级的是
A.溶液 B.悬浊液 C.胶体 D.乳浊液
9.为了控制疾病,经常会用到各类消毒剂。下列消毒剂的有效成分属于盐的是
A.0.3%的高锰酸钾溶液 B.3%的双氧水
C.15%的过氧乙酸溶液 D.75%的医用酒精
10.下列关于胶体的叙述不正确的是
A.光线透过胶体时,胶体中可发生丁达尔效应
B.用平行光照射溶液和胶体时,产生的现象相同
C.胶体能吸附水中悬浮物形成固体颗粒沉降,达到净水目的
D.胶体区别其他分散系本质特征是分散质的微粒直径在1~100nm之间
11.于谦的《石灰吟》,赞颂了石灰石(碳酸钙)“粉骨碎身浑不怕,要留清白在人间”的品格。石灰(CaO)可用于治病在我国早已有之。《本草经注》中记载有“今近山生石,青白色,作灶烧竟,以水沃之,即热蒸而解末矣”,该记载描述了碳酸钙煅烧成石灰,石灰再遇水时的现象。下列过程中未发生化学变化的是
A.粉碎石灰石 B.煅烧石灰石 C.石灰遇水 D.石灰遇二氧化碳
12.下列关于物质的分类正确的是
酸 碱 盐 碱性氧化物 酸性氧化物
A CO
B HClO CaO
C
D KOH NaCl NO
A.A B.B C.C D.D
13.当光束通过下列物质时,会出现丁达尔效应的是
①胶体 ②盐酸 ③蔗糖溶液 ④云、雾 ⑤豆浆
A.①④⑤ B.②③⑤ C.②③④ D.①④
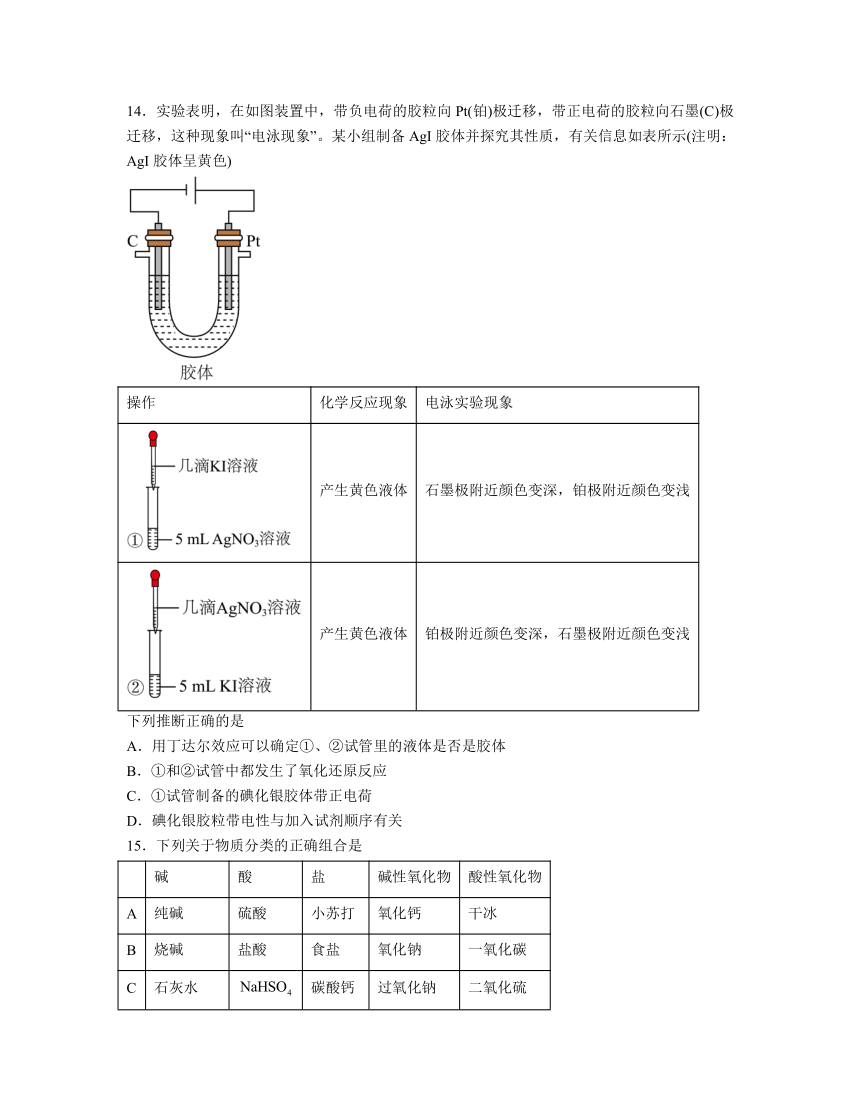
14.实验表明,在如图装置中,带负电荷的胶粒向Pt(铂)极迁移,带正电荷的胶粒向石墨(C)极迁移,这种现象叫“电泳现象”。某小组制备AgI胶体并探究其性质,有关信息如表所示(注明:AgI胶体呈黄色)
操作 化学反应现象 电泳实验现象
产生黄色液体 石墨极附近颜色变深,铂极附近颜色变浅
产生黄色液体 铂极附近颜色变深,石墨极附近颜色变浅
下列推断正确的是
A.用丁达尔效应可以确定①、②试管里的液体是否是胶体
B.①和②试管中都发生了氧化还原反应
C.①试管制备的碘化银胶体带正电荷
D.碘化银胶粒带电性与加入试剂顺序有关
15.下列关于物质分类的正确组合是
碱 酸 盐 碱性氧化物 酸性氧化物
A 纯碱 硫酸 小苏打 氧化钙 干冰
B 烧碱 盐酸 食盐 氧化钠 一氧化碳
C 石灰水 碳酸钙 过氧化钠 二氧化硫
D HNO3 Na2SiO3 氧化铁 三氧化硫
A.A B.B C.C D.D
二、填空题
16.酸的性质(以H2SO4为例)
(1)酸碱指示剂变色:_______。
(2)与活泼金属反应:如与Zn反应_______,反应类型为置换反应。
(3)与碱的中和反应:如与NaOH反应 _______,反应类型为复分解反应。
(4)与碱性氧化物反应:如与CuO反应 _______,反应类型为复分解反应。
(5)与某些盐反应:如与Na2CO3反应_______,反应类型为复分解反应。
17.用下列物质的序号填空:
①空气 ②铜片 ③高锰酸钾 ④无水乙醇 ⑤豆浆 ⑥干冰 ⑦苛性钠,其中属于混合物的是______,属于胶体的是__________,属于电解质的是 ________,属于非电解质的是___________。
18.I.对于数以千万计的化学物质和如此丰富的化学变化,分类法的作用几乎是无可替代的。如:纯净物根据其组成和性质可进行如下分类。
(1)如图所示的分类方法属于_______。
(2)某化学兴趣小组对下列四组物质进行研究:
A.
B.
C.溶液、蒸馏水、悬浊液、胶体
D.
填写下列空白:
A组 B组 C组 D组
分类标准 含氧酸 _______ 分散系 _______
不属于该类别的物质 _______ _______ Fe2O3
II.现有下列七种物质:① ②铝 ③ ④ ⑤硝酸 ⑥ ⑦氢氧化铁悬浊液
(3)其中属于混合物的是_______,属于氧化物的是_______,属于单质的是_______(均填序号)。
(4)上述物质中有两种易溶于水的物质之间可发生酸碱中和反应,该反应对应的化学方程式为_______。
III.甘肃马家窑遗址出土的青铜刀是我国最早冶炼的青铜器,由于时间久远,其表面有一层“绿锈”,“绿锈”俗称“铜绿”,是铜和空气中的水蒸气、、作用产生的,化学式为,“铜绿”能跟酸反应生成铜盐、和。某同学利用以下反应实现了“铜→铜绿→……→铜”的转化。
(5)从物质分类标准看,“铜绿”属于_______(填字母)。
A.酸 B.碱 C.盐 D.氧化物
(6)写出B的化学式:_______。
(7)请写出铜绿与盐酸反应的化学方程式:_______。
(8)上述转化过程中属于化合反应的是_______。
三、元素或物质推断题
19.给图中①~⑤选择适当的物质,使连有“-”线的两物质能发生反应。供选择的试剂有稀硫酸、二氧化碳、铜片、食盐、生石灰、一氧化碳、碳酸钾、铝片和木炭粉。
(1)请推断它们的化学式分别为①______;②______;③_____;④______;⑤_____。
(2)写出下列序号物质之间反应的化学方程式:
①和②:_______;
②和④:_______;
②和⑤:_______;
④和⑤:_______。
四、实验题
20.甲、乙两同学分别进行Fe(OH)3胶体的制备及相关实验。试回答下列问题:
(1)甲同学向25 mL沸水中逐滴加入5~6滴FeCl3饱和溶液;继续加热,最终得到悬浊液,可能的原因是___________;
(2)乙同学向25 mL煮沸的蒸馏水中逐滴加入5~6滴FeCl3饱和溶液;继续煮沸至溶液呈___________,停止加热;
(3)制备Fe(OH)3胶体涉及的化学反应方程式为___________;
(4)检验乙同学胶体制备是否成功的方法是___________效应,若制备成功,乙同学利用所制得的Fe(OH)3胶体进行下列实验:
①将其装入U形管内,用石墨作电极,接通直流电,通电一段时间后发现阴极附近的颜色逐渐变深,这表明Fe(OH)3胶粒带___________电荷(填“正”或“负”);
②向其中加入稀H2SO4溶液,产生的现象___________;
③欲对该实验制得的胶体进行提纯,应该采取的方法是___________。
【参考答案】
一、选择题
1.A
解析:A.稀硫酸是硫酸的水溶液,属于混合物,故A正确;
B.Cu2(OH)2CO3能电离出碳酸根离子、铜离子、氢氧根离子,属于盐,故B错误;
C.NH3·H2O电离出的阴离子全是氢氧根离子,NH3·H2O属于碱,故C错误;
D.氧化物中只含两种元素,HCOOH含有C、H、O三种元素,HCOOH不是氧化物,故D错误;
选A。
2.D
解析:A.Fe和盐酸反应生成FeCl2和氢气,故不选A;
B.H2O2受热分解为水和氧气,故不选B;
C.CaCl2溶液和二氧化碳不反应,故不选C;
D.CuSO4溶液和铁反应生成硫酸亚铁和铜,铜和氧气反应生成CuO,故选D;
选D。
3.A
解析:A.广彩人物纹大碗主要成分为硅酸盐,属于无机非金属材料,不属于合金,A正确;
B.明代铁锚主要成分是铁合金,属于合金材料,B错误;
C.海兽葡萄纹铜镜为铜锡合金,由金属材料制成,C错误;
D.鎏金转鸭广钟主要成分是铜和真金,属于合金材料,D错误;
故选A。
4.D
解析:A.Fe(OH)3胶体的分散质微粒直径比较大,能够使光线发生散射作用而沿直线传播,即光束照射Fe(OH)3胶体时能够发生丁达尔效应,A正确;
B.胶体分散质微粒直径小于滤纸缝隙,因此能够通过滤纸,故将得到Fe(OH)3胶体与溶液的混合物放在过滤器上进行过滤,滤纸上无残留固体,B正确;
C.Fe(OH)3胶体粒子直径比较大,能够选择性吸附正电荷而带正电,因此通直流电时,Fe(OH)3胶体粒子会向负电荷较多的阴极定向移动,C正确;
D.Fe(OH)3胶体粒子表面积大,具有强的吸附性,能够吸附水中悬浮的固体小颗粒,使之形成沉淀而析出,因此具有净水作用;但其不具有强氧化性,因此不能可用于水的消毒,D错误;
故合理选项是D。
5.A
【分析】在水溶液或熔融态可以导电的化合物为电解质;在水溶液和熔融态均不导电的化合物为非电解质。
解析:A.Na2SO4为电解质,CO2为非电解质,故A正确;
B.铜为单质,既不是电解质也不是非电解质,二氧化硫为非电解质,故B错误;
C.NaCl、BaSO4两者均为电解质,故C错误;
D.稀盐酸为混合物,既不是电解质也不是非电解质,氨气是非电解质,故D错误;
故选A。
6.B
解析:A.小苏打即NaHCO3为酸式盐,不是正盐,故A错误;
B.HClO3为氯酸,属于酸,故B正确;
C.苛性钠即NaOH为碱,不是盐,故C错误;
D.纯碱即Na2CO3,是盐不是碱,故D错误;
故选B。
7.D
解析:A.纳米碳酸钙是将碳酸钙粉碎为纳米级大小,但没有形成混合物,因此与胶体不具有相似的性质,A错误;
B.将碳酸钙粉碎为纳米级大小,但没有形成分散系,因此纳米碳酸钙不会产生丁达尔效应,B错误;
C.纳米碳酸钙和原来碳酸钙是同种物质,因此化学性质完全相同,C错误;
D.纳米碳酸钙的粒子直径比滤纸的缝隙直径小,因此能透过滤纸,D正确;
故合理选项是D。
8.C
解析:溶液的微粒直径小于1nm,浊液的微粒直径大于100nm,胶体的微粒直径为1-100nm之间,则纳米级(1~100nm,)的超细粉末粒子与胶体的微粒直径具有相同数量级,故选C。
9.A
解析:A.0.3%的高锰酸钾溶液即KMnO4,有效成分属于盐,故A符合题意;
B.3%的双氧水即H2O2,有效成分属于氧化物,故B不符合题意;
C.15%的过氧乙酸溶液即CH3COOOH,有效成分属于有机物,故C不符合题意;
D.75%的医用酒精即CH3CH2OH,有效成分属于氧化物,故D不符合题意。
综上所述,答案为A。
10.B
解析:A.丁达尔现象是胶体的性质,光线透过胶体时,胶体中可发生丁达尔效应,故A正确;
B.胶体具有丁达尔现象,溶液无此性质,用聚光手电筒照射NaCl溶液和Fe(OH)3胶体时,产生的现象不相同,故B错误;
C.Fe(OH)3胶体具有较大的表面积,具有吸附悬浮杂质的作用,Fe(OH)3胶体能够吸附水中悬浮的固体颗粒并沉降,达到净水目的,故C正确;
D.分散质微粒直径大小是分散系的本质区别,胶体区别于其他分散系的本质特征是分散质的微粒直径在1~100nm之间,故D正确。
故答案选:B。
11.A
解析:A.粉碎石灰石只是改变石灰石的形状,是物理变化,A符合题意;
B.煅烧石灰石,碳酸钙受热分解生成氧化钙和二氧化碳,是化学变化,B不符合题意;
C.石灰遇水,氧化钙和水反应生成氢氧化钙,是化学变化,C不符合题意;
D.石灰与二氧化碳生成碳酸钙,是化学变化,D不符合题意;
故答案选A。
12.B
解析:A.CO是不成盐氧化物,不是碱性氧化物,故A错误;
B.HClO属于酸、属于碱、NaHCO3属于盐、CaO是碱性氧化物、SO2是酸性氧化物,故B正确;
C.Na2CO3属于盐,不是碱,故C错误;
D.NaHSO4属于盐、NO是不成盐氧化物,故D错误;
故选B。
13.A
【分析】只有当光线通过胶体时才可能产生丁达尔效应,据此分析解答。
解析:①当光束通过Fe(OH)3胶体时,会使光线发生散射作用而有一条光亮的通路,即产生了丁达尔效应,①符合题意;
②盐酸是溶液,不属于胶体,故当光束通过水时不会出现丁达尔效应, ②不符合题意;
③蔗糖溶液属于溶液,不属于胶体,因此当光束通过蔗糖水溶液时不会出现丁达尔效应, ③不符合题意;
④云、雾属于胶体,故当光束通过云、雾等胶体时,会使光线发生散射作用而产生丁达尔效应,④符合题意;
⑤豆浆属于胶体,因此当光束通过时会出现丁达尔效应, ⑤符合题意;
选A。
14.A
解析:A.胶体能产生丁达尔效应,溶液不能产生,A项正确;
B.硝酸银和碘化钾混合发生复分解反应,B项错误;
C.胶体是分散系,不显电性,胶粒带电荷,C项错误;
D.碘化银胶粒可能带正电荷,也可能带负电荷,与反应物相对量有关。①试管中AgNO3过量,胶粒带正电荷;②试管中KI过量,胶粒带负电荷,D项错误。
故选A。
15.D
解析:A.纯碱是碳酸钠,属于盐,故A错误;
B.一氧化碳既不是酸性氧化物又不是碱性氧化物,故B错误;
C.是盐、过氧化钠是过氧化物,故C错误;
D.电离出的阴离子全是氢氧根离子,是碱;HNO3是含氧酸;Na2SiO3是硅酸盐;氧化铁与盐酸反应生成氯化铁和水,氧化铁是碱性氧化物;三氧化硫和氢氧化钠反应生成硫酸钠和水,三氧化硫是酸性氧化物,故D正确;
选D。
二、填空题
16.(1)遇石蕊试液变红
(2)Zn+H2SO4=ZnSO4+H2↑
(3)2NaOH+H2SO4=Na2SO4+2H2O
(4)CuO+H2SO4=CuSO4+H2O
(5)H2SO4+Na2CO3=Na2SO4+CO2↑+H2O
解析:酸是电离产生的阳离子全部是H+,阴离子是酸根阴离子的化合物。由于都可以电离产生H+,因此酸具有通性。
(1)H2SO4是酸,具有酸的通性,可以使紫色石蕊试液变红色;
(2)H2SO4与比较活泼金属Zn发生置换反应产生ZnSO4、H2,该反应的化学方程式为:Zn+H2SO4=ZnSO4+H2↑;
(3)H2SO4与碱NaOH反应产生Na2SO4、H2O,反应的化学方程式为:2NaOH+H2SO4=Na2SO4+2H2O;
(4)H2SO4与碱性氧化物如CuO反应产生CuSO4、H2O,反应的化学方程式为:CuO+H2SO4=CuSO4+H2O;
(5)H2SO4与盐Na2CO3反应,产生Na2SO4、H2O、CO2,反应的化学方程式为:H2SO4+Na2CO3=Na2SO4+CO2↑+H2O。
17. ①⑤ ⑤ ③⑦ ④⑥
【分析】由两种或多种物质混合而成的物质为混合物;分散质粒子直径在1~100nm之间的分散系为胶体;在水溶液或熔融状态下能导电的化合物为电解质;在水溶液和熔融状态下不能导电的化合物为非电解质,根据概念进行分析判断。
解析:根据概念可知:①空气为混合物; ②铜片为金属单质,能导电,但不是电解质,也不是非电解质;③高锰酸钾是在水溶液或熔融状态下能导电的化合物,属于电解质;④无水乙醇,水溶液中不导电,属于非电解质;⑤豆浆的分散质离子直径在1~100nm之间,属于胶体,也是混合物;⑥干冰,属于非电解质;⑦苛性钠的主要成分是NaOH,属于电解质;因此属于混合物的是①⑤;属于胶体的是⑤;属于电解质的是③⑦;属于非电解质的是④⑥。
18.(1)树状分类法
(2) HCl 阳离子种类 蒸馏水 碱
(3) ⑦ ③④ ①②
(4)2HNO3+=Ba(NO3)2+2H2O
(5)C
(6)CuO
(7)
(8)①
解析:(1)将同类事物按照某种属性进行分类,按照层次,一层一层来分,就像一棵大树,该分类方法为树状分类法。
(2)A组中均属于酸,其中除HCl外,其余均为含氧酸;B组中均属于盐,除外,其余盐中阳离子均为Na+;C组溶液、蒸馏水、悬浊液、胶体中,除纯净物蒸馏水外,其余均属于分散系;D组中,除氧化物Fe2O3外,其余均属于碱。
(3)七种物质:① ②铝 ③ ④ ⑤硝酸 ⑥ ⑦氢氧化铁悬浊液中,属于混合物的有:⑦氢氧化铁悬浊液;属于氧化物的有:③、④;属于单质的有:① ②铝。
(4)上述7种物质中易溶于水的酸为硝酸,易溶于水的碱为,二者发生酸碱中和的化学方程式为2HNO3+=Ba(NO3)2+2H2O。
(5)铜绿化学式为,化学式可改写为Cu(OH)2·CuCO3,属于盐类化合物,故答案为C。
(6)Cu(OH)2属于弱碱,具有不稳定性,受热易分解为CuO,CuO与H2在加热条件下发生置换反应生成Cu,因此B的化学式为CuO。
(7)铜绿化学式为,能跟酸反应生成铜盐、和,因此铜绿与盐酸反应的化学方程式为。
(8)铜绿属于难溶性盐,无法直接与碱反应生成Cu(OH)2,因此需要先将铜绿转化为可溶铜盐,再利用可溶铜盐与碱反应生成Cu(OH)2,因此②为酸,③为碱,即转化流程为,其中属于化合反应的为铜与空气中水蒸气、、反应生成铜绿,故答案为①。
三、元素或物质推断题
19. Al H2SO4 CO2 CaO K2CO3 2Al+3H2SO4=Al2(SO4)3+3H2↑ H2SO4+CaO=CaSO4↓+H2O H2SO4+K2CO3=K2SO4+H2O+CO2↑ H2O+CaO+K2CO3=CaCO3↓+2KOH
【分析】根据可供选择的试剂(稀硫酸、二氧化碳、铜片、食盐、生石灰、一氧化碳、碳酸钾、铝片和木炭粉可知,其中属于酸的只有硫酸,②是H2SO4;能与硫酸反应的单质是铝片,①是Al;能与硫酸反应的盐和氧化物分别为碳酸钾和生石灰,⑤是K2CO3,④是CaO;能与生石灰反应的氧化物为二氧化碳,③是CO2,由此分析。
解析:(1)根据分析,各物质的化学式分别为①Al;②H2SO4;③CO2;④CaO;⑤K2CO3;
(2)根据分析:①是Al,②是H2SO4,Al和H2SO4反应生成硫酸铝和氢气,化学方程式为:2Al+3H2SO4=Al2(SO4)3+3H2↑;
②是H2SO4,④是CaO,H2SO4和CaO反应生成硫酸钙和水,化学方程式为:H2SO4+CaO=CaSO4↓+H2O;
②是H2SO4,⑤是K2CO3,H2SO4和K2CO3反应生成硫酸钾、水、二氧化碳,化学方程式为:H2SO4+K2CO3=K2SO4+H2O+CO2↑;
④是CaO,⑤是K2CO3,CaO和K2CO3溶液反应生成碳酸钙和氢氧化钾,化学方程式为:H2O+CaO+K2CO3=CaCO3↓+2KOH。
四、实验题
20.(1)未用蒸馏水而用自来水煮沸
(2)红褐色
(3)FeCl3+3H2OFe(OH)3(胶体)+3HCl
(4) 丁达尔 正 先产生红褐色沉淀,后沉淀溶解,溶液变为浅黄色 渗析
解析:(1)自来水中有矿物质离子,胶体遇电解质离子会聚沉,因此甲同学得到悬浊液,可能是用自来水煮沸,故答案为:未用蒸馏水而用自来水煮沸;
(2)Fe(OH)3胶体为红褐色,因此乙同学因煮沸至溶液呈红褐色再停止加热,故答案为:红褐色;
(3)用FeCl3饱和溶液制备Fe(OH)3胶体的化学反应方程式为:FeCl3+3H2OFe(OH)3(胶体)+3HCl,故答案为:FeCl3+3H2OFe(OH)3(胶体)+3HCl;
(4)胶体具有丁达尔效应:当光束通过胶体时,从侧面观察到一条光亮的“通路”,则证明有胶体生成;①胶体胶粒带电,胶体具有电泳性质,将Fe(OH)3胶体装入U形管内,用石墨作电极,接通直流电,与负极相连的阴极附近的颜色逐渐变深,说明胶粒向负极移动,Fe(OH)3胶粒带正电;②加入稀H2SO4溶液会使Fe(OH)3胶体聚沉为Fe(OH)3沉淀,H2SO4还会溶解Fe(OH)3沉淀生成Fe2(SO4)3,Fe3+为黄色离子,产生的现象为先产生红褐色沉淀,后沉淀溶解,溶液变为浅黄色;③胶体粒子不可以透过半透膜,而小分子、离子等可以透过半透膜,所以可用渗析法提纯胶体;故答案为:丁达尔;正;先产生红褐色沉淀,后沉淀溶解,溶液变为浅黄色;渗析。
一、选择题
1.下列有关物质的分类正确的是
A.混合物:稀硫酸 B.碱:Cu2(OH)2CO3 C.盐:NH3.H2O D.氧化物:HCOOH
2.下列物质下列物质间的每一个转化都能通过一步反应实现的是
A.Fe2O3FeFeCl3 B.H2O2H2H2O
C.CaCl2溶液CaCO3CO2 D.CuSO4溶液CuCuO
3.下列广州博物馆馆藏文物中,不属于由金属材料制成的是
文物
选项 A.广彩人物纹大碗 B.明代铁锚 C.海兽葡萄纹铜镜 D.鎏金转鸭广钟
A.A B.B C.C D.D
4.将FeCl3饱和溶液逐滴滴入到沸水中,再加热至红褐色即得到Fe(OH)3胶体。下列说法错误的是
A.光束照射Fe(OH)3胶体时会产生丁达尔现象
B.将所得胶体过滤,滤纸上无残留固体
C.通直流电时,Fe(OH)3胶体粒子会定向移动
D.Fe(OH)3胶体粒子有吸附性,可用于水的消毒
5.下列各组物质,前者属于电解质,后者属于非电解质的是
A.Na2SO4、CO2 B.Cu、SO2 C.NaCl、BaSO4 D.稀盐酸、NH3
6.下列各物质的分类、名称(或俗名)、化学式都正确的是
选项 分类 名称(或俗名) 化学式
A 正盐 小苏打 NaHCO3
B 酸 氯酸 HClO3
C 盐 苛性钠 NaOH
D 碱 纯碱 Na2CO3
A.A B.B C.C D.D
7.有人设想将碳酸钙通过特殊的加工方法使之变为纳米碳酸钙(即碳酸钙粒子直径是纳米级),这将引起建筑材料的性能发生巨变。下列关于纳米碳酸钙的推测可能正确的是
A.纳米碳酸钙是与胶体相似的分散系
B.纳米碳酸钙会产生丁达尔效应
C.纳米碳酸钙化学性质已与原来碳酸钙完全不同
D.纳米碳酸钙的粒子能透过滤纸
8.用特殊方法把固体物质加工到纳米级(1~100nm,)的超细粉末粒子,然后制得纳米材料,下列分散系中的分散质的微粒直径和这种粒子具有相同数量级的是
A.溶液 B.悬浊液 C.胶体 D.乳浊液
9.为了控制疾病,经常会用到各类消毒剂。下列消毒剂的有效成分属于盐的是
A.0.3%的高锰酸钾溶液 B.3%的双氧水
C.15%的过氧乙酸溶液 D.75%的医用酒精
10.下列关于胶体的叙述不正确的是
A.光线透过胶体时,胶体中可发生丁达尔效应
B.用平行光照射溶液和胶体时,产生的现象相同
C.胶体能吸附水中悬浮物形成固体颗粒沉降,达到净水目的
D.胶体区别其他分散系本质特征是分散质的微粒直径在1~100nm之间
11.于谦的《石灰吟》,赞颂了石灰石(碳酸钙)“粉骨碎身浑不怕,要留清白在人间”的品格。石灰(CaO)可用于治病在我国早已有之。《本草经注》中记载有“今近山生石,青白色,作灶烧竟,以水沃之,即热蒸而解末矣”,该记载描述了碳酸钙煅烧成石灰,石灰再遇水时的现象。下列过程中未发生化学变化的是
A.粉碎石灰石 B.煅烧石灰石 C.石灰遇水 D.石灰遇二氧化碳
12.下列关于物质的分类正确的是
酸 碱 盐 碱性氧化物 酸性氧化物
A CO
B HClO CaO
C
D KOH NaCl NO
A.A B.B C.C D.D
13.当光束通过下列物质时,会出现丁达尔效应的是
①胶体 ②盐酸 ③蔗糖溶液 ④云、雾 ⑤豆浆
A.①④⑤ B.②③⑤ C.②③④ D.①④
14.实验表明,在如图装置中,带负电荷的胶粒向Pt(铂)极迁移,带正电荷的胶粒向石墨(C)极迁移,这种现象叫“电泳现象”。某小组制备AgI胶体并探究其性质,有关信息如表所示(注明:AgI胶体呈黄色)
操作 化学反应现象 电泳实验现象
产生黄色液体 石墨极附近颜色变深,铂极附近颜色变浅
产生黄色液体 铂极附近颜色变深,石墨极附近颜色变浅
下列推断正确的是
A.用丁达尔效应可以确定①、②试管里的液体是否是胶体
B.①和②试管中都发生了氧化还原反应
C.①试管制备的碘化银胶体带正电荷
D.碘化银胶粒带电性与加入试剂顺序有关
15.下列关于物质分类的正确组合是
碱 酸 盐 碱性氧化物 酸性氧化物
A 纯碱 硫酸 小苏打 氧化钙 干冰
B 烧碱 盐酸 食盐 氧化钠 一氧化碳
C 石灰水 碳酸钙 过氧化钠 二氧化硫
D HNO3 Na2SiO3 氧化铁 三氧化硫
A.A B.B C.C D.D
二、填空题
16.酸的性质(以H2SO4为例)
(1)酸碱指示剂变色:_______。
(2)与活泼金属反应:如与Zn反应_______,反应类型为置换反应。
(3)与碱的中和反应:如与NaOH反应 _______,反应类型为复分解反应。
(4)与碱性氧化物反应:如与CuO反应 _______,反应类型为复分解反应。
(5)与某些盐反应:如与Na2CO3反应_______,反应类型为复分解反应。
17.用下列物质的序号填空:
①空气 ②铜片 ③高锰酸钾 ④无水乙醇 ⑤豆浆 ⑥干冰 ⑦苛性钠,其中属于混合物的是______,属于胶体的是__________,属于电解质的是 ________,属于非电解质的是___________。
18.I.对于数以千万计的化学物质和如此丰富的化学变化,分类法的作用几乎是无可替代的。如:纯净物根据其组成和性质可进行如下分类。
(1)如图所示的分类方法属于_______。
(2)某化学兴趣小组对下列四组物质进行研究:
A.
B.
C.溶液、蒸馏水、悬浊液、胶体
D.
填写下列空白:
A组 B组 C组 D组
分类标准 含氧酸 _______ 分散系 _______
不属于该类别的物质 _______ _______ Fe2O3
II.现有下列七种物质:① ②铝 ③ ④ ⑤硝酸 ⑥ ⑦氢氧化铁悬浊液
(3)其中属于混合物的是_______,属于氧化物的是_______,属于单质的是_______(均填序号)。
(4)上述物质中有两种易溶于水的物质之间可发生酸碱中和反应,该反应对应的化学方程式为_______。
III.甘肃马家窑遗址出土的青铜刀是我国最早冶炼的青铜器,由于时间久远,其表面有一层“绿锈”,“绿锈”俗称“铜绿”,是铜和空气中的水蒸气、、作用产生的,化学式为,“铜绿”能跟酸反应生成铜盐、和。某同学利用以下反应实现了“铜→铜绿→……→铜”的转化。
(5)从物质分类标准看,“铜绿”属于_______(填字母)。
A.酸 B.碱 C.盐 D.氧化物
(6)写出B的化学式:_______。
(7)请写出铜绿与盐酸反应的化学方程式:_______。
(8)上述转化过程中属于化合反应的是_______。
三、元素或物质推断题
19.给图中①~⑤选择适当的物质,使连有“-”线的两物质能发生反应。供选择的试剂有稀硫酸、二氧化碳、铜片、食盐、生石灰、一氧化碳、碳酸钾、铝片和木炭粉。
(1)请推断它们的化学式分别为①______;②______;③_____;④______;⑤_____。
(2)写出下列序号物质之间反应的化学方程式:
①和②:_______;
②和④:_______;
②和⑤:_______;
④和⑤:_______。
四、实验题
20.甲、乙两同学分别进行Fe(OH)3胶体的制备及相关实验。试回答下列问题:
(1)甲同学向25 mL沸水中逐滴加入5~6滴FeCl3饱和溶液;继续加热,最终得到悬浊液,可能的原因是___________;
(2)乙同学向25 mL煮沸的蒸馏水中逐滴加入5~6滴FeCl3饱和溶液;继续煮沸至溶液呈___________,停止加热;
(3)制备Fe(OH)3胶体涉及的化学反应方程式为___________;
(4)检验乙同学胶体制备是否成功的方法是___________效应,若制备成功,乙同学利用所制得的Fe(OH)3胶体进行下列实验:
①将其装入U形管内,用石墨作电极,接通直流电,通电一段时间后发现阴极附近的颜色逐渐变深,这表明Fe(OH)3胶粒带___________电荷(填“正”或“负”);
②向其中加入稀H2SO4溶液,产生的现象___________;
③欲对该实验制得的胶体进行提纯,应该采取的方法是___________。
【参考答案】
一、选择题
1.A
解析:A.稀硫酸是硫酸的水溶液,属于混合物,故A正确;
B.Cu2(OH)2CO3能电离出碳酸根离子、铜离子、氢氧根离子,属于盐,故B错误;
C.NH3·H2O电离出的阴离子全是氢氧根离子,NH3·H2O属于碱,故C错误;
D.氧化物中只含两种元素,HCOOH含有C、H、O三种元素,HCOOH不是氧化物,故D错误;
选A。
2.D
解析:A.Fe和盐酸反应生成FeCl2和氢气,故不选A;
B.H2O2受热分解为水和氧气,故不选B;
C.CaCl2溶液和二氧化碳不反应,故不选C;
D.CuSO4溶液和铁反应生成硫酸亚铁和铜,铜和氧气反应生成CuO,故选D;
选D。
3.A
解析:A.广彩人物纹大碗主要成分为硅酸盐,属于无机非金属材料,不属于合金,A正确;
B.明代铁锚主要成分是铁合金,属于合金材料,B错误;
C.海兽葡萄纹铜镜为铜锡合金,由金属材料制成,C错误;
D.鎏金转鸭广钟主要成分是铜和真金,属于合金材料,D错误;
故选A。
4.D
解析:A.Fe(OH)3胶体的分散质微粒直径比较大,能够使光线发生散射作用而沿直线传播,即光束照射Fe(OH)3胶体时能够发生丁达尔效应,A正确;
B.胶体分散质微粒直径小于滤纸缝隙,因此能够通过滤纸,故将得到Fe(OH)3胶体与溶液的混合物放在过滤器上进行过滤,滤纸上无残留固体,B正确;
C.Fe(OH)3胶体粒子直径比较大,能够选择性吸附正电荷而带正电,因此通直流电时,Fe(OH)3胶体粒子会向负电荷较多的阴极定向移动,C正确;
D.Fe(OH)3胶体粒子表面积大,具有强的吸附性,能够吸附水中悬浮的固体小颗粒,使之形成沉淀而析出,因此具有净水作用;但其不具有强氧化性,因此不能可用于水的消毒,D错误;
故合理选项是D。
5.A
【分析】在水溶液或熔融态可以导电的化合物为电解质;在水溶液和熔融态均不导电的化合物为非电解质。
解析:A.Na2SO4为电解质,CO2为非电解质,故A正确;
B.铜为单质,既不是电解质也不是非电解质,二氧化硫为非电解质,故B错误;
C.NaCl、BaSO4两者均为电解质,故C错误;
D.稀盐酸为混合物,既不是电解质也不是非电解质,氨气是非电解质,故D错误;
故选A。
6.B
解析:A.小苏打即NaHCO3为酸式盐,不是正盐,故A错误;
B.HClO3为氯酸,属于酸,故B正确;
C.苛性钠即NaOH为碱,不是盐,故C错误;
D.纯碱即Na2CO3,是盐不是碱,故D错误;
故选B。
7.D
解析:A.纳米碳酸钙是将碳酸钙粉碎为纳米级大小,但没有形成混合物,因此与胶体不具有相似的性质,A错误;
B.将碳酸钙粉碎为纳米级大小,但没有形成分散系,因此纳米碳酸钙不会产生丁达尔效应,B错误;
C.纳米碳酸钙和原来碳酸钙是同种物质,因此化学性质完全相同,C错误;
D.纳米碳酸钙的粒子直径比滤纸的缝隙直径小,因此能透过滤纸,D正确;
故合理选项是D。
8.C
解析:溶液的微粒直径小于1nm,浊液的微粒直径大于100nm,胶体的微粒直径为1-100nm之间,则纳米级(1~100nm,)的超细粉末粒子与胶体的微粒直径具有相同数量级,故选C。
9.A
解析:A.0.3%的高锰酸钾溶液即KMnO4,有效成分属于盐,故A符合题意;
B.3%的双氧水即H2O2,有效成分属于氧化物,故B不符合题意;
C.15%的过氧乙酸溶液即CH3COOOH,有效成分属于有机物,故C不符合题意;
D.75%的医用酒精即CH3CH2OH,有效成分属于氧化物,故D不符合题意。
综上所述,答案为A。
10.B
解析:A.丁达尔现象是胶体的性质,光线透过胶体时,胶体中可发生丁达尔效应,故A正确;
B.胶体具有丁达尔现象,溶液无此性质,用聚光手电筒照射NaCl溶液和Fe(OH)3胶体时,产生的现象不相同,故B错误;
C.Fe(OH)3胶体具有较大的表面积,具有吸附悬浮杂质的作用,Fe(OH)3胶体能够吸附水中悬浮的固体颗粒并沉降,达到净水目的,故C正确;
D.分散质微粒直径大小是分散系的本质区别,胶体区别于其他分散系的本质特征是分散质的微粒直径在1~100nm之间,故D正确。
故答案选:B。
11.A
解析:A.粉碎石灰石只是改变石灰石的形状,是物理变化,A符合题意;
B.煅烧石灰石,碳酸钙受热分解生成氧化钙和二氧化碳,是化学变化,B不符合题意;
C.石灰遇水,氧化钙和水反应生成氢氧化钙,是化学变化,C不符合题意;
D.石灰与二氧化碳生成碳酸钙,是化学变化,D不符合题意;
故答案选A。
12.B
解析:A.CO是不成盐氧化物,不是碱性氧化物,故A错误;
B.HClO属于酸、属于碱、NaHCO3属于盐、CaO是碱性氧化物、SO2是酸性氧化物,故B正确;
C.Na2CO3属于盐,不是碱,故C错误;
D.NaHSO4属于盐、NO是不成盐氧化物,故D错误;
故选B。
13.A
【分析】只有当光线通过胶体时才可能产生丁达尔效应,据此分析解答。
解析:①当光束通过Fe(OH)3胶体时,会使光线发生散射作用而有一条光亮的通路,即产生了丁达尔效应,①符合题意;
②盐酸是溶液,不属于胶体,故当光束通过水时不会出现丁达尔效应, ②不符合题意;
③蔗糖溶液属于溶液,不属于胶体,因此当光束通过蔗糖水溶液时不会出现丁达尔效应, ③不符合题意;
④云、雾属于胶体,故当光束通过云、雾等胶体时,会使光线发生散射作用而产生丁达尔效应,④符合题意;
⑤豆浆属于胶体,因此当光束通过时会出现丁达尔效应, ⑤符合题意;
选A。
14.A
解析:A.胶体能产生丁达尔效应,溶液不能产生,A项正确;
B.硝酸银和碘化钾混合发生复分解反应,B项错误;
C.胶体是分散系,不显电性,胶粒带电荷,C项错误;
D.碘化银胶粒可能带正电荷,也可能带负电荷,与反应物相对量有关。①试管中AgNO3过量,胶粒带正电荷;②试管中KI过量,胶粒带负电荷,D项错误。
故选A。
15.D
解析:A.纯碱是碳酸钠,属于盐,故A错误;
B.一氧化碳既不是酸性氧化物又不是碱性氧化物,故B错误;
C.是盐、过氧化钠是过氧化物,故C错误;
D.电离出的阴离子全是氢氧根离子,是碱;HNO3是含氧酸;Na2SiO3是硅酸盐;氧化铁与盐酸反应生成氯化铁和水,氧化铁是碱性氧化物;三氧化硫和氢氧化钠反应生成硫酸钠和水,三氧化硫是酸性氧化物,故D正确;
选D。
二、填空题
16.(1)遇石蕊试液变红
(2)Zn+H2SO4=ZnSO4+H2↑
(3)2NaOH+H2SO4=Na2SO4+2H2O
(4)CuO+H2SO4=CuSO4+H2O
(5)H2SO4+Na2CO3=Na2SO4+CO2↑+H2O
解析:酸是电离产生的阳离子全部是H+,阴离子是酸根阴离子的化合物。由于都可以电离产生H+,因此酸具有通性。
(1)H2SO4是酸,具有酸的通性,可以使紫色石蕊试液变红色;
(2)H2SO4与比较活泼金属Zn发生置换反应产生ZnSO4、H2,该反应的化学方程式为:Zn+H2SO4=ZnSO4+H2↑;
(3)H2SO4与碱NaOH反应产生Na2SO4、H2O,反应的化学方程式为:2NaOH+H2SO4=Na2SO4+2H2O;
(4)H2SO4与碱性氧化物如CuO反应产生CuSO4、H2O,反应的化学方程式为:CuO+H2SO4=CuSO4+H2O;
(5)H2SO4与盐Na2CO3反应,产生Na2SO4、H2O、CO2,反应的化学方程式为:H2SO4+Na2CO3=Na2SO4+CO2↑+H2O。
17. ①⑤ ⑤ ③⑦ ④⑥
【分析】由两种或多种物质混合而成的物质为混合物;分散质粒子直径在1~100nm之间的分散系为胶体;在水溶液或熔融状态下能导电的化合物为电解质;在水溶液和熔融状态下不能导电的化合物为非电解质,根据概念进行分析判断。
解析:根据概念可知:①空气为混合物; ②铜片为金属单质,能导电,但不是电解质,也不是非电解质;③高锰酸钾是在水溶液或熔融状态下能导电的化合物,属于电解质;④无水乙醇,水溶液中不导电,属于非电解质;⑤豆浆的分散质离子直径在1~100nm之间,属于胶体,也是混合物;⑥干冰,属于非电解质;⑦苛性钠的主要成分是NaOH,属于电解质;因此属于混合物的是①⑤;属于胶体的是⑤;属于电解质的是③⑦;属于非电解质的是④⑥。
18.(1)树状分类法
(2) HCl 阳离子种类 蒸馏水 碱
(3) ⑦ ③④ ①②
(4)2HNO3+=Ba(NO3)2+2H2O
(5)C
(6)CuO
(7)
(8)①
解析:(1)将同类事物按照某种属性进行分类,按照层次,一层一层来分,就像一棵大树,该分类方法为树状分类法。
(2)A组中均属于酸,其中除HCl外,其余均为含氧酸;B组中均属于盐,除外,其余盐中阳离子均为Na+;C组溶液、蒸馏水、悬浊液、胶体中,除纯净物蒸馏水外,其余均属于分散系;D组中,除氧化物Fe2O3外,其余均属于碱。
(3)七种物质:① ②铝 ③ ④ ⑤硝酸 ⑥ ⑦氢氧化铁悬浊液中,属于混合物的有:⑦氢氧化铁悬浊液;属于氧化物的有:③、④;属于单质的有:① ②铝。
(4)上述7种物质中易溶于水的酸为硝酸,易溶于水的碱为,二者发生酸碱中和的化学方程式为2HNO3+=Ba(NO3)2+2H2O。
(5)铜绿化学式为,化学式可改写为Cu(OH)2·CuCO3,属于盐类化合物,故答案为C。
(6)Cu(OH)2属于弱碱,具有不稳定性,受热易分解为CuO,CuO与H2在加热条件下发生置换反应生成Cu,因此B的化学式为CuO。
(7)铜绿化学式为,能跟酸反应生成铜盐、和,因此铜绿与盐酸反应的化学方程式为。
(8)铜绿属于难溶性盐,无法直接与碱反应生成Cu(OH)2,因此需要先将铜绿转化为可溶铜盐,再利用可溶铜盐与碱反应生成Cu(OH)2,因此②为酸,③为碱,即转化流程为,其中属于化合反应的为铜与空气中水蒸气、、反应生成铜绿,故答案为①。
三、元素或物质推断题
19. Al H2SO4 CO2 CaO K2CO3 2Al+3H2SO4=Al2(SO4)3+3H2↑ H2SO4+CaO=CaSO4↓+H2O H2SO4+K2CO3=K2SO4+H2O+CO2↑ H2O+CaO+K2CO3=CaCO3↓+2KOH
【分析】根据可供选择的试剂(稀硫酸、二氧化碳、铜片、食盐、生石灰、一氧化碳、碳酸钾、铝片和木炭粉可知,其中属于酸的只有硫酸,②是H2SO4;能与硫酸反应的单质是铝片,①是Al;能与硫酸反应的盐和氧化物分别为碳酸钾和生石灰,⑤是K2CO3,④是CaO;能与生石灰反应的氧化物为二氧化碳,③是CO2,由此分析。
解析:(1)根据分析,各物质的化学式分别为①Al;②H2SO4;③CO2;④CaO;⑤K2CO3;
(2)根据分析:①是Al,②是H2SO4,Al和H2SO4反应生成硫酸铝和氢气,化学方程式为:2Al+3H2SO4=Al2(SO4)3+3H2↑;
②是H2SO4,④是CaO,H2SO4和CaO反应生成硫酸钙和水,化学方程式为:H2SO4+CaO=CaSO4↓+H2O;
②是H2SO4,⑤是K2CO3,H2SO4和K2CO3反应生成硫酸钾、水、二氧化碳,化学方程式为:H2SO4+K2CO3=K2SO4+H2O+CO2↑;
④是CaO,⑤是K2CO3,CaO和K2CO3溶液反应生成碳酸钙和氢氧化钾,化学方程式为:H2O+CaO+K2CO3=CaCO3↓+2KOH。
四、实验题
20.(1)未用蒸馏水而用自来水煮沸
(2)红褐色
(3)FeCl3+3H2OFe(OH)3(胶体)+3HCl
(4) 丁达尔 正 先产生红褐色沉淀,后沉淀溶解,溶液变为浅黄色 渗析
解析:(1)自来水中有矿物质离子,胶体遇电解质离子会聚沉,因此甲同学得到悬浊液,可能是用自来水煮沸,故答案为:未用蒸馏水而用自来水煮沸;
(2)Fe(OH)3胶体为红褐色,因此乙同学因煮沸至溶液呈红褐色再停止加热,故答案为:红褐色;
(3)用FeCl3饱和溶液制备Fe(OH)3胶体的化学反应方程式为:FeCl3+3H2OFe(OH)3(胶体)+3HCl,故答案为:FeCl3+3H2OFe(OH)3(胶体)+3HCl;
(4)胶体具有丁达尔效应:当光束通过胶体时,从侧面观察到一条光亮的“通路”,则证明有胶体生成;①胶体胶粒带电,胶体具有电泳性质,将Fe(OH)3胶体装入U形管内,用石墨作电极,接通直流电,与负极相连的阴极附近的颜色逐渐变深,说明胶粒向负极移动,Fe(OH)3胶粒带正电;②加入稀H2SO4溶液会使Fe(OH)3胶体聚沉为Fe(OH)3沉淀,H2SO4还会溶解Fe(OH)3沉淀生成Fe2(SO4)3,Fe3+为黄色离子,产生的现象为先产生红褐色沉淀,后沉淀溶解,溶液变为浅黄色;③胶体粒子不可以透过半透膜,而小分子、离子等可以透过半透膜,所以可用渗析法提纯胶体;故答案为:丁达尔;正;先产生红褐色沉淀,后沉淀溶解,溶液变为浅黄色;渗析。
