专题5微观结构与物质的多样性测试高一上学期化学苏教版(2019)必修第一册(含解析)
文档属性
| 名称 | 专题5微观结构与物质的多样性测试高一上学期化学苏教版(2019)必修第一册(含解析) |

|
|
| 格式 | docx | ||
| 文件大小 | 488.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-06-17 16:44:30 | ||
图片预览




文档简介
专题5 微观结构与物质的多样性 测试
一、单选题
1.短周期元素X、Y是元素周期表中第ⅦA族的两种元素,X原子的电子层数比Y原子的电子层数少。下列说法不正确的是
A.HX的酸性比HY的弱
B.X的最简单气态氢化物比Y的稳定
C.X的单质能将Y的单质从KY的水溶液中置换出来
D.X的非金属性比Y的强
2.下列说法正确的是
A.红磷转化为白磷,属于物理变化
B.石墨导电、金刚石不导电,故二者不是同素异形体
C.和分子式不同,化学性质相同
D.单质硫有、、等,它们都是硫的同素异形体
3.下列说法正确的是
A.第四周期元素中,锰原子价电子层中未成对电子数最多
B.含有极性键的分子一定是极性分子
C.丙氨酸()存在手性异构体
D.NaCl熔化和CO2气化克服的作用力类型相同
4.下列物质中,既含有非极性共价键又含有极性共价键是
A.NaOH B.H2O2 C.Na2O2 D.H2S
5.元素周期表和元素周期律可以指导人们进行规律性的推测和判断。下列说法不合理的是
A.由水溶液的酸性:HCl>HF,不能推断出元素的非金属性:Cl>F
B.人们可以在周期表的过渡元素中寻找催化剂和耐腐蚀、耐高温的合金材料
C.原子半径随着周期序数的增加而增加
D.短周期元素形成的微粒X2-和Y2+核外电子排布相同,离子半径:X2->Y2+
6.下列离子方程式书写正确的是
A.金属钠与水反应:
B.和溶液混合:
C.碳酸氢钠溶液与盐酸反应:
D.向溶液中加入过量的氨水:
7.下列关于物质性质的比较不正确的是
A.酸性: HClO4> HBrO4> HIO4
B.原子半径: Na>Al>S>Cl
C.非金属性: Cl>S>O>C
D.稳定性: HF> HCl> HBr> HI
8.下列化学用语的表示正确的是
A.乙烯的结构简式:CH2CH2
B.乙醇的分子式:C2H5OH
C.聚丙烯的结构简式:
D.乙烯的球棍模型:
9.下列说法中不正确的是
A.N2的电子式是 B.NaOH中既含有离子键也含有共价键
C.NaF属于盐 D.KI是常见的还原剂
10.下列物质的分类组合正确的是
①金刚石、氢氧化铁胶体、豆浆均为混合物;②HClO、CH3COOH、H2CO3均为酸;
③NaOH、NH4HCO3、KMnO4均为强电解质;④Na2O2、Na2O、MgO均为碱性氧化物;
⑤金刚石、石墨、C60互为同素异形体。
A.②⑤ B.②③⑤ C.①②③⑤ D.④⑤
11.下列化学用语正确的是
A.正丁烷的结构简式: B.丙烷分子的空间填充模型:
C.甲烷分子的球棍模型: D.羟基的电子式:
12.为实现“双碳”目标,某科研小组设计捕获二氧化碳生成甲酸的过程如图所示。下列说法正确的是(NA为阿伏加德罗常数的值)
A.标准状况下,22.4 L CO2中所含的电子数目为16NA
B.10.1 g N(C2H5)3中所含的非极性共价键数目为1.8NA
C.22 g CO2与N2O混合物中所含氧原子的数目为NA
D.100 g 46%的甲酸水溶液中所含的氧原子数目为5NA
13.氯元素的原子结构示意图为,下列说法正确的是
A.氯原子在化学反应中易失去电子
B.氯原子易得到电子形成稳定的氯离子
C.氯元素的化合价只有-1价
D.氯在元素周期表中位于第3周期第Ⅶ族
14.某酸根离子的电子数比硝酸根离子的电子数多10,则下列说法中正确的是
A.R与N原子电子层数相同
B.R与N原子最外层电子数相同
C.R与N的简单负离子所带的电荷数相同
D.中R元素与中N元素的化合价相同
15.根据元素周期律,下列推断错误的是
A.原子半径:C > N B.热稳定性:HF < HCl
C.还原性:Mg > Al D.碱性:NaOH<KOH
二、填空题
16.下图中的甲、乙、丙、丁代表化学中常见的四种物质,相互转化的关系如下所示。其中甲、乙、丙为均含有同一种金属元素的无机化合物,常温下0.1 mol/L的丁溶液pH为13,其焰色反应为黄色。
(1)请写出甲中加入过量的丁直接生成丙的离子方程式:______________________。
(2)请写出反应(Ⅲ)的离子方程式为___________________________。
17.利用物质的结构与性质对周期表进行研究,有助于我们更好地掌握同类知识。
I.2019年是元素周期表发表150周年,期间科学家为完善周期表做出了不懈努力。中国科学院院士张青莲教授曾主持测定了铟(49In)等9种元素相对原子质量的新值,被采用为国际新标准。
(1)In在周期表中的位置是_______。
(2)In的最高价氧化物对应的水化物的碱性_______Ba(OH)2的碱性(填“>”或“<”)。
(3)的中子数与电子数的差值为_______。
II.硒(34Se)是动物和人体所必需的微量元素之一,也是重要的工业原料,与氧同族。
(4)Se原子结构示意图可表示为_______。
(5)下列说法合理的是_______。
a.SeO2既有氧化性又有还原性 b.沸点:H2O < H2S < H2Se
c.热稳定性:H2Se18.氮化钠()是科学家制备的一种重要的化合物,它与水作用可产生。请回答下列问题:
(1)的电子式是_______,该化合物是由_______键形成的。
(2)与盐酸反应的化学方程式是_______。
(3)在题(2)反应的生成物中,含有共价键的是_______。
(4)比较中两种微粒的半径: _______。(填“>”“<”或“=”)
19.金属及其化合物在人类的历史上有着重要的作用。回答下列有关问题:
(1)向20 mL沸水中逐滴滴加2 mL饱和FeCl3溶液,继续加热至液体呈红褐色,形成的分散系中分散质微粒的直径大小范围是___________。
(2)最近两年,随着神舟号系列飞船和蛟龙号潜艇性能的进一步优化,我国已成功实现“上天入地”。在上天入地时,为了给工作仓内工作人员提供氧气,一般要携带一种淡黄色粉末,其化学式为___________,将其撒入脱脂棉,滴加几滴水,脱脂棉能被点燃,说明反应___________。
(3)电子工业上可用FeCl3溶液腐蚀电路板上的铜,写出该反应的离子方程式:___________。
(4)胃舒平(主要成分为氢氧化铝)可用于治疗胃酸过多,氢氧化铝体现___________性;___________(填“能”或“不能”)用氢氧化钠溶液代替。
(5)将硫酸亚铁与稀硫酸混合,二者不反应,滴入H2O2后,溶液很快变成黄色,该反应的离子方程式为___________。
(6)NaHSO4是一种酸式盐,写出NaHSO4在水中的电离方程式___________。
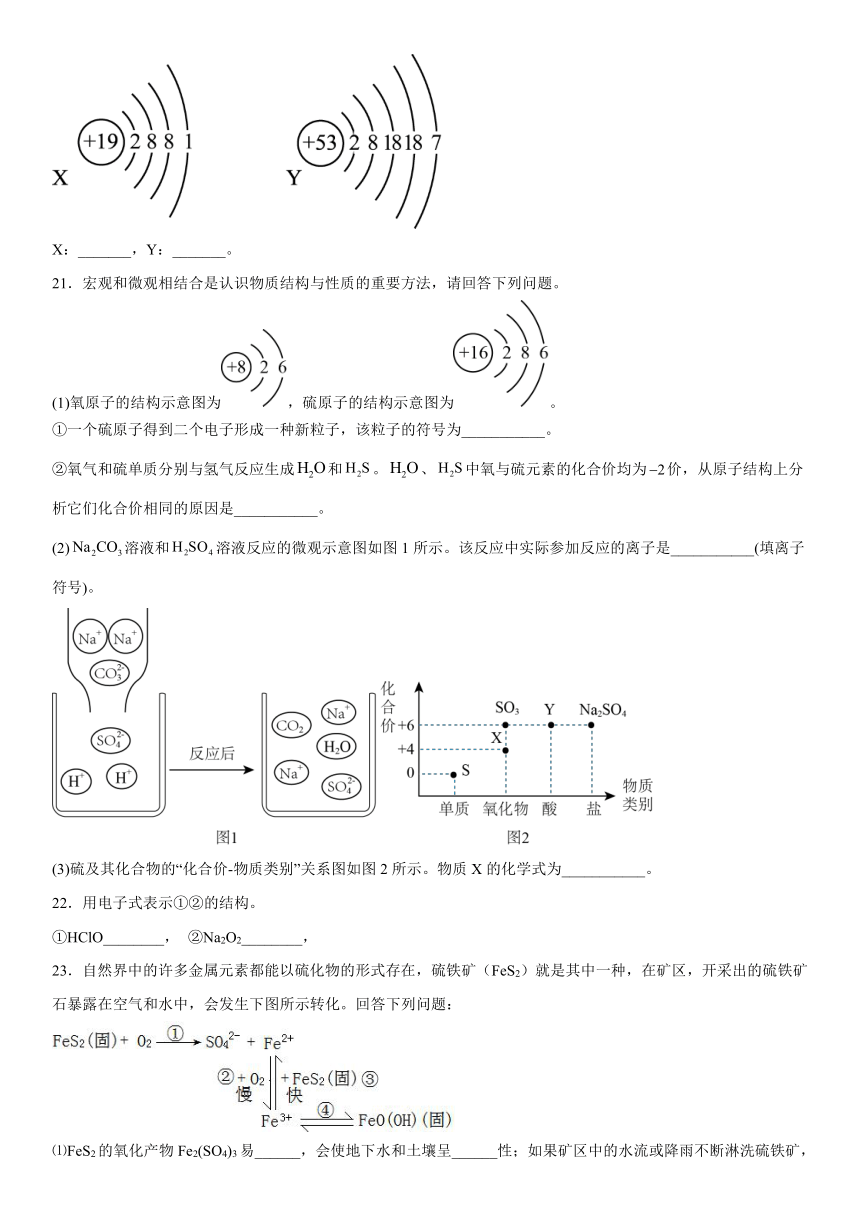
20.已知某主族元素的原子结构示意图如下,请写出它们在周期表中的位置。
X:_______,Y:_______。
21.宏观和微观相结合是认识物质结构与性质的重要方法,请回答下列问题。
(1)氧原子的结构示意图为,硫原子的结构示意图为。
①一个硫原子得到二个电子形成一种新粒子,该粒子的符号为___________。
②氧气和硫单质分别与氢气反应生成和。、中氧与硫元素的化合价均为价,从原子结构上分析它们化合价相同的原因是___________。
(2)溶液和溶液反应的微观示意图如图1所示。该反应中实际参加反应的离子是___________(填离子符号)。
(3)硫及其化合物的“化合价-物质类别”关系图如图2所示。物质X的化学式为___________。
22.用电子式表示①②的结构。
①HClO________, ②Na2O2________,
23.自然界中的许多金属元素都能以硫化物的形式存在,硫铁矿(FeS2)就是其中一种,在矿区,开采出的硫铁矿石暴露在空气和水中,会发生下图所示转化。回答下列问题:
⑴FeS2的氧化产物Fe2(SO4)3易______,会使地下水和土壤呈______性;如果矿区中的水流或降雨不断淋洗硫铁矿,FeS2最终转化为____________。
⑵写出FeS2的电子式:____________。
⑶写出图中①③两个反应的离子方程式:
①____________________________________,
③____________________________________。
参考答案:
1.C
【分析】短周期元素X、Y是元素周期表中第ⅦA族的两种元素。X原子的电子层数比Y原子的电子层数少,可推知X为F元素、Y为Cl元素。
【详解】A.HF属于弱酸,HCl属于强酸,HF的酸性比HCl的弱,故A正确;
B.非金属性F>Cl,故氢化物稳定性:HF>HCl,故B正确;
C.氟气与水发生反应,不能置换出氯气,故C错误;
D.同主族自上而下非金属性减弱,故非金属性F>Cl,故D正确;
故选:C。
2.D
【详解】A.红磷转化为白磷,生成了新物质,属于化学变化,A错误;
B.石墨和金刚石是均由碳元素组成的不同单质,属于同素异形体,B错误;
C.和分子式不同,化学性质有较大不同,C错误;
D.单质硫有、、等,它们都是硫的同素异形体,D正确;
故选D。
3.C
【详解】A.第四周期元素中,外围电子排布为ndxnsy,且能级处于半满稳定状态时,含有的未成对电子数最多,即外围电子排布为3d54s1,此元素为铬,故A错误;
B.二氧化碳分子中碳氧键为极性键,但二氧化碳分子为非极性分子,故B错误;
C.丙氨酸分子中2号碳上连接四种不同的原子团,为手性碳原子,所以存在手性异构,故C正确;
D.NaCl熔化克服的是离子键,CO2气化克服的是分子间作用力,故D错误;
故答案为C。
【点睛】手性碳原子判断注意:手性碳原子一定是饱和碳原子;手性碳原子所连接的四个基团要是不同的,然后根据手性分子是含有手性碳原子的分子。
4.B
【详解】A.NaOH由Na+和OH-构成,含有离子键和极性共价键,A不符合题意;
B.H2O2的结构式为H-O-O-H,含有O-H极性共价键和O-O非极性共价键,B符合题意;
C.Na2O2由Na+和构成,含有离子键和非极性共价键,C不符合题意;
D.H2S的结构式为H-S-H,只含有极性共价键,D不符合题意;
故选B。
5.C
【详解】A.元素的非金属性越强,其最高价氧化物对应的水化物的酸性就越强,所以由水溶液的酸性:HCl>HF,不能推断出元素的非金属性:Cl>F,A选项正确;
B.过渡金属元素种类繁多,结构复杂,因此可在过渡元素中寻找催化剂和耐腐蚀、耐高温的合金材料,B选项正确;
C.同一主族元素的原子半径随着周期序数的增加而增加,C选项错误;
D.微粒X2-和Y2+核外电子排布相同,根据“阴上阳下”的原则,Y的原子序数大于X的原子序数,则离子半径:X2->Y2+,D选项正确;
答案选C。
6.D
【详解】A.金属钠与水反应:,故A错误;
B.和溶液混合,没有按照比例拆分,因此离子方程式为:,故B错误;
C.碳酸氢钠溶液与盐酸反应,碳酸氢根不能拆:,故C错误;
D.向溶液中加入过量的氨水:,故D正确。
综上所述,答案为D。
7.C
【详解】A.非金属性Cl>Br>I,则酸性:HClO4>HBrO4>HIO4,故A正确;
B.同周期主族元素从左向右原子半径减小,则原子半径:Na>Al>S>Cl,故B正确;
C.同周期主族元素从左向右非金属性增强,同主族从上到下非金属性减弱,且最高价含氧的酸性越强、对应非金属性越强,则非金属性:O>Cl>S>C,故C错误;
D.非金属性F>Cl>Br>I,则稳定性:HF>HCl>HBr>HI,故D正确;
故选:C。
8.D
【详解】A. 乙烯的结构简式:CH2=CH2,A错误;
B. 乙醇的分子式:C2H6O,B错误;
C. 聚丙烯的结构简式:,C错误;
D. 乙烯为平面构型,含碳碳双键,球棍模型正确,D正确;
故选D。
9.A
【详解】A.氮原子最外层有5个电子,要达到稳定结构得形成三对共用电子对,电子式为 ,选项A错误;
B.氢氧化钠是离子化合物,其中含有离子键,氢氧两种元素之间形成共价键,即氢氧化钠中含有离子键和共价键,选项B正确;
C.NaF是由钠离子和氟离子构成的化合物,属于盐,选项C正确;
D.KI中碘离子具有较强还原性,是常见的还原剂,选项D正确;
答案选A。
10.B
【详解】①金刚石是碳元素的一种单质,属于纯净物,不是混合物,①错误;
②HClO、CH3COOH、H2CO3都是化合物,电离产生的阳离子全部是H+,阴离子是酸根离子,因此它们都是酸,②正确;
③NaOH是强碱,属于强电解质;NH4HCO3、KMnO4都是盐、都是强电解质,③正确;
④Na2O2与水反应产生NaOH、O2,该氧化物为过氧化物,不是碱性氧化物,④错误;
⑤金刚石、石墨、C60都是C元素的单质,它们性质不同,互为同素异形体,⑤正确;
综上所述可知:说法正确的是②③⑤,故合理选项是B。
11.D
【详解】A.正丁烷中4个碳原子在一条链上,故其结构简式为CH3CH2CH2CH3,故A错误;
B.用小球和小棍表示的模型为球棍模型,故为丙烷的球棍模型,故B错误;
C.能表示物质中各原子之间的成键方式和大小比例的模型和空间填充模型,故为甲烷的空间填充模型,其球棍模型为,故C错误;
D.羟基内氢原子与氧原子羟基只共用1对电子对、O原子最外层电子数为7,属于中性原子团,其电子式为,故D正确;
故选:D。
12.D
【详解】A.标准状况下,22.4LCO2的物质的量为1mol,每个CO2分子中含有6+8×2=22个电子,所以共22NA个电子,A错误;
B.10.1g N(C2H5)3的物质的量为n==0.1mol,每个N(C2H5)3分子中含有3个C-C键为非极性键,所以故0.1mol此物质中含有的非极性键数目为0.3NA,B错误;
C.二氧化碳与一氧化二氮分子中含有氧原子个数不相等,只知道混合物的质量,无法计算含有氧原子数目,C错误;
D.100g46%的甲酸水溶液中,含有甲酸分子的物质的量为=1mol,含有氧原子的物质的量为1mol×2=2mol,含水的物质的量为=3mol,含有氧原子的物质的量为3mol×1=3mol,故该溶液中含有氧原子数为(2mol+3mol)×NAmol-1=5NA,D正确;
综上所述答案为D。
13.B
【详解】A.氯原子最外层电子数为7,易得到电子形成8电子稳定结构,A项错误;
B.氯原子最外层有7个电子,易得到1个电子形成稳定的氯离子,B项正确;
C.氯元素的化合价有-1,0,+1,+4,+5,+7等价,C项错误;
D.氯元素在元素周期表中位于第3周期第ⅦA族,D项错误;
答案选B。
14.D
【详解】A.和所带电荷数一样,且的电子数比硝酸根离子的电子数多10,所以R的质子数为7+10=17,R为Cl,R电子层数为3,N的电子层数为2,电子层数不同,故A错误;
B.R是Cl,最外层电子数是7个,N的最外层电子数是5个,R与N原子最外层电子数不相同,故B错误;
C.R与N的简单负离子分别是Cl-、N3-,二者所带的电荷数不相同,故C错误;
D.和均带1个负电荷,且氧元素化合价均是-2价,所以R、N元素的化合价均为+5,故D正确;
故选D。
15.B
【详解】A.同周期元素,从左到右原子半径依次减小,则碳原子的原子半径大于氮原子,故A正确;
B.元素的非金属性越强,氢化物的热稳定性越强,氟元素的非金属性强于氯元素,则氟化氢的热稳定性强于氯化氢,故B错误;
C.元素的金属性越强,金属单质的还原性越强,镁元素的金属性强于铝元素,则镁的还原性强于铝,故C正确;
D.元素的金属性越强,最高价氧化物对应水化物的碱性越强,钠元素的金属性弱于钾元素,则氢氧化钠的碱性弱于氢氧化钾,故D正确;
故选B。
16. Al3++ 4OH-==+ 2H2O Al3++3+6H2O==4Al(OH)3↓
【分析】甲、乙、丙、丁代表化学中常见的四种物质,常温下0.1 mol/L的丁溶液pH为13,其焰色反应为黄色,则丁应为NaOH,其中甲、乙、丙为均含有同一种金属元素的无机化合物,由流程图可知,甲与NaOH可以反应生成乙,乙与NaOH可以反应生成丙,甲和丙可以反应生成乙,则甲为可溶性铝盐,乙为Al(OH)3,丙为偏铝酸盐,
【详解】由以上分析知,甲为可溶性铝盐,乙为Al(OH)3,丙为偏铝酸盐,丁为NaOH,
(1)甲为可溶性铝盐,丁应为NaOH,则甲中加入过量的丁直接生成丙的离子方程式Al3++ 4OH-==+ 2H2O;
(2)反应(Ⅲ)可溶性铝盐与偏铝酸盐发生双水解反应,离子方程式为Al3++3+6H2O==4Al(OH)3↓。
17.(1)第五周期ⅢA族
(2)<
(3)17
(4)
(5)ad
【解析】(1)
稀有气体元素54Xe位于第五周期零族,根据稀有气体元素定位法可知49In是在周期表中的位置是第五周期ⅢA族;
(2)
Ba位于周期表第六周期ⅡA族,In位于第五周期ⅢA族,因此非金属性Ba强于In,In的最高价氧化物对应的水化物的碱性(3)
的中子数与电子数的差值=(115-49)-49=17;
(4)
Se为34号元素,位于第四周期ⅥA族,其原子结构示意图可表示为;
(5)
a.Se为第ⅥA族元素,最高价态为+6,最低价为-2价,因此SeO2既有氧化性又有还原性,a正确;
b.同主族元素简单氢化物的沸点从上到下升高,但H2O分子间存在氢键,沸点比H2S、H2Se均高,b错误;
c.非金属性:Sed.Se和Br位于同一周期,Br在右,因此非金属性:Se选ad。
18.(1) 离子
(2)Na3N+4HCl=3NaCl+NH4Cl
(3)NH4Cl
(4)<
【详解】(1)氮化钠是由钠离子与氮离子通过离子键结合成的离子化合物,电子式为;
(2)Na3N与盐酸反应生成氯化钠和氯化铵,方程式Na3N+4HCl=3NaCl+NH4Cl;
(3)题(2)反应的生成物中,NH4Cl既含共价键又含离子键,NaCl只有离子键;
(4)钠离子与氮离子具有相同的核外电子排布,根据具有相同电子层结构的离子,半径随着原子序数的递增而减小,由钠的原子序数大于氮的原子序数,所以<。
19. 1nm~100nm或者10-9m~10-7m Na2O2 放热反应 2Fe3++Cu=Cu2++2Fe2+ 弱碱性 不能 2Fe2++H2O2+2H+=2Fe3++2H2O NaHSO4=Na++H++SO
【详解】(1)向沸水中滴加2mL饱和FeCl3溶液,继续加热至液体呈红褐色,得到氢氧化铁胶体,胶体中分散质的微粒直径大小为1nm~100nm或者10-9m~10-7m之间;故答案为1nm~100nm或者10-9m~10-7m;
(2)淡黄色粉末,能提供氧气,即该物质为过氧化钠,其化学式为Na2O2;过氧化钠能与水反应2Na2O2+2H2O=4NaOH+O2↑,脱脂棉燃烧,说明该反应为放热反应;故答案为Na2O2;放热反应;
(3)Fe3+具有强氧化性,与Cu发生2Fe3++Cu=Cu2++2Fe2+;故答案为2Fe3++Cu=Cu2++2Fe2+;
(4)氢氧化铝能治疗胃酸过多,体现氢氧化铝的弱碱性;氢氧化钠的碱性太强,因此不能用氢氧化钠溶液代替氢氧化铝;故答案为弱碱性;不能;
(5)H2O2具有强氧化性,能将Fe2+氧化成Fe3+,其离子方程式为2Fe2++H2O2+2H+=2Fe3++2H2O;故答案为2Fe2++H2O2+2H+=2Fe3++2H2O;
(6)NaHSO4为强电解质,在水溶液中的电离方程式为NaHSO4=Na++H++SO;故答案为NaHSO4=Na++H++SO。
20. 第四周期第ⅠA族 第五周期第ⅦA族
【详解】由X的原子结构示意图可知,其原子核外有4个电子层,则X位于第四周期,最外层电子数为1,位于第ⅠA族,则X在元素周期表中的位置为第四周期第ⅠA族;由Y的原子结构示意图可知,其原子核外有5个电子层,则Y位于第五周期,最外层电子数为7,位于第ⅦA族,则Y在元素周期表中的位置为第五周期第ⅦA族,故答案为:第四周期第ⅠA族;第五周期第ⅦA族。
21.(1) 氧原子和硫原子的最外层均为6个电子,均易得到2个电子形成8电子稳定结构
(2)和
(3)
【分析】(1)
①一个硫原子得到二个电子形成一种新粒子,该粒子的符号为;
②、中氧与硫元素的化合价均为价,从原子结构上分析它们化合价相同的原因是氧原子和硫原子的最外层均为6个电子,均易得到2个电子形成8电子稳定结构;
(2)
根据溶液和溶液反应的微观示意图所示,反应前后该反应中实际参加反应的离子是和没有变化,实际参加反应的离子是和;
(3)
根据硫及其化合物的“化合价-物质类别”关系图所示,物质X属于S是+4价的氧化物,化学式为。
22.
【详解】①HClO为共价化合物,分子中氢原子、氯原子与氧原子之间分别通过共用电子对形成共价键,其电子式为,故答案为:;
②Na2O2为离子化合物,每个钠原子给出一个电子,氧原子与氧原子之间通过共用电子对形成共价键,同时每个氧原子接受钠提供的一个电子,与钠之间形成离子键,其电子式为,故答案为:。
23. 水解 酸 FeO(OH)
【分析】(1)Fe2(SO4)3是强酸弱碱盐,易水解,使地下水和土壤呈酸性;由转化图可知,如果矿区中的水流或降雨不断淋洗硫铁矿,FeS2最终转化为FeO(OH);
(2)FeS2为离子化合物,由Fe2+、S22-构成;
(3)反应①为FeS2被氧气氧化生成硫酸根;反应③为Fe3+与FeS2反应生成Fe2+和硫酸根,二者皆为氧化还原反应,根据得失电子守恒、电荷守恒、元素守恒配平离子方程式。
【详解】(1)Fe2(SO4)3是强酸弱碱盐,易水解,使地下水和土壤呈酸性;由转化图可知,如果矿区中的水流或降雨不断淋洗硫铁矿,FeS2最终转化为FeO(OH);
故答案为:水解;酸;FeO(OH);
(2)FeS2为离子化合物,由Fe2+、S22-构成,其电子式为;
故答案为:;
(3)反应①为FeS2被氧气氧化生成硫酸根,根据得失电子守恒、电荷守恒、元素守恒配平方程式为:;
反应③为Fe3+与FeS2反应生成Fe2+和硫酸根,根据得失电子守恒、电荷守恒、元素守恒配平方程式为:;
故答案为:;。
一、单选题
1.短周期元素X、Y是元素周期表中第ⅦA族的两种元素,X原子的电子层数比Y原子的电子层数少。下列说法不正确的是
A.HX的酸性比HY的弱
B.X的最简单气态氢化物比Y的稳定
C.X的单质能将Y的单质从KY的水溶液中置换出来
D.X的非金属性比Y的强
2.下列说法正确的是
A.红磷转化为白磷,属于物理变化
B.石墨导电、金刚石不导电,故二者不是同素异形体
C.和分子式不同,化学性质相同
D.单质硫有、、等,它们都是硫的同素异形体
3.下列说法正确的是
A.第四周期元素中,锰原子价电子层中未成对电子数最多
B.含有极性键的分子一定是极性分子
C.丙氨酸()存在手性异构体
D.NaCl熔化和CO2气化克服的作用力类型相同
4.下列物质中,既含有非极性共价键又含有极性共价键是
A.NaOH B.H2O2 C.Na2O2 D.H2S
5.元素周期表和元素周期律可以指导人们进行规律性的推测和判断。下列说法不合理的是
A.由水溶液的酸性:HCl>HF,不能推断出元素的非金属性:Cl>F
B.人们可以在周期表的过渡元素中寻找催化剂和耐腐蚀、耐高温的合金材料
C.原子半径随着周期序数的增加而增加
D.短周期元素形成的微粒X2-和Y2+核外电子排布相同,离子半径:X2->Y2+
6.下列离子方程式书写正确的是
A.金属钠与水反应:
B.和溶液混合:
C.碳酸氢钠溶液与盐酸反应:
D.向溶液中加入过量的氨水:
7.下列关于物质性质的比较不正确的是
A.酸性: HClO4> HBrO4> HIO4
B.原子半径: Na>Al>S>Cl
C.非金属性: Cl>S>O>C
D.稳定性: HF> HCl> HBr> HI
8.下列化学用语的表示正确的是
A.乙烯的结构简式:CH2CH2
B.乙醇的分子式:C2H5OH
C.聚丙烯的结构简式:
D.乙烯的球棍模型:
9.下列说法中不正确的是
A.N2的电子式是 B.NaOH中既含有离子键也含有共价键
C.NaF属于盐 D.KI是常见的还原剂
10.下列物质的分类组合正确的是
①金刚石、氢氧化铁胶体、豆浆均为混合物;②HClO、CH3COOH、H2CO3均为酸;
③NaOH、NH4HCO3、KMnO4均为强电解质;④Na2O2、Na2O、MgO均为碱性氧化物;
⑤金刚石、石墨、C60互为同素异形体。
A.②⑤ B.②③⑤ C.①②③⑤ D.④⑤
11.下列化学用语正确的是
A.正丁烷的结构简式: B.丙烷分子的空间填充模型:
C.甲烷分子的球棍模型: D.羟基的电子式:
12.为实现“双碳”目标,某科研小组设计捕获二氧化碳生成甲酸的过程如图所示。下列说法正确的是(NA为阿伏加德罗常数的值)
A.标准状况下,22.4 L CO2中所含的电子数目为16NA
B.10.1 g N(C2H5)3中所含的非极性共价键数目为1.8NA
C.22 g CO2与N2O混合物中所含氧原子的数目为NA
D.100 g 46%的甲酸水溶液中所含的氧原子数目为5NA
13.氯元素的原子结构示意图为,下列说法正确的是
A.氯原子在化学反应中易失去电子
B.氯原子易得到电子形成稳定的氯离子
C.氯元素的化合价只有-1价
D.氯在元素周期表中位于第3周期第Ⅶ族
14.某酸根离子的电子数比硝酸根离子的电子数多10,则下列说法中正确的是
A.R与N原子电子层数相同
B.R与N原子最外层电子数相同
C.R与N的简单负离子所带的电荷数相同
D.中R元素与中N元素的化合价相同
15.根据元素周期律,下列推断错误的是
A.原子半径:C > N B.热稳定性:HF < HCl
C.还原性:Mg > Al D.碱性:NaOH<KOH
二、填空题
16.下图中的甲、乙、丙、丁代表化学中常见的四种物质,相互转化的关系如下所示。其中甲、乙、丙为均含有同一种金属元素的无机化合物,常温下0.1 mol/L的丁溶液pH为13,其焰色反应为黄色。
(1)请写出甲中加入过量的丁直接生成丙的离子方程式:______________________。
(2)请写出反应(Ⅲ)的离子方程式为___________________________。
17.利用物质的结构与性质对周期表进行研究,有助于我们更好地掌握同类知识。
I.2019年是元素周期表发表150周年,期间科学家为完善周期表做出了不懈努力。中国科学院院士张青莲教授曾主持测定了铟(49In)等9种元素相对原子质量的新值,被采用为国际新标准。
(1)In在周期表中的位置是_______。
(2)In的最高价氧化物对应的水化物的碱性_______Ba(OH)2的碱性(填“>”或“<”)。
(3)的中子数与电子数的差值为_______。
II.硒(34Se)是动物和人体所必需的微量元素之一,也是重要的工业原料,与氧同族。
(4)Se原子结构示意图可表示为_______。
(5)下列说法合理的是_______。
a.SeO2既有氧化性又有还原性 b.沸点:H2O < H2S < H2Se
c.热稳定性:H2Se
(1)的电子式是_______,该化合物是由_______键形成的。
(2)与盐酸反应的化学方程式是_______。
(3)在题(2)反应的生成物中,含有共价键的是_______。
(4)比较中两种微粒的半径: _______。(填“>”“<”或“=”)
19.金属及其化合物在人类的历史上有着重要的作用。回答下列有关问题:
(1)向20 mL沸水中逐滴滴加2 mL饱和FeCl3溶液,继续加热至液体呈红褐色,形成的分散系中分散质微粒的直径大小范围是___________。
(2)最近两年,随着神舟号系列飞船和蛟龙号潜艇性能的进一步优化,我国已成功实现“上天入地”。在上天入地时,为了给工作仓内工作人员提供氧气,一般要携带一种淡黄色粉末,其化学式为___________,将其撒入脱脂棉,滴加几滴水,脱脂棉能被点燃,说明反应___________。
(3)电子工业上可用FeCl3溶液腐蚀电路板上的铜,写出该反应的离子方程式:___________。
(4)胃舒平(主要成分为氢氧化铝)可用于治疗胃酸过多,氢氧化铝体现___________性;___________(填“能”或“不能”)用氢氧化钠溶液代替。
(5)将硫酸亚铁与稀硫酸混合,二者不反应,滴入H2O2后,溶液很快变成黄色,该反应的离子方程式为___________。
(6)NaHSO4是一种酸式盐,写出NaHSO4在水中的电离方程式___________。
20.已知某主族元素的原子结构示意图如下,请写出它们在周期表中的位置。
X:_______,Y:_______。
21.宏观和微观相结合是认识物质结构与性质的重要方法,请回答下列问题。
(1)氧原子的结构示意图为,硫原子的结构示意图为。
①一个硫原子得到二个电子形成一种新粒子,该粒子的符号为___________。
②氧气和硫单质分别与氢气反应生成和。、中氧与硫元素的化合价均为价,从原子结构上分析它们化合价相同的原因是___________。
(2)溶液和溶液反应的微观示意图如图1所示。该反应中实际参加反应的离子是___________(填离子符号)。
(3)硫及其化合物的“化合价-物质类别”关系图如图2所示。物质X的化学式为___________。
22.用电子式表示①②的结构。
①HClO________, ②Na2O2________,
23.自然界中的许多金属元素都能以硫化物的形式存在,硫铁矿(FeS2)就是其中一种,在矿区,开采出的硫铁矿石暴露在空气和水中,会发生下图所示转化。回答下列问题:
⑴FeS2的氧化产物Fe2(SO4)3易______,会使地下水和土壤呈______性;如果矿区中的水流或降雨不断淋洗硫铁矿,FeS2最终转化为____________。
⑵写出FeS2的电子式:____________。
⑶写出图中①③两个反应的离子方程式:
①____________________________________,
③____________________________________。
参考答案:
1.C
【分析】短周期元素X、Y是元素周期表中第ⅦA族的两种元素。X原子的电子层数比Y原子的电子层数少,可推知X为F元素、Y为Cl元素。
【详解】A.HF属于弱酸,HCl属于强酸,HF的酸性比HCl的弱,故A正确;
B.非金属性F>Cl,故氢化物稳定性:HF>HCl,故B正确;
C.氟气与水发生反应,不能置换出氯气,故C错误;
D.同主族自上而下非金属性减弱,故非金属性F>Cl,故D正确;
故选:C。
2.D
【详解】A.红磷转化为白磷,生成了新物质,属于化学变化,A错误;
B.石墨和金刚石是均由碳元素组成的不同单质,属于同素异形体,B错误;
C.和分子式不同,化学性质有较大不同,C错误;
D.单质硫有、、等,它们都是硫的同素异形体,D正确;
故选D。
3.C
【详解】A.第四周期元素中,外围电子排布为ndxnsy,且能级处于半满稳定状态时,含有的未成对电子数最多,即外围电子排布为3d54s1,此元素为铬,故A错误;
B.二氧化碳分子中碳氧键为极性键,但二氧化碳分子为非极性分子,故B错误;
C.丙氨酸分子中2号碳上连接四种不同的原子团,为手性碳原子,所以存在手性异构,故C正确;
D.NaCl熔化克服的是离子键,CO2气化克服的是分子间作用力,故D错误;
故答案为C。
【点睛】手性碳原子判断注意:手性碳原子一定是饱和碳原子;手性碳原子所连接的四个基团要是不同的,然后根据手性分子是含有手性碳原子的分子。
4.B
【详解】A.NaOH由Na+和OH-构成,含有离子键和极性共价键,A不符合题意;
B.H2O2的结构式为H-O-O-H,含有O-H极性共价键和O-O非极性共价键,B符合题意;
C.Na2O2由Na+和构成,含有离子键和非极性共价键,C不符合题意;
D.H2S的结构式为H-S-H,只含有极性共价键,D不符合题意;
故选B。
5.C
【详解】A.元素的非金属性越强,其最高价氧化物对应的水化物的酸性就越强,所以由水溶液的酸性:HCl>HF,不能推断出元素的非金属性:Cl>F,A选项正确;
B.过渡金属元素种类繁多,结构复杂,因此可在过渡元素中寻找催化剂和耐腐蚀、耐高温的合金材料,B选项正确;
C.同一主族元素的原子半径随着周期序数的增加而增加,C选项错误;
D.微粒X2-和Y2+核外电子排布相同,根据“阴上阳下”的原则,Y的原子序数大于X的原子序数,则离子半径:X2->Y2+,D选项正确;
答案选C。
6.D
【详解】A.金属钠与水反应:,故A错误;
B.和溶液混合,没有按照比例拆分,因此离子方程式为:,故B错误;
C.碳酸氢钠溶液与盐酸反应,碳酸氢根不能拆:,故C错误;
D.向溶液中加入过量的氨水:,故D正确。
综上所述,答案为D。
7.C
【详解】A.非金属性Cl>Br>I,则酸性:HClO4>HBrO4>HIO4,故A正确;
B.同周期主族元素从左向右原子半径减小,则原子半径:Na>Al>S>Cl,故B正确;
C.同周期主族元素从左向右非金属性增强,同主族从上到下非金属性减弱,且最高价含氧的酸性越强、对应非金属性越强,则非金属性:O>Cl>S>C,故C错误;
D.非金属性F>Cl>Br>I,则稳定性:HF>HCl>HBr>HI,故D正确;
故选:C。
8.D
【详解】A. 乙烯的结构简式:CH2=CH2,A错误;
B. 乙醇的分子式:C2H6O,B错误;
C. 聚丙烯的结构简式:,C错误;
D. 乙烯为平面构型,含碳碳双键,球棍模型正确,D正确;
故选D。
9.A
【详解】A.氮原子最外层有5个电子,要达到稳定结构得形成三对共用电子对,电子式为 ,选项A错误;
B.氢氧化钠是离子化合物,其中含有离子键,氢氧两种元素之间形成共价键,即氢氧化钠中含有离子键和共价键,选项B正确;
C.NaF是由钠离子和氟离子构成的化合物,属于盐,选项C正确;
D.KI中碘离子具有较强还原性,是常见的还原剂,选项D正确;
答案选A。
10.B
【详解】①金刚石是碳元素的一种单质,属于纯净物,不是混合物,①错误;
②HClO、CH3COOH、H2CO3都是化合物,电离产生的阳离子全部是H+,阴离子是酸根离子,因此它们都是酸,②正确;
③NaOH是强碱,属于强电解质;NH4HCO3、KMnO4都是盐、都是强电解质,③正确;
④Na2O2与水反应产生NaOH、O2,该氧化物为过氧化物,不是碱性氧化物,④错误;
⑤金刚石、石墨、C60都是C元素的单质,它们性质不同,互为同素异形体,⑤正确;
综上所述可知:说法正确的是②③⑤,故合理选项是B。
11.D
【详解】A.正丁烷中4个碳原子在一条链上,故其结构简式为CH3CH2CH2CH3,故A错误;
B.用小球和小棍表示的模型为球棍模型,故为丙烷的球棍模型,故B错误;
C.能表示物质中各原子之间的成键方式和大小比例的模型和空间填充模型,故为甲烷的空间填充模型,其球棍模型为,故C错误;
D.羟基内氢原子与氧原子羟基只共用1对电子对、O原子最外层电子数为7,属于中性原子团,其电子式为,故D正确;
故选:D。
12.D
【详解】A.标准状况下,22.4LCO2的物质的量为1mol,每个CO2分子中含有6+8×2=22个电子,所以共22NA个电子,A错误;
B.10.1g N(C2H5)3的物质的量为n==0.1mol,每个N(C2H5)3分子中含有3个C-C键为非极性键,所以故0.1mol此物质中含有的非极性键数目为0.3NA,B错误;
C.二氧化碳与一氧化二氮分子中含有氧原子个数不相等,只知道混合物的质量,无法计算含有氧原子数目,C错误;
D.100g46%的甲酸水溶液中,含有甲酸分子的物质的量为=1mol,含有氧原子的物质的量为1mol×2=2mol,含水的物质的量为=3mol,含有氧原子的物质的量为3mol×1=3mol,故该溶液中含有氧原子数为(2mol+3mol)×NAmol-1=5NA,D正确;
综上所述答案为D。
13.B
【详解】A.氯原子最外层电子数为7,易得到电子形成8电子稳定结构,A项错误;
B.氯原子最外层有7个电子,易得到1个电子形成稳定的氯离子,B项正确;
C.氯元素的化合价有-1,0,+1,+4,+5,+7等价,C项错误;
D.氯元素在元素周期表中位于第3周期第ⅦA族,D项错误;
答案选B。
14.D
【详解】A.和所带电荷数一样,且的电子数比硝酸根离子的电子数多10,所以R的质子数为7+10=17,R为Cl,R电子层数为3,N的电子层数为2,电子层数不同,故A错误;
B.R是Cl,最外层电子数是7个,N的最外层电子数是5个,R与N原子最外层电子数不相同,故B错误;
C.R与N的简单负离子分别是Cl-、N3-,二者所带的电荷数不相同,故C错误;
D.和均带1个负电荷,且氧元素化合价均是-2价,所以R、N元素的化合价均为+5,故D正确;
故选D。
15.B
【详解】A.同周期元素,从左到右原子半径依次减小,则碳原子的原子半径大于氮原子,故A正确;
B.元素的非金属性越强,氢化物的热稳定性越强,氟元素的非金属性强于氯元素,则氟化氢的热稳定性强于氯化氢,故B错误;
C.元素的金属性越强,金属单质的还原性越强,镁元素的金属性强于铝元素,则镁的还原性强于铝,故C正确;
D.元素的金属性越强,最高价氧化物对应水化物的碱性越强,钠元素的金属性弱于钾元素,则氢氧化钠的碱性弱于氢氧化钾,故D正确;
故选B。
16. Al3++ 4OH-==+ 2H2O Al3++3+6H2O==4Al(OH)3↓
【分析】甲、乙、丙、丁代表化学中常见的四种物质,常温下0.1 mol/L的丁溶液pH为13,其焰色反应为黄色,则丁应为NaOH,其中甲、乙、丙为均含有同一种金属元素的无机化合物,由流程图可知,甲与NaOH可以反应生成乙,乙与NaOH可以反应生成丙,甲和丙可以反应生成乙,则甲为可溶性铝盐,乙为Al(OH)3,丙为偏铝酸盐,
【详解】由以上分析知,甲为可溶性铝盐,乙为Al(OH)3,丙为偏铝酸盐,丁为NaOH,
(1)甲为可溶性铝盐,丁应为NaOH,则甲中加入过量的丁直接生成丙的离子方程式Al3++ 4OH-==+ 2H2O;
(2)反应(Ⅲ)可溶性铝盐与偏铝酸盐发生双水解反应,离子方程式为Al3++3+6H2O==4Al(OH)3↓。
17.(1)第五周期ⅢA族
(2)<
(3)17
(4)
(5)ad
【解析】(1)
稀有气体元素54Xe位于第五周期零族,根据稀有气体元素定位法可知49In是在周期表中的位置是第五周期ⅢA族;
(2)
Ba位于周期表第六周期ⅡA族,In位于第五周期ⅢA族,因此非金属性Ba强于In,In的最高价氧化物对应的水化物的碱性
的中子数与电子数的差值=(115-49)-49=17;
(4)
Se为34号元素,位于第四周期ⅥA族,其原子结构示意图可表示为;
(5)
a.Se为第ⅥA族元素,最高价态为+6,最低价为-2价,因此SeO2既有氧化性又有还原性,a正确;
b.同主族元素简单氢化物的沸点从上到下升高,但H2O分子间存在氢键,沸点比H2S、H2Se均高,b错误;
c.非金属性:Se
18.(1) 离子
(2)Na3N+4HCl=3NaCl+NH4Cl
(3)NH4Cl
(4)<
【详解】(1)氮化钠是由钠离子与氮离子通过离子键结合成的离子化合物,电子式为;
(2)Na3N与盐酸反应生成氯化钠和氯化铵,方程式Na3N+4HCl=3NaCl+NH4Cl;
(3)题(2)反应的生成物中,NH4Cl既含共价键又含离子键,NaCl只有离子键;
(4)钠离子与氮离子具有相同的核外电子排布,根据具有相同电子层结构的离子,半径随着原子序数的递增而减小,由钠的原子序数大于氮的原子序数,所以<。
19. 1nm~100nm或者10-9m~10-7m Na2O2 放热反应 2Fe3++Cu=Cu2++2Fe2+ 弱碱性 不能 2Fe2++H2O2+2H+=2Fe3++2H2O NaHSO4=Na++H++SO
【详解】(1)向沸水中滴加2mL饱和FeCl3溶液,继续加热至液体呈红褐色,得到氢氧化铁胶体,胶体中分散质的微粒直径大小为1nm~100nm或者10-9m~10-7m之间;故答案为1nm~100nm或者10-9m~10-7m;
(2)淡黄色粉末,能提供氧气,即该物质为过氧化钠,其化学式为Na2O2;过氧化钠能与水反应2Na2O2+2H2O=4NaOH+O2↑,脱脂棉燃烧,说明该反应为放热反应;故答案为Na2O2;放热反应;
(3)Fe3+具有强氧化性,与Cu发生2Fe3++Cu=Cu2++2Fe2+;故答案为2Fe3++Cu=Cu2++2Fe2+;
(4)氢氧化铝能治疗胃酸过多,体现氢氧化铝的弱碱性;氢氧化钠的碱性太强,因此不能用氢氧化钠溶液代替氢氧化铝;故答案为弱碱性;不能;
(5)H2O2具有强氧化性,能将Fe2+氧化成Fe3+,其离子方程式为2Fe2++H2O2+2H+=2Fe3++2H2O;故答案为2Fe2++H2O2+2H+=2Fe3++2H2O;
(6)NaHSO4为强电解质,在水溶液中的电离方程式为NaHSO4=Na++H++SO;故答案为NaHSO4=Na++H++SO。
20. 第四周期第ⅠA族 第五周期第ⅦA族
【详解】由X的原子结构示意图可知,其原子核外有4个电子层,则X位于第四周期,最外层电子数为1,位于第ⅠA族,则X在元素周期表中的位置为第四周期第ⅠA族;由Y的原子结构示意图可知,其原子核外有5个电子层,则Y位于第五周期,最外层电子数为7,位于第ⅦA族,则Y在元素周期表中的位置为第五周期第ⅦA族,故答案为:第四周期第ⅠA族;第五周期第ⅦA族。
21.(1) 氧原子和硫原子的最外层均为6个电子,均易得到2个电子形成8电子稳定结构
(2)和
(3)
【分析】(1)
①一个硫原子得到二个电子形成一种新粒子,该粒子的符号为;
②、中氧与硫元素的化合价均为价,从原子结构上分析它们化合价相同的原因是氧原子和硫原子的最外层均为6个电子,均易得到2个电子形成8电子稳定结构;
(2)
根据溶液和溶液反应的微观示意图所示,反应前后该反应中实际参加反应的离子是和没有变化,实际参加反应的离子是和;
(3)
根据硫及其化合物的“化合价-物质类别”关系图所示,物质X属于S是+4价的氧化物,化学式为。
22.
【详解】①HClO为共价化合物,分子中氢原子、氯原子与氧原子之间分别通过共用电子对形成共价键,其电子式为,故答案为:;
②Na2O2为离子化合物,每个钠原子给出一个电子,氧原子与氧原子之间通过共用电子对形成共价键,同时每个氧原子接受钠提供的一个电子,与钠之间形成离子键,其电子式为,故答案为:。
23. 水解 酸 FeO(OH)
【分析】(1)Fe2(SO4)3是强酸弱碱盐,易水解,使地下水和土壤呈酸性;由转化图可知,如果矿区中的水流或降雨不断淋洗硫铁矿,FeS2最终转化为FeO(OH);
(2)FeS2为离子化合物,由Fe2+、S22-构成;
(3)反应①为FeS2被氧气氧化生成硫酸根;反应③为Fe3+与FeS2反应生成Fe2+和硫酸根,二者皆为氧化还原反应,根据得失电子守恒、电荷守恒、元素守恒配平离子方程式。
【详解】(1)Fe2(SO4)3是强酸弱碱盐,易水解,使地下水和土壤呈酸性;由转化图可知,如果矿区中的水流或降雨不断淋洗硫铁矿,FeS2最终转化为FeO(OH);
故答案为:水解;酸;FeO(OH);
(2)FeS2为离子化合物,由Fe2+、S22-构成,其电子式为;
故答案为:;
(3)反应①为FeS2被氧气氧化生成硫酸根,根据得失电子守恒、电荷守恒、元素守恒配平方程式为:;
反应③为Fe3+与FeS2反应生成Fe2+和硫酸根,根据得失电子守恒、电荷守恒、元素守恒配平方程式为:;
故答案为:;。
