专题6生命活动的物质基础—糖类、油脂、蛋白质单元测试卷高二下学期化学苏教版(2019)选择性必修3(含解析)
文档属性
| 名称 | 专题6生命活动的物质基础—糖类、油脂、蛋白质单元测试卷高二下学期化学苏教版(2019)选择性必修3(含解析) |

|
|
| 格式 | docx | ||
| 文件大小 | 329.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-06-17 00:00:00 | ||
图片预览




文档简介
专题6《生命活动的物质基础—糖类、油脂、蛋白质》单元测试卷
一、单选题
1.我国人民在悠久的历史中创造了绚丽多彩的中华文化。下列说法错误的是( )
A.“春蚕到死丝方尽,蜡炬成灰泪始干”中涉及氧化还原反应
B.“川麻不浆,以胶(动物胶和明矾)作黄纸”,“胶”中的明矾作杀菌剂
C.“伦乃造意,用树肤、麻头及敝布、鱼网以为纸”,树肤、麻头等富含纤维素
D.“忽闻海上有仙山,山在虚无缥缈间”的海市蜃楼是一种自然现象,与胶体知识有关
2.在日常生活中我们常说开门七件事:①柴;②米;③油;④盐;⑤酱;⑥醋;⑦茶。你认为其中含有有机物的是
A.除②外都含有 B.除⑦外都含有 C.除④外都含有 D.全部含有
3.下列化学实验中的操作、现象及结论都正确的是
选项 操作 现象 结论
A 将苯加入溴水中充分振荡后静置 下层接近无色 苯分子中含碳碳双键
B 淀粉溶液和稀硫酸共热后,加入新制的氢氧化铜悬浊液,加热煮沸 未出现砖红色沉淀 淀粉未水解
C 向两份蛋白质溶液中分别滴加饱和NaCl溶液和溶液 均有固体析出 蛋白质均发生变性
D 向苯和甲苯中分别滴加少量酸性溶液,充分振荡 苯中下层溶液为紫红色,甲苯中溶液为无色 苯环使甲基变活泼
A.A B.B C.C D.D
4.从科技前沿到日常生活,化学无处不在。下列说法错误的是
A.北京冬奥会的吉祥物“冰墩墩”使用的聚乙烯属于高分子化合物
B.“天和”核心舱中使用的氮化硼陶瓷基复合材料属于高分子化合物
C.葡萄酒中通常添加微量,具有杀菌并防止营养成分被氧化的作用
D.地沟油不能食用,但可以用来制肥皂或生物柴油,实现变废为宝
5.糖类、油脂、蛋白质是生命体的重要物质,下列说法正确的是
A.蔗糖水解产物只有葡萄糖 B.鸡蛋清溶液加硫酸镁会发生变性
C.油脂的氢化是加成反应 D.淀粉和纤维素互为同分异构体
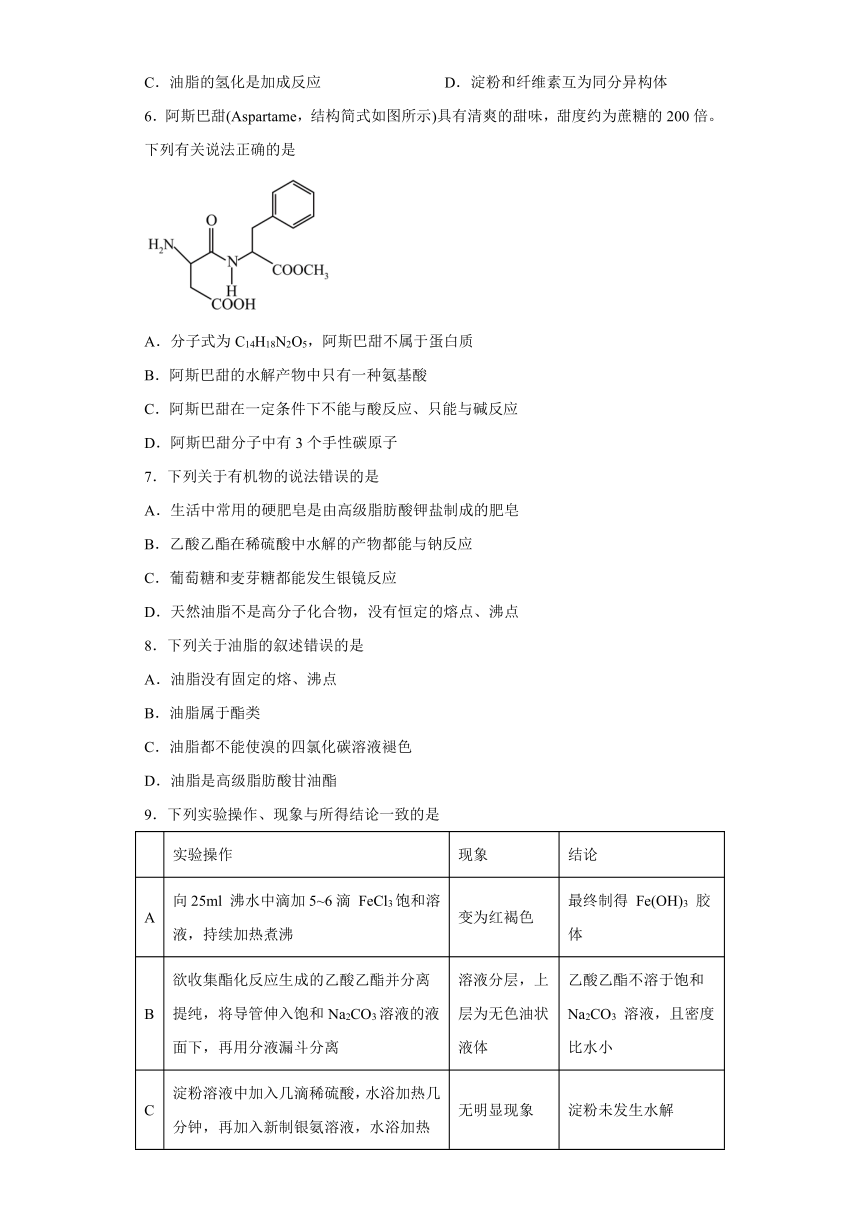
6.阿斯巴甜(Aspartame,结构简式如图所示)具有清爽的甜味,甜度约为蔗糖的200倍。下列有关说法正确的是
A.分子式为C14H18N2O5,阿斯巴甜不属于蛋白质
B.阿斯巴甜的水解产物中只有一种氨基酸
C.阿斯巴甜在一定条件下不能与酸反应、只能与碱反应
D.阿斯巴甜分子中有3个手性碳原子
7.下列关于有机物的说法错误的是
A.生活中常用的硬肥皂是由高级脂肪酸钾盐制成的肥皂
B.乙酸乙酯在稀硫酸中水解的产物都能与钠反应
C.葡萄糖和麦芽糖都能发生银镜反应
D.天然油脂不是高分子化合物,没有恒定的熔点、沸点
8.下列关于油脂的叙述错误的是
A.油脂没有固定的熔、沸点
B.油脂属于酯类
C.油脂都不能使溴的四氯化碳溶液褪色
D.油脂是高级脂肪酸甘油酯
9.下列实验操作、现象与所得结论一致的是
实验操作 现象 结论
A 向25ml 沸水中滴加5~6滴 FeCl3饱和溶液,持续加热煮沸 变为红褐色 最终制得 Fe(OH)3 胶体
B 欲收集酯化反应生成的乙酸乙酯并分离提纯,将导管伸入饱和Na2CO3溶液的液面下,再用分液漏斗分离 溶液分层,上层为无色油状液体 乙酸乙酯不溶于饱和Na2CO3 溶液,且密度比水小
C 淀粉溶液中加入几滴稀硫酸,水浴加热几分钟,再加入新制银氨溶液,水浴加热 无明显现象 淀粉未发生水解
D 向两支盛有KI3溶液的试管中,分别滴加淀粉溶液和AgNO3溶液 前者溶液变蓝,后者有黄色沉淀 KI3溶液中存在平衡:I3- I2+I-
A.A B.B C.C D.D
10.下列关于蛋白质的叙述正确的是
A.利用蛋白质盐析的性质,可分离、提纯蛋白质
B.温度越高,酶的催化效率越高
C.重金属盐能使蛋白质变性,所以吞服“钡餐”会引起中毒
D.所有蛋白质遇到浓硝酸均会显黄色
11.蛋白质受某些因素的影响,其空间结构发生变化(一级结构不变),引起其理化性质和生物活性的变化,此时发生了蛋白质的。
A.水解 B.变性 C.盐析 D.溶解
12.有机化学对人类生活有着十分重要的作用。下列说法错误的是
A.通过有机反应可以合成自然界不存在的新物质
B.石油裂化、油脂硬化、橡胶老化均是化学变化
C.塑料、合成纤维、合成橡胶均是通过加聚反应来合成
D.蛋白质、纤维素、核酸均属生物大分子,均能发生水解反应
13.《后汉书·郡国志》中记载:“石出泉水……其水有肥,燃之极明,不可食,县人谓之石漆。”《酉阳杂俎》一书:“高奴县石脂水,水腻,浮上如漆,采以膏车及燃灯极明。”这里的“石漆”“石脂水”是指
A.油脂 B.油漆 C.石油 D.甘油
14.实验探究是化学学科的魅力所在。下列有关实验操作、现象和结论均正确的是
选项 实验操作 实验现象 结论
A 向平衡体系2NO2N2O4中加压 红棕色变浅 平衡正向移动
B 向淀粉溶液中加入稀硫酸,加热几分钟,冷却后再加入新制Cu(OH)2悬浊液,加热 溶液中未观察到砖红色沉淀产生 淀粉没有水解
C 将大小相同的Al和Mg分别投入到相同浓度的NaOH溶液中 Al溶解有气泡产生,Mg无现象 Al的金属性强于Mg
D 向海带灰的浸取液中滴加适量氯水,再加入CCl4萃取 分层,下层出现紫红色 海带中含有碘元素
A.A B.B C.C D.D
15.由实验操作和现象,可得出相应正确结论是
实验操作 实验现象 解释或结论
A 将铁锈溶于浓盐酸中,滴入高锰酸钾溶液 紫色褪去 铁锈中含有二价铁
B 石蜡油加强热,将产生的气体通入Br2的CCl4溶液 溶液红棕色变无色 产生的气体中含有烯烃
C 向蔗糖溶液中滴加稀硫酸,水浴加热,加入新制Cu(OH)2悬浊液 无砖红色沉淀 蔗糖未发生水解
D 加热试管中的聚氯乙烯薄膜碎片 试管口润湿的蓝色石蕊试纸变红 氯乙烯加聚是可逆反应
A.A B.B C.C D.D
二、填空题
16.氨基酸是具有两性特点的有机物,在结构上都具有的官能团名称是__、__。我们从食物中摄取的__在胃液中的胃蛋白酶和胰蛋白酶的作用下发生__反应,生成氨基酸,它被人体吸收后,重新合成人体所需要的各种__。
17.根据要求回答下列问题。
(1)碳-14可用于考古断代,写出能表示质量数和质子数的碳-14原子:_______。
(2)在没有洗洁精的年代,多用纯碱和温度较高的水洗涤餐具上的油污,解释去污原理:_______。
(3)我国科学家发明了利用二氧化碳制备淀粉。淀粉水解可制得葡萄糖,如下图:
淀粉水解的化学方程式是_______,滴加新制的银氨溶液并水浴加热,未观察到预期的银镜现象,原因是_______。
(4)在烧杯中盛有20mL滴加几滴酚酞试剂的稀NaOH溶液,然后向其中加入一药匙粉末,溶液的红色最终_______(填“加深”“变浅”“不变”或“消失”)。
三、实验题
18.可再生的生物质资源的应用是科学家研究的重大课题。我国科学家研发了葡萄糖的各种应用。
Ⅰ.淀粉是绿色植物光合作用的产物,淀粉在酸或酶的作用下水解,生成一系列产物,最终生成葡萄糖。
(1)写出淀粉在稀硫酸作催化剂发生水解反应的化学方程式____。
(2)某小组同学欲检验淀粉水解后产生葡萄糖,按如图进行实验,未观察到产生红色沉淀,原因是____。
Ⅱ.聚乳酸是一种可生物降解的高分子材料,主要用于制造可降解纤维、可降解塑料和医用材料。以葡萄糖为原料可以制备聚乳酸,相互转化关系如图:
(3)反应②的化学方程式为____。
(4)两分子的乳酸发生酯化反应可以生成六元环状化合物,写出该反应的化学方程式___。
Ⅲ.葡萄糖在不同的氧化剂作用下可以发生以下转化关系:
→→
已知A和B都不能发生银镜反应,且以下几类有机化合物被氧化的容易程度:RCHO>R—CH2OH>。
(5)A脱水可得到具有五元环状结构的酯C或具有六元环状结构的酯D,写出C的结构简式____。
(6)写出B的结构简式____。
19.工业上常以淀粉为原料生产葡萄糖、酒精和醋酸等。其转化过程如下:
(1)实验室检验淀粉是否完全水解的试剂是_______(写名称)。
(2)醋酸中所含官能团的名称是_______。
(3)工业上还可以利用乙烯和水在一定条件下制取乙醇,该反应的反应类型为_______。
(4)实验室采用如图所示装置制备乙酸乙酯。
①该反应的化学方程式为_______。
②反应结束后,从右侧试管混合物中分离出乙酸乙酯,请简述操作方法:_______。
③实验结束后,取下盛有饱和溶液的试管,再沿该试管内壁缓缓加入紫色石蕊试液(整个过程不振荡试管),发现石蕊试液层存在于饱和溶液层与乙酸乙酯层之间。下列有关该实验的分析正确的是_______。
A.乙酸乙酯中含有杂质
B.乙酸乙酯的密度小于饱和溶液
C.石蕊试液层的颜色由上而下分别呈蓝、紫、红
四、计算题
20.参考下列①~③项内容,回答问题:
①皂化值,是使1g油脂皂化所需要的KOH的毫克数。
②碘值,是使100g油脂与碘加成时消耗单质碘的克数。
③几种油脂的皂化值、碘值列表如下:
花生油 亚麻仁油 牛油 黄油 硬化大豆油 大豆油
皂化值 190 180 192 226 193 193
碘值 90 182 38 38 5 126
(1)甘油酯(相对分子质量为884)形成的油,用KOH皂化时,其皂化值为________,反应的化学方程式:_______________________。
(2)填空回答:
①亚麻仁油比花生油所含的________________;
②黄油比牛油________________;
③硬化大豆油的碘值小的原因是________________。
(3)为使碘值为180的100g鱼油硬化,所需的氢气的体积在标准状况下为多少升 _____________ 。
(4)用下列结构式所代表的酯,若皂化值为430,求n为多少 _____________并完成下列反应方程式,
→________________+________________。
21.有葡萄糖和麦芽糖的混合物90g,溶于足量的水中,在稀硫酸催化下充分反应后,用NaOH溶液中和水解液,再加入足量的Cu(OH)2悬浊液并加热煮沸,测得生成Cu2O沉淀为75.6g,求原混合物中麦芽糖的质量分数。
参考答案:
1.B
【详解】A.蜡烛的燃烧反应属于氧化还原反应,故A正确;
B.明矾只有净水作用,没有杀菌作用,故B错误;
C.树肤、麻头中富含纤维素,故C正确;
D.空气属于胶体,海市蜃楼的出现是光的一种折射现象,所以和胶体知识有关,故D正确;
答案选:B。
2.C
【详解】①柴的主要成分是纤维素,②米中含有淀粉,③油属于油脂,⑥醋中含有醋酸,纤维素、淀粉、油脂、醋酸均属于有机物;⑤酱、⑦茶中均含有多种有机物;日常生活中的④盐是指氯化钠,属于无机物,故选C。
3.D
【详解】A.苯的密度小于水,将苯加入溴水中充分振荡后静置,下层接近无色,说明溴在苯中的溶解度大于在水中的溶解度,苯分子不存在碳碳双键,故A错误;
B.检验淀粉是否水解时应先调溶液为碱性,再加新制氢氧化铜悬浊液,加热煮沸,直接加入新制氢氧化铜时优先发生中和反应,达不到实验目的,故B错误;
C.向两份蛋白质溶液中分别滴加饱和NaCl溶液和溶液,均有固体析出,前者是因为盐析,后者是因为蛋白质遇重金属离子变性,故C错误;
D.向苯和甲苯中分别滴加少量酸性溶液,充分振荡,苯与不反应,下层为紫红色;甲苯被酸性氧化成苯甲酸而褪色,下层为无色,说明苯环使甲基变活泼,故D正确;
故选D。
4.B
【详解】A.聚乙烯是乙烯通过加聚反应得到,属于高分子化合物,故A正确;
B.氮化硼陶瓷是新型无机非金属材料,故B错误;
C.葡萄酒中通常添加微量,作抗氧剂,具有杀菌并防止营养成分被氧化的作用,故C正确;
D.地沟油不能食用,地沟油主要是油脂,但可以用来制肥皂或生物柴油,实现变废为宝,故D正确。
综上所述,答案为B。
5.C
【详解】A.蔗糖水解生成葡萄糖和果糖,A项错误;
B.重金属盐才能使蛋白质变性,而鸡蛋清溶液加硫酸镁,蛋白质发生盐析,而不会变性,B项错误;
C.油脂的氢化是油与氢气发生加成反应生成脂肪,C项正确;
D.淀粉和纤维素的化学式为(C6H10O5)n,化学式中的n值不同,故淀粉和纤维素不互为同分异构体,D项错误;
答案选C。
6.A
【详解】A.由结构可知分子式为C14H18N2O5,阿斯巴甜只有1个肽键,不属于蛋白质,故A正确;
B.水解时肽键、酯基均断裂,生成氨基丁二酸、氨基苯丙酸,两种氨基酸,故B错误;
C.含氨基、﹣COOH,能与酸、碱反应,故C错误;
D.连接4个不同基团的C原子为手性碳原子,结构中与氨基、亚氨基相连的C为手性碳,共有2个,故D错误;
故选:A。
7.A
【详解】A.硬肥皂的主要成分为高级脂肪酸钠盐,A错误;
B.乙酸乙酯在稀硫酸中水解的产物为乙酸和乙醇,都能与钠反应,B正确;
C.葡萄糖含醛基、麦芽糖是一种还原性糖,都能发生银镜反应,C正确;
D.天然油脂是各种高级脂肪酸的甘油酯组成的混合物,不是高分子化合物,没有恒定的熔点、沸点,D正确;
答案选A。
8.C
【详解】A.油脂是混合物,没有固定的熔、沸点,A项正确;
B.油脂是高级脂肪酸甘油酯,属于酯类,B项正确;
C.有的油脂含有不饱和键(如植物油),能发生加成反应,可以使溴的四氯化碳溶液褪色,C项错误;
D.油脂是高级脂肪酸甘油酯,D项正确;
答案选C。
9.D
【详解】A.向25ml 沸水中滴加5~6滴 FeCl3饱和溶液,继续煮沸,溶液呈红褐色时,停止加热,得到Fe(OH)3 胶体,故A错误;
B.欲收集酯化反应生成的乙酸乙酯并分离提纯,为防止倒吸,导管不能在饱和Na2CO3溶液的液面下,故B错误;
C.淀粉溶液中加入几滴稀硫酸,水浴加热几分钟,加入氢氧化钠使溶液呈碱性,再加入新制银氨溶液,水浴加热,故C错误;
D.KI3溶液中存在I3-I2+I-,所以分别滴加淀粉溶液和AgNO3溶液,前者溶液变蓝,后者有黄色沉淀,故D正确;
答案选D。
10.A
【详解】A.蛋白质的盐析是一个可逆过程,析出的蛋白质在水中仍能溶解,不影响其活性,多次盐析和溶解可分离、提纯蛋白质,故A正确;
B.酶的主要成分是蛋白质,温度太高,蛋白质会发生变性,酶的催化效率会降低,故B错误;
C.“钡餐”的成分是硫酸钡,硫酸钡不溶于酸,无法电离出钡离子,不会引起中毒,故C错误;
D.含苯环的蛋白质遇到浓硝酸会显黄色,不是所有的,故D错误;
故选A。
11.B
【详解】在某些物理或化学因素的影响下,引起蛋白质理化性质和生物活性的变化,此时发生了蛋白质的变性,答案选B。
【点睛】
12.C
【详解】A.通过有机反应可以合成自然界不存在的新物质,例如聚乙烯等人工合成高分子化合物,A正确;
B. 石油裂化可得到裂化汽油等产品、油脂硬化得到氢化植物油、橡胶老化中涉及碳碳双键断裂等引起结构变化,均有新物质生成、均是化学变化,B正确;
C.合成纤维例如聚酯纤维、聚酰胺等可通过缩聚反应生成, C不正确;
D. 蛋白质、纤维素、核酸均属生物大分子,均能发生水解反应,蛋白质水解最终得到氨基酸、纤维素水解得到葡萄糖、核酸水解得到核苷酸、核苷酸还能进一步水解, D正确;
答案选C。
13.C
【详解】《后汉书郡国志》中记载:“石出泉水其水有肥,燃之极明,不可食,县人谓之石漆。”可以知道,此石漆是在自然界存在的,且不能食用,可以燃烧,火焰明亮;《酉阳杂俎》一书:“高奴县石脂水,水腻,浮上如漆,采以膏车及燃灯极明。”可以知道,石脂水难溶于水,且浮在水面上,说明密度比水小,且颜色呈黑色,燃烧时火焰明亮,综上所述,只有石油符合题意;
选C。
14.D
【详解】A.向平衡体系2NO2N2O4中加压,NO2浓度增大,气体颜色先变深,后又因2NO2N2O4的平衡正向移动,颜色逐渐变浅,因此现象应为气体颜色先变深后变浅,故A错误;
B.加入稀硫酸使淀粉水解后,应在碱性环境下检验葡萄糖,即应先加过量的NaOH中和稀硫酸,再加入新制Cu(OH)2悬浊液,故B错误;
C.根据金属单质与水或酸反应置换出氢的难易判断金属性的强弱,与NaOH是否反应不能作为判断金属性强弱的依据,故C错误;
D.向海带灰的浸取液中滴加适量氯水,再加入CCl4萃取,溶液分层,下层出现紫红色,说明生成了I2,从而证明海带中含有碘元素,故D正确;
答案选D。
15.B
【详解】A.亚铁离子、浓盐酸均可被酸性高锰酸钾溶液氧化,紫色褪去,不能证明铁锈中含有二价铁,故A错误;
B.不饱和烃与溴发生加成反应,由实验操作和现象可知,气体中含有烯烃,故B正确;
C.蔗糖水解后,在碱性溶液中检验葡萄糖,水解后没有加NaOH中和硫酸,操作不合理,不能证明蔗糖未水解,故C错误;
D.加热聚氯乙烯,生成HCl可使润湿的蓝色石蕊试纸变红,由实验操作及现象不能证明氯乙烯加聚是可逆反应,故D错误;
故选:B。
16. 氨基 羧基 蛋白质 水解 蛋白质
【详解】氨基酸是具有两性特点的有机物,在结构上都具有的官能团名称是氨基和羧基。蛋白质在胃液中的胃蛋白酶和胰蛋白酶的作用下发生水解反应,生成氨基酸,被人体吸收后,重新合成新的蛋白质。
17.(1)
(2)油污的主要成分是油脂,纯碱水解显碱性,碱性条件下油脂水解,且温度高能促进和油脂的水解,合理即可
(3) 未加NaOH溶液中和稀硫酸(合理即可)
(4)消失
【解析】(1)
碳的质量数为14,质子数为6,则其原子可表示为。
(2)
多用纯碱和温度较高的水洗涤餐具上的油污,去污原理为:油污的主要成分是油脂,纯碱水解显碱性,碱性条件下油脂水解,且温度高能促进和油脂的水解;
(3)
淀粉水解生成葡萄糖,则反应方程式为,酸性条件下,淀粉水解后溶液为酸性,需加NaOH溶液中和其中的稀硫酸,用银氨溶液检验醛基需要在碱性条件下,未观察到预期的银镜现象,原因是未加NaOH溶液中和稀硫酸;
(4)
具有强氧化性,且其溶于水除生成外,还生成具有强氧化性的,使酚酞褪色,最终溶液的红色消失。
18.(1)(C6H10O5)n(淀粉)+nH2OnC6H12O6(葡萄糖)
(2)水解后未加入NaOH中和溶液至碱性
(3)n+(n-1)H2O
(4)2+2H2O
(5)
(6)HOOC(CHOH)4COOH
【详解】(1)淀粉在稀硫酸作催化剂时发生水解反应生成葡萄糖,反应的化学方程式为:(C6H10O5)n(淀粉)+nH2OnC6H12O6(葡萄糖)。
(2)检验淀粉水解后产生了葡萄糖,必须在碱性条件下用新制氢氧化铜悬浊液与水解液共热;图示实验未观察到产生红色沉淀的原因是:水解后未加入NaOH中和溶液至碱性。
(3)乳酸中含羧基和羟基,乳酸发生缩聚反应生成聚乳酸,反应的化学方程式为:n+(n-1)H2O。
(4)两分子乳酸发生分子间酯化反应生成六元环状化合物,反应的化学方程式为:2+2H2O。
(5)葡萄糖的分子式为C6H12O6、结构简式为HOCH2(CHOH)4CHO,根据A、B的分子式可知,葡萄糖→A以及A→B均为氧化反应,结合“有机物被氧化的容易程度:RCHO>R—CH2OH>”,A和B都不能发生银镜反应,则A的结构简式为HOCH2(CHOH)4COOH,B的结构简式为HOOC(CHOH)4COOH;A脱水可得到具有五元环状结构的酯C或具有六元环状结构的酯D,则C的结构简式为,D的结构简式为:。
(6)B的结构简式为HOOC(CHOH)4COOH。
19. 碘水 羧基 加成反应 将混合物加入分液漏斗中,充分振荡、静置,将水层从分液漏斗下口放出,再将上层乙酸乙酯从分液漏斗上口倒出 AB
【分析】(1)淀粉遇碘变蓝;
(2)醋酸的结构简式为:CH3COOH;
(3)乙烯和水在一定条件下制取乙醇,该反应的反应类型为加成反应;
(4)①该反应利用乙酸和乙醇,在浓硫酸和加热作用下,制备乙酸乙酯;
②乙酸乙酯不溶于水,反应结束后,采用分液法分离;
③由于乙酸、乙醇和乙酸乙酯都是易挥发的液体,故试管中收集的产品中一定混有乙酸和乙醇,乙酸显酸性,碳酸钠溶液显碱性。
【详解】(1)淀粉遇碘变蓝,实验室检验淀粉是否完全水解的试剂是碘水,故答案为:碘水;
(2)醋酸的结构简式为:CH3COOH,所含官能团的名称是羧基,故答案为:羧基;
(3)乙烯和水在一定条件下制取乙醇,该反应的反应类型为加成反应,故答案为:加成反应;
(4)①该反应利用乙酸和乙醇,在浓硫酸和加热作用下,制备乙酸乙酯,其化学方程式为:,故答案为:;
②反应结束后,从右侧试管混合物中分离出乙酸乙酯,操作方法:将混合物加入分液漏斗中,充分振荡、静置,将水层从分液漏斗下口放出,再将上层乙酸乙酯从分液漏斗上口倒出,故答案为:将混合物加入分液漏斗中,充分振荡、静置,将水层从分液漏斗下口放出,再将上层乙酸乙酯从分液漏斗上口倒出;
③A.由于乙酸、乙醇和乙酸乙酯都是易挥发的液体,故试管中收集的产品中一定混有乙酸和乙醇,A项正确;
B.乙酸乙酯的密度小于饱和溶液,乙酸乙酯在上层,B项正确;
C.石蕊试液层为三层环,乙酸乙酯的密度比水小,其中的杂质乙酸使石蕊变红;中间的石蕊显紫色;碳酸钠溶液显碱性,故下层的石蕊显蓝色,故由上而下是红、紫、蓝,C项不正确;
故答案为:AB。
【点睛】本题难点(4)③,判断反应后收集装置中的现象,要根据物质的性质判断。该反应中,乙醇和乙酸易挥发,故试管中收集的产品中一定混有乙酸和乙醇,乙酸显酸性,碳酸钠溶液显碱性,不振荡试管情况下,可以快速判断试管现象。
20.(1) 190 (C17H2COO)3C3H5+3KOH→3C17H23COOK+C3H5(OH)3
(2) 不饱和脂肪酸(酸根)多 低级脂肪酸(酸根)多 不饱和键少
(3)15.9 L
(4) 4 C4H9COOK C2H5OH
【分析】(1)皂化值是指1g油脂发生皂化反应需要消耗多少氢氧化钾;
(2)油脂相对分子质量越小,皂化值越大:油脂相对分子质量越大,皂化值越小;而碘值越大,不饱和键数目越多;碘值越小,不饱和键数目越小;
(3)1mol碘单质相当于1mol氢气;
(4)酯水解时,1mol酯耗1mol KOH。
【详解】(1)(C17H33COO)3C3H5用氢氧化钾皂化时,反应方程式为:(C17H33COO)3C3H5+3KOH3C17H33COOK+C3H5(OH)3,可得关系式:
即皂化值为:3×g×1000≈190g;
(2)①亚麻仁油和花生油相比,皂化值相近,但碘值要大近两倍,亚麻仁油所含有不饱和脂肪酸(酸根)多;因此,本题正确答案是:不饱和脂肪酸(酸根)多。
②黄油比牛油的皂化值大,而碘值相等,说明黄油的平均相对分子质量较小,黄油所含有低级脂肪酸(酸根)多;因此,本题正确答案是:低级脂肪酸(酸根)多。
③硬化大豆油碘值很小,是因为已经经过硬化处理,含有的碳碳双键很少,所以烃基中的不饱和键较少;因此,本题正确答案是:不饱和键少。
(3)碘值是100g油脂加成碘的克数,不饱和烃基加成碘或氢气的物质的量相等,故有:I2~H2关系:设需H2V L,
解得:V=22.4× L=15.9 L;
(4)酯水解时,1mol酯耗1mol KOH,
即:
解得:n=4,反应方程式为:C4H9COOC2H5+KOH→C4H9COOK+C2H5OH。
21.95%
【详解】麦芽糖是二糖,1mol麦芽糖水解后产生2mol葡萄糖,1mol葡萄糖含有1mol醛基,而1mol醛基与Cu(OH)2悬浊液反应生成1molCu2O,即C6H12O6~Cu2O, ,设葡萄糖的物质的量是x,麦芽糖的物质的量是y,
解得y=0.25mol, ,其质量分数是 。
【点睛】二糖中,1mol蔗糖水解生成1mol葡萄糖和1mol果糖;1mol麦芽糖水解生成1mol葡萄糖。多糖中,淀粉、纤维素完全水解所得产物均为葡萄糖。
一、单选题
1.我国人民在悠久的历史中创造了绚丽多彩的中华文化。下列说法错误的是( )
A.“春蚕到死丝方尽,蜡炬成灰泪始干”中涉及氧化还原反应
B.“川麻不浆,以胶(动物胶和明矾)作黄纸”,“胶”中的明矾作杀菌剂
C.“伦乃造意,用树肤、麻头及敝布、鱼网以为纸”,树肤、麻头等富含纤维素
D.“忽闻海上有仙山,山在虚无缥缈间”的海市蜃楼是一种自然现象,与胶体知识有关
2.在日常生活中我们常说开门七件事:①柴;②米;③油;④盐;⑤酱;⑥醋;⑦茶。你认为其中含有有机物的是
A.除②外都含有 B.除⑦外都含有 C.除④外都含有 D.全部含有
3.下列化学实验中的操作、现象及结论都正确的是
选项 操作 现象 结论
A 将苯加入溴水中充分振荡后静置 下层接近无色 苯分子中含碳碳双键
B 淀粉溶液和稀硫酸共热后,加入新制的氢氧化铜悬浊液,加热煮沸 未出现砖红色沉淀 淀粉未水解
C 向两份蛋白质溶液中分别滴加饱和NaCl溶液和溶液 均有固体析出 蛋白质均发生变性
D 向苯和甲苯中分别滴加少量酸性溶液,充分振荡 苯中下层溶液为紫红色,甲苯中溶液为无色 苯环使甲基变活泼
A.A B.B C.C D.D
4.从科技前沿到日常生活,化学无处不在。下列说法错误的是
A.北京冬奥会的吉祥物“冰墩墩”使用的聚乙烯属于高分子化合物
B.“天和”核心舱中使用的氮化硼陶瓷基复合材料属于高分子化合物
C.葡萄酒中通常添加微量,具有杀菌并防止营养成分被氧化的作用
D.地沟油不能食用,但可以用来制肥皂或生物柴油,实现变废为宝
5.糖类、油脂、蛋白质是生命体的重要物质,下列说法正确的是
A.蔗糖水解产物只有葡萄糖 B.鸡蛋清溶液加硫酸镁会发生变性
C.油脂的氢化是加成反应 D.淀粉和纤维素互为同分异构体
6.阿斯巴甜(Aspartame,结构简式如图所示)具有清爽的甜味,甜度约为蔗糖的200倍。下列有关说法正确的是
A.分子式为C14H18N2O5,阿斯巴甜不属于蛋白质
B.阿斯巴甜的水解产物中只有一种氨基酸
C.阿斯巴甜在一定条件下不能与酸反应、只能与碱反应
D.阿斯巴甜分子中有3个手性碳原子
7.下列关于有机物的说法错误的是
A.生活中常用的硬肥皂是由高级脂肪酸钾盐制成的肥皂
B.乙酸乙酯在稀硫酸中水解的产物都能与钠反应
C.葡萄糖和麦芽糖都能发生银镜反应
D.天然油脂不是高分子化合物,没有恒定的熔点、沸点
8.下列关于油脂的叙述错误的是
A.油脂没有固定的熔、沸点
B.油脂属于酯类
C.油脂都不能使溴的四氯化碳溶液褪色
D.油脂是高级脂肪酸甘油酯
9.下列实验操作、现象与所得结论一致的是
实验操作 现象 结论
A 向25ml 沸水中滴加5~6滴 FeCl3饱和溶液,持续加热煮沸 变为红褐色 最终制得 Fe(OH)3 胶体
B 欲收集酯化反应生成的乙酸乙酯并分离提纯,将导管伸入饱和Na2CO3溶液的液面下,再用分液漏斗分离 溶液分层,上层为无色油状液体 乙酸乙酯不溶于饱和Na2CO3 溶液,且密度比水小
C 淀粉溶液中加入几滴稀硫酸,水浴加热几分钟,再加入新制银氨溶液,水浴加热 无明显现象 淀粉未发生水解
D 向两支盛有KI3溶液的试管中,分别滴加淀粉溶液和AgNO3溶液 前者溶液变蓝,后者有黄色沉淀 KI3溶液中存在平衡:I3- I2+I-
A.A B.B C.C D.D
10.下列关于蛋白质的叙述正确的是
A.利用蛋白质盐析的性质,可分离、提纯蛋白质
B.温度越高,酶的催化效率越高
C.重金属盐能使蛋白质变性,所以吞服“钡餐”会引起中毒
D.所有蛋白质遇到浓硝酸均会显黄色
11.蛋白质受某些因素的影响,其空间结构发生变化(一级结构不变),引起其理化性质和生物活性的变化,此时发生了蛋白质的。
A.水解 B.变性 C.盐析 D.溶解
12.有机化学对人类生活有着十分重要的作用。下列说法错误的是
A.通过有机反应可以合成自然界不存在的新物质
B.石油裂化、油脂硬化、橡胶老化均是化学变化
C.塑料、合成纤维、合成橡胶均是通过加聚反应来合成
D.蛋白质、纤维素、核酸均属生物大分子,均能发生水解反应
13.《后汉书·郡国志》中记载:“石出泉水……其水有肥,燃之极明,不可食,县人谓之石漆。”《酉阳杂俎》一书:“高奴县石脂水,水腻,浮上如漆,采以膏车及燃灯极明。”这里的“石漆”“石脂水”是指
A.油脂 B.油漆 C.石油 D.甘油
14.实验探究是化学学科的魅力所在。下列有关实验操作、现象和结论均正确的是
选项 实验操作 实验现象 结论
A 向平衡体系2NO2N2O4中加压 红棕色变浅 平衡正向移动
B 向淀粉溶液中加入稀硫酸,加热几分钟,冷却后再加入新制Cu(OH)2悬浊液,加热 溶液中未观察到砖红色沉淀产生 淀粉没有水解
C 将大小相同的Al和Mg分别投入到相同浓度的NaOH溶液中 Al溶解有气泡产生,Mg无现象 Al的金属性强于Mg
D 向海带灰的浸取液中滴加适量氯水,再加入CCl4萃取 分层,下层出现紫红色 海带中含有碘元素
A.A B.B C.C D.D
15.由实验操作和现象,可得出相应正确结论是
实验操作 实验现象 解释或结论
A 将铁锈溶于浓盐酸中,滴入高锰酸钾溶液 紫色褪去 铁锈中含有二价铁
B 石蜡油加强热,将产生的气体通入Br2的CCl4溶液 溶液红棕色变无色 产生的气体中含有烯烃
C 向蔗糖溶液中滴加稀硫酸,水浴加热,加入新制Cu(OH)2悬浊液 无砖红色沉淀 蔗糖未发生水解
D 加热试管中的聚氯乙烯薄膜碎片 试管口润湿的蓝色石蕊试纸变红 氯乙烯加聚是可逆反应
A.A B.B C.C D.D
二、填空题
16.氨基酸是具有两性特点的有机物,在结构上都具有的官能团名称是__、__。我们从食物中摄取的__在胃液中的胃蛋白酶和胰蛋白酶的作用下发生__反应,生成氨基酸,它被人体吸收后,重新合成人体所需要的各种__。
17.根据要求回答下列问题。
(1)碳-14可用于考古断代,写出能表示质量数和质子数的碳-14原子:_______。
(2)在没有洗洁精的年代,多用纯碱和温度较高的水洗涤餐具上的油污,解释去污原理:_______。
(3)我国科学家发明了利用二氧化碳制备淀粉。淀粉水解可制得葡萄糖,如下图:
淀粉水解的化学方程式是_______,滴加新制的银氨溶液并水浴加热,未观察到预期的银镜现象,原因是_______。
(4)在烧杯中盛有20mL滴加几滴酚酞试剂的稀NaOH溶液,然后向其中加入一药匙粉末,溶液的红色最终_______(填“加深”“变浅”“不变”或“消失”)。
三、实验题
18.可再生的生物质资源的应用是科学家研究的重大课题。我国科学家研发了葡萄糖的各种应用。
Ⅰ.淀粉是绿色植物光合作用的产物,淀粉在酸或酶的作用下水解,生成一系列产物,最终生成葡萄糖。
(1)写出淀粉在稀硫酸作催化剂发生水解反应的化学方程式____。
(2)某小组同学欲检验淀粉水解后产生葡萄糖,按如图进行实验,未观察到产生红色沉淀,原因是____。
Ⅱ.聚乳酸是一种可生物降解的高分子材料,主要用于制造可降解纤维、可降解塑料和医用材料。以葡萄糖为原料可以制备聚乳酸,相互转化关系如图:
(3)反应②的化学方程式为____。
(4)两分子的乳酸发生酯化反应可以生成六元环状化合物,写出该反应的化学方程式___。
Ⅲ.葡萄糖在不同的氧化剂作用下可以发生以下转化关系:
→→
已知A和B都不能发生银镜反应,且以下几类有机化合物被氧化的容易程度:RCHO>R—CH2OH>。
(5)A脱水可得到具有五元环状结构的酯C或具有六元环状结构的酯D,写出C的结构简式____。
(6)写出B的结构简式____。
19.工业上常以淀粉为原料生产葡萄糖、酒精和醋酸等。其转化过程如下:
(1)实验室检验淀粉是否完全水解的试剂是_______(写名称)。
(2)醋酸中所含官能团的名称是_______。
(3)工业上还可以利用乙烯和水在一定条件下制取乙醇,该反应的反应类型为_______。
(4)实验室采用如图所示装置制备乙酸乙酯。
①该反应的化学方程式为_______。
②反应结束后,从右侧试管混合物中分离出乙酸乙酯,请简述操作方法:_______。
③实验结束后,取下盛有饱和溶液的试管,再沿该试管内壁缓缓加入紫色石蕊试液(整个过程不振荡试管),发现石蕊试液层存在于饱和溶液层与乙酸乙酯层之间。下列有关该实验的分析正确的是_______。
A.乙酸乙酯中含有杂质
B.乙酸乙酯的密度小于饱和溶液
C.石蕊试液层的颜色由上而下分别呈蓝、紫、红
四、计算题
20.参考下列①~③项内容,回答问题:
①皂化值,是使1g油脂皂化所需要的KOH的毫克数。
②碘值,是使100g油脂与碘加成时消耗单质碘的克数。
③几种油脂的皂化值、碘值列表如下:
花生油 亚麻仁油 牛油 黄油 硬化大豆油 大豆油
皂化值 190 180 192 226 193 193
碘值 90 182 38 38 5 126
(1)甘油酯(相对分子质量为884)形成的油,用KOH皂化时,其皂化值为________,反应的化学方程式:_______________________。
(2)填空回答:
①亚麻仁油比花生油所含的________________;
②黄油比牛油________________;
③硬化大豆油的碘值小的原因是________________。
(3)为使碘值为180的100g鱼油硬化,所需的氢气的体积在标准状况下为多少升 _____________ 。
(4)用下列结构式所代表的酯,若皂化值为430,求n为多少 _____________并完成下列反应方程式,
→________________+________________。
21.有葡萄糖和麦芽糖的混合物90g,溶于足量的水中,在稀硫酸催化下充分反应后,用NaOH溶液中和水解液,再加入足量的Cu(OH)2悬浊液并加热煮沸,测得生成Cu2O沉淀为75.6g,求原混合物中麦芽糖的质量分数。
参考答案:
1.B
【详解】A.蜡烛的燃烧反应属于氧化还原反应,故A正确;
B.明矾只有净水作用,没有杀菌作用,故B错误;
C.树肤、麻头中富含纤维素,故C正确;
D.空气属于胶体,海市蜃楼的出现是光的一种折射现象,所以和胶体知识有关,故D正确;
答案选:B。
2.C
【详解】①柴的主要成分是纤维素,②米中含有淀粉,③油属于油脂,⑥醋中含有醋酸,纤维素、淀粉、油脂、醋酸均属于有机物;⑤酱、⑦茶中均含有多种有机物;日常生活中的④盐是指氯化钠,属于无机物,故选C。
3.D
【详解】A.苯的密度小于水,将苯加入溴水中充分振荡后静置,下层接近无色,说明溴在苯中的溶解度大于在水中的溶解度,苯分子不存在碳碳双键,故A错误;
B.检验淀粉是否水解时应先调溶液为碱性,再加新制氢氧化铜悬浊液,加热煮沸,直接加入新制氢氧化铜时优先发生中和反应,达不到实验目的,故B错误;
C.向两份蛋白质溶液中分别滴加饱和NaCl溶液和溶液,均有固体析出,前者是因为盐析,后者是因为蛋白质遇重金属离子变性,故C错误;
D.向苯和甲苯中分别滴加少量酸性溶液,充分振荡,苯与不反应,下层为紫红色;甲苯被酸性氧化成苯甲酸而褪色,下层为无色,说明苯环使甲基变活泼,故D正确;
故选D。
4.B
【详解】A.聚乙烯是乙烯通过加聚反应得到,属于高分子化合物,故A正确;
B.氮化硼陶瓷是新型无机非金属材料,故B错误;
C.葡萄酒中通常添加微量,作抗氧剂,具有杀菌并防止营养成分被氧化的作用,故C正确;
D.地沟油不能食用,地沟油主要是油脂,但可以用来制肥皂或生物柴油,实现变废为宝,故D正确。
综上所述,答案为B。
5.C
【详解】A.蔗糖水解生成葡萄糖和果糖,A项错误;
B.重金属盐才能使蛋白质变性,而鸡蛋清溶液加硫酸镁,蛋白质发生盐析,而不会变性,B项错误;
C.油脂的氢化是油与氢气发生加成反应生成脂肪,C项正确;
D.淀粉和纤维素的化学式为(C6H10O5)n,化学式中的n值不同,故淀粉和纤维素不互为同分异构体,D项错误;
答案选C。
6.A
【详解】A.由结构可知分子式为C14H18N2O5,阿斯巴甜只有1个肽键,不属于蛋白质,故A正确;
B.水解时肽键、酯基均断裂,生成氨基丁二酸、氨基苯丙酸,两种氨基酸,故B错误;
C.含氨基、﹣COOH,能与酸、碱反应,故C错误;
D.连接4个不同基团的C原子为手性碳原子,结构中与氨基、亚氨基相连的C为手性碳,共有2个,故D错误;
故选:A。
7.A
【详解】A.硬肥皂的主要成分为高级脂肪酸钠盐,A错误;
B.乙酸乙酯在稀硫酸中水解的产物为乙酸和乙醇,都能与钠反应,B正确;
C.葡萄糖含醛基、麦芽糖是一种还原性糖,都能发生银镜反应,C正确;
D.天然油脂是各种高级脂肪酸的甘油酯组成的混合物,不是高分子化合物,没有恒定的熔点、沸点,D正确;
答案选A。
8.C
【详解】A.油脂是混合物,没有固定的熔、沸点,A项正确;
B.油脂是高级脂肪酸甘油酯,属于酯类,B项正确;
C.有的油脂含有不饱和键(如植物油),能发生加成反应,可以使溴的四氯化碳溶液褪色,C项错误;
D.油脂是高级脂肪酸甘油酯,D项正确;
答案选C。
9.D
【详解】A.向25ml 沸水中滴加5~6滴 FeCl3饱和溶液,继续煮沸,溶液呈红褐色时,停止加热,得到Fe(OH)3 胶体,故A错误;
B.欲收集酯化反应生成的乙酸乙酯并分离提纯,为防止倒吸,导管不能在饱和Na2CO3溶液的液面下,故B错误;
C.淀粉溶液中加入几滴稀硫酸,水浴加热几分钟,加入氢氧化钠使溶液呈碱性,再加入新制银氨溶液,水浴加热,故C错误;
D.KI3溶液中存在I3-I2+I-,所以分别滴加淀粉溶液和AgNO3溶液,前者溶液变蓝,后者有黄色沉淀,故D正确;
答案选D。
10.A
【详解】A.蛋白质的盐析是一个可逆过程,析出的蛋白质在水中仍能溶解,不影响其活性,多次盐析和溶解可分离、提纯蛋白质,故A正确;
B.酶的主要成分是蛋白质,温度太高,蛋白质会发生变性,酶的催化效率会降低,故B错误;
C.“钡餐”的成分是硫酸钡,硫酸钡不溶于酸,无法电离出钡离子,不会引起中毒,故C错误;
D.含苯环的蛋白质遇到浓硝酸会显黄色,不是所有的,故D错误;
故选A。
11.B
【详解】在某些物理或化学因素的影响下,引起蛋白质理化性质和生物活性的变化,此时发生了蛋白质的变性,答案选B。
【点睛】
12.C
【详解】A.通过有机反应可以合成自然界不存在的新物质,例如聚乙烯等人工合成高分子化合物,A正确;
B. 石油裂化可得到裂化汽油等产品、油脂硬化得到氢化植物油、橡胶老化中涉及碳碳双键断裂等引起结构变化,均有新物质生成、均是化学变化,B正确;
C.合成纤维例如聚酯纤维、聚酰胺等可通过缩聚反应生成, C不正确;
D. 蛋白质、纤维素、核酸均属生物大分子,均能发生水解反应,蛋白质水解最终得到氨基酸、纤维素水解得到葡萄糖、核酸水解得到核苷酸、核苷酸还能进一步水解, D正确;
答案选C。
13.C
【详解】《后汉书郡国志》中记载:“石出泉水其水有肥,燃之极明,不可食,县人谓之石漆。”可以知道,此石漆是在自然界存在的,且不能食用,可以燃烧,火焰明亮;《酉阳杂俎》一书:“高奴县石脂水,水腻,浮上如漆,采以膏车及燃灯极明。”可以知道,石脂水难溶于水,且浮在水面上,说明密度比水小,且颜色呈黑色,燃烧时火焰明亮,综上所述,只有石油符合题意;
选C。
14.D
【详解】A.向平衡体系2NO2N2O4中加压,NO2浓度增大,气体颜色先变深,后又因2NO2N2O4的平衡正向移动,颜色逐渐变浅,因此现象应为气体颜色先变深后变浅,故A错误;
B.加入稀硫酸使淀粉水解后,应在碱性环境下检验葡萄糖,即应先加过量的NaOH中和稀硫酸,再加入新制Cu(OH)2悬浊液,故B错误;
C.根据金属单质与水或酸反应置换出氢的难易判断金属性的强弱,与NaOH是否反应不能作为判断金属性强弱的依据,故C错误;
D.向海带灰的浸取液中滴加适量氯水,再加入CCl4萃取,溶液分层,下层出现紫红色,说明生成了I2,从而证明海带中含有碘元素,故D正确;
答案选D。
15.B
【详解】A.亚铁离子、浓盐酸均可被酸性高锰酸钾溶液氧化,紫色褪去,不能证明铁锈中含有二价铁,故A错误;
B.不饱和烃与溴发生加成反应,由实验操作和现象可知,气体中含有烯烃,故B正确;
C.蔗糖水解后,在碱性溶液中检验葡萄糖,水解后没有加NaOH中和硫酸,操作不合理,不能证明蔗糖未水解,故C错误;
D.加热聚氯乙烯,生成HCl可使润湿的蓝色石蕊试纸变红,由实验操作及现象不能证明氯乙烯加聚是可逆反应,故D错误;
故选:B。
16. 氨基 羧基 蛋白质 水解 蛋白质
【详解】氨基酸是具有两性特点的有机物,在结构上都具有的官能团名称是氨基和羧基。蛋白质在胃液中的胃蛋白酶和胰蛋白酶的作用下发生水解反应,生成氨基酸,被人体吸收后,重新合成新的蛋白质。
17.(1)
(2)油污的主要成分是油脂,纯碱水解显碱性,碱性条件下油脂水解,且温度高能促进和油脂的水解,合理即可
(3) 未加NaOH溶液中和稀硫酸(合理即可)
(4)消失
【解析】(1)
碳的质量数为14,质子数为6,则其原子可表示为。
(2)
多用纯碱和温度较高的水洗涤餐具上的油污,去污原理为:油污的主要成分是油脂,纯碱水解显碱性,碱性条件下油脂水解,且温度高能促进和油脂的水解;
(3)
淀粉水解生成葡萄糖,则反应方程式为,酸性条件下,淀粉水解后溶液为酸性,需加NaOH溶液中和其中的稀硫酸,用银氨溶液检验醛基需要在碱性条件下,未观察到预期的银镜现象,原因是未加NaOH溶液中和稀硫酸;
(4)
具有强氧化性,且其溶于水除生成外,还生成具有强氧化性的,使酚酞褪色,最终溶液的红色消失。
18.(1)(C6H10O5)n(淀粉)+nH2OnC6H12O6(葡萄糖)
(2)水解后未加入NaOH中和溶液至碱性
(3)n+(n-1)H2O
(4)2+2H2O
(5)
(6)HOOC(CHOH)4COOH
【详解】(1)淀粉在稀硫酸作催化剂时发生水解反应生成葡萄糖,反应的化学方程式为:(C6H10O5)n(淀粉)+nH2OnC6H12O6(葡萄糖)。
(2)检验淀粉水解后产生了葡萄糖,必须在碱性条件下用新制氢氧化铜悬浊液与水解液共热;图示实验未观察到产生红色沉淀的原因是:水解后未加入NaOH中和溶液至碱性。
(3)乳酸中含羧基和羟基,乳酸发生缩聚反应生成聚乳酸,反应的化学方程式为:n+(n-1)H2O。
(4)两分子乳酸发生分子间酯化反应生成六元环状化合物,反应的化学方程式为:2+2H2O。
(5)葡萄糖的分子式为C6H12O6、结构简式为HOCH2(CHOH)4CHO,根据A、B的分子式可知,葡萄糖→A以及A→B均为氧化反应,结合“有机物被氧化的容易程度:RCHO>R—CH2OH>”,A和B都不能发生银镜反应,则A的结构简式为HOCH2(CHOH)4COOH,B的结构简式为HOOC(CHOH)4COOH;A脱水可得到具有五元环状结构的酯C或具有六元环状结构的酯D,则C的结构简式为,D的结构简式为:。
(6)B的结构简式为HOOC(CHOH)4COOH。
19. 碘水 羧基 加成反应 将混合物加入分液漏斗中,充分振荡、静置,将水层从分液漏斗下口放出,再将上层乙酸乙酯从分液漏斗上口倒出 AB
【分析】(1)淀粉遇碘变蓝;
(2)醋酸的结构简式为:CH3COOH;
(3)乙烯和水在一定条件下制取乙醇,该反应的反应类型为加成反应;
(4)①该反应利用乙酸和乙醇,在浓硫酸和加热作用下,制备乙酸乙酯;
②乙酸乙酯不溶于水,反应结束后,采用分液法分离;
③由于乙酸、乙醇和乙酸乙酯都是易挥发的液体,故试管中收集的产品中一定混有乙酸和乙醇,乙酸显酸性,碳酸钠溶液显碱性。
【详解】(1)淀粉遇碘变蓝,实验室检验淀粉是否完全水解的试剂是碘水,故答案为:碘水;
(2)醋酸的结构简式为:CH3COOH,所含官能团的名称是羧基,故答案为:羧基;
(3)乙烯和水在一定条件下制取乙醇,该反应的反应类型为加成反应,故答案为:加成反应;
(4)①该反应利用乙酸和乙醇,在浓硫酸和加热作用下,制备乙酸乙酯,其化学方程式为:,故答案为:;
②反应结束后,从右侧试管混合物中分离出乙酸乙酯,操作方法:将混合物加入分液漏斗中,充分振荡、静置,将水层从分液漏斗下口放出,再将上层乙酸乙酯从分液漏斗上口倒出,故答案为:将混合物加入分液漏斗中,充分振荡、静置,将水层从分液漏斗下口放出,再将上层乙酸乙酯从分液漏斗上口倒出;
③A.由于乙酸、乙醇和乙酸乙酯都是易挥发的液体,故试管中收集的产品中一定混有乙酸和乙醇,A项正确;
B.乙酸乙酯的密度小于饱和溶液,乙酸乙酯在上层,B项正确;
C.石蕊试液层为三层环,乙酸乙酯的密度比水小,其中的杂质乙酸使石蕊变红;中间的石蕊显紫色;碳酸钠溶液显碱性,故下层的石蕊显蓝色,故由上而下是红、紫、蓝,C项不正确;
故答案为:AB。
【点睛】本题难点(4)③,判断反应后收集装置中的现象,要根据物质的性质判断。该反应中,乙醇和乙酸易挥发,故试管中收集的产品中一定混有乙酸和乙醇,乙酸显酸性,碳酸钠溶液显碱性,不振荡试管情况下,可以快速判断试管现象。
20.(1) 190 (C17H2COO)3C3H5+3KOH→3C17H23COOK+C3H5(OH)3
(2) 不饱和脂肪酸(酸根)多 低级脂肪酸(酸根)多 不饱和键少
(3)15.9 L
(4) 4 C4H9COOK C2H5OH
【分析】(1)皂化值是指1g油脂发生皂化反应需要消耗多少氢氧化钾;
(2)油脂相对分子质量越小,皂化值越大:油脂相对分子质量越大,皂化值越小;而碘值越大,不饱和键数目越多;碘值越小,不饱和键数目越小;
(3)1mol碘单质相当于1mol氢气;
(4)酯水解时,1mol酯耗1mol KOH。
【详解】(1)(C17H33COO)3C3H5用氢氧化钾皂化时,反应方程式为:(C17H33COO)3C3H5+3KOH3C17H33COOK+C3H5(OH)3,可得关系式:
即皂化值为:3×g×1000≈190g;
(2)①亚麻仁油和花生油相比,皂化值相近,但碘值要大近两倍,亚麻仁油所含有不饱和脂肪酸(酸根)多;因此,本题正确答案是:不饱和脂肪酸(酸根)多。
②黄油比牛油的皂化值大,而碘值相等,说明黄油的平均相对分子质量较小,黄油所含有低级脂肪酸(酸根)多;因此,本题正确答案是:低级脂肪酸(酸根)多。
③硬化大豆油碘值很小,是因为已经经过硬化处理,含有的碳碳双键很少,所以烃基中的不饱和键较少;因此,本题正确答案是:不饱和键少。
(3)碘值是100g油脂加成碘的克数,不饱和烃基加成碘或氢气的物质的量相等,故有:I2~H2关系:设需H2V L,
解得:V=22.4× L=15.9 L;
(4)酯水解时,1mol酯耗1mol KOH,
即:
解得:n=4,反应方程式为:C4H9COOC2H5+KOH→C4H9COOK+C2H5OH。
21.95%
【详解】麦芽糖是二糖,1mol麦芽糖水解后产生2mol葡萄糖,1mol葡萄糖含有1mol醛基,而1mol醛基与Cu(OH)2悬浊液反应生成1molCu2O,即C6H12O6~Cu2O, ,设葡萄糖的物质的量是x,麦芽糖的物质的量是y,
解得y=0.25mol, ,其质量分数是 。
【点睛】二糖中,1mol蔗糖水解生成1mol葡萄糖和1mol果糖;1mol麦芽糖水解生成1mol葡萄糖。多糖中,淀粉、纤维素完全水解所得产物均为葡萄糖。
