专题3 从海水中获得的化学物质 单元检测题 高一上学期化学苏教版(2020)必修第一册(含解析)
文档属性
| 名称 | 专题3 从海水中获得的化学物质 单元检测题 高一上学期化学苏教版(2020)必修第一册(含解析) |

|
|
| 格式 | docx | ||
| 文件大小 | 887.4KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-06-17 00:00:00 | ||
图片预览


文档简介
专题3 从海水中获得的化学物质 单元检测题
一、单选题
1.如图所示,在A处通入已经干燥的氯气,当关闭B处的弹簧夹时,C处的红布条逐渐褪色:当打开B处的弹簧夹后,C处的红布条看不到明显现象。则D瓶中盛放的溶液可能是
①饱和NaCl溶液 ②NaOH溶液 ③H2O ④浓硫酸
A.①② B.①③ C.②④ D.③④
2.下列不属于纯碱在工业生的用途的是
A.纺织 B.制药 C.制皂 D.工业制备氯气
3.下列离子方程式书写正确的是
A.Cl2与水反应:Cl2+H2O=2H++Cl-+ClO-
B.硫酸与氢氧化钡溶液反应:H++OH-+Ba2++SO=H2O+BaSO4↓
C.过氧化钠与水反应:O+2H2O=2OH-+O2↑
D.NaHCO3溶液中加入过量澄清石灰水:Ca2++HCO+OH-=CaCO3↓+H2O
4.下列化合物中一般不能通过单质与氯气直接化合制得的是
A.FeCl2 B.FeCl3 C.CuCl2 D.NaCl
5.下列说法错误的是
A.分液漏斗使用前需检查是否漏水
B.分液时,先将分液漏斗中的下层液体从下口放出,再将上层液体从上口倒出
C.为保证分液漏斗内的液体顺利流下,需将玻璃塞上的凹槽对准漏斗口上的小孔或将玻璃塞拿下
D.用铂丝做焰色反应实验时,若焰色呈黄色,说明待测物质中一定含有钠元素,不含钾元素
6.下列叙述中,不符合化学事实的是
A.1965年我国科学家首次成功合成了结晶牛胰岛素
B.《梦溪笔谈》中记载“熬胆矾铁釜,久之亦化为铜”,是发生了置换反应
C.侯氏制碱法所制得“碱”的主要成分是氢氧化钠
D.五彩缤纷的烟花利用了焰色试验的原理
7.为了除去NaHCO3溶液中含有的Na2CO3,下列方案可行的是
A.滴加适量盐酸 B.滴加BaCl2溶液,后过滤
C.通入足量的CO2气体 D.加热溶液
8.工业上制取的化学反应为,下列说法正确的是
A.在反应中被氧化
B.在反应中失去电子
C.在反应中作氧化剂
D.生成1个分子时,转移的电子数为2
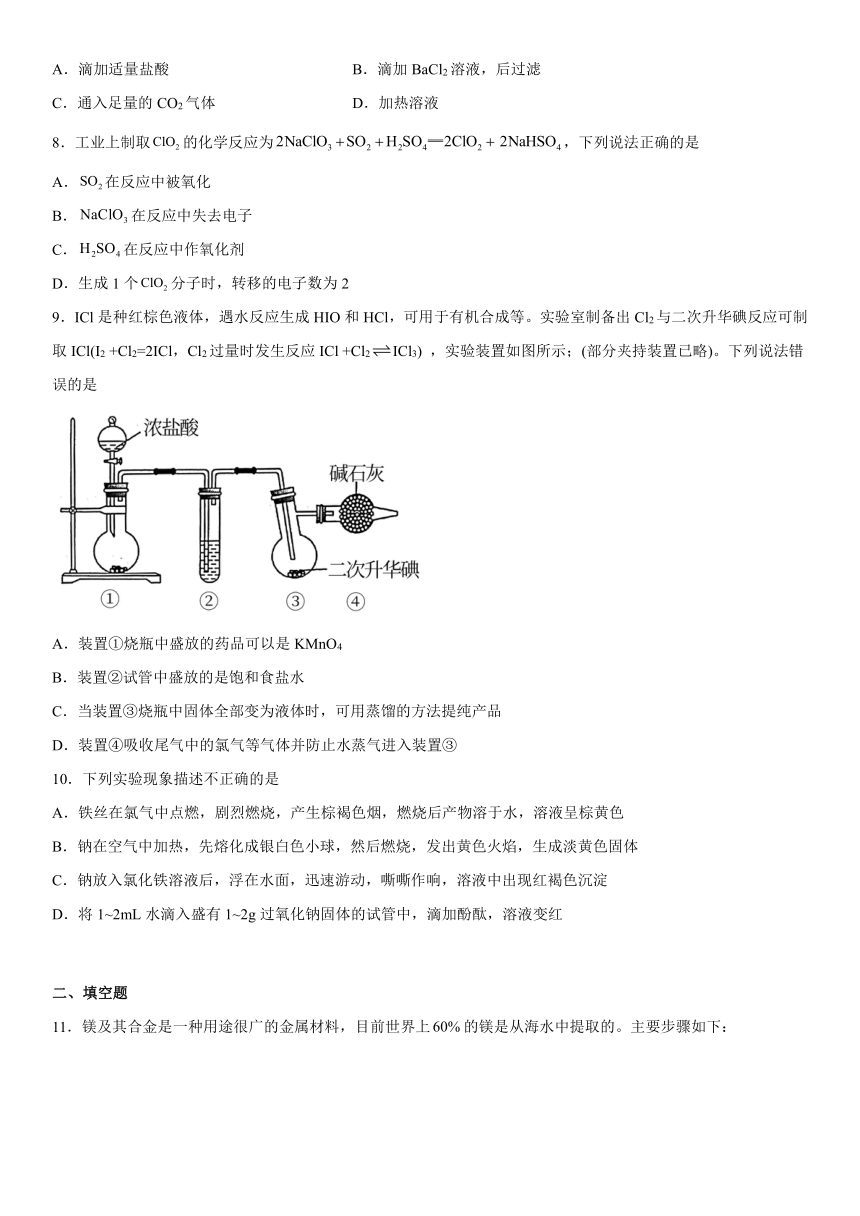
9.ICl是种红棕色液体,遇水反应生成HIO和HCl,可用于有机合成等。实验室制备出Cl2与二次升华碘反应可制取ICl(I2 +Cl2=2ICl,Cl2过量时发生反应ICl +Cl2ICl3) ,实验装置如图所示;(部分夹持装置已略)。下列说法错误的是
A.装置①烧瓶中盛放的药品可以是KMnO4
B.装置②试管中盛放的是饱和食盐水
C.当装置③烧瓶中固体全部变为液体时,可用蒸馏的方法提纯产品
D.装置④吸收尾气中的氯气等气体并防止水蒸气进入装置③
10.下列实验现象描述不正确的是
A.铁丝在氯气中点燃,剧烈燃烧,产生棕褐色烟,燃烧后产物溶于水,溶液呈棕黄色
B.钠在空气中加热,先熔化成银白色小球,然后燃烧,发出黄色火焰,生成淡黄色固体
C.钠放入氯化铁溶液后,浮在水面,迅速游动,嘶嘶作响,溶液中出现红褐色沉淀
D.将1~2mL水滴入盛有1~2g过氧化钠固体的试管中,滴加酚酞,溶液变红
二、填空题
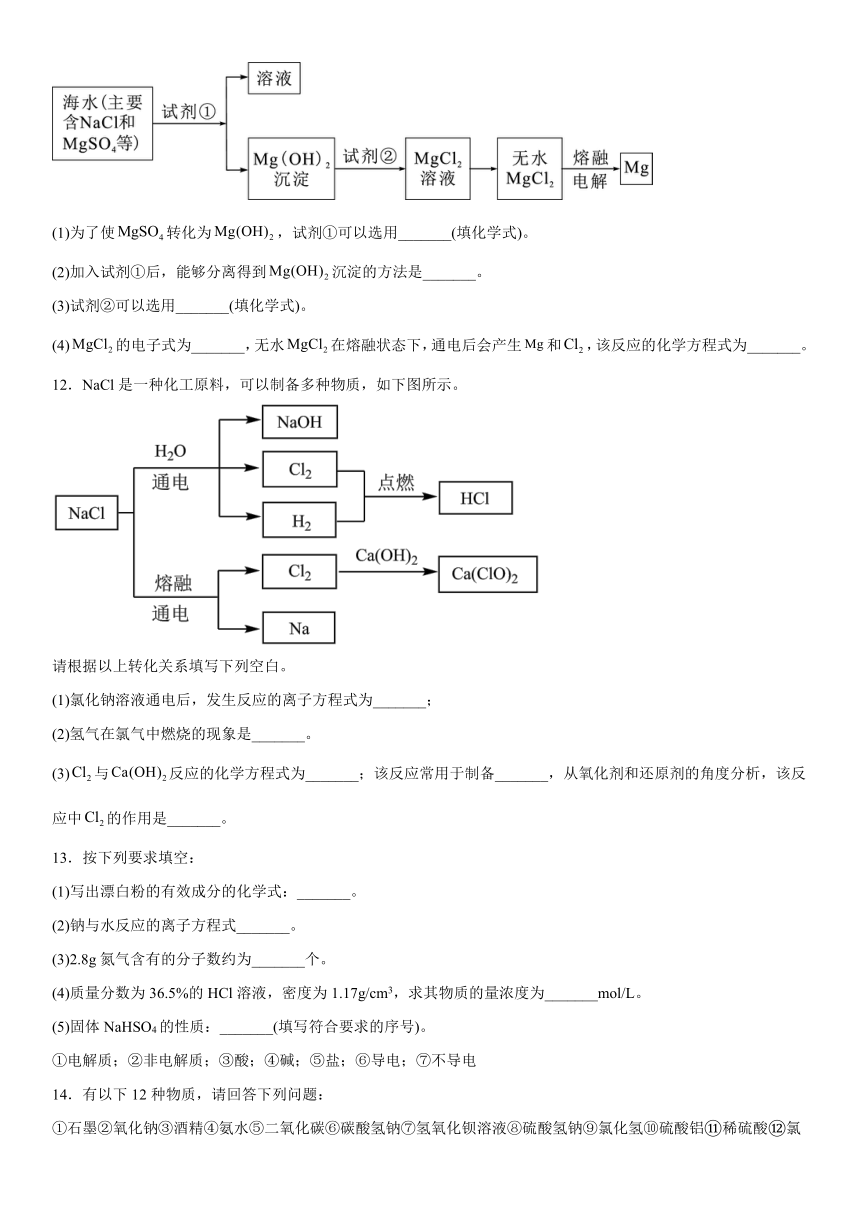
11.镁及其合金是一种用途很广的金属材料,目前世界上的镁是从海水中提取的。主要步骤如下:
(1)为了使转化为,试剂①可以选用_______(填化学式)。
(2)加入试剂①后,能够分离得到沉淀的方法是_______。
(3)试剂②可以选用_______(填化学式)。
(4)的电子式为_______,无水在熔融状态下,通电后会产生和,该反应的化学方程式为_______。
12.NaCl是一种化工原料,可以制备多种物质,如下图所示。
请根据以上转化关系填写下列空白。
(1)氯化钠溶液通电后,发生反应的离子方程式为_______;
(2)氢气在氯气中燃烧的现象是_______。
(3)与反应的化学方程式为_______;该反应常用于制备_______,从氧化剂和还原剂的角度分析,该反应中的作用是_______。
13.按下列要求填空:
(1)写出漂白粉的有效成分的化学式:_______。
(2)钠与水反应的离子方程式_______。
(3)2.8g氮气含有的分子数约为_______个。
(4)质量分数为36.5%的HCl溶液,密度为1.17g/cm3,求其物质的量浓度为_______mol/L。
(5)固体NaHSO4的性质:_______(填写符合要求的序号)。
①电解质;②非电解质;③酸;④碱;⑤盐;⑥导电;⑦不导电
14.有以下12种物质,请回答下列问题:
①石墨②氧化钠③酒精④氨水⑤二氧化碳⑥碳酸氢钠⑦氢氧化钡溶液⑧硫酸氢钠⑨氯化氢⑩硫酸铝 稀硫酸 氯化银
(1)其中能导电的是___;属于电解质的是___;属于非电解质的是___。
(2)写出物质⑧溶于水的电离方程式:___。
(3)写出物质⑦和 反应的离子方程式:___。
(4)写出物质⑥和⑨在水中发生反应的离子方程式:___。
15.国际化学年的中国宣传口号是“化学——我们的生活,我们的未来”。学习化学应该明白“从生活中来,到生活中去”的道理。请填空:
(1)金属钠着火时,不能用水灭火,原因是_______(用离子方程式表示)。
(2)常温下铁遇水不反应,但在高温条件下二者能发生反应,书写二者反应的化学方程式___。
(3)热水瓶用久后,瓶胆内常附着一层水垢(主要成分是CaCO3),用食醋能较好的清除,其原理是_______(用离子方程式表示)。
(4)铝合金材料在生活生产中应用广泛,如铝合金门窗、飞机外壳、航空航天等,且具有密度小、易加工、不易腐蚀等优点,Al与氢氧化钠溶液反应的离子方程式为___。
(5)设计实验检验实验室用KClO3和MnO2制取氧气后的产物中是否存在Cl-____。
三、计算题
16.在标准状况下进行甲、乙、丙三组实验。三组实验各取同浓度的盐酸30mL,加入同一种镁铝合金粉末,产生气体。有关数据列表如表(气体体积均为标准状况下测得):
实验序号 甲 乙 丙
合金质量/g 0.255 0.385 0.459
生成气体/ml 280 336 336
(1)甲组实验中,盐酸_____;乙组实验中,盐酸_____(填“过量“、“适量“或“不足“)。
(2)该盐酸的物质的量浓度_____。
(3)合金中Mg、Al的物质的量之比为____。
(4)在丙组实验后,向容器中加入1mol/L的NaOH溶液,恰好使合金中的铝元素全部转化为,并使Mg2+刚好沉淀完全,则溶液中的物质的量为_____mol;溶液中Na+的物质的量为______mol。
17.碳酸钠和碳酸氢钠是用途广泛的化合物。在实验室中,充分加热碳酸钠和碳酸氢钠的混合物,完全反应后称得剩余固体质量为,求混合物中碳酸氢钠的质量分数_______。
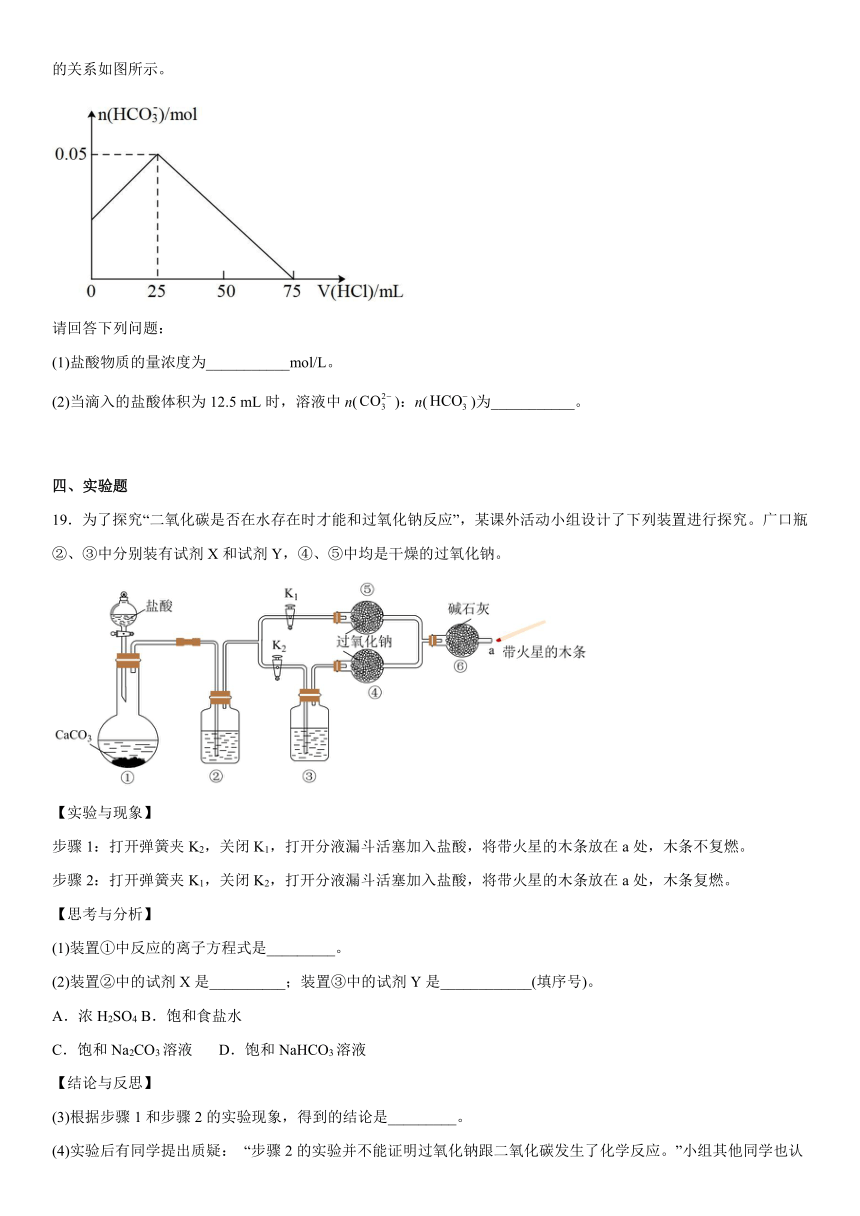
18.在Na2CO3和NaHCO3混合溶液中缓慢滴加一定浓度的盐酸,测得溶液中物质的量与所加盐酸体积之间的关系如图所示。
请回答下列问题:
(1)盐酸物质的量浓度为___________mol/L。
(2)当滴入的盐酸体积为12.5 mL时,溶液中n():n()为___________。
四、实验题
19.为了探究“二氧化碳是否在水存在时才能和过氧化钠反应”,某课外活动小组设计了下列装置进行探究。广口瓶②、③中分别装有试剂X和试剂Y,④、⑤中均是干燥的过氧化钠。
【实验与现象】
步骤1:打开弹簧夹K2,关闭K1,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处,木条不复燃。
步骤2:打开弹簧夹K1,关闭K2,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处,木条复燃。
【思考与分析】
(1)装置①中反应的离子方程式是_________。
(2)装置②中的试剂X是__________;装置③中的试剂Y是____________(填序号)。
A.浓H2SO4 B.饱和食盐水
C.饱和Na2CO3溶液 D.饱和NaHCO3溶液
【结论与反思】
(3)根据步骤1和步骤2的实验现象,得到的结论是_________。
(4)实验后有同学提出质疑: “步骤2的实验并不能证明过氧化钠跟二氧化碳发生了化学反应。”小组其他同学也认为很有道理,请写出其理由的方程式_______________。
(5)若要证明“过氧化钠跟二氧化碳发生了化学反应”,需要补充的实验操作是:取⑤中反应后的少量固体,___________________。
20.KMnO4是一种氧化剂,实验室常用KMnO4和浓盐酸反应制备Cl2。下图是制备 NaClO溶液的装置图。
完成下列填空:
(1)医疗上可用稀高锰酸钾溶液来给伤口消毒,你认为这是利用了KMnO4的_______(选填“氧化性”、“还原性”)
(2)高锰酸钾溶于水的电离方程式为_______它属于(选填“强电解质”、“弱电解质”、“非电解质”);
(3)B装置中饱和食盐水的作用是_______;
(4)D装置中NaOH的作用是_______(用离子反应方程式表示);
(5)除去Cl2中混有的氯化氢和水蒸气气体,选用的药品及顺序正确的是_______(填序号);
A.水、碱石灰 B.饱和食盐水、浓硫酸
C.无水氯化钙、饱和食盐水 D.烧碱溶液、浓硫酸
参考答案:
1.B
【解析】干燥的Cl2没有漂白性,湿润的Cl2具有漂白性;当关闭B处的弹簧夹时,C处的红布条逐渐褪色,说明干燥的Cl2变为湿润的Cl2;当关闭B处的弹簧夹后,C处的红布条看不到明显现象,说明干燥的Cl2无变化。
【解析】①关闭B处的弹簧夹时,干燥的Cl2通入到饱和NaCl溶液中,干燥的Cl2变为湿润的Cl2,C处的红布条逐渐褪色;
②关闭B处的弹簧夹时,干燥的Cl2通入到NaOH溶液中,干燥的Cl2被吸收,C处的红布条看不到明显现象;
③关闭B处的弹簧夹时,干燥的Cl2通入到H2O中,干燥的Cl2变为湿润的Cl2,C处的红布条逐渐褪色;
④关闭B处的弹簧夹时,干燥的Cl2通入到浓硫酸中,干燥的Cl2无变化,C处的红布条看不到明显现象;
综上所述,D瓶中盛放的溶液可能是①③,故选B。
2.D
【解析】纯碱是碳酸钠,是重要的化工原料之一,广泛应用于轻工日化、建材、化学工业、食品工业、冶金、纺织、石油、国防、医药等领域, 用作制造其他化学品的原料、清洗剂、洗涤剂,也用于照相术和分析领域;不用于工业制备氯气,故选D
3.D
【解析】A.HClO为弱酸,书写离子方程式时不能拆开,故为Cl2+H2O=H++Cl-+HClO,故A错误;
B.硫酸与氢氧化钡溶液反应的离子方程式为:2H++2OH-+Ba2++SO=2H2O+BaSO4↓,故B错误;
C.过氧化钠书写离子方程式时不能拆开,故C错误;
D.NaHCO3溶液中加入过量澄清石灰水生成碳酸钙沉淀和氢氧化钠、水,故离子方程式为Ca2++HCO+OH-=CaCO3↓+H2O,故D正确;
故选D。
4.A
【解析】A.氯气和铁化合反应得到氯化铁得不到氯化亚铁,A符合题意;
B.氯气和铁化合反应得到氯化铁,B不符合题意;
C.氯气和铜化合反应得到氯化铜,C不符合题意;
D.氯气和钠化合反应得到氯化钠,D不符合题意;
故选A。
5.D
【解析】由于Na的焰色反应呈黄色,而钾的焰色反应呈紫色,黄色很容易掩盖紫色,故进行钾的焰色反应时需透过蓝色钴玻璃进行观察以滤去黄色的光,即用铂丝做焰色反应实验时,若焰色呈黄色,说明待测物质中一定含有钠元素,但不能确定是否含钾元素,需透过蓝色钴玻璃进行观察,是否观察到紫色才可确定是否含钾,故答案为:D。
6.C
【解析】A.1965年,我国科学家在世界上首次成功合成了具有生命活力的蛋白质——结晶牛胰岛素,A不符合题意;
B.“熬胆矾铁釜,久之亦化为铜”,发生反应Fe+CuSO4=FeSO4+Cu,属于置换反应,B不符合题意;
C.侯氏制碱法利用NaCl、NH3、CO2、H2O为原料,制得了NH4Cl和NaHCO3,然后加热分解NaHCO3生成纯碱Na2CO3,所制得“碱”的主要成分是碳酸钠,C符合题意;
D.五彩缤纷的烟花是利用金属离子发生焰色试验的原理,从而产生不同的焰色,D不符合题意;
故选C。
7.C
【解析】A.盐酸与NaHCO3也能发生反应,不能选用,故A错误;
B.为确保碳酸钠除尽,所加氯化钡溶液应过量,在碳酸氢钠溶液中会引入氯化钠和氯化钡等新杂质,故B错误;
C.通入足量的二氧化碳,能与碳酸钠反应生成碳酸氢钠,且不引入新杂质,故C正确;
D.加热溶液导致碳酸氢钠分解成碳酸钠,故D错误;
故选:C。
8.A
【解析】在反应中元素化合价变化情况:。
A.在该反应中, S元素化合价由SO2中的+4价变为反应后NaHSO4中的+6价,化合价升高,失去电子,被氧化,A正确;
B.在反应中Cl元素化合价由反应前中的+5价变为反应后ClO2中的+2价,化合价降低,得到电子,被还原,所以作氧化剂,B错误;
C.中元素化合价在反应前后未发生变化,所以既不作氧化剂也不作还原剂,C错误;
D.反应中元素由+5价降低到+4价,降低1价,所以每生成1个分子时,转移的电子数为1,D错误;
故合理选项是A。
9.B
【解析】根据题意,整个过程中,装置③中应该在无水环境中进行,且氯气不能过量。
【解析】A. 装置①中无加热装置,而该装置为实验室制取氯气的装置,所以烧瓶中的固体可以为高锰酸钾,故A正确;
B. 进入装置③中的气体应该为干燥的氯气,所以②试管中盛放的是浓硫酸,故B错误;
C. 根据碘蒸气与氯化碘的沸点不同,可以通过蒸馏的方法分离提纯,故C正确;
D. 装置④用于吸收多余的氯气,同时防止空气中的水进入装置③,故D正确;
故选B。
10.D
【解析】A.铁丝在氯气中点燃,剧烈燃烧,产生棕褐色烟,产物为FeCl3,溶于水,溶液呈棕黄色,故A正确;
B.钠在空气中加热,先熔化成银白色小球,然后燃烧,发出黄色火焰,生成过氧化钠,为淡黄色固体,故B正确;
C.钠放入氯化铁溶液后,钠与水反应生成氢氧化钠和氢气,则现象为钠浮在水面,迅速游动,嘶嘶作响;生成的氢氧化钠与氯化铁反应生成氢氧化铁,氢氧化铁为红褐色,难溶于水,则现象为溶液中出现红褐色沉淀,故C正确;
D.过氧化钠与水反应生成氢氧化钠和氧气,中间产物具有漂白性,则滴加酚酞,溶液先变红后褪色,故D错误;
答案选D。
11.(1)
(2)过滤
(3)
(4)
【解析】(1)
煅烧海水中的贝壳生成CaO,CaO溶于水生成Ca(OH)2,向海水中加入Ca(OH)2悬浊液可将Mg2+转化为Mg(OH)2沉淀,所以试剂①可以选用低成本的Ca(OH)2;
(2)
Mg(OH)2为难溶于水的固体沉淀,可用过滤方式进行分离;
(3)
Mg(OH)2+2HCl=MgCl2+2H2O,试剂②可以选用HCl;
(4)
MgCl2的电子式为,电解熔融氯化镁的反应方程式为。
12.(1)
(2)氢气在氯气中安静燃烧,发出苍白色火焰,瓶口处有白雾出现
(3) 2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O 漂白粉 既做氧化剂,又做还原剂
【解析】(1)氯化钠溶液通电后,电解生成氯气、氢气、氢氧化钠,发生反应的离子方程式为;
(2)氢气在氯气中安静燃烧,火焰呈苍白色,在集气瓶口出现白雾;
(3)与反应生成氯化钙、次氯酸钙、水,化学方程式为;该反应常用于制备漂白粉,反应中氯元素化合价从0价部分升高到+1价,部分降低到-1价,的作用是既作氧化剂又作还原剂。
13.(1)Ca(ClO)2
(2)2Na+2H2O=2Na++2OH-+H2↑
(3)6.02×1022
(4)11.7
(5)①⑤⑦
【解析】(1)漂白粉的主要成分为CaCl2和Ca(ClO)2,其有效成分为Ca(ClO)2;
(2)钠与水反应生成NaOH和氢气,离子方程式为2Na+2H2O=2Na++2OH-+H2↑;
(3)2.8g氮气的物质的量为=0.1mol,所含分子数为0.1NA,即6.02×1022个;
(4)设溶液体积为1L,则其质量为1L×10-3×1.17g/mol=1170g,则溶质HCl的质量为1170g×36.5%,所以物质的量浓度为=11.7mol/L;
(5)NaHSO4在水溶液中、熔融状态均可以导电,是电解质,由金属阳离子和酸根阴离子构成,属于盐,固体NaHSO4没有自由移动的离子,不能导电,故选①⑤⑦。
14. ①④⑦ ②⑥⑧⑨⑩ ③⑤ NaHSO4=Na++H++SO Ba2++SO+2OH-+2H+=BaSO4↓+2H2O HCO+H+=H2O+CO2↑
【解析】(1)①石墨中有自由移动的电子,可以导电,但它是单质,不属于电解质,也不属于非电解质;
②氧化钠是离子化合物,但室温下呈固体态,离子不能自由移动,所以不能导电,在熔融状态下可以导电,属于电解质;
③酒精是由分子构成的化合物,没有带电微粒,不能导电,属于非电解质;
④氨水中含有自由移动的离子,可以导电,但它是混合物,不是电解质,也不是非电解质;
⑤二氧化碳是由分子构成的化合物,没有带电微粒,不能导电,属于非电解质;
⑥碳酸氢钠是离子化合物,但室温下呈固体态,离子不能自由移动,所以不能导电,在熔融状态下可以导电,属于电解质;
⑦氢氧化钡溶液中含有自由移动的离子,可以导电,但它是混合物,不属于电解质,也不属于非电解质;
⑧硫酸氢钠是离子化合物,室温下呈固体态,离子不能自由移动,不能导电,在水中在水分子作用下产生自由移动的离子,所以属于电解质;
⑨氯化氢是由分子构成的化合物,没有带电微粒,不能导电,在水中在水分子作用下产生自由移动的离子,所以属于电解质;
⑩硫酸铝是盐,是离子化合物,但室温下呈固体态,离子不能自由移动,所以不能导电,在熔融状态下可以导电,属于电解质;
稀硫酸中含有自由移动的离子,能够导电,但它是混合物,不属于电解质,也不属于非电解质;
氯化银是盐,是离子化合物,但室温下呈固体态,离子不能自由移动,所以不能导电,在熔融状态下可以导电,属于电解质;
故能导电的是①④⑦ ;属于电解质的是②⑥⑧⑨⑩ ;属于非电解质的是③⑤;
(2)物质⑧为硫酸氢钠,硫酸氢钠溶于水,电离产生Na+、H+、SO,电离方程式为:NaHSO4=Na+ +H++ SO;
(3)⑦氢氧化钡溶液与 稀硫酸,氢氧化钡与硫酸反应产生硫酸钡沉淀和水,反应的离子方程式为:Ba2++SO+2OH-+2H+=BaSO4↓+2H2O;
(4)⑥碳酸氢钠、⑨氯化氢,碳酸氢钠与HCl在水中发生反应,产生氯化钠、水、二氧化碳,反应的离子方程式为:HCO+H+=H2O+CO2↑。
15.(1)2Na+2 H2O=2 Na++2 OH-+H 2↑
(2)3Fe+4H2O(g)Fe3O4+4H2
(3)CaCO3+2CH3COOH=2Ca2++2CH3COO-+H2O+CO2 ↑
(4)2Al+2 OH-+2 H2O=2+3H 2↑
(5)取少量产物加水溶解,静置,取上层清液于试管,加HNO3酸化的AgNO3,如产生白色沉淀,则存在Cl-
【解析】(1)
金属钠能与水反应产生易燃的氢气2Na+2 H2O=2 Na++2 OH-+H 2↑;
(2)
铁和水蒸气高温生成四氧化铁和氢气3Fe+4H2O(g)Fe3O4+4H2;
(3)
醋酸的酸性强于碳酸,故能反应CaCO3+2CH3COOH=2Ca2++2CH3COO-+H2O+CO2 ↑;
(4)
铝与氢氧化钠溶液反应产生偏铝酸钠和氢气,反应为2Al+2 OH-+2 H2O=2+3H 2↑;
(5)
检验氯离子的方法为:取少量产物加水溶解,静置,取上层清液于试管,加HNO3酸化的AgNO3,如产生白色沉淀,则存在Cl-。
16. 过量 不足 1mol/L 1:1 0.009 0.039
【解析】从表中数据可知,在甲实验的基础上,再加入镁铝合金,生成氢气的体积继续增大,则甲中合金完全反应,盐酸有剩余;乙中合金的质量约为甲中合金质量的倍数为≈1.5,乙中生成氢气的体积为甲中氢气体积的倍数为=1.2,则表明乙中合金过量。
【解析】(1)由分析知,甲组实验中,盐酸过量;乙组实验中,合金过量,则盐酸不足。答案为:过量;不足;
(2)乙中,合金过量,则盐酸与金属完全反应生成H2,该盐酸的物质的量浓度为 =1mol/L。答案为:1mol/L;
(3)甲中,合金完全反应,设Mg、Al的物质的量分别为x、y
则24x+27y=0.255
x+1.5y==0.0125
从而求出x=y=0.005mol,合金中Mg、Al的物质的量之比为1:1。答案为:1:1;
(4)丙组合金的质量是甲组合金质量的倍数为=1.8,则所含Mg、Al的物质的量都为1.8mol×0.005mol=0.009mol,溶液中的物质的量为0.009mol;依据电荷守恒,n(Na+)= n(Cl-)+ n[]=1mol/L×0.03L+0.009mol=0.039mol。答案为:0.009;0.039。
【点睛】当溶液中发生多个反应时,可采用终态法建立电荷守恒等求解。
17.52.5%
【解析】充分加热固体混合物,发生的化学反应为,随着CO2和H2O的挥发,固体质量就会减少,则Δm=m(CO2+H2O),以此作答。
【解析】根据题意,Δm=m(CO2+H2O)=4.80g-3.87g=0.93g,列出关系式:,则混合物中碳酸氢钠的质量分数=,故答案为:52.5%。
18.(1)1
(2)1:3
【解析】(1)
在加入HCl的体积在0~25 mL时发生反应:Na2CO3+HCl=NaCl+NaHCO3,在加入盐酸溶液的体积在25~75 mL时发生反应:NaHCO3+HCl=NaCl+H2O+CO2↑。根据C元素守恒可知原混合溶液中n(Na2CO3)+n(NaHCO3)=0.05 mol。由方程式NaHCO3+HCl=NaCl+H2O+CO2↑中物质反应转化关系可知n(HCl)=n(NaHCO3)=0.05 mol,发生该反应的HCl体积是V(HCl)=75 mL-25 mL=50 mL,则该盐酸溶液的物质的量浓度c(HCl)=;
(2)
加入HCl的体积在0~25 mL时发生反应:Na2CO3+HCl=NaCl+NaHCO3,可知原溶液中n(Na2CO3)=n(HCl)=1 mol/L×0.025 L=0.025 mol,则原固体中NaHCO3的物质的量为n(NaHCO3)=0.05 mol-0.025 mol=0.025 mol。当滴入的盐酸体积为12.5 mL时,反应消耗Na2CO3的物质的量n(Na2CO3)=n(HCl)=1 mol/L×0.0125 L=0.0125 mol,因此此时溶液中剩余Na2CO3的物质的量为0.025 mol-0.0125 mol=0.0125 mol,其中含有的NaHCO3的物质的量为0.025 mol+0.0125 mol=0.0375 mol,所以此时n(Na2CO3):n(NaHCO3)=0.0125 mol:0.0375 mol=1:3,因此此时溶液中n():n()=1:3。
19. CaCO3+2H+=Ca2++H2O+CO2↑ D A 有水存在时过氧化钠跟二氧化碳发生了化学反应 2Na2O2+2H2O=4NaOH+O2↑ 加入稀盐酸,将产生的气体通入澄清的石灰水中
【解析】①中盐酸和碳酸钙反应生成二氧化碳,②用于除去CO2中的杂质HCl,应为饱和碳酸氢钠溶液,③应为浓硫酸,干燥气体;④⑤为对比试验,用于判断干燥的二氧化碳是否与过氧化钠反应,⑥可避免空气中的水、二氧化碳进入④⑤,影响实验结果的判断,最后用带火星的木条检验是否生成氧气。
【解析】(1)装置①中盐酸和碳酸钙反应生成二氧化碳,反应的化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑,碳酸钙难溶于水,应该写化学式,反应的离子方程式是CaCO3+2H+=Ca2++H2O+CO2↑;
(2)②装置:除去CO2中的杂质HCl,盐酸易挥发,装置②中试剂应为饱和NaHCO3溶液,NaHCO3与盐酸反应生成氯化钠、水和二氧化碳,离子方程式:+H+=H2O+CO2↑,故答案为D;装置③是浓硫酸,作用是干燥CO2气体,故答案为A;
(3)过氧化钠与二氧化碳反应生成碳酸钠和氧气,步骤1:打开弹簧夹K2,关闭K1,打开分液漏斗活塞加入盐酸,④中没有水蒸气,a处带火星木条不复燃,则二氧化碳不能和过氧化钠反应,所以不能生成氧气,步骤2:打开弹簧夹K1,关闭K2,打开分液漏斗活塞加入盐酸,⑤有水蒸气,a处带火星木条复燃,则二氧化碳能和过氧化钠反应生成氧气,所以得到的结论是:有水存在时过氧化钠能够跟二氧化碳发生了化学反应;
(4)气体中有水,水也可与Na2O2反应产生O2使木条复燃;过氧化钠与水反应生成氢氧化钠和氧气,该反应的方程式为:2Na2O2+2H2O=4NaOH+O2↑;
(5)二氧化碳与过氧化钠产生碳酸钠,水与过氧化钠反应产生氢氧化钠,所以若证明产物中含有碳酸钠,就证明了二氧化碳和过氧化钠发生了反应,所以加入稀盐酸,将产生的气体通入澄清的石灰水中,如果澄清石灰水变浑浊,即生成了碳酸钙沉淀,则证明二氧化碳和过氧化钠反应生成了碳酸钠溶液。
【点睛】本题考查过氧化钠的性质及实验探究,掌握物质的性质及混合物分离提纯方法是解题关键,注意把握物质的性质、实验的原理和操作方法,侧重考查学生的分析能力和实验能力。
20.(1)氧化性
(2)KMnO4=K++MnO;强电解质
(3)除去氯气中的氯化氢
(4)Cl2+2OH-=Cl-+ClO-+H2O
(5)B
【解析】装置A用KMnO4和浓盐酸反应制备Cl2,浓盐酸易挥发,制备的氯气中含有氯化氢,氯化氢易溶于水,氯气在饱和食盐水中溶解度不大,据此装置B的饱和食盐水除杂,装置C为氯气和NaOH溶液反应制取NaClO,氯气有毒,过量的氯气直接排放到空气中能引起空气污染,应用装置D进行尾气处理,氯气能够与氢氧化钠反应,被氢氧化钠吸收;
(1)
高锰酸钾与双氧水都具有强的氧化性,能够使蛋白质变性,可用作杀菌消毒,利用其氧化性;
(2)
高锰酸钾属于钾盐,溶于水完全电离,电离方程式为KMnO4=K++MnO,它属于强电解质;
(3)
浓盐酸易挥发,制备的氯气中含有氯化氢,氯化氢易溶于水,氯气在饱和食盐水中溶解度不大,所以可以用装有饱和食盐水的洗气瓶除去氯气中的氯化氢;
(4)
氯气有毒,过量的氯气直接排放到空气中能引起空气污染,应进行尾气处理,氯气能够与氢氧化钠反应,被氢氧化钠吸收,离子反应方程式Cl2+2OH-=Cl-+ClO-+H2O;
(5)
除去Cl2中混有的水蒸气和氯化氢气体,氯化氢易溶于水,氯气在饱和食盐水中溶解度不大,所以可以用装有饱和食盐水的洗气瓶除去氯气中的氯化氢,用浓硫酸吸收水蒸气,选用的药品及顺序正确的是B。
一、单选题
1.如图所示,在A处通入已经干燥的氯气,当关闭B处的弹簧夹时,C处的红布条逐渐褪色:当打开B处的弹簧夹后,C处的红布条看不到明显现象。则D瓶中盛放的溶液可能是
①饱和NaCl溶液 ②NaOH溶液 ③H2O ④浓硫酸
A.①② B.①③ C.②④ D.③④
2.下列不属于纯碱在工业生的用途的是
A.纺织 B.制药 C.制皂 D.工业制备氯气
3.下列离子方程式书写正确的是
A.Cl2与水反应:Cl2+H2O=2H++Cl-+ClO-
B.硫酸与氢氧化钡溶液反应:H++OH-+Ba2++SO=H2O+BaSO4↓
C.过氧化钠与水反应:O+2H2O=2OH-+O2↑
D.NaHCO3溶液中加入过量澄清石灰水:Ca2++HCO+OH-=CaCO3↓+H2O
4.下列化合物中一般不能通过单质与氯气直接化合制得的是
A.FeCl2 B.FeCl3 C.CuCl2 D.NaCl
5.下列说法错误的是
A.分液漏斗使用前需检查是否漏水
B.分液时,先将分液漏斗中的下层液体从下口放出,再将上层液体从上口倒出
C.为保证分液漏斗内的液体顺利流下,需将玻璃塞上的凹槽对准漏斗口上的小孔或将玻璃塞拿下
D.用铂丝做焰色反应实验时,若焰色呈黄色,说明待测物质中一定含有钠元素,不含钾元素
6.下列叙述中,不符合化学事实的是
A.1965年我国科学家首次成功合成了结晶牛胰岛素
B.《梦溪笔谈》中记载“熬胆矾铁釜,久之亦化为铜”,是发生了置换反应
C.侯氏制碱法所制得“碱”的主要成分是氢氧化钠
D.五彩缤纷的烟花利用了焰色试验的原理
7.为了除去NaHCO3溶液中含有的Na2CO3,下列方案可行的是
A.滴加适量盐酸 B.滴加BaCl2溶液,后过滤
C.通入足量的CO2气体 D.加热溶液
8.工业上制取的化学反应为,下列说法正确的是
A.在反应中被氧化
B.在反应中失去电子
C.在反应中作氧化剂
D.生成1个分子时,转移的电子数为2
9.ICl是种红棕色液体,遇水反应生成HIO和HCl,可用于有机合成等。实验室制备出Cl2与二次升华碘反应可制取ICl(I2 +Cl2=2ICl,Cl2过量时发生反应ICl +Cl2ICl3) ,实验装置如图所示;(部分夹持装置已略)。下列说法错误的是
A.装置①烧瓶中盛放的药品可以是KMnO4
B.装置②试管中盛放的是饱和食盐水
C.当装置③烧瓶中固体全部变为液体时,可用蒸馏的方法提纯产品
D.装置④吸收尾气中的氯气等气体并防止水蒸气进入装置③
10.下列实验现象描述不正确的是
A.铁丝在氯气中点燃,剧烈燃烧,产生棕褐色烟,燃烧后产物溶于水,溶液呈棕黄色
B.钠在空气中加热,先熔化成银白色小球,然后燃烧,发出黄色火焰,生成淡黄色固体
C.钠放入氯化铁溶液后,浮在水面,迅速游动,嘶嘶作响,溶液中出现红褐色沉淀
D.将1~2mL水滴入盛有1~2g过氧化钠固体的试管中,滴加酚酞,溶液变红
二、填空题
11.镁及其合金是一种用途很广的金属材料,目前世界上的镁是从海水中提取的。主要步骤如下:
(1)为了使转化为,试剂①可以选用_______(填化学式)。
(2)加入试剂①后,能够分离得到沉淀的方法是_______。
(3)试剂②可以选用_______(填化学式)。
(4)的电子式为_______,无水在熔融状态下,通电后会产生和,该反应的化学方程式为_______。
12.NaCl是一种化工原料,可以制备多种物质,如下图所示。
请根据以上转化关系填写下列空白。
(1)氯化钠溶液通电后,发生反应的离子方程式为_______;
(2)氢气在氯气中燃烧的现象是_______。
(3)与反应的化学方程式为_______;该反应常用于制备_______,从氧化剂和还原剂的角度分析,该反应中的作用是_______。
13.按下列要求填空:
(1)写出漂白粉的有效成分的化学式:_______。
(2)钠与水反应的离子方程式_______。
(3)2.8g氮气含有的分子数约为_______个。
(4)质量分数为36.5%的HCl溶液,密度为1.17g/cm3,求其物质的量浓度为_______mol/L。
(5)固体NaHSO4的性质:_______(填写符合要求的序号)。
①电解质;②非电解质;③酸;④碱;⑤盐;⑥导电;⑦不导电
14.有以下12种物质,请回答下列问题:
①石墨②氧化钠③酒精④氨水⑤二氧化碳⑥碳酸氢钠⑦氢氧化钡溶液⑧硫酸氢钠⑨氯化氢⑩硫酸铝 稀硫酸 氯化银
(1)其中能导电的是___;属于电解质的是___;属于非电解质的是___。
(2)写出物质⑧溶于水的电离方程式:___。
(3)写出物质⑦和 反应的离子方程式:___。
(4)写出物质⑥和⑨在水中发生反应的离子方程式:___。
15.国际化学年的中国宣传口号是“化学——我们的生活,我们的未来”。学习化学应该明白“从生活中来,到生活中去”的道理。请填空:
(1)金属钠着火时,不能用水灭火,原因是_______(用离子方程式表示)。
(2)常温下铁遇水不反应,但在高温条件下二者能发生反应,书写二者反应的化学方程式___。
(3)热水瓶用久后,瓶胆内常附着一层水垢(主要成分是CaCO3),用食醋能较好的清除,其原理是_______(用离子方程式表示)。
(4)铝合金材料在生活生产中应用广泛,如铝合金门窗、飞机外壳、航空航天等,且具有密度小、易加工、不易腐蚀等优点,Al与氢氧化钠溶液反应的离子方程式为___。
(5)设计实验检验实验室用KClO3和MnO2制取氧气后的产物中是否存在Cl-____。
三、计算题
16.在标准状况下进行甲、乙、丙三组实验。三组实验各取同浓度的盐酸30mL,加入同一种镁铝合金粉末,产生气体。有关数据列表如表(气体体积均为标准状况下测得):
实验序号 甲 乙 丙
合金质量/g 0.255 0.385 0.459
生成气体/ml 280 336 336
(1)甲组实验中,盐酸_____;乙组实验中,盐酸_____(填“过量“、“适量“或“不足“)。
(2)该盐酸的物质的量浓度_____。
(3)合金中Mg、Al的物质的量之比为____。
(4)在丙组实验后,向容器中加入1mol/L的NaOH溶液,恰好使合金中的铝元素全部转化为,并使Mg2+刚好沉淀完全,则溶液中的物质的量为_____mol;溶液中Na+的物质的量为______mol。
17.碳酸钠和碳酸氢钠是用途广泛的化合物。在实验室中,充分加热碳酸钠和碳酸氢钠的混合物,完全反应后称得剩余固体质量为,求混合物中碳酸氢钠的质量分数_______。
18.在Na2CO3和NaHCO3混合溶液中缓慢滴加一定浓度的盐酸,测得溶液中物质的量与所加盐酸体积之间的关系如图所示。
请回答下列问题:
(1)盐酸物质的量浓度为___________mol/L。
(2)当滴入的盐酸体积为12.5 mL时,溶液中n():n()为___________。
四、实验题
19.为了探究“二氧化碳是否在水存在时才能和过氧化钠反应”,某课外活动小组设计了下列装置进行探究。广口瓶②、③中分别装有试剂X和试剂Y,④、⑤中均是干燥的过氧化钠。
【实验与现象】
步骤1:打开弹簧夹K2,关闭K1,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处,木条不复燃。
步骤2:打开弹簧夹K1,关闭K2,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处,木条复燃。
【思考与分析】
(1)装置①中反应的离子方程式是_________。
(2)装置②中的试剂X是__________;装置③中的试剂Y是____________(填序号)。
A.浓H2SO4 B.饱和食盐水
C.饱和Na2CO3溶液 D.饱和NaHCO3溶液
【结论与反思】
(3)根据步骤1和步骤2的实验现象,得到的结论是_________。
(4)实验后有同学提出质疑: “步骤2的实验并不能证明过氧化钠跟二氧化碳发生了化学反应。”小组其他同学也认为很有道理,请写出其理由的方程式_______________。
(5)若要证明“过氧化钠跟二氧化碳发生了化学反应”,需要补充的实验操作是:取⑤中反应后的少量固体,___________________。
20.KMnO4是一种氧化剂,实验室常用KMnO4和浓盐酸反应制备Cl2。下图是制备 NaClO溶液的装置图。
完成下列填空:
(1)医疗上可用稀高锰酸钾溶液来给伤口消毒,你认为这是利用了KMnO4的_______(选填“氧化性”、“还原性”)
(2)高锰酸钾溶于水的电离方程式为_______它属于(选填“强电解质”、“弱电解质”、“非电解质”);
(3)B装置中饱和食盐水的作用是_______;
(4)D装置中NaOH的作用是_______(用离子反应方程式表示);
(5)除去Cl2中混有的氯化氢和水蒸气气体,选用的药品及顺序正确的是_______(填序号);
A.水、碱石灰 B.饱和食盐水、浓硫酸
C.无水氯化钙、饱和食盐水 D.烧碱溶液、浓硫酸
参考答案:
1.B
【解析】干燥的Cl2没有漂白性,湿润的Cl2具有漂白性;当关闭B处的弹簧夹时,C处的红布条逐渐褪色,说明干燥的Cl2变为湿润的Cl2;当关闭B处的弹簧夹后,C处的红布条看不到明显现象,说明干燥的Cl2无变化。
【解析】①关闭B处的弹簧夹时,干燥的Cl2通入到饱和NaCl溶液中,干燥的Cl2变为湿润的Cl2,C处的红布条逐渐褪色;
②关闭B处的弹簧夹时,干燥的Cl2通入到NaOH溶液中,干燥的Cl2被吸收,C处的红布条看不到明显现象;
③关闭B处的弹簧夹时,干燥的Cl2通入到H2O中,干燥的Cl2变为湿润的Cl2,C处的红布条逐渐褪色;
④关闭B处的弹簧夹时,干燥的Cl2通入到浓硫酸中,干燥的Cl2无变化,C处的红布条看不到明显现象;
综上所述,D瓶中盛放的溶液可能是①③,故选B。
2.D
【解析】纯碱是碳酸钠,是重要的化工原料之一,广泛应用于轻工日化、建材、化学工业、食品工业、冶金、纺织、石油、国防、医药等领域, 用作制造其他化学品的原料、清洗剂、洗涤剂,也用于照相术和分析领域;不用于工业制备氯气,故选D
3.D
【解析】A.HClO为弱酸,书写离子方程式时不能拆开,故为Cl2+H2O=H++Cl-+HClO,故A错误;
B.硫酸与氢氧化钡溶液反应的离子方程式为:2H++2OH-+Ba2++SO=2H2O+BaSO4↓,故B错误;
C.过氧化钠书写离子方程式时不能拆开,故C错误;
D.NaHCO3溶液中加入过量澄清石灰水生成碳酸钙沉淀和氢氧化钠、水,故离子方程式为Ca2++HCO+OH-=CaCO3↓+H2O,故D正确;
故选D。
4.A
【解析】A.氯气和铁化合反应得到氯化铁得不到氯化亚铁,A符合题意;
B.氯气和铁化合反应得到氯化铁,B不符合题意;
C.氯气和铜化合反应得到氯化铜,C不符合题意;
D.氯气和钠化合反应得到氯化钠,D不符合题意;
故选A。
5.D
【解析】由于Na的焰色反应呈黄色,而钾的焰色反应呈紫色,黄色很容易掩盖紫色,故进行钾的焰色反应时需透过蓝色钴玻璃进行观察以滤去黄色的光,即用铂丝做焰色反应实验时,若焰色呈黄色,说明待测物质中一定含有钠元素,但不能确定是否含钾元素,需透过蓝色钴玻璃进行观察,是否观察到紫色才可确定是否含钾,故答案为:D。
6.C
【解析】A.1965年,我国科学家在世界上首次成功合成了具有生命活力的蛋白质——结晶牛胰岛素,A不符合题意;
B.“熬胆矾铁釜,久之亦化为铜”,发生反应Fe+CuSO4=FeSO4+Cu,属于置换反应,B不符合题意;
C.侯氏制碱法利用NaCl、NH3、CO2、H2O为原料,制得了NH4Cl和NaHCO3,然后加热分解NaHCO3生成纯碱Na2CO3,所制得“碱”的主要成分是碳酸钠,C符合题意;
D.五彩缤纷的烟花是利用金属离子发生焰色试验的原理,从而产生不同的焰色,D不符合题意;
故选C。
7.C
【解析】A.盐酸与NaHCO3也能发生反应,不能选用,故A错误;
B.为确保碳酸钠除尽,所加氯化钡溶液应过量,在碳酸氢钠溶液中会引入氯化钠和氯化钡等新杂质,故B错误;
C.通入足量的二氧化碳,能与碳酸钠反应生成碳酸氢钠,且不引入新杂质,故C正确;
D.加热溶液导致碳酸氢钠分解成碳酸钠,故D错误;
故选:C。
8.A
【解析】在反应中元素化合价变化情况:。
A.在该反应中, S元素化合价由SO2中的+4价变为反应后NaHSO4中的+6价,化合价升高,失去电子,被氧化,A正确;
B.在反应中Cl元素化合价由反应前中的+5价变为反应后ClO2中的+2价,化合价降低,得到电子,被还原,所以作氧化剂,B错误;
C.中元素化合价在反应前后未发生变化,所以既不作氧化剂也不作还原剂,C错误;
D.反应中元素由+5价降低到+4价,降低1价,所以每生成1个分子时,转移的电子数为1,D错误;
故合理选项是A。
9.B
【解析】根据题意,整个过程中,装置③中应该在无水环境中进行,且氯气不能过量。
【解析】A. 装置①中无加热装置,而该装置为实验室制取氯气的装置,所以烧瓶中的固体可以为高锰酸钾,故A正确;
B. 进入装置③中的气体应该为干燥的氯气,所以②试管中盛放的是浓硫酸,故B错误;
C. 根据碘蒸气与氯化碘的沸点不同,可以通过蒸馏的方法分离提纯,故C正确;
D. 装置④用于吸收多余的氯气,同时防止空气中的水进入装置③,故D正确;
故选B。
10.D
【解析】A.铁丝在氯气中点燃,剧烈燃烧,产生棕褐色烟,产物为FeCl3,溶于水,溶液呈棕黄色,故A正确;
B.钠在空气中加热,先熔化成银白色小球,然后燃烧,发出黄色火焰,生成过氧化钠,为淡黄色固体,故B正确;
C.钠放入氯化铁溶液后,钠与水反应生成氢氧化钠和氢气,则现象为钠浮在水面,迅速游动,嘶嘶作响;生成的氢氧化钠与氯化铁反应生成氢氧化铁,氢氧化铁为红褐色,难溶于水,则现象为溶液中出现红褐色沉淀,故C正确;
D.过氧化钠与水反应生成氢氧化钠和氧气,中间产物具有漂白性,则滴加酚酞,溶液先变红后褪色,故D错误;
答案选D。
11.(1)
(2)过滤
(3)
(4)
【解析】(1)
煅烧海水中的贝壳生成CaO,CaO溶于水生成Ca(OH)2,向海水中加入Ca(OH)2悬浊液可将Mg2+转化为Mg(OH)2沉淀,所以试剂①可以选用低成本的Ca(OH)2;
(2)
Mg(OH)2为难溶于水的固体沉淀,可用过滤方式进行分离;
(3)
Mg(OH)2+2HCl=MgCl2+2H2O,试剂②可以选用HCl;
(4)
MgCl2的电子式为,电解熔融氯化镁的反应方程式为。
12.(1)
(2)氢气在氯气中安静燃烧,发出苍白色火焰,瓶口处有白雾出现
(3) 2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O 漂白粉 既做氧化剂,又做还原剂
【解析】(1)氯化钠溶液通电后,电解生成氯气、氢气、氢氧化钠,发生反应的离子方程式为;
(2)氢气在氯气中安静燃烧,火焰呈苍白色,在集气瓶口出现白雾;
(3)与反应生成氯化钙、次氯酸钙、水,化学方程式为;该反应常用于制备漂白粉,反应中氯元素化合价从0价部分升高到+1价,部分降低到-1价,的作用是既作氧化剂又作还原剂。
13.(1)Ca(ClO)2
(2)2Na+2H2O=2Na++2OH-+H2↑
(3)6.02×1022
(4)11.7
(5)①⑤⑦
【解析】(1)漂白粉的主要成分为CaCl2和Ca(ClO)2,其有效成分为Ca(ClO)2;
(2)钠与水反应生成NaOH和氢气,离子方程式为2Na+2H2O=2Na++2OH-+H2↑;
(3)2.8g氮气的物质的量为=0.1mol,所含分子数为0.1NA,即6.02×1022个;
(4)设溶液体积为1L,则其质量为1L×10-3×1.17g/mol=1170g,则溶质HCl的质量为1170g×36.5%,所以物质的量浓度为=11.7mol/L;
(5)NaHSO4在水溶液中、熔融状态均可以导电,是电解质,由金属阳离子和酸根阴离子构成,属于盐,固体NaHSO4没有自由移动的离子,不能导电,故选①⑤⑦。
14. ①④⑦ ②⑥⑧⑨⑩ ③⑤ NaHSO4=Na++H++SO Ba2++SO+2OH-+2H+=BaSO4↓+2H2O HCO+H+=H2O+CO2↑
【解析】(1)①石墨中有自由移动的电子,可以导电,但它是单质,不属于电解质,也不属于非电解质;
②氧化钠是离子化合物,但室温下呈固体态,离子不能自由移动,所以不能导电,在熔融状态下可以导电,属于电解质;
③酒精是由分子构成的化合物,没有带电微粒,不能导电,属于非电解质;
④氨水中含有自由移动的离子,可以导电,但它是混合物,不是电解质,也不是非电解质;
⑤二氧化碳是由分子构成的化合物,没有带电微粒,不能导电,属于非电解质;
⑥碳酸氢钠是离子化合物,但室温下呈固体态,离子不能自由移动,所以不能导电,在熔融状态下可以导电,属于电解质;
⑦氢氧化钡溶液中含有自由移动的离子,可以导电,但它是混合物,不属于电解质,也不属于非电解质;
⑧硫酸氢钠是离子化合物,室温下呈固体态,离子不能自由移动,不能导电,在水中在水分子作用下产生自由移动的离子,所以属于电解质;
⑨氯化氢是由分子构成的化合物,没有带电微粒,不能导电,在水中在水分子作用下产生自由移动的离子,所以属于电解质;
⑩硫酸铝是盐,是离子化合物,但室温下呈固体态,离子不能自由移动,所以不能导电,在熔融状态下可以导电,属于电解质;
稀硫酸中含有自由移动的离子,能够导电,但它是混合物,不属于电解质,也不属于非电解质;
氯化银是盐,是离子化合物,但室温下呈固体态,离子不能自由移动,所以不能导电,在熔融状态下可以导电,属于电解质;
故能导电的是①④⑦ ;属于电解质的是②⑥⑧⑨⑩ ;属于非电解质的是③⑤;
(2)物质⑧为硫酸氢钠,硫酸氢钠溶于水,电离产生Na+、H+、SO,电离方程式为:NaHSO4=Na+ +H++ SO;
(3)⑦氢氧化钡溶液与 稀硫酸,氢氧化钡与硫酸反应产生硫酸钡沉淀和水,反应的离子方程式为:Ba2++SO+2OH-+2H+=BaSO4↓+2H2O;
(4)⑥碳酸氢钠、⑨氯化氢,碳酸氢钠与HCl在水中发生反应,产生氯化钠、水、二氧化碳,反应的离子方程式为:HCO+H+=H2O+CO2↑。
15.(1)2Na+2 H2O=2 Na++2 OH-+H 2↑
(2)3Fe+4H2O(g)Fe3O4+4H2
(3)CaCO3+2CH3COOH=2Ca2++2CH3COO-+H2O+CO2 ↑
(4)2Al+2 OH-+2 H2O=2+3H 2↑
(5)取少量产物加水溶解,静置,取上层清液于试管,加HNO3酸化的AgNO3,如产生白色沉淀,则存在Cl-
【解析】(1)
金属钠能与水反应产生易燃的氢气2Na+2 H2O=2 Na++2 OH-+H 2↑;
(2)
铁和水蒸气高温生成四氧化铁和氢气3Fe+4H2O(g)Fe3O4+4H2;
(3)
醋酸的酸性强于碳酸,故能反应CaCO3+2CH3COOH=2Ca2++2CH3COO-+H2O+CO2 ↑;
(4)
铝与氢氧化钠溶液反应产生偏铝酸钠和氢气,反应为2Al+2 OH-+2 H2O=2+3H 2↑;
(5)
检验氯离子的方法为:取少量产物加水溶解,静置,取上层清液于试管,加HNO3酸化的AgNO3,如产生白色沉淀,则存在Cl-。
16. 过量 不足 1mol/L 1:1 0.009 0.039
【解析】从表中数据可知,在甲实验的基础上,再加入镁铝合金,生成氢气的体积继续增大,则甲中合金完全反应,盐酸有剩余;乙中合金的质量约为甲中合金质量的倍数为≈1.5,乙中生成氢气的体积为甲中氢气体积的倍数为=1.2,则表明乙中合金过量。
【解析】(1)由分析知,甲组实验中,盐酸过量;乙组实验中,合金过量,则盐酸不足。答案为:过量;不足;
(2)乙中,合金过量,则盐酸与金属完全反应生成H2,该盐酸的物质的量浓度为 =1mol/L。答案为:1mol/L;
(3)甲中,合金完全反应,设Mg、Al的物质的量分别为x、y
则24x+27y=0.255
x+1.5y==0.0125
从而求出x=y=0.005mol,合金中Mg、Al的物质的量之比为1:1。答案为:1:1;
(4)丙组合金的质量是甲组合金质量的倍数为=1.8,则所含Mg、Al的物质的量都为1.8mol×0.005mol=0.009mol,溶液中的物质的量为0.009mol;依据电荷守恒,n(Na+)= n(Cl-)+ n[]=1mol/L×0.03L+0.009mol=0.039mol。答案为:0.009;0.039。
【点睛】当溶液中发生多个反应时,可采用终态法建立电荷守恒等求解。
17.52.5%
【解析】充分加热固体混合物,发生的化学反应为,随着CO2和H2O的挥发,固体质量就会减少,则Δm=m(CO2+H2O),以此作答。
【解析】根据题意,Δm=m(CO2+H2O)=4.80g-3.87g=0.93g,列出关系式:,则混合物中碳酸氢钠的质量分数=,故答案为:52.5%。
18.(1)1
(2)1:3
【解析】(1)
在加入HCl的体积在0~25 mL时发生反应:Na2CO3+HCl=NaCl+NaHCO3,在加入盐酸溶液的体积在25~75 mL时发生反应:NaHCO3+HCl=NaCl+H2O+CO2↑。根据C元素守恒可知原混合溶液中n(Na2CO3)+n(NaHCO3)=0.05 mol。由方程式NaHCO3+HCl=NaCl+H2O+CO2↑中物质反应转化关系可知n(HCl)=n(NaHCO3)=0.05 mol,发生该反应的HCl体积是V(HCl)=75 mL-25 mL=50 mL,则该盐酸溶液的物质的量浓度c(HCl)=;
(2)
加入HCl的体积在0~25 mL时发生反应:Na2CO3+HCl=NaCl+NaHCO3,可知原溶液中n(Na2CO3)=n(HCl)=1 mol/L×0.025 L=0.025 mol,则原固体中NaHCO3的物质的量为n(NaHCO3)=0.05 mol-0.025 mol=0.025 mol。当滴入的盐酸体积为12.5 mL时,反应消耗Na2CO3的物质的量n(Na2CO3)=n(HCl)=1 mol/L×0.0125 L=0.0125 mol,因此此时溶液中剩余Na2CO3的物质的量为0.025 mol-0.0125 mol=0.0125 mol,其中含有的NaHCO3的物质的量为0.025 mol+0.0125 mol=0.0375 mol,所以此时n(Na2CO3):n(NaHCO3)=0.0125 mol:0.0375 mol=1:3,因此此时溶液中n():n()=1:3。
19. CaCO3+2H+=Ca2++H2O+CO2↑ D A 有水存在时过氧化钠跟二氧化碳发生了化学反应 2Na2O2+2H2O=4NaOH+O2↑ 加入稀盐酸,将产生的气体通入澄清的石灰水中
【解析】①中盐酸和碳酸钙反应生成二氧化碳,②用于除去CO2中的杂质HCl,应为饱和碳酸氢钠溶液,③应为浓硫酸,干燥气体;④⑤为对比试验,用于判断干燥的二氧化碳是否与过氧化钠反应,⑥可避免空气中的水、二氧化碳进入④⑤,影响实验结果的判断,最后用带火星的木条检验是否生成氧气。
【解析】(1)装置①中盐酸和碳酸钙反应生成二氧化碳,反应的化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑,碳酸钙难溶于水,应该写化学式,反应的离子方程式是CaCO3+2H+=Ca2++H2O+CO2↑;
(2)②装置:除去CO2中的杂质HCl,盐酸易挥发,装置②中试剂应为饱和NaHCO3溶液,NaHCO3与盐酸反应生成氯化钠、水和二氧化碳,离子方程式:+H+=H2O+CO2↑,故答案为D;装置③是浓硫酸,作用是干燥CO2气体,故答案为A;
(3)过氧化钠与二氧化碳反应生成碳酸钠和氧气,步骤1:打开弹簧夹K2,关闭K1,打开分液漏斗活塞加入盐酸,④中没有水蒸气,a处带火星木条不复燃,则二氧化碳不能和过氧化钠反应,所以不能生成氧气,步骤2:打开弹簧夹K1,关闭K2,打开分液漏斗活塞加入盐酸,⑤有水蒸气,a处带火星木条复燃,则二氧化碳能和过氧化钠反应生成氧气,所以得到的结论是:有水存在时过氧化钠能够跟二氧化碳发生了化学反应;
(4)气体中有水,水也可与Na2O2反应产生O2使木条复燃;过氧化钠与水反应生成氢氧化钠和氧气,该反应的方程式为:2Na2O2+2H2O=4NaOH+O2↑;
(5)二氧化碳与过氧化钠产生碳酸钠,水与过氧化钠反应产生氢氧化钠,所以若证明产物中含有碳酸钠,就证明了二氧化碳和过氧化钠发生了反应,所以加入稀盐酸,将产生的气体通入澄清的石灰水中,如果澄清石灰水变浑浊,即生成了碳酸钙沉淀,则证明二氧化碳和过氧化钠反应生成了碳酸钠溶液。
【点睛】本题考查过氧化钠的性质及实验探究,掌握物质的性质及混合物分离提纯方法是解题关键,注意把握物质的性质、实验的原理和操作方法,侧重考查学生的分析能力和实验能力。
20.(1)氧化性
(2)KMnO4=K++MnO;强电解质
(3)除去氯气中的氯化氢
(4)Cl2+2OH-=Cl-+ClO-+H2O
(5)B
【解析】装置A用KMnO4和浓盐酸反应制备Cl2,浓盐酸易挥发,制备的氯气中含有氯化氢,氯化氢易溶于水,氯气在饱和食盐水中溶解度不大,据此装置B的饱和食盐水除杂,装置C为氯气和NaOH溶液反应制取NaClO,氯气有毒,过量的氯气直接排放到空气中能引起空气污染,应用装置D进行尾气处理,氯气能够与氢氧化钠反应,被氢氧化钠吸收;
(1)
高锰酸钾与双氧水都具有强的氧化性,能够使蛋白质变性,可用作杀菌消毒,利用其氧化性;
(2)
高锰酸钾属于钾盐,溶于水完全电离,电离方程式为KMnO4=K++MnO,它属于强电解质;
(3)
浓盐酸易挥发,制备的氯气中含有氯化氢,氯化氢易溶于水,氯气在饱和食盐水中溶解度不大,所以可以用装有饱和食盐水的洗气瓶除去氯气中的氯化氢;
(4)
氯气有毒,过量的氯气直接排放到空气中能引起空气污染,应进行尾气处理,氯气能够与氢氧化钠反应,被氢氧化钠吸收,离子反应方程式Cl2+2OH-=Cl-+ClO-+H2O;
(5)
除去Cl2中混有的水蒸气和氯化氢气体,氯化氢易溶于水,氯气在饱和食盐水中溶解度不大,所以可以用装有饱和食盐水的洗气瓶除去氯气中的氯化氢,用浓硫酸吸收水蒸气,选用的药品及顺序正确的是B。
