专题6第二单元化学反应中的热同步练习 (含答案)2022——2023学年高一化学下学期苏教版(2019)必修第二册
文档属性
| 名称 | 专题6第二单元化学反应中的热同步练习 (含答案)2022——2023学年高一化学下学期苏教版(2019)必修第二册 |

|
|
| 格式 | docx | ||
| 文件大小 | 516.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-06-18 00:00:00 | ||
图片预览




文档简介
专题6第二单元化学反应中的热同步练习
单选题
1. 理论研究表明,在和下,异构化反应过程的能量变化如图所示,下列有关说法正确的是( )
A. 比稳定
B. 逆反应的活化能为
C. 反应物断键吸收的总能量小于生成物成键放出的总能量
D. 该反应的热化学方程式为
2. 根据能量变化示意图,下列说法正确的是( )
A. 状态是液态,则状态一定是气态
B. 状态是液态,则状态一定是气态
C. 状态状态
D. 断裂状态和中的化学键需要吸收的能量为
3. 下列说法不正确的是( )
A. ,则每生成放热
B. 天然气的主要成分甲烷是高效、较洁净的燃料
C. 天然气是不可再生能源
D. 使用催化剂,可以改变反应的反应热
4. 单斜硫和正交硫转化为二氧化硫的能量变化如图所示,下列说法正确的是( )
A. 单斜,正交,
B. 正交硫比单斜硫稳定
C. 相同物质的量的正交硫比单斜硫所含有的能量高
D. 表示断裂中的共价键所吸收的能量比形成中的共价键所放出的能量少
5. 某反应由两步反应构成,它的反应能量曲线如图,下列叙述正确的是
A. 两步反应均为吸热反应 B. 三种化合物中最稳定
C. 与的能量差为 D. 反应,反应条件一定要加热
6. 一定条件下,石墨转化为金刚石的能量变化如图所示.在该条件下,下列结论正确的是.( )
A. 石墨转化为金刚石是放热反应 B. 金刚石比石墨稳定
C. 等质量的金刚石和石墨完全燃烧释放的热量不同 D. 金刚石和石墨的燃烧产物属于空气污染物
7. 下列依据热化学方程式得出的结论正确的是 ( )
A. 已知 ;则氢气的燃烧热为
B. 已知 石墨, 金刚石,;则金刚石比石墨稳定
C. 已知 ,则含 的稀溶液与稀盐酸完全中和,放出 的热量
D. 己知 ; ,则
8. 化学能可与热能、电能等相互转化。下列说法正确的是
A. 图Ⅰ所示的装置能将化学能转化为电能
B. 中和反应中,反应物的总能量比生成物的总能量低
C. 化学反应中能量变化的主要原因是化学键的断裂与形成
D. 图Ⅱ所示的反应为吸热反应
9. 和在催化剂表面合成氨的微观历程及能量变化的示意图如下,用、、分别表示、、,已知:,该反应属于放热反应。下列说法正确的是( )
A. 催化剂仅起到吸附和的作用,对化学反应速率没有影响
B. 过程,是放热过程
C. 过程,原子和原子形成了含有非极性键的
D. 合成氨反应中,反应物断键吸收能量小于生成物形成新键释放的能量
10. 化学能与热能、电能等能相互转化,关于化学能与其他能量相互转化的说法错误的是
A. 化学反应中能量变化的主要原因是化学键的断裂与生成
B. 铝热反应中,反应物的总能量比生成物的总能量低
C. 图所示的装置不能将化学能转变为电能
D. 图所示的反应为放热反应
11. 已知反应的能量变化如图所示、均为正值,下列说法正确的是( )
A. 该反应吸收的能最为
B. 破坏反应物中的化学键所吸收的能量小于形成生成物中化学键所放出的能量
C. 和的总能量一定高于和的总能量
D. 该反应只有在加热条件下才能进行
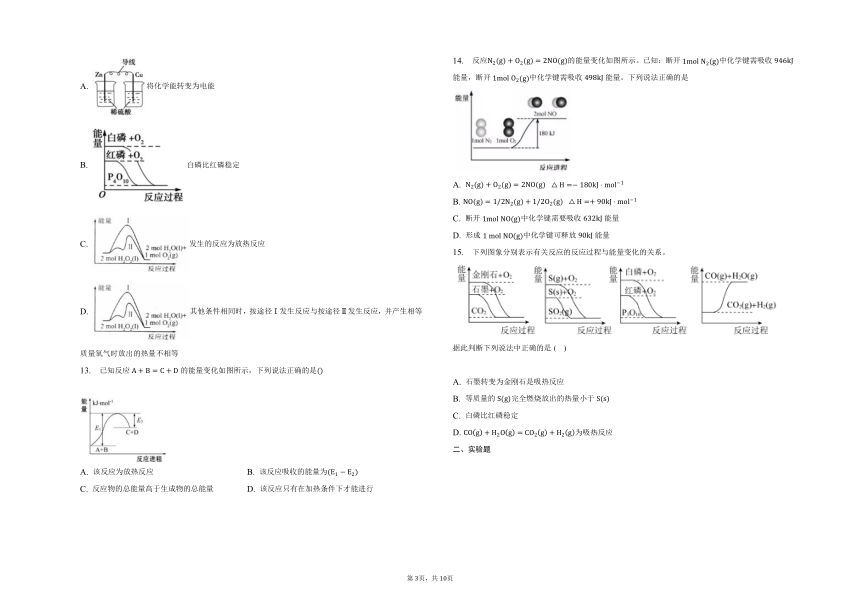
12. 化学能与热能、电能等可以相互转化.关于化学能与其他能量相互转化的说法正确的是( )
A. 将化学能转变为电能
B. 白磷比红磷稳定
C. 发生的反应为放热反应
D. 其他条件相同时,按途径Ⅰ发生反应与按途径Ⅱ发生反应,并产生相等质量氧气时放出的热量不相等
13. 已知反应的能量变化如图所示,下列说法正确的是
A. 该反应为放热反应 B. 该反应吸收的能量为
C. 反应物的总能量高于生成物的总能量 D. 该反应只有在加热条件下才能进行
14. 反应的能量变化如图所示。已知:断开中化学键需吸收能量,断开中化学键需吸收能量。下列说法正确的是
A.
B.
C. 断开中化学键需要吸收能量
D. 形成中化学键可释放能量
15. 下列图象分别表示有关反应的反应过程与能量变化的关系。
据此判断下列说法中正确的是( )
A. 石墨转变为金刚石是吸热反应
B. 等质量的完全燃烧放出的热量小于
C. 白磷比红磷稳定
D. 为吸热反应
二、实验题
16. 为了研究化学反应的能量变化情况,某同学设计了如图所示装置。当向盛有的试管中滴加试剂时,看到形管中甲处液面下降乙处液面上升。试回答下列问题:
该反应为________反应填“放热”或“吸热”。
和的总能量比和的总能量________填“高”或“低”。
物质中的化学能通过化学反应转化成____________释放出来。
反应物化学键断裂吸收的能量________填“高”或“低”于生成物化学键形成放出的能量。
写出一个符合题中条件的化学方程式:_________________________________。
17. 生产生活中的化学反应都伴随着能量的变化,请根据有关知识回答下列问题:
反应,生成物能量总和_______填“大于”、“小于”或“等于”反应物能量总和。
已知:常温常压下,甲烷气体在足量氧气中充分燃烧生成液态水和二氧化碳气体时放出热量,写出甲烷气体的燃烧热的热化学方程式:_______________。
焙烧产生的可用于制硫酸。
已知:、时, ;
;
;
则与反应生成的热化学方程式是______________。
某实验小组用的溶液和的溶液进行中和反应的反应热测定。
若需配制溶液,则需用量筒量取_______密度为,质量分数为的浓硫酸。
测定稀硫酸和氢氧化钠稀溶液反应的反应热的实验装置如图所示。则仪器的名称为_______。
取溶液和溶液进行实验,实验数据如下表。
实验次数 反应物温度 反应前体系的温度 反应后体系的温度 温度差
温度差的平均值为_______。
近似认为的溶液和的溶液的密度都是,中和后生成的溶液的比热容。则测得生成时中和反应的反应热_______取小数点后一位。
上述结果与理论值有偏差,产生此偏差的原因可能是_______填标号。
实验装置保温、隔热效果差
用量筒量取溶液的体积时仰视读数
把溶液一次性倒入盛有溶液的小烧杯中
碎泡沫塑料的作用是____________________________。
三、简答题
18. Ⅰ,金刚石 ;
,石墨
则金刚石转化为石墨的热化学方程式为______________________,由热化学方程式看来更稳定的是_____。
; ; ;则的_______________________。用、、代数式表示
下图是反应过程中的能量变化图。
由图可知,反应物的总键能________填“”、“”或者“”生成物的总键能。
已知的燃烧热为, ,则_________填“”“”或“”。
火箭和导弹表面的薄层是耐高温物质。将石墨、铝粉和二氧化钛按一定比例混合在高温下煅烧,所得物质可作耐高温材料: ,则反应过程中,每转移电子放出的热量为_________。
19. 某反应过程中的能量变化如图所示,回答问题。
该反应是_______填“吸热”或“放热”反应,反应的________用含的代数式表示。
该反应过程中,断裂旧化学键吸收的总能量_____填“”“ ”或“”形成新化学键释放的总能量。
已知:
则: ______________。
已知拆开键、键、键分别需要的能量是、、,则气体分解生成与的热化学方程式为________________________________
已知:时, ,则碳的燃烧热数值_____填,,。
答案和解析
1.【答案】
【解析】
【分析】
本题考查反应热与焓变,明确图示曲线变化的意义为解答关键,注意化学反应与能量变化的关系,试题侧重考查学生的分析能力及灵活运用基础知识的能力,题目难度不大。
【解答】
A.能量越低越稳定,的能量低于的能量,所以比稳定,故A错误;
B.根据题图可知逆反应的活化能为,故B错误;
C.该反应为吸热反应,故反应物断键吸收的总能量大于生成物成键放出的总能量,故C错误;
D.反应热为生成物总能量减去反应物总能量,热化学方程式为,故D正确。
2.【答案】
【解析】
【分析】
本题考查了化学反应与能量的变化、反应热的计算等知识,难度一般,侧重基础知识的考查。
【解答】
A.状态是液态,状态不能确定,故A错误;
B.状态是液态,状态不能确定,故B错误;
C.状态状态 ,故C正确;
D.断裂化学键的量不确定,由图不能确定化学键断裂吸收的能量,故D错误。
故选C。
3.【答案】
【解析】该热化学方程式表示气态与 气态,反应产生液态放出的热量,A正确;
天然气的主要成分甲烷燃烧产生,,放出大量的热量,因此是高效、较洁净的燃料,B正确;
天然气属于化石能源,是远古时代的动植物遗体、遗骸经过漫长的历史时期形成的,短时间内不能产生,因此属于不可再生能源,C正确;
使用催化剂,只能改变反应途径,不能改变反应物、生成物的能量,因此不能改变反应的反应热,D错误。
4.【答案】
【解析】
【分析】
本题考查了化学反应中的能量变化,正确理解图象中曲线的含义是解题的关键,注意物质的能量越高越不稳定,正确判断反应热、活化能与键能的关系。。
【解答】
A.单斜硫的能量比正交硫的能量高,,单斜,正交,为放热反应,故A错误;
B.物质的能量越高越不稳定,则正交硫比单斜硫稳定,故B正确;
C.由图象可以看出,单斜硫的能量比正交硫的能量高,故C错误;
D.式反应需断裂单斜硫中键和键,不仅仅是断裂中的共价键所吸收的能量,故D错误。
故选B。
5.【答案】
【解析】略
6.【答案】
【解析】略
7.【答案】
【解析】
【分析】
本题考查燃烧热、中和热概念,反应热与物质稳定性的关系,盖斯定律的应用,难度不大。
【解答】
A.燃烧热是指可燃物完全燃烧生成稳定化合物时放出的热量,燃烧生成液态水,故A错误;
B.已知石墨,金刚石,;,反应是吸热反应,金刚石能量高于石墨,所以金刚石比石墨的键能小,因此是石墨比金刚石稳定,故B错误;
C.已知,则含物质的量为的稀溶液与稀盐酸完全中和,放出的热量,故C正确;
D.已知;;,一氧化碳燃烧生成二氧化碳放热,焓变是负值,所以,故D错误。
故选C。
8.【答案】
【解析】A.该装置不能构成闭合回路,不能构成原电池,则不能将化学能转化为电能,故A错误;
B.中和反应为放热反应,则反应物总能量大于生成物总能量,故B错误;
C.断键吸收热量、成键放出热量,化学反应实质是旧化学键的断裂和新化学键的形成,所以化学反应中能量变化的主要原因是化学键的断裂与形成,故C正确;
D.图Ⅱ所示反应物总能量大于生成物总能量,则该反应为放热反应,否则为吸热反应,根据图知,反应物总能量大于生成物总能量,则为放热反应,故D错误;
故答案为。
9.【答案】
【解析】略
10.【答案】
【解析】A.化学反应时断键要吸收能量,成键要放出能量,所以化学反应中能量变化的主要原因是化学键的断裂与生成,A正确;
B.铝热反应是放热反应,反应物的总能量应大于生成物的总能量,B错误;
C.图没有形成闭合回路,不能形成原电池,不能将化学能转化为电能,C正确;
D.图所示反应物的总能量大于生成物总能量,此反应是放热反应,D正确;
答案选B。
11.【答案】
【解析】
【分析】
本题考查吸热反应和放热反应、化学反应与能量图象的相关知识,能正确的由图判断反应的吸、放热情况是解题的关键。
【解答】
A.断键吸收的能量成键放出的能量,故A正确;
B.图象分析反应物能量低于生成物,结合能量守恒分析反应是吸热反应,所以破坏反应物中的化学键所吸收的能量大于形成生成物中化学键所放出的能量,故B错误;
C.图象分析可知反应过程中反应物能量低于生成物能量,故C错误;
D.某些吸热反应不需要加热也可以发生,如氢氧化钡晶体和铵盐发生的吸热反应,故D错误。
故选A。
12.【答案】
【解析】
【分析】
本题考查能量图像与原电池,为高频考点,把握反应中能量变化、能量转化形式为解答的关键,侧重分析与应用能力的考查,题目难度不大。
【解答】
A.没有构成闭合回路,不能形成原电池,则不能将化学能转变为电能,故A错误;
B.由能量与反应过程图可知,红磷能量比白磷低,而能量越低,物质越稳定,故白磷不如红磷稳定,故B错误;
C.生成物的能量比反应物的能量低,故该反应为放热反应,故C正确;
D.途径Ⅰ与途径Ⅱ生成物的量相同,反应结束后能量相同,故产生相同质量的氧气时放出的热量相同,故D错误。
故选C。
13.【答案】
【解析】
【分析】
本题考查了化学反应能量变化分析,图象分析方法和应用,注意反应吸热放热和反应条件关系的判断应用,题目较简单。
【解答】
A.图象分析反应物能量低于生成物,结合能量守恒分析反应是吸热反应,故A错误;
B.断键吸收的能量成键放出的能量,故B正确;
C.图象分析可知反应过程中反应物能量低于生成物能量,故C错误;
D.某些吸热反应不需要加热也可以发生,如氢氧化钡晶体和铵盐发生的吸热反应,故D错误。
故选B。
14.【答案】
【解析】
【分析】
本题考查化学反应中的能量变化,解答这类问题应注意从宏观和微观角度分析化学反应中的能量变化,试题难度一般。
【解答】
A.据图可知该反应为吸热反应,反应 , ,故A错误;
B.反应 ,生成 反应放热 ,故 B错误;
C.根据键能与反应热的关系可知断开化学键需要吸收的能量为,故C正确;
D.形成中化学键可释放的能量为,故D错误。
故选C。
15.【答案】
【解析】
【分析】
本题考查了图象分析判断,焓变和物质能量的变化分析是关键,题目较简单。
【解答】
A.由图可知金刚石能量高于石墨,石墨转变为金刚石是吸热反应,故A正确;
B.由图可知气态硫的能量高于固态硫,等质量的完全燃烧放出的热量大于,故B错误;
C.由图可知白磷能量高于红磷,能量越低越稳定,红磷比白磷稳定,故C错误;
D.由图可知反应物的能量总和高于生成物的能量总和,反应是放热反应,故D错误。
故选A。
16.【答案】放热
高
热能
低
【解析】
【分析】
本题考查了化学反应中的吸热反应与放热反应,注意掌握化学反应中能量变化与反应物、生成物总能量的关系,明确化学键断裂、形成与化学反应能量变化的关系。
【解答】
由于发生反应,型管中甲处液面下降乙处液面上升,根据气体具有热胀冷缩的性质可以判断该反应为放热反应,
故答案为:放热;
由于的反应为吸热反应,所以和的总能量比和的总能量高,
故答案为:高;
化学变化伴随着物质和能量变化,物质中的化学能通过化学反应转化成热能释放出来,
故答案为:热能;
化学反应中旧键断裂吸收能量,新键生成放出能量,该反应为吸热反应,则反应物化学键断裂吸收的能量低于生成物化学键形成放出的能量,
故答案为:低;
该反应为放热反应,且不需要加热既能够发生,如铝与稀盐酸的反应,反应的化学方程式为:。
17.【答案】小于;
;
玻璃搅拌器;
;
;
;
保温、隔热,减少实验过程中的热量损失;
【解析】
【分析】本题考查化学反应原理,涉及常见放热反应、热化学方程式书写、盖斯定律、中和热测定等等,综合性强,难度一般,侧重对知识的灵活运用。
【解答】的燃烧属于放热反应,生成物能量总和小于反应物能量总和;甲烷气体在足量氧气中充分燃烧生成液态水和二氧化碳气体时放出热量,则反应放出,甲烷气体的燃烧热的热化学方程式:;
式 ,式 ,式 ,式式式得到;
密度为,质量分数为的浓硫酸的物质的量浓度,稀释过程中硫酸的物质的量不变,则需要浓硫酸的体积,
故答案为:;
实验中要让酸碱快速反应,需要使用玻璃搅拌器搅拌;
进行的四次实验的反应前后的温度差分别是:、、、,第一次实验误差偏大,应该舍去,则该实验的平均温度差为,
故答案为:;
二者反应,所得溶液的质量,反应放出的热量,,,酸、碱发生中和反应时、按:的物质的量关系反应,,所以反应产生水的物质的量按的物质的量计算,反应产生水的物质的量,则测定的中和热,
故答案为:;
实验装置保温、隔热效果差,使热量散失,反应放出热量偏小,导致中和热偏小,故正确;
量取溶液的体积时仰视读数,则碱的物质的量偏大,反应放出的热量偏多,使中和热偏大,故错误;
一次性把溶液倒入盛有溶液的小烧杯中,减少了实验过程中的热量损失,使测定值更接近,与实验事实不符合,故错误;
答案为;
中和热测定关键是减少实验过程中的热量损失,在大小烧杯之间填充碎泡沫塑料,可以更好的保温、隔热,减少实验过程中热量损失,
故答案为:保温、隔热,减少实验过程中热量损失。
18.【答案】,金刚石,石墨;石墨
【解析】
【分析】
本题考查盖斯定律、物质的稳定性、能量变化图、燃烧热、依据热化学方程式的计算等,解答这类问题应熟练掌握化学反应中的能量变化相关知识点,试题难度一般。
【解答】
,金刚石
,石墨
根据盖斯盖斯定律由可得,金刚石,石墨;根据该方程式可知金刚石能量高于石墨,所以石墨较稳定;
根据盖斯定律由可得的;
根据能量变化关系图分析可知反应放热,根据键能与焓变的关系可知反应物的总键能生成物的总键能;
根据燃烧热的概念可知甲醇生成液态水和气态二氧化碳时放出的热量为,由于气态水转化为液态水放热,所以;
根据方程式分析可知转移电子放出的热量为,则转移电子放出的热量为。
19.【答案】吸热;
【解析】
【分析】
本题考查化学反应中的能量变化,题目难度中等,掌握反应热的求算方法和盖斯定律是解题的关键。
【解答】
由图可知,反应物的总能量小于生成物的总能量,故该反应为吸热反应,反应的,
故答案为:吸热;;
该反应为吸热反应,断裂旧化学键吸收的总能量形成新化学键释放的总能量,
故答案为:;
已知: ,,由盖斯定律可得,
故答案为:;
气体分解生成与 的热化学方程式为 ,
故答案为: ;
碳的燃烧热指的是碳完全燃烧生成二氧化碳时放出的热量,时, ,故碳的燃烧热数值 ,
故答案为:。
第1页,共1页
单选题
1. 理论研究表明,在和下,异构化反应过程的能量变化如图所示,下列有关说法正确的是( )
A. 比稳定
B. 逆反应的活化能为
C. 反应物断键吸收的总能量小于生成物成键放出的总能量
D. 该反应的热化学方程式为
2. 根据能量变化示意图,下列说法正确的是( )
A. 状态是液态,则状态一定是气态
B. 状态是液态,则状态一定是气态
C. 状态状态
D. 断裂状态和中的化学键需要吸收的能量为
3. 下列说法不正确的是( )
A. ,则每生成放热
B. 天然气的主要成分甲烷是高效、较洁净的燃料
C. 天然气是不可再生能源
D. 使用催化剂,可以改变反应的反应热
4. 单斜硫和正交硫转化为二氧化硫的能量变化如图所示,下列说法正确的是( )
A. 单斜,正交,
B. 正交硫比单斜硫稳定
C. 相同物质的量的正交硫比单斜硫所含有的能量高
D. 表示断裂中的共价键所吸收的能量比形成中的共价键所放出的能量少
5. 某反应由两步反应构成,它的反应能量曲线如图,下列叙述正确的是
A. 两步反应均为吸热反应 B. 三种化合物中最稳定
C. 与的能量差为 D. 反应,反应条件一定要加热
6. 一定条件下,石墨转化为金刚石的能量变化如图所示.在该条件下,下列结论正确的是.( )
A. 石墨转化为金刚石是放热反应 B. 金刚石比石墨稳定
C. 等质量的金刚石和石墨完全燃烧释放的热量不同 D. 金刚石和石墨的燃烧产物属于空气污染物
7. 下列依据热化学方程式得出的结论正确的是 ( )
A. 已知 ;则氢气的燃烧热为
B. 已知 石墨, 金刚石,;则金刚石比石墨稳定
C. 已知 ,则含 的稀溶液与稀盐酸完全中和,放出 的热量
D. 己知 ; ,则
8. 化学能可与热能、电能等相互转化。下列说法正确的是
A. 图Ⅰ所示的装置能将化学能转化为电能
B. 中和反应中,反应物的总能量比生成物的总能量低
C. 化学反应中能量变化的主要原因是化学键的断裂与形成
D. 图Ⅱ所示的反应为吸热反应
9. 和在催化剂表面合成氨的微观历程及能量变化的示意图如下,用、、分别表示、、,已知:,该反应属于放热反应。下列说法正确的是( )
A. 催化剂仅起到吸附和的作用,对化学反应速率没有影响
B. 过程,是放热过程
C. 过程,原子和原子形成了含有非极性键的
D. 合成氨反应中,反应物断键吸收能量小于生成物形成新键释放的能量
10. 化学能与热能、电能等能相互转化,关于化学能与其他能量相互转化的说法错误的是
A. 化学反应中能量变化的主要原因是化学键的断裂与生成
B. 铝热反应中,反应物的总能量比生成物的总能量低
C. 图所示的装置不能将化学能转变为电能
D. 图所示的反应为放热反应
11. 已知反应的能量变化如图所示、均为正值,下列说法正确的是( )
A. 该反应吸收的能最为
B. 破坏反应物中的化学键所吸收的能量小于形成生成物中化学键所放出的能量
C. 和的总能量一定高于和的总能量
D. 该反应只有在加热条件下才能进行
12. 化学能与热能、电能等可以相互转化.关于化学能与其他能量相互转化的说法正确的是( )
A. 将化学能转变为电能
B. 白磷比红磷稳定
C. 发生的反应为放热反应
D. 其他条件相同时,按途径Ⅰ发生反应与按途径Ⅱ发生反应,并产生相等质量氧气时放出的热量不相等
13. 已知反应的能量变化如图所示,下列说法正确的是
A. 该反应为放热反应 B. 该反应吸收的能量为
C. 反应物的总能量高于生成物的总能量 D. 该反应只有在加热条件下才能进行
14. 反应的能量变化如图所示。已知:断开中化学键需吸收能量,断开中化学键需吸收能量。下列说法正确的是
A.
B.
C. 断开中化学键需要吸收能量
D. 形成中化学键可释放能量
15. 下列图象分别表示有关反应的反应过程与能量变化的关系。
据此判断下列说法中正确的是( )
A. 石墨转变为金刚石是吸热反应
B. 等质量的完全燃烧放出的热量小于
C. 白磷比红磷稳定
D. 为吸热反应
二、实验题
16. 为了研究化学反应的能量变化情况,某同学设计了如图所示装置。当向盛有的试管中滴加试剂时,看到形管中甲处液面下降乙处液面上升。试回答下列问题:
该反应为________反应填“放热”或“吸热”。
和的总能量比和的总能量________填“高”或“低”。
物质中的化学能通过化学反应转化成____________释放出来。
反应物化学键断裂吸收的能量________填“高”或“低”于生成物化学键形成放出的能量。
写出一个符合题中条件的化学方程式:_________________________________。
17. 生产生活中的化学反应都伴随着能量的变化,请根据有关知识回答下列问题:
反应,生成物能量总和_______填“大于”、“小于”或“等于”反应物能量总和。
已知:常温常压下,甲烷气体在足量氧气中充分燃烧生成液态水和二氧化碳气体时放出热量,写出甲烷气体的燃烧热的热化学方程式:_______________。
焙烧产生的可用于制硫酸。
已知:、时, ;
;
;
则与反应生成的热化学方程式是______________。
某实验小组用的溶液和的溶液进行中和反应的反应热测定。
若需配制溶液,则需用量筒量取_______密度为,质量分数为的浓硫酸。
测定稀硫酸和氢氧化钠稀溶液反应的反应热的实验装置如图所示。则仪器的名称为_______。
取溶液和溶液进行实验,实验数据如下表。
实验次数 反应物温度 反应前体系的温度 反应后体系的温度 温度差
温度差的平均值为_______。
近似认为的溶液和的溶液的密度都是,中和后生成的溶液的比热容。则测得生成时中和反应的反应热_______取小数点后一位。
上述结果与理论值有偏差,产生此偏差的原因可能是_______填标号。
实验装置保温、隔热效果差
用量筒量取溶液的体积时仰视读数
把溶液一次性倒入盛有溶液的小烧杯中
碎泡沫塑料的作用是____________________________。
三、简答题
18. Ⅰ,金刚石 ;
,石墨
则金刚石转化为石墨的热化学方程式为______________________,由热化学方程式看来更稳定的是_____。
; ; ;则的_______________________。用、、代数式表示
下图是反应过程中的能量变化图。
由图可知,反应物的总键能________填“”、“”或者“”生成物的总键能。
已知的燃烧热为, ,则_________填“”“”或“”。
火箭和导弹表面的薄层是耐高温物质。将石墨、铝粉和二氧化钛按一定比例混合在高温下煅烧,所得物质可作耐高温材料: ,则反应过程中,每转移电子放出的热量为_________。
19. 某反应过程中的能量变化如图所示,回答问题。
该反应是_______填“吸热”或“放热”反应,反应的________用含的代数式表示。
该反应过程中,断裂旧化学键吸收的总能量_____填“”“ ”或“”形成新化学键释放的总能量。
已知:
则: ______________。
已知拆开键、键、键分别需要的能量是、、,则气体分解生成与的热化学方程式为________________________________
已知:时, ,则碳的燃烧热数值_____填,,。
答案和解析
1.【答案】
【解析】
【分析】
本题考查反应热与焓变,明确图示曲线变化的意义为解答关键,注意化学反应与能量变化的关系,试题侧重考查学生的分析能力及灵活运用基础知识的能力,题目难度不大。
【解答】
A.能量越低越稳定,的能量低于的能量,所以比稳定,故A错误;
B.根据题图可知逆反应的活化能为,故B错误;
C.该反应为吸热反应,故反应物断键吸收的总能量大于生成物成键放出的总能量,故C错误;
D.反应热为生成物总能量减去反应物总能量,热化学方程式为,故D正确。
2.【答案】
【解析】
【分析】
本题考查了化学反应与能量的变化、反应热的计算等知识,难度一般,侧重基础知识的考查。
【解答】
A.状态是液态,状态不能确定,故A错误;
B.状态是液态,状态不能确定,故B错误;
C.状态状态 ,故C正确;
D.断裂化学键的量不确定,由图不能确定化学键断裂吸收的能量,故D错误。
故选C。
3.【答案】
【解析】该热化学方程式表示气态与 气态,反应产生液态放出的热量,A正确;
天然气的主要成分甲烷燃烧产生,,放出大量的热量,因此是高效、较洁净的燃料,B正确;
天然气属于化石能源,是远古时代的动植物遗体、遗骸经过漫长的历史时期形成的,短时间内不能产生,因此属于不可再生能源,C正确;
使用催化剂,只能改变反应途径,不能改变反应物、生成物的能量,因此不能改变反应的反应热,D错误。
4.【答案】
【解析】
【分析】
本题考查了化学反应中的能量变化,正确理解图象中曲线的含义是解题的关键,注意物质的能量越高越不稳定,正确判断反应热、活化能与键能的关系。。
【解答】
A.单斜硫的能量比正交硫的能量高,,单斜,正交,为放热反应,故A错误;
B.物质的能量越高越不稳定,则正交硫比单斜硫稳定,故B正确;
C.由图象可以看出,单斜硫的能量比正交硫的能量高,故C错误;
D.式反应需断裂单斜硫中键和键,不仅仅是断裂中的共价键所吸收的能量,故D错误。
故选B。
5.【答案】
【解析】略
6.【答案】
【解析】略
7.【答案】
【解析】
【分析】
本题考查燃烧热、中和热概念,反应热与物质稳定性的关系,盖斯定律的应用,难度不大。
【解答】
A.燃烧热是指可燃物完全燃烧生成稳定化合物时放出的热量,燃烧生成液态水,故A错误;
B.已知石墨,金刚石,;,反应是吸热反应,金刚石能量高于石墨,所以金刚石比石墨的键能小,因此是石墨比金刚石稳定,故B错误;
C.已知,则含物质的量为的稀溶液与稀盐酸完全中和,放出的热量,故C正确;
D.已知;;,一氧化碳燃烧生成二氧化碳放热,焓变是负值,所以,故D错误。
故选C。
8.【答案】
【解析】A.该装置不能构成闭合回路,不能构成原电池,则不能将化学能转化为电能,故A错误;
B.中和反应为放热反应,则反应物总能量大于生成物总能量,故B错误;
C.断键吸收热量、成键放出热量,化学反应实质是旧化学键的断裂和新化学键的形成,所以化学反应中能量变化的主要原因是化学键的断裂与形成,故C正确;
D.图Ⅱ所示反应物总能量大于生成物总能量,则该反应为放热反应,否则为吸热反应,根据图知,反应物总能量大于生成物总能量,则为放热反应,故D错误;
故答案为。
9.【答案】
【解析】略
10.【答案】
【解析】A.化学反应时断键要吸收能量,成键要放出能量,所以化学反应中能量变化的主要原因是化学键的断裂与生成,A正确;
B.铝热反应是放热反应,反应物的总能量应大于生成物的总能量,B错误;
C.图没有形成闭合回路,不能形成原电池,不能将化学能转化为电能,C正确;
D.图所示反应物的总能量大于生成物总能量,此反应是放热反应,D正确;
答案选B。
11.【答案】
【解析】
【分析】
本题考查吸热反应和放热反应、化学反应与能量图象的相关知识,能正确的由图判断反应的吸、放热情况是解题的关键。
【解答】
A.断键吸收的能量成键放出的能量,故A正确;
B.图象分析反应物能量低于生成物,结合能量守恒分析反应是吸热反应,所以破坏反应物中的化学键所吸收的能量大于形成生成物中化学键所放出的能量,故B错误;
C.图象分析可知反应过程中反应物能量低于生成物能量,故C错误;
D.某些吸热反应不需要加热也可以发生,如氢氧化钡晶体和铵盐发生的吸热反应,故D错误。
故选A。
12.【答案】
【解析】
【分析】
本题考查能量图像与原电池,为高频考点,把握反应中能量变化、能量转化形式为解答的关键,侧重分析与应用能力的考查,题目难度不大。
【解答】
A.没有构成闭合回路,不能形成原电池,则不能将化学能转变为电能,故A错误;
B.由能量与反应过程图可知,红磷能量比白磷低,而能量越低,物质越稳定,故白磷不如红磷稳定,故B错误;
C.生成物的能量比反应物的能量低,故该反应为放热反应,故C正确;
D.途径Ⅰ与途径Ⅱ生成物的量相同,反应结束后能量相同,故产生相同质量的氧气时放出的热量相同,故D错误。
故选C。
13.【答案】
【解析】
【分析】
本题考查了化学反应能量变化分析,图象分析方法和应用,注意反应吸热放热和反应条件关系的判断应用,题目较简单。
【解答】
A.图象分析反应物能量低于生成物,结合能量守恒分析反应是吸热反应,故A错误;
B.断键吸收的能量成键放出的能量,故B正确;
C.图象分析可知反应过程中反应物能量低于生成物能量,故C错误;
D.某些吸热反应不需要加热也可以发生,如氢氧化钡晶体和铵盐发生的吸热反应,故D错误。
故选B。
14.【答案】
【解析】
【分析】
本题考查化学反应中的能量变化,解答这类问题应注意从宏观和微观角度分析化学反应中的能量变化,试题难度一般。
【解答】
A.据图可知该反应为吸热反应,反应 , ,故A错误;
B.反应 ,生成 反应放热 ,故 B错误;
C.根据键能与反应热的关系可知断开化学键需要吸收的能量为,故C正确;
D.形成中化学键可释放的能量为,故D错误。
故选C。
15.【答案】
【解析】
【分析】
本题考查了图象分析判断,焓变和物质能量的变化分析是关键,题目较简单。
【解答】
A.由图可知金刚石能量高于石墨,石墨转变为金刚石是吸热反应,故A正确;
B.由图可知气态硫的能量高于固态硫,等质量的完全燃烧放出的热量大于,故B错误;
C.由图可知白磷能量高于红磷,能量越低越稳定,红磷比白磷稳定,故C错误;
D.由图可知反应物的能量总和高于生成物的能量总和,反应是放热反应,故D错误。
故选A。
16.【答案】放热
高
热能
低
【解析】
【分析】
本题考查了化学反应中的吸热反应与放热反应,注意掌握化学反应中能量变化与反应物、生成物总能量的关系,明确化学键断裂、形成与化学反应能量变化的关系。
【解答】
由于发生反应,型管中甲处液面下降乙处液面上升,根据气体具有热胀冷缩的性质可以判断该反应为放热反应,
故答案为:放热;
由于的反应为吸热反应,所以和的总能量比和的总能量高,
故答案为:高;
化学变化伴随着物质和能量变化,物质中的化学能通过化学反应转化成热能释放出来,
故答案为:热能;
化学反应中旧键断裂吸收能量,新键生成放出能量,该反应为吸热反应,则反应物化学键断裂吸收的能量低于生成物化学键形成放出的能量,
故答案为:低;
该反应为放热反应,且不需要加热既能够发生,如铝与稀盐酸的反应,反应的化学方程式为:。
17.【答案】小于;
;
玻璃搅拌器;
;
;
;
保温、隔热,减少实验过程中的热量损失;
【解析】
【分析】本题考查化学反应原理,涉及常见放热反应、热化学方程式书写、盖斯定律、中和热测定等等,综合性强,难度一般,侧重对知识的灵活运用。
【解答】的燃烧属于放热反应,生成物能量总和小于反应物能量总和;甲烷气体在足量氧气中充分燃烧生成液态水和二氧化碳气体时放出热量,则反应放出,甲烷气体的燃烧热的热化学方程式:;
式 ,式 ,式 ,式式式得到;
密度为,质量分数为的浓硫酸的物质的量浓度,稀释过程中硫酸的物质的量不变,则需要浓硫酸的体积,
故答案为:;
实验中要让酸碱快速反应,需要使用玻璃搅拌器搅拌;
进行的四次实验的反应前后的温度差分别是:、、、,第一次实验误差偏大,应该舍去,则该实验的平均温度差为,
故答案为:;
二者反应,所得溶液的质量,反应放出的热量,,,酸、碱发生中和反应时、按:的物质的量关系反应,,所以反应产生水的物质的量按的物质的量计算,反应产生水的物质的量,则测定的中和热,
故答案为:;
实验装置保温、隔热效果差,使热量散失,反应放出热量偏小,导致中和热偏小,故正确;
量取溶液的体积时仰视读数,则碱的物质的量偏大,反应放出的热量偏多,使中和热偏大,故错误;
一次性把溶液倒入盛有溶液的小烧杯中,减少了实验过程中的热量损失,使测定值更接近,与实验事实不符合,故错误;
答案为;
中和热测定关键是减少实验过程中的热量损失,在大小烧杯之间填充碎泡沫塑料,可以更好的保温、隔热,减少实验过程中热量损失,
故答案为:保温、隔热,减少实验过程中热量损失。
18.【答案】,金刚石,石墨;石墨
【解析】
【分析】
本题考查盖斯定律、物质的稳定性、能量变化图、燃烧热、依据热化学方程式的计算等,解答这类问题应熟练掌握化学反应中的能量变化相关知识点,试题难度一般。
【解答】
,金刚石
,石墨
根据盖斯盖斯定律由可得,金刚石,石墨;根据该方程式可知金刚石能量高于石墨,所以石墨较稳定;
根据盖斯定律由可得的;
根据能量变化关系图分析可知反应放热,根据键能与焓变的关系可知反应物的总键能生成物的总键能;
根据燃烧热的概念可知甲醇生成液态水和气态二氧化碳时放出的热量为,由于气态水转化为液态水放热,所以;
根据方程式分析可知转移电子放出的热量为,则转移电子放出的热量为。
19.【答案】吸热;
【解析】
【分析】
本题考查化学反应中的能量变化,题目难度中等,掌握反应热的求算方法和盖斯定律是解题的关键。
【解答】
由图可知,反应物的总能量小于生成物的总能量,故该反应为吸热反应,反应的,
故答案为:吸热;;
该反应为吸热反应,断裂旧化学键吸收的总能量形成新化学键释放的总能量,
故答案为:;
已知: ,,由盖斯定律可得,
故答案为:;
气体分解生成与 的热化学方程式为 ,
故答案为: ;
碳的燃烧热指的是碳完全燃烧生成二氧化碳时放出的热量,时, ,故碳的燃烧热数值 ,
故答案为:。
第1页,共1页
