专题7第一单元氮的固定同步练习(含答案)2022——2023学年高一化学下学期苏教版(2019)必修第二册
文档属性
| 名称 | 专题7第一单元氮的固定同步练习(含答案)2022——2023学年高一化学下学期苏教版(2019)必修第二册 |
|
|
| 格式 | docx | ||
| 文件大小 | 355.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-06-18 00:00:00 | ||
图片预览



文档简介
专题7第一单元氮的固定同步练习
一、单选题
1. 下列关于氮及其化合物的说法正确的是( )
A. 化学性质稳定,可用作保护气
B. 、均为大气污染气体,在大气中可稳定存在
C. 、均易溶于水
D. 、均能与水发生反应
2. 无色的混合气体甲,可能含、、、中的几种,将一定量的甲气体经过如图实验的处理,结果得到酸性溶液,而几乎无气体剩余,则甲气体的组成为( )
A. 、 B. 、 C. 、 D. 、、
3. 常温下,将盛有和的混合气体的试管倒立于水槽中并向其中通入,一段时间后,试管内还剩余气体,则通入的体积可能为 ( )
A. B. C. D.
4. 把体积的气体,依次通过下列个分别装有饱和溶液、浓硫酸、的装置后,用排水法把残留气体收集到集气瓶中,集气瓶内气体应是同温同压下测定( )
A. 体积 B. 体积和体积
C. 体积 D. 体积
5. 下列关于和的叙述正确的是 ( )
A. 都能溶于水且与水反应生成相应的酸 B. 都是酸性氧化物,都能与强碱溶液反应
C. 可以通过铜与硝酸制取 D. 常温下都可以被氧气氧化
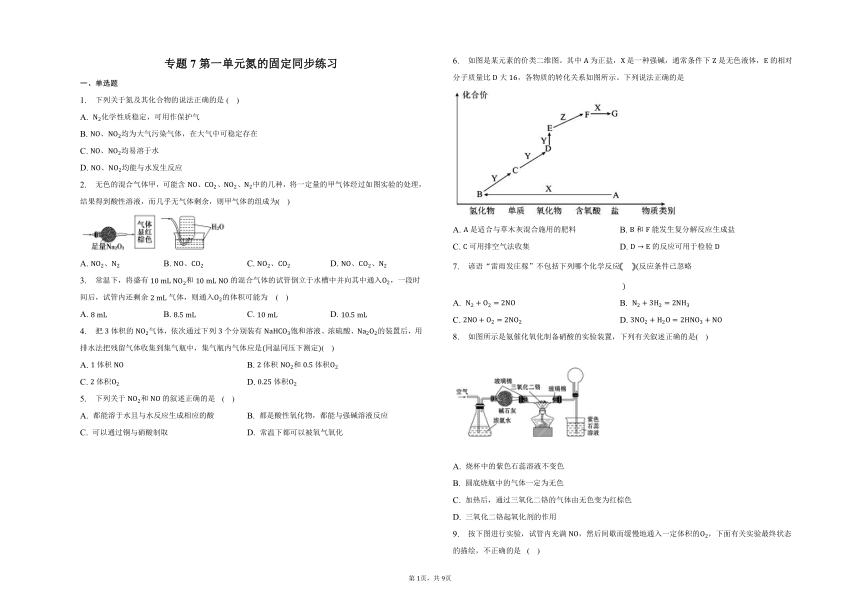
6. 如图是某元素的价类二维图。其中为正盐,是一种强碱,通常条件下是无色液体,的相对分子质量比大,各物质的转化关系如图所示。下列说法正确的是
A. 是适合与草木灰混合施用的肥料 B. 和能发生复分解反应生成盐
C. 可用排空气法收集 D. 的反应可用于检验
7. 谚语“雷雨发庄稼”不包括下列哪个化学反应 反应条件已忽略
A. B.
C. D.
8. 如图所示是氨催化氧化制备硝酸的实验装置,下列有关叙述正确的是( )
A. 烧杯中的紫色石蕊溶液不变色
B. 圆底烧瓶中的气体一定为无色
C. 加热后,通过三氧化二铬的气体由无色变为红棕色
D. 三氧化二铬起氧化剂的作用
9. 按下图进行实验,试管内充满,然后间歇而缓慢地通入一定体积的,下面有关实验最终状态的描绘,不正确的是 ( )
A. 若最终有气体剩余,气体可能是 B. 若最终有气体剩余,气体呈红棕色
C. 试管内溶液为稀硝酸 D. 试管内液面高度肯定会上升
10. 某无色混合气体中可能含、、、、中的几种。将混合气体经过如图所示的处理后,几乎无气体剩余,则下列说法正确的是
A. 混合气体中一定含有、、 B. 混合气体中可能含有
C. 混合气体中的体积分数为 D. 混合气体中的体积分数最大
11. 某混合气体中可能含有、、、、中的两种或多种气体,现将此无色透明的混合气体通过品红溶液后,品红溶液褪色,把剩余气体排入空气中,很快变为红棕色。下列对于原混合气体成分的判断中正确的是( )
A. 肯定有和 B. 肯定有
C. 可能有和 D. 可能有、、三种气体
12. 下列实验操作一定能达到相应实验目的是
实验目的 实验操作
验证 向与混合液中加入适量溶液
证明的酸性强于 向溶液中通入少量
鉴别乙酸乙酯和乙酸 分别加入饱和溶液
验证中是否含有 向混合气体中通入观察颜色是否加深
A. B. C. D.
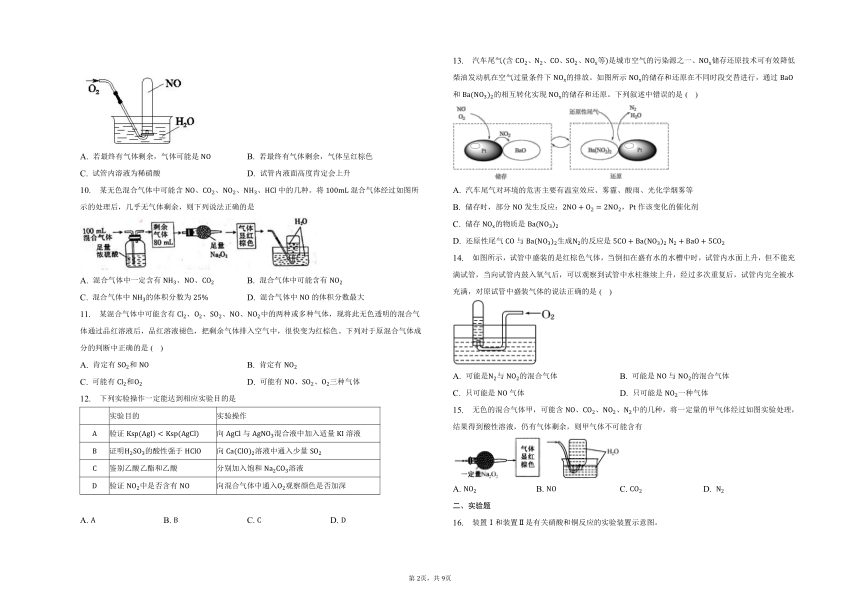
13. 汽车尾气含、、、、等是城市空气的污染源之一、储存还原技术可有效降低柴油发动机在空气过量条件下的排放。如图所示的储存和还原在不同时段交替进行,通过和的相互转化实现的储存和还原。下列叙述中错误的是( )
A. 汽车尾气对环境的危害主要有温室效应、雾霾、酸雨、光化学烟雾等
B. 储存时,部分发生反应:,作该变化的催化剂
C. 储存的物质是
D. 还原性尾气与生成的反应是
14. 如图所示,试管中盛装的是红棕色气体,当倒扣在盛有水的水槽中时,试管内水面上升,但不能充满试管,当向试管内鼓入氧气后,可以观察到试管中水柱继续上升,经过多次重复后,试管内完全被水充满,对原试管中盛装气体的说法正确的是( )
A. 可能是与的混合气体 B. 可能是与的混合气体
C. 只可能是气体 D. 只可能是一种气体
15. 无色的混合气体甲,可能含、、、中的几种,将一定量的甲气体经过如图实验处理,结果得到酸性溶液,仍有气体剩余,则甲气体不可能含有
A. B. C. D.
二、实验题
16. 装置Ⅰ和装置Ⅱ是有关硝酸和铜反应的实验装置示意图。
若用装置Ⅰ进行铜与浓硝酸反应的实验,最大的缺点是__________________________。若用装置Ⅰ来证明铜与稀硝酸反应生成气体,其最大缺点是不能与浓硝酸跟铜反应形成鲜明对照,简述原因:_____________________________________________________________________________________________________________________________________________________________。
若用装置Ⅱ进行适当操作,即可克服上述缺点,还能使上述两反应在同一试管中先后连续进行,实验步骤如下。
步骤一:组装好装置并________________后,加入浓硝酸铜片接近酸液,塞紧胶塞。
步骤二:________________________操作使反应发生。当导管口有少量红棕色气体逸出时,________________________操作使反应停止。同时将导管插入水中。稍后能观察到水沿导管倒吸至试管中,产生此现象的原因是________________________。还可能观察到的明显现象是________填标号。
溶液由蓝色变为无色 红棕色气体变为无色
17. 某研究性学习小组的同学通过查阅资料知,可与炽热的铜粉发生反应,他们设计如图装置夹持装置已略去进行实验验证。
已知:能被酸性高锰酸钾溶液氧化生成。
请回答下列问题:
实验开始前,应进行的一步操作是 ______;装置中发生反应的化学方程式为 ______。
装置的作用为 ______;装置中所用的酸性干燥剂的化学式是 ______。
装置中反应开始前,需要先打开,向装置中通入一段时间的或,其目的是 ______。
实验过程中,装置中铜粉变黑,装置中溶液颜色变浅,则装置中发生反应的化学方程式为 ______;请设计一种简单的实验方案,证明实验中装置中有生成 ______写出主要的操作过程、现象、结论。
假设实验结束后,从装置中收集到,气体,为使全部被水吸收,应向集气瓶内通入 ______。
三、简答题
18. 氮及其化合物与生产生活关系密切。请完成下列填空:
某学校化学学习小组为探究二氧化氮的性质,按下图所示装置进行实验。
装置甲中盛放浓硝酸的仪器的名称是______,装置丙中的试管内发生反应的离子方程式为:______。
实验过程中装置乙、丙中出现的现象分别是______;______。
在医疗上有重要的应用,曾被科学家作为研究的重要物质。现有容积为的试管盛满后倒扣于水槽中,再向试管中通入一定体积后,试管内气体的体积为试管容积的一半,则通入的的在相同条件下体积为______。
A.
在盛有一定量浓硝酸的试管中加入的铜片发生反应。请回答下列问题:
开始阶段,反应的化学方程式为______,后一阶段生成的气体为______,若两者恰好完全反应整个反应过程共产生标准状况下气体,则反应过程中被还原的的物质的量为______ ,参加反应的的物质的量为______ 。
反应结束后往试管中加入铜片,再加入少量的稀硫酸,这时铜片上又有气泡产生,反应的离子方程式为______。
19. A、、、是中学化学中的常见物质,其中为单质。各物质的转化关系如下:
若是空气中含量最多的气体。
下列叙述中,正确的是___填字母。
可用向上排空气法收集 的基本反应类型为化合反应
的浓溶液见光易分解,一般保存在棕色试剂瓶中
写出与水反应的化学方程式_____________________________
实验室制取的最简单氢化物装置如图所示,回答下列问题
试管中的试剂为_________________;装置的作用是___________。
若、、、的焰色反应均为黄色,为淡黄色固体,在加热条件下可直接转化为。
的化学方程式是_______________________________________
、、均能与水发生反应。与水反应的实验现象中,能说明该反应放热、的熔点低的是___。若单质与水反应。产生的气体在标准状况下的体积为_______.
答案和解析
1.【答案】
【解析】
【分析】
本题主要考查氮及其化合物的相关性质,题目难度中等,注意不同物质之间性质的差别。
【解答】
A.氮气的化学性质稳定,很难发生化学反应,通常作保护气,故A正确;
B.、均是污染性气体,和氧气能反应生成二氧化氮,不能在大气中稳定存在,故B错误;
C.一氧化氮难溶于水,故C错误;
D.一氧化氮难溶于水,也不能与水反应,故D错误。
故选A。
2.【答案】
【解析】解:二氧化氮是红棕色的气体,所以无色混合气体甲中一定不存在二氧化氮;
二氧化碳可以和过氧化钠反应生成碳酸钠和氧气,反应的化学方程式为:,
一氧化氮无色,与氧气立即反应变为红棕色的二氧化氮,通过足量的过氧化钠后气体显红棕色,说明有、,排水法收集气体,广口瓶被上升的水注满,说明没有,所以甲气体的组成为:、;
故选:。
二氧化氮是红棕色的气体,浓硫酸可以和氨气反应,二氧化碳可以和过氧化钠反应生成氢氧化钠和氧气,一氧化氮无色,与氧气立即反应变为红棕色的二氧化氮,氮气不溶于水,将一定量的甲气体经过如图实验的处理,结果得到酸性溶液,而几乎无气体剩余,说明无氮气,据此分析解答.
本题考查常见气体的检验和性质,把握常见气体的化学性质及气体的溶解性是解题的关键,注意二氧化碳和过氧化钠的反应,题目难度不大.
3.【答案】
【解析】
【分析】
本题考查了有关混合物反应的化学计算,题目难度中等,明确反应后剩余气体组成为解答关键,注意掌握、二氧化氮与氧气、水转化成硝酸的反应原理,要求学生掌握讨论法在化学计算中的应用。
【解答】剩余的气体可能为氧气,有可能为,当剩余的气体为氧气时,二氧化氮和完全反应,可以根据方程式、计算出通入氧气的总体积;
当剩余的气体为时,可以看作二氧化氮完全反应,反应消耗了,还剩余,然后根据反应方程式计算出消耗的氧气的体积。
当剩下的气体为时,和 说明完全反应生成硝酸,则:
,
,
所以通入的氧气体积为:;
当剩余的气体为时,可以认为 完全反应生成硝酸,中剩余,有转化成硝酸,则:
,
,
所以通入氧气的体积为:,
故选:。
4.【答案】
【解析】体积通入溶液中发生反应:,,经过浓硫酸干燥得到体积和体积气体。再通过发生反应为:生成体积氧气,然后,此时剩余体积和体积。通过水发生反应:,故剩余体积氧气。
5.【答案】
【解析】
【分析】
本题考查了和的性质,试题较为基础,难度不大,注意相关知识的积累即可解答。
【解答】
A.能溶于水,与水反应生成和;既不溶于水,也不与水反应,A错误;
B.和都不是酸性氧化物,B错误;
C.可以通过铜与浓硝酸制取,铜与稀硝酸制取,C正确;
D.常温下可以被氧气氧化,不可以,D错误;
故选C。
6.【答案】
【解析】
【分析】
本题以元素化合物的推断为载体考查了元素化合物的性质,通过元素化合物的推断考查学生的推理、分析、判断等能力,正确推断元素化合物是解本题的关键。
【解答】
为正盐,是一种强碱,与生成,为氢化物,铵盐与强碱反应生成,为,的相对分子质量比的相对分子质量大,说明和反应,、是氧化物,分子式相差一个氧原子;又是酸,说明是,被氧气氧化生成单质,氮气被氧气氧化生成,为,被氧气氧化生成,为,与水反应生成硝酸,为硝酸,硝酸与强碱反应生成硝酸盐。据此解答。
A.铵盐属于铵态氮肥,草木灰中含属钾肥,但溶于水显碱性,两者混合会互促水解,释放出,降低肥效,故A错误;
B.氨气与硝酸可以发生化合反应生成硝酸铵,故B错误;
C.为氮气,其密度与空气接近,不可用排空气法收集,可以排水法收集,故C错误;
D.为无色气体,易与氧气反应,将与空气接触,有红棕色气体生成,如观察到红棕色,则说明生成,故D正确。
故选D。
7.【答案】
【解析】
【分析】
本题主要考查了雷雨肥田原理,氮气、一氧化氮、二氧化氮的化学性质,理解反应原理、正确书写化学方程式是解答的关键,题目难度不大。
【解答】
“雷雨发庄稼”,空气中的在放电条件下与直接化合生成无色且不溶于水的一氧化氮气体:;一氧化氮常温下易与空气中的反应生成红棕色的二氧化氮气体:;二氧化氮与水反应生成硝酸和一氧化氮:,生成的硝酸随雨水淋洒到大地上,同土壤中的矿物相互作用,生成可溶于水的硝酸盐可作氮肥,植物生长得更好。“雷雨发庄稼”不包括氮气和氢气合成氨的反应,故B符合题意。
故选B。
8.【答案】
【解析】
【分析】
本题考查硝酸的制备实验评价,为高频考点,把握实验装置的作用、物质的性质及发生的反应为解答的关键,侧重分析与实验能力的考查,题目难度不大。
【解答】
由实验装置可知,氨气被碱石灰干燥后,在大试管中氨气与氧气反应生成,圆底烧瓶中被氧化生成红棕色,与水反生成硝酸,
A.硝酸遇石蕊变红,则烧杯中的紫色石蕊溶液变红,故A错误
B.圆底烧瓶中的气体可能为红棕色,故B错误
C.加热后,通过三氧化二铬的催化作用生成无色,被氧化生成红棕色的气体,故C正确;
D.氨气与氧气在三氧化二铬的催化作用反应生成和水,故D错误
故选C。
9.【答案】
【解析】解:若氧气不足,最终有气体剩余,气体可能是,故A正确;
B.二氧化氮与水反应,最终剩余气体不可能为红棕色,故B错误;
C.反应生成硝酸,试管内溶液为稀硝酸,故C正确;
D.生成硝酸易溶于水,试管内液面高度肯定会上升,故D正确;
故选:。
试管内装有,然后间歇而缓慢地通入,当一氧化氮和氧气恰好反应生成硝酸时发生,溶液充满试管,以此来解答。
本题考查物质的性质,为高频考点,把握物质的性质、反应与现象为解答的关键,侧重分析与应用能力的考查,注意元素化合物知识的应用,题目难度不大。
10.【答案】
【解析】
【分析】
本题考查常见气体的检验和性质,是一道气体的鉴别题目,注意氨气的碱性、注意二氧化碳和过氧化钠的反应,题目难度不大。
【解答】
二氧化氮是红棕色的气体,所以混合气体甲中一定不存在,硫酸和碱性气体能反应,所以甲气体经过足量的浓硫酸,溢出剩余气体,说明一定有且存在体积为,的体积分数为,二氧化碳可以和过氧化钠反应生成碳酸钠和氧气,反应的化学方程式为:,与甲气体的组成无关,一氧化氮无色,与氧气立即反应变为红棕色的二氧化氮,通过足量的过氧化钠后气体显红棕色,说明有、,排水法收集气体,广口瓶被上升的水注满,说明与的体积比为:。
A.甲中气体有、、,故A正确;
B.混合气体中不含有,故B错误;
C.甲中的体积分数,故C错误;
D.由方程式,,最后无气体剩余可知与的体积比为:,则的体积分数不是最大,故D错误。
故选A。
11.【答案】
【解析】
【分析】
本题考查混合气体组成的推断,意在考查学生的分析推理能力,解题关键是掌握氯气、二氧化硫、氮氧化物的性质。
【解答】
该气体无色,排除了、气体;该气体能使品红溶液褪色,则一定含有气体;将剩余气体排放到空气中,气体迅速变为红棕色,判断一定含有气体,则一定无,一定含有的气体是、,一定没有的气体为、、,故A正确。
12.【答案】
【解析】A.与反应生成沉淀,不能比较、的大小,故A错误;
B.溶液中通入少量,发生氧化还原反应生成硫酸钙,则不能比较、的酸性强弱,故B错误;
C.乙酸与饱和碳酸钠溶液反应有气泡产生,与乙酸乙酯分层,现象不同,可鉴别,故C正确;
D.与氧气反应生成二氧化氮气体,红棕色变化不明显,不能验证中是否含有,故D错误;
本题考查化学实验方案的评价,为高频考点,把握物质的性质、难溶电解质、物质的鉴别、实验技能为解答的关键,侧重分析与实验能力的考查,注意元素化合物知识的应用,题目难度不大。
13.【答案】
【解析】
【分析】
略
【解答】
A.汽车尾气含、、等,会造成温室效应,灰尘会造成雾霾,、在空气中生成硫酸,导致酸雨产生,造成光化学烟雾,故A正确;
B.储存时,一氧化氮和氧气反应生成了二氧化氮,反应:,作该变化的催化剂,故B正确;
C.储存时,氧化钡、一氧化氮和氧气反应生成了硝酸钡,所以储存时,吸收 如 ,的物质是,故C错误;
D.还原时,发生的反应是一氧化碳和硝酸钡反应生成氮气、氧化钡和二氧化碳,化学方程式为:,故D正确;
故选:。
14.【答案】
【解析】
【分析】
本题考查氮氧化物、氧气于水反应的分析,难度不大,注意题目中的“只”、“仅”、“可能”、“都”等关键词的含义,是做出正确判断的关键。
【解答】
A.氮气不溶于水,且其与氧气在常温常压下不反应,所以水最终不可能充满试管,项错误;
B.若原试管中含有的是一氧化氮和二氧化氮的混合气体,之前发生的反应是,通入氧气之后,可发生,气体恰好发生反应时,试管内完全被水充满,项正确;
C.是无色气体,不溶于水,不与水反应,当倒扣在盛有水的水槽中时,试管内水面不会上升,故C错误;
D.结合选项B可知,还可以是与的混合气体,故D错误。
故选B。
15.【答案】
【解析】
【分析】
考查常见气体的检验和性质,把握常见气体的化学性质及气体的溶解性是解题的关键。
【解答】
二氧化氮是红棕色的气体,所以无色混合气体甲中一定不存在二氧化氮二氧化碳可以和过氧化钠反应生成碳酸钠和氧气,反应的化学方程式为:,一氧化氮无色,与氧气立即反应变为红棕色的二氧化氮,通过足量的过氧化钠后气体显红棕色,说明有、,排水法收集气体, 仍有气体剩余,说明有,所以甲气体中一定无
故答案为。
16.【答案】生成的或氮的氧化物扩散到大气中,污染环境;生成的与空气相接触,被氧化成红棕色的气体;
检验气密性;将铜片插入溶液中或向左侧倾斜试管,使铜片浸在浓硝酸中;抽动铜片使其和溶液脱离接触;与水反应,气体体积减小,使导管内压强减小,气压差将水压入试管中;
【解析】略
17.【答案】检验装置的气密性 浓 转化成 排尽装置中的空气,防止与、发生反应 取适量中溶液放入试管中,加入稀硫酸后再加入铜片,若试管口有红棕色气体生成,则说明有生成,否则没有生成
【解析】
【分析】
本题是一道实验方案的设计和探究题,涉及反应原理分析,并熟练运用化学方程式或离子反应方程表示,对学生分析和解决问题的能力要求较高,综合性强,题目难度中等。
【解答】
实验开始前需要检验装置的气密性,关闭、,将导管未端置于盛水的水槽中,用酒精灯微热三颈烧瓶,水槽中有气泡产生,撤去酒精灯后导管中有一段倒吸的水柱,证明气密性良好;装置制备,发生反应的化学方程式为浓,
故答案为:检验装置的气密性;浓;
实验的目的是用与发生反应,则装置发生的反应是,装置的作用是将转化成;装置中的固体酸性干燥剂为,
故答案为:转化成;;
因为能与发生反应生成,加热状态下与生成,因此反应开始前通入一段时间的或,目的是排尽装置中的空气,防止与、发生反应,
故答案为:排尽装置中的空气,防止与、发生反应;
中铜粉变黑,说明铜与发生反应,生成和,装置中反应的化学方程式为;根据信息能与酸性高锰酸钾溶液发生反应,即装置的目的是除去未反应的,反应的化学方程式为;证明的存在,在酸性条件下具有强氧化性,方法是取适量中溶液放入试管中,加入稀硫酸后再加入铜片,若试管口有红棕色气体生成,则说明有生成,否则没有生成,
故答案为:;取适量中溶液放入试管中,加入稀硫酸后再加入铜片,若试管口有红棕色气体生成,则说明有生成,否则没有生成;
和先发生,然后发生,可以得到总反应式为,故气体需要,
故答案为:。
18.【答案】分液漏斗;
产生红棕色气体 蒸馏水中有气泡,生成无色气体
浓;;;
【解析】
【分析】
本题考查性质方案的设计,题目难度中等,明确氮元素及其化合物性质为解答关键,注意掌握守恒书写在化学计算中的应用,试题培养了学生的分析能力及综合应用能力。
【解答】
装置甲中盛放浓硝酸的仪器的名称是分液漏斗;
二氧化氮经导管进入丙装置和水反应生成硝酸和,该反应的离子方程式为:,
故答案为:分液漏斗; ;
铜和浓硝酸在装置甲中反应浓,生成红棕色的二氧化氮气体进入乙装置,所以装置乙中出现的现象为生成红棕色气体;二氧化氮经导管进入丙装置和水反应,所以装置丙中出现的现象蒸馏水中有气泡产生,生成无色气体,
故答案为:产生红棕色气体;蒸馏水中有气泡,生成无色气体;
、和水反应生成硝酸,化学方程式为:,
若剩余气体为,反应消耗的体积为:,则通入的体积;
若剩余气体为,完全反应,同时消耗的氧气的体积为:,则通入的体积为:,
根据分析可知,则通入的的在相同条件下体积可能为,
故答案为:;
开始时与浓硝酸反应生成二氧化氮,发生反应为:浓,随着反应的进行,浓硝酸浓度逐渐减小,当变为稀硝酸后,稀硝酸与反应生成气体;
若两者恰好完全反应整个反应过程共产生标准状况下气体,即生成和的混合气体,根据原子守恒,反应过程中被还原的的物质的量为;反应后生成硝酸铜中含有的物质的量为:,则参加反应的的物质的量为:,
故答案为:浓;;;;
与稀释反应生成硝酸铜,反应后溶液中氢离子消耗完毕,但硝酸根离子有剩余,若再加入少量的稀硫酸,相当于稀硝酸溶液,铜与稀硝酸反应生成硝酸铜、和水,发生反应的离子方程式为:,
故答案为:。
19.【答案】;
;
、;干燥氨气;
;
融化成小球;。
【解析】
【分析】
本题主要考查化学方程式的书写,难度不大,需要学生熟练掌握。
【解答】
空气中含量最多的气体是氮气,
,是氮气与氧气反应生成一氧化氮,是一氧化氮与氧气反应生成二氧化氮,是二氧化氮与水反应生成硝酸,
下列叙述中,正确的是
一氧化氮容易被空气氧化,不能用排空气法收集,故错误;
的基本反应类型为化合反应,故正确;
浓硝酸见光易分解,一般保存在棕色试剂瓶中,故正确;
故选;
二氧化氮与水反应的化学方程式为:,
故答案为:;
实验室制取氨气所需试剂为:、,装置的作用是干燥氨气,
故答案为:、;干燥氨气;
若、、、的焰色反应均为黄色,说明含有钠,为淡黄色固体,说明为过氧化钠,在加热条件下可直接转化为,说明是金属钠。
是过氧化钠与水反应,化学方程式是:,
故答案为:;
与水反应的实验现象中,能说明该反应放热、的熔点低的是:融化成小球,单质钠与水反应生成氢气,在标准状况下的体积为。
故答案为:融化成小球;。
第1页,共1页
一、单选题
1. 下列关于氮及其化合物的说法正确的是( )
A. 化学性质稳定,可用作保护气
B. 、均为大气污染气体,在大气中可稳定存在
C. 、均易溶于水
D. 、均能与水发生反应
2. 无色的混合气体甲,可能含、、、中的几种,将一定量的甲气体经过如图实验的处理,结果得到酸性溶液,而几乎无气体剩余,则甲气体的组成为( )
A. 、 B. 、 C. 、 D. 、、
3. 常温下,将盛有和的混合气体的试管倒立于水槽中并向其中通入,一段时间后,试管内还剩余气体,则通入的体积可能为 ( )
A. B. C. D.
4. 把体积的气体,依次通过下列个分别装有饱和溶液、浓硫酸、的装置后,用排水法把残留气体收集到集气瓶中,集气瓶内气体应是同温同压下测定( )
A. 体积 B. 体积和体积
C. 体积 D. 体积
5. 下列关于和的叙述正确的是 ( )
A. 都能溶于水且与水反应生成相应的酸 B. 都是酸性氧化物,都能与强碱溶液反应
C. 可以通过铜与硝酸制取 D. 常温下都可以被氧气氧化
6. 如图是某元素的价类二维图。其中为正盐,是一种强碱,通常条件下是无色液体,的相对分子质量比大,各物质的转化关系如图所示。下列说法正确的是
A. 是适合与草木灰混合施用的肥料 B. 和能发生复分解反应生成盐
C. 可用排空气法收集 D. 的反应可用于检验
7. 谚语“雷雨发庄稼”不包括下列哪个化学反应 反应条件已忽略
A. B.
C. D.
8. 如图所示是氨催化氧化制备硝酸的实验装置,下列有关叙述正确的是( )
A. 烧杯中的紫色石蕊溶液不变色
B. 圆底烧瓶中的气体一定为无色
C. 加热后,通过三氧化二铬的气体由无色变为红棕色
D. 三氧化二铬起氧化剂的作用
9. 按下图进行实验,试管内充满,然后间歇而缓慢地通入一定体积的,下面有关实验最终状态的描绘,不正确的是 ( )
A. 若最终有气体剩余,气体可能是 B. 若最终有气体剩余,气体呈红棕色
C. 试管内溶液为稀硝酸 D. 试管内液面高度肯定会上升
10. 某无色混合气体中可能含、、、、中的几种。将混合气体经过如图所示的处理后,几乎无气体剩余,则下列说法正确的是
A. 混合气体中一定含有、、 B. 混合气体中可能含有
C. 混合气体中的体积分数为 D. 混合气体中的体积分数最大
11. 某混合气体中可能含有、、、、中的两种或多种气体,现将此无色透明的混合气体通过品红溶液后,品红溶液褪色,把剩余气体排入空气中,很快变为红棕色。下列对于原混合气体成分的判断中正确的是( )
A. 肯定有和 B. 肯定有
C. 可能有和 D. 可能有、、三种气体
12. 下列实验操作一定能达到相应实验目的是
实验目的 实验操作
验证 向与混合液中加入适量溶液
证明的酸性强于 向溶液中通入少量
鉴别乙酸乙酯和乙酸 分别加入饱和溶液
验证中是否含有 向混合气体中通入观察颜色是否加深
A. B. C. D.
13. 汽车尾气含、、、、等是城市空气的污染源之一、储存还原技术可有效降低柴油发动机在空气过量条件下的排放。如图所示的储存和还原在不同时段交替进行,通过和的相互转化实现的储存和还原。下列叙述中错误的是( )
A. 汽车尾气对环境的危害主要有温室效应、雾霾、酸雨、光化学烟雾等
B. 储存时,部分发生反应:,作该变化的催化剂
C. 储存的物质是
D. 还原性尾气与生成的反应是
14. 如图所示,试管中盛装的是红棕色气体,当倒扣在盛有水的水槽中时,试管内水面上升,但不能充满试管,当向试管内鼓入氧气后,可以观察到试管中水柱继续上升,经过多次重复后,试管内完全被水充满,对原试管中盛装气体的说法正确的是( )
A. 可能是与的混合气体 B. 可能是与的混合气体
C. 只可能是气体 D. 只可能是一种气体
15. 无色的混合气体甲,可能含、、、中的几种,将一定量的甲气体经过如图实验处理,结果得到酸性溶液,仍有气体剩余,则甲气体不可能含有
A. B. C. D.
二、实验题
16. 装置Ⅰ和装置Ⅱ是有关硝酸和铜反应的实验装置示意图。
若用装置Ⅰ进行铜与浓硝酸反应的实验,最大的缺点是__________________________。若用装置Ⅰ来证明铜与稀硝酸反应生成气体,其最大缺点是不能与浓硝酸跟铜反应形成鲜明对照,简述原因:_____________________________________________________________________________________________________________________________________________________________。
若用装置Ⅱ进行适当操作,即可克服上述缺点,还能使上述两反应在同一试管中先后连续进行,实验步骤如下。
步骤一:组装好装置并________________后,加入浓硝酸铜片接近酸液,塞紧胶塞。
步骤二:________________________操作使反应发生。当导管口有少量红棕色气体逸出时,________________________操作使反应停止。同时将导管插入水中。稍后能观察到水沿导管倒吸至试管中,产生此现象的原因是________________________。还可能观察到的明显现象是________填标号。
溶液由蓝色变为无色 红棕色气体变为无色
17. 某研究性学习小组的同学通过查阅资料知,可与炽热的铜粉发生反应,他们设计如图装置夹持装置已略去进行实验验证。
已知:能被酸性高锰酸钾溶液氧化生成。
请回答下列问题:
实验开始前,应进行的一步操作是 ______;装置中发生反应的化学方程式为 ______。
装置的作用为 ______;装置中所用的酸性干燥剂的化学式是 ______。
装置中反应开始前,需要先打开,向装置中通入一段时间的或,其目的是 ______。
实验过程中,装置中铜粉变黑,装置中溶液颜色变浅,则装置中发生反应的化学方程式为 ______;请设计一种简单的实验方案,证明实验中装置中有生成 ______写出主要的操作过程、现象、结论。
假设实验结束后,从装置中收集到,气体,为使全部被水吸收,应向集气瓶内通入 ______。
三、简答题
18. 氮及其化合物与生产生活关系密切。请完成下列填空:
某学校化学学习小组为探究二氧化氮的性质,按下图所示装置进行实验。
装置甲中盛放浓硝酸的仪器的名称是______,装置丙中的试管内发生反应的离子方程式为:______。
实验过程中装置乙、丙中出现的现象分别是______;______。
在医疗上有重要的应用,曾被科学家作为研究的重要物质。现有容积为的试管盛满后倒扣于水槽中,再向试管中通入一定体积后,试管内气体的体积为试管容积的一半,则通入的的在相同条件下体积为______。
A.
在盛有一定量浓硝酸的试管中加入的铜片发生反应。请回答下列问题:
开始阶段,反应的化学方程式为______,后一阶段生成的气体为______,若两者恰好完全反应整个反应过程共产生标准状况下气体,则反应过程中被还原的的物质的量为______ ,参加反应的的物质的量为______ 。
反应结束后往试管中加入铜片,再加入少量的稀硫酸,这时铜片上又有气泡产生,反应的离子方程式为______。
19. A、、、是中学化学中的常见物质,其中为单质。各物质的转化关系如下:
若是空气中含量最多的气体。
下列叙述中,正确的是___填字母。
可用向上排空气法收集 的基本反应类型为化合反应
的浓溶液见光易分解,一般保存在棕色试剂瓶中
写出与水反应的化学方程式_____________________________
实验室制取的最简单氢化物装置如图所示,回答下列问题
试管中的试剂为_________________;装置的作用是___________。
若、、、的焰色反应均为黄色,为淡黄色固体,在加热条件下可直接转化为。
的化学方程式是_______________________________________
、、均能与水发生反应。与水反应的实验现象中,能说明该反应放热、的熔点低的是___。若单质与水反应。产生的气体在标准状况下的体积为_______.
答案和解析
1.【答案】
【解析】
【分析】
本题主要考查氮及其化合物的相关性质,题目难度中等,注意不同物质之间性质的差别。
【解答】
A.氮气的化学性质稳定,很难发生化学反应,通常作保护气,故A正确;
B.、均是污染性气体,和氧气能反应生成二氧化氮,不能在大气中稳定存在,故B错误;
C.一氧化氮难溶于水,故C错误;
D.一氧化氮难溶于水,也不能与水反应,故D错误。
故选A。
2.【答案】
【解析】解:二氧化氮是红棕色的气体,所以无色混合气体甲中一定不存在二氧化氮;
二氧化碳可以和过氧化钠反应生成碳酸钠和氧气,反应的化学方程式为:,
一氧化氮无色,与氧气立即反应变为红棕色的二氧化氮,通过足量的过氧化钠后气体显红棕色,说明有、,排水法收集气体,广口瓶被上升的水注满,说明没有,所以甲气体的组成为:、;
故选:。
二氧化氮是红棕色的气体,浓硫酸可以和氨气反应,二氧化碳可以和过氧化钠反应生成氢氧化钠和氧气,一氧化氮无色,与氧气立即反应变为红棕色的二氧化氮,氮气不溶于水,将一定量的甲气体经过如图实验的处理,结果得到酸性溶液,而几乎无气体剩余,说明无氮气,据此分析解答.
本题考查常见气体的检验和性质,把握常见气体的化学性质及气体的溶解性是解题的关键,注意二氧化碳和过氧化钠的反应,题目难度不大.
3.【答案】
【解析】
【分析】
本题考查了有关混合物反应的化学计算,题目难度中等,明确反应后剩余气体组成为解答关键,注意掌握、二氧化氮与氧气、水转化成硝酸的反应原理,要求学生掌握讨论法在化学计算中的应用。
【解答】剩余的气体可能为氧气,有可能为,当剩余的气体为氧气时,二氧化氮和完全反应,可以根据方程式、计算出通入氧气的总体积;
当剩余的气体为时,可以看作二氧化氮完全反应,反应消耗了,还剩余,然后根据反应方程式计算出消耗的氧气的体积。
当剩下的气体为时,和 说明完全反应生成硝酸,则:
,
,
所以通入的氧气体积为:;
当剩余的气体为时,可以认为 完全反应生成硝酸,中剩余,有转化成硝酸,则:
,
,
所以通入氧气的体积为:,
故选:。
4.【答案】
【解析】体积通入溶液中发生反应:,,经过浓硫酸干燥得到体积和体积气体。再通过发生反应为:生成体积氧气,然后,此时剩余体积和体积。通过水发生反应:,故剩余体积氧气。
5.【答案】
【解析】
【分析】
本题考查了和的性质,试题较为基础,难度不大,注意相关知识的积累即可解答。
【解答】
A.能溶于水,与水反应生成和;既不溶于水,也不与水反应,A错误;
B.和都不是酸性氧化物,B错误;
C.可以通过铜与浓硝酸制取,铜与稀硝酸制取,C正确;
D.常温下可以被氧气氧化,不可以,D错误;
故选C。
6.【答案】
【解析】
【分析】
本题以元素化合物的推断为载体考查了元素化合物的性质,通过元素化合物的推断考查学生的推理、分析、判断等能力,正确推断元素化合物是解本题的关键。
【解答】
为正盐,是一种强碱,与生成,为氢化物,铵盐与强碱反应生成,为,的相对分子质量比的相对分子质量大,说明和反应,、是氧化物,分子式相差一个氧原子;又是酸,说明是,被氧气氧化生成单质,氮气被氧气氧化生成,为,被氧气氧化生成,为,与水反应生成硝酸,为硝酸,硝酸与强碱反应生成硝酸盐。据此解答。
A.铵盐属于铵态氮肥,草木灰中含属钾肥,但溶于水显碱性,两者混合会互促水解,释放出,降低肥效,故A错误;
B.氨气与硝酸可以发生化合反应生成硝酸铵,故B错误;
C.为氮气,其密度与空气接近,不可用排空气法收集,可以排水法收集,故C错误;
D.为无色气体,易与氧气反应,将与空气接触,有红棕色气体生成,如观察到红棕色,则说明生成,故D正确。
故选D。
7.【答案】
【解析】
【分析】
本题主要考查了雷雨肥田原理,氮气、一氧化氮、二氧化氮的化学性质,理解反应原理、正确书写化学方程式是解答的关键,题目难度不大。
【解答】
“雷雨发庄稼”,空气中的在放电条件下与直接化合生成无色且不溶于水的一氧化氮气体:;一氧化氮常温下易与空气中的反应生成红棕色的二氧化氮气体:;二氧化氮与水反应生成硝酸和一氧化氮:,生成的硝酸随雨水淋洒到大地上,同土壤中的矿物相互作用,生成可溶于水的硝酸盐可作氮肥,植物生长得更好。“雷雨发庄稼”不包括氮气和氢气合成氨的反应,故B符合题意。
故选B。
8.【答案】
【解析】
【分析】
本题考查硝酸的制备实验评价,为高频考点,把握实验装置的作用、物质的性质及发生的反应为解答的关键,侧重分析与实验能力的考查,题目难度不大。
【解答】
由实验装置可知,氨气被碱石灰干燥后,在大试管中氨气与氧气反应生成,圆底烧瓶中被氧化生成红棕色,与水反生成硝酸,
A.硝酸遇石蕊变红,则烧杯中的紫色石蕊溶液变红,故A错误
B.圆底烧瓶中的气体可能为红棕色,故B错误
C.加热后,通过三氧化二铬的催化作用生成无色,被氧化生成红棕色的气体,故C正确;
D.氨气与氧气在三氧化二铬的催化作用反应生成和水,故D错误
故选C。
9.【答案】
【解析】解:若氧气不足,最终有气体剩余,气体可能是,故A正确;
B.二氧化氮与水反应,最终剩余气体不可能为红棕色,故B错误;
C.反应生成硝酸,试管内溶液为稀硝酸,故C正确;
D.生成硝酸易溶于水,试管内液面高度肯定会上升,故D正确;
故选:。
试管内装有,然后间歇而缓慢地通入,当一氧化氮和氧气恰好反应生成硝酸时发生,溶液充满试管,以此来解答。
本题考查物质的性质,为高频考点,把握物质的性质、反应与现象为解答的关键,侧重分析与应用能力的考查,注意元素化合物知识的应用,题目难度不大。
10.【答案】
【解析】
【分析】
本题考查常见气体的检验和性质,是一道气体的鉴别题目,注意氨气的碱性、注意二氧化碳和过氧化钠的反应,题目难度不大。
【解答】
二氧化氮是红棕色的气体,所以混合气体甲中一定不存在,硫酸和碱性气体能反应,所以甲气体经过足量的浓硫酸,溢出剩余气体,说明一定有且存在体积为,的体积分数为,二氧化碳可以和过氧化钠反应生成碳酸钠和氧气,反应的化学方程式为:,与甲气体的组成无关,一氧化氮无色,与氧气立即反应变为红棕色的二氧化氮,通过足量的过氧化钠后气体显红棕色,说明有、,排水法收集气体,广口瓶被上升的水注满,说明与的体积比为:。
A.甲中气体有、、,故A正确;
B.混合气体中不含有,故B错误;
C.甲中的体积分数,故C错误;
D.由方程式,,最后无气体剩余可知与的体积比为:,则的体积分数不是最大,故D错误。
故选A。
11.【答案】
【解析】
【分析】
本题考查混合气体组成的推断,意在考查学生的分析推理能力,解题关键是掌握氯气、二氧化硫、氮氧化物的性质。
【解答】
该气体无色,排除了、气体;该气体能使品红溶液褪色,则一定含有气体;将剩余气体排放到空气中,气体迅速变为红棕色,判断一定含有气体,则一定无,一定含有的气体是、,一定没有的气体为、、,故A正确。
12.【答案】
【解析】A.与反应生成沉淀,不能比较、的大小,故A错误;
B.溶液中通入少量,发生氧化还原反应生成硫酸钙,则不能比较、的酸性强弱,故B错误;
C.乙酸与饱和碳酸钠溶液反应有气泡产生,与乙酸乙酯分层,现象不同,可鉴别,故C正确;
D.与氧气反应生成二氧化氮气体,红棕色变化不明显,不能验证中是否含有,故D错误;
本题考查化学实验方案的评价,为高频考点,把握物质的性质、难溶电解质、物质的鉴别、实验技能为解答的关键,侧重分析与实验能力的考查,注意元素化合物知识的应用,题目难度不大。
13.【答案】
【解析】
【分析】
略
【解答】
A.汽车尾气含、、等,会造成温室效应,灰尘会造成雾霾,、在空气中生成硫酸,导致酸雨产生,造成光化学烟雾,故A正确;
B.储存时,一氧化氮和氧气反应生成了二氧化氮,反应:,作该变化的催化剂,故B正确;
C.储存时,氧化钡、一氧化氮和氧气反应生成了硝酸钡,所以储存时,吸收 如 ,的物质是,故C错误;
D.还原时,发生的反应是一氧化碳和硝酸钡反应生成氮气、氧化钡和二氧化碳,化学方程式为:,故D正确;
故选:。
14.【答案】
【解析】
【分析】
本题考查氮氧化物、氧气于水反应的分析,难度不大,注意题目中的“只”、“仅”、“可能”、“都”等关键词的含义,是做出正确判断的关键。
【解答】
A.氮气不溶于水,且其与氧气在常温常压下不反应,所以水最终不可能充满试管,项错误;
B.若原试管中含有的是一氧化氮和二氧化氮的混合气体,之前发生的反应是,通入氧气之后,可发生,气体恰好发生反应时,试管内完全被水充满,项正确;
C.是无色气体,不溶于水,不与水反应,当倒扣在盛有水的水槽中时,试管内水面不会上升,故C错误;
D.结合选项B可知,还可以是与的混合气体,故D错误。
故选B。
15.【答案】
【解析】
【分析】
考查常见气体的检验和性质,把握常见气体的化学性质及气体的溶解性是解题的关键。
【解答】
二氧化氮是红棕色的气体,所以无色混合气体甲中一定不存在二氧化氮二氧化碳可以和过氧化钠反应生成碳酸钠和氧气,反应的化学方程式为:,一氧化氮无色,与氧气立即反应变为红棕色的二氧化氮,通过足量的过氧化钠后气体显红棕色,说明有、,排水法收集气体, 仍有气体剩余,说明有,所以甲气体中一定无
故答案为。
16.【答案】生成的或氮的氧化物扩散到大气中,污染环境;生成的与空气相接触,被氧化成红棕色的气体;
检验气密性;将铜片插入溶液中或向左侧倾斜试管,使铜片浸在浓硝酸中;抽动铜片使其和溶液脱离接触;与水反应,气体体积减小,使导管内压强减小,气压差将水压入试管中;
【解析】略
17.【答案】检验装置的气密性 浓 转化成 排尽装置中的空气,防止与、发生反应 取适量中溶液放入试管中,加入稀硫酸后再加入铜片,若试管口有红棕色气体生成,则说明有生成,否则没有生成
【解析】
【分析】
本题是一道实验方案的设计和探究题,涉及反应原理分析,并熟练运用化学方程式或离子反应方程表示,对学生分析和解决问题的能力要求较高,综合性强,题目难度中等。
【解答】
实验开始前需要检验装置的气密性,关闭、,将导管未端置于盛水的水槽中,用酒精灯微热三颈烧瓶,水槽中有气泡产生,撤去酒精灯后导管中有一段倒吸的水柱,证明气密性良好;装置制备,发生反应的化学方程式为浓,
故答案为:检验装置的气密性;浓;
实验的目的是用与发生反应,则装置发生的反应是,装置的作用是将转化成;装置中的固体酸性干燥剂为,
故答案为:转化成;;
因为能与发生反应生成,加热状态下与生成,因此反应开始前通入一段时间的或,目的是排尽装置中的空气,防止与、发生反应,
故答案为:排尽装置中的空气,防止与、发生反应;
中铜粉变黑,说明铜与发生反应,生成和,装置中反应的化学方程式为;根据信息能与酸性高锰酸钾溶液发生反应,即装置的目的是除去未反应的,反应的化学方程式为;证明的存在,在酸性条件下具有强氧化性,方法是取适量中溶液放入试管中,加入稀硫酸后再加入铜片,若试管口有红棕色气体生成,则说明有生成,否则没有生成,
故答案为:;取适量中溶液放入试管中,加入稀硫酸后再加入铜片,若试管口有红棕色气体生成,则说明有生成,否则没有生成;
和先发生,然后发生,可以得到总反应式为,故气体需要,
故答案为:。
18.【答案】分液漏斗;
产生红棕色气体 蒸馏水中有气泡,生成无色气体
浓;;;
【解析】
【分析】
本题考查性质方案的设计,题目难度中等,明确氮元素及其化合物性质为解答关键,注意掌握守恒书写在化学计算中的应用,试题培养了学生的分析能力及综合应用能力。
【解答】
装置甲中盛放浓硝酸的仪器的名称是分液漏斗;
二氧化氮经导管进入丙装置和水反应生成硝酸和,该反应的离子方程式为:,
故答案为:分液漏斗; ;
铜和浓硝酸在装置甲中反应浓,生成红棕色的二氧化氮气体进入乙装置,所以装置乙中出现的现象为生成红棕色气体;二氧化氮经导管进入丙装置和水反应,所以装置丙中出现的现象蒸馏水中有气泡产生,生成无色气体,
故答案为:产生红棕色气体;蒸馏水中有气泡,生成无色气体;
、和水反应生成硝酸,化学方程式为:,
若剩余气体为,反应消耗的体积为:,则通入的体积;
若剩余气体为,完全反应,同时消耗的氧气的体积为:,则通入的体积为:,
根据分析可知,则通入的的在相同条件下体积可能为,
故答案为:;
开始时与浓硝酸反应生成二氧化氮,发生反应为:浓,随着反应的进行,浓硝酸浓度逐渐减小,当变为稀硝酸后,稀硝酸与反应生成气体;
若两者恰好完全反应整个反应过程共产生标准状况下气体,即生成和的混合气体,根据原子守恒,反应过程中被还原的的物质的量为;反应后生成硝酸铜中含有的物质的量为:,则参加反应的的物质的量为:,
故答案为:浓;;;;
与稀释反应生成硝酸铜,反应后溶液中氢离子消耗完毕,但硝酸根离子有剩余,若再加入少量的稀硫酸,相当于稀硝酸溶液,铜与稀硝酸反应生成硝酸铜、和水,发生反应的离子方程式为:,
故答案为:。
19.【答案】;
;
、;干燥氨气;
;
融化成小球;。
【解析】
【分析】
本题主要考查化学方程式的书写,难度不大,需要学生熟练掌握。
【解答】
空气中含量最多的气体是氮气,
,是氮气与氧气反应生成一氧化氮,是一氧化氮与氧气反应生成二氧化氮,是二氧化氮与水反应生成硝酸,
下列叙述中,正确的是
一氧化氮容易被空气氧化,不能用排空气法收集,故错误;
的基本反应类型为化合反应,故正确;
浓硝酸见光易分解,一般保存在棕色试剂瓶中,故正确;
故选;
二氧化氮与水反应的化学方程式为:,
故答案为:;
实验室制取氨气所需试剂为:、,装置的作用是干燥氨气,
故答案为:、;干燥氨气;
若、、、的焰色反应均为黄色,说明含有钠,为淡黄色固体,说明为过氧化钠,在加热条件下可直接转化为,说明是金属钠。
是过氧化钠与水反应,化学方程式是:,
故答案为:;
与水反应的实验现象中,能说明该反应放热、的熔点低的是:融化成小球,单质钠与水反应生成氢气,在标准状况下的体积为。
故答案为:融化成小球;。
第1页,共1页
