第3章有机合成及其应用合成高分子化合物单元测试卷高二下学期化学鲁科版(2019)选择性必修3(含解析)
文档属性
| 名称 | 第3章有机合成及其应用合成高分子化合物单元测试卷高二下学期化学鲁科版(2019)选择性必修3(含解析) |

|
|
| 格式 | docx | ||
| 文件大小 | 1.3MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-06-18 00:00:00 | ||
图片预览




文档简介
第3章《有机合成及其应用 合成高分子化合物》单元测试卷
一、单选题
1.下列说法不正确的是
A.光谱分析就是利用原子光谱上的特征谱线来鉴定元素
B.用红热的铁针刺涂有石蜡的水晶柱面,熔化的石蜡呈圆形
C.手性催化剂只催化或者主要催化一种手性分子的合成,而不得到它的手性异构分子。
D.过渡金属离子对多种配体具有很强的结合力,因而,过渡金属配合物远比主族金属配合物多
2.在核磁共振氢谱中出现两组峰,其氢原子数之比为1:1的化合物是
A.CH3CH2CH3 B.
C.CH3—O—CH3 D.
3.下列说法不正确的是
A.通过红外光谱分析可以区分丁醛和乙酸乙酯
B.可利用原子光谱上的特征谱线来鉴定元素
C.的核磁共振氢谱中有5组峰
D.对乙醇和二甲醚进行质谱分析,质谱图完全相同
4.下列有机物中,一氯取代物有2种的是( )
①;②;③;④
A.①③ B.②③ C.①④ D.②④
5.下列芳香烃的一氯取代物的同分异构体数目最多的是
A.连二苯
B.菲
C.蒽
D.连三苯
6.化学与生活密切相关,下列叙述正确的是
A.糖类、油脂、蛋白质是人体基本营养物质,均属于高分子
B.乙醇汽油是一种新型化合物
C.向牛奶中加入白醋会产生沉淀,这是因为发生了酸碱中和反应
D.氢氟酸可用于蚀刻玻璃、石英制品
7.茉莉醛具有浓郁的茉莉花香,其结构简式如图,关于茉莉醛的说法正确的是
A.茉莉醛与苯甲醛互为同系物
B.1mol茉莉醛与足量银氨溶液反应,生成1mol银单质
C.茉莉醛使酸性高锰酸钾溶液褪色证明茉莉醛分子中含有碳碳双键
D.在一定条件下能与苯酚发生缩聚反应生成高分子化合物
8.叶蝉散对水稻叶蝉和飞虱具有较强的触杀作用,防效迅速,但残效不长。工业上用邻异丙基苯酚合成叶蝉散的过程如下:
下列有关说法正确的是
A.叶蝉散的分子式是 B.叶蝉散分子中含有羧基
C.叶蝉散的核磁共振氢谱有8组吸收峰 D.邻异丙基苯酚与互为同系物
9.某酯类化合物a的分子式为C35H50O6,1 mol该酯类化合物a完全水解可得到1 mol甘油、2 mol不饱和脂肪酸b和1 mol直链饱和脂肪酸c,经测定c的相对分子质量为228,则不饱和脂肪酸b的分子式为
A.C9H10O2 B.C9H12O2
C.C9H16O2 D.C9H17O2
10.新版人民币的发行,引发了人们对有关人民币中化学知识的关注。下列表述不正确的是
A.制造人民币所用的棉花、优质针叶木等原料的主要成分是纤维素
B.用于人民币票面文字等处的油墨中所含有的Fe2O3是一种磁性物质
C.防伪荧光油墨由颜料与树脂等制成,其中树脂属于有机高分子材料
D.某种验钞笔中含有碘酒溶液,遇假钞呈现蓝色,其中遇碘变蓝的是淀粉
11.某高分子化合物的结构简式如图。下列叙述错误的是
A.聚合度为n B.单体为
C.链节为 D.该高分子化合物是混合物
12.3- O-咖啡酰奎尼酸是金银花抗菌、抗病毒的有效成分之一,其分子结构如下图。下列关于3 -O-咖啡酰奎尼酸的说法不正确的是
A.存在顺反异构现象
B.能发生取代反应和消去反应
C.1 mol 3- O-咖啡酰奎尼酸与足量的金属钠反应,可产生2.5mol H2
D.1 mol 3 -O咖啡酰奎尼酸与足量溴水反应,最多消耗3 mol Br2
13.下列各组有机化合物中,不论三者以什么比例混合,只要总物质的量一定,则完全燃烧时消耗氧气的质量不变的是
A.,, B.,,
C.,, D.,,
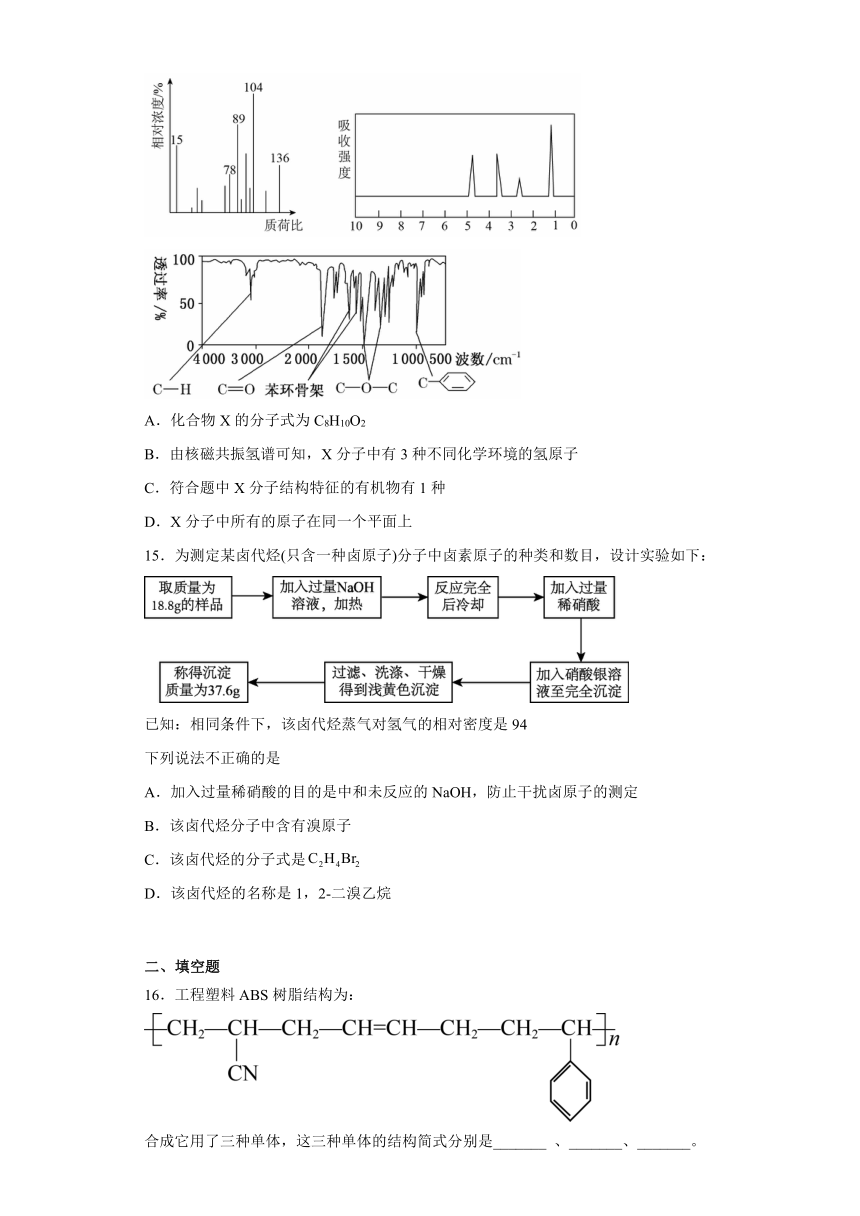
14.将6.8g的X完全燃烧生成3.6g的H2O和8.96L(标准状况)的CO2,X的核磁共振氢谱有4个峰且面积之比为3:2:2:1。X分子中只含一个苯环且苯环上只有一个取代基,其质谱图、核磁共振氢谱与红外光谱如图,关于X的下列叙述正确的是
A.化合物X的分子式为C8H10O2
B.由核磁共振氢谱可知,X分子中有3种不同化学环境的氢原子
C.符合题中X分子结构特征的有机物有1种
D.X分子中所有的原子在同一个平面上
15.为测定某卤代烃(只含一种卤原子)分子中卤素原子的种类和数目,设计实验如下:
已知:相同条件下,该卤代烃蒸气对氢气的相对密度是94
下列说法不正确的是
A.加入过量稀硝酸的目的是中和未反应的NaOH,防止干扰卤原子的测定
B.该卤代烃分子中含有溴原子
C.该卤代烃的分子式是
D.该卤代烃的名称是1,2-二溴乙烷
二、填空题
16.工程塑料ABS树脂结构为:
合成它用了三种单体,这三种单体的结构简式分别是_______ 、_______、_______。
17.合成路线流程图示例如下:
请设计合理方案,以甲苯为主要原料,其他物质可根据需要自主选择,合成局部麻醉剂氯普鲁卡因盐酸盐的中间体。________
18.按要求答题
(1)CH3C(CH3)2CH2CH3的命名:_______;
(2)10mL某气态烷烃,在50mLO2中充分燃烧,得到液态水以及体积为35mL的混合气体(气体体积均在相同条件下测定)。该气态烷烃的分子式是_______;
(3)将丙烯(CH3CH=CH2)通入溴的四氯化碳溶液中,发生的化学方程式为_______,该反应的反应类型是_______;
(4)写出丙烯在一定条件下发生加聚反应的化学方程式_______;
(5)现有CH4、C2H4、C2H6、C4H8四种烃:
①若其中两种烃无论以何种比例混合,只要总物质的量一定,燃烧生成的CO2的物质的量就一定,则这两种烃是_______;
②若其中两种烃无论以何种比例混合,只要总质量一定,消耗氧气的质量就一定,则这两种烃是_______;
(6)乙烷与一定量氯气光照条件下反应,生成的产物有_______种。
三、实验题
19.利用下列实验药品进行实验,能顺利达到实验目的的是
实验目的 实验药品
A 证明乙炔能和反应 电石、饱和食盐水、溶液和溴水
B 提纯苯的溴代反应中溴苯 苯、液溴、Fe粉、水
C 检验溴乙烷中的溴原子 溴乙烷、溶液和溶液
D 验证乙醇消去产物有乙烯 乙醇、浓硫酸和溴水
A.A B.B C.C D.D
20.实验表明,当乙醛加入到溴水中,溴水会褪色。针对此现象,某小组同学依据乙醛结构进行探究。
【实验假设】
(1)假设Ⅰ:醛基含有不饱和键,可与发生_________反应(填反应类型)。
假设Ⅱ:乙醛具有α-H,可与溴水发生取代反应。一元取代反应如下:
无论是几元取代,参加反应的与生成的HBr物质的量之比为_________。
假设Ⅲ:乙醛具有较强的还原性,可被溴水氧化为乙酸,补全下面反应方程式。
_________
【实验过程】针对以上假设,该小组同学设计了两组方案。
方案Ⅰ:通过对比反应现象判断反应类型。
序号 操作 现象
试管1 1mL溴水+1mL乙醛,充分振荡后静置 褪色
试管2 1mL溴的溶液+1mL乙醛,充分振荡后静置 ____
结论:假设Ⅰ不成立。
(2)试管2中的实验现象为__________。
方案Ⅱ:通过测定反应后混合液的pH判断反应类型。
序号 操作 pH
试管1 加入20mL溴水,再加入10mL苯酚溶液,待完全反应后(苯酚过量),测定混合液pH 1.85[]
试管2 加入20mL相同浓度的溴水,再加入10mL 20%的乙醛溶液(乙醛过量),3min后完全褪色,测定混合液pH ____________
注:苯酚和乙酸的电离及温度变化对混合液pH的影响可忽略。
(3)写出苯酚与溴水反应的化学方程式:____________________________________。
(4)若试管2中反应后混合液的pH=1.85,则证明乙醛与溴水的反应类型为______反应;若pH接近______,则证明为氧化反应(lg2≈0.3);若pH介于两者之间,则证明两种反应类型皆有。
【实验结论与反思】
(5)根据实验数据得出结论:乙醛与溴水发生氧化反应。查阅资料,乙醛并非直接与发生反应,而是与次溴酸(HBrO)反应,从平衡移动的角度解释乙醛使溴水褪色的原因:______________。
(6)已知柠檬醛的结构如图,结合上述实验,检验柠檬醛分子中存在碳碳双键的合理方法为 (填字母序号)。
A.向酸性高锰酸钾溶液中加适量柠檬醛,观察其是否褪色
B.向溴水中加适量柠檬醛,观察其是否褪色
C.向溴的溶液中加适量柠檬醛,观察其是否褪色
D.向新制氢氧化铜悬浊液中加适量柠檬醛,加热,冷却后取上层清液再加溴水,观察其是否褪色
21.酯类是工业上重要的有机原料,具有广泛用途。乙酸苯甲酯对花香和果香的香韵具有提升作用,故常用于化妆品和食品工业。乙酸苯甲酯的合成路线如下:
已知:R-ClR-OH,R-为烃基
(1)乙酸苯甲酯的分子式是________,B所含官能团的名称是________。
(2)写出反应③的化学反应方程式:________。反应①的反应类型是__________,反应③的反应类型是________________。
(3)下列转化中________(填序号)原子的理论利用率为100%,符合绿色化学的要求。
A.乙醇制取乙醛 B.由制备 C.2CH3CHO+O22A
(4)提纯乙酸苯甲酯的有关实验步骤如下:将反应液冷至室温后倒入分液漏斗中,分别用饱和碳酸钠溶液和水洗涤,分出的产物加入少量无水MgSO4固体,静置片刻,过滤除去MgSO4固体,进行蒸馏,收集馏分,得到乙酸苯甲酯。
回答下列问题:
①在洗涤、分液操作中。应充分振荡,然后静置,待分层后________(填标号)。
a.直接将乙酸苯甲酯从分液漏斗上口倒出
b.直按将乙酸苯甲酯从分液漏斗下口放出
c.先将水层从分液漏斗的下口放出,再将乙酸苯甲酯从下口放出
d.先将水层从分液漏斗的下口放出,再将乙酸苯甲酯从上口放出
②实验中加入少量无水MgSO4的目的是__________________。
③在蒸馏操作中,仪器选择及安装都正确的是____________(填标号)。
(注:箭头方向表示水流方向)
参考答案:
1.B
【来源】辽宁省沈阳市第二中学2021-2022学年高二上学期期末考试化学试题
【详解】A.不同元素原子的吸收光谱或发射光谱不同,常利用原子光谱上的特征谱线来鉴定元素,故A正确;
B.晶体具有各向异性,所以用红热的铁针刺涂有石蜡的水晶柱面,熔化的石蜡呈椭圆形,故B错误;
C.在手性催化中,潜手性化合物在反应过程中会与手性催化剂形成一种最稳定的过渡态,从而只会诱导出一种手性分子,所以利用手性催化剂合成主要(或只)得到一种手性分子,而不得到它的手性异构分子,故C正确;
D.由于许多过渡元素金属离子对多种配体具有很强的结合力,能形成种类繁多的配合物,所以过渡金属配合物远比主族金属的配合物多,故D正确;
答案选B。
2.D
【来源】宁夏平罗中学2021-2022学年高二上学期第一次月考化学试题
【详解】A.CH3CH2CH3有2种等效氢,其氢原子数之比为3:1,核磁共振氢谱中出现两组峰,故不选A;
B.有3种等效氢,其氢原子数之比为3:3:2,核磁共振氢谱中出现三组峰,故不选B;
C.CH3—O—CH3有1种等效氢,核磁共振氢谱中出现一组峰,故不选C;
D. 有2种等效氢,其氢原子数之比为1:1,核磁共振氢谱中出现两组峰,故选D;
故答案选D。
3.D
【来源】浙江省衢州市2021-2022学年高二下学期6月教学质量检测化学试题
【详解】A.红外光谱仪可确定有机物中官能团及化学键,丁醛含醛基,乙酸乙酯含酯基,则红外光谱仪可以区分丁醛和乙酸乙酯,故A正确;
B.不同元素原子的吸收光谱或发射光谱不同,常利用原子光谱上的特征谱线来鉴定元素,故B正确;
C.有5种H原子,则核磁共振氢谱中有5组峰,故C正确;
D.乙醇和二甲醚结构不同,最大荷比相同,则质谱图不完全相同,故D错误;
故选:D。
4.B
【来源】吉林省田家炳高中、东辽二高等五校2021-2022学年高一下学期期末考试化学试题
【详解】根据有机物的等效氢有几种,其一氯取代物就有几种:
①有3种等效氢,则其一氯取代物有3种,不符合题意;
②有2种等效氢,则其一氯取代物有2种,符合题意;
③有2种等效氢,则其一氯取代物有2种,符合题意;
④有1种等效氢,则其一氯取代物有1种,不符合题意;
故答案为B。
5.B
【来源】2015-2016学年福建省八县一中高二下学期期末化学试卷(带解析)
【详解】A.连二苯,有两条对称轴和1个对称中心,有3种氢原子,一氯代物数目为3;
B.菲,有一条对称轴,有5种氢原子,一氯代物数目为5;
C.蒽两条对称轴和1个对称中心,有3种氢原子,一氯代物数目为3 ;
D.连三苯,有两条对称轴和1个对称中心,有4种氢原子,一氯代物数目为4;
故选B。
6.D
【来源】湖南师范大学附属中学2022-2023学年高三上学期月考卷(六)化学试题
【详解】A.油脂不属于高分子化合物,A错误;
B.乙醇汽油是一种混合物,B错误;
C.牛奶中含有蛋白质,加入果汁使蛋白质凝聚而沉淀,不是发生了酸碱中和反应,C错误;
D.氢氟酸可与SiO2反应生成SiF4气体和H2O,因此可利用氢氟酸刻蚀玻璃、石英制品,D正确;
故选D。
7.D
【来源】山东省日照市2021-2022学年高二下学期期末考试化学试题
【详解】A.由茉莉醛结构可知,其含有碳碳双键和醛基,而苯甲醛只含有醛基,二者官能团不相同,故不互为同系物,故A错误;
B.1mol茉莉醛含有1mol的醛基,与足量银氨溶液反应生成2mol银单质,故B错误;
C.茉莉醛含有的碳碳双键和醛基均能使酸性高锰酸钾溶液褪色,不能证明茉莉醛分子中含有碳碳双键,故C错误;
D.茉莉醛含有醛基,在一定条件下能与苯酚发生缩聚反应,生成高分子化合物,故D正确;
故答案选D。
8.C
【来源】第一~二节综合拔高练
【详解】A.根据叶蝉散的结构简式可得其分子式是,A错误;
B.由叶蝉散的分子结构可知叶蝉散中不含有,B错误;
C.由叶蝉散的结构简式可知,叶蝉散分子中含有8种不同化学环境的氢原子,则叶蝉散的核磁共振氢谱有8组吸收峰,C正确;
D.邻异丙基苯酚属于酚,属于醇,二者类别不同,则邻异丙基苯酚与不互为同系物,D错误;
综上,本题选C。
9.A
【来源】江西省宜春市铜鼓中学2021-2022学年高二下学期第二次月考(普通班)化学试题
【分析】根据酯基水解规律:1mol酯基和1mol水分子水解生成1mol羧基和1mol羟基,再根据原子守恒进行判断;
【详解】根据酯水解的生成醇和酸,利用水解规律生成1mol甘油,即含有三个羟基同时生成三个羧基,根据c的相对分子质量及属于直链饱和脂肪酸进行假设c的化学式为CnH2n+1COOH,利用相对分子质量时228判断c的化学式为C13H27COOH,C35H50O6+3H2O=C3H8O3+2CXHyOz+C13H27COOH,解得x=9,y=10,z=2;故b的分子式为:C9H10O2;
故选答案A;
【点睛】此题考查酯水解的规律,根据水解反应特点进行判断。
10.B
【来源】【全国市级联考】内蒙古呼和浩特市2018届高三第二次模拟考试理科综合化学试题
【详解】A.棉花、优质针叶木等的主要成分是纤维素,A正确;
B.Fe2O3没有磁性,Fe2O3不是磁性物质,Fe3O4是磁性物质,B错误;
C.树脂相对分子质量很大,树脂属于有机高分子材料,C正确;
D.验钞笔中含有碘酒溶液,遇假钞呈现蓝色,遇碘变蓝的是淀粉,D正确;
故答案选B。
11.C
【来源】广东省湛江市2019-2020学年高一下学期期末调研考试化学试题
【详解】 为一定条件下发生加聚反应生成的高分子化合物,聚合度为n,单体为,链节为 ,由于聚合度n为不确定值, 属于混合物,则C错误,故选C。
12.D
【来源】1_2024届高二下期中化学试题
【详解】A.碳碳双键两端的基团不同,则存在顺反异构现象,故A正确;
B.分子中含有羟基,且与羟基直接相邻的碳上有氢,故能发生取代反应和消去反应,故B正确;
C.羟基、酚羟基均可以和钠反应,故1 mol 3- O-咖啡酰奎尼酸与足量的金属钠反应,可产生2.5mol H2,故C正确;
D.碳碳双键、酚羟基邻对位氢均可以和溴反应,故1 mol 3 -O咖啡酰奎尼酸与足量溴水反应,最多消耗4mol Br2,故D错误。
故选D。
13.B
【来源】专题1有机化学的发展及研究思路本专题达标检测
【分析】有机物分子式为时,1mol该有机物完全燃烧时消耗O2的物质的量为;有机物分子式为时,1mol该有机物完全燃烧时消耗O2的物质的量为,有机物总物质的量一定,完全燃烧时消耗氧气的质量不变,说明有机物()分子的与有机物()分子的相同,据此分析判断。
【详解】A.的,的,的,A不符合题意;
B.的,的,的,B符合题意;
C.的,的,的,C不符合题意;
D.的,的,的,D不符合题意;
答案选B。
14.C
【来源】广东省梅州市梅江区梅州中学2021-2022学年高二下学期阶段性考试(一)化学试题
【分析】由质谱图可知,X的相对分子质量为136,n(X)=,3.6gH2O的物质的量n(H2O)=,8.96L(标准状况)CO2的物质的量n(CO2)=,则X中n(H)=2n(H2O)=0.4mol,n(C)=n(CO2)=0.4mol,m(H)=nM=0.4mol×1g/mol=0.4g,m(C)=0.4mol×12g/mol=4.8g,0.4g+4.8g<6.8g,所以X中含有O元素,m(O)=6.8g-4.8g-0.4g=1.6g,n(O)=,n(X):n(C):n(H):n(O)=0.05mol:0.4mol:0.4mol:0.1mol=1:8:8:2,化合物X的分子式为C8H8O2,其核磁共振氢谱有4个峰且面积之比为3:2:2:1,X分子中只含一个苯环且苯环上只有一个取代基,说明X分子中含有4种H原子,苯环上有三种氢原子,个数分别为1、2、2,所以侧链中含有-CH3,结合红外光谱可知,分子中存在酯基,且存在 结构,故有机物X的结构简式为,据此分析解答。
【详解】A.由质谱图可知,X的相对分子质量为136,分析可知n(C):n(H):n(O)=0.4mol:0.4mol:0.1mol=8:8:2,化合物X的分子式为C8H8O2,故A错误;
B.X的结构简式为,含有H种类为共4种,故B错误;
C.由上述分析可知,符合题中X分子结构特征的有机物有1种,其结构简式为,故C正确;
D.由上述分析可知,X为,分子的侧链中含有-CH3,甲基是四面体结构,所有原子不可能全部共平面,故D错误;
故选:C。
15.D
【来源】北京市第一六一中学2021-2022学年高二下学期期中考试化学试题
【详解】A.卤代烃的水解需要在碱性溶液中进行,加入硝酸银溶液检验卤素原子前需要先加入稀硝酸中和过量的氢氧化钠溶液,防止干扰卤素原子的测定,A正确;
B.根据信息得到浅黄色沉淀可知,卤代烃分子中含有溴原子,B正确;
C.相同条件下,该卤代烃蒸汽对氢气的相对密度是94,则其相对分子质量为94×2=188,卤代烃样品的质量为18.8g, 该卤代烃n== =0.1mol,称得沉淀的质量为37.6g,n(AgBr)===0.2mol,Br的物质的量与卤代烃的物质的量之比为2: 1,所以卤代烃中的Br原子数目为2,卤代烃中的Br原子数目为2,其相对分子质量为188,所以分子中烃基的式量为188-80×2=28,烃基的式量除以12,商为碳原子数,余数为氢原子数,所以该烃基为-C2H4,所以卤代烃的分子式为C2H4Br2,C正确;
D.由C分析可知所以卤代烃的分子式为C2H4Br2,所以其结构简式为:CH2BrCH2Br或CH3CHBr2,所以名称为1,2-二溴乙烷,1,1-二溴乙烷,D不正确;
故选D。
16. CH2=CH-CN CH2=CH-CH=CH2
【来源】2011-2012学年浙江省温州市十校联合体高二上学期期中考试化学试题
【分析】此类题目,首先要根据高聚物的结构简式判断高聚物是加聚产物还是缩聚产物,然后根据推断单体的方法作出判断,加聚产物的单体推断方法:
(1)凡链节的主链上只有两个碳原子(无其它原子)的高聚物,其合成单体必为一种,将两半链闭合即可;
(2)凡链节主链上只有四个碳原子(无其它原子)且链节无双键的高聚物,其单体必为两种,在正中间画线断开,然后将四个半键闭合即可;
(3)凡链节中主碳链为6个碳原子,其规律是“见双键,四个碳,无双键,两个碳”画线断开,然后将半键闭合,即将单双键互换。
【详解】该高聚物的形成过程属于加聚反应,加聚反应是由不饱和单体(如碳碳双键,碳碳叁键以及碳氧双键等)聚合高分子的反应,其产物只有一种高分子化合物,凡链节中主碳链为6个碳原子,其规律是“见双键,四个碳,无双键,两个碳”画线断开,然后将半键闭合,即将单双键互换,直接合成该高聚物的物质为: CH2=CH-CN、 CH2=CH-CH=CH2、;因此,本题正确答案是:CH2=CH-CN、CH2=CH-CH=CH2、。
17.
【来源】第九章有机化学基础第62讲有机合成推断及合成路线设计
【详解】甲苯和浓硝酸在浓硫酸加热过程中反应生成,与氯气在催化剂作用下反应生成,在高锰酸钾酸性溶液中发生氧化反应生成,和乙醇在浓硫酸加热条件下反应生成,其合成路线为;故答案为: 。
18.(1)2,2-二甲基丁烷
(2)C2H6
(3) CH3CH=CH2+Br2→CH3CHBrCH2Br 加成反应
(4)nCH3CH=CH2
(5) C2H4、C2H6 C2H4、C4H8
(6)10
【来源】辽宁省沈阳市东北育才学校2021-2022高一下学期期中考试化学试题
【解析】(1)
CH3C(CH3)2CH2CH3属于烷烃,其名称为2,2-二甲基丁烷;
(2)
设该气态烷烃的分子式为CnH2n+2,则:
解得n=2,因此其分子式为C2H6;
(3)
将丙烯通入溴的四氯化碳溶液中发生加成反应,发生的化学方程式为CH3CH=CH2+Br2→CH3CHBrCH2Br;
(4)
丙烯在一定条件下发生加聚反应生成聚丙烯的化学方程式为nCH3CH=CH2;
(5)
①若其中两种烃无论以何种比例混合,只要总物质的量一定,燃烧生成的CO2的物质的量就一定,说明分子中碳原子的个数一定是相同的,则这两种烃是C2H4、C2H6;
②若其中两种烃无论以何种比例混合,只要总质量一定,消耗氧气的质量就一定,这说明两种烃的最简式是相同的,则这两种烃是C2H4、C4H8;
(6)
乙烷分子中含有6个氢原子,与一定量氯气光照条件下反应,生成的产物有一氯乙烷(1种)、二氯乙烷(2种)、三氯乙烷(2种)、四氯乙烷(2种)、五氯乙烷(1种)、六氯乙烷(1种)及HCl,总共10种物质。
19.A
【来源】北京首都师范大学附属中学2023届高三上学期10月份月考化学试题
【详解】A.生成的乙炔中含硫化氢等,硫酸铜溶液可除去杂质,乙炔与溴水发生加成反应,可证明乙炔能和Br2反应,故A正确;
B.提纯苯的溴代反应中溴苯缺少氢氧化钠溶液的洗涤,故B错误;
C.水解后在酸性溶液中检验卤素离子,缺少硝酸不能完成实验,故C错误;
D.浓硫酸使乙醇脱水后,C与浓硫酸反应生成二氧化硫,二氧化硫、乙烯均与溴水反应,缺少NaOH溶液除杂不能完成实验,故D错误;
故答案选A。
20.(1) 加成反应 1:1
(2)溶液分层,溴水不褪色;
(3)
(4) 取代反应 1.55
(5)乙醛与HBrO反应,使得平衡正向移动,消耗,溶液褪色
(6)C
【来源】北京市海淀区2022-2023学年高三上学期期中考试化学试题
【分析】乙醛结构中含有不饱和键,α-H,具有较强的还原性,可能与溴发生加成反应,取代反应和氧化反应;溴水和苯酚溶液反应为取代反应,翻译后混合液pH值为1.85,将溴水与乙醛溶液反应,如果pH=1.85,则证明乙醛与溴水的反应类型为取代反应;如果发生氧化反应,生成的HBr为取代反应的2倍,所以,pH=1.55,所以若pH接近1.55,则证明为氧化反应;若pH介于两者之间,则证明两种反应类型皆有;据此分析解题。
【详解】(1)假设Ⅰ:可以与双键发生加成反应,醛基含有不饱和键,可与发生加成反应;故答案为加成反应;
假设Ⅱ:发生取代反应时,参加反应的其中一个Br原子取代H原子,另一个Br与被取代的H生成HBr,所以无论是几元取代,参加反应的与生成的HBr物质的量之比为1:1,故答案为1:1;
假设Ⅲ:乙醛具有较强的还原性,可被溴水氧化为乙酸,反应方程式为;故答案为;
(2)1mL溴的溶液+1mL乙醛,充分振荡后静置,溶液分层,溴水不褪色;故答案为溶液分层,溴水不褪色;
(3)溴水与苯酚发生取代反应,反应为;故答案为;
(4)若试管2中反应后混合液的pH=1.85,与试管1中pH一致,则证明乙醛与溴水的反应类型为取代反应;如果发生氧化反应,生成的HBr为取代反应的2倍,所以,pH=1.55,所以若pH接近1.55,则证明为氧化反应;应故答案为取代反应;1.55;
(5)与水反应式为,乙醛与HBrO反应,使得平衡正向移动,消耗,溶液褪色;故答案为乙醛与HBrO反应,使得平衡正向移动,消耗,溶液褪色;
(6)柠檬醛分子中含有碳碳双键和醛基,根据上述实验,检验柠檬醛分子中存在碳碳双健是方法是向溴的溶液中加适量柠檬醛,观察其是否褪色;选项C符合题意,故答案选C。
【点睛】本题主要考查化学实验方案的评价,题目难度中等,注意根据反应的类型判断反应可能的产物,把握实验原理是解题的关键。
21. C9H10O2 羟基 CH3COOH + + H2O 氧化反应 酯化反应(或取代反应) C d 干燥 b
【来源】【全国市级联考】广东省潮州市2017-2018学年下学期期末考试高一化学试题
【详解】分析:乙醇发生催化氧化生成乙醛,乙醛进一步发生氧化反应生成A为CH3COOH,甲苯与氯气发生取代反应生成,发生水解反应生成B为,乙酸与苯甲醇发生酯化反应得到乙酸苯甲酯,据此解答。
详解:(1)根据乙酸苯甲酯的结构简式可知其分子式是C9H10O2;根据以上分析可知B为,含有官能团为羟基;
(2)反应③是酯化反应,反应的化学反应方程式为CH3COOH++H2O。反应①是乙醇的催化氧化;
(3)A.乙醇制取乙醛,有水生成,原子的理论利用率不是100%,A不符合;B.甲苯制备,有HCl生成,原子的理论利用率不是100%,B不符合;C.反应2CH3CHO+O22CH3COOH中生成物只有乙酸,原子的理论利用率为100%,符合绿色化学的要求,C符合,答案为C;
(4)①由于酯的密度比水小,二者互不相溶,因此水在下层,酯在上层;分液时,要先将水层从分液漏斗的下口放出,待到两层液体界面时关闭分液漏斗的活塞,再将乙酸苯甲酯从上口放出,所以正确的为d,答案选d;
②实验中加入少量无水硫酸镁的目的是吸收酯中少量的水分,对乙酸苯甲酯进行干燥;
③在蒸馏操作中,温度计的水银球要放在蒸馏烧瓶的支管口处,所以ad错误;c中使用的是球形冷凝管容易使产品滞留,不能全部收集到锥形瓶中,因此仪器及装置安装正确的是b,答案选b。
点睛:本题考查了有机推断,常见仪器的构造与安装、混合物的分离、提纯、物质的制取、药品的选择及使用等知识,题目难度较大。试题涉及的题量较大,知识点较多,充分培养了学生的分析、理解能力及灵活应用所学知识的能力。熟练掌握常见有机物结构与性质、化学实验基本操作为解答关键,注意明确常见有机物官能团名称、反应类型,能够正确书写常见有机反应方程式。
一、单选题
1.下列说法不正确的是
A.光谱分析就是利用原子光谱上的特征谱线来鉴定元素
B.用红热的铁针刺涂有石蜡的水晶柱面,熔化的石蜡呈圆形
C.手性催化剂只催化或者主要催化一种手性分子的合成,而不得到它的手性异构分子。
D.过渡金属离子对多种配体具有很强的结合力,因而,过渡金属配合物远比主族金属配合物多
2.在核磁共振氢谱中出现两组峰,其氢原子数之比为1:1的化合物是
A.CH3CH2CH3 B.
C.CH3—O—CH3 D.
3.下列说法不正确的是
A.通过红外光谱分析可以区分丁醛和乙酸乙酯
B.可利用原子光谱上的特征谱线来鉴定元素
C.的核磁共振氢谱中有5组峰
D.对乙醇和二甲醚进行质谱分析,质谱图完全相同
4.下列有机物中,一氯取代物有2种的是( )
①;②;③;④
A.①③ B.②③ C.①④ D.②④
5.下列芳香烃的一氯取代物的同分异构体数目最多的是
A.连二苯
B.菲
C.蒽
D.连三苯
6.化学与生活密切相关,下列叙述正确的是
A.糖类、油脂、蛋白质是人体基本营养物质,均属于高分子
B.乙醇汽油是一种新型化合物
C.向牛奶中加入白醋会产生沉淀,这是因为发生了酸碱中和反应
D.氢氟酸可用于蚀刻玻璃、石英制品
7.茉莉醛具有浓郁的茉莉花香,其结构简式如图,关于茉莉醛的说法正确的是
A.茉莉醛与苯甲醛互为同系物
B.1mol茉莉醛与足量银氨溶液反应,生成1mol银单质
C.茉莉醛使酸性高锰酸钾溶液褪色证明茉莉醛分子中含有碳碳双键
D.在一定条件下能与苯酚发生缩聚反应生成高分子化合物
8.叶蝉散对水稻叶蝉和飞虱具有较强的触杀作用,防效迅速,但残效不长。工业上用邻异丙基苯酚合成叶蝉散的过程如下:
下列有关说法正确的是
A.叶蝉散的分子式是 B.叶蝉散分子中含有羧基
C.叶蝉散的核磁共振氢谱有8组吸收峰 D.邻异丙基苯酚与互为同系物
9.某酯类化合物a的分子式为C35H50O6,1 mol该酯类化合物a完全水解可得到1 mol甘油、2 mol不饱和脂肪酸b和1 mol直链饱和脂肪酸c,经测定c的相对分子质量为228,则不饱和脂肪酸b的分子式为
A.C9H10O2 B.C9H12O2
C.C9H16O2 D.C9H17O2
10.新版人民币的发行,引发了人们对有关人民币中化学知识的关注。下列表述不正确的是
A.制造人民币所用的棉花、优质针叶木等原料的主要成分是纤维素
B.用于人民币票面文字等处的油墨中所含有的Fe2O3是一种磁性物质
C.防伪荧光油墨由颜料与树脂等制成,其中树脂属于有机高分子材料
D.某种验钞笔中含有碘酒溶液,遇假钞呈现蓝色,其中遇碘变蓝的是淀粉
11.某高分子化合物的结构简式如图。下列叙述错误的是
A.聚合度为n B.单体为
C.链节为 D.该高分子化合物是混合物
12.3- O-咖啡酰奎尼酸是金银花抗菌、抗病毒的有效成分之一,其分子结构如下图。下列关于3 -O-咖啡酰奎尼酸的说法不正确的是
A.存在顺反异构现象
B.能发生取代反应和消去反应
C.1 mol 3- O-咖啡酰奎尼酸与足量的金属钠反应,可产生2.5mol H2
D.1 mol 3 -O咖啡酰奎尼酸与足量溴水反应,最多消耗3 mol Br2
13.下列各组有机化合物中,不论三者以什么比例混合,只要总物质的量一定,则完全燃烧时消耗氧气的质量不变的是
A.,, B.,,
C.,, D.,,
14.将6.8g的X完全燃烧生成3.6g的H2O和8.96L(标准状况)的CO2,X的核磁共振氢谱有4个峰且面积之比为3:2:2:1。X分子中只含一个苯环且苯环上只有一个取代基,其质谱图、核磁共振氢谱与红外光谱如图,关于X的下列叙述正确的是
A.化合物X的分子式为C8H10O2
B.由核磁共振氢谱可知,X分子中有3种不同化学环境的氢原子
C.符合题中X分子结构特征的有机物有1种
D.X分子中所有的原子在同一个平面上
15.为测定某卤代烃(只含一种卤原子)分子中卤素原子的种类和数目,设计实验如下:
已知:相同条件下,该卤代烃蒸气对氢气的相对密度是94
下列说法不正确的是
A.加入过量稀硝酸的目的是中和未反应的NaOH,防止干扰卤原子的测定
B.该卤代烃分子中含有溴原子
C.该卤代烃的分子式是
D.该卤代烃的名称是1,2-二溴乙烷
二、填空题
16.工程塑料ABS树脂结构为:
合成它用了三种单体,这三种单体的结构简式分别是_______ 、_______、_______。
17.合成路线流程图示例如下:
请设计合理方案,以甲苯为主要原料,其他物质可根据需要自主选择,合成局部麻醉剂氯普鲁卡因盐酸盐的中间体。________
18.按要求答题
(1)CH3C(CH3)2CH2CH3的命名:_______;
(2)10mL某气态烷烃,在50mLO2中充分燃烧,得到液态水以及体积为35mL的混合气体(气体体积均在相同条件下测定)。该气态烷烃的分子式是_______;
(3)将丙烯(CH3CH=CH2)通入溴的四氯化碳溶液中,发生的化学方程式为_______,该反应的反应类型是_______;
(4)写出丙烯在一定条件下发生加聚反应的化学方程式_______;
(5)现有CH4、C2H4、C2H6、C4H8四种烃:
①若其中两种烃无论以何种比例混合,只要总物质的量一定,燃烧生成的CO2的物质的量就一定,则这两种烃是_______;
②若其中两种烃无论以何种比例混合,只要总质量一定,消耗氧气的质量就一定,则这两种烃是_______;
(6)乙烷与一定量氯气光照条件下反应,生成的产物有_______种。
三、实验题
19.利用下列实验药品进行实验,能顺利达到实验目的的是
实验目的 实验药品
A 证明乙炔能和反应 电石、饱和食盐水、溶液和溴水
B 提纯苯的溴代反应中溴苯 苯、液溴、Fe粉、水
C 检验溴乙烷中的溴原子 溴乙烷、溶液和溶液
D 验证乙醇消去产物有乙烯 乙醇、浓硫酸和溴水
A.A B.B C.C D.D
20.实验表明,当乙醛加入到溴水中,溴水会褪色。针对此现象,某小组同学依据乙醛结构进行探究。
【实验假设】
(1)假设Ⅰ:醛基含有不饱和键,可与发生_________反应(填反应类型)。
假设Ⅱ:乙醛具有α-H,可与溴水发生取代反应。一元取代反应如下:
无论是几元取代,参加反应的与生成的HBr物质的量之比为_________。
假设Ⅲ:乙醛具有较强的还原性,可被溴水氧化为乙酸,补全下面反应方程式。
_________
【实验过程】针对以上假设,该小组同学设计了两组方案。
方案Ⅰ:通过对比反应现象判断反应类型。
序号 操作 现象
试管1 1mL溴水+1mL乙醛,充分振荡后静置 褪色
试管2 1mL溴的溶液+1mL乙醛,充分振荡后静置 ____
结论:假设Ⅰ不成立。
(2)试管2中的实验现象为__________。
方案Ⅱ:通过测定反应后混合液的pH判断反应类型。
序号 操作 pH
试管1 加入20mL溴水,再加入10mL苯酚溶液,待完全反应后(苯酚过量),测定混合液pH 1.85[]
试管2 加入20mL相同浓度的溴水,再加入10mL 20%的乙醛溶液(乙醛过量),3min后完全褪色,测定混合液pH ____________
注:苯酚和乙酸的电离及温度变化对混合液pH的影响可忽略。
(3)写出苯酚与溴水反应的化学方程式:____________________________________。
(4)若试管2中反应后混合液的pH=1.85,则证明乙醛与溴水的反应类型为______反应;若pH接近______,则证明为氧化反应(lg2≈0.3);若pH介于两者之间,则证明两种反应类型皆有。
【实验结论与反思】
(5)根据实验数据得出结论:乙醛与溴水发生氧化反应。查阅资料,乙醛并非直接与发生反应,而是与次溴酸(HBrO)反应,从平衡移动的角度解释乙醛使溴水褪色的原因:______________。
(6)已知柠檬醛的结构如图,结合上述实验,检验柠檬醛分子中存在碳碳双键的合理方法为 (填字母序号)。
A.向酸性高锰酸钾溶液中加适量柠檬醛,观察其是否褪色
B.向溴水中加适量柠檬醛,观察其是否褪色
C.向溴的溶液中加适量柠檬醛,观察其是否褪色
D.向新制氢氧化铜悬浊液中加适量柠檬醛,加热,冷却后取上层清液再加溴水,观察其是否褪色
21.酯类是工业上重要的有机原料,具有广泛用途。乙酸苯甲酯对花香和果香的香韵具有提升作用,故常用于化妆品和食品工业。乙酸苯甲酯的合成路线如下:
已知:R-ClR-OH,R-为烃基
(1)乙酸苯甲酯的分子式是________,B所含官能团的名称是________。
(2)写出反应③的化学反应方程式:________。反应①的反应类型是__________,反应③的反应类型是________________。
(3)下列转化中________(填序号)原子的理论利用率为100%,符合绿色化学的要求。
A.乙醇制取乙醛 B.由制备 C.2CH3CHO+O22A
(4)提纯乙酸苯甲酯的有关实验步骤如下:将反应液冷至室温后倒入分液漏斗中,分别用饱和碳酸钠溶液和水洗涤,分出的产物加入少量无水MgSO4固体,静置片刻,过滤除去MgSO4固体,进行蒸馏,收集馏分,得到乙酸苯甲酯。
回答下列问题:
①在洗涤、分液操作中。应充分振荡,然后静置,待分层后________(填标号)。
a.直接将乙酸苯甲酯从分液漏斗上口倒出
b.直按将乙酸苯甲酯从分液漏斗下口放出
c.先将水层从分液漏斗的下口放出,再将乙酸苯甲酯从下口放出
d.先将水层从分液漏斗的下口放出,再将乙酸苯甲酯从上口放出
②实验中加入少量无水MgSO4的目的是__________________。
③在蒸馏操作中,仪器选择及安装都正确的是____________(填标号)。
(注:箭头方向表示水流方向)
参考答案:
1.B
【来源】辽宁省沈阳市第二中学2021-2022学年高二上学期期末考试化学试题
【详解】A.不同元素原子的吸收光谱或发射光谱不同,常利用原子光谱上的特征谱线来鉴定元素,故A正确;
B.晶体具有各向异性,所以用红热的铁针刺涂有石蜡的水晶柱面,熔化的石蜡呈椭圆形,故B错误;
C.在手性催化中,潜手性化合物在反应过程中会与手性催化剂形成一种最稳定的过渡态,从而只会诱导出一种手性分子,所以利用手性催化剂合成主要(或只)得到一种手性分子,而不得到它的手性异构分子,故C正确;
D.由于许多过渡元素金属离子对多种配体具有很强的结合力,能形成种类繁多的配合物,所以过渡金属配合物远比主族金属的配合物多,故D正确;
答案选B。
2.D
【来源】宁夏平罗中学2021-2022学年高二上学期第一次月考化学试题
【详解】A.CH3CH2CH3有2种等效氢,其氢原子数之比为3:1,核磁共振氢谱中出现两组峰,故不选A;
B.有3种等效氢,其氢原子数之比为3:3:2,核磁共振氢谱中出现三组峰,故不选B;
C.CH3—O—CH3有1种等效氢,核磁共振氢谱中出现一组峰,故不选C;
D. 有2种等效氢,其氢原子数之比为1:1,核磁共振氢谱中出现两组峰,故选D;
故答案选D。
3.D
【来源】浙江省衢州市2021-2022学年高二下学期6月教学质量检测化学试题
【详解】A.红外光谱仪可确定有机物中官能团及化学键,丁醛含醛基,乙酸乙酯含酯基,则红外光谱仪可以区分丁醛和乙酸乙酯,故A正确;
B.不同元素原子的吸收光谱或发射光谱不同,常利用原子光谱上的特征谱线来鉴定元素,故B正确;
C.有5种H原子,则核磁共振氢谱中有5组峰,故C正确;
D.乙醇和二甲醚结构不同,最大荷比相同,则质谱图不完全相同,故D错误;
故选:D。
4.B
【来源】吉林省田家炳高中、东辽二高等五校2021-2022学年高一下学期期末考试化学试题
【详解】根据有机物的等效氢有几种,其一氯取代物就有几种:
①有3种等效氢,则其一氯取代物有3种,不符合题意;
②有2种等效氢,则其一氯取代物有2种,符合题意;
③有2种等效氢,则其一氯取代物有2种,符合题意;
④有1种等效氢,则其一氯取代物有1种,不符合题意;
故答案为B。
5.B
【来源】2015-2016学年福建省八县一中高二下学期期末化学试卷(带解析)
【详解】A.连二苯,有两条对称轴和1个对称中心,有3种氢原子,一氯代物数目为3;
B.菲,有一条对称轴,有5种氢原子,一氯代物数目为5;
C.蒽两条对称轴和1个对称中心,有3种氢原子,一氯代物数目为3 ;
D.连三苯,有两条对称轴和1个对称中心,有4种氢原子,一氯代物数目为4;
故选B。
6.D
【来源】湖南师范大学附属中学2022-2023学年高三上学期月考卷(六)化学试题
【详解】A.油脂不属于高分子化合物,A错误;
B.乙醇汽油是一种混合物,B错误;
C.牛奶中含有蛋白质,加入果汁使蛋白质凝聚而沉淀,不是发生了酸碱中和反应,C错误;
D.氢氟酸可与SiO2反应生成SiF4气体和H2O,因此可利用氢氟酸刻蚀玻璃、石英制品,D正确;
故选D。
7.D
【来源】山东省日照市2021-2022学年高二下学期期末考试化学试题
【详解】A.由茉莉醛结构可知,其含有碳碳双键和醛基,而苯甲醛只含有醛基,二者官能团不相同,故不互为同系物,故A错误;
B.1mol茉莉醛含有1mol的醛基,与足量银氨溶液反应生成2mol银单质,故B错误;
C.茉莉醛含有的碳碳双键和醛基均能使酸性高锰酸钾溶液褪色,不能证明茉莉醛分子中含有碳碳双键,故C错误;
D.茉莉醛含有醛基,在一定条件下能与苯酚发生缩聚反应,生成高分子化合物,故D正确;
故答案选D。
8.C
【来源】第一~二节综合拔高练
【详解】A.根据叶蝉散的结构简式可得其分子式是,A错误;
B.由叶蝉散的分子结构可知叶蝉散中不含有,B错误;
C.由叶蝉散的结构简式可知,叶蝉散分子中含有8种不同化学环境的氢原子,则叶蝉散的核磁共振氢谱有8组吸收峰,C正确;
D.邻异丙基苯酚属于酚,属于醇,二者类别不同,则邻异丙基苯酚与不互为同系物,D错误;
综上,本题选C。
9.A
【来源】江西省宜春市铜鼓中学2021-2022学年高二下学期第二次月考(普通班)化学试题
【分析】根据酯基水解规律:1mol酯基和1mol水分子水解生成1mol羧基和1mol羟基,再根据原子守恒进行判断;
【详解】根据酯水解的生成醇和酸,利用水解规律生成1mol甘油,即含有三个羟基同时生成三个羧基,根据c的相对分子质量及属于直链饱和脂肪酸进行假设c的化学式为CnH2n+1COOH,利用相对分子质量时228判断c的化学式为C13H27COOH,C35H50O6+3H2O=C3H8O3+2CXHyOz+C13H27COOH,解得x=9,y=10,z=2;故b的分子式为:C9H10O2;
故选答案A;
【点睛】此题考查酯水解的规律,根据水解反应特点进行判断。
10.B
【来源】【全国市级联考】内蒙古呼和浩特市2018届高三第二次模拟考试理科综合化学试题
【详解】A.棉花、优质针叶木等的主要成分是纤维素,A正确;
B.Fe2O3没有磁性,Fe2O3不是磁性物质,Fe3O4是磁性物质,B错误;
C.树脂相对分子质量很大,树脂属于有机高分子材料,C正确;
D.验钞笔中含有碘酒溶液,遇假钞呈现蓝色,遇碘变蓝的是淀粉,D正确;
故答案选B。
11.C
【来源】广东省湛江市2019-2020学年高一下学期期末调研考试化学试题
【详解】 为一定条件下发生加聚反应生成的高分子化合物,聚合度为n,单体为,链节为 ,由于聚合度n为不确定值, 属于混合物,则C错误,故选C。
12.D
【来源】1_2024届高二下期中化学试题
【详解】A.碳碳双键两端的基团不同,则存在顺反异构现象,故A正确;
B.分子中含有羟基,且与羟基直接相邻的碳上有氢,故能发生取代反应和消去反应,故B正确;
C.羟基、酚羟基均可以和钠反应,故1 mol 3- O-咖啡酰奎尼酸与足量的金属钠反应,可产生2.5mol H2,故C正确;
D.碳碳双键、酚羟基邻对位氢均可以和溴反应,故1 mol 3 -O咖啡酰奎尼酸与足量溴水反应,最多消耗4mol Br2,故D错误。
故选D。
13.B
【来源】专题1有机化学的发展及研究思路本专题达标检测
【分析】有机物分子式为时,1mol该有机物完全燃烧时消耗O2的物质的量为;有机物分子式为时,1mol该有机物完全燃烧时消耗O2的物质的量为,有机物总物质的量一定,完全燃烧时消耗氧气的质量不变,说明有机物()分子的与有机物()分子的相同,据此分析判断。
【详解】A.的,的,的,A不符合题意;
B.的,的,的,B符合题意;
C.的,的,的,C不符合题意;
D.的,的,的,D不符合题意;
答案选B。
14.C
【来源】广东省梅州市梅江区梅州中学2021-2022学年高二下学期阶段性考试(一)化学试题
【分析】由质谱图可知,X的相对分子质量为136,n(X)=,3.6gH2O的物质的量n(H2O)=,8.96L(标准状况)CO2的物质的量n(CO2)=,则X中n(H)=2n(H2O)=0.4mol,n(C)=n(CO2)=0.4mol,m(H)=nM=0.4mol×1g/mol=0.4g,m(C)=0.4mol×12g/mol=4.8g,0.4g+4.8g<6.8g,所以X中含有O元素,m(O)=6.8g-4.8g-0.4g=1.6g,n(O)=,n(X):n(C):n(H):n(O)=0.05mol:0.4mol:0.4mol:0.1mol=1:8:8:2,化合物X的分子式为C8H8O2,其核磁共振氢谱有4个峰且面积之比为3:2:2:1,X分子中只含一个苯环且苯环上只有一个取代基,说明X分子中含有4种H原子,苯环上有三种氢原子,个数分别为1、2、2,所以侧链中含有-CH3,结合红外光谱可知,分子中存在酯基,且存在 结构,故有机物X的结构简式为,据此分析解答。
【详解】A.由质谱图可知,X的相对分子质量为136,分析可知n(C):n(H):n(O)=0.4mol:0.4mol:0.1mol=8:8:2,化合物X的分子式为C8H8O2,故A错误;
B.X的结构简式为,含有H种类为共4种,故B错误;
C.由上述分析可知,符合题中X分子结构特征的有机物有1种,其结构简式为,故C正确;
D.由上述分析可知,X为,分子的侧链中含有-CH3,甲基是四面体结构,所有原子不可能全部共平面,故D错误;
故选:C。
15.D
【来源】北京市第一六一中学2021-2022学年高二下学期期中考试化学试题
【详解】A.卤代烃的水解需要在碱性溶液中进行,加入硝酸银溶液检验卤素原子前需要先加入稀硝酸中和过量的氢氧化钠溶液,防止干扰卤素原子的测定,A正确;
B.根据信息得到浅黄色沉淀可知,卤代烃分子中含有溴原子,B正确;
C.相同条件下,该卤代烃蒸汽对氢气的相对密度是94,则其相对分子质量为94×2=188,卤代烃样品的质量为18.8g, 该卤代烃n== =0.1mol,称得沉淀的质量为37.6g,n(AgBr)===0.2mol,Br的物质的量与卤代烃的物质的量之比为2: 1,所以卤代烃中的Br原子数目为2,卤代烃中的Br原子数目为2,其相对分子质量为188,所以分子中烃基的式量为188-80×2=28,烃基的式量除以12,商为碳原子数,余数为氢原子数,所以该烃基为-C2H4,所以卤代烃的分子式为C2H4Br2,C正确;
D.由C分析可知所以卤代烃的分子式为C2H4Br2,所以其结构简式为:CH2BrCH2Br或CH3CHBr2,所以名称为1,2-二溴乙烷,1,1-二溴乙烷,D不正确;
故选D。
16. CH2=CH-CN CH2=CH-CH=CH2
【来源】2011-2012学年浙江省温州市十校联合体高二上学期期中考试化学试题
【分析】此类题目,首先要根据高聚物的结构简式判断高聚物是加聚产物还是缩聚产物,然后根据推断单体的方法作出判断,加聚产物的单体推断方法:
(1)凡链节的主链上只有两个碳原子(无其它原子)的高聚物,其合成单体必为一种,将两半链闭合即可;
(2)凡链节主链上只有四个碳原子(无其它原子)且链节无双键的高聚物,其单体必为两种,在正中间画线断开,然后将四个半键闭合即可;
(3)凡链节中主碳链为6个碳原子,其规律是“见双键,四个碳,无双键,两个碳”画线断开,然后将半键闭合,即将单双键互换。
【详解】该高聚物的形成过程属于加聚反应,加聚反应是由不饱和单体(如碳碳双键,碳碳叁键以及碳氧双键等)聚合高分子的反应,其产物只有一种高分子化合物,凡链节中主碳链为6个碳原子,其规律是“见双键,四个碳,无双键,两个碳”画线断开,然后将半键闭合,即将单双键互换,直接合成该高聚物的物质为: CH2=CH-CN、 CH2=CH-CH=CH2、;因此,本题正确答案是:CH2=CH-CN、CH2=CH-CH=CH2、。
17.
【来源】第九章有机化学基础第62讲有机合成推断及合成路线设计
【详解】甲苯和浓硝酸在浓硫酸加热过程中反应生成,与氯气在催化剂作用下反应生成,在高锰酸钾酸性溶液中发生氧化反应生成,和乙醇在浓硫酸加热条件下反应生成,其合成路线为;故答案为: 。
18.(1)2,2-二甲基丁烷
(2)C2H6
(3) CH3CH=CH2+Br2→CH3CHBrCH2Br 加成反应
(4)nCH3CH=CH2
(5) C2H4、C2H6 C2H4、C4H8
(6)10
【来源】辽宁省沈阳市东北育才学校2021-2022高一下学期期中考试化学试题
【解析】(1)
CH3C(CH3)2CH2CH3属于烷烃,其名称为2,2-二甲基丁烷;
(2)
设该气态烷烃的分子式为CnH2n+2,则:
解得n=2,因此其分子式为C2H6;
(3)
将丙烯通入溴的四氯化碳溶液中发生加成反应,发生的化学方程式为CH3CH=CH2+Br2→CH3CHBrCH2Br;
(4)
丙烯在一定条件下发生加聚反应生成聚丙烯的化学方程式为nCH3CH=CH2;
(5)
①若其中两种烃无论以何种比例混合,只要总物质的量一定,燃烧生成的CO2的物质的量就一定,说明分子中碳原子的个数一定是相同的,则这两种烃是C2H4、C2H6;
②若其中两种烃无论以何种比例混合,只要总质量一定,消耗氧气的质量就一定,这说明两种烃的最简式是相同的,则这两种烃是C2H4、C4H8;
(6)
乙烷分子中含有6个氢原子,与一定量氯气光照条件下反应,生成的产物有一氯乙烷(1种)、二氯乙烷(2种)、三氯乙烷(2种)、四氯乙烷(2种)、五氯乙烷(1种)、六氯乙烷(1种)及HCl,总共10种物质。
19.A
【来源】北京首都师范大学附属中学2023届高三上学期10月份月考化学试题
【详解】A.生成的乙炔中含硫化氢等,硫酸铜溶液可除去杂质,乙炔与溴水发生加成反应,可证明乙炔能和Br2反应,故A正确;
B.提纯苯的溴代反应中溴苯缺少氢氧化钠溶液的洗涤,故B错误;
C.水解后在酸性溶液中检验卤素离子,缺少硝酸不能完成实验,故C错误;
D.浓硫酸使乙醇脱水后,C与浓硫酸反应生成二氧化硫,二氧化硫、乙烯均与溴水反应,缺少NaOH溶液除杂不能完成实验,故D错误;
故答案选A。
20.(1) 加成反应 1:1
(2)溶液分层,溴水不褪色;
(3)
(4) 取代反应 1.55
(5)乙醛与HBrO反应,使得平衡正向移动,消耗,溶液褪色
(6)C
【来源】北京市海淀区2022-2023学年高三上学期期中考试化学试题
【分析】乙醛结构中含有不饱和键,α-H,具有较强的还原性,可能与溴发生加成反应,取代反应和氧化反应;溴水和苯酚溶液反应为取代反应,翻译后混合液pH值为1.85,将溴水与乙醛溶液反应,如果pH=1.85,则证明乙醛与溴水的反应类型为取代反应;如果发生氧化反应,生成的HBr为取代反应的2倍,所以,pH=1.55,所以若pH接近1.55,则证明为氧化反应;若pH介于两者之间,则证明两种反应类型皆有;据此分析解题。
【详解】(1)假设Ⅰ:可以与双键发生加成反应,醛基含有不饱和键,可与发生加成反应;故答案为加成反应;
假设Ⅱ:发生取代反应时,参加反应的其中一个Br原子取代H原子,另一个Br与被取代的H生成HBr,所以无论是几元取代,参加反应的与生成的HBr物质的量之比为1:1,故答案为1:1;
假设Ⅲ:乙醛具有较强的还原性,可被溴水氧化为乙酸,反应方程式为;故答案为;
(2)1mL溴的溶液+1mL乙醛,充分振荡后静置,溶液分层,溴水不褪色;故答案为溶液分层,溴水不褪色;
(3)溴水与苯酚发生取代反应,反应为;故答案为;
(4)若试管2中反应后混合液的pH=1.85,与试管1中pH一致,则证明乙醛与溴水的反应类型为取代反应;如果发生氧化反应,生成的HBr为取代反应的2倍,所以,pH=1.55,所以若pH接近1.55,则证明为氧化反应;应故答案为取代反应;1.55;
(5)与水反应式为,乙醛与HBrO反应,使得平衡正向移动,消耗,溶液褪色;故答案为乙醛与HBrO反应,使得平衡正向移动,消耗,溶液褪色;
(6)柠檬醛分子中含有碳碳双键和醛基,根据上述实验,检验柠檬醛分子中存在碳碳双健是方法是向溴的溶液中加适量柠檬醛,观察其是否褪色;选项C符合题意,故答案选C。
【点睛】本题主要考查化学实验方案的评价,题目难度中等,注意根据反应的类型判断反应可能的产物,把握实验原理是解题的关键。
21. C9H10O2 羟基 CH3COOH + + H2O 氧化反应 酯化反应(或取代反应) C d 干燥 b
【来源】【全国市级联考】广东省潮州市2017-2018学年下学期期末考试高一化学试题
【详解】分析:乙醇发生催化氧化生成乙醛,乙醛进一步发生氧化反应生成A为CH3COOH,甲苯与氯气发生取代反应生成,发生水解反应生成B为,乙酸与苯甲醇发生酯化反应得到乙酸苯甲酯,据此解答。
详解:(1)根据乙酸苯甲酯的结构简式可知其分子式是C9H10O2;根据以上分析可知B为,含有官能团为羟基;
(2)反应③是酯化反应,反应的化学反应方程式为CH3COOH++H2O。反应①是乙醇的催化氧化;
(3)A.乙醇制取乙醛,有水生成,原子的理论利用率不是100%,A不符合;B.甲苯制备,有HCl生成,原子的理论利用率不是100%,B不符合;C.反应2CH3CHO+O22CH3COOH中生成物只有乙酸,原子的理论利用率为100%,符合绿色化学的要求,C符合,答案为C;
(4)①由于酯的密度比水小,二者互不相溶,因此水在下层,酯在上层;分液时,要先将水层从分液漏斗的下口放出,待到两层液体界面时关闭分液漏斗的活塞,再将乙酸苯甲酯从上口放出,所以正确的为d,答案选d;
②实验中加入少量无水硫酸镁的目的是吸收酯中少量的水分,对乙酸苯甲酯进行干燥;
③在蒸馏操作中,温度计的水银球要放在蒸馏烧瓶的支管口处,所以ad错误;c中使用的是球形冷凝管容易使产品滞留,不能全部收集到锥形瓶中,因此仪器及装置安装正确的是b,答案选b。
点睛:本题考查了有机推断,常见仪器的构造与安装、混合物的分离、提纯、物质的制取、药品的选择及使用等知识,题目难度较大。试题涉及的题量较大,知识点较多,充分培养了学生的分析、理解能力及灵活应用所学知识的能力。熟练掌握常见有机物结构与性质、化学实验基本操作为解答关键,注意明确常见有机物官能团名称、反应类型,能够正确书写常见有机反应方程式。
