阶段性综合练习(考查内容专题4、专题5、专题6)(含解析)2022-2023学年下学期高二化学苏教版(2019)选择性必修3
文档属性
| 名称 | 阶段性综合练习(考查内容专题4、专题5、专题6)(含解析)2022-2023学年下学期高二化学苏教版(2019)选择性必修3 |
|
|
| 格式 | docx | ||
| 文件大小 | 1.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-06-18 00:00:00 | ||
图片预览




文档简介
阶段性综合练习(考查内容专题4、专题5、专题6)
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1.某种聚碳酸酯的透光性好,可制成车、船的挡风玻璃,以及眼镜镜片、光盘等,其结构可表示为: ,原来合成聚碳酸酯的一种原料是有毒的光气(,又称碳酰氯)。为贯彻绿色化学理念,可以改用碳酸二甲酯()与什么缩合聚合生产聚碳酸酯
A.二卤化物 B.二酚类物质 C.二醇类物质 D.二烯类物质
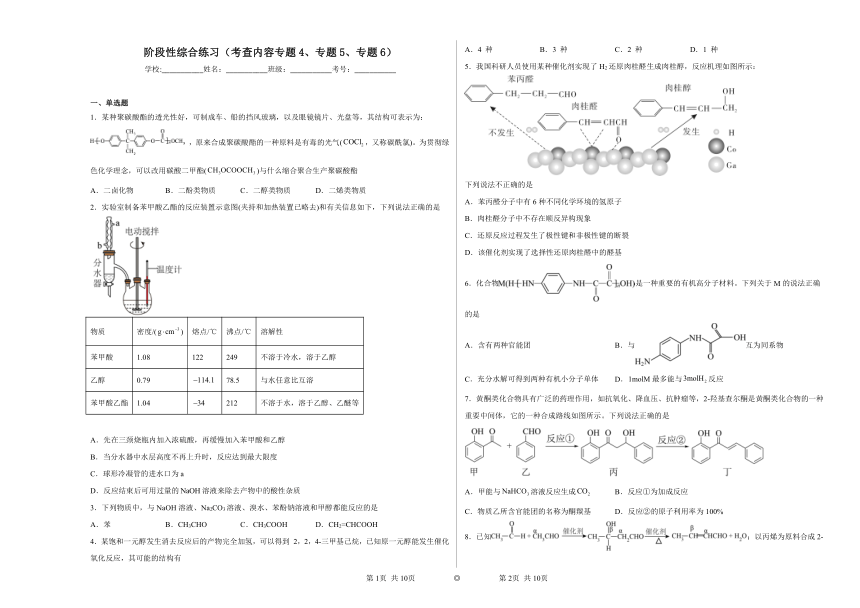
2.实验室制备苯甲酸乙酯的反应装置示意图(夹持和加热装置已略去)和有关信息如下,下列说法正确的是
物质 密度/() 熔点/ 沸点/ 溶解性
苯甲酸 1.08 122 249 不溶于冷水,溶于乙醇
乙醇 0.79 78.5 与水任意比互溶
苯甲酸乙酯 1.04 212 不溶于水,溶于乙醇、乙醚等
A.先在三颈烧瓶内加入浓硫酸,再缓慢加入苯甲酸和乙醇
B.当分水器中水层高度不再上升时,反应达到最大限度
C.球形冷凝管的进水口为a
D.反应结束后可用过量的溶液来除去产物中的酸性杂质
3.下列物质中,与NaOH溶液、Na2CO3溶液、溴水、苯酚钠溶液和甲醇都能反应的是
A.苯 B.CH3CHO C.CH3COOH D.CH2=CHCOOH
4.某饱和一元醇发生消去反应后的产物完全加氢,可以得到 2,2,4-三甲基己烷,已知原一元醇能发生催化氧化反应,其可能的结构有
A.4 种 B.3 种 C.2 种 D.1 种
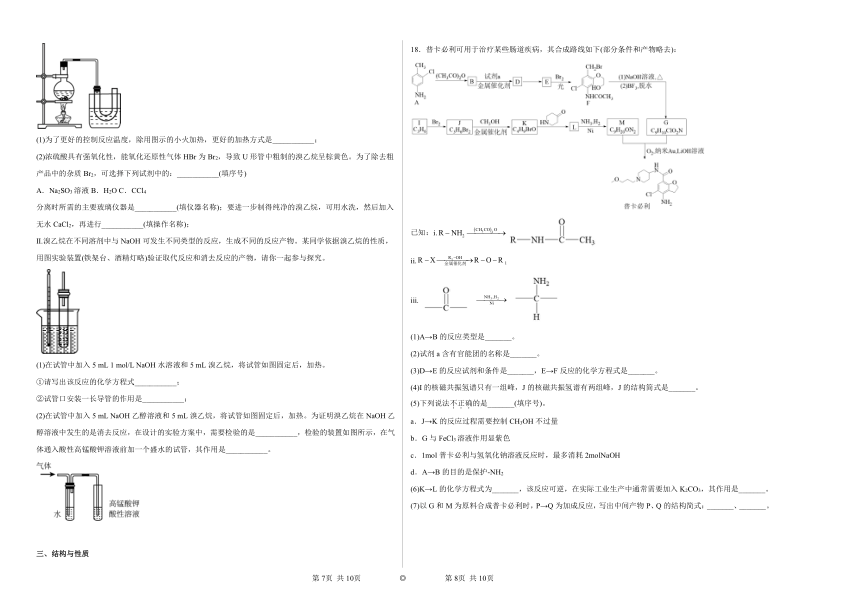
5.我国科研人员使用某种催化剂实现了H2还原肉桂醛生成肉桂醇,反应机理如图所示:
下列说法不正确的是
A.苯丙醛分子中有6种不同化学环境的氢原子
B.肉桂醛分子中不存在顺反异构现象
C.还原反应过程发生了极性键和非极性键的断裂
D.该催化剂实现了选择性还原肉桂醛中的醛基
6.化合物是一种重要的有机高分子材料。下列关于M的说法正确的是
A.含有两种官能团 B.与互为同系物
C.充分水解可得到两种有机小分子单体 D.最多能与反应
7.黄酮类化合物具有广泛的药理作用,如抗氧化、降血压、抗肿瘤等,2-羟基查尔酮是黄酮类化合物的一种重要中间体,它的一种合成路线如图所示。下列说法正确的是
A.甲能与溶液反应生成 B.反应①为加成反应
C.物质乙所含官能团的名称为酮羰基 D.反应②的原子利用率为100%
8.已知;以丙烯为原料合成2-甲基-1-丙醇的过程如下,丙烯2-甲基-1-丙醇。下列说法错误的是
A.丙烯→I的反应可生成两种产物 B.II的结构简式为
C.试剂a可用作食品添加剂 D.IV能使溴水褪色
9.有机化合物N可用于早期诊断阿兹海默症,其结构简式如下:
下列关于N的说法正确的是
A.分子式为
B.分子中共线的碳原子最多有4个
C.能与NaOH水溶液反应,1molN最多可消耗1molNaOH
D.能与浓溴水反应,1molN最多可消耗
10.聚酰胺(PA)具有良好的力学性能,一种合成路线如下图所示。下列说法不正确的是。
A.Y中含有五元环 B.②是酯化反应
C.该合成路线中甲醇可循环使用 D.PA可发生水解反应重新生成Z
11.下列物质中,不属于有机高分子的是
A.淀粉 B.油脂 C.蛋白质 D.核酸
A.A B.B C.C D.D
12.淀粉和纤维素的结构如图所示,下列说法正确的是
A.淀粉和纤维素互为同分异构体
B.纤维素通过水解反应可制得纤维素硝酸酯
C.淀粉和纤维素水解都可以生成葡萄糖
D.葡萄糖、链式核糖、环式核糖中都含有醛基
13.青霉素是一种良效广谱抗生素,经酸性水解后得到青霉素氨基酸分子的结构简式如图所示,下列关于该物质的叙述不正确的是
A.属于α-氨基酸
B.既能和盐酸反应,又能和氢氧化钠溶液反应
C.核磁共振氢谱上共有6个峰
D.青霉素过敏严重者会导致死亡,用药前一定要进行皮肤敏感试验
14.下列关于高分子材料的说法错误的是
A.棉花、羊毛、蚕丝属于天然纤维
B.婴幼儿尿不湿以高吸水性树脂为原料
C.水晶饰品属于合成高分子材料
D.天然橡胶的单体是异戊二烯),结构简式为
15.下列说法正确的是
A.按系统命名法,化合物的名称为二甲基乙基庚烷
B.丙氨酸和苯丙氨酸脱水,最多可生成3种二肽
C.化合物是苯的同系物
D.三硝酸甘油酯的分子式为
二、实验题
16.1-溴丁烷,为无色透明液体,可用作溶剂及有机合成时的烷基化试剂及中间体等;实验室用1-丁醇、溴化钠和过量的浓硫酸共热制得。该反应的实验装置图(省略加热装置及夹持装置)和有关数据如下:
名称 分子量 密度g/mL 沸点(℃) 溶解性
水 乙醇 硫酸
正丁醇 74 0.810 118.0 微溶 溶 溶
正溴丁烷 137 1.275 101.6 不溶 溶 不溶
实验步骤如下:
步骤一:在A中加入20.0 mL蒸馏水,再加入30.0 mL浓H2SO4,振摇冷却至室温,再依次加入18.0mL 1-丁醇及25g NaBr,充分摇振后加入几粒碎瓷片,按上图连接装置,用小火加热至沸,回流40min(此过程中,要经常摇动)。冷却后,改成蒸馏装置,得到粗产品。
步骤二:将粗产品依次用水洗、浓H2SO4洗、水洗、饱和NaHCO3溶液洗,最后再水洗;产物移入干燥的锥形瓶中,用无水CaCl2固体间歇摇动,静置片刻,过滤除去CaCl2固体,进行蒸馏纯化,收集99~103℃馏分,得1-溴丁烷18.0g。
回答下列问题:
(1)已知本实验中发生的第一步反应为NaBr+H2SO4(浓)=HBr↑+NaHSO4,则下一步制备1-溴丁烷的化学方程式为_______。
(2)选用下图装置进行步骤二中最后的蒸馏纯化,其中仪器D的名称为_______。
(3)通过查阅资料发现实验室制取1-溴丁烷的反应有一定的可逆性,因此步骤一中加入的浓硫酸的作用除了与溴化钠反应生成溴化氢之外还有_______(从化学平衡的角度来说明)。
(4)该实验中可能生成的有机副产物是_______、_______(写结构简式)。
(5)经步骤一制得的粗产品常呈现黄色,除利用NaHCO3溶液外还可选用下列哪种试剂除去该杂质_______(填字母)。
a.NaHSO3 b.Na2SO4 c.C2H5OH d.H2O2
(6)步骤二中,用浓硫酸洗的目的是_______,用饱和碳酸氢钠溶液洗的目的是洗去硫酸等酸性物质,实验中不能用NaOH溶液来代替,原因是_______。
(7)本实验的产率是_______。(用百分数表示,结果保留三位有效数字)
17.溴乙烷是卤代烃的代表,通过对溴乙烷的探究来掌握卤代烃的性质,可以达到举一反三、触类旁通的效果。
I.已知:NaBr+H2SO4(浓)NaHSO4+ HBr
CH3CH2OH+HBrCH3CH2Br+H2O
溴乙烷的沸点38.4℃,实验室制备溴乙烷(CH3CH2Br)的装置和步骤如下:
①检查装置的气密性,向装置图所示的U形管和大烧杯中加入冰水;
②在圆底烧瓶中加入10mL95%乙醇、28mL78%浓硫酸,然后加入研细的13g溴化钠和几粒碎瓷片;
③小心加热,使其充分反应。请回答下列问题:
(1)为了更好的控制反应温度,除用图示的小火加热,更好的加热方式是___________;
(2)浓硫酸具有强氧化性,能氧化还原性气体HBr为Br2,导致U形管中粗制的溴乙烷呈棕黄色。为了除去粗产品中的杂质Br2,可选择下列试剂中的:___________(填序号)
A.Na2SO3溶液B.H2O C.CCl4
分离时所需的主要玻璃仪器是___________(填仪器名称);要进一步制得纯净的溴乙烷,可用水洗,然后加入无水CaCl2,再进行___________(填操作名称);
II.溴乙烷在不同溶剂中与NaOH可发生不同类型的反应,生成不同的反应产物。某同学依据溴乙烷的性质,用图实验装置(铁架台、酒精灯略)验证取代反应和消去反应的产物,请你一起参与探究。
(1)在试管中加入5 mL 1 mol/L NaOH水溶液和5 mL溴乙烷,将试管如图固定后,加热。
①请写出该反应的化学方程式___________;
②试管口安装一长导管的作用是___________;
(2)在试管中加入5 mL NaOH乙醇溶液和5 mL溴乙烷,将试管如图固定后,加热。为证明溴乙烷在NaOH乙醇溶液中发生的是消去反应,在设计的实验方案中,需要检验的是___________,检验的装置如图所示,在气体通入酸性高锰酸钾溶液前加一个盛水的试管,其作用是___________。
三、结构与性质
18.普卡必利可用于治疗某些肠道疾病,其合成路线如下(部分条件和产物略去):
已知:i.
ii.
iii.
(1)A→B的反应类型是_______。
(2)试剂a含有官能团的名称是_______。
(3)D→E的反应试剂和条件是_______,E→F反应的化学方程式是_______。
(4)I的核磁共振氢谱只有一组峰,J的核磁共振氢谱有两组峰,J的结构简式是_______。
(5)下列说法不正确的是_______(填序号)。
a.J→K的反应过程需要控制CH3OH不过量
b.G与FeCl3溶液作用显紫色
c.1mol普卡必利与氢氧化钠溶液反应时,最多消耗2molNaOH
d.A→B的目的是保护-NH2
(6)K→L的化学方程式为_______,该反应可逆,在实际工业生产中通常需要加入K2CO3,其作用是_______。
(7)以G和M为原料合成普卡必利时,P→Q为加成反应,写出中间产物P、Q的结构简式:_______、_______。
四、有机推断题
19.以淀粉为主要原料合成一种有机酸B的合成路线如下图所示。
(1)检验反应①是否进行完毕,可使用的试剂是___________(填序号)。
A.FeCl3溶液 B.碘水
C.新制的Cu(OH)2悬浊液 D.NaOH溶液
(2)葡萄糖的化学式为___________,反应⑤的反应类型为___________。
(3)反应②和③的化学方程式依次为___________、___________。
(4)X中溶剂为CCl4,则反应④的现象为___________。
(5)已知B的相对分子质量为118,其中碳、氢两种元素的质量分数分别为40.68%、5.08%,其余为氧元素,则B的分子式为___________。
第1页 共4页 ◎ 第2页 共4页
第1页 共4页 ◎ 第2页 共4页
参考答案:
1.B
【详解】由结构简式可知,碳酸二甲酯一定条件下能与 发生缩聚反应生成聚碳酸酯, 分子中含有2个酚羟基,属于二酚类物质,故选B。
2.B
【详解】A.浓硫酸被稀释时会释放大量热,应该先在三颈烧瓶内加入乙醇,再缓慢加入浓硫酸和苯甲酸,故A错误;
B.苯甲酸和乙醇发生酯化反应生成苯甲酸乙酯和水,当水的质量不在变化时,说明反应达到最大限度,故B正确;
C.球形冷凝管的进水应克服水的重力充满冷凝管口,方向为下进上出,即从b口进,故C错误;
D.苯甲酸乙酯在碱性环境中会发生水解,反应结束后不能用过量的溶液来除去产物中的酸性杂质,故D错误;
故选B。
3.D
【详解】A.苯与五种物质都不反应,故A不选;
B.乙醛含有醛基,能被溴水氧化,与其他物质都不反应,故B不选;
C.乙酸含有羧基,与溴水不反应,与另外几种物质均反应,故C不选;
D.丙烯酸含有碳碳双键和羧基,与NaOH溶液发生中和反应,与Na2CO3发生复分解反应生成二氧化碳,与溴水发生加成反应,与苯酚钠发生复分解反应,生成苯酚,强酸制取弱酸,和甲醇发生酯化反应,和五种物质都能反应,故D选;
答案选D。
4.A
【详解】某饱和一元醇发生消去反应的产物是单烯烃,完全加氢生成烷烃2,2,4-三甲基己烷,原一元醇能发生催化氧化反应,其可能的结构有 、 、 、 ,共4种,选A。
5.B
【详解】A.根据苯丙醛分子结构简式,可知该物质分子中含有6种不同化学环境的氢原子,A正确;
B.肉桂醛分子结构简式是,该物质分子中碳碳双键两侧均连有两种不同的原子或原子团,因此该物质存在顺反异构现象,B错误;
C.还原反应过程中H-H键、C=O键断裂,二者分别为非极性键和极性键,C正确;
D.肉桂醛在该催化条件下,只有醛基与氢气发生了加成反应,说明该催化剂可选择性还原肉桂醛中的醛基,D正确;
故合理选项是B。
6.C
【详解】A.该分子中,含有氨基,酰胺基和羧基三种官能团,A错误;
B.为高分子化合物,分子中含多个酰胺基,与不互为同系物,B错误;
C.充分水解可得到苯二胺和乙二酸两种有机小分子单体,C正确;
D.M为高分子化合物,只有苯环能和氢气反应,最多能与反应,D错误;
故选C。
7.B
【详解】A.甲中含有酚羟基和酮羰基,二者都不能与溶液反应生成,故A错误;
B.由甲、乙和丙的结构简式可以推知反应①为加成反应,故B正确;
C.物质乙所含官能团的名称为醛基,故C错误;
D.由丙和丁的结构简式可以推知丙发生消去反应生成丁,同时还有H2O生成,反应②的原子利用率不是100%,故D错误;
故选B。
8.C
【分析】丙烯和HCl发生加成反应生成CH3CH2CH2Cl,CH3CH2CH2Cl在碱性条件下发生水解生成,发生催化氧化反应生成CH3CH2CHO,CH3CH2CHO和HCHO发生已知信息的反应生成HOCH2CH(CH3)CHO,HOCH2CH(CH3)CHO发生消去反应得到CH2=C(CH3)CHO,CH2=C(CH3)CHO再和H2发生加成反应得到2-甲基-1-丙醇,以此解答。
【详解】A.CH3CH=CH2和HCl发生加成反应可以生成两种产物:CH3CHClCH3、CH3CH2CH2Cl,故A正确;
B.由分析可知,CH3CH2CH2Cl在碱性条件下发生水解生成,II的结构简式为,故B正确;
C.由分析可知,a为HCHO,HCHO是一种有毒物质,不可用作食品添加剂,故C错误;
D.由分析可知,IV为CH2=C(CH3)CHO,含有碳碳双键,能使溴水褪色,故D正确;
故选C。
9.B
【详解】A.由分子的结构可知,分子式为C17H17O2Br,A错误;
B.如图所示, 箭头指向的4个C一定共直线,B正确;
C.N中的碳卤键、酚羟基都能与NaOH的水溶液反应,因此1molN最多可消耗2molNaOH,C错误;
D.N与浓溴水反应, ,1、2处可发生取代反应,3处可发生加成反应,因此可消耗3mol溴,D错误;
故选B。
10.D
【分析】Z和发生缩聚反应生成PA,结合Z的分子式可以推知Z为,Y和CH3OH发生酯化反应生成Z,则Y为,以此解答。
【详解】A.由分析可知,Y为,含有五元环,故A正确;
B.由分析可知,Y和CH3OH发生酯化反应生成Z,②是酯化反应,故B正确;
C.由Z和PA的结构简式可以推知,Z和发生缩聚反应生成PA的过程中会生成甲醇,可循环使用,故C正确;
D.由Z和PA的结构简式可以推知,PA可发生水解反应得到,不能直接得到Z,故D错误;
故选D。
11.B
【分析】高分子化合物是相对分子质量为几万、几十万的很大的化合物;
【详解】A.淀粉是多糖,属于有机高分子,A不选;
B.油脂相对分子质量较小,不属于有机高分子B选;
C.蛋白质是由氨基酸聚合形成的有机高分子,C不选;
D.核酸是由核苷酸聚合形成的有机高分子,D不选;
故选B。
12.C
【详解】A.淀粉和纤维素都是天然高分子化合物,两者的聚合度n值不同,所以淀粉和纤维素不互为同分异构体,故A错误;
B.一定条件下纤维素与浓硝酸、浓硫酸共热发生酯化反应生成纤维素硝酸酯,故B错误;
C.一定条件下淀粉和纤维素都能发生水解反应生成葡萄糖,故C正确;
D.环式核糖中不含有醛基,故D错误;
故选C。
13.C
【详解】A.该物质分子中含有的氨基、羧基都连接在同一个C原子上,因此都是属于α-氨基酸,A正确;
B.该物质分子中含有氨基,能够与盐酸发生反应;含有羧基,因此能够与NaOH溶液发生反应,B正确;
C.根据物质结构简式可知:其分子中含有5种不同的H原子,因此核磁共振氢谱上共有5个峰,C错误;
D.有些人对青霉素有过敏反应,严重者会导致死亡,因此用药前一定要进行皮肤敏感试验,D正确;
故合理选项是C。
14.C
【详解】A.棉花是天然植物纤维,羊毛和蚕丝为天然动物纤维,A正确;
B.高吸水树脂是具有一定交联程度的高聚物,它能够很快吸收比自身重量大数百倍的水形成凝胶,可用于生成婴幼儿尿不湿,B正确;
C.水晶的主要成分是二氧化硅,不属于合成高分子材料,C错误;
D.异戊二烯( )发生加聚反应生成天然橡胶( ),故天然橡胶的单体是异戊二烯,D正确;
答案选C。
15.D
【详解】A.按系统命名法,化合物书写为,其名称为二甲基乙基庚烷,故A错误;
B.丙氨酸和苯丙氨酸脱水,丙氨酸自身生成二肽一种,苯丙氨酸自身生成二肽一种,丙氨酸的羧基和苯丙氨酸的氨基生成二肽一种,丙氨酸的氨基和苯丙氨酸的羧基生成二肽一种,最多可生成4种二肽,故B错误;
C.苯的同系物是含有一个苯环,烷烃取代苯环上的氢原子,因此化合物不是苯的同系物,故C错误;
D.1mol甘油和3mol硝酸发生酯化反应得到1mol三硝酸甘油酯和3mol水,因此三硝酸甘油酯分子式为,故D正确。
综上所述,答案为D。
16. CH3CH2CH2CH2OH+HBrCH3CH2CH2CH2Br+H2O 蒸馏烧瓶 浓硫酸有吸水性,吸收生成的水,使平衡正向移动,提高产率 CH3CH2CH=CH2 CH3CH2CH2CH2OCH2CH2CH2CH3 a 洗去未反应的1-丁醇 碱性过强,1-溴丁烷会水解,降低产率 66.7%
【分析】NaBr和浓H2SO4反应生成HBr,HBr与正丁醇反应可制备1-溴丁烷,化学方程式为CH3CH2CH2CH2OH+HBrCH3CH2CH2CH2Br+H2O,蒸馏得到粗产品,将粗产品用水洗后,用浓硫酸洗,洗去未反应的1-丁醇,再用水洗,除去浓硫酸,用饱和NaHCO3溶液洗,除去Br2,再用水洗,除去NaHCO3,将产物移入干燥的锥形瓶中,用无水CaCl2固体间歇摇动,静置片刻,过滤除去CaCl2固体,除去产物中的水,进行蒸馏纯化,收集99~103℃馏分,得1-溴丁烷。
【详解】(1)第一步制备HBr后,HBr与正丁醇反应可制备1-溴丁烷,化学方程式为CH3CH2CH2CH2OH+HBrCH3CH2CH2CH2Br+H2O;
(2)仪器D是蒸馏烧瓶;
(3)制取1-溴丁烷的反应有一定的可逆性,浓硫酸有吸水性,吸收生成的水,使平衡正向移动,提高产率;
(4)1-丁醇在浓硫酸加热的条件下能发生消去反应生成CH3CH2CH=CH2,1-丁醇在浓硫酸加热的条件下还可分子间脱水生成CH3CH2CH2CH2OCH2CH2CH2CH3,则该实验中可能生成的有机副产物是:CH3CH2CH=CH2、CH3CH2CH2CH2OCH2CH2CH2CH3;
(5)经步骤一制得的粗产品常呈现黄色主要是因为产物中混有副产物溴,除了用碳酸氢钠洗去溴外,还可以用亚硫酸氢钠洗去溴,答案选a;
(6)步骤二中,用浓硫酸洗的目的是洗去未反应的1-丁醇;若用氢氧化钠洗涤,碱性过强,1-溴丁烷会水解,降低产率;
(7)加入1-丁醇的物质的量为,则理论上生成1-溴丁烷的物质的量为,则产率为。
17. 水浴加热 A 分液漏斗 蒸馏 CH3CH2Br+NaOHCH3CH2OH+NaBr 冷凝回流减少溴乙烷的损失 乙烯 除去乙烯中混有的乙醇
【分析】I.用水浴加热使烧瓶均匀受热,溴化钠、浓硫酸在烧瓶中反应产生HBr,HBr和乙醇在烧瓶中反应产生溴乙烷,溴乙烷的沸点较低,挥发到U形管中用冰水冷凝得到液态的溴乙烷;
II.溴乙烷在NaOH水溶液中发生取代反应产生乙醇,在NaOH醇溶液中发生消去反应产生乙烯,可用溴的水溶液、溴的四氯化碳溶液、或除去乙醇后通入酸性高锰酸钾溶液检验发生的是消去反应。
【详解】I.(1)为了更好的控制温度,除用图示的小火加热外,最好用水浴加热的方法;
(2)在U形管内有Br2:
A. Na2SO3能与溴发生氧化还原反应,可除去溴,A项符合题意;
B.溴在水中的溶解度小于在溴乙烷中的溶解度,无法加水除杂,B项不符合题意;
C.溴和溴乙烷都能溶于四氯化碳,不能将二者分离,C项不符合题意;
答案选A;
加入Na2SO3溶液反应,静置、分层、然后分液,使用的主要仪器是分液漏斗;
要进一步制得纯净的C2H5Br,可用水洗,分液后再加入无水CaCl2,利用沸点不同再进行蒸馏;
II.(1)①溴乙烷在NaOH水溶液中加热发生取代反应,反应的化学方程式为CH3CH2Br+NaOHCH3CH2OH+NaBr;
②溴乙烷的沸点38.4℃,溴乙烷易挥发,用长导管进行冷凝回流减少溴乙烷的损失;
(2)溴乙烷在NaOH乙醇溶液中加热发生消去反应产生乙烯,因此为证明溴乙烷在NaOH乙醇溶液中发生的是消去反应,需检验乙烯;
检验乙烯可根据其能使酸性高锰酸钾褪色的原理进行,但同时乙醇易挥发且能使酸性高锰酸钾褪色,故需要除去乙烯中的乙醇,乙醇能溶于水,而乙烯不能溶于水,故在气体通入酸性高锰酸钾溶液前加一个盛水的试管,其作用是除去乙烯中混有的乙醇。
18.(1)取代反应
(2)羟基
(3) Cl2、FeCl3 +Br2+HBr
(4)BrCH2CH2CH2Br
(5)bc
(6) H3COCH2CH2CH2Br++HBr 促进平衡正向移动,提高原料的利用率
(7)
【分析】由A()及F()的结构简式,可确定B为,D为,E为,G为,M为,L为。I为,J为BrCH2CH2CH2Br,K为H3COCH2CH2CH2Br。
【详解】(1)由A()+(CH3CO)2O→B()+CH3COOH,反应类型是取代反应。答案为:取代反应;
(2)B为,D为,则试剂a为HOCH2CH2OH,含有官能团的名称是羟基。答案为:羟基;
(3)D()→E(),是苯环上发生的取代反应,反应试剂和条件是Cl2、FeCl3,E()→F(),是侧链上发生取代反应,反应的化学方程式是+Br2+HBr。答案为:Cl2、FeCl3;+Br2+HBr;
(4)I的核磁共振氢谱只有一组峰,则I为,J的核磁共振氢谱有两组峰,J的结构简式是BrCH2CH2CH2Br。答案为:BrCH2CH2CH2Br;
(5)a.J(BrCH2CH2CH2Br)→K(H3COCH2CH2CH2Br)的反应过程,若CH3OH足量,则会生成另一种副产物CH3OCH2CH2CH2OCH3,所以需要控制CH3OH不过量,A正确;
b.G()分子中不含有酚羟基,不能与FeCl3溶液作用,b不正确;
c.1mol普卡必利与氢氧化钠溶液反应时,酰胺键、碳氯键都能与NaOH发生反应,最多消耗3molNaOH,c不正确;
d.A()→B(),在后绪反应中,-NHCOCH3又转化为-NH2,则表明目的是保护-NH2,d正确;
故选bc。答案为:bc;
(6)K(H3COCH2CH2CH2Br)与反应→L()和HBr,化学方程式为H3COCH2CH2CH2Br++HBr,该反应可逆,在实际工业生产中通常需要加入K2CO3,可与反应生成的HBr反应,从而促进平衡正向移动,所以其作用是:促进平衡正向移动,提高原料的利用率。答案为:H3COCH2CH2CH2Br++HBr;促进平衡正向移动,提高原料的利用率;
(7)G为,由P的分子式,可确定P为,M为,则Q为。答案为:;。
【点睛】由已知有机物推断未知有机物时,既可采用顺推法,也可采用逆推法。
19. B C6H12O6 取代反应 2C2H5OH+O2 2CH3CHO+2H2O C2H5OH CH2=CH2↑+H2O 溴的四氯化碳溶液变浅或褪色 C4H6O4
【分析】本流程的目的是以淀粉为原料,通过水解、氧化、消去等一系列过程制取丁二酸,先将淀粉在无机酸的催化作用下制取葡萄糖,再将葡萄糖在酒化酶的催化作用下分解为乙醇和二氧化碳,乙醇催化氧化可制得乙醛(A);乙醇在浓硫酸、170℃的条件下发生消去反应生成乙烯和水,乙烯与溴的四氯化碳溶液发生加成反应生成BrCH2CH2Br,BrCH2CH2Br与NaCN发生取代反应生成NCCH2CH2CN,NCCH2CH2CN在酸性条件下水解,便可得到HOOCCH2CH2COOH。
【详解】(1)检验反应①是否进行完毕,需要检验淀粉是否存在,所以可使用的试剂是碘水,故选B。答案为:B;
(2)葡萄糖由淀粉(C6H10O5)n水解生成,所以葡萄糖的化学式为C6H12O6,反应⑤为BrCH2CH2Br与NaCN发生反应生成NCCH2CH2CN和NaBr,所以反应类型为取代反应。答案为:C6H12O6;取代反应;
(3)反应②为乙醇催化氧化可制得乙醛,反应③为乙醇在浓硫酸、170℃的条件下发生消去反应生成乙烯和水,化学方程式依次为2C2H5OH+O2 2CH3CHO+2H2O、C2H5OH CH2=CH2↑+H2O。答案为:2C2H5OH+O2 2CH3CHO+2H2O;C2H5OH CH2=CH2↑+H2O;
(4)X中溶剂为CCl4,发生的是CH2=CH2与Br2的加成反应,生成物BrCH2CH2Br呈无色,则反应④的现象为溴的四氯化碳溶液变浅或褪色。答案为:溴的四氯化碳溶液变浅或褪色;
(5)1mol有机物B中,含碳原子的物质的量为mol≈4mol,含氢原子的物质的量为mol≈6mol,含氧原子的物质的量为mol≈4mol,从而得出B的分子式为C4H6O4。答案为:C4H6O4。
【点睛】在书写乙醇的消去反应时,反应条件一定要指明“浓硫酸、170℃”。
答案第1页,共2页
答案第1页,共2页
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1.某种聚碳酸酯的透光性好,可制成车、船的挡风玻璃,以及眼镜镜片、光盘等,其结构可表示为: ,原来合成聚碳酸酯的一种原料是有毒的光气(,又称碳酰氯)。为贯彻绿色化学理念,可以改用碳酸二甲酯()与什么缩合聚合生产聚碳酸酯
A.二卤化物 B.二酚类物质 C.二醇类物质 D.二烯类物质
2.实验室制备苯甲酸乙酯的反应装置示意图(夹持和加热装置已略去)和有关信息如下,下列说法正确的是
物质 密度/() 熔点/ 沸点/ 溶解性
苯甲酸 1.08 122 249 不溶于冷水,溶于乙醇
乙醇 0.79 78.5 与水任意比互溶
苯甲酸乙酯 1.04 212 不溶于水,溶于乙醇、乙醚等
A.先在三颈烧瓶内加入浓硫酸,再缓慢加入苯甲酸和乙醇
B.当分水器中水层高度不再上升时,反应达到最大限度
C.球形冷凝管的进水口为a
D.反应结束后可用过量的溶液来除去产物中的酸性杂质
3.下列物质中,与NaOH溶液、Na2CO3溶液、溴水、苯酚钠溶液和甲醇都能反应的是
A.苯 B.CH3CHO C.CH3COOH D.CH2=CHCOOH
4.某饱和一元醇发生消去反应后的产物完全加氢,可以得到 2,2,4-三甲基己烷,已知原一元醇能发生催化氧化反应,其可能的结构有
A.4 种 B.3 种 C.2 种 D.1 种
5.我国科研人员使用某种催化剂实现了H2还原肉桂醛生成肉桂醇,反应机理如图所示:
下列说法不正确的是
A.苯丙醛分子中有6种不同化学环境的氢原子
B.肉桂醛分子中不存在顺反异构现象
C.还原反应过程发生了极性键和非极性键的断裂
D.该催化剂实现了选择性还原肉桂醛中的醛基
6.化合物是一种重要的有机高分子材料。下列关于M的说法正确的是
A.含有两种官能团 B.与互为同系物
C.充分水解可得到两种有机小分子单体 D.最多能与反应
7.黄酮类化合物具有广泛的药理作用,如抗氧化、降血压、抗肿瘤等,2-羟基查尔酮是黄酮类化合物的一种重要中间体,它的一种合成路线如图所示。下列说法正确的是
A.甲能与溶液反应生成 B.反应①为加成反应
C.物质乙所含官能团的名称为酮羰基 D.反应②的原子利用率为100%
8.已知;以丙烯为原料合成2-甲基-1-丙醇的过程如下,丙烯2-甲基-1-丙醇。下列说法错误的是
A.丙烯→I的反应可生成两种产物 B.II的结构简式为
C.试剂a可用作食品添加剂 D.IV能使溴水褪色
9.有机化合物N可用于早期诊断阿兹海默症,其结构简式如下:
下列关于N的说法正确的是
A.分子式为
B.分子中共线的碳原子最多有4个
C.能与NaOH水溶液反应,1molN最多可消耗1molNaOH
D.能与浓溴水反应,1molN最多可消耗
10.聚酰胺(PA)具有良好的力学性能,一种合成路线如下图所示。下列说法不正确的是。
A.Y中含有五元环 B.②是酯化反应
C.该合成路线中甲醇可循环使用 D.PA可发生水解反应重新生成Z
11.下列物质中,不属于有机高分子的是
A.淀粉 B.油脂 C.蛋白质 D.核酸
A.A B.B C.C D.D
12.淀粉和纤维素的结构如图所示,下列说法正确的是
A.淀粉和纤维素互为同分异构体
B.纤维素通过水解反应可制得纤维素硝酸酯
C.淀粉和纤维素水解都可以生成葡萄糖
D.葡萄糖、链式核糖、环式核糖中都含有醛基
13.青霉素是一种良效广谱抗生素,经酸性水解后得到青霉素氨基酸分子的结构简式如图所示,下列关于该物质的叙述不正确的是
A.属于α-氨基酸
B.既能和盐酸反应,又能和氢氧化钠溶液反应
C.核磁共振氢谱上共有6个峰
D.青霉素过敏严重者会导致死亡,用药前一定要进行皮肤敏感试验
14.下列关于高分子材料的说法错误的是
A.棉花、羊毛、蚕丝属于天然纤维
B.婴幼儿尿不湿以高吸水性树脂为原料
C.水晶饰品属于合成高分子材料
D.天然橡胶的单体是异戊二烯),结构简式为
15.下列说法正确的是
A.按系统命名法,化合物的名称为二甲基乙基庚烷
B.丙氨酸和苯丙氨酸脱水,最多可生成3种二肽
C.化合物是苯的同系物
D.三硝酸甘油酯的分子式为
二、实验题
16.1-溴丁烷,为无色透明液体,可用作溶剂及有机合成时的烷基化试剂及中间体等;实验室用1-丁醇、溴化钠和过量的浓硫酸共热制得。该反应的实验装置图(省略加热装置及夹持装置)和有关数据如下:
名称 分子量 密度g/mL 沸点(℃) 溶解性
水 乙醇 硫酸
正丁醇 74 0.810 118.0 微溶 溶 溶
正溴丁烷 137 1.275 101.6 不溶 溶 不溶
实验步骤如下:
步骤一:在A中加入20.0 mL蒸馏水,再加入30.0 mL浓H2SO4,振摇冷却至室温,再依次加入18.0mL 1-丁醇及25g NaBr,充分摇振后加入几粒碎瓷片,按上图连接装置,用小火加热至沸,回流40min(此过程中,要经常摇动)。冷却后,改成蒸馏装置,得到粗产品。
步骤二:将粗产品依次用水洗、浓H2SO4洗、水洗、饱和NaHCO3溶液洗,最后再水洗;产物移入干燥的锥形瓶中,用无水CaCl2固体间歇摇动,静置片刻,过滤除去CaCl2固体,进行蒸馏纯化,收集99~103℃馏分,得1-溴丁烷18.0g。
回答下列问题:
(1)已知本实验中发生的第一步反应为NaBr+H2SO4(浓)=HBr↑+NaHSO4,则下一步制备1-溴丁烷的化学方程式为_______。
(2)选用下图装置进行步骤二中最后的蒸馏纯化,其中仪器D的名称为_______。
(3)通过查阅资料发现实验室制取1-溴丁烷的反应有一定的可逆性,因此步骤一中加入的浓硫酸的作用除了与溴化钠反应生成溴化氢之外还有_______(从化学平衡的角度来说明)。
(4)该实验中可能生成的有机副产物是_______、_______(写结构简式)。
(5)经步骤一制得的粗产品常呈现黄色,除利用NaHCO3溶液外还可选用下列哪种试剂除去该杂质_______(填字母)。
a.NaHSO3 b.Na2SO4 c.C2H5OH d.H2O2
(6)步骤二中,用浓硫酸洗的目的是_______,用饱和碳酸氢钠溶液洗的目的是洗去硫酸等酸性物质,实验中不能用NaOH溶液来代替,原因是_______。
(7)本实验的产率是_______。(用百分数表示,结果保留三位有效数字)
17.溴乙烷是卤代烃的代表,通过对溴乙烷的探究来掌握卤代烃的性质,可以达到举一反三、触类旁通的效果。
I.已知:NaBr+H2SO4(浓)NaHSO4+ HBr
CH3CH2OH+HBrCH3CH2Br+H2O
溴乙烷的沸点38.4℃,实验室制备溴乙烷(CH3CH2Br)的装置和步骤如下:
①检查装置的气密性,向装置图所示的U形管和大烧杯中加入冰水;
②在圆底烧瓶中加入10mL95%乙醇、28mL78%浓硫酸,然后加入研细的13g溴化钠和几粒碎瓷片;
③小心加热,使其充分反应。请回答下列问题:
(1)为了更好的控制反应温度,除用图示的小火加热,更好的加热方式是___________;
(2)浓硫酸具有强氧化性,能氧化还原性气体HBr为Br2,导致U形管中粗制的溴乙烷呈棕黄色。为了除去粗产品中的杂质Br2,可选择下列试剂中的:___________(填序号)
A.Na2SO3溶液B.H2O C.CCl4
分离时所需的主要玻璃仪器是___________(填仪器名称);要进一步制得纯净的溴乙烷,可用水洗,然后加入无水CaCl2,再进行___________(填操作名称);
II.溴乙烷在不同溶剂中与NaOH可发生不同类型的反应,生成不同的反应产物。某同学依据溴乙烷的性质,用图实验装置(铁架台、酒精灯略)验证取代反应和消去反应的产物,请你一起参与探究。
(1)在试管中加入5 mL 1 mol/L NaOH水溶液和5 mL溴乙烷,将试管如图固定后,加热。
①请写出该反应的化学方程式___________;
②试管口安装一长导管的作用是___________;
(2)在试管中加入5 mL NaOH乙醇溶液和5 mL溴乙烷,将试管如图固定后,加热。为证明溴乙烷在NaOH乙醇溶液中发生的是消去反应,在设计的实验方案中,需要检验的是___________,检验的装置如图所示,在气体通入酸性高锰酸钾溶液前加一个盛水的试管,其作用是___________。
三、结构与性质
18.普卡必利可用于治疗某些肠道疾病,其合成路线如下(部分条件和产物略去):
已知:i.
ii.
iii.
(1)A→B的反应类型是_______。
(2)试剂a含有官能团的名称是_______。
(3)D→E的反应试剂和条件是_______,E→F反应的化学方程式是_______。
(4)I的核磁共振氢谱只有一组峰,J的核磁共振氢谱有两组峰,J的结构简式是_______。
(5)下列说法不正确的是_______(填序号)。
a.J→K的反应过程需要控制CH3OH不过量
b.G与FeCl3溶液作用显紫色
c.1mol普卡必利与氢氧化钠溶液反应时,最多消耗2molNaOH
d.A→B的目的是保护-NH2
(6)K→L的化学方程式为_______,该反应可逆,在实际工业生产中通常需要加入K2CO3,其作用是_______。
(7)以G和M为原料合成普卡必利时,P→Q为加成反应,写出中间产物P、Q的结构简式:_______、_______。
四、有机推断题
19.以淀粉为主要原料合成一种有机酸B的合成路线如下图所示。
(1)检验反应①是否进行完毕,可使用的试剂是___________(填序号)。
A.FeCl3溶液 B.碘水
C.新制的Cu(OH)2悬浊液 D.NaOH溶液
(2)葡萄糖的化学式为___________,反应⑤的反应类型为___________。
(3)反应②和③的化学方程式依次为___________、___________。
(4)X中溶剂为CCl4,则反应④的现象为___________。
(5)已知B的相对分子质量为118,其中碳、氢两种元素的质量分数分别为40.68%、5.08%,其余为氧元素,则B的分子式为___________。
第1页 共4页 ◎ 第2页 共4页
第1页 共4页 ◎ 第2页 共4页
参考答案:
1.B
【详解】由结构简式可知,碳酸二甲酯一定条件下能与 发生缩聚反应生成聚碳酸酯, 分子中含有2个酚羟基,属于二酚类物质,故选B。
2.B
【详解】A.浓硫酸被稀释时会释放大量热,应该先在三颈烧瓶内加入乙醇,再缓慢加入浓硫酸和苯甲酸,故A错误;
B.苯甲酸和乙醇发生酯化反应生成苯甲酸乙酯和水,当水的质量不在变化时,说明反应达到最大限度,故B正确;
C.球形冷凝管的进水应克服水的重力充满冷凝管口,方向为下进上出,即从b口进,故C错误;
D.苯甲酸乙酯在碱性环境中会发生水解,反应结束后不能用过量的溶液来除去产物中的酸性杂质,故D错误;
故选B。
3.D
【详解】A.苯与五种物质都不反应,故A不选;
B.乙醛含有醛基,能被溴水氧化,与其他物质都不反应,故B不选;
C.乙酸含有羧基,与溴水不反应,与另外几种物质均反应,故C不选;
D.丙烯酸含有碳碳双键和羧基,与NaOH溶液发生中和反应,与Na2CO3发生复分解反应生成二氧化碳,与溴水发生加成反应,与苯酚钠发生复分解反应,生成苯酚,强酸制取弱酸,和甲醇发生酯化反应,和五种物质都能反应,故D选;
答案选D。
4.A
【详解】某饱和一元醇发生消去反应的产物是单烯烃,完全加氢生成烷烃2,2,4-三甲基己烷,原一元醇能发生催化氧化反应,其可能的结构有 、 、 、 ,共4种,选A。
5.B
【详解】A.根据苯丙醛分子结构简式,可知该物质分子中含有6种不同化学环境的氢原子,A正确;
B.肉桂醛分子结构简式是,该物质分子中碳碳双键两侧均连有两种不同的原子或原子团,因此该物质存在顺反异构现象,B错误;
C.还原反应过程中H-H键、C=O键断裂,二者分别为非极性键和极性键,C正确;
D.肉桂醛在该催化条件下,只有醛基与氢气发生了加成反应,说明该催化剂可选择性还原肉桂醛中的醛基,D正确;
故合理选项是B。
6.C
【详解】A.该分子中,含有氨基,酰胺基和羧基三种官能团,A错误;
B.为高分子化合物,分子中含多个酰胺基,与不互为同系物,B错误;
C.充分水解可得到苯二胺和乙二酸两种有机小分子单体,C正确;
D.M为高分子化合物,只有苯环能和氢气反应,最多能与反应,D错误;
故选C。
7.B
【详解】A.甲中含有酚羟基和酮羰基,二者都不能与溶液反应生成,故A错误;
B.由甲、乙和丙的结构简式可以推知反应①为加成反应,故B正确;
C.物质乙所含官能团的名称为醛基,故C错误;
D.由丙和丁的结构简式可以推知丙发生消去反应生成丁,同时还有H2O生成,反应②的原子利用率不是100%,故D错误;
故选B。
8.C
【分析】丙烯和HCl发生加成反应生成CH3CH2CH2Cl,CH3CH2CH2Cl在碱性条件下发生水解生成,发生催化氧化反应生成CH3CH2CHO,CH3CH2CHO和HCHO发生已知信息的反应生成HOCH2CH(CH3)CHO,HOCH2CH(CH3)CHO发生消去反应得到CH2=C(CH3)CHO,CH2=C(CH3)CHO再和H2发生加成反应得到2-甲基-1-丙醇,以此解答。
【详解】A.CH3CH=CH2和HCl发生加成反应可以生成两种产物:CH3CHClCH3、CH3CH2CH2Cl,故A正确;
B.由分析可知,CH3CH2CH2Cl在碱性条件下发生水解生成,II的结构简式为,故B正确;
C.由分析可知,a为HCHO,HCHO是一种有毒物质,不可用作食品添加剂,故C错误;
D.由分析可知,IV为CH2=C(CH3)CHO,含有碳碳双键,能使溴水褪色,故D正确;
故选C。
9.B
【详解】A.由分子的结构可知,分子式为C17H17O2Br,A错误;
B.如图所示, 箭头指向的4个C一定共直线,B正确;
C.N中的碳卤键、酚羟基都能与NaOH的水溶液反应,因此1molN最多可消耗2molNaOH,C错误;
D.N与浓溴水反应, ,1、2处可发生取代反应,3处可发生加成反应,因此可消耗3mol溴,D错误;
故选B。
10.D
【分析】Z和发生缩聚反应生成PA,结合Z的分子式可以推知Z为,Y和CH3OH发生酯化反应生成Z,则Y为,以此解答。
【详解】A.由分析可知,Y为,含有五元环,故A正确;
B.由分析可知,Y和CH3OH发生酯化反应生成Z,②是酯化反应,故B正确;
C.由Z和PA的结构简式可以推知,Z和发生缩聚反应生成PA的过程中会生成甲醇,可循环使用,故C正确;
D.由Z和PA的结构简式可以推知,PA可发生水解反应得到,不能直接得到Z,故D错误;
故选D。
11.B
【分析】高分子化合物是相对分子质量为几万、几十万的很大的化合物;
【详解】A.淀粉是多糖,属于有机高分子,A不选;
B.油脂相对分子质量较小,不属于有机高分子B选;
C.蛋白质是由氨基酸聚合形成的有机高分子,C不选;
D.核酸是由核苷酸聚合形成的有机高分子,D不选;
故选B。
12.C
【详解】A.淀粉和纤维素都是天然高分子化合物,两者的聚合度n值不同,所以淀粉和纤维素不互为同分异构体,故A错误;
B.一定条件下纤维素与浓硝酸、浓硫酸共热发生酯化反应生成纤维素硝酸酯,故B错误;
C.一定条件下淀粉和纤维素都能发生水解反应生成葡萄糖,故C正确;
D.环式核糖中不含有醛基,故D错误;
故选C。
13.C
【详解】A.该物质分子中含有的氨基、羧基都连接在同一个C原子上,因此都是属于α-氨基酸,A正确;
B.该物质分子中含有氨基,能够与盐酸发生反应;含有羧基,因此能够与NaOH溶液发生反应,B正确;
C.根据物质结构简式可知:其分子中含有5种不同的H原子,因此核磁共振氢谱上共有5个峰,C错误;
D.有些人对青霉素有过敏反应,严重者会导致死亡,因此用药前一定要进行皮肤敏感试验,D正确;
故合理选项是C。
14.C
【详解】A.棉花是天然植物纤维,羊毛和蚕丝为天然动物纤维,A正确;
B.高吸水树脂是具有一定交联程度的高聚物,它能够很快吸收比自身重量大数百倍的水形成凝胶,可用于生成婴幼儿尿不湿,B正确;
C.水晶的主要成分是二氧化硅,不属于合成高分子材料,C错误;
D.异戊二烯( )发生加聚反应生成天然橡胶( ),故天然橡胶的单体是异戊二烯,D正确;
答案选C。
15.D
【详解】A.按系统命名法,化合物书写为,其名称为二甲基乙基庚烷,故A错误;
B.丙氨酸和苯丙氨酸脱水,丙氨酸自身生成二肽一种,苯丙氨酸自身生成二肽一种,丙氨酸的羧基和苯丙氨酸的氨基生成二肽一种,丙氨酸的氨基和苯丙氨酸的羧基生成二肽一种,最多可生成4种二肽,故B错误;
C.苯的同系物是含有一个苯环,烷烃取代苯环上的氢原子,因此化合物不是苯的同系物,故C错误;
D.1mol甘油和3mol硝酸发生酯化反应得到1mol三硝酸甘油酯和3mol水,因此三硝酸甘油酯分子式为,故D正确。
综上所述,答案为D。
16. CH3CH2CH2CH2OH+HBrCH3CH2CH2CH2Br+H2O 蒸馏烧瓶 浓硫酸有吸水性,吸收生成的水,使平衡正向移动,提高产率 CH3CH2CH=CH2 CH3CH2CH2CH2OCH2CH2CH2CH3 a 洗去未反应的1-丁醇 碱性过强,1-溴丁烷会水解,降低产率 66.7%
【分析】NaBr和浓H2SO4反应生成HBr,HBr与正丁醇反应可制备1-溴丁烷,化学方程式为CH3CH2CH2CH2OH+HBrCH3CH2CH2CH2Br+H2O,蒸馏得到粗产品,将粗产品用水洗后,用浓硫酸洗,洗去未反应的1-丁醇,再用水洗,除去浓硫酸,用饱和NaHCO3溶液洗,除去Br2,再用水洗,除去NaHCO3,将产物移入干燥的锥形瓶中,用无水CaCl2固体间歇摇动,静置片刻,过滤除去CaCl2固体,除去产物中的水,进行蒸馏纯化,收集99~103℃馏分,得1-溴丁烷。
【详解】(1)第一步制备HBr后,HBr与正丁醇反应可制备1-溴丁烷,化学方程式为CH3CH2CH2CH2OH+HBrCH3CH2CH2CH2Br+H2O;
(2)仪器D是蒸馏烧瓶;
(3)制取1-溴丁烷的反应有一定的可逆性,浓硫酸有吸水性,吸收生成的水,使平衡正向移动,提高产率;
(4)1-丁醇在浓硫酸加热的条件下能发生消去反应生成CH3CH2CH=CH2,1-丁醇在浓硫酸加热的条件下还可分子间脱水生成CH3CH2CH2CH2OCH2CH2CH2CH3,则该实验中可能生成的有机副产物是:CH3CH2CH=CH2、CH3CH2CH2CH2OCH2CH2CH2CH3;
(5)经步骤一制得的粗产品常呈现黄色主要是因为产物中混有副产物溴,除了用碳酸氢钠洗去溴外,还可以用亚硫酸氢钠洗去溴,答案选a;
(6)步骤二中,用浓硫酸洗的目的是洗去未反应的1-丁醇;若用氢氧化钠洗涤,碱性过强,1-溴丁烷会水解,降低产率;
(7)加入1-丁醇的物质的量为,则理论上生成1-溴丁烷的物质的量为,则产率为。
17. 水浴加热 A 分液漏斗 蒸馏 CH3CH2Br+NaOHCH3CH2OH+NaBr 冷凝回流减少溴乙烷的损失 乙烯 除去乙烯中混有的乙醇
【分析】I.用水浴加热使烧瓶均匀受热,溴化钠、浓硫酸在烧瓶中反应产生HBr,HBr和乙醇在烧瓶中反应产生溴乙烷,溴乙烷的沸点较低,挥发到U形管中用冰水冷凝得到液态的溴乙烷;
II.溴乙烷在NaOH水溶液中发生取代反应产生乙醇,在NaOH醇溶液中发生消去反应产生乙烯,可用溴的水溶液、溴的四氯化碳溶液、或除去乙醇后通入酸性高锰酸钾溶液检验发生的是消去反应。
【详解】I.(1)为了更好的控制温度,除用图示的小火加热外,最好用水浴加热的方法;
(2)在U形管内有Br2:
A. Na2SO3能与溴发生氧化还原反应,可除去溴,A项符合题意;
B.溴在水中的溶解度小于在溴乙烷中的溶解度,无法加水除杂,B项不符合题意;
C.溴和溴乙烷都能溶于四氯化碳,不能将二者分离,C项不符合题意;
答案选A;
加入Na2SO3溶液反应,静置、分层、然后分液,使用的主要仪器是分液漏斗;
要进一步制得纯净的C2H5Br,可用水洗,分液后再加入无水CaCl2,利用沸点不同再进行蒸馏;
II.(1)①溴乙烷在NaOH水溶液中加热发生取代反应,反应的化学方程式为CH3CH2Br+NaOHCH3CH2OH+NaBr;
②溴乙烷的沸点38.4℃,溴乙烷易挥发,用长导管进行冷凝回流减少溴乙烷的损失;
(2)溴乙烷在NaOH乙醇溶液中加热发生消去反应产生乙烯,因此为证明溴乙烷在NaOH乙醇溶液中发生的是消去反应,需检验乙烯;
检验乙烯可根据其能使酸性高锰酸钾褪色的原理进行,但同时乙醇易挥发且能使酸性高锰酸钾褪色,故需要除去乙烯中的乙醇,乙醇能溶于水,而乙烯不能溶于水,故在气体通入酸性高锰酸钾溶液前加一个盛水的试管,其作用是除去乙烯中混有的乙醇。
18.(1)取代反应
(2)羟基
(3) Cl2、FeCl3 +Br2+HBr
(4)BrCH2CH2CH2Br
(5)bc
(6) H3COCH2CH2CH2Br++HBr 促进平衡正向移动,提高原料的利用率
(7)
【分析】由A()及F()的结构简式,可确定B为,D为,E为,G为,M为,L为。I为,J为BrCH2CH2CH2Br,K为H3COCH2CH2CH2Br。
【详解】(1)由A()+(CH3CO)2O→B()+CH3COOH,反应类型是取代反应。答案为:取代反应;
(2)B为,D为,则试剂a为HOCH2CH2OH,含有官能团的名称是羟基。答案为:羟基;
(3)D()→E(),是苯环上发生的取代反应,反应试剂和条件是Cl2、FeCl3,E()→F(),是侧链上发生取代反应,反应的化学方程式是+Br2+HBr。答案为:Cl2、FeCl3;+Br2+HBr;
(4)I的核磁共振氢谱只有一组峰,则I为,J的核磁共振氢谱有两组峰,J的结构简式是BrCH2CH2CH2Br。答案为:BrCH2CH2CH2Br;
(5)a.J(BrCH2CH2CH2Br)→K(H3COCH2CH2CH2Br)的反应过程,若CH3OH足量,则会生成另一种副产物CH3OCH2CH2CH2OCH3,所以需要控制CH3OH不过量,A正确;
b.G()分子中不含有酚羟基,不能与FeCl3溶液作用,b不正确;
c.1mol普卡必利与氢氧化钠溶液反应时,酰胺键、碳氯键都能与NaOH发生反应,最多消耗3molNaOH,c不正确;
d.A()→B(),在后绪反应中,-NHCOCH3又转化为-NH2,则表明目的是保护-NH2,d正确;
故选bc。答案为:bc;
(6)K(H3COCH2CH2CH2Br)与反应→L()和HBr,化学方程式为H3COCH2CH2CH2Br++HBr,该反应可逆,在实际工业生产中通常需要加入K2CO3,可与反应生成的HBr反应,从而促进平衡正向移动,所以其作用是:促进平衡正向移动,提高原料的利用率。答案为:H3COCH2CH2CH2Br++HBr;促进平衡正向移动,提高原料的利用率;
(7)G为,由P的分子式,可确定P为,M为,则Q为。答案为:;。
【点睛】由已知有机物推断未知有机物时,既可采用顺推法,也可采用逆推法。
19. B C6H12O6 取代反应 2C2H5OH+O2 2CH3CHO+2H2O C2H5OH CH2=CH2↑+H2O 溴的四氯化碳溶液变浅或褪色 C4H6O4
【分析】本流程的目的是以淀粉为原料,通过水解、氧化、消去等一系列过程制取丁二酸,先将淀粉在无机酸的催化作用下制取葡萄糖,再将葡萄糖在酒化酶的催化作用下分解为乙醇和二氧化碳,乙醇催化氧化可制得乙醛(A);乙醇在浓硫酸、170℃的条件下发生消去反应生成乙烯和水,乙烯与溴的四氯化碳溶液发生加成反应生成BrCH2CH2Br,BrCH2CH2Br与NaCN发生取代反应生成NCCH2CH2CN,NCCH2CH2CN在酸性条件下水解,便可得到HOOCCH2CH2COOH。
【详解】(1)检验反应①是否进行完毕,需要检验淀粉是否存在,所以可使用的试剂是碘水,故选B。答案为:B;
(2)葡萄糖由淀粉(C6H10O5)n水解生成,所以葡萄糖的化学式为C6H12O6,反应⑤为BrCH2CH2Br与NaCN发生反应生成NCCH2CH2CN和NaBr,所以反应类型为取代反应。答案为:C6H12O6;取代反应;
(3)反应②为乙醇催化氧化可制得乙醛,反应③为乙醇在浓硫酸、170℃的条件下发生消去反应生成乙烯和水,化学方程式依次为2C2H5OH+O2 2CH3CHO+2H2O、C2H5OH CH2=CH2↑+H2O。答案为:2C2H5OH+O2 2CH3CHO+2H2O;C2H5OH CH2=CH2↑+H2O;
(4)X中溶剂为CCl4,发生的是CH2=CH2与Br2的加成反应,生成物BrCH2CH2Br呈无色,则反应④的现象为溴的四氯化碳溶液变浅或褪色。答案为:溴的四氯化碳溶液变浅或褪色;
(5)1mol有机物B中,含碳原子的物质的量为mol≈4mol,含氢原子的物质的量为mol≈6mol,含氧原子的物质的量为mol≈4mol,从而得出B的分子式为C4H6O4。答案为:C4H6O4。
【点睛】在书写乙醇的消去反应时,反应条件一定要指明“浓硫酸、170℃”。
答案第1页,共2页
答案第1页,共2页
同课章节目录
