专题5药物合成的重要原料—卤代烃、胺、酰胺单元检测题高二下学期化学苏教版(2019)选择性必修3(含解析)
文档属性
| 名称 | 专题5药物合成的重要原料—卤代烃、胺、酰胺单元检测题高二下学期化学苏教版(2019)选择性必修3(含解析) |

|
|
| 格式 | docx | ||
| 文件大小 | 1.7MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-06-19 00:00:00 | ||
图片预览




文档简介
专题5《药物合成的重要原料—卤代烃、胺、酰胺》单元检测题
一、单选题(共13题)
1.有8种物质:①乙酸②苯乙烯③葡萄糖④苯⑤甲苯⑥溴乙烷⑦聚丙烯⑧乙醇。其中既不能使酸性KMnO4溶液褪色,也不能与溴水反应使溴水褪色的是
A.①②③⑤ B.④⑥⑦⑧ C.①④⑥⑦ D.②③⑤⑧
2.某有机物其结构简式为,关于该有机物下列叙述正确的是
A.不能使酸性KMnO4溶液褪色
B.能使溴水褪色
C.在加热和催化剂作用下,最多能和3mol H2反应
D.一定条件下,能和NaOH的醇溶液反应
3.阿魏酸(结构如图)存在于蔬菜和坚果中,在化妆品中主要作为收敛剂、抗炎剂。下列说法错误的是
A.分子式为,碳原子有两种杂化方式
B.可以使的溶液、酸性高锰酸钾溶液褪色
C.阿魏酸最多可与发生反应
D.分子中所有碳原子一定处于同一平面内
4.金纳米粒子催化剂对有机锡与苄基溴化物的Stille偶联反应,具有高效催化作用,反应过程如图。下列说法错误的是
A.X属于芳香烃 B.Z可以发生取代反应、氧化反应和加成反应
C.X和Z均不可能所有原子共平面 D.可用溴的四氯化碳溶液鉴别X和Z
5.一种天然产物具有抗肿瘤、镇痉等生物活性,其结构简式如图。下列关于该天然产物的说法正确的是
A.该有机物的分子式为C15H18O3
B.该分子中的所有碳原子可能共平面
C.1mol该物质最多能与4 molH2发生加成反应
D.该有机物既能与溴水反应,又能使酸性KMnO4溶液褪色,还能发生皂化反应
6.化合物Y能用于高性能光学树脂的合成,可由化合物X与2-甲基丙烯酰氯在一定条件下反应制得如图,下列有关化合物X、Y的说法正确的是
A.X分子中所有原子一定在同一平面上 B.Y分子中有4种化学环境不同的氢原子
C.X、Y均不能使酸性溶液褪色 D.X→Y的反应为取代反应
7.布洛芬片常用来减轻感冒症状,其结构简式如图,下列有关说法错误的是
A.布洛芬的分子式为
B.布洛芬与苯乙酸是同系物,都能和碳酸氢钠反应
C.1mol布洛芬最多能与3mol氢气发生加成反应
D.布洛芬在苯环上发生取代反应,其一氯代物有4种
8.下列说法不正确的是
A.核酸是由许多核苷酸单体形成的聚合物
B.酰胺在酸或碱存在并加热的条件下均可发生水解反应
C.1—氯丙烷和2—氯丙烷分别与NaOH乙醇溶液共热反应产物相同
D.苯酚钠溶液中通入少量CO2气体,生成苯酚和Na2CO3
9.某市拟投资建设一个工业酒精厂,目的是用工业酒精与汽油混合制成“乙醇汽油”。已知制酒精的方法有三种:
①
②
③
↑
从绿色化学(“原子利用率”最大化)的角度看,制酒精最好的方法是
A.① B.③ C.①③ D.①②③
10.从紫草植物中提取出的萘醌类物质具有抗肿瘤及免疫调节的作用,结构如图所示。下列说法错误的是
A.1mol该物质能与2molNaOH溶液发生反应
B.存在含有2个苯环的同分异构体
C.使高锰酸钾溶液、溴蒸气褪色的原理相同
D.至少有11个碳原子共平面
11.下列有关物质应用的说法正确的是
A.CCl4可作有机溶剂,也可作灭火剂
B.二氧化硫可大量用于食品增白
C.工厂中常用的静电除尘装置是根据胶体带电的性质设计的
D.硅是生产光纤制品的基本原料
12.有机物M、N、Q的转化关系为:下列说法正确的是
A.M分子中的所有原子均在同一平面
B.上述两步反应依次属于加成反应和取代反应
C.Q与乙醇互为同系物,且均能使酸性KMnO4溶液褪色
D.M与H2加成后的产物,一氯代物有6种
13.下列说法正确的是
A.等物质的量的苯和苯甲酸完全燃烧消耗氧气的量相等
B.将1mL苯加入到2mL溴的四氯化碳溶液中,振荡后静置,可观察到液体分层,上层呈橙红色
C.己烷有4种同分异构体,它们的熔点、沸点各不相同
D.与互为同分异构体,谱显示两者均有三种不同的氢原子且三种氢原子的比例相同,故不能用来鉴别
二、非选择题(共10题)
14.某课题组以甲苯为主要原料,采用以下路线合成镇静催眠药物——苯巴比妥:
已知:。
以乙醇为原料可合成,请设计合成路线________(用流程图表示,无机试剂任选)。
15.写方程
(1)写出乙醇CH3CH2OH催化氧化反应的化学方程式:_______。
(2)乙烯生成聚乙烯的反应方程式:_______。
(3)甲苯与浓硝酸和浓硫酸的混合生成三硝基甲苯的反应:_______。
(4)溴乙烷与氢氧化钠的醇溶液共热的消去反应方程式:_______。
三、实验题
16.氯苯在染料、医药工业中用于制造重要有机中间体,实验室模拟液相合成法(加热装置都已略去)见下图,在三颈烧瓶中加入催化剂FeCl3及50.0mL苯,有关物质的性质如表格所示:
名称 相对分子质量 沸点/(℃) 密度/(g/mL)
苯 78 78 0.88
氯苯 112.5 132.2 1.1
邻二氯苯 147 180.4 1.3
回答下列问题:
(1)A反应器是利用实验室法制取氯气,装置中空导管a的作用是_________________。
(2)实验需要把干燥纯净的氯气通入装有干燥苯的反应器D中制备氯苯,装置B、C中的试剂分别是________________和浓硫酸,D的反应温度宜控制在70℃~80℃,不宜过高,原因为①温度过高,反应易得到二氯苯;②_____________________,球形冷凝管的出水口是____________(填“b”或“c”),d出口的尾气主要成分有_____________。
(3)从D中得到粗产品(氯化液),其提纯过程如下图:
①碱洗后分离出粗氯苯的操作必须使用的玻璃仪器有_______________。
②实验中最终得到产品为14.7g,产率为________________(精确到0.1%)。
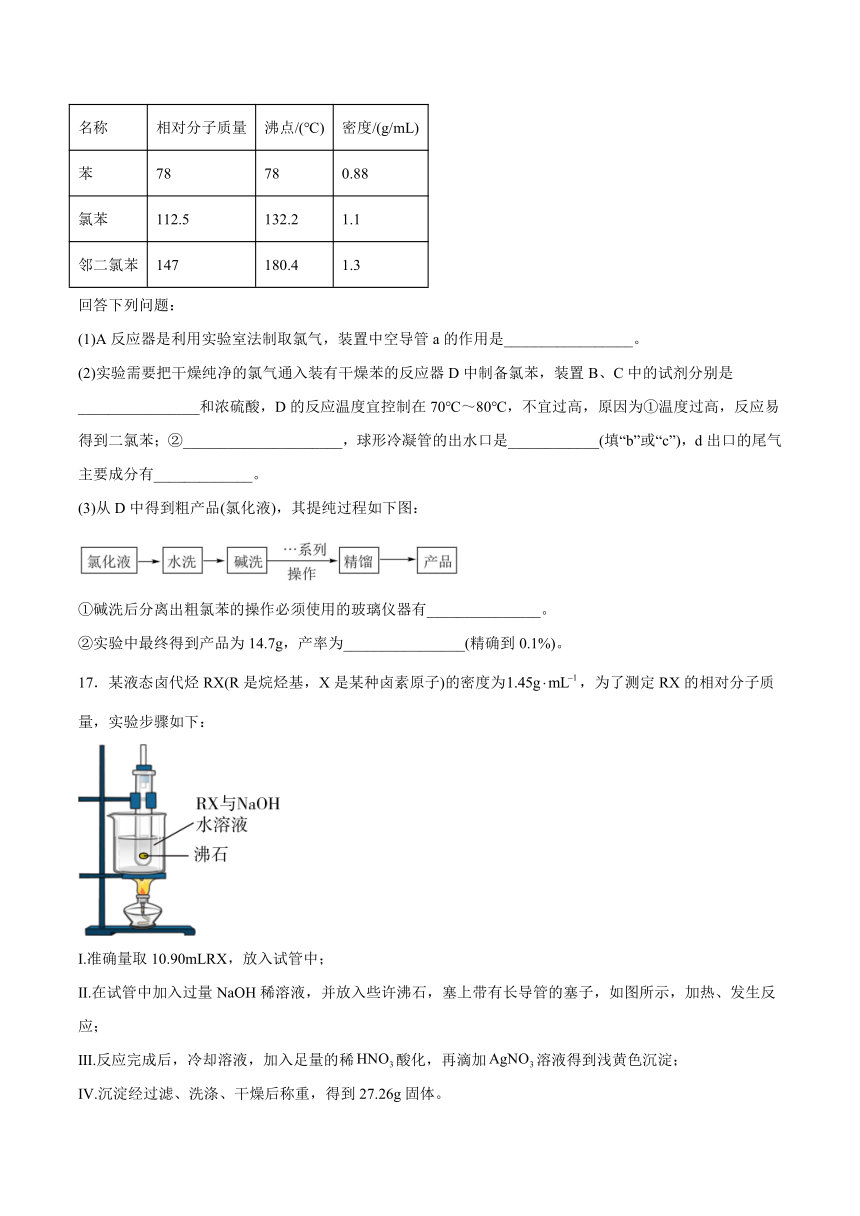
17.某液态卤代烃RX(R是烷烃基,X是某种卤素原子)的密度为,为了测定RX的相对分子质量,实验步骤如下:
Ⅰ.准确量取10.90mLRX,放入试管中;
Ⅱ.在试管中加入过量NaOH稀溶液,并放入些许沸石,塞上带有长导管的塞子,如图所示,加热、发生反应;
Ⅲ.反应完成后,冷却溶液,加入足量的稀酸化,再滴加溶液得到浅黄色沉淀;
Ⅳ.沉淀经过滤、洗涤、干燥后称重,得到27.26g固体。
回答下列问题:
已知:不考虑实验过程中造成的质量损失。
(1)步骤Ⅳ中,过滤时常用到的玻璃仪器有烧杯、_______、_______。
(2)步骤Ⅱ中,发生有机反应的反应类型为_______,若实验进行过程中,发现未加入沸石,则应采取的措施是_______。
(3)步骤Ⅲ中,加入稀的作用是_______。
(4)依据上述实验步骤所提供的实验数据,RX的结构简式为_______。
(5)若步骤Ⅲ中加入稀的量不足,则测得卤代烃的相对分子质量将_______(填“偏大”、“偏小”或“无影响”)。
四、计算题
18.150℃时,将0.1mol某气态烷烃A和气态单烯烃B的混合气体与足量氧气完全燃烧后,恢复到初始温度,气体体积不变,将燃烧后的气体缓慢通过浓硫酸后再用碱石灰完全吸收,碱石灰增重7.92g。试回答:
(1)混合气体的组分为___________(简要写出推理过程)
(2)___________
19.由一种气态烷烃和一种气态单烯烃组成的混合气体,它对H2的相对密度是13.2,将1L的混合气体和4LO2在容积固定的密闭容器中完全燃烧并保持原来的温度(120℃),测得密闭容器内压强比反应前增加了4%,试确定混合气体的成分及体积比。
20.有机化合物的相关计算
(1)有机物①CH4 ②C2H4 ③C2H2④甲苯 ⑤甲醛(HCHO)⑥乙酸
等物质的量的上述有机物完全燃烧耗氧量最多的是______________;
等质量的上述有机物完全燃烧耗氧量最多的是______________;
等质量的上述有机物完全燃烧耗氧量相同的是______________。
(2)将0.1mol两种气体烃组成的混合气完全燃烧后得3.36L(标况)CO2和3.6g水,则一定含有 __________________;可能含有________________。
(3)某气态烃和气态单烯烃组成的混合气体在同温同压下对氢气的相对密度为13,取标准状况下此混合气体2.24 L通入足量溴水中,溴水增重1.4g,此两种烃的分子式分别是___________________。
(4)常温下,20mL某烃A和100mL氧气(过量)混合,点燃,使其充分燃烧后恢复到原状况,残留气体体积为70mL。则该烃可能为___________。
A.C2H6 B.C3H6 C.C4H6 D.C5H6
21.图中烃A是植物生长调节剂,它的产量可以用来衡量一个国家的石油化工发展水平;D是一种高分子材料,此类物质大量使用易造成“白色污染”。回答下列问题:
的结构简式为___;E中含有官能团的名称为_____。
关于上述有机物,下列说法不正确的是____ 填序号。
a.A和D均能使溴水或酸性高锰酸钾溶液褪色,但B不能
b.B的二氯代物有2种
c.反应②是取代反应
d.实验室制取H时常用饱和溶液除去H中的杂质
反应⑤的化学方程式为______;反应⑥的化学方程式为______。
22.化合物M是一种消毒剂和消炎药物的中间体。以化合物A、B为原料制备M的一种合成路线如图所示:
已知:①
②
③
回答下列问题:
(1)A的结构简式为____;B的化学名称为____;由C生成D的反应类型为____;E中含氧官能团的名称为____。
(2)由D和C5H12NCl制备H时,常加入适量CH3CH2ONa,其目的为____。
(3)G的顺式结构简式为____。
(4)由G和H生成M的化学方程式为____。
(5)同时满足下列条件的F的同分异构体有____种(不考虑立体异构)。
①既能发生银镜反应,又能与FeCl3溶液发生显色反应。
②核磁共振氢谱中有4组吸收峰。
(6)已知:-NH2易被氧化。参照上述合成路线和信息,以甲苯为原料(无机试剂任选),设计制备 的合成路线:____。
23.尼泊金甲酯和香兰素在食品、化妆品行业有广泛用途。它们的结构简式如下:
(1)尼泊金甲酯中显酸性的官能团是_______(填名称)。
(2)下列说法中,正确的是_______(填标号)。
A.尼泊金甲酯和香兰素分子式都是C8H8O3
B.尼泊金甲酯和香兰素都能发生水解反应
C.1 mol尼泊金甲酯或香兰素均能与4 mol H2发生加成反应
D.利用银氨溶液可以区别尼泊金甲酯和香兰素
(3)写出尼泊金甲酯与NaOH溶液反应的化学方程式:_______。
(4)大茴香酸与香兰素互为同分异构体,它是一种羧酸,且具备以下3个特点。大茴香酸的结构简式为_______。
a.分子中含有甲基
b.遇FeCl3溶液不显紫色
c.苯环上的一氯代物只有两种
(5)以丁香油酚为原料,通过下列路线合成香兰素。
(注:分离方法和其他产物已经略去;乙酸酐的结构简式为:(CH3CO)2O)
①由和ClCH2CH=CH2合成丁香油酚的反应类型为_______。
②步骤Ⅱ中,反应的化学方程式为_______。
③W的结构简式为_______。
参考答案:
1.C 2.B 3.D 4.A 5.A 6.D 7.D 8.D 9.A 10.C 11.A 12.D 13.A
14.
15.(1)CH3CH2OH+O22CH3CHO+2H2O
(2)nCH2=CH2
(3)
(4)CH3CH2Br+NaOHCH2=CH2↑+NaBr+H2O
16. 平衡气压 饱和NaCl溶液 温度过高,苯挥发造成原料利用率低 c Cl2、苯、HCl 分液漏斗、烧杯 23.2%
17.(1) 漏斗 玻璃棒
(2) 取代反应(或水解反应) 先停止加热并冷却至室温,然后补加沸石
(3)除去未反应完的NaOH
(4)CH3CH2Br
(5)偏小
18.(1)甲烷、乙烯
(2)1:4
19.CH4、C3H6;3:2
20. ④ ① ⑤和⑥ 甲烷 乙烯或丙炔 CH4、C4H8 A B
21. CH2=CH2 羟基
a 2CH3CH2OH+O22CH3CHO+2H2O CH3CH2OH+CH3COOHCH3COOCH2CH3+H2O
22.(1) 苯乙醛 还原反应 羟基
(2)CH3CH2ONa可与反应生成的HCl反应,有利于反应正向进行,增大产品产率(或原料利用率)
(3)
(4)
(5)4
(6)
23.(1)羟基
(2)AD
(3)+NaOH +CH3OH+H2O
(4)
(5) 取代反应 + +CH3COOH
一、单选题(共13题)
1.有8种物质:①乙酸②苯乙烯③葡萄糖④苯⑤甲苯⑥溴乙烷⑦聚丙烯⑧乙醇。其中既不能使酸性KMnO4溶液褪色,也不能与溴水反应使溴水褪色的是
A.①②③⑤ B.④⑥⑦⑧ C.①④⑥⑦ D.②③⑤⑧
2.某有机物其结构简式为,关于该有机物下列叙述正确的是
A.不能使酸性KMnO4溶液褪色
B.能使溴水褪色
C.在加热和催化剂作用下,最多能和3mol H2反应
D.一定条件下,能和NaOH的醇溶液反应
3.阿魏酸(结构如图)存在于蔬菜和坚果中,在化妆品中主要作为收敛剂、抗炎剂。下列说法错误的是
A.分子式为,碳原子有两种杂化方式
B.可以使的溶液、酸性高锰酸钾溶液褪色
C.阿魏酸最多可与发生反应
D.分子中所有碳原子一定处于同一平面内
4.金纳米粒子催化剂对有机锡与苄基溴化物的Stille偶联反应,具有高效催化作用,反应过程如图。下列说法错误的是
A.X属于芳香烃 B.Z可以发生取代反应、氧化反应和加成反应
C.X和Z均不可能所有原子共平面 D.可用溴的四氯化碳溶液鉴别X和Z
5.一种天然产物具有抗肿瘤、镇痉等生物活性,其结构简式如图。下列关于该天然产物的说法正确的是
A.该有机物的分子式为C15H18O3
B.该分子中的所有碳原子可能共平面
C.1mol该物质最多能与4 molH2发生加成反应
D.该有机物既能与溴水反应,又能使酸性KMnO4溶液褪色,还能发生皂化反应
6.化合物Y能用于高性能光学树脂的合成,可由化合物X与2-甲基丙烯酰氯在一定条件下反应制得如图,下列有关化合物X、Y的说法正确的是
A.X分子中所有原子一定在同一平面上 B.Y分子中有4种化学环境不同的氢原子
C.X、Y均不能使酸性溶液褪色 D.X→Y的反应为取代反应
7.布洛芬片常用来减轻感冒症状,其结构简式如图,下列有关说法错误的是
A.布洛芬的分子式为
B.布洛芬与苯乙酸是同系物,都能和碳酸氢钠反应
C.1mol布洛芬最多能与3mol氢气发生加成反应
D.布洛芬在苯环上发生取代反应,其一氯代物有4种
8.下列说法不正确的是
A.核酸是由许多核苷酸单体形成的聚合物
B.酰胺在酸或碱存在并加热的条件下均可发生水解反应
C.1—氯丙烷和2—氯丙烷分别与NaOH乙醇溶液共热反应产物相同
D.苯酚钠溶液中通入少量CO2气体,生成苯酚和Na2CO3
9.某市拟投资建设一个工业酒精厂,目的是用工业酒精与汽油混合制成“乙醇汽油”。已知制酒精的方法有三种:
①
②
③
↑
从绿色化学(“原子利用率”最大化)的角度看,制酒精最好的方法是
A.① B.③ C.①③ D.①②③
10.从紫草植物中提取出的萘醌类物质具有抗肿瘤及免疫调节的作用,结构如图所示。下列说法错误的是
A.1mol该物质能与2molNaOH溶液发生反应
B.存在含有2个苯环的同分异构体
C.使高锰酸钾溶液、溴蒸气褪色的原理相同
D.至少有11个碳原子共平面
11.下列有关物质应用的说法正确的是
A.CCl4可作有机溶剂,也可作灭火剂
B.二氧化硫可大量用于食品增白
C.工厂中常用的静电除尘装置是根据胶体带电的性质设计的
D.硅是生产光纤制品的基本原料
12.有机物M、N、Q的转化关系为:下列说法正确的是
A.M分子中的所有原子均在同一平面
B.上述两步反应依次属于加成反应和取代反应
C.Q与乙醇互为同系物,且均能使酸性KMnO4溶液褪色
D.M与H2加成后的产物,一氯代物有6种
13.下列说法正确的是
A.等物质的量的苯和苯甲酸完全燃烧消耗氧气的量相等
B.将1mL苯加入到2mL溴的四氯化碳溶液中,振荡后静置,可观察到液体分层,上层呈橙红色
C.己烷有4种同分异构体,它们的熔点、沸点各不相同
D.与互为同分异构体,谱显示两者均有三种不同的氢原子且三种氢原子的比例相同,故不能用来鉴别
二、非选择题(共10题)
14.某课题组以甲苯为主要原料,采用以下路线合成镇静催眠药物——苯巴比妥:
已知:。
以乙醇为原料可合成,请设计合成路线________(用流程图表示,无机试剂任选)。
15.写方程
(1)写出乙醇CH3CH2OH催化氧化反应的化学方程式:_______。
(2)乙烯生成聚乙烯的反应方程式:_______。
(3)甲苯与浓硝酸和浓硫酸的混合生成三硝基甲苯的反应:_______。
(4)溴乙烷与氢氧化钠的醇溶液共热的消去反应方程式:_______。
三、实验题
16.氯苯在染料、医药工业中用于制造重要有机中间体,实验室模拟液相合成法(加热装置都已略去)见下图,在三颈烧瓶中加入催化剂FeCl3及50.0mL苯,有关物质的性质如表格所示:
名称 相对分子质量 沸点/(℃) 密度/(g/mL)
苯 78 78 0.88
氯苯 112.5 132.2 1.1
邻二氯苯 147 180.4 1.3
回答下列问题:
(1)A反应器是利用实验室法制取氯气,装置中空导管a的作用是_________________。
(2)实验需要把干燥纯净的氯气通入装有干燥苯的反应器D中制备氯苯,装置B、C中的试剂分别是________________和浓硫酸,D的反应温度宜控制在70℃~80℃,不宜过高,原因为①温度过高,反应易得到二氯苯;②_____________________,球形冷凝管的出水口是____________(填“b”或“c”),d出口的尾气主要成分有_____________。
(3)从D中得到粗产品(氯化液),其提纯过程如下图:
①碱洗后分离出粗氯苯的操作必须使用的玻璃仪器有_______________。
②实验中最终得到产品为14.7g,产率为________________(精确到0.1%)。
17.某液态卤代烃RX(R是烷烃基,X是某种卤素原子)的密度为,为了测定RX的相对分子质量,实验步骤如下:
Ⅰ.准确量取10.90mLRX,放入试管中;
Ⅱ.在试管中加入过量NaOH稀溶液,并放入些许沸石,塞上带有长导管的塞子,如图所示,加热、发生反应;
Ⅲ.反应完成后,冷却溶液,加入足量的稀酸化,再滴加溶液得到浅黄色沉淀;
Ⅳ.沉淀经过滤、洗涤、干燥后称重,得到27.26g固体。
回答下列问题:
已知:不考虑实验过程中造成的质量损失。
(1)步骤Ⅳ中,过滤时常用到的玻璃仪器有烧杯、_______、_______。
(2)步骤Ⅱ中,发生有机反应的反应类型为_______,若实验进行过程中,发现未加入沸石,则应采取的措施是_______。
(3)步骤Ⅲ中,加入稀的作用是_______。
(4)依据上述实验步骤所提供的实验数据,RX的结构简式为_______。
(5)若步骤Ⅲ中加入稀的量不足,则测得卤代烃的相对分子质量将_______(填“偏大”、“偏小”或“无影响”)。
四、计算题
18.150℃时,将0.1mol某气态烷烃A和气态单烯烃B的混合气体与足量氧气完全燃烧后,恢复到初始温度,气体体积不变,将燃烧后的气体缓慢通过浓硫酸后再用碱石灰完全吸收,碱石灰增重7.92g。试回答:
(1)混合气体的组分为___________(简要写出推理过程)
(2)___________
19.由一种气态烷烃和一种气态单烯烃组成的混合气体,它对H2的相对密度是13.2,将1L的混合气体和4LO2在容积固定的密闭容器中完全燃烧并保持原来的温度(120℃),测得密闭容器内压强比反应前增加了4%,试确定混合气体的成分及体积比。
20.有机化合物的相关计算
(1)有机物①CH4 ②C2H4 ③C2H2④甲苯 ⑤甲醛(HCHO)⑥乙酸
等物质的量的上述有机物完全燃烧耗氧量最多的是______________;
等质量的上述有机物完全燃烧耗氧量最多的是______________;
等质量的上述有机物完全燃烧耗氧量相同的是______________。
(2)将0.1mol两种气体烃组成的混合气完全燃烧后得3.36L(标况)CO2和3.6g水,则一定含有 __________________;可能含有________________。
(3)某气态烃和气态单烯烃组成的混合气体在同温同压下对氢气的相对密度为13,取标准状况下此混合气体2.24 L通入足量溴水中,溴水增重1.4g,此两种烃的分子式分别是___________________。
(4)常温下,20mL某烃A和100mL氧气(过量)混合,点燃,使其充分燃烧后恢复到原状况,残留气体体积为70mL。则该烃可能为___________。
A.C2H6 B.C3H6 C.C4H6 D.C5H6
21.图中烃A是植物生长调节剂,它的产量可以用来衡量一个国家的石油化工发展水平;D是一种高分子材料,此类物质大量使用易造成“白色污染”。回答下列问题:
的结构简式为___;E中含有官能团的名称为_____。
关于上述有机物,下列说法不正确的是____ 填序号。
a.A和D均能使溴水或酸性高锰酸钾溶液褪色,但B不能
b.B的二氯代物有2种
c.反应②是取代反应
d.实验室制取H时常用饱和溶液除去H中的杂质
反应⑤的化学方程式为______;反应⑥的化学方程式为______。
22.化合物M是一种消毒剂和消炎药物的中间体。以化合物A、B为原料制备M的一种合成路线如图所示:
已知:①
②
③
回答下列问题:
(1)A的结构简式为____;B的化学名称为____;由C生成D的反应类型为____;E中含氧官能团的名称为____。
(2)由D和C5H12NCl制备H时,常加入适量CH3CH2ONa,其目的为____。
(3)G的顺式结构简式为____。
(4)由G和H生成M的化学方程式为____。
(5)同时满足下列条件的F的同分异构体有____种(不考虑立体异构)。
①既能发生银镜反应,又能与FeCl3溶液发生显色反应。
②核磁共振氢谱中有4组吸收峰。
(6)已知:-NH2易被氧化。参照上述合成路线和信息,以甲苯为原料(无机试剂任选),设计制备 的合成路线:____。
23.尼泊金甲酯和香兰素在食品、化妆品行业有广泛用途。它们的结构简式如下:
(1)尼泊金甲酯中显酸性的官能团是_______(填名称)。
(2)下列说法中,正确的是_______(填标号)。
A.尼泊金甲酯和香兰素分子式都是C8H8O3
B.尼泊金甲酯和香兰素都能发生水解反应
C.1 mol尼泊金甲酯或香兰素均能与4 mol H2发生加成反应
D.利用银氨溶液可以区别尼泊金甲酯和香兰素
(3)写出尼泊金甲酯与NaOH溶液反应的化学方程式:_______。
(4)大茴香酸与香兰素互为同分异构体,它是一种羧酸,且具备以下3个特点。大茴香酸的结构简式为_______。
a.分子中含有甲基
b.遇FeCl3溶液不显紫色
c.苯环上的一氯代物只有两种
(5)以丁香油酚为原料,通过下列路线合成香兰素。
(注:分离方法和其他产物已经略去;乙酸酐的结构简式为:(CH3CO)2O)
①由和ClCH2CH=CH2合成丁香油酚的反应类型为_______。
②步骤Ⅱ中,反应的化学方程式为_______。
③W的结构简式为_______。
参考答案:
1.C 2.B 3.D 4.A 5.A 6.D 7.D 8.D 9.A 10.C 11.A 12.D 13.A
14.
15.(1)CH3CH2OH+O22CH3CHO+2H2O
(2)nCH2=CH2
(3)
(4)CH3CH2Br+NaOHCH2=CH2↑+NaBr+H2O
16. 平衡气压 饱和NaCl溶液 温度过高,苯挥发造成原料利用率低 c Cl2、苯、HCl 分液漏斗、烧杯 23.2%
17.(1) 漏斗 玻璃棒
(2) 取代反应(或水解反应) 先停止加热并冷却至室温,然后补加沸石
(3)除去未反应完的NaOH
(4)CH3CH2Br
(5)偏小
18.(1)甲烷、乙烯
(2)1:4
19.CH4、C3H6;3:2
20. ④ ① ⑤和⑥ 甲烷 乙烯或丙炔 CH4、C4H8 A B
21. CH2=CH2 羟基
a 2CH3CH2OH+O22CH3CHO+2H2O CH3CH2OH+CH3COOHCH3COOCH2CH3+H2O
22.(1) 苯乙醛 还原反应 羟基
(2)CH3CH2ONa可与反应生成的HCl反应,有利于反应正向进行,增大产品产率(或原料利用率)
(3)
(4)
(5)4
(6)
23.(1)羟基
(2)AD
(3)+NaOH +CH3OH+H2O
(4)
(5) 取代反应 + +CH3COOH
