第3章第2节从化石燃料中获取有机化合物同步练习 (含答案)2022-2023学年下学期高一化学鲁科版(2019)必修第二册
文档属性
| 名称 | 第3章第2节从化石燃料中获取有机化合物同步练习 (含答案)2022-2023学年下学期高一化学鲁科版(2019)必修第二册 |

|
|
| 格式 | docx | ||
| 文件大小 | 320.3KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-06-19 00:00:00 | ||
图片预览




文档简介
第3章第2节从化石燃料中获取有机化合物同步练习
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1.化学与生产生活息息相关。下列说法中,正确的是
A.聚氯乙烯塑料可用作不粘锅的耐热涂层
B.用热的纯碱溶液可清洗衣物上的汽油污渍
C.氯碱工业中,可用浓氨水检查氯气管道是否泄漏
D.金属钠着火时,可用碳酸氢钠干粉灭火器扑灭
2.2022年12月4日,神舟十四号载人飞船返回舱在东风着陆场成功着陆。下列说法不正确的是
A.氧化铝陶瓷可作火箭腹部的隔热瓦,说明氧化铝熔点高
B.舱体表面的低密度烧蚀涂层中使用的苯基硅橡胶是有机高分子材料
C.飞船身上的“超薄皮肤”——铝合金蒙皮板的强度、硬度比金属铝小
D.空间站的能源为柔性砷化镓太阳能电池阵,砷化镓属于半导体材料
3.材料对于促进生产发展、改善人类生活发挥着巨大作用。下列有关材料的说法正确的是
A.不锈钢中含有铬、镍等元素,具有很强的抗腐蚀能力
B.用来生产电闸、灯口等产品的酚醛树脂属于聚酯类化合物
C.汽车机盖上使用的碳纤维是一种新型有机高分子材料
D.在钢中加入某些稀土元素,可降低钢的韧性、塑性等
4.下列有关煤的叙述正确的是
A.煤是由有机物和无机物组成的复杂的混合物,主要含碳、氢元素
B.煤在空气中加强热可得焦炭、煤焦油、粗氨水和焦炉气
C.推广使用煤液化和气化技术,可减少二氧化碳等温室气体的排放
D.煤的气化的主要反应是
5.下列关于乙烷、乙烯、乙炔的说法正确的是
①它们既不是同系物,也不是同分异构体 ②乙烷属于饱和烃,乙烯、乙炔属于不饱和烃
③乙烯、乙炔能使溴水褪色,乙烷不能使溴水褪色 ④它们都能燃烧
⑤它们都能使酸性溶液褪色
A.①③④ B.①②③⑤ C.②③④⑤ D.①②③④
6.下列有关化学品的使用正确的是
A.凡含有食品添加剂的食物对人体均有害,不可食用
B.聚乙烯、聚氯乙烯制成的塑料袋都可用于食品包装
C.适量的食品添加剂可以改变食物的色、香、味、营养结构、腐败时间等,如可以在食盐中加碘、酱油中补铁,食物中加维生素,这些做法都是积极的,对人体有益的
D.苏打片(成分NaHCO3)、胃舒平[成分是Al(OH)3]都可用于胃溃疡病人胃酸过多的治疗
7.已知(b)、(c)、(d)的分子式均为C6H6,下列说法正确的是
A.b的同分异构体只有c和d两种
B.b、c、d的二氯代物均只有三种
C.b、c、d均可与酸性高锰酸钾溶液反应
D.b、c、d中只有b的所有原子处于同一平面
8.以下结构表示的物质中是烷烃的是
①CH3OH ②CH2=CH2 ③ ④CH3CH3
A.①和② B.①和③ C.①和④ D.③和④
9.苯乙烯是一种重要的有机化工原料,其结构简式为,它不可能具有的性质是
A.易溶于水,不易溶于有机溶剂
B.在空气中燃烧产生黑烟
C.它能使溴的四氯化碳溶液褪色,也能使酸性高锰酸钾溶液褪色
D.能发生加成反应
10.科学家在-100℃的低温下合成了一种结构简式为的烃X,实验测得其分子中只有一种氢原子,根据分析,下列说法中不正确的是
A.X的分子式为C5H4
B.X能使酸性高锰酸钾溶液褪色
C.1molX在一定条件下可与2mol氢气发生反应
D.X的一氯代物只有2种
11.由乙烯的结构和性质推测丙烯(CH2=CH—CH3)的结构或性质正确的是
A.不能使酸性KMnO4溶液褪色
B.所有的原子都在同一平面内
C.能使溴的四氯化碳溶液褪色
D.与HCl在一定条件下能加成,并只得到一种产物
12.下列各反应中属于加成反应的是
①+Br2→BrCH=CHBr
②H2+Cl22HCl
③
④CH3CH3+2Cl2CH2ClCH2Cl+2HCl
A.①② B.②③
C.①③ D.②④
13.对比甲烷和乙烯的燃烧反应,下列叙述中正确的是
A.二者燃烧时现象完全相同
B.点燃前都不需验纯
C.甲烷燃烧的火焰呈淡蓝色,乙烯燃烧的火焰较明亮且伴有黑烟
D.二者燃烧时都有黑烟生成
14.下列除杂方法不正确的是
A.除去乙烷中混有的少量乙烯:通入稀溴水中,干燥
B.除去溴苯中混有的少量单质溴:加入足量的NaOH溶液,振荡、静置、分液
C.除去75%的乙醇中的水制无水乙醇:加入生石灰,振荡、静置、蒸馏
D.除去乙醇中混有的少量苯,可通过分液的方法实现
15.下列关于苯的说法不正确的是
A.苯不能燃烧 B.苯密度小于水
C.苯不能使酸性高锰酸钾溶液褪色 D.一定条件下,苯可与浓硝酸发生取代反应
二、实验题
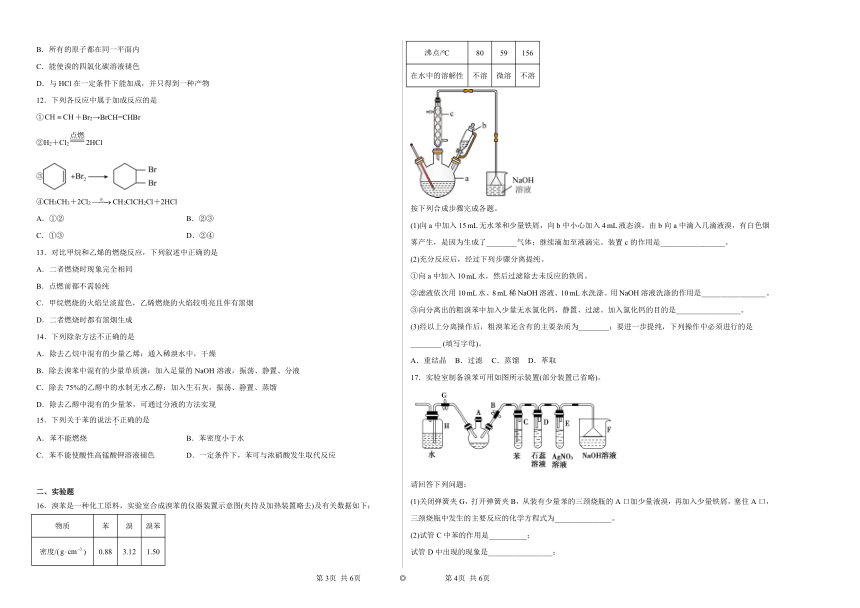
16.溴苯是一种化工原料,实验室合成溴苯的仪器装置示意图(夹持及加热装置略去)及有关数据如下:
物质 苯 溴 溴苯
密度/() 0.88 3.12 1.50
沸点/℃ 80 59 156
在水中的溶解性 不溶 微溶 不溶
按下列合成步骤完成各题。
(1)向a中加入15无水苯和少量铁屑,向b中小心加入4液态溴。由b向a中滴入几滴液溴,有白色烟雾产生,是因为生成了________气体;继续滴加至液滴完。装置c的作用是_________________。
(2)充分反应后,经过下列步骤分离提纯。
①向a中加入10水,然后过滤除去未反应的铁屑。
②滤液依次用10水、8稀溶液、10水洗涤。用溶液洗涤的作用是_________________。
③向分离出的粗溴苯中加入少量无水氯化钙,静置、过滤。加入氯化钙的目的是_________________。
(3)经以上分离操作后,粗溴苯还含有的主要杂质为________;要进一步提纯,下列操作中必须进行的是________ (填写字母)。
A.重结晶 B.过滤 C.蒸馏 D.萃取
17.实验室制备溴苯可用如图所示装置(部分装置已省略)。
请回答下列问题:
(1)关闭弹簧夹G,打开弹簧夹B,从装有少量苯的三颈烧瓶的A口加少量液溴,再加入少量铁屑,塞住A口,三颈烧瓶中发生的主要反应的化学方程式为_______________。
(2)试管C中苯的作用是__________;
试管D中出现的现象是_________________;
试管E中出现的现象是______________。
(3)待三颈烧瓶中的反应进行到仍有气泡冒出时打开弹簧夹G,关闭弹簧夹B,可以看到的现象是_______________。
三、工业流程题
18.我国资源丰富,合理开发利用资源,才能实现可持续发展。
Ⅰ.以原油为原科生产有机高分子材料聚乙烯、聚丙烯的流程如下:
(1)流程中②表示的加工方法是____(填序号)。
A.分馏 B.聚合 C.裂解 D.干馏
(2)写出聚乙烯的结构简式_______。
Ⅱ.浩瀚的海洋中蕴藏着丰富的资源。从海水中可以提取很多有用的物质,例如从海水制盐所得到的卤水中可以提取碘。活性炭吸附法是工业提取碘的方法之一,其流程如下:
资料显示:
ⅰ. pH=2 时, NaNO2溶液只能将I-氧化为I2,同时生成 NO
ⅱ. I2+5Cl2+6H2O=2HIO3+10HCl; 氧化性:KMnO4>Cl2
ⅲ. 2Fe3++2I-=2Fe2++I2
(3)写出反应①的离子方程式_______。
(4)方案甲中,根据 I2的特性,分离操作 X 应为___________、冷凝结晶。
(5)Cl2、酸性KMnO4等都是常用的强氧化剂,但该工艺中氧化卤水中的 I-却选择了价格较高的NaNO2,原因是_______。
(6)方案乙中,已知反应③过滤后,滤液中仍存在少量的 I2、I-。 为了检验滤液中的 I-,某小组同学设计如下实验方案,请将实验步骤补充完整。
实验中可供选择的试剂:稀H2SO4、淀粉溶液、Fe2(SO4)3溶液、CCl4。
a.将滤液用CCl4多次萃取、分液,直到水层用淀粉溶液检验不出碘单质存在,
b.从水层取少量溶液于试管中,_______。
四、有机推断题
19.已知A是石油化学工业重要的基本原料,相对分子质量为28,在一定条件下能发生下图所示的转化关系.
(1)写出有机物A~F的结构简式_________分子中官能团的名称和所属的有机物类别.__________
(2)写出实现下列转化的化学方程式,并注明反应类型.
①A→F_______________
②B→C_______________
③B+D→E__________
第1页 共4页 ◎ 第2页 共4页
第1页 共4页 ◎ 第2页 共4页
参考答案:
1.C
【详解】A.聚氯乙烯塑料不耐热,不能用作不粘锅的耐热涂层,故A错误;
B.汽油不能和碳酸钠溶液反应,也不溶于碳酸钠溶液,不能用热的纯碱溶液可清洗衣物上的汽油污渍,故B错误;
C.氯碱工业中,可用浓氨水检查氯气管道是否泄漏,氨气遇到氯气会产生白烟,故C正确;
D.金属钠为活泼金属,着火时,可与二氧化碳、水反应,则金属钠着火时,不可用碳酸氢钠干粉灭火器扑灭,故D错误;
故选C。
2.C
【详解】A.火箭腹部有高热量区,使用氧化铝陶瓷作隔热瓦,说明氧化铝熔点高,A正确;
B.苯基硅橡胶属于有机高分子材料,B正确;
C.合金的强度和硬度一般都比组成它的各成分金属大,C错误;
D.砷化镓可用于制备柔性砷化镓太阳能电池阵,说明砷化镓能导电,类比硅可用于制造太阳能电池,可知其为半导体材料,D正确;
故选C。
【点睛】合金的强度和硬度一般都比组成它的各成分金属大,这是因为一种金属原子或非金属原子在其他金属原子的晶体结构中占据了一定位置,会造成金属晶体结构的变形,从而使金属晶体在发生错位时阻力上升、形变困难,导致其强度、硬度增大。
3.A
【详解】A.不锈钢中含有铬、镍元素,能改变金属的内部结构,使铁合金具有很强的抗腐蚀能力,A项正确;
B.酚醛树脂是由酚类和醛类聚合而成的,不属于聚酯,B项错误;
C.碳纤维属于碳单质,不是新型有机高分子材料,C项错误;
D.在钢中加入某些稀土元素形成的合金,可增强钢的韧性、塑性等,D项错误;
故选A。
4.A
【详解】A.煤中有机质是复杂的高分子有机化合物,主要由碳、氢、氧、氮、硫和磷等元素组成,而碳、氢、氧三者总和约占有机质的95%以上;煤中的无机质也含有少量的碳、氢、氧、硫等元素,A正确;
B.煤在空气中加强热会燃烧,要想将煤干馏,需隔绝空气加强热,B错误;
C.煤的液化和气化,不能减少二氧化碳等温室气体的排放,C错误;
D.煤的气化主要是煤与水蒸气发生置换反应,生成水煤气,C(s)+H2O(g)CO(g)+H2(g),D错误;
故答案为:A。
5.D
【详解】①乙烷、乙烯和乙炔结构不相似,分子式也不同,所以它们既不是同系物,也不是同分异构体,故①正确;
②乙烷是饱和烃,乙烯、乙炔中含有碳碳不饱和键,因此乙烯和乙炔是不饱和烃,故②正确;
③乙烯、乙炔中碳碳不饱和键能和溴水发生加成反应而使溴水褪色,乙烷和溴水不反应因而不能使溴水褪色,故③正确;
④它们都属于有机物,都能燃烧,故④正确;
⑤乙烯和乙炔中碳碳不饱和键能被酸性高锰酸钾溶液氧化而使酸性高锰酸钾溶液褪色,乙烷性质稳定和高锰酸钾溶液不反应,所以不能使酸性高锰酸钾溶液褪色,故⑤错误;
综上所述,①②③④正确,故选D。
6.C
【详解】A.含有食品添加剂的食物不一定对人体有害,在规定范围内合理使用食品添加剂,对人体健康不会产生不良影响,故A错误;
B.聚乙烯无毒,聚乙烯做成的塑料可用于食品包装袋,聚氯乙烯是由聚氯乙烯树脂、增塑剂和防老剂组成的树脂,本身并无毒性,所加的增塑剂、防老剂等主要辅料有毒性,因此聚氯乙烯制成的塑料不能用于食品包装袋,故B错误;
C.适量的食品添加剂可以改变食物的色、香、味、营养结构、腐败时间等,如可以在食盐中加碘、酱油中补铁,食物中加维生素,这些做法都是积极的,对人体有益的,故C正确;
D.苏打片与胃酸产生CO2,二氧化碳加速胃溃疡,因此苏打片不用于胃溃疡病人胃酸过多,故D错误;
答案为C。
7.D
【详解】A.b是苯,其同分异构体还可以是链状不饱和烃,同分异构体有多种,不止d和p两种,A错误;
B.c分子中氢原子分为2类,根据定一移一可知c的二氯代物是6种,B错误;
C.b、d分子中不存在碳碳双键,不与酸性高锰酸钾溶液发生反应,C错误;
D.苯是平面形结构,所有原子共平面,d、c中均含有饱和碳原子,所有原子不可能共平面,D正确;
故答案为D。
8.D
【详解】①CH3OH含有羟基为醇类, ②CH2=CH2 为乙烯是烯烃,③为异丁烷, ④CH3CH3为乙烷,是烷烃,综上所述故选D。
9.A
【详解】A.苯乙烯为烃,难溶于水,易溶于有机溶剂,选A;
B.苯乙烯的分子式为C8H8,与苯的最简式相同,即含碳量很高,故燃烧时产生黑烟,B不选;
C.因分子中含有碳碳双键,所以苯乙烯能与溴水发生加成反应而使溴水褪色;苯乙烯能被酸性高锰酸钾溶液氧化,而使酸性KMnO4溶液褪色,C不选;
D.苯乙烯中苯环能与H2发生加成反应,苯乙烯中的碳碳双键和溴、卤化氢、氢气等发生加成反应,D不选;
故本题选A。
10.D
【详解】A.根据烃X的结构简式可知其分子式为C5H4,A正确;
B.X分子中含碳碳双键,能使酸性KMnO4溶液褪色,B正确;
C.X分子中含两个碳碳双键,1molX在一定条件下可与2mol氢气发生加成反应,C正确;
D.由结构对称性可知,分子中只有一种位置的H,一氯代物只有1种,D错误;
故选D。
11.C
【详解】A.因丙烯分子同乙烯分子一样含有碳碳双键,所以能被酸性KMnO4溶液氧化而使之褪色,A错误;
B.因丙烯分子中含有甲基(—CH3),甲基是三角锥的空间结构,故丙烯中所有原子不可能在同一平面内,B错误;
C.丙烯能与溴发生加成反应,而使溴的四氯化碳溶液褪色,C正确;
D.丙烯能与HCl加成得到两种产物,D错误;
故本题选C。
12.C
【详解】①含有碳碳三键,+Br2→BrCH=CHBr属于加成反应;
②H2+Cl22HCl属于化合反应;
③环己烯含有碳碳双键, 属于加成反应;
④CH3CH3+2Cl2CH2ClCH2Cl+2HCl属于取代应;故①③属于加成反应,故C正确;
故选C。
13.C
【分析】因为甲烷和乙烯的含碳量不同,故燃烧时的现象不同,甲烷含碳量较低,火焰呈淡蓝色,不产生黑烟,而乙烯含碳量较高,燃烧时火焰较明亮且伴有黑烟
【详解】A.二者燃烧时现象不相同,故A错误;
B.CH4与C2H4都是可燃性气体,若气体不纯,点燃时可能发生爆炸,因此点燃前需验纯,故B正确;
C.甲烷含碳量较低,燃烧时不产生黑烟,而乙烯含碳量较高,燃烧时火焰较明亮且伴有黑烟,故C正确;
D.甲烷含碳量较低,燃烧时不产生黑烟,而乙烯含碳量较高,燃烧时火焰较明亮且伴有黑烟,故D错误;
故选C。
14.D
【详解】A.乙烯与溴水中Br2发生加成反应生成1,2 二溴乙烷,乙烷不反应,经洗气干燥后可得纯净乙烷,A正确;
B.溴与NaOH溶液反应生成易溶于水的溴化钠和次溴酸钠,然后分液可达目的,B正确;
C.生石灰与水反应生成Ca(OH)2,后蒸馏可得无水乙醇,C正确;
D.乙醇与苯互溶,利用分液法无法实现分离,D错误;
故选D。
15.A
【详解】A.苯能燃烧,充分反应后生成二氧化碳和水,A项错误;
B.苯密度小于水,B项正确;
C.苯的结构中含有单双键交替的大π键,不能使酸性高锰酸钾溶液褪色,C项正确;
D.一定条件下,苯可与浓硝酸发生取代反应,D项正确;
故答案选A。
16.(1) HBr 冷凝回流作用
(2) 除去未反应的Br2 干燥溴苯
(3) 苯 C
【详解】(1)a中,Fe和溴发生氧化反应生成溴化铁,在溴化铁作催化剂条件下,苯和溴发生取代反应生成溴苯和HBr,HBr遇水蒸气生成氢溴酸小液滴而产生白雾,冷凝管有冷凝回流作用,提高反应物的利用率;生成的HBr和挥发出的溴通过导气管进入a中和氢氧化钠反应生成钠盐。故答案为:HBr;冷凝回流作用;
(2)②通过分液进一步提纯粗溴苯的过程中,需要使用分液漏斗,溴苯中含有溴,加NaOH溶液,把未反应的Br2转变为NaBr和NaBrO洗到水中;故答案为:除去未反应的Br2;
③向分离出的粗溴苯中加入少量的无水氯化钙,静置、过滤。加入氯化钙的目的是:加入干燥剂,无水氯化钙能干燥溴苯,故答案为:干燥溴苯;
(3)反应后得到的溴苯中溶有少量未反应的苯。利用沸点不同,苯的沸点小,被蒸馏出,溴苯留在母液中,所以采取蒸馏的方法分离溴苯与苯,
故答案为:苯;C;
17.(1)+Br2+HBr↑
(2) 吸收挥发出来的溴蒸气 产生白雾,溶液变红 产生淡黄色沉淀
(3)广口瓶中的水沿导管进入三颈烧瓶中,瓶中液体出现分层
【分析】苯和液溴发生反应生成溴苯和溴化氢,溴易挥发,苯可以吸收溴化氢中的溴,溴化氢溶于水显酸性,能使石蕊溶液变红,溴化氢溶于水发生电离,电离出来的Br-和硝酸银溶液中的Ag+生成AgBr淡黄色沉淀,HBr极易溶于水,用NaOH溶液吸收时需要防止倒吸。
(1)
三颈烧瓶中发生的主要反应是苯和液溴的取代反应,反应的化学方程式为:+Br2+HBr↑。
(2)
溴易挥发,生成的溴化氢中混有溴蒸气,所以试管C中苯的作用是吸收挥发出来的溴蒸气。溴化氢易挥发,溶于水显酸性,所以试管D中出现的现象是产生白雾,溶液变红。溴化银是淡黄色沉淀,所以试管E中出现的现象是产生淡黄色沉淀。
(3)
待三颈烧瓶中的反应进行到仍有气泡冒出时打开弹簧夹G,关闭弹簧夹B,由于HBr极易溶于水,水会倒吸进三颈烧瓶中,又因为溴苯不溶于水,所以可以看到的现象是广口瓶中的水沿导管进入三颈烧瓶中,瓶中液体出现分层。
18.(1)C
(2)
(3)2I-+2+4H+=2NO↑+I2+2H2O
(4)升华(或加热)
(5)氯气、酸性高锰酸钾都是强氧化剂,会继续氧化I2
(6)滴加少量Fe2(SO4)3溶液,再滴加几滴淀粉溶液,振荡
【分析】(1)
原油是多种烷烃、环烷烃的混合物,主要存在状态是液态。根据它们沸点的不同,将互溶的液态混合物进行分离,采用的方法是分馏,然后以C4-C10的烃类混合物为原料,采用裂解方法制取得到乙烯、丙烯等烯烃,烯烃中含有不饱和的碳碳双键,在一定条件下发生加成反应产生聚乙烯、聚丙烯,故操作操作②是裂解,合理选项是C。
(2)
乙烯在一定条件下发生加成反应产生聚乙烯,其结构简式是。
(3)
在酸性条件下具有氧化性,会将I-氧化产生I2,被还原产生NO,同时产生H2O,根据电子守恒、电荷守恒、原子守恒,可得该反应的离子方程式为:2I-+2+4H+=2NO↑+I2+2H2O。
(4)
酸性条件下、I-反应产生的I2,根据碘单质受热时发生升华的特性,在低温下干燥,然后经升华、冷凝、结晶就得到粗碘。
(5)
Cl2、酸性KMnO4等都是常用的强氧化剂,但该工艺中氧化卤水中的I-却选择了价格较高的NaNO2,这是是由于它们的氧化性太强,会将反应产生的I2进一步氧化。
(6)
I-具有还原性,Fe3+具有氧化性,二者会发生氧化还原反应产生I2,I2使淀粉溶液变为蓝色,故检验滤液中的 I-操作方法是:将滤液用CCl4多次萃取、分液,直到水层用淀粉溶液检验不出碘单质存在,然后滴加少量Fe2(SO4)3溶液,再滴加几滴淀粉溶液,振荡,若溶液变为蓝色,说明其中含有I-;若溶液不变蓝色,则溶液中不含I-。
19.(1) A为CH2=CH2,B为CH3CH2OH,C为CH3CHO,D为CH3COOH,E为CH3COOC2H5,F为CH3CH2Br A:官能团为碳碳双键,属于烯烃;B:官能团为羟基,属于醇类;C:官能团为醛基,属于醛类;D:官能团为羧基,属于羧酸类;E:官能团为酯基,属于酯类;F:官能团为溴原子,属于卤代烃类
(2) CH2=CH2+HBrCH3CH2Br;属于加成反应 2CH3CH2OH+O22CH3CHO+2H2O;属于氧化反应 CH3COOH+CH3CH2OH CH3COOC2H5+ H2O,属于取代反应或酯化反应
【分析】A是石油化学工业重要的基本原料,相对分子质量为28,A为乙烯;乙烯水化制备乙醇B,乙醇氧化为乙醛C、继续氧化为乙酸D,乙醇和乙酸发生酯化反应生成乙酸乙酯E;乙烯与溴化氢发生加成生成溴乙烷,据以上分析进行解答。
(1)
结合以上分析可知,有机物A~F的结构简式分别为:A为CH2=CH2,官能团为碳碳双键,属于烯烃;B为CH3CH2OH,官能团为羟基,属于醇类;C为CH3CHO,官能团为醛基,属于醛类;D为CH3COOH,官能团为羧基,属于羧酸类;E为CH3COOC2H5,官能团为酯基,属于酯类;F为CH3CH2Br,官能团为溴原子,属于卤代烃类;
(2)
①A→F:乙烯与溴化氢在一定条件下发生加成生成溴乙烷,化学方程式为:CH2=CH2+HBrCH3CH2Br;属于加成反应;
②B→C:乙醇催化氧化为乙醛,化学方程式为:2CH3CH2OH+O22CH3CHO+2H2O;属于氧化反应;
③B+D→E:乙醇和乙酸发生取代反应生成乙酸乙酯,化学方程式为:CH3COOH+CH3CH2OH CH3COOC2H5+ H2O,属于取代反应或酯化反应;
答案第1页,共2页
答案第1页,共2页
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1.化学与生产生活息息相关。下列说法中,正确的是
A.聚氯乙烯塑料可用作不粘锅的耐热涂层
B.用热的纯碱溶液可清洗衣物上的汽油污渍
C.氯碱工业中,可用浓氨水检查氯气管道是否泄漏
D.金属钠着火时,可用碳酸氢钠干粉灭火器扑灭
2.2022年12月4日,神舟十四号载人飞船返回舱在东风着陆场成功着陆。下列说法不正确的是
A.氧化铝陶瓷可作火箭腹部的隔热瓦,说明氧化铝熔点高
B.舱体表面的低密度烧蚀涂层中使用的苯基硅橡胶是有机高分子材料
C.飞船身上的“超薄皮肤”——铝合金蒙皮板的强度、硬度比金属铝小
D.空间站的能源为柔性砷化镓太阳能电池阵,砷化镓属于半导体材料
3.材料对于促进生产发展、改善人类生活发挥着巨大作用。下列有关材料的说法正确的是
A.不锈钢中含有铬、镍等元素,具有很强的抗腐蚀能力
B.用来生产电闸、灯口等产品的酚醛树脂属于聚酯类化合物
C.汽车机盖上使用的碳纤维是一种新型有机高分子材料
D.在钢中加入某些稀土元素,可降低钢的韧性、塑性等
4.下列有关煤的叙述正确的是
A.煤是由有机物和无机物组成的复杂的混合物,主要含碳、氢元素
B.煤在空气中加强热可得焦炭、煤焦油、粗氨水和焦炉气
C.推广使用煤液化和气化技术,可减少二氧化碳等温室气体的排放
D.煤的气化的主要反应是
5.下列关于乙烷、乙烯、乙炔的说法正确的是
①它们既不是同系物,也不是同分异构体 ②乙烷属于饱和烃,乙烯、乙炔属于不饱和烃
③乙烯、乙炔能使溴水褪色,乙烷不能使溴水褪色 ④它们都能燃烧
⑤它们都能使酸性溶液褪色
A.①③④ B.①②③⑤ C.②③④⑤ D.①②③④
6.下列有关化学品的使用正确的是
A.凡含有食品添加剂的食物对人体均有害,不可食用
B.聚乙烯、聚氯乙烯制成的塑料袋都可用于食品包装
C.适量的食品添加剂可以改变食物的色、香、味、营养结构、腐败时间等,如可以在食盐中加碘、酱油中补铁,食物中加维生素,这些做法都是积极的,对人体有益的
D.苏打片(成分NaHCO3)、胃舒平[成分是Al(OH)3]都可用于胃溃疡病人胃酸过多的治疗
7.已知(b)、(c)、(d)的分子式均为C6H6,下列说法正确的是
A.b的同分异构体只有c和d两种
B.b、c、d的二氯代物均只有三种
C.b、c、d均可与酸性高锰酸钾溶液反应
D.b、c、d中只有b的所有原子处于同一平面
8.以下结构表示的物质中是烷烃的是
①CH3OH ②CH2=CH2 ③ ④CH3CH3
A.①和② B.①和③ C.①和④ D.③和④
9.苯乙烯是一种重要的有机化工原料,其结构简式为,它不可能具有的性质是
A.易溶于水,不易溶于有机溶剂
B.在空气中燃烧产生黑烟
C.它能使溴的四氯化碳溶液褪色,也能使酸性高锰酸钾溶液褪色
D.能发生加成反应
10.科学家在-100℃的低温下合成了一种结构简式为的烃X,实验测得其分子中只有一种氢原子,根据分析,下列说法中不正确的是
A.X的分子式为C5H4
B.X能使酸性高锰酸钾溶液褪色
C.1molX在一定条件下可与2mol氢气发生反应
D.X的一氯代物只有2种
11.由乙烯的结构和性质推测丙烯(CH2=CH—CH3)的结构或性质正确的是
A.不能使酸性KMnO4溶液褪色
B.所有的原子都在同一平面内
C.能使溴的四氯化碳溶液褪色
D.与HCl在一定条件下能加成,并只得到一种产物
12.下列各反应中属于加成反应的是
①+Br2→BrCH=CHBr
②H2+Cl22HCl
③
④CH3CH3+2Cl2CH2ClCH2Cl+2HCl
A.①② B.②③
C.①③ D.②④
13.对比甲烷和乙烯的燃烧反应,下列叙述中正确的是
A.二者燃烧时现象完全相同
B.点燃前都不需验纯
C.甲烷燃烧的火焰呈淡蓝色,乙烯燃烧的火焰较明亮且伴有黑烟
D.二者燃烧时都有黑烟生成
14.下列除杂方法不正确的是
A.除去乙烷中混有的少量乙烯:通入稀溴水中,干燥
B.除去溴苯中混有的少量单质溴:加入足量的NaOH溶液,振荡、静置、分液
C.除去75%的乙醇中的水制无水乙醇:加入生石灰,振荡、静置、蒸馏
D.除去乙醇中混有的少量苯,可通过分液的方法实现
15.下列关于苯的说法不正确的是
A.苯不能燃烧 B.苯密度小于水
C.苯不能使酸性高锰酸钾溶液褪色 D.一定条件下,苯可与浓硝酸发生取代反应
二、实验题
16.溴苯是一种化工原料,实验室合成溴苯的仪器装置示意图(夹持及加热装置略去)及有关数据如下:
物质 苯 溴 溴苯
密度/() 0.88 3.12 1.50
沸点/℃ 80 59 156
在水中的溶解性 不溶 微溶 不溶
按下列合成步骤完成各题。
(1)向a中加入15无水苯和少量铁屑,向b中小心加入4液态溴。由b向a中滴入几滴液溴,有白色烟雾产生,是因为生成了________气体;继续滴加至液滴完。装置c的作用是_________________。
(2)充分反应后,经过下列步骤分离提纯。
①向a中加入10水,然后过滤除去未反应的铁屑。
②滤液依次用10水、8稀溶液、10水洗涤。用溶液洗涤的作用是_________________。
③向分离出的粗溴苯中加入少量无水氯化钙,静置、过滤。加入氯化钙的目的是_________________。
(3)经以上分离操作后,粗溴苯还含有的主要杂质为________;要进一步提纯,下列操作中必须进行的是________ (填写字母)。
A.重结晶 B.过滤 C.蒸馏 D.萃取
17.实验室制备溴苯可用如图所示装置(部分装置已省略)。
请回答下列问题:
(1)关闭弹簧夹G,打开弹簧夹B,从装有少量苯的三颈烧瓶的A口加少量液溴,再加入少量铁屑,塞住A口,三颈烧瓶中发生的主要反应的化学方程式为_______________。
(2)试管C中苯的作用是__________;
试管D中出现的现象是_________________;
试管E中出现的现象是______________。
(3)待三颈烧瓶中的反应进行到仍有气泡冒出时打开弹簧夹G,关闭弹簧夹B,可以看到的现象是_______________。
三、工业流程题
18.我国资源丰富,合理开发利用资源,才能实现可持续发展。
Ⅰ.以原油为原科生产有机高分子材料聚乙烯、聚丙烯的流程如下:
(1)流程中②表示的加工方法是____(填序号)。
A.分馏 B.聚合 C.裂解 D.干馏
(2)写出聚乙烯的结构简式_______。
Ⅱ.浩瀚的海洋中蕴藏着丰富的资源。从海水中可以提取很多有用的物质,例如从海水制盐所得到的卤水中可以提取碘。活性炭吸附法是工业提取碘的方法之一,其流程如下:
资料显示:
ⅰ. pH=2 时, NaNO2溶液只能将I-氧化为I2,同时生成 NO
ⅱ. I2+5Cl2+6H2O=2HIO3+10HCl; 氧化性:KMnO4>Cl2
ⅲ. 2Fe3++2I-=2Fe2++I2
(3)写出反应①的离子方程式_______。
(4)方案甲中,根据 I2的特性,分离操作 X 应为___________、冷凝结晶。
(5)Cl2、酸性KMnO4等都是常用的强氧化剂,但该工艺中氧化卤水中的 I-却选择了价格较高的NaNO2,原因是_______。
(6)方案乙中,已知反应③过滤后,滤液中仍存在少量的 I2、I-。 为了检验滤液中的 I-,某小组同学设计如下实验方案,请将实验步骤补充完整。
实验中可供选择的试剂:稀H2SO4、淀粉溶液、Fe2(SO4)3溶液、CCl4。
a.将滤液用CCl4多次萃取、分液,直到水层用淀粉溶液检验不出碘单质存在,
b.从水层取少量溶液于试管中,_______。
四、有机推断题
19.已知A是石油化学工业重要的基本原料,相对分子质量为28,在一定条件下能发生下图所示的转化关系.
(1)写出有机物A~F的结构简式_________分子中官能团的名称和所属的有机物类别.__________
(2)写出实现下列转化的化学方程式,并注明反应类型.
①A→F_______________
②B→C_______________
③B+D→E__________
第1页 共4页 ◎ 第2页 共4页
第1页 共4页 ◎ 第2页 共4页
参考答案:
1.C
【详解】A.聚氯乙烯塑料不耐热,不能用作不粘锅的耐热涂层,故A错误;
B.汽油不能和碳酸钠溶液反应,也不溶于碳酸钠溶液,不能用热的纯碱溶液可清洗衣物上的汽油污渍,故B错误;
C.氯碱工业中,可用浓氨水检查氯气管道是否泄漏,氨气遇到氯气会产生白烟,故C正确;
D.金属钠为活泼金属,着火时,可与二氧化碳、水反应,则金属钠着火时,不可用碳酸氢钠干粉灭火器扑灭,故D错误;
故选C。
2.C
【详解】A.火箭腹部有高热量区,使用氧化铝陶瓷作隔热瓦,说明氧化铝熔点高,A正确;
B.苯基硅橡胶属于有机高分子材料,B正确;
C.合金的强度和硬度一般都比组成它的各成分金属大,C错误;
D.砷化镓可用于制备柔性砷化镓太阳能电池阵,说明砷化镓能导电,类比硅可用于制造太阳能电池,可知其为半导体材料,D正确;
故选C。
【点睛】合金的强度和硬度一般都比组成它的各成分金属大,这是因为一种金属原子或非金属原子在其他金属原子的晶体结构中占据了一定位置,会造成金属晶体结构的变形,从而使金属晶体在发生错位时阻力上升、形变困难,导致其强度、硬度增大。
3.A
【详解】A.不锈钢中含有铬、镍元素,能改变金属的内部结构,使铁合金具有很强的抗腐蚀能力,A项正确;
B.酚醛树脂是由酚类和醛类聚合而成的,不属于聚酯,B项错误;
C.碳纤维属于碳单质,不是新型有机高分子材料,C项错误;
D.在钢中加入某些稀土元素形成的合金,可增强钢的韧性、塑性等,D项错误;
故选A。
4.A
【详解】A.煤中有机质是复杂的高分子有机化合物,主要由碳、氢、氧、氮、硫和磷等元素组成,而碳、氢、氧三者总和约占有机质的95%以上;煤中的无机质也含有少量的碳、氢、氧、硫等元素,A正确;
B.煤在空气中加强热会燃烧,要想将煤干馏,需隔绝空气加强热,B错误;
C.煤的液化和气化,不能减少二氧化碳等温室气体的排放,C错误;
D.煤的气化主要是煤与水蒸气发生置换反应,生成水煤气,C(s)+H2O(g)CO(g)+H2(g),D错误;
故答案为:A。
5.D
【详解】①乙烷、乙烯和乙炔结构不相似,分子式也不同,所以它们既不是同系物,也不是同分异构体,故①正确;
②乙烷是饱和烃,乙烯、乙炔中含有碳碳不饱和键,因此乙烯和乙炔是不饱和烃,故②正确;
③乙烯、乙炔中碳碳不饱和键能和溴水发生加成反应而使溴水褪色,乙烷和溴水不反应因而不能使溴水褪色,故③正确;
④它们都属于有机物,都能燃烧,故④正确;
⑤乙烯和乙炔中碳碳不饱和键能被酸性高锰酸钾溶液氧化而使酸性高锰酸钾溶液褪色,乙烷性质稳定和高锰酸钾溶液不反应,所以不能使酸性高锰酸钾溶液褪色,故⑤错误;
综上所述,①②③④正确,故选D。
6.C
【详解】A.含有食品添加剂的食物不一定对人体有害,在规定范围内合理使用食品添加剂,对人体健康不会产生不良影响,故A错误;
B.聚乙烯无毒,聚乙烯做成的塑料可用于食品包装袋,聚氯乙烯是由聚氯乙烯树脂、增塑剂和防老剂组成的树脂,本身并无毒性,所加的增塑剂、防老剂等主要辅料有毒性,因此聚氯乙烯制成的塑料不能用于食品包装袋,故B错误;
C.适量的食品添加剂可以改变食物的色、香、味、营养结构、腐败时间等,如可以在食盐中加碘、酱油中补铁,食物中加维生素,这些做法都是积极的,对人体有益的,故C正确;
D.苏打片与胃酸产生CO2,二氧化碳加速胃溃疡,因此苏打片不用于胃溃疡病人胃酸过多,故D错误;
答案为C。
7.D
【详解】A.b是苯,其同分异构体还可以是链状不饱和烃,同分异构体有多种,不止d和p两种,A错误;
B.c分子中氢原子分为2类,根据定一移一可知c的二氯代物是6种,B错误;
C.b、d分子中不存在碳碳双键,不与酸性高锰酸钾溶液发生反应,C错误;
D.苯是平面形结构,所有原子共平面,d、c中均含有饱和碳原子,所有原子不可能共平面,D正确;
故答案为D。
8.D
【详解】①CH3OH含有羟基为醇类, ②CH2=CH2 为乙烯是烯烃,③为异丁烷, ④CH3CH3为乙烷,是烷烃,综上所述故选D。
9.A
【详解】A.苯乙烯为烃,难溶于水,易溶于有机溶剂,选A;
B.苯乙烯的分子式为C8H8,与苯的最简式相同,即含碳量很高,故燃烧时产生黑烟,B不选;
C.因分子中含有碳碳双键,所以苯乙烯能与溴水发生加成反应而使溴水褪色;苯乙烯能被酸性高锰酸钾溶液氧化,而使酸性KMnO4溶液褪色,C不选;
D.苯乙烯中苯环能与H2发生加成反应,苯乙烯中的碳碳双键和溴、卤化氢、氢气等发生加成反应,D不选;
故本题选A。
10.D
【详解】A.根据烃X的结构简式可知其分子式为C5H4,A正确;
B.X分子中含碳碳双键,能使酸性KMnO4溶液褪色,B正确;
C.X分子中含两个碳碳双键,1molX在一定条件下可与2mol氢气发生加成反应,C正确;
D.由结构对称性可知,分子中只有一种位置的H,一氯代物只有1种,D错误;
故选D。
11.C
【详解】A.因丙烯分子同乙烯分子一样含有碳碳双键,所以能被酸性KMnO4溶液氧化而使之褪色,A错误;
B.因丙烯分子中含有甲基(—CH3),甲基是三角锥的空间结构,故丙烯中所有原子不可能在同一平面内,B错误;
C.丙烯能与溴发生加成反应,而使溴的四氯化碳溶液褪色,C正确;
D.丙烯能与HCl加成得到两种产物,D错误;
故本题选C。
12.C
【详解】①含有碳碳三键,+Br2→BrCH=CHBr属于加成反应;
②H2+Cl22HCl属于化合反应;
③环己烯含有碳碳双键, 属于加成反应;
④CH3CH3+2Cl2CH2ClCH2Cl+2HCl属于取代应;故①③属于加成反应,故C正确;
故选C。
13.C
【分析】因为甲烷和乙烯的含碳量不同,故燃烧时的现象不同,甲烷含碳量较低,火焰呈淡蓝色,不产生黑烟,而乙烯含碳量较高,燃烧时火焰较明亮且伴有黑烟
【详解】A.二者燃烧时现象不相同,故A错误;
B.CH4与C2H4都是可燃性气体,若气体不纯,点燃时可能发生爆炸,因此点燃前需验纯,故B正确;
C.甲烷含碳量较低,燃烧时不产生黑烟,而乙烯含碳量较高,燃烧时火焰较明亮且伴有黑烟,故C正确;
D.甲烷含碳量较低,燃烧时不产生黑烟,而乙烯含碳量较高,燃烧时火焰较明亮且伴有黑烟,故D错误;
故选C。
14.D
【详解】A.乙烯与溴水中Br2发生加成反应生成1,2 二溴乙烷,乙烷不反应,经洗气干燥后可得纯净乙烷,A正确;
B.溴与NaOH溶液反应生成易溶于水的溴化钠和次溴酸钠,然后分液可达目的,B正确;
C.生石灰与水反应生成Ca(OH)2,后蒸馏可得无水乙醇,C正确;
D.乙醇与苯互溶,利用分液法无法实现分离,D错误;
故选D。
15.A
【详解】A.苯能燃烧,充分反应后生成二氧化碳和水,A项错误;
B.苯密度小于水,B项正确;
C.苯的结构中含有单双键交替的大π键,不能使酸性高锰酸钾溶液褪色,C项正确;
D.一定条件下,苯可与浓硝酸发生取代反应,D项正确;
故答案选A。
16.(1) HBr 冷凝回流作用
(2) 除去未反应的Br2 干燥溴苯
(3) 苯 C
【详解】(1)a中,Fe和溴发生氧化反应生成溴化铁,在溴化铁作催化剂条件下,苯和溴发生取代反应生成溴苯和HBr,HBr遇水蒸气生成氢溴酸小液滴而产生白雾,冷凝管有冷凝回流作用,提高反应物的利用率;生成的HBr和挥发出的溴通过导气管进入a中和氢氧化钠反应生成钠盐。故答案为:HBr;冷凝回流作用;
(2)②通过分液进一步提纯粗溴苯的过程中,需要使用分液漏斗,溴苯中含有溴,加NaOH溶液,把未反应的Br2转变为NaBr和NaBrO洗到水中;故答案为:除去未反应的Br2;
③向分离出的粗溴苯中加入少量的无水氯化钙,静置、过滤。加入氯化钙的目的是:加入干燥剂,无水氯化钙能干燥溴苯,故答案为:干燥溴苯;
(3)反应后得到的溴苯中溶有少量未反应的苯。利用沸点不同,苯的沸点小,被蒸馏出,溴苯留在母液中,所以采取蒸馏的方法分离溴苯与苯,
故答案为:苯;C;
17.(1)+Br2+HBr↑
(2) 吸收挥发出来的溴蒸气 产生白雾,溶液变红 产生淡黄色沉淀
(3)广口瓶中的水沿导管进入三颈烧瓶中,瓶中液体出现分层
【分析】苯和液溴发生反应生成溴苯和溴化氢,溴易挥发,苯可以吸收溴化氢中的溴,溴化氢溶于水显酸性,能使石蕊溶液变红,溴化氢溶于水发生电离,电离出来的Br-和硝酸银溶液中的Ag+生成AgBr淡黄色沉淀,HBr极易溶于水,用NaOH溶液吸收时需要防止倒吸。
(1)
三颈烧瓶中发生的主要反应是苯和液溴的取代反应,反应的化学方程式为:+Br2+HBr↑。
(2)
溴易挥发,生成的溴化氢中混有溴蒸气,所以试管C中苯的作用是吸收挥发出来的溴蒸气。溴化氢易挥发,溶于水显酸性,所以试管D中出现的现象是产生白雾,溶液变红。溴化银是淡黄色沉淀,所以试管E中出现的现象是产生淡黄色沉淀。
(3)
待三颈烧瓶中的反应进行到仍有气泡冒出时打开弹簧夹G,关闭弹簧夹B,由于HBr极易溶于水,水会倒吸进三颈烧瓶中,又因为溴苯不溶于水,所以可以看到的现象是广口瓶中的水沿导管进入三颈烧瓶中,瓶中液体出现分层。
18.(1)C
(2)
(3)2I-+2+4H+=2NO↑+I2+2H2O
(4)升华(或加热)
(5)氯气、酸性高锰酸钾都是强氧化剂,会继续氧化I2
(6)滴加少量Fe2(SO4)3溶液,再滴加几滴淀粉溶液,振荡
【分析】(1)
原油是多种烷烃、环烷烃的混合物,主要存在状态是液态。根据它们沸点的不同,将互溶的液态混合物进行分离,采用的方法是分馏,然后以C4-C10的烃类混合物为原料,采用裂解方法制取得到乙烯、丙烯等烯烃,烯烃中含有不饱和的碳碳双键,在一定条件下发生加成反应产生聚乙烯、聚丙烯,故操作操作②是裂解,合理选项是C。
(2)
乙烯在一定条件下发生加成反应产生聚乙烯,其结构简式是。
(3)
在酸性条件下具有氧化性,会将I-氧化产生I2,被还原产生NO,同时产生H2O,根据电子守恒、电荷守恒、原子守恒,可得该反应的离子方程式为:2I-+2+4H+=2NO↑+I2+2H2O。
(4)
酸性条件下、I-反应产生的I2,根据碘单质受热时发生升华的特性,在低温下干燥,然后经升华、冷凝、结晶就得到粗碘。
(5)
Cl2、酸性KMnO4等都是常用的强氧化剂,但该工艺中氧化卤水中的I-却选择了价格较高的NaNO2,这是是由于它们的氧化性太强,会将反应产生的I2进一步氧化。
(6)
I-具有还原性,Fe3+具有氧化性,二者会发生氧化还原反应产生I2,I2使淀粉溶液变为蓝色,故检验滤液中的 I-操作方法是:将滤液用CCl4多次萃取、分液,直到水层用淀粉溶液检验不出碘单质存在,然后滴加少量Fe2(SO4)3溶液,再滴加几滴淀粉溶液,振荡,若溶液变为蓝色,说明其中含有I-;若溶液不变蓝色,则溶液中不含I-。
19.(1) A为CH2=CH2,B为CH3CH2OH,C为CH3CHO,D为CH3COOH,E为CH3COOC2H5,F为CH3CH2Br A:官能团为碳碳双键,属于烯烃;B:官能团为羟基,属于醇类;C:官能团为醛基,属于醛类;D:官能团为羧基,属于羧酸类;E:官能团为酯基,属于酯类;F:官能团为溴原子,属于卤代烃类
(2) CH2=CH2+HBrCH3CH2Br;属于加成反应 2CH3CH2OH+O22CH3CHO+2H2O;属于氧化反应 CH3COOH+CH3CH2OH CH3COOC2H5+ H2O,属于取代反应或酯化反应
【分析】A是石油化学工业重要的基本原料,相对分子质量为28,A为乙烯;乙烯水化制备乙醇B,乙醇氧化为乙醛C、继续氧化为乙酸D,乙醇和乙酸发生酯化反应生成乙酸乙酯E;乙烯与溴化氢发生加成生成溴乙烷,据以上分析进行解答。
(1)
结合以上分析可知,有机物A~F的结构简式分别为:A为CH2=CH2,官能团为碳碳双键,属于烯烃;B为CH3CH2OH,官能团为羟基,属于醇类;C为CH3CHO,官能团为醛基,属于醛类;D为CH3COOH,官能团为羧基,属于羧酸类;E为CH3COOC2H5,官能团为酯基,属于酯类;F为CH3CH2Br,官能团为溴原子,属于卤代烃类;
(2)
①A→F:乙烯与溴化氢在一定条件下发生加成生成溴乙烷,化学方程式为:CH2=CH2+HBrCH3CH2Br;属于加成反应;
②B→C:乙醇催化氧化为乙醛,化学方程式为:2CH3CH2OH+O22CH3CHO+2H2O;属于氧化反应;
③B+D→E:乙醇和乙酸发生取代反应生成乙酸乙酯,化学方程式为:CH3COOH+CH3CH2OH CH3COOC2H5+ H2O,属于取代反应或酯化反应;
答案第1页,共2页
答案第1页,共2页
