第八章化学与可持续发展单元通关卷(含解析)高一下学期化学人教版(2019)必修第二册
文档属性
| 名称 | 第八章化学与可持续发展单元通关卷(含解析)高一下学期化学人教版(2019)必修第二册 |  | |
| 格式 | docx | ||
| 文件大小 | 345.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-06-20 07:39:35 | ||
图片预览



文档简介
第八章化学与可持续发展单元通关卷
一、单选题
1.化学与生产、生活密切相关。下列说法错误的是
A.燃煤中加入CaO可以减少温室气体CO2的排放
B.肥皂水可用作蚊虫叮咬处的清洗剂
C.纳米铁粉可以除被污染水体中的重金属离子
D.硅胶可用作袋装食品、瓶装药品等的干燥剂
2.绿色化学的核心是反应过程的绿色化,即要求原料物质中的所有原子完全被利用且全部转入期望的产品中。下列过程不符合绿色化学理念的是
A.
B.甲烷与氯气反应制氯仿:
C.甲烷、CO合成乙酸乙酯:
D.烯烃与水煤气发生羰基合成反应:
3.“垃圾分类就是新时尚”,实行垃圾分类,创造美好生活。下列垃圾不属于厨房垃圾的是
A.蛋壳 B.果皮 C.剩菜 D.漂白粉
4.可用于治疗胃酸过多的物质是
A.碳酸氢钠 B.氯化钠 C.氯化钾 D.氢氧化钠
5.昆明市预计在2020年底前基本建成生活垃圾分类处理系统。下列关于垃圾处理的说法不正确的是
A.废旧塑料瓶可回收利用 B.废旧电池可直接掩埋
C.电子垃圾可用适当的方法回收利用 D.厨余垃圾可经生物技术处理堆肥
6.在给定条件下,下列选项所示的物质间转化均能实现的是
A.
B.
C.
D.
7.下列说法中,正确的是
A.煤和石油都是不可再生的化石能源,其主要组成元素均为碳、氢元素,二者都是混合物
B.煤的干馏和石油的分馏原理相同,都是化学变化
C.煤的液化主要是为了得到苯等重要的有机化工原料
D.煤干馏得到的煤焦油,其主要用途就是再经蒸馏得到高品质燃油
8.最理想的“原子经济”就是反应物中的原子全部转化为欲制得的产物,即原子利用率为100%。下列反应能体现“原子经济”原则的是
A.乙醇与乙酸的酯化反应 B.蔗糖的水解
C.以苯和溴为原料生产溴苯 D.乙烯与水反应生成乙醇
9.下列金属冶炼的反应原理,不正确的是( )
A.2MgCl2(熔融)Mg+Cl2↑ B.Fe2O3+3CO2Fe+3CO2
C.HgSHg+S D.2Al2O3(熔融)4Al+3O2↑
10.废弃的铝制易拉罐应投入的垃圾桶上贴有的垃圾分类标志是
A.有害垃圾
B.可回收物
C.餐厨垃圾
D.其他垃圾
11.下列说法正确的是
A.最重要的人工固氮途径是工业合成氨
B.光束通过硫酸铜溶液时,可观察到丁达尔效应
C.卢瑟福认为原子是坚实的、不可再分的实心球
D.长期服用阿司匹林可预防某些疾病,没有副作用
12.迄今为止,煤、石油和天然气等化石能源仍然是人类使用的主要能源。下列有关煤、石油和天然气的说法中,错误的是
A.石油通过裂化,可以获得碳原子数较少的轻质油 B.煤液化后可以转变为石油
C.天然气是一种清洁的化石燃料 D.石油裂解后可得到短链不饱和烃
13.中国向世界庄严宣布:二氧化碳排放力争在2030年前达到峰值,在2060年前达到碳中和。下列措施不能减少碳排放的是
A.推广“液态阳光”技术,促使CO2加氢转化为液态燃料
B.在汽车排气管里安装催化转化装置
C.倡导低碳生活,注意节约用电
D.利用风能、水能等可再生能源发电替代火力发电
14.下列说法正确的是
A.石墨烯属于有机物 B.蒸发海水就能从海水中获得碘、烧碱和食盐
C.二氧化硅材料广泛用于光纤通讯 D.粗硅制备单晶硅不涉及氧化还原反应
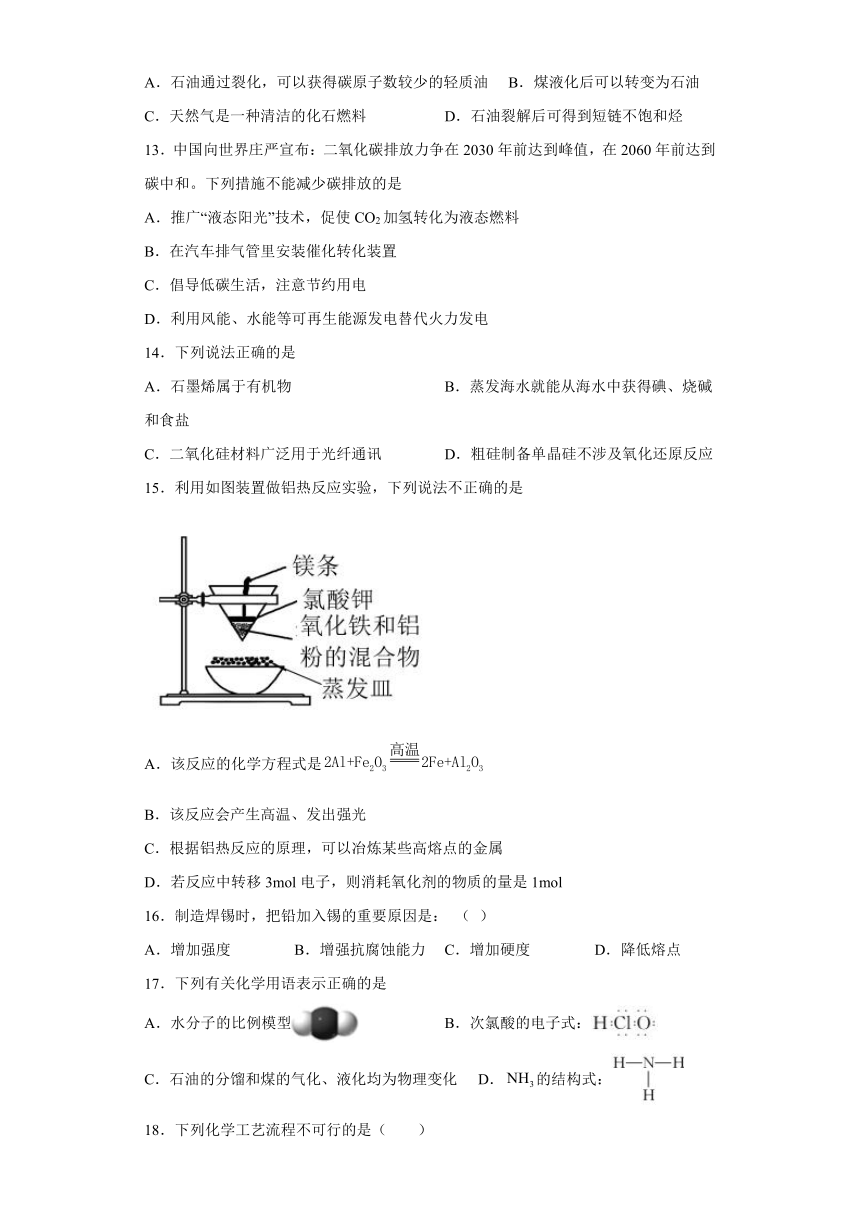
15.利用如图装置做铝热反应实验,下列说法不正确的是
A.该反应的化学方程式是
B.该反应会产生高温、发出强光
C.根据铝热反应的原理,可以冶炼某些高熔点的金属
D.若反应中转移3mol电子,则消耗氧化剂的物质的量是1mol
16.制造焊锡时,把铅加入锡的重要原因是: ( )
A.增加强度 B.增强抗腐蚀能力 C.增加硬度 D.降低熔点
17.下列有关化学用语表示正确的是
A.水分子的比例模型 B.次氯酸的电子式:
C.石油的分馏和煤的气化、液化均为物理变化 D.的结构式:
18.下列化学工艺流程不可行的是( )
A.实验室从海带中提取单质碘取样→灼烧→溶解→过滤→萃取→蒸馏
B.石英砂粗硅粗SiCl4高纯硅
C.FeS2SO2SO3H2SO4
D.铝土矿NaAlO2(aq)Al(OH)3Al2O3Al
二、填空题
19.要使垃圾中宝贵的再生资源得到充分利用,必须对垃圾进行分类,不同地区分类方法不同。如图是一些地区采用的垃圾分类图标。
(1)图C的文字已模糊不清,从图中可以看出它表示的是_______。
A.可回收物 B.可堆肥垃圾 C.可燃垃圾 D.有害垃圾
(2)上述各图中适宜于堆肥处理的垃圾是_______。
(3)图D表示的垃圾若随意丢弃,会造成环境污染,这种污染通常称为_______。该类塑料主要包括_______类、_______类、聚丙烯类等。
(4)图A废电池需要集中处理,主要原因是电池中的_______掺入生活垃圾中进行填埋时,会通过渗滤污染水体和土壤。
20.煤的干馏可分离出煤中含有的煤焦油。( )
21.请根据题意选择下列物质,并用其字母代号填空:
(1)一种红棕色粉末,常用于红色油漆和涂料的是____________
(2)要使浑浊的水变澄清,可使用____;
(3)要中和钢铁厂、电镀厂产生的酸性废水,可使用____;
(4)使焙制糕点松软可以添加____;
(5)家用大理石台面变粗糙的原因之一是滴上了____;
(6)误食假酒会使人中毒或者失明,其有害成分是____.
三、实验题
22.我国资源丰富,合理开发利用资源,才能实现可持续发展。
Ⅰ.以原油为原科生产有机高分子材料聚乙烯、聚丙烯的流程如图:
(1)流程中②表示的加工方法是___(填序号)。
A.分馏 B.聚合 C.裂解 D.干馏
(2)写出聚乙烯的结构简式___。
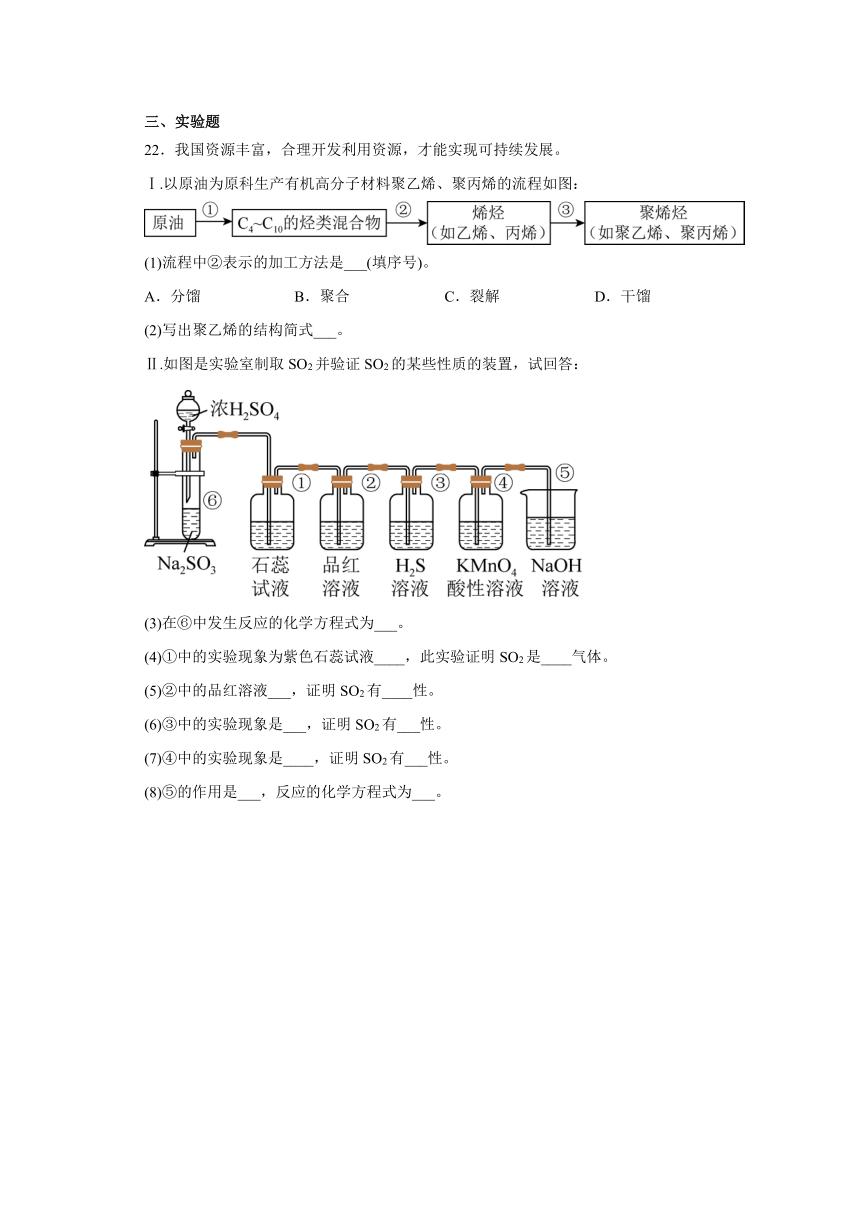
Ⅱ.如图是实验室制取SO2并验证SO2的某些性质的装置,试回答:
(3)在⑥中发生反应的化学方程式为___。
(4)①中的实验现象为紫色石蕊试液____,此实验证明SO2是____气体。
(5)②中的品红溶液___,证明SO2有____性。
(6)③中的实验现象是___,证明SO2有___性。
(7)④中的实验现象是____,证明SO2有___性。
(8)⑤的作用是___,反应的化学方程式为___。
参考答案:
1.A
【详解】本题考查化学与生活。
详解:加入氧化钙,氧化钙可与煤燃烧生成的二氧化硫在氧气中发生反应生成硫酸钙,减少二氧化硫排放量,但二氧化碳排放量没有减少,A错误;
肥皂水显碱性,与蚊虫叮咬处释放的酸发生中和反应,发生了化学反应,B正确;
纳米铁粉和污染水体中Pb2+、Cu2+、Hg2+发生置换反应生成金属单质而治理污染,C正确;
硅胶疏松具有吸水性,所以可用作实验室和袋装食品、瓶装药品等的干燥剂,D正确。
故选A。
2.B
【详解】根据绿色化学的核心是反应过程的绿色化,即要求原料物质中的所有原子完全被利用且全部转入期望的产品中,加成反应、加聚反应、化合反应都符合绿色化学理念。、、反应物完全转化为期望的产品中;甲烷与氯气反应制氯仿:是取代反应,反应物没有完全转化为期望的产品中,故B符合题意;
综上所述,答案为B。
3.D
【详解】A.蛋壳是鸡蛋壳,属于厨房垃圾,故A不符合题意;
B.果皮属于厨房垃圾,故B不符合题意;
C.剩菜剩饭都属于厨房垃圾,故C不符合题意;
D.漂白粉是工业产品,不属于厨房垃圾,故D符合题意。
综上所述,答案为D。
4.A
【分析】能用于治疗胃酸(含盐酸)过多的物质需具备能与盐酸反应且对人体无害的性质。
【详解】A、碳酸氢钠可与盐酸发生反应生成氯化钠和水以及二氧化碳,可用于治疗胃酸过多,选项A正确;B、NaCl不与盐酸反应,不能用于治疗胃酸过多,选项B错误;C、KCl不与盐酸反应,不能用于治疗胃酸过多,选项C错误;D、氢氧化钠具有极强的腐蚀性,对人体有害,不能用于治疗胃酸过多,选项D错误;答案选A。
【点睛】本题考查了常见物质的实际用途,完成此题,可以依据已有的知识进行。
5.B
【详解】A.废塑料瓶主要由聚乙烯或聚丙烯制造而成,可回收利用,属于可回收物,A选项正确;
B.废旧电池中含有重金属如铅、汞、镉等,将废旧电池直接掩埋会污染土壤、水源,废旧电池应集中回收处理,B选项错误;
C.电子产品含有重金属,任意抛弃会造成地下水污染,要在无污染的条件下进行回收,使之成为有用的资源,C选项正确;
D.厨余垃圾经生化处理转化为沼气和有机肥料,从而产生绿色有机食品和清洁燃料,D选项正确;
答案选B。
6.B
【详解】A.电解熔融的氧化铝制铝而不是氯化铝,A错误;
B.氯化镁与氢氧化钙发生复分解反应生成氢氧化镁,氢氧化镁受热分解生成氧化镁,B正确;
C.铁与氯气反应生成,C错误;
D.电解熔融的制取金属镁,D错误;
故选B。
7.A
【详解】A.煤和石油主要组成元素均为碳、氢元素,二者都是复杂混合物,均属于不可再生化石能源,A正确;
B.煤的干馏是化学变化,而石油分馏是物理变化,B错误;
C.煤的液化是把煤转变为液体燃料的过程,主要是为了得到甲醇等液体燃料、重要的有机化工原料,C错误;
D.煤焦油主要用于分离出苯、甲苯、二甲苯等有机化工原料,D错误;
故选A。
8.D
【详解】A.乙醇与乙酸的酯化反应生成乙酸乙酯和水,不符合原子的利用率为100%要求,故A不选;
B.蔗糖水解生成葡萄糖和果糖,不符合原子的利用率为100%要求,故B不选;
C.苯和溴反应生成溴苯和溴化氢,不符合原子的利用率为100%要求,故C不选;
D.乙烯与水反应生成乙醇是加成反应,原料分子中的原子全部转化成所需要的产物,符合原子的利用率为100%要求,故D符合题意;
故选D。
9.C
【详解】A.金属用电解氯化镁的方法,故正确;
B.铁用热还原法冶炼,故正确;
C.金属汞用氧化汞加热的方法,故错误;
D.电解氧化铝制取金属铝,故正确。
故选C。
10.B
【详解】A、废弃的铝制易拉罐是可回收物,不能投入贴有有害垃圾的垃圾桶,故不选A;
B、废弃的铝制易拉罐是可回收物,应投入贴有可回收物的垃圾桶,故选B;
C、废弃的铝制易拉罐是可回收物,不能投入贴有餐厨垃圾的垃圾桶,故不选C;
D、废弃的铝制易拉罐是可回收物,不能投入贴有其他垃圾的垃圾桶,故不选D。
11.A
【详解】A.工业合成氨是氮气和氢气在高温、高压、催化剂条件下反应生成氨气,属于人工固氮,故A正确;
B.硫酸铜溶液不是胶体,光束通过硫酸铜溶液时,不能观察到丁达尔效应,故B错误;
C.道尔顿认为原子是坚实的、不可再分的实心球,卢瑟福提出核式原子模型,故C错误;
D.长期服用阿司匹林可预防某些心脑血管疾病,有一定的副作用,如胃肠道反应、肝损害、肾损害等,故D错误;
选A。
12.B
【详解】A.石油裂化和裂解的目的是为了将重油中的碳链变短,从而得到生活和工业中需求量较大的产物。裂化的主要目的是为了获得轻质油,故A正确;
B.煤液化后可以转变为甲醇等化工原料,不转变为石油,故B错误;
C.天然气的主要成分为甲烷,充分燃烧后生成物为二氧化碳和水,为清洁的化石燃料,故C正确;
D.石油裂解后可得到短链不饱和烃,如乙烯、丙烯等化工原料,故D正确;
故选B。
13.B
【详解】A.将CO2加氢转化为液态燃料,可减少CO2排放,实现碳中和,选项A不符合题意;
B.汽车排气管中催化转化装置可以将CO与氮氧化物转化为CO2、N2等无污染物质,但不能减少CO2排放,选项B符合题意;
C.低碳生活可减少CO2排放,选项C不符合题意;
D.火力发电过程中产生大量CO2,利用新能源代替火力发电可减少CO2排放,选项D不符合题意;
答案选B。
14.C
【详解】A. 石墨烯是一种由碳原子组成的二维碳纳米材料,它是碳的单质,不属于烯烃,也不属于有机物,故A错误;
B. 蒸发海水就能从海水中获得食盐,但不能获得碘、烧碱,要通过化学方法提取、制备,故B错误;
C. 二氧化硅是制造玻璃、石英玻璃、水玻璃、光导纤维、电子工业的重要部件、光学仪器、工艺品和耐火材料的原料,是科学研究的重要材料,故C正确;
D. 粗硅制备单晶硅涉及Si(粗硅)+2Cl2 SiCl4、2H2+SiCl4Si(单晶硅)+4HCl这两个氧化还原反应,故D错误;
故选C。
15.D
【详解】A.铝热反应为高温下铝与氧化铁发生置换反应生成铁和氧化铝,反应的化学方程式是,故A正确;
B.铝热反应发生时会放出大量的热,产生高温、发出强光,故B正确;
C.铝热反应发生时会放出大量的热,可以冶炼某些高熔点的金属,如Fe、Cr、Mn、W等,故C正确;
D.铝热反应为高温下铝与氧化铁发生置换反应生成铁和氧化铝,反应时氧化铁为氧化剂,若反应中转移3mol电子,消耗氧化铁的物质的量为3mol×=0.5mol,故D错误;
故选D。
16.D
【详解】因合金熔点比成分金属低,硬度比成分金属大,所以制造焊锡时,把铅加入锡的重要原因是降低熔点,
答案选D。
【点睛】合金的熔点低于纯金属。
17.D
【详解】A.水分子的空间构型为V形,比例模型为,故A错误;
B.次氯酸的结构式为Cl—O—H,电子式为,故B错误;
C.煤的气化、液化过程中有新物质生成,属于化学变化,故C错误;
D.氨分子中每个氮原子与3个氢原子各共用一对电子,结构式为,故D正确;
故选D。
18.A
【详解】A.海带中碘是以碘离子形式存在,提取时需要氧化为单质,提取单质碘的工艺为:取样→灼烧→溶解→过滤→氧化→萃取→蒸馏,A错误;
B.碳与二氧化硅反应生成Si和CO,硅与氯气反应生成四氯化硅,最后氢气还原四氯化硅,B正确;
D.FeS2与氧气反应生成二氧化硫、二氧化硫催化氧化生成三氧化硫,三氧化硫与水反应生成硫酸,C正确;
D.氧化铝与NaOH反应生成偏铝酸钠,偏铝酸钠与过量二氧化碳反应生成氢氧化铝,氢氧化铝受热分解生成氧化铝,电解氧化铝生成铝,D正确;
答案选A。
19. D B 白色污染 聚乙烯 聚氯乙烯 铅、镉、银等元素
【详解】(1)图C预示该类垃圾对环境会造成污染,不利于植物的生长,故属于有害垃圾标志,此处选B;
(2)厨余垃圾中残留的有机物,在微生物作用下可分解为小分子水、氨、硝酸等,为植物生长提供肥料,故此处选B;
(3)塑料为有机高分子,在环境中很难降解,容易造成白色污染,故此处填白色污染;该类塑料一般通过加聚反应制得,主要包括聚乙烯类、聚氯乙烯类、聚丙烯类等等;
(4)电池中通常含有重金属元素,如铅蓄电池中的Pb元素,锌锰干电池中的Zn、Mn元素,镍镉电池中的Cd元素,银锌纽扣电池中的Ag元素等,这些重金属元素进入土壤中会污染水体和土壤,故需集中处理,此处填铅、镉、银等元素。
20.错误
【详解】煤经干馏能生产出焦炭、煤焦油、粗氨水和焦炉气等,故错误。
21. B A D C F E
【详解】解:(1)只有Fe2O3为红棕色,则常用于红色油漆和涂料的是B,故答案为B;
(2)只有明矾可水解生成胶体,用于水的净化,故答案为A;
(3)中和钢铁厂、电镀厂产生的酸性废水,选择碱,且便宜易得,则选择D,故答案为D;
(4)使焙制糕点松软可以添加,选择与酸反应且生成二氧化碳的物质,则使焙制糕点松软可以添加C,故答案为C;
(5)家用大理石台面变粗糙,与酸发生复分解反应,则家用大理石台面变粗糙的原因之一是滴上了F,故答案为F;
(6)误食假酒会使人中毒或者失明,其有害成分是E,故答案为E.
【点评】本题考查物质的性质及应用,为高频考点,把握性质与用途的关系、化学与生活的关系为解答的关键,侧重分析与应用能力的考查,题目难度不大.
22.(1)C
(2)
(3)Na2SO3+H2SO4(浓)=Na2SO4+SO2↑+H2O
(4) ①试液变红色 酸性
(5) ②褪色 漂白性
(6) 淡黄色沉淀生成 氧化
(7) 紫红色褪色 还原
(8) 吸收SO2;防止SO2污染环境 SO2+2NaOH=Na2SO3+H2O
【解析】(1)
流程中②表示的加工方法是裂解,多碳烃经裂解的到小碳数的烃;
(2)
乙烯加聚得到聚乙烯,聚乙烯的结构简式;
(3)
⑥中为亚硫酸钠和稀硫酸反应生成二氧化硫气体,反应的化学方程式为:Na2SO3+H2SO4(浓)=Na2SO4+SO2↑+H2O。
(4)
①中为紫色石蕊试液,二氧化硫溶于水和水反应生成亚硫酸,SO2 + H2O = H2SO3,亚硫酸为弱酸,可以使紫色石蕊试液变红说明二氧化硫具有酸性;
(5)
②中为品红溶液,二氧化硫与品红化合生成无色物质,能使品红溶液褪色,故二氧化硫具有漂白性;
(6)
③中SO2中+4价S具有氧化性,硫化氢中-2价S具有还原性,二氧化硫能把硫化氢氧化成单质硫,本身被还原成单质硫,反应方程式为SO2 + 2H2S = 3S↓+2H2O,所以③中现象是有淡黄色沉淀生成,SO2具有氧化性;
(7)
④中高锰酸钾溶液具有氧化性,溶液颜色为紫红色,SO2中S为+4价具有还原性,两者发生氧化还原反应,溶液褪色,该反应中二氧化硫为还原剂,具有还原性;
(8)
二氧化硫有毒,不能直接排放到空气中,二氧化硫酸性氧化物能够与氢氧化钠反应生成亚硫酸钠和水,所以可以用氢氧化钠溶液吸收二氧化硫,防止SO2污染环境,反应的化学方程式为:SO2+2NaOH=Na2SO3+H2O。
一、单选题
1.化学与生产、生活密切相关。下列说法错误的是
A.燃煤中加入CaO可以减少温室气体CO2的排放
B.肥皂水可用作蚊虫叮咬处的清洗剂
C.纳米铁粉可以除被污染水体中的重金属离子
D.硅胶可用作袋装食品、瓶装药品等的干燥剂
2.绿色化学的核心是反应过程的绿色化,即要求原料物质中的所有原子完全被利用且全部转入期望的产品中。下列过程不符合绿色化学理念的是
A.
B.甲烷与氯气反应制氯仿:
C.甲烷、CO合成乙酸乙酯:
D.烯烃与水煤气发生羰基合成反应:
3.“垃圾分类就是新时尚”,实行垃圾分类,创造美好生活。下列垃圾不属于厨房垃圾的是
A.蛋壳 B.果皮 C.剩菜 D.漂白粉
4.可用于治疗胃酸过多的物质是
A.碳酸氢钠 B.氯化钠 C.氯化钾 D.氢氧化钠
5.昆明市预计在2020年底前基本建成生活垃圾分类处理系统。下列关于垃圾处理的说法不正确的是
A.废旧塑料瓶可回收利用 B.废旧电池可直接掩埋
C.电子垃圾可用适当的方法回收利用 D.厨余垃圾可经生物技术处理堆肥
6.在给定条件下,下列选项所示的物质间转化均能实现的是
A.
B.
C.
D.
7.下列说法中,正确的是
A.煤和石油都是不可再生的化石能源,其主要组成元素均为碳、氢元素,二者都是混合物
B.煤的干馏和石油的分馏原理相同,都是化学变化
C.煤的液化主要是为了得到苯等重要的有机化工原料
D.煤干馏得到的煤焦油,其主要用途就是再经蒸馏得到高品质燃油
8.最理想的“原子经济”就是反应物中的原子全部转化为欲制得的产物,即原子利用率为100%。下列反应能体现“原子经济”原则的是
A.乙醇与乙酸的酯化反应 B.蔗糖的水解
C.以苯和溴为原料生产溴苯 D.乙烯与水反应生成乙醇
9.下列金属冶炼的反应原理,不正确的是( )
A.2MgCl2(熔融)Mg+Cl2↑ B.Fe2O3+3CO2Fe+3CO2
C.HgSHg+S D.2Al2O3(熔融)4Al+3O2↑
10.废弃的铝制易拉罐应投入的垃圾桶上贴有的垃圾分类标志是
A.有害垃圾
B.可回收物
C.餐厨垃圾
D.其他垃圾
11.下列说法正确的是
A.最重要的人工固氮途径是工业合成氨
B.光束通过硫酸铜溶液时,可观察到丁达尔效应
C.卢瑟福认为原子是坚实的、不可再分的实心球
D.长期服用阿司匹林可预防某些疾病,没有副作用
12.迄今为止,煤、石油和天然气等化石能源仍然是人类使用的主要能源。下列有关煤、石油和天然气的说法中,错误的是
A.石油通过裂化,可以获得碳原子数较少的轻质油 B.煤液化后可以转变为石油
C.天然气是一种清洁的化石燃料 D.石油裂解后可得到短链不饱和烃
13.中国向世界庄严宣布:二氧化碳排放力争在2030年前达到峰值,在2060年前达到碳中和。下列措施不能减少碳排放的是
A.推广“液态阳光”技术,促使CO2加氢转化为液态燃料
B.在汽车排气管里安装催化转化装置
C.倡导低碳生活,注意节约用电
D.利用风能、水能等可再生能源发电替代火力发电
14.下列说法正确的是
A.石墨烯属于有机物 B.蒸发海水就能从海水中获得碘、烧碱和食盐
C.二氧化硅材料广泛用于光纤通讯 D.粗硅制备单晶硅不涉及氧化还原反应
15.利用如图装置做铝热反应实验,下列说法不正确的是
A.该反应的化学方程式是
B.该反应会产生高温、发出强光
C.根据铝热反应的原理,可以冶炼某些高熔点的金属
D.若反应中转移3mol电子,则消耗氧化剂的物质的量是1mol
16.制造焊锡时,把铅加入锡的重要原因是: ( )
A.增加强度 B.增强抗腐蚀能力 C.增加硬度 D.降低熔点
17.下列有关化学用语表示正确的是
A.水分子的比例模型 B.次氯酸的电子式:
C.石油的分馏和煤的气化、液化均为物理变化 D.的结构式:
18.下列化学工艺流程不可行的是( )
A.实验室从海带中提取单质碘取样→灼烧→溶解→过滤→萃取→蒸馏
B.石英砂粗硅粗SiCl4高纯硅
C.FeS2SO2SO3H2SO4
D.铝土矿NaAlO2(aq)Al(OH)3Al2O3Al
二、填空题
19.要使垃圾中宝贵的再生资源得到充分利用,必须对垃圾进行分类,不同地区分类方法不同。如图是一些地区采用的垃圾分类图标。
(1)图C的文字已模糊不清,从图中可以看出它表示的是_______。
A.可回收物 B.可堆肥垃圾 C.可燃垃圾 D.有害垃圾
(2)上述各图中适宜于堆肥处理的垃圾是_______。
(3)图D表示的垃圾若随意丢弃,会造成环境污染,这种污染通常称为_______。该类塑料主要包括_______类、_______类、聚丙烯类等。
(4)图A废电池需要集中处理,主要原因是电池中的_______掺入生活垃圾中进行填埋时,会通过渗滤污染水体和土壤。
20.煤的干馏可分离出煤中含有的煤焦油。( )
21.请根据题意选择下列物质,并用其字母代号填空:
(1)一种红棕色粉末,常用于红色油漆和涂料的是____________
(2)要使浑浊的水变澄清,可使用____;
(3)要中和钢铁厂、电镀厂产生的酸性废水,可使用____;
(4)使焙制糕点松软可以添加____;
(5)家用大理石台面变粗糙的原因之一是滴上了____;
(6)误食假酒会使人中毒或者失明,其有害成分是____.
三、实验题
22.我国资源丰富,合理开发利用资源,才能实现可持续发展。
Ⅰ.以原油为原科生产有机高分子材料聚乙烯、聚丙烯的流程如图:
(1)流程中②表示的加工方法是___(填序号)。
A.分馏 B.聚合 C.裂解 D.干馏
(2)写出聚乙烯的结构简式___。
Ⅱ.如图是实验室制取SO2并验证SO2的某些性质的装置,试回答:
(3)在⑥中发生反应的化学方程式为___。
(4)①中的实验现象为紫色石蕊试液____,此实验证明SO2是____气体。
(5)②中的品红溶液___,证明SO2有____性。
(6)③中的实验现象是___,证明SO2有___性。
(7)④中的实验现象是____,证明SO2有___性。
(8)⑤的作用是___,反应的化学方程式为___。
参考答案:
1.A
【详解】本题考查化学与生活。
详解:加入氧化钙,氧化钙可与煤燃烧生成的二氧化硫在氧气中发生反应生成硫酸钙,减少二氧化硫排放量,但二氧化碳排放量没有减少,A错误;
肥皂水显碱性,与蚊虫叮咬处释放的酸发生中和反应,发生了化学反应,B正确;
纳米铁粉和污染水体中Pb2+、Cu2+、Hg2+发生置换反应生成金属单质而治理污染,C正确;
硅胶疏松具有吸水性,所以可用作实验室和袋装食品、瓶装药品等的干燥剂,D正确。
故选A。
2.B
【详解】根据绿色化学的核心是反应过程的绿色化,即要求原料物质中的所有原子完全被利用且全部转入期望的产品中,加成反应、加聚反应、化合反应都符合绿色化学理念。、、反应物完全转化为期望的产品中;甲烷与氯气反应制氯仿:是取代反应,反应物没有完全转化为期望的产品中,故B符合题意;
综上所述,答案为B。
3.D
【详解】A.蛋壳是鸡蛋壳,属于厨房垃圾,故A不符合题意;
B.果皮属于厨房垃圾,故B不符合题意;
C.剩菜剩饭都属于厨房垃圾,故C不符合题意;
D.漂白粉是工业产品,不属于厨房垃圾,故D符合题意。
综上所述,答案为D。
4.A
【分析】能用于治疗胃酸(含盐酸)过多的物质需具备能与盐酸反应且对人体无害的性质。
【详解】A、碳酸氢钠可与盐酸发生反应生成氯化钠和水以及二氧化碳,可用于治疗胃酸过多,选项A正确;B、NaCl不与盐酸反应,不能用于治疗胃酸过多,选项B错误;C、KCl不与盐酸反应,不能用于治疗胃酸过多,选项C错误;D、氢氧化钠具有极强的腐蚀性,对人体有害,不能用于治疗胃酸过多,选项D错误;答案选A。
【点睛】本题考查了常见物质的实际用途,完成此题,可以依据已有的知识进行。
5.B
【详解】A.废塑料瓶主要由聚乙烯或聚丙烯制造而成,可回收利用,属于可回收物,A选项正确;
B.废旧电池中含有重金属如铅、汞、镉等,将废旧电池直接掩埋会污染土壤、水源,废旧电池应集中回收处理,B选项错误;
C.电子产品含有重金属,任意抛弃会造成地下水污染,要在无污染的条件下进行回收,使之成为有用的资源,C选项正确;
D.厨余垃圾经生化处理转化为沼气和有机肥料,从而产生绿色有机食品和清洁燃料,D选项正确;
答案选B。
6.B
【详解】A.电解熔融的氧化铝制铝而不是氯化铝,A错误;
B.氯化镁与氢氧化钙发生复分解反应生成氢氧化镁,氢氧化镁受热分解生成氧化镁,B正确;
C.铁与氯气反应生成,C错误;
D.电解熔融的制取金属镁,D错误;
故选B。
7.A
【详解】A.煤和石油主要组成元素均为碳、氢元素,二者都是复杂混合物,均属于不可再生化石能源,A正确;
B.煤的干馏是化学变化,而石油分馏是物理变化,B错误;
C.煤的液化是把煤转变为液体燃料的过程,主要是为了得到甲醇等液体燃料、重要的有机化工原料,C错误;
D.煤焦油主要用于分离出苯、甲苯、二甲苯等有机化工原料,D错误;
故选A。
8.D
【详解】A.乙醇与乙酸的酯化反应生成乙酸乙酯和水,不符合原子的利用率为100%要求,故A不选;
B.蔗糖水解生成葡萄糖和果糖,不符合原子的利用率为100%要求,故B不选;
C.苯和溴反应生成溴苯和溴化氢,不符合原子的利用率为100%要求,故C不选;
D.乙烯与水反应生成乙醇是加成反应,原料分子中的原子全部转化成所需要的产物,符合原子的利用率为100%要求,故D符合题意;
故选D。
9.C
【详解】A.金属用电解氯化镁的方法,故正确;
B.铁用热还原法冶炼,故正确;
C.金属汞用氧化汞加热的方法,故错误;
D.电解氧化铝制取金属铝,故正确。
故选C。
10.B
【详解】A、废弃的铝制易拉罐是可回收物,不能投入贴有有害垃圾的垃圾桶,故不选A;
B、废弃的铝制易拉罐是可回收物,应投入贴有可回收物的垃圾桶,故选B;
C、废弃的铝制易拉罐是可回收物,不能投入贴有餐厨垃圾的垃圾桶,故不选C;
D、废弃的铝制易拉罐是可回收物,不能投入贴有其他垃圾的垃圾桶,故不选D。
11.A
【详解】A.工业合成氨是氮气和氢气在高温、高压、催化剂条件下反应生成氨气,属于人工固氮,故A正确;
B.硫酸铜溶液不是胶体,光束通过硫酸铜溶液时,不能观察到丁达尔效应,故B错误;
C.道尔顿认为原子是坚实的、不可再分的实心球,卢瑟福提出核式原子模型,故C错误;
D.长期服用阿司匹林可预防某些心脑血管疾病,有一定的副作用,如胃肠道反应、肝损害、肾损害等,故D错误;
选A。
12.B
【详解】A.石油裂化和裂解的目的是为了将重油中的碳链变短,从而得到生活和工业中需求量较大的产物。裂化的主要目的是为了获得轻质油,故A正确;
B.煤液化后可以转变为甲醇等化工原料,不转变为石油,故B错误;
C.天然气的主要成分为甲烷,充分燃烧后生成物为二氧化碳和水,为清洁的化石燃料,故C正确;
D.石油裂解后可得到短链不饱和烃,如乙烯、丙烯等化工原料,故D正确;
故选B。
13.B
【详解】A.将CO2加氢转化为液态燃料,可减少CO2排放,实现碳中和,选项A不符合题意;
B.汽车排气管中催化转化装置可以将CO与氮氧化物转化为CO2、N2等无污染物质,但不能减少CO2排放,选项B符合题意;
C.低碳生活可减少CO2排放,选项C不符合题意;
D.火力发电过程中产生大量CO2,利用新能源代替火力发电可减少CO2排放,选项D不符合题意;
答案选B。
14.C
【详解】A. 石墨烯是一种由碳原子组成的二维碳纳米材料,它是碳的单质,不属于烯烃,也不属于有机物,故A错误;
B. 蒸发海水就能从海水中获得食盐,但不能获得碘、烧碱,要通过化学方法提取、制备,故B错误;
C. 二氧化硅是制造玻璃、石英玻璃、水玻璃、光导纤维、电子工业的重要部件、光学仪器、工艺品和耐火材料的原料,是科学研究的重要材料,故C正确;
D. 粗硅制备单晶硅涉及Si(粗硅)+2Cl2 SiCl4、2H2+SiCl4Si(单晶硅)+4HCl这两个氧化还原反应,故D错误;
故选C。
15.D
【详解】A.铝热反应为高温下铝与氧化铁发生置换反应生成铁和氧化铝,反应的化学方程式是,故A正确;
B.铝热反应发生时会放出大量的热,产生高温、发出强光,故B正确;
C.铝热反应发生时会放出大量的热,可以冶炼某些高熔点的金属,如Fe、Cr、Mn、W等,故C正确;
D.铝热反应为高温下铝与氧化铁发生置换反应生成铁和氧化铝,反应时氧化铁为氧化剂,若反应中转移3mol电子,消耗氧化铁的物质的量为3mol×=0.5mol,故D错误;
故选D。
16.D
【详解】因合金熔点比成分金属低,硬度比成分金属大,所以制造焊锡时,把铅加入锡的重要原因是降低熔点,
答案选D。
【点睛】合金的熔点低于纯金属。
17.D
【详解】A.水分子的空间构型为V形,比例模型为,故A错误;
B.次氯酸的结构式为Cl—O—H,电子式为,故B错误;
C.煤的气化、液化过程中有新物质生成,属于化学变化,故C错误;
D.氨分子中每个氮原子与3个氢原子各共用一对电子,结构式为,故D正确;
故选D。
18.A
【详解】A.海带中碘是以碘离子形式存在,提取时需要氧化为单质,提取单质碘的工艺为:取样→灼烧→溶解→过滤→氧化→萃取→蒸馏,A错误;
B.碳与二氧化硅反应生成Si和CO,硅与氯气反应生成四氯化硅,最后氢气还原四氯化硅,B正确;
D.FeS2与氧气反应生成二氧化硫、二氧化硫催化氧化生成三氧化硫,三氧化硫与水反应生成硫酸,C正确;
D.氧化铝与NaOH反应生成偏铝酸钠,偏铝酸钠与过量二氧化碳反应生成氢氧化铝,氢氧化铝受热分解生成氧化铝,电解氧化铝生成铝,D正确;
答案选A。
19. D B 白色污染 聚乙烯 聚氯乙烯 铅、镉、银等元素
【详解】(1)图C预示该类垃圾对环境会造成污染,不利于植物的生长,故属于有害垃圾标志,此处选B;
(2)厨余垃圾中残留的有机物,在微生物作用下可分解为小分子水、氨、硝酸等,为植物生长提供肥料,故此处选B;
(3)塑料为有机高分子,在环境中很难降解,容易造成白色污染,故此处填白色污染;该类塑料一般通过加聚反应制得,主要包括聚乙烯类、聚氯乙烯类、聚丙烯类等等;
(4)电池中通常含有重金属元素,如铅蓄电池中的Pb元素,锌锰干电池中的Zn、Mn元素,镍镉电池中的Cd元素,银锌纽扣电池中的Ag元素等,这些重金属元素进入土壤中会污染水体和土壤,故需集中处理,此处填铅、镉、银等元素。
20.错误
【详解】煤经干馏能生产出焦炭、煤焦油、粗氨水和焦炉气等,故错误。
21. B A D C F E
【详解】解:(1)只有Fe2O3为红棕色,则常用于红色油漆和涂料的是B,故答案为B;
(2)只有明矾可水解生成胶体,用于水的净化,故答案为A;
(3)中和钢铁厂、电镀厂产生的酸性废水,选择碱,且便宜易得,则选择D,故答案为D;
(4)使焙制糕点松软可以添加,选择与酸反应且生成二氧化碳的物质,则使焙制糕点松软可以添加C,故答案为C;
(5)家用大理石台面变粗糙,与酸发生复分解反应,则家用大理石台面变粗糙的原因之一是滴上了F,故答案为F;
(6)误食假酒会使人中毒或者失明,其有害成分是E,故答案为E.
【点评】本题考查物质的性质及应用,为高频考点,把握性质与用途的关系、化学与生活的关系为解答的关键,侧重分析与应用能力的考查,题目难度不大.
22.(1)C
(2)
(3)Na2SO3+H2SO4(浓)=Na2SO4+SO2↑+H2O
(4) ①试液变红色 酸性
(5) ②褪色 漂白性
(6) 淡黄色沉淀生成 氧化
(7) 紫红色褪色 还原
(8) 吸收SO2;防止SO2污染环境 SO2+2NaOH=Na2SO3+H2O
【解析】(1)
流程中②表示的加工方法是裂解,多碳烃经裂解的到小碳数的烃;
(2)
乙烯加聚得到聚乙烯,聚乙烯的结构简式;
(3)
⑥中为亚硫酸钠和稀硫酸反应生成二氧化硫气体,反应的化学方程式为:Na2SO3+H2SO4(浓)=Na2SO4+SO2↑+H2O。
(4)
①中为紫色石蕊试液,二氧化硫溶于水和水反应生成亚硫酸,SO2 + H2O = H2SO3,亚硫酸为弱酸,可以使紫色石蕊试液变红说明二氧化硫具有酸性;
(5)
②中为品红溶液,二氧化硫与品红化合生成无色物质,能使品红溶液褪色,故二氧化硫具有漂白性;
(6)
③中SO2中+4价S具有氧化性,硫化氢中-2价S具有还原性,二氧化硫能把硫化氢氧化成单质硫,本身被还原成单质硫,反应方程式为SO2 + 2H2S = 3S↓+2H2O,所以③中现象是有淡黄色沉淀生成,SO2具有氧化性;
(7)
④中高锰酸钾溶液具有氧化性,溶液颜色为紫红色,SO2中S为+4价具有还原性,两者发生氧化还原反应,溶液褪色,该反应中二氧化硫为还原剂,具有还原性;
(8)
二氧化硫有毒,不能直接排放到空气中,二氧化硫酸性氧化物能够与氢氧化钠反应生成亚硫酸钠和水,所以可以用氢氧化钠溶液吸收二氧化硫,防止SO2污染环境,反应的化学方程式为:SO2+2NaOH=Na2SO3+H2O。
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
