2023年6月广东省肇庆市普通高中学业水平合格性考试高一化学模拟3(含答案)
文档属性
| 名称 | 2023年6月广东省肇庆市普通高中学业水平合格性考试高一化学模拟3(含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 547.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-06-20 00:00:00 | ||
图片预览


文档简介
2023年6月广东省肇庆市普通高中学业水平合格性考试高一化学模拟(三)
一、单项选题:本大题共35小题,每小题2分,共70分。在每小题列出的四个选项中,只有一个选项符合题目要求。
1. 材料改善生活。下列物体的主要材质属于无机非金属材料的是
A. C919使用的轮胎 B. 塑料水桶
C. 高铁钢轨 D. 陶瓷碗
2. 我国劳动人民很早就掌握了酿酒技术,为美好生活创造了喜庆气氛,“诗酒趁年华”。酒中含有乙醇,乙醇的结构简式为
A. CH3CH3 B. CH3COOH
C. CH2=CH2 D. CH3CH2OH
3. 傍晚,无数光柱透过云层,将天空映照得非常美丽。该光柱
A. 源于丁达尔效应 B. 证明空气是纯净物
C. 由O2无规则运动引起 D. 由N2的“惰性”引起
4. 磷酸盐氧同位素技术在土壤磷循环中有重要应用。关于的说法正确的是
A. 中子数为8 B. 与O互为同位素
C. 质量数为16 D. 核外电子数为10
5. 自然界的氮循环为生物体提供氮元素。氮原子的电子式为
A. N B. C. D.
6. 2022年10月,长征五号B运载火箭成功将“梦天”实验舱送入预定轨道。该火箭用到大量铝合金材料,下列性质与铝合金材料的航天应用无关的是
A. 低密度 B. 耐酸蚀 C. 耐磨损 D. 强韧性
7.为了除去SO2中少量的HCl气体,应将混合气体通入( )
A.NaHSO3饱和溶液 B.溴水 C.NaOH溶液 D.NaHCO3饱和溶液
8. 二十大报告提出:“积极稳妥推进碳达峰碳中和。”下列做法不利于实现“碳达峰碳中和”目标的是
A. 居民取暖和工厂生产大量使用脱硫的燃煤
B. 提高新能源汽车在城市公共交通中的使用比例
C. 利用化学方法将CO2转化为用途广泛的化工原料
D. 加快风能、太阳能、生物质能等可再生能源的发展和利用
9. 科学使用消毒液是阻断病毒传播的有效方式之一、下列关于“84”消毒液(有效成分是NaClO)的说法,错误的是
A. 应在阴凉处密闭保存 B. 能杀菌消毒,利用的是HClO的强氧化性
C. 最好与浓盐酸混合使用 D. 制备原理为Cl2+2NaOH=NaClO+NaCl+H2O
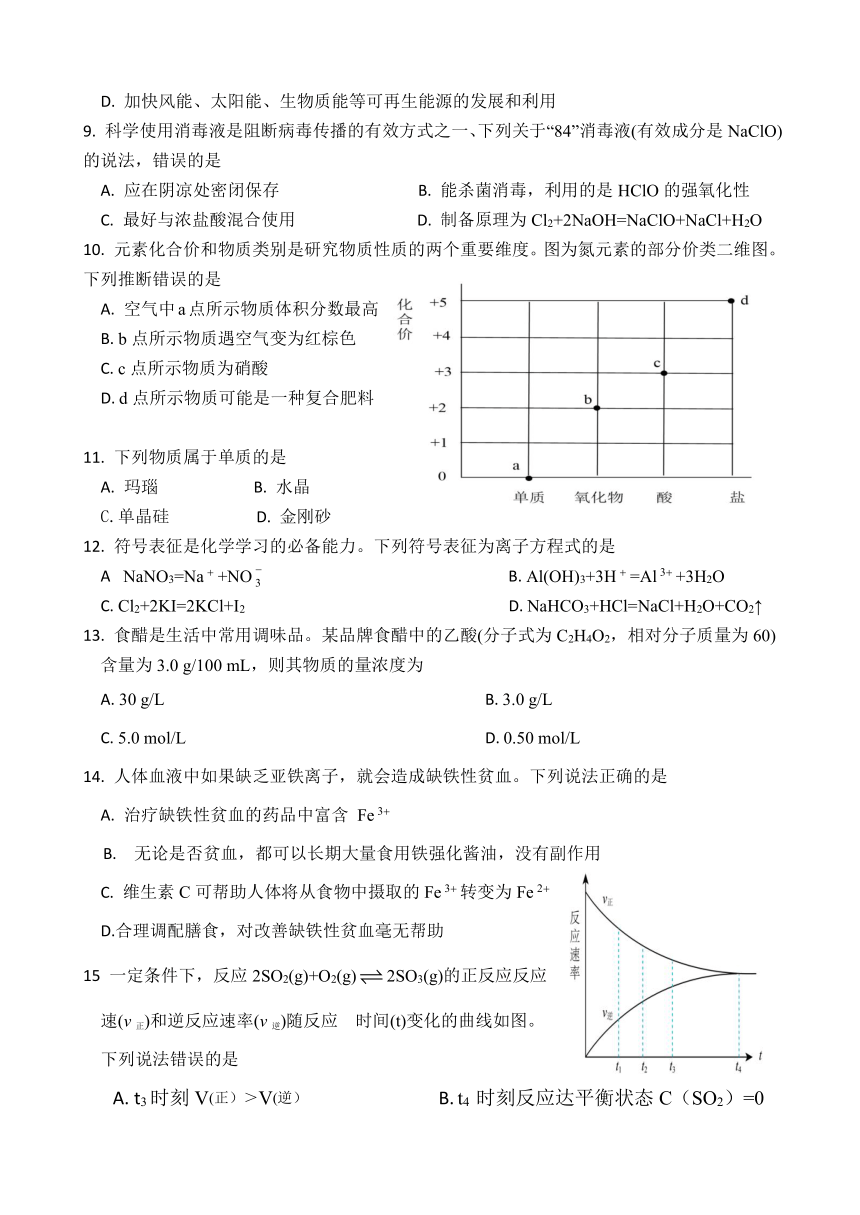
10. 元素化合价和物质类别是研究物质性质的两个重要维度。图为氮元素的部分价类二维图。下列推断错误的是
A. 空气中a点所示物质体积分数最高
B. b点所示物质遇空气变为红棕色
C. c点所示物质为硝酸
D. d点所示物质可能是一种复合肥料
11. 下列物质属于单质的是
A. 玛瑙 B. 水晶
C.单晶硅 D. 金刚砂
12. 符号表征是化学学习的必备能力。下列符号表征为离子方程式的是
A NaNO3=Na+NO B. Al(OH)3+3H=Al+3H2O
C. Cl2+2KI=2KCl+I2 D. NaHCO3+HCl=NaCl+H2O+CO2↑
13. 食醋是生活中常用调味品。某品牌食醋中的乙酸(分子式为C2H4O2,相对分子质量为60)含量为3.0 g/100 mL,则其物质的量浓度为
A. 30 g/L B. 3.0 g/L
C. 5.0 mol/L D. 0.50 mol/L
14. 人体血液中如果缺乏亚铁离子,就会造成缺铁性贫血。下列说法正确的是
A. 治疗缺铁性贫血的药品中富含 Fe
B. 无论是否贫血,都可以长期大量食用铁强化酱油,没有副作用
C. 维生素C可帮助人体将从食物中摄取的Fe转变为Fe
D.合理调配膳食,对改善缺铁性贫血毫无帮助
15 一定条件下,反应2SO2(g)+O2(g)2SO3(g)的正反应反应
速(v正)和逆反应速率(v逆)随反应 时间(t)变化的曲线如图。
下列说法错误的是
A. t3时刻V(正)>V(逆) B. t4 时刻反应达平衡状态C(SO2)=0
C. . t4 后各物质的质量保持不变 D.. t4 后反应没有停止,是动态平衡
16.. 在化工生产中,调控反应条件很重要。下列能提高合成氨反应速率的是
A. 使用空气做反应物 B. 减小c(H2)
C. 使用合适的催化剂 D. 降低温度
17. 下列方法中,通过调控温度改变反应速率而减缓食物腐败变质的是
A. 用冰箱冷藏酸奶 B. 在葡萄酒酿制过程中使用SO2
C. 大米抽真空包装 D. 制作香肠时加入适量亚硝酸钠
18. 一种新型高效净水剂[AlFe(OH)nCl6-n]m属于无机高分子化合物,可应用于生活和工业用水的处理。其中,铁元素的化合价为
A. +2 B. +3 C +4 D. +6
19. 小明利用家庭用品进行如图所示的导电性实验。用自来水配制约0.2 mol/L的下列物质的溶液,实验时灯泡亮度最弱的是
A. 白醋 B. 食盐 C. 蔗糖 D. 小苏打
20. 下列反应既属于化合反应,又属于氧化还原反应的是
A. Cl2+H2O=HCl+HClO B. 2Na2O2+2H2O=4NaOH+O2↑
C. 3NO2+H2O=2HNO3+NO D. 4Fe(OH)2+O2+2H2O=4Fe(OH)3
21. 丁烷(C4H10)裂解可得到乙烯和乙烷。下列说法正确的是
A. 乙烯与乙烷互为同系物 B. 乙烯与乙烷互为同分异构体
C. 丁烷有2种同分异构体 D. C4H9Cl与CH3Cl互为同素异形体
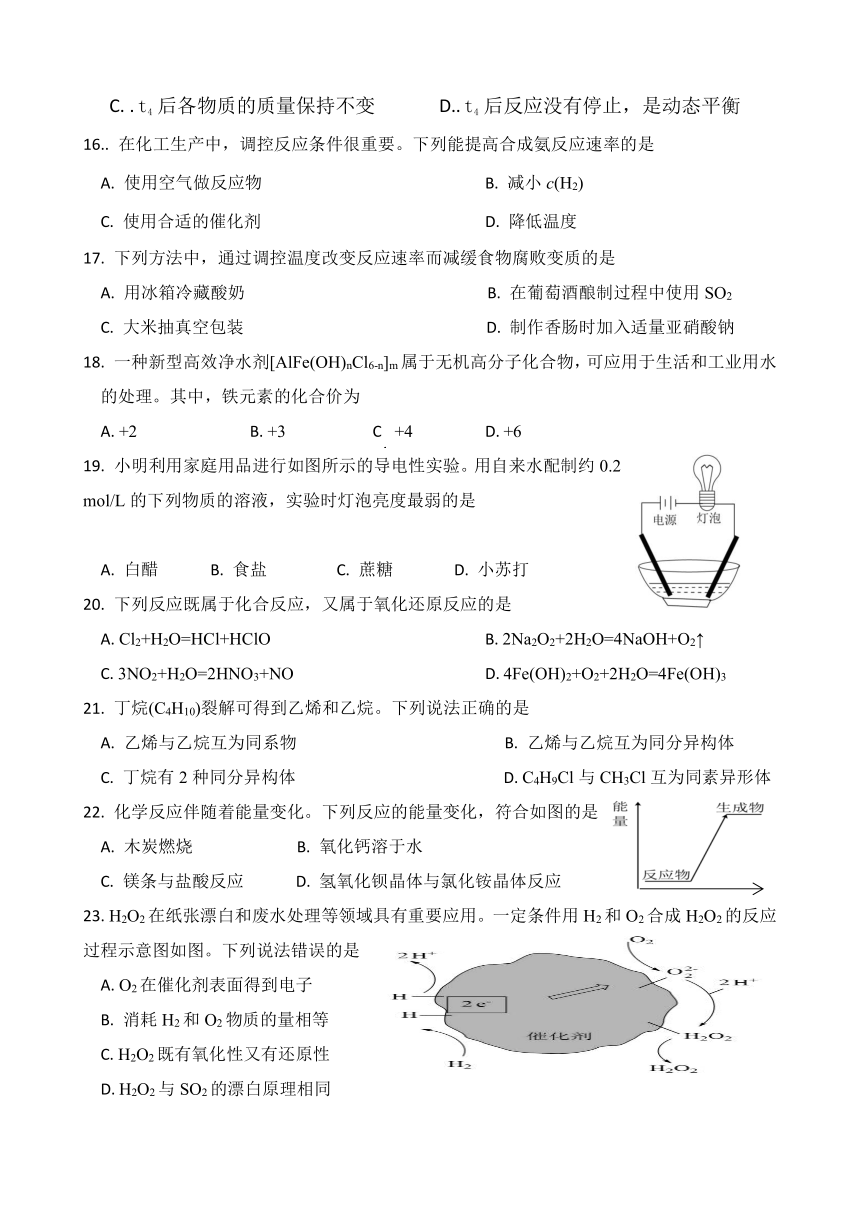
22. 化学反应伴随着能量变化。下列反应的能量变化,符合如图的是
A. 木炭燃烧 B. 氧化钙溶于水
C. 镁条与盐酸反应 D. 氢氧化钡晶体与氯化铵晶体反应
23. H2O2在纸张漂白和废水处理等领域具有重要应用。一定条件用H2和O2合成H2O2的反应过程示意图如图。下列说法错误的是
A. O2在催化剂表面得到电子
B. 消耗H2和O2物质的量相等
C. H2O2既有氧化性又有还原性
D. H2O2与SO2的漂白原理相同
24. 下列实验室突发事件的应对措施,错误的是
A. 割伤后,用药棉将伤口清理干净,然后用1%硼酸消毒
B. 溅出的少量酒精着火时,用湿布或灭火毯覆盖火源以灭火
C. 轻微烫伤后,先用洁净的冷水处理,降低局部温度,然后涂上烫伤药膏
D. 酸沾到皮肤上,应立即用大量水冲洗,然后用3%~5% NaHCO3溶液冲洗
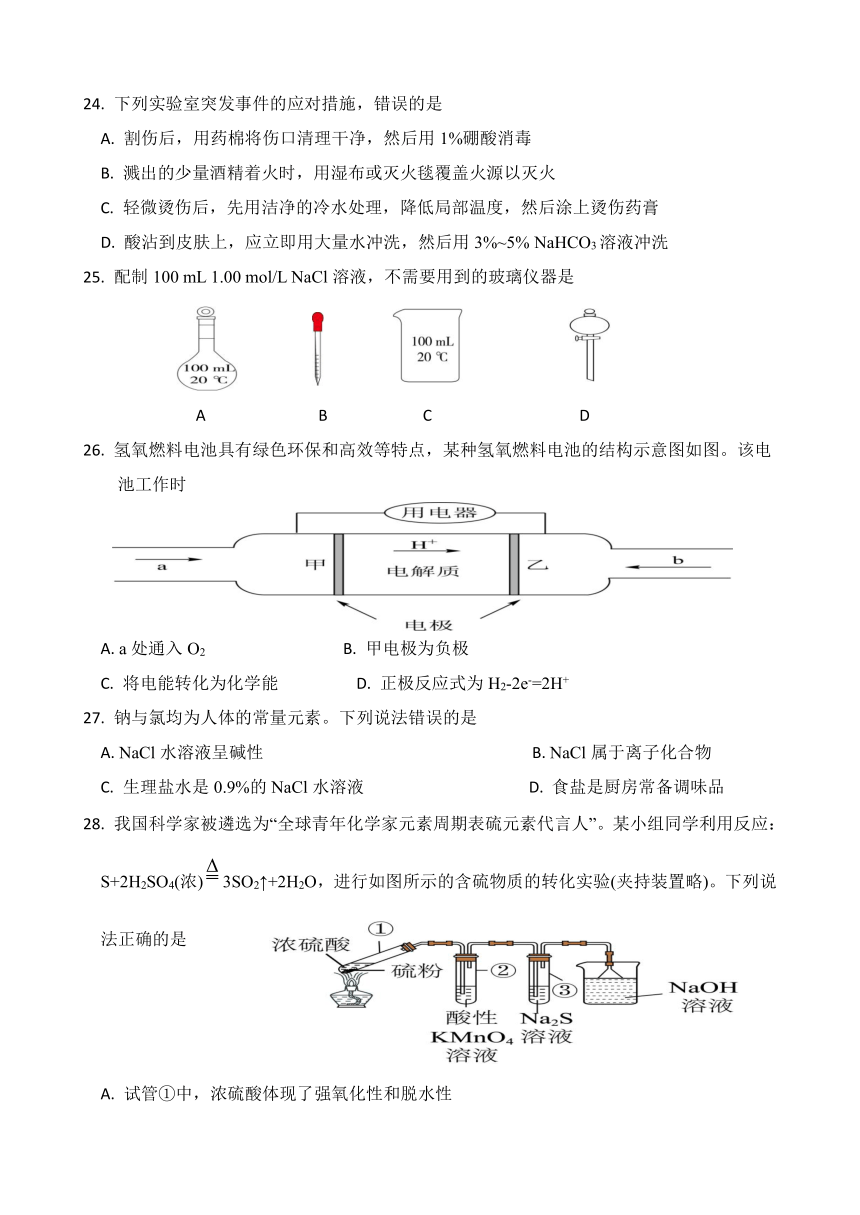
25. 配制100 mL 1.00 mol/L NaCl溶液,不需要用到的玻璃仪器是
A B C D
26. 氢氧燃料电池具有绿色环保和高效等特点,某种氢氧燃料电池的结构示意图如图。该电池工作时
A. a处通入O2 B. 甲电极为负极
C. 将电能转化为化学能 D. 正极反应式为H2-2e-=2H+
27. 钠与氯均为人体的常量元素。下列说法错误的是
A. NaCl水溶液呈碱性 B. NaCl属于离子化合物
C. 生理盐水是0.9%的NaCl水溶液 D. 食盐是厨房常备调味品
28. 我国科学家被遴选为“全球青年化学家元素周期表硫元素代言人”。某小组同学利用反应:S+2H2SO4(浓)3SO2↑+2H2O,进行如图所示的含硫物质的转化实验(夹持装置略)。下列说法正确的是
A. 试管①中,浓硫酸体现了强氧化性和脱水性
B. 试管②中,溶液褪色,体现+4价硫元素的氧化性
C. 试管③中,有淡黄色沉淀出现,体现-2价硫元素的还原性
D. 烧杯中的反应为SO3+2NaOH=Na2SO4+H2O
29. 化学与生活息息相关。对下列做法或现象的解释,错误的是
选项 做法或现象 解释
A 节日燃放的烟花五彩缤纷 钠元素的焰色为绿色
B 硝酸铵化肥安全改性处理后施用 硝酸铵受热或撞击易爆
C 食盐中添加碘酸钾 碘酸钾属于营养强化剂
D 铝制餐具不宜长时间存放碱性食物 碱性物质能腐蚀铝制品
30. 实验室中因保存不当,NH4Cl和Na2CO3两个试剂瓶的标签被污损,只能辨认出标签上的字母N。下列试剂不能区分NH4Cl和Na2CO3的是
A. 稀硝酸 B. NaCl溶液
C. NaOH溶液 D. BaCl2溶液
31. 春秋初年我国已掌握了冶铁技术,其部分原理是Fe2O3+3CO2Fe+3CO2。下列有关说法正确的是
A. 该反应是置换反应 B. Fe2O3可用作外墙涂料和油漆
C. Fe在Cl2中燃烧生成FeCl2 D. Fe2O3常温下能与水反应生成Fe(OH)3
32. 1 mol下列物质在O2中完全燃烧,生成水的质量最小的是
A. C2H2 B. C2H4 C. C2H6 D. CH3COOCH2CH3
33. 下列关于乙烯与Br2发生加成反应的说法,正确的是
A. 乙烯中含有离子键 B. Br2是共价化合物
C. 反应中有非极性键断裂 D. 产物中只含有极性键
34. 一种“金相”腐蚀剂含有浓度较高的Fe3+和H+,其中还可能大量存在的阴离子是
A. OH B. CO C. Na+ D. Cl
35. 下列关于煤和石油综合利用的说法,错误的是
A. 煤的干馏是物理变化 B. 水煤气可催化转化为甲醇
C. 利用组分沸点差异进行石油分馏 D. 石化产品可为医药行业提供原料
二、不定项选择题:本大题共15小题,每小题2分,共30分。在每小题列出的四个选项中,至少有一个选项符合题目要求,少选且正确给1分,未选、多选、错选均不给分。
36、(1)已知A、B、C、D为气体,E、F为固体,G是氯化钙,它们之间的转化关系如图所示:
①对以上各物质说法正确的是
A物质可能是H2 B.C物质是HCl C.F物质是熟石灰 D.H物质是水
②此流程中涉及到的化学方程式正确的是
A.H2+Cl22HCl B.2NH4Cl+Ca(OH)2CaCl2+2NH3↑+2H2O
C.NH4Cl + NaOH NaCl + NH3↑+H2O D.MnO2 + 4HCl(浓) MnCl2 +Cl2 +H2O
③下列说法错误的是
A.检验D气体的方法是:使湿润的红色石蕊试纸变蓝 B.C和D相遇有白烟生成
C.D可以做制冷剂,干燥D用碱石灰 D.E中只有离子键
(2)某教师在课堂上用下图所示的装置来验证浓硫酸与铜是否发生反应并探讨反应所产生气体的性质。Cu + 2H2SO4(浓) CuSO4 +SO2↑ + 2H2O
④对于乙装置,说法正确的是
A.SO2气体具有还原性,使品红溶液褪色,SO2气体可以做食品添加剂
B.SO2气体具有漂白性,使品红溶液褪色
C.若气体使品红溶液褪色,加热后又恢复红色,说明是SO2气体
D.试管口浸有碱液的棉花可吸收多余的SO2气体,因为SO2气体有毒
⑤若要收集试管甲中生成的SO2气体,可以采用收集方法是
A排水法 B 向上排空气法 C 向下排空气法 D,排NaOH溶液
37、下图是元素周期表的一部分,针对表中①~⑦元素,填写下列空白:
族 周期 IA 0
1 ⑧ IIA IIIA IVA VA VIA VIIA ⑨
2 ① ② ③
3 ④ ⑤ ⑥ ⑦
(1)对⑧⑨元素说法正确的是
A.⑧单质通常是双原子分子,⑨单质是单原子分子 B. 3H质量数是3,中子数是1
C. ⑧属于ⅠA主族元素,是碱金属 D. .⑧单质是最轻的气体,有三种同位素
(2)被选作相对原子质量标准的核素是
A. B. C. D.
(3)下列比较正确的是
A.②和⑥两种元素的原子半径大小为:② < ⑥
B. ④和⑤两种元素的金属性强弱顺序为:④ > ⑤
C. ②③⑦的氢化物稳定性比较:② < ③ ③>⑦
D. 最高价氧化物的水化物碱性比较:④>⑤
(4)下列说法正确的是
A.元素④与⑦形成的化合物只含离子键,属于离子化合物。
B.⑤的单质,最高价氧化物,最高价氧化物的水化物都能和盐酸反应,也能和NaOH溶液反应
C. ③的氢化物水溶液是弱酸,不能刻蚀玻璃
D. ②的氢化物不能制取化肥,但可以做制冷剂
(5)对各种元素的实验室制法或工业制法错误的是
A. ④单质的制法是电解熔融的氯化物 B. ⑤单质的制法是电解熔融的氧化物
C. ⑧ 单质的制法:可用Zn与盐酸反应 D. ⑦单质可用MnO2与稀盐酸加热制取
38.(13分)乙烯是石油裂解气的主要成分,它的产量通常用来衡量一个国家的石油化工发展水平。请回答下列问题。
(1)对乙烯的说法不正确的是
A 乙烯属于不饱和烃,平面结构。可做果实催熟剂
B乙烯可与Br2水发生加成反应使其褪色,
C.乙烯使酸性高锰酸钾褪色发生的是氧化还原反应
D.乙烯发生加聚反应生成高分子聚乙烯,聚乙烯有固定的熔沸点
(2)对乙烯的描述正确的是 A.结构简式: B球棍模型
C. 电子式: D.结构式:
(3)鉴别甲烷和乙烯可用的试剂是
A.稀硫酸 B.溴的四氯化碳溶液 C.水 D.酸性高锰酸钾溶液
(4)已知2 CH3CHO + O22 CH3COOH。若以乙烯为主要原料合成乙酸,其合成路 线如图所示。
乙烯 A B 乙酸
有关方程式正确的是
A.①方程式是:
B.②方程式是:
C.④方程式是:
D.⑤方程式是:
(5)流程中的反应类型错误的是
A. ①是加成反应 B. ⑤是酯化反应,就是取代反应
C. ②③是还原反应,有机物做氧化剂 D. ④是加聚反应
2023年6月广东省肇庆市普通高中学业水平合格性考试高一化学模拟(三)
答题栏
姓名 班级 成绩
一、单项选择题
题号 1 2 3 4 5 6 7 8 9 10 11 12
答案
题号 13 14 15 16 17 18 19 20 21 22 23 24
答案
题号 25 26 27 28 29 30 31 32 33 34 35
答案
二、不定项选择题
题号36 ① ② ③ ④ ⑤
答案
题号37 (1) (2) (3) (4) (5)
答案
题号38 (1) (2) (3) (4) (5)
答案
2023年6月广东省肇庆市普通高中学业水平合格性考试高一化学模拟(三)答案
一、单项选择题
题号 1 2 3 4 5 6 7 8 9 10 11 12
答案 D D A B C B A A C C C B
题号 13 14 15 16 17 18 19 20 21 22 23 24
答案 D C B C A B A D C D D D
题号 25 26 27 28 29 30 31 32 33 34 35
答案 D B A C A B B A C D A
二、不定项选择题
题号36 ① ② ③ ④ ⑤
答案 ABCD AB D BCD B
题号37 (1) (2) (3) (4) (5)
答案 AD B ABCD AB D
题号38 (1) (2) (3) (4) (5)
答案 D ABCD BD ABCD C
一、单项选题:本大题共35小题,每小题2分,共70分。在每小题列出的四个选项中,只有一个选项符合题目要求。
1. 材料改善生活。下列物体的主要材质属于无机非金属材料的是
A. C919使用的轮胎 B. 塑料水桶
C. 高铁钢轨 D. 陶瓷碗
2. 我国劳动人民很早就掌握了酿酒技术,为美好生活创造了喜庆气氛,“诗酒趁年华”。酒中含有乙醇,乙醇的结构简式为
A. CH3CH3 B. CH3COOH
C. CH2=CH2 D. CH3CH2OH
3. 傍晚,无数光柱透过云层,将天空映照得非常美丽。该光柱
A. 源于丁达尔效应 B. 证明空气是纯净物
C. 由O2无规则运动引起 D. 由N2的“惰性”引起
4. 磷酸盐氧同位素技术在土壤磷循环中有重要应用。关于的说法正确的是
A. 中子数为8 B. 与O互为同位素
C. 质量数为16 D. 核外电子数为10
5. 自然界的氮循环为生物体提供氮元素。氮原子的电子式为
A. N B. C. D.
6. 2022年10月,长征五号B运载火箭成功将“梦天”实验舱送入预定轨道。该火箭用到大量铝合金材料,下列性质与铝合金材料的航天应用无关的是
A. 低密度 B. 耐酸蚀 C. 耐磨损 D. 强韧性
7.为了除去SO2中少量的HCl气体,应将混合气体通入( )
A.NaHSO3饱和溶液 B.溴水 C.NaOH溶液 D.NaHCO3饱和溶液
8. 二十大报告提出:“积极稳妥推进碳达峰碳中和。”下列做法不利于实现“碳达峰碳中和”目标的是
A. 居民取暖和工厂生产大量使用脱硫的燃煤
B. 提高新能源汽车在城市公共交通中的使用比例
C. 利用化学方法将CO2转化为用途广泛的化工原料
D. 加快风能、太阳能、生物质能等可再生能源的发展和利用
9. 科学使用消毒液是阻断病毒传播的有效方式之一、下列关于“84”消毒液(有效成分是NaClO)的说法,错误的是
A. 应在阴凉处密闭保存 B. 能杀菌消毒,利用的是HClO的强氧化性
C. 最好与浓盐酸混合使用 D. 制备原理为Cl2+2NaOH=NaClO+NaCl+H2O
10. 元素化合价和物质类别是研究物质性质的两个重要维度。图为氮元素的部分价类二维图。下列推断错误的是
A. 空气中a点所示物质体积分数最高
B. b点所示物质遇空气变为红棕色
C. c点所示物质为硝酸
D. d点所示物质可能是一种复合肥料
11. 下列物质属于单质的是
A. 玛瑙 B. 水晶
C.单晶硅 D. 金刚砂
12. 符号表征是化学学习的必备能力。下列符号表征为离子方程式的是
A NaNO3=Na+NO B. Al(OH)3+3H=Al+3H2O
C. Cl2+2KI=2KCl+I2 D. NaHCO3+HCl=NaCl+H2O+CO2↑
13. 食醋是生活中常用调味品。某品牌食醋中的乙酸(分子式为C2H4O2,相对分子质量为60)含量为3.0 g/100 mL,则其物质的量浓度为
A. 30 g/L B. 3.0 g/L
C. 5.0 mol/L D. 0.50 mol/L
14. 人体血液中如果缺乏亚铁离子,就会造成缺铁性贫血。下列说法正确的是
A. 治疗缺铁性贫血的药品中富含 Fe
B. 无论是否贫血,都可以长期大量食用铁强化酱油,没有副作用
C. 维生素C可帮助人体将从食物中摄取的Fe转变为Fe
D.合理调配膳食,对改善缺铁性贫血毫无帮助
15 一定条件下,反应2SO2(g)+O2(g)2SO3(g)的正反应反应
速(v正)和逆反应速率(v逆)随反应 时间(t)变化的曲线如图。
下列说法错误的是
A. t3时刻V(正)>V(逆) B. t4 时刻反应达平衡状态C(SO2)=0
C. . t4 后各物质的质量保持不变 D.. t4 后反应没有停止,是动态平衡
16.. 在化工生产中,调控反应条件很重要。下列能提高合成氨反应速率的是
A. 使用空气做反应物 B. 减小c(H2)
C. 使用合适的催化剂 D. 降低温度
17. 下列方法中,通过调控温度改变反应速率而减缓食物腐败变质的是
A. 用冰箱冷藏酸奶 B. 在葡萄酒酿制过程中使用SO2
C. 大米抽真空包装 D. 制作香肠时加入适量亚硝酸钠
18. 一种新型高效净水剂[AlFe(OH)nCl6-n]m属于无机高分子化合物,可应用于生活和工业用水的处理。其中,铁元素的化合价为
A. +2 B. +3 C +4 D. +6
19. 小明利用家庭用品进行如图所示的导电性实验。用自来水配制约0.2 mol/L的下列物质的溶液,实验时灯泡亮度最弱的是
A. 白醋 B. 食盐 C. 蔗糖 D. 小苏打
20. 下列反应既属于化合反应,又属于氧化还原反应的是
A. Cl2+H2O=HCl+HClO B. 2Na2O2+2H2O=4NaOH+O2↑
C. 3NO2+H2O=2HNO3+NO D. 4Fe(OH)2+O2+2H2O=4Fe(OH)3
21. 丁烷(C4H10)裂解可得到乙烯和乙烷。下列说法正确的是
A. 乙烯与乙烷互为同系物 B. 乙烯与乙烷互为同分异构体
C. 丁烷有2种同分异构体 D. C4H9Cl与CH3Cl互为同素异形体
22. 化学反应伴随着能量变化。下列反应的能量变化,符合如图的是
A. 木炭燃烧 B. 氧化钙溶于水
C. 镁条与盐酸反应 D. 氢氧化钡晶体与氯化铵晶体反应
23. H2O2在纸张漂白和废水处理等领域具有重要应用。一定条件用H2和O2合成H2O2的反应过程示意图如图。下列说法错误的是
A. O2在催化剂表面得到电子
B. 消耗H2和O2物质的量相等
C. H2O2既有氧化性又有还原性
D. H2O2与SO2的漂白原理相同
24. 下列实验室突发事件的应对措施,错误的是
A. 割伤后,用药棉将伤口清理干净,然后用1%硼酸消毒
B. 溅出的少量酒精着火时,用湿布或灭火毯覆盖火源以灭火
C. 轻微烫伤后,先用洁净的冷水处理,降低局部温度,然后涂上烫伤药膏
D. 酸沾到皮肤上,应立即用大量水冲洗,然后用3%~5% NaHCO3溶液冲洗
25. 配制100 mL 1.00 mol/L NaCl溶液,不需要用到的玻璃仪器是
A B C D
26. 氢氧燃料电池具有绿色环保和高效等特点,某种氢氧燃料电池的结构示意图如图。该电池工作时
A. a处通入O2 B. 甲电极为负极
C. 将电能转化为化学能 D. 正极反应式为H2-2e-=2H+
27. 钠与氯均为人体的常量元素。下列说法错误的是
A. NaCl水溶液呈碱性 B. NaCl属于离子化合物
C. 生理盐水是0.9%的NaCl水溶液 D. 食盐是厨房常备调味品
28. 我国科学家被遴选为“全球青年化学家元素周期表硫元素代言人”。某小组同学利用反应:S+2H2SO4(浓)3SO2↑+2H2O,进行如图所示的含硫物质的转化实验(夹持装置略)。下列说法正确的是
A. 试管①中,浓硫酸体现了强氧化性和脱水性
B. 试管②中,溶液褪色,体现+4价硫元素的氧化性
C. 试管③中,有淡黄色沉淀出现,体现-2价硫元素的还原性
D. 烧杯中的反应为SO3+2NaOH=Na2SO4+H2O
29. 化学与生活息息相关。对下列做法或现象的解释,错误的是
选项 做法或现象 解释
A 节日燃放的烟花五彩缤纷 钠元素的焰色为绿色
B 硝酸铵化肥安全改性处理后施用 硝酸铵受热或撞击易爆
C 食盐中添加碘酸钾 碘酸钾属于营养强化剂
D 铝制餐具不宜长时间存放碱性食物 碱性物质能腐蚀铝制品
30. 实验室中因保存不当,NH4Cl和Na2CO3两个试剂瓶的标签被污损,只能辨认出标签上的字母N。下列试剂不能区分NH4Cl和Na2CO3的是
A. 稀硝酸 B. NaCl溶液
C. NaOH溶液 D. BaCl2溶液
31. 春秋初年我国已掌握了冶铁技术,其部分原理是Fe2O3+3CO2Fe+3CO2。下列有关说法正确的是
A. 该反应是置换反应 B. Fe2O3可用作外墙涂料和油漆
C. Fe在Cl2中燃烧生成FeCl2 D. Fe2O3常温下能与水反应生成Fe(OH)3
32. 1 mol下列物质在O2中完全燃烧,生成水的质量最小的是
A. C2H2 B. C2H4 C. C2H6 D. CH3COOCH2CH3
33. 下列关于乙烯与Br2发生加成反应的说法,正确的是
A. 乙烯中含有离子键 B. Br2是共价化合物
C. 反应中有非极性键断裂 D. 产物中只含有极性键
34. 一种“金相”腐蚀剂含有浓度较高的Fe3+和H+,其中还可能大量存在的阴离子是
A. OH B. CO C. Na+ D. Cl
35. 下列关于煤和石油综合利用的说法,错误的是
A. 煤的干馏是物理变化 B. 水煤气可催化转化为甲醇
C. 利用组分沸点差异进行石油分馏 D. 石化产品可为医药行业提供原料
二、不定项选择题:本大题共15小题,每小题2分,共30分。在每小题列出的四个选项中,至少有一个选项符合题目要求,少选且正确给1分,未选、多选、错选均不给分。
36、(1)已知A、B、C、D为气体,E、F为固体,G是氯化钙,它们之间的转化关系如图所示:
①对以上各物质说法正确的是
A物质可能是H2 B.C物质是HCl C.F物质是熟石灰 D.H物质是水
②此流程中涉及到的化学方程式正确的是
A.H2+Cl22HCl B.2NH4Cl+Ca(OH)2CaCl2+2NH3↑+2H2O
C.NH4Cl + NaOH NaCl + NH3↑+H2O D.MnO2 + 4HCl(浓) MnCl2 +Cl2 +H2O
③下列说法错误的是
A.检验D气体的方法是:使湿润的红色石蕊试纸变蓝 B.C和D相遇有白烟生成
C.D可以做制冷剂,干燥D用碱石灰 D.E中只有离子键
(2)某教师在课堂上用下图所示的装置来验证浓硫酸与铜是否发生反应并探讨反应所产生气体的性质。Cu + 2H2SO4(浓) CuSO4 +SO2↑ + 2H2O
④对于乙装置,说法正确的是
A.SO2气体具有还原性,使品红溶液褪色,SO2气体可以做食品添加剂
B.SO2气体具有漂白性,使品红溶液褪色
C.若气体使品红溶液褪色,加热后又恢复红色,说明是SO2气体
D.试管口浸有碱液的棉花可吸收多余的SO2气体,因为SO2气体有毒
⑤若要收集试管甲中生成的SO2气体,可以采用收集方法是
A排水法 B 向上排空气法 C 向下排空气法 D,排NaOH溶液
37、下图是元素周期表的一部分,针对表中①~⑦元素,填写下列空白:
族 周期 IA 0
1 ⑧ IIA IIIA IVA VA VIA VIIA ⑨
2 ① ② ③
3 ④ ⑤ ⑥ ⑦
(1)对⑧⑨元素说法正确的是
A.⑧单质通常是双原子分子,⑨单质是单原子分子 B. 3H质量数是3,中子数是1
C. ⑧属于ⅠA主族元素,是碱金属 D. .⑧单质是最轻的气体,有三种同位素
(2)被选作相对原子质量标准的核素是
A. B. C. D.
(3)下列比较正确的是
A.②和⑥两种元素的原子半径大小为:② < ⑥
B. ④和⑤两种元素的金属性强弱顺序为:④ > ⑤
C. ②③⑦的氢化物稳定性比较:② < ③ ③>⑦
D. 最高价氧化物的水化物碱性比较:④>⑤
(4)下列说法正确的是
A.元素④与⑦形成的化合物只含离子键,属于离子化合物。
B.⑤的单质,最高价氧化物,最高价氧化物的水化物都能和盐酸反应,也能和NaOH溶液反应
C. ③的氢化物水溶液是弱酸,不能刻蚀玻璃
D. ②的氢化物不能制取化肥,但可以做制冷剂
(5)对各种元素的实验室制法或工业制法错误的是
A. ④单质的制法是电解熔融的氯化物 B. ⑤单质的制法是电解熔融的氧化物
C. ⑧ 单质的制法:可用Zn与盐酸反应 D. ⑦单质可用MnO2与稀盐酸加热制取
38.(13分)乙烯是石油裂解气的主要成分,它的产量通常用来衡量一个国家的石油化工发展水平。请回答下列问题。
(1)对乙烯的说法不正确的是
A 乙烯属于不饱和烃,平面结构。可做果实催熟剂
B乙烯可与Br2水发生加成反应使其褪色,
C.乙烯使酸性高锰酸钾褪色发生的是氧化还原反应
D.乙烯发生加聚反应生成高分子聚乙烯,聚乙烯有固定的熔沸点
(2)对乙烯的描述正确的是 A.结构简式: B球棍模型
C. 电子式: D.结构式:
(3)鉴别甲烷和乙烯可用的试剂是
A.稀硫酸 B.溴的四氯化碳溶液 C.水 D.酸性高锰酸钾溶液
(4)已知2 CH3CHO + O22 CH3COOH。若以乙烯为主要原料合成乙酸,其合成路 线如图所示。
乙烯 A B 乙酸
有关方程式正确的是
A.①方程式是:
B.②方程式是:
C.④方程式是:
D.⑤方程式是:
(5)流程中的反应类型错误的是
A. ①是加成反应 B. ⑤是酯化反应,就是取代反应
C. ②③是还原反应,有机物做氧化剂 D. ④是加聚反应
2023年6月广东省肇庆市普通高中学业水平合格性考试高一化学模拟(三)
答题栏
姓名 班级 成绩
一、单项选择题
题号 1 2 3 4 5 6 7 8 9 10 11 12
答案
题号 13 14 15 16 17 18 19 20 21 22 23 24
答案
题号 25 26 27 28 29 30 31 32 33 34 35
答案
二、不定项选择题
题号36 ① ② ③ ④ ⑤
答案
题号37 (1) (2) (3) (4) (5)
答案
题号38 (1) (2) (3) (4) (5)
答案
2023年6月广东省肇庆市普通高中学业水平合格性考试高一化学模拟(三)答案
一、单项选择题
题号 1 2 3 4 5 6 7 8 9 10 11 12
答案 D D A B C B A A C C C B
题号 13 14 15 16 17 18 19 20 21 22 23 24
答案 D C B C A B A D C D D D
题号 25 26 27 28 29 30 31 32 33 34 35
答案 D B A C A B B A C D A
二、不定项选择题
题号36 ① ② ③ ④ ⑤
答案 ABCD AB D BCD B
题号37 (1) (2) (3) (4) (5)
答案 AD B ABCD AB D
题号38 (1) (2) (3) (4) (5)
答案 D ABCD BD ABCD C
同课章节目录
