人教版高中化学选择性必修二 2.3.1共价键的极性 教案
文档属性
| 名称 | 人教版高中化学选择性必修二 2.3.1共价键的极性 教案 |

|
|
| 格式 | docx | ||
| 文件大小 | 494.3KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-06-20 00:00:00 | ||
图片预览

文档简介
第二章 分子结构与性质
第二节 分子的空间结构
2.3.1共价键的极性
【教材分析】
本节是在学习了共价键和分子的立体构型的基础上,进一步来认识分子的一些性质,包括共价键的极性和非极性,并由此引出一些共价分子的性质及其应用;范德华力、氢键及其对物质性质的影响,特别是物质的熔沸点及溶解性等;教学时要注意引导学生运用“物质结构决定物质性质,性质反映结构”的观念来理解和解释分子的性质。
【课程目标】
课程目标 学科素养
1.能从共用电子对是否发生偏移的角度认识键的极性的实质是成键原子分别带正电和负电。 2.知道分子可以分为极性分子和非极性分子。 3.知道分子极性和分子中键的极性、分子的空间结构密切相关。 a.微观辨识:能从微观角度理解共价键的极性和分子极性的关系。
b.模型认知:通过键的极性对物质性质的影响的探析,形成“结构决定性质"的认知模型。
【教学重难点】
教学重点:极性分子与非极性分子的判断
教学难点:极性分子与非极性分子的判断
【教学过程】
【情境引入】
微波炉的加热原理
任务一:分子的极性
【讲解】
分子的极性
(1)极性分子:分子的正电中心和负电中心不重合,使分子的某一部分呈正电性,另一部分呈负电性,这样的分子是极性分子。如HCl、H2O等。
(2)非极性分子:分子的正电中心和负电中性重合,使分子没有带正电和带负电的两部分,这样的分子是非极性分子。如P4、CO2等。
【设疑】
为什么水分子内部正电中心和负电中心不重合?
共用电子对在两原子周围出现的机会是否相同?即共用电子对是否偏移
【讲解】
有些共用电子对的两个原子由于电负性不同,那么共用电子对在两原子周围出现的机会便不同,即共用电子对发生偏移。有些共用电子对的两个原子由于电负性相同,那么共用电子对在两原子周围出现的机会相同,即共用电子对不发生偏移。
根据共用电子对是否偏移,可以将共价键分为极性键和非极性键。
任务二:键的极性
【讲解】
2.键的极性
以HCl分子为例,HCl分子是由不同元素的原子构成的,Cl原子的电负性大于H原子,致使共用电子对发生偏移,那么会使H原子呈正电性、Cl原子呈负电性。以Cl2分子为例,Cl2分子是由同种元素的原子构成的,每个Cl原子的电负性相同,致使共用电子对不发生偏移,使成键原子呈电中性。
【讲解】
判断分子的极性可依据分子中的化学键的极性向量和。
从向量的角度认识分子的极性,若分子中共价键的极性的向量和等于0,则分子中没有带正电和带负电的两部分,为非极性分子,如BF3、CH4等。
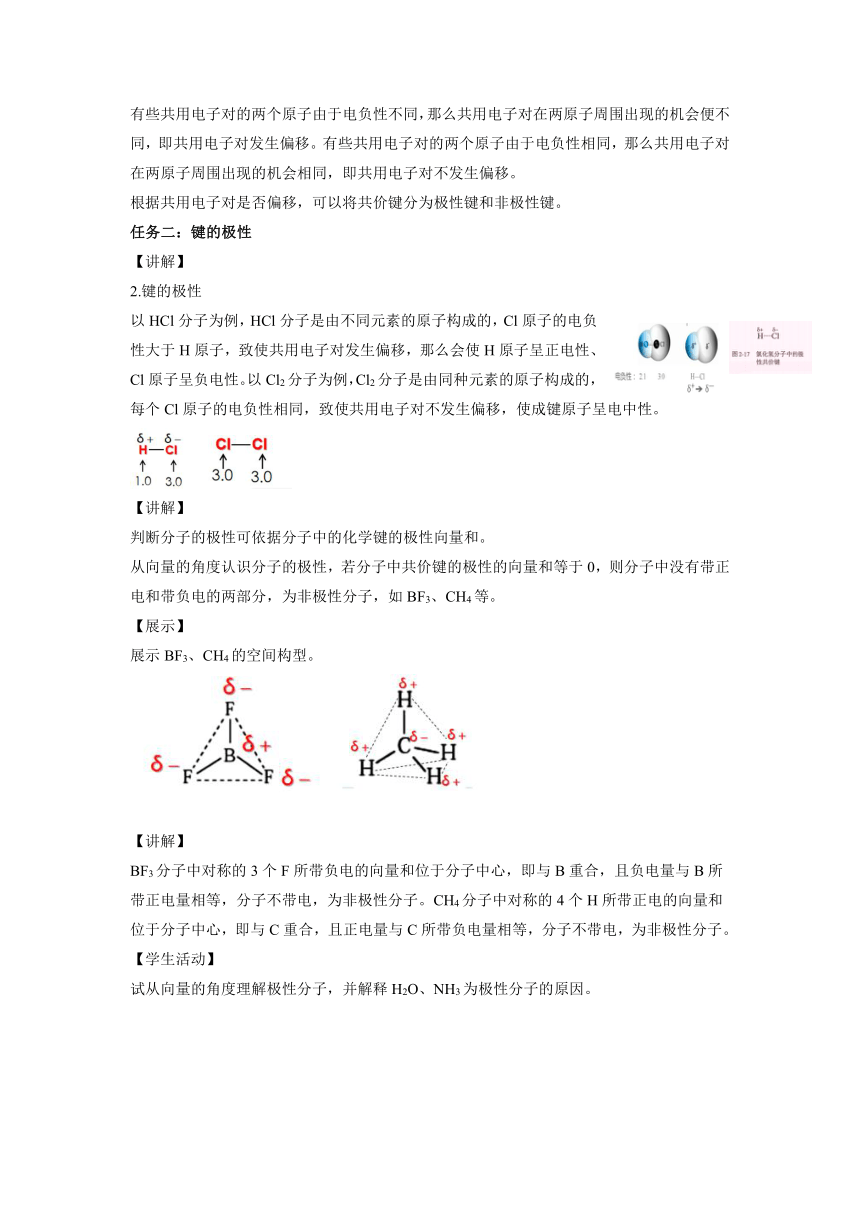
【展示】
展示BF3、CH4的空间构型。
【讲解】
BF3分子中对称的3个F所带负电的向量和位于分子中心,即与B重合,且负电量与B所带正电量相等,分子不带电,为非极性分子。CH4分子中对称的4个H所带正电的向量和位于分子中心,即与C重合,且正电量与C所带负电量相等,分子不带电,为非极性分子。
【学生活动】
试从向量的角度理解极性分子,并解释H2O、NH3为极性分子的原因。
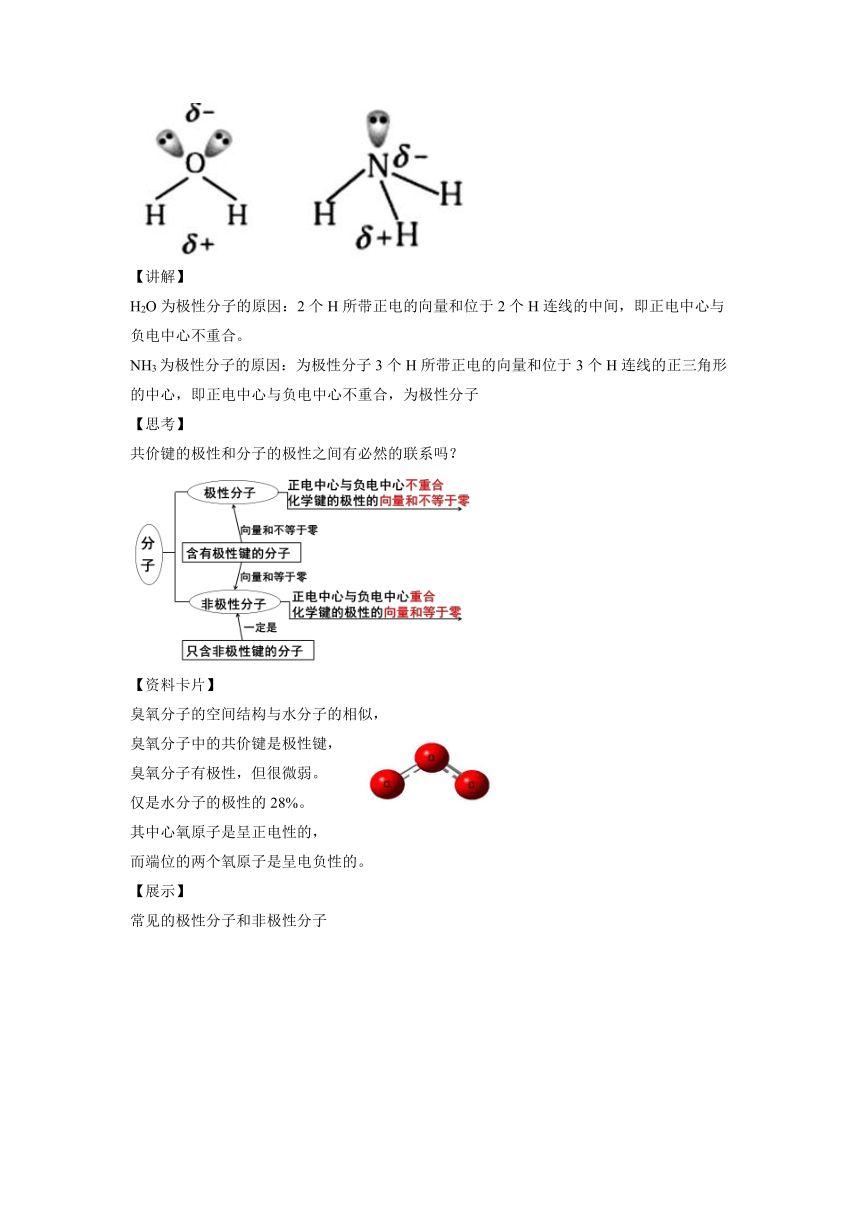
【讲解】
H2O为极性分子的原因:2个H所带正电的向量和位于2个H连线的中间,即正电中心与负电中心不重合。
NH3为极性分子的原因:为极性分子3个H所带正电的向量和位于3个H连线的正三角形的中心,即正电中心与负电中心不重合,为极性分子
【思考】
共价键的极性和分子的极性之间有必然的联系吗?
【资料卡片】
臭氧分子的空间结构与水分子的相似,
臭氧分子中的共价键是极性键,
臭氧分子有极性,但很微弱。
仅是水分子的极性的28%。
其中心氧原子是呈正电性的,
而端位的两个氧原子是呈电负性的。
【展示】
常见的极性分子和非极性分子
【思考交流】
如何判断分子的极性?
任务三:判断分子极性的方法
【讲解】
化合价法
2、根据分子的空间结构判断
【总结】
分子极性的判断方法
分子的极性是由分子中所含共价键的极性与分子的立体构型两方面共同决定的。
(1)只含有非极性键的双原子分子或多原子分子大多是非极性分子,如O2、H2、P4、C60。
(2)含有极性键的双原子分子都是极性分子,如HCl、HF、HBr。
(3)含有极性键的多原子分子,立体构型对称的是非极性分子;立体构型不对称的是极性分子。
(4)判断ABn型分子极性的经验规律:
①若中心原子A的化合价的绝对值等于该元素所在的主族序数,则为非极性分子;若不等,则为极性分子。
②若中心原子有孤电子对,则为极性分子;若无孤电子对,则为非极性分子。如CS2、BF3、SO3、CH4为非极性分子;H2S、SO2、NH3、PCl3为极性分子。
【课堂练习】
根据图2-18,思考和回答下列问题:
(1)以下双原子分子中,哪些是极性分子,哪些是非极性分子
H2O2 Cl2 HCl
(2)P4和C60是极性分子还是非极性分子
(3)以下化合物分子中,哪些是极性分子,哪些是非极性分子
CO2 HCN H2O NH3 BF3 CH4 CH3Cl
【讲解】
以下双原子分子中,H2O2、 HCl是极性分子, Cl2 是非极性分子。
P4和C60是非极性分子。
HCN、H2O、NH3、CH3Cl是极性分子,CO2、 BF3、CH4是非极性分子。
【点拨】
①稀有气体分子是非极性分子,但不含共价键
②臭氧是极性分子,共价键为极性键
③H2O2是由极性键和非极性键构成的极性分子
【拓展延伸】
表面活性剂
阅读教材,了解表面活性剂和细胞膜并回答问题。
【思考交流】
为什么钠和水的反应比钠和乙醇的反应剧烈?
【讲解】
乙醇分子中的C2H5—是推电子基团,使得乙醇分子中的电子云向着远离乙基的方向偏移,羟基的极性比水分子中的小,因而钠和乙醇的反应不如钠和水的剧烈
任务四:键的极性对化学性质的影响
【讲解】
键的极性对物质的化学性质有重要的影响。例如,羧酸是一大类含羧基(—COOH)的有机酸,羧基可电离出H+而呈酸性。羧酸的酸性可用pKa的大小来衡量,pKa越小,酸性越强。羧酸的酸性大小与其分子的组成和结构有关,如下表所示。
不同羧酸的pKa
羧酸 pKa
丙酸(C2H5COOH) 4.88
乙酸(CH3COOH) 4.76
甲酸(HCOOH) 3.75
氯乙酸(CH2ClCOOH) 2.86
二氯乙酸(CHCl2COOH) 1.29
三氯乙酸(CCl3COOH) 0.65
三氟乙酸(CF3COOH) 0.23
【学生活动】
为什么甲酸、乙酸、丙酸的酸性逐渐减弱?
CF3COOH的酸性大于CCl3COOH,解释原因。
试分析羧酸的酸性与分子的组成和结构的关系。
【提示】
1.烃基是推电子基团,烃基越长推电子效应越大,使羧基中的烃基的极性越小,羧酸的酸性越弱。所以,甲酸的酸性大于乙酸的,乙酸的酸性大于丙酸的……随着烃基加长,酸性的差异越来越小。
2.三氟乙酸的酸性大于三氯乙酸的,这是由于氟的电负性大于氯的电负性,F—C的极性大于Cc的极性,使F3C一的极性大于Cl3C一的极性,导致三氟乙酸的羧基中的羟基的极性更大,更易电离出氢离子。同理,三氯乙酸的酸性大于二氯乙酸的,二氯乙酸的酸性大于氯乙酸的。
3.①与羧酸(—COOH)相连的C—X(X为卤素原子)的极性越大,羧酸的酸性越大;C—X的数量越多,羧酸的酸性越大,如酸性:CF3COOH>CCl3COOH>CH3COOH;CCl3COOH>CHCl2COOH>CH2ClCOOH。
②烃基越长,羧酸的酸性越小,如酸性:C2H5COOH<CH3COOH<HCOOH。
【课堂练习】
见课件
【拓展延伸】
分子结构修饰
不改变分子的主体骨架,保持分子的基本结构不变,仅改变分子结构中的某些基团而得到新的分子,分子被修饰后,其性质也可以发生显著的变化
【课堂小结】
回顾本节课的内容,本节课需要掌握判断分子的共价键和极性。
第二节 分子的空间结构
2.3.1共价键的极性
【教材分析】
本节是在学习了共价键和分子的立体构型的基础上,进一步来认识分子的一些性质,包括共价键的极性和非极性,并由此引出一些共价分子的性质及其应用;范德华力、氢键及其对物质性质的影响,特别是物质的熔沸点及溶解性等;教学时要注意引导学生运用“物质结构决定物质性质,性质反映结构”的观念来理解和解释分子的性质。
【课程目标】
课程目标 学科素养
1.能从共用电子对是否发生偏移的角度认识键的极性的实质是成键原子分别带正电和负电。 2.知道分子可以分为极性分子和非极性分子。 3.知道分子极性和分子中键的极性、分子的空间结构密切相关。 a.微观辨识:能从微观角度理解共价键的极性和分子极性的关系。
b.模型认知:通过键的极性对物质性质的影响的探析,形成“结构决定性质"的认知模型。
【教学重难点】
教学重点:极性分子与非极性分子的判断
教学难点:极性分子与非极性分子的判断
【教学过程】
【情境引入】
微波炉的加热原理
任务一:分子的极性
【讲解】
分子的极性
(1)极性分子:分子的正电中心和负电中心不重合,使分子的某一部分呈正电性,另一部分呈负电性,这样的分子是极性分子。如HCl、H2O等。
(2)非极性分子:分子的正电中心和负电中性重合,使分子没有带正电和带负电的两部分,这样的分子是非极性分子。如P4、CO2等。
【设疑】
为什么水分子内部正电中心和负电中心不重合?
共用电子对在两原子周围出现的机会是否相同?即共用电子对是否偏移
【讲解】
有些共用电子对的两个原子由于电负性不同,那么共用电子对在两原子周围出现的机会便不同,即共用电子对发生偏移。有些共用电子对的两个原子由于电负性相同,那么共用电子对在两原子周围出现的机会相同,即共用电子对不发生偏移。
根据共用电子对是否偏移,可以将共价键分为极性键和非极性键。
任务二:键的极性
【讲解】
2.键的极性
以HCl分子为例,HCl分子是由不同元素的原子构成的,Cl原子的电负性大于H原子,致使共用电子对发生偏移,那么会使H原子呈正电性、Cl原子呈负电性。以Cl2分子为例,Cl2分子是由同种元素的原子构成的,每个Cl原子的电负性相同,致使共用电子对不发生偏移,使成键原子呈电中性。
【讲解】
判断分子的极性可依据分子中的化学键的极性向量和。
从向量的角度认识分子的极性,若分子中共价键的极性的向量和等于0,则分子中没有带正电和带负电的两部分,为非极性分子,如BF3、CH4等。
【展示】
展示BF3、CH4的空间构型。
【讲解】
BF3分子中对称的3个F所带负电的向量和位于分子中心,即与B重合,且负电量与B所带正电量相等,分子不带电,为非极性分子。CH4分子中对称的4个H所带正电的向量和位于分子中心,即与C重合,且正电量与C所带负电量相等,分子不带电,为非极性分子。
【学生活动】
试从向量的角度理解极性分子,并解释H2O、NH3为极性分子的原因。
【讲解】
H2O为极性分子的原因:2个H所带正电的向量和位于2个H连线的中间,即正电中心与负电中心不重合。
NH3为极性分子的原因:为极性分子3个H所带正电的向量和位于3个H连线的正三角形的中心,即正电中心与负电中心不重合,为极性分子
【思考】
共价键的极性和分子的极性之间有必然的联系吗?
【资料卡片】
臭氧分子的空间结构与水分子的相似,
臭氧分子中的共价键是极性键,
臭氧分子有极性,但很微弱。
仅是水分子的极性的28%。
其中心氧原子是呈正电性的,
而端位的两个氧原子是呈电负性的。
【展示】
常见的极性分子和非极性分子
【思考交流】
如何判断分子的极性?
任务三:判断分子极性的方法
【讲解】
化合价法
2、根据分子的空间结构判断
【总结】
分子极性的判断方法
分子的极性是由分子中所含共价键的极性与分子的立体构型两方面共同决定的。
(1)只含有非极性键的双原子分子或多原子分子大多是非极性分子,如O2、H2、P4、C60。
(2)含有极性键的双原子分子都是极性分子,如HCl、HF、HBr。
(3)含有极性键的多原子分子,立体构型对称的是非极性分子;立体构型不对称的是极性分子。
(4)判断ABn型分子极性的经验规律:
①若中心原子A的化合价的绝对值等于该元素所在的主族序数,则为非极性分子;若不等,则为极性分子。
②若中心原子有孤电子对,则为极性分子;若无孤电子对,则为非极性分子。如CS2、BF3、SO3、CH4为非极性分子;H2S、SO2、NH3、PCl3为极性分子。
【课堂练习】
根据图2-18,思考和回答下列问题:
(1)以下双原子分子中,哪些是极性分子,哪些是非极性分子
H2O2 Cl2 HCl
(2)P4和C60是极性分子还是非极性分子
(3)以下化合物分子中,哪些是极性分子,哪些是非极性分子
CO2 HCN H2O NH3 BF3 CH4 CH3Cl
【讲解】
以下双原子分子中,H2O2、 HCl是极性分子, Cl2 是非极性分子。
P4和C60是非极性分子。
HCN、H2O、NH3、CH3Cl是极性分子,CO2、 BF3、CH4是非极性分子。
【点拨】
①稀有气体分子是非极性分子,但不含共价键
②臭氧是极性分子,共价键为极性键
③H2O2是由极性键和非极性键构成的极性分子
【拓展延伸】
表面活性剂
阅读教材,了解表面活性剂和细胞膜并回答问题。
【思考交流】
为什么钠和水的反应比钠和乙醇的反应剧烈?
【讲解】
乙醇分子中的C2H5—是推电子基团,使得乙醇分子中的电子云向着远离乙基的方向偏移,羟基的极性比水分子中的小,因而钠和乙醇的反应不如钠和水的剧烈
任务四:键的极性对化学性质的影响
【讲解】
键的极性对物质的化学性质有重要的影响。例如,羧酸是一大类含羧基(—COOH)的有机酸,羧基可电离出H+而呈酸性。羧酸的酸性可用pKa的大小来衡量,pKa越小,酸性越强。羧酸的酸性大小与其分子的组成和结构有关,如下表所示。
不同羧酸的pKa
羧酸 pKa
丙酸(C2H5COOH) 4.88
乙酸(CH3COOH) 4.76
甲酸(HCOOH) 3.75
氯乙酸(CH2ClCOOH) 2.86
二氯乙酸(CHCl2COOH) 1.29
三氯乙酸(CCl3COOH) 0.65
三氟乙酸(CF3COOH) 0.23
【学生活动】
为什么甲酸、乙酸、丙酸的酸性逐渐减弱?
CF3COOH的酸性大于CCl3COOH,解释原因。
试分析羧酸的酸性与分子的组成和结构的关系。
【提示】
1.烃基是推电子基团,烃基越长推电子效应越大,使羧基中的烃基的极性越小,羧酸的酸性越弱。所以,甲酸的酸性大于乙酸的,乙酸的酸性大于丙酸的……随着烃基加长,酸性的差异越来越小。
2.三氟乙酸的酸性大于三氯乙酸的,这是由于氟的电负性大于氯的电负性,F—C的极性大于Cc的极性,使F3C一的极性大于Cl3C一的极性,导致三氟乙酸的羧基中的羟基的极性更大,更易电离出氢离子。同理,三氯乙酸的酸性大于二氯乙酸的,二氯乙酸的酸性大于氯乙酸的。
3.①与羧酸(—COOH)相连的C—X(X为卤素原子)的极性越大,羧酸的酸性越大;C—X的数量越多,羧酸的酸性越大,如酸性:CF3COOH>CCl3COOH>CH3COOH;CCl3COOH>CHCl2COOH>CH2ClCOOH。
②烃基越长,羧酸的酸性越小,如酸性:C2H5COOH<CH3COOH<HCOOH。
【课堂练习】
见课件
【拓展延伸】
分子结构修饰
不改变分子的主体骨架,保持分子的基本结构不变,仅改变分子结构中的某些基团而得到新的分子,分子被修饰后,其性质也可以发生显著的变化
【课堂小结】
回顾本节课的内容,本节课需要掌握判断分子的共价键和极性。
