8.1自然资源的开发利用 课件(共32张ppt)化学人教版(2019)必修第二册
文档属性
| 名称 | 8.1自然资源的开发利用 课件(共32张ppt)化学人教版(2019)必修第二册 |

|
|
| 格式 | pptx | ||
| 文件大小 | 8.7MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-06-20 00:00:00 | ||
图片预览











文档简介
(共32张PPT)
公司简介
适用于产品介绍/企业宣传/合作洽谈
第八章 化学与可持续发展
第一节 自然资源的开发利用
自主学习——各美其美
以 美 育 美 美 美 共 美
除金、铂等极少数金属,绝大多数金属元素以化合态的形式存在于自然界。
【思考】自然界中的金属是以什么形式存在的呢?
【思考】地壳中含量最高和次高的金属元素是什么?
含量最高的是铝,其次是铁。
黄铜矿
金矿
赤铁矿
(CuFeS2)
合作学习——美美共美
以 美 育 美 美 美 共 美
石器时代先进入青铜器时代,继而进入铁器时代,而铝的利用要比铜和铁晚得多,仅仅是100多年前的事情.所以利用的先后顺序为铜、铁、铝
【回忆】人类使用铝铁铜三种金属的顺序是什么?
【思考】地壳中铝的含量比铁和铜高,但是铝使用的时间却远远晚于铜和铁,这是为什么呢?不同活动性顺序的金属,提取的方法一样吗?
青铜器时代
铁器时代
开发使用铝
(距今100多年前)
(公元前2500年)
(公元前4000年)
Au、Ag、Cu、
Fe、
古代
现代
Al、
Ti
金属越活泼,越难冶炼。
自主学习——各美其美
以 美 育 美 美 美 共 美
一、金属的冶炼
将金属从其化合物中还原出来的过程,工业上称之为金属的冶炼。
2.冶炼的定义
n+
M
得电子
M
(被还原)
3.冶炼的实质
1.金属提取过程
富集
冶炼
精炼
目的:除去杂质,提高矿石中的有用成分的含量
目的:得到金属单质
目的:提高金属的纯度
自主学习——各美其美
以 美 育 美 美 美 共 美
4.冶炼的方法
K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au
电解法
热还原法
热分解法
物理方法
金属活动性顺序
强 弱
自主学习——各美其美
以 美 育 美 美 美 共 美
(1).物理方法
适用于极不活泼的金属,如Pt、Au
如“沙土淘金”就是利用水冲洗沙子,将沙土冲走,剩下密度很大的金砂,再进一步分离便可得到金属纯金。
K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au
自主学习——各美其美
以 美 育 美 美 美 共 美
(2).热分解法
对一些不活泼金属,可以直接用加热分解的方法将它们从其化合物中还原出来。
K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au
如古代炼丹术士葛洪的《抱朴子》中“丹砂烧之成水银”
HgS ===2Hg + S
2HgO === 2Hg + O2 ↑
2Ag2O === 4Ag + O2 ↑
常见的还有:
自主学习——各美其美
以 美 育 美 美 美 共 美
(3).电解法
适用于一些非常活泼的金属,采用一般的还原剂很难将它们从其化合物中还原出来,工业上常用电解法冶炼。
K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au
MgCl2 (熔融) Mg + Cl2 ↑
电解
2NaCl (熔融) 2Na+Cl2 ↑
电解
2Al2O3 (熔融) 4Al + 3O2 ↑
电解
冰晶石
冰晶石的作用是降低Al2O3的熔化温度
合作学习——美美共美
以 美 育 美 美 美 共 美
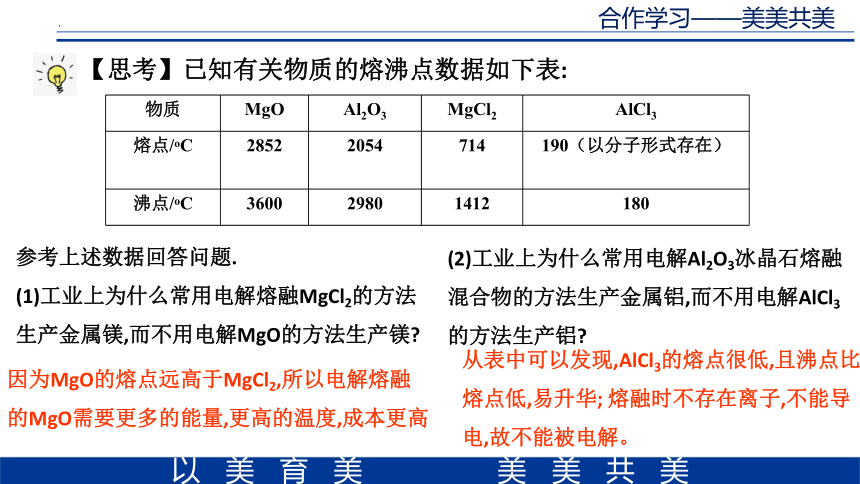
【思考】已知有关物质的熔沸点数据如下表:
物质 MgO Al2O3 MgCl2 AlCl3
熔点/oC 2852 2054 714 190(以分子形式存在)
沸点/oC 3600 2980 1412 180
参考上述数据回答问题.
(1)工业上为什么常用电解熔融MgCl2的方法生产金属镁,而不用电解MgO的方法生产镁
(2)工业上为什么常用电解Al2O3冰晶石熔融混合物的方法生产金属铝,而不用电解AlCl3的方法生产铝
因为MgO的熔点远高于MgCl2,所以电解熔融
的MgO需要更多的能量,更高的温度,成本更高
从表中可以发现,AlCl3的熔点很低,且沸点比熔点低,易升华; 熔融时不存在离子,不能导电,故不能被电解。
自主学习——各美其美
以 美 育 美 美 美 共 美
(4).热还原法
大部分金属的冶炼都是通过在高温下发生的氧化还原反应完成的。
K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au
常见的还原剂:CO、H2、C(焦炭)、活泼金属(如铝热反应)
Fe2O3+3CO === 2Fe + 3CO2
高温
CuO+H2 === Cu + H2O
高温
自主学习——各美其美
以 美 育 美 美 美 共 美
(4.1)铝热反应
以铝粉和金属氧化物反应,获得金属单质的反应。
原理:活泼金属置换不活泼金属
自主学习——各美其美
以 美 育 美 美 美 共 美
4.1铝热反应
现象:镁条剧烈燃烧,放出大量的热,发出耀眼的白光,纸漏斗内剧烈反应,纸漏斗被烧穿,有熔融物落入沙中
Fe2O3+2Al 2Fe + Al2O3
高温
【思考】
1、铝热反应需要高温条件,是否还需要持续加热?
2、实验中,镁条、氯酸钾的作用是什么
3、蒸发皿中铺少量细沙的作用是什么?
防止蒸发皿炸裂,防止熔融的液体溅出伤人
不需要
引燃剂和助燃剂
铝热剂
自主学习——各美其美
以 美 育 美 美 美 共 美
4.1铝热反应
铝热反应的原理可以应用在生产上,如用于焊接钢轨等。在冶金工业上也常用这一反应原理,冶炼钒、铬、锰等高熔点金属。
Fe2O3+2Al 2Fe + Al2O3
高温
3MnO2+4Al 3Mn+ 2Al2O3
高温
Cr2O3+2Al 2Cr + Al2O3
高温
3Co3O4+8Al 9Co + 4Al2O3
高温
3V2O5+10Al 6V+ 5Al2O3
高温
自主学习——各美其美
以 美 育 美 美 美 共 美
5.其他金属冶炼方法
信州铅山县有苦泉,流以为涧。其水熬之,则成胆矾,烹胆矾则成铜。熬胆矾铁釜,久之异化为铜。
——沈括《梦溪笔谈》
用矿(硫化矿,主要成分为Cu2S)二百五十箩……入大旋风炉,连烹(灼烧) 三日三夜,方见成铜。
——明·陆容《菽园杂记》
湿法炼铜
火法炼铜
CuSO4 + Fe == Cu + FeSO4
Cu2S+O2 == 2Cu+SO2
高温
自主学习——各美其美
以 美 育 美 美 美 共 美
Page 99 --- 思考与讨论
计算表明,生产1 mol铝消耗的电能至少为1.8×106 J,回收铝制饮料罐得到铝与从铝土矿相比,前者的能耗仅为后者的3%-5%。通过对上述数据的分析和比较,并结合图8-1和图8-2,你想到了什么?
加强废旧金属的回收和再利用
合理开发和利用金属资源的有效途径:
防止金属的腐蚀
形成绿色化学观念和可持续发展意识
开发环保高效的金属冶炼方法
以 美 育 美 美 美 共 美
课堂小结——追求至美
化学反应与热能
电解法
K Ca Na Mg Al
热还原法
Zn Fe Sn Pb Cu
热分解法
Hg Ag
物理法
Pt Au
以 美 育 美 美 美 共 美
反馈检测——追求至美
1. 工业上冶炼金属一般用热分解法、热还原法和电解法。你认为选择方法的主要依据是( )
A. 金属在自然界的存在形式
B. 金属元素在地壳中的含量
C. 金属熔点高低
D. 金属阳离子得电子的能力
D
以 美 育 美 美 美 共 美
反馈检测——追求至美
2. 下列各种冶炼方法中,可以制得相应金属的是( )
A. 加热氧化铝
B. 电解熔融氯化钠
C. 加热碳酸钙
D. 氯化钠与铝粉高温共热
B
以 美 育 美 美 美 共 美
反馈检测——追求至美
3.下列反应原理不符合工业冶炼金属实际情况的是( )
A、
B、
C、
D、
C
2MgO ===
HgO ===
△
2 2Hg + O2 ↑
3MnO2+4Al === 3Mn+ 2Al2O3
高温
电解
2Mg + O2 ↑
Fe3O4+4CO === 3Fe + 4CO2
高温
自主学习——各美其美
以 美 育 美 美 美 共 美
分离盐分
提取淡水
直接利用
海水淡化
海水水资源
电渗析法
膜分离法
循环冷却
蒸馏法
离子交换法
二、海水水资源的利用
直接使用海水作火电厂、核电厂的循环冷却水
通过从海水中提取淡水或从海水中把盐分离出去,都可以达到淡化海水的目的。
自主学习——各美其美
以 美 育 美 美 美 共 美
1、海水的直接利用
基于安全角度
【思考】为什么核电站往往建立在海边?
大亚湾核电站
减少输电成本
利用海水降温
核电站的蒸汽在汽轮机里做功后出来的是乏气,而乏气是无法再给水泵运输的,需要在凝汽器中冷却成凝结水。
自主学习——各美其美
以 美 育 美 美 美 共 美
2、海水的淡化
将海水加热至沸腾汽化,然后将蒸气冷凝而得到蒸馏水。
1、蒸馏法
√最早使用,技术成熟
×成本较高
太阳能蒸发装置
自主学习——各美其美
以 美 育 美 美 美 共 美
蒸馏法-实验室蒸馏
加热装置 冷凝装置 接收装置
冷凝水:下进上出
温度计水银球处于支管口处
液体体积不应该超过容积的2/3,不应少于1/3
加入沸石/碎瓷片,防暴沸
利用各成分的沸点不同,分离(互溶)液态混合物的物理分离方法。
自主学习——各美其美
以 美 育 美 美 美 共 美
蒸馏法-实验室蒸馏
主要仪器:蒸馏烧瓶、直形冷凝管、牛角管、锥形瓶
操作步骤:连接装置→检查装置气密性→向烧瓶中加入海水和碎瓷片→接通冷却水→给烧瓶加热→收集蒸馏水→停止对烧瓶加热→待冷却至室温后停止通入冷却水→整理仪器。
先停止加热,后停止通入冷却水
自主学习——各美其美
2、电渗析法
氯化钠水溶液
水
阴离子交换膜
阳离子交换膜
+ -
利用电场的作用,强行将离子向电极处吸引,致使电极中间部位的离子浓度大为下降,从而制得淡水。
电源
自主学习——各美其美
以 美 育 美 美 美 共 美
3、离子交换法
离子交换树脂可以把阴阳离子分别交换出来,使水得到纯化。
HR + Na+ = NaR + H+
ROH + Cl— = RCl +OH—
H++OH- =H2O
自主学习——各美其美
以 美 育 美 美 美 共 美
3、膜分离法
利用膜的选择性分离实现料液的不同组分的分离、纯化、浓缩。
自主学习——各美其美
以 美 育 美 美 美 共 美
3、海水制盐
浓缩海水
盐田
饱和食盐水
粗盐
母液
风吹日晒
析出晶体
风吹日晒
蒸发水分
精盐
“母液”也叫“苦卤”,含有高浓度的K+、Mg2+、Br-和SO42-等,可从中提取多种化工原料。
提纯
引入
自主学习——各美其美
以 美 育 美 美 美 共 美
4.海水提溴-具体步骤
步骤 原理
浓缩 海水晒盐和海水淡化后的母液中Br-得到浓缩
氧化 2Br-+Cl2===Br2+2Cl-
吹出 利用溴的挥发性,通入热空气将溴从海水中吹出,进入吸收塔
吸收 Br2+SO2+2H2O===4H++SO42-+2Br-
氧化 2Br-+Cl2===Br2+2Cl-
分离 富集后的Br2通过蒸馏、冷凝得到液溴
【思考】为什么不直接用氧化室中得到的溴水混合物蒸馏?
氧化室中的溴水混合物中溴单质浓度低,如果直接蒸馏,处理量大,生产成本高。
拓展学习——追求至美
5、海水提镁
富含Mg2+海水
贝壳CaCO3
高温煅烧
CaO
沉降池
过滤网
沉降过滤
Mg(OH)2
△
MgO
(耐火材料)
HCl溶液
MgCl2溶液
MgCl2
熔融电解
Mg
Cl2
蒸发浓缩
冷却结晶
在HCl氛围中脱水
MgCl2 + Ca(OH)2 = Mg(OH)2 ↓ + CaCl2
Mg(OH)2 + 2HCl = MgCl2 + 2H2O
MgCl2 = Mg + Cl2↑
MgCl2·6H2O = MgCl2 + 6H2O
HCl
MgCl2·6H2O溶液
石灰乳
6、海带提碘
稀硫酸
过氧化氢溶液或Cl2
灼烧
浸泡
过滤
蒸馏
海带灰
海带
悬浊液
含I-滤液
碘水
碘的CCl4溶液
单质碘
操作1
操作2
操作3
操作4
操作5
试剂1
试剂2
萃取
分液
生物
富集
海水
分液漏斗
2I-+ H2O2+2H+ = I2 +2H2O
或Cl2+2I-=I2+2Cl-
增强H2O2的氧化性;抑制I2与水反应
拓展学习——追求至美
稀硫酸作用:
公司简介
适用于产品介绍/企业宣传/合作洽谈
第八章 化学与可持续发展
第一节 自然资源的开发利用
自主学习——各美其美
以 美 育 美 美 美 共 美
除金、铂等极少数金属,绝大多数金属元素以化合态的形式存在于自然界。
【思考】自然界中的金属是以什么形式存在的呢?
【思考】地壳中含量最高和次高的金属元素是什么?
含量最高的是铝,其次是铁。
黄铜矿
金矿
赤铁矿
(CuFeS2)
合作学习——美美共美
以 美 育 美 美 美 共 美
石器时代先进入青铜器时代,继而进入铁器时代,而铝的利用要比铜和铁晚得多,仅仅是100多年前的事情.所以利用的先后顺序为铜、铁、铝
【回忆】人类使用铝铁铜三种金属的顺序是什么?
【思考】地壳中铝的含量比铁和铜高,但是铝使用的时间却远远晚于铜和铁,这是为什么呢?不同活动性顺序的金属,提取的方法一样吗?
青铜器时代
铁器时代
开发使用铝
(距今100多年前)
(公元前2500年)
(公元前4000年)
Au、Ag、Cu、
Fe、
古代
现代
Al、
Ti
金属越活泼,越难冶炼。
自主学习——各美其美
以 美 育 美 美 美 共 美
一、金属的冶炼
将金属从其化合物中还原出来的过程,工业上称之为金属的冶炼。
2.冶炼的定义
n+
M
得电子
M
(被还原)
3.冶炼的实质
1.金属提取过程
富集
冶炼
精炼
目的:除去杂质,提高矿石中的有用成分的含量
目的:得到金属单质
目的:提高金属的纯度
自主学习——各美其美
以 美 育 美 美 美 共 美
4.冶炼的方法
K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au
电解法
热还原法
热分解法
物理方法
金属活动性顺序
强 弱
自主学习——各美其美
以 美 育 美 美 美 共 美
(1).物理方法
适用于极不活泼的金属,如Pt、Au
如“沙土淘金”就是利用水冲洗沙子,将沙土冲走,剩下密度很大的金砂,再进一步分离便可得到金属纯金。
K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au
自主学习——各美其美
以 美 育 美 美 美 共 美
(2).热分解法
对一些不活泼金属,可以直接用加热分解的方法将它们从其化合物中还原出来。
K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au
如古代炼丹术士葛洪的《抱朴子》中“丹砂烧之成水银”
HgS ===2Hg + S
2HgO === 2Hg + O2 ↑
2Ag2O === 4Ag + O2 ↑
常见的还有:
自主学习——各美其美
以 美 育 美 美 美 共 美
(3).电解法
适用于一些非常活泼的金属,采用一般的还原剂很难将它们从其化合物中还原出来,工业上常用电解法冶炼。
K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au
MgCl2 (熔融) Mg + Cl2 ↑
电解
2NaCl (熔融) 2Na+Cl2 ↑
电解
2Al2O3 (熔融) 4Al + 3O2 ↑
电解
冰晶石
冰晶石的作用是降低Al2O3的熔化温度
合作学习——美美共美
以 美 育 美 美 美 共 美
【思考】已知有关物质的熔沸点数据如下表:
物质 MgO Al2O3 MgCl2 AlCl3
熔点/oC 2852 2054 714 190(以分子形式存在)
沸点/oC 3600 2980 1412 180
参考上述数据回答问题.
(1)工业上为什么常用电解熔融MgCl2的方法生产金属镁,而不用电解MgO的方法生产镁
(2)工业上为什么常用电解Al2O3冰晶石熔融混合物的方法生产金属铝,而不用电解AlCl3的方法生产铝
因为MgO的熔点远高于MgCl2,所以电解熔融
的MgO需要更多的能量,更高的温度,成本更高
从表中可以发现,AlCl3的熔点很低,且沸点比熔点低,易升华; 熔融时不存在离子,不能导电,故不能被电解。
自主学习——各美其美
以 美 育 美 美 美 共 美
(4).热还原法
大部分金属的冶炼都是通过在高温下发生的氧化还原反应完成的。
K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au
常见的还原剂:CO、H2、C(焦炭)、活泼金属(如铝热反应)
Fe2O3+3CO === 2Fe + 3CO2
高温
CuO+H2 === Cu + H2O
高温
自主学习——各美其美
以 美 育 美 美 美 共 美
(4.1)铝热反应
以铝粉和金属氧化物反应,获得金属单质的反应。
原理:活泼金属置换不活泼金属
自主学习——各美其美
以 美 育 美 美 美 共 美
4.1铝热反应
现象:镁条剧烈燃烧,放出大量的热,发出耀眼的白光,纸漏斗内剧烈反应,纸漏斗被烧穿,有熔融物落入沙中
Fe2O3+2Al 2Fe + Al2O3
高温
【思考】
1、铝热反应需要高温条件,是否还需要持续加热?
2、实验中,镁条、氯酸钾的作用是什么
3、蒸发皿中铺少量细沙的作用是什么?
防止蒸发皿炸裂,防止熔融的液体溅出伤人
不需要
引燃剂和助燃剂
铝热剂
自主学习——各美其美
以 美 育 美 美 美 共 美
4.1铝热反应
铝热反应的原理可以应用在生产上,如用于焊接钢轨等。在冶金工业上也常用这一反应原理,冶炼钒、铬、锰等高熔点金属。
Fe2O3+2Al 2Fe + Al2O3
高温
3MnO2+4Al 3Mn+ 2Al2O3
高温
Cr2O3+2Al 2Cr + Al2O3
高温
3Co3O4+8Al 9Co + 4Al2O3
高温
3V2O5+10Al 6V+ 5Al2O3
高温
自主学习——各美其美
以 美 育 美 美 美 共 美
5.其他金属冶炼方法
信州铅山县有苦泉,流以为涧。其水熬之,则成胆矾,烹胆矾则成铜。熬胆矾铁釜,久之异化为铜。
——沈括《梦溪笔谈》
用矿(硫化矿,主要成分为Cu2S)二百五十箩……入大旋风炉,连烹(灼烧) 三日三夜,方见成铜。
——明·陆容《菽园杂记》
湿法炼铜
火法炼铜
CuSO4 + Fe == Cu + FeSO4
Cu2S+O2 == 2Cu+SO2
高温
自主学习——各美其美
以 美 育 美 美 美 共 美
Page 99 --- 思考与讨论
计算表明,生产1 mol铝消耗的电能至少为1.8×106 J,回收铝制饮料罐得到铝与从铝土矿相比,前者的能耗仅为后者的3%-5%。通过对上述数据的分析和比较,并结合图8-1和图8-2,你想到了什么?
加强废旧金属的回收和再利用
合理开发和利用金属资源的有效途径:
防止金属的腐蚀
形成绿色化学观念和可持续发展意识
开发环保高效的金属冶炼方法
以 美 育 美 美 美 共 美
课堂小结——追求至美
化学反应与热能
电解法
K Ca Na Mg Al
热还原法
Zn Fe Sn Pb Cu
热分解法
Hg Ag
物理法
Pt Au
以 美 育 美 美 美 共 美
反馈检测——追求至美
1. 工业上冶炼金属一般用热分解法、热还原法和电解法。你认为选择方法的主要依据是( )
A. 金属在自然界的存在形式
B. 金属元素在地壳中的含量
C. 金属熔点高低
D. 金属阳离子得电子的能力
D
以 美 育 美 美 美 共 美
反馈检测——追求至美
2. 下列各种冶炼方法中,可以制得相应金属的是( )
A. 加热氧化铝
B. 电解熔融氯化钠
C. 加热碳酸钙
D. 氯化钠与铝粉高温共热
B
以 美 育 美 美 美 共 美
反馈检测——追求至美
3.下列反应原理不符合工业冶炼金属实际情况的是( )
A、
B、
C、
D、
C
2MgO ===
HgO ===
△
2 2Hg + O2 ↑
3MnO2+4Al === 3Mn+ 2Al2O3
高温
电解
2Mg + O2 ↑
Fe3O4+4CO === 3Fe + 4CO2
高温
自主学习——各美其美
以 美 育 美 美 美 共 美
分离盐分
提取淡水
直接利用
海水淡化
海水水资源
电渗析法
膜分离法
循环冷却
蒸馏法
离子交换法
二、海水水资源的利用
直接使用海水作火电厂、核电厂的循环冷却水
通过从海水中提取淡水或从海水中把盐分离出去,都可以达到淡化海水的目的。
自主学习——各美其美
以 美 育 美 美 美 共 美
1、海水的直接利用
基于安全角度
【思考】为什么核电站往往建立在海边?
大亚湾核电站
减少输电成本
利用海水降温
核电站的蒸汽在汽轮机里做功后出来的是乏气,而乏气是无法再给水泵运输的,需要在凝汽器中冷却成凝结水。
自主学习——各美其美
以 美 育 美 美 美 共 美
2、海水的淡化
将海水加热至沸腾汽化,然后将蒸气冷凝而得到蒸馏水。
1、蒸馏法
√最早使用,技术成熟
×成本较高
太阳能蒸发装置
自主学习——各美其美
以 美 育 美 美 美 共 美
蒸馏法-实验室蒸馏
加热装置 冷凝装置 接收装置
冷凝水:下进上出
温度计水银球处于支管口处
液体体积不应该超过容积的2/3,不应少于1/3
加入沸石/碎瓷片,防暴沸
利用各成分的沸点不同,分离(互溶)液态混合物的物理分离方法。
自主学习——各美其美
以 美 育 美 美 美 共 美
蒸馏法-实验室蒸馏
主要仪器:蒸馏烧瓶、直形冷凝管、牛角管、锥形瓶
操作步骤:连接装置→检查装置气密性→向烧瓶中加入海水和碎瓷片→接通冷却水→给烧瓶加热→收集蒸馏水→停止对烧瓶加热→待冷却至室温后停止通入冷却水→整理仪器。
先停止加热,后停止通入冷却水
自主学习——各美其美
2、电渗析法
氯化钠水溶液
水
阴离子交换膜
阳离子交换膜
+ -
利用电场的作用,强行将离子向电极处吸引,致使电极中间部位的离子浓度大为下降,从而制得淡水。
电源
自主学习——各美其美
以 美 育 美 美 美 共 美
3、离子交换法
离子交换树脂可以把阴阳离子分别交换出来,使水得到纯化。
HR + Na+ = NaR + H+
ROH + Cl— = RCl +OH—
H++OH- =H2O
自主学习——各美其美
以 美 育 美 美 美 共 美
3、膜分离法
利用膜的选择性分离实现料液的不同组分的分离、纯化、浓缩。
自主学习——各美其美
以 美 育 美 美 美 共 美
3、海水制盐
浓缩海水
盐田
饱和食盐水
粗盐
母液
风吹日晒
析出晶体
风吹日晒
蒸发水分
精盐
“母液”也叫“苦卤”,含有高浓度的K+、Mg2+、Br-和SO42-等,可从中提取多种化工原料。
提纯
引入
自主学习——各美其美
以 美 育 美 美 美 共 美
4.海水提溴-具体步骤
步骤 原理
浓缩 海水晒盐和海水淡化后的母液中Br-得到浓缩
氧化 2Br-+Cl2===Br2+2Cl-
吹出 利用溴的挥发性,通入热空气将溴从海水中吹出,进入吸收塔
吸收 Br2+SO2+2H2O===4H++SO42-+2Br-
氧化 2Br-+Cl2===Br2+2Cl-
分离 富集后的Br2通过蒸馏、冷凝得到液溴
【思考】为什么不直接用氧化室中得到的溴水混合物蒸馏?
氧化室中的溴水混合物中溴单质浓度低,如果直接蒸馏,处理量大,生产成本高。
拓展学习——追求至美
5、海水提镁
富含Mg2+海水
贝壳CaCO3
高温煅烧
CaO
沉降池
过滤网
沉降过滤
Mg(OH)2
△
MgO
(耐火材料)
HCl溶液
MgCl2溶液
MgCl2
熔融电解
Mg
Cl2
蒸发浓缩
冷却结晶
在HCl氛围中脱水
MgCl2 + Ca(OH)2 = Mg(OH)2 ↓ + CaCl2
Mg(OH)2 + 2HCl = MgCl2 + 2H2O
MgCl2 = Mg + Cl2↑
MgCl2·6H2O = MgCl2 + 6H2O
HCl
MgCl2·6H2O溶液
石灰乳
6、海带提碘
稀硫酸
过氧化氢溶液或Cl2
灼烧
浸泡
过滤
蒸馏
海带灰
海带
悬浊液
含I-滤液
碘水
碘的CCl4溶液
单质碘
操作1
操作2
操作3
操作4
操作5
试剂1
试剂2
萃取
分液
生物
富集
海水
分液漏斗
2I-+ H2O2+2H+ = I2 +2H2O
或Cl2+2I-=I2+2Cl-
增强H2O2的氧化性;抑制I2与水反应
拓展学习——追求至美
稀硫酸作用:
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
