第1章认识化学科学单元测试卷高一上学期化学鲁科版(2019)必修第一册(含解析)
文档属性
| 名称 | 第1章认识化学科学单元测试卷高一上学期化学鲁科版(2019)必修第一册(含解析) |

|
|
| 格式 | docx | ||
| 文件大小 | 334.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-06-20 00:00:00 | ||
图片预览




文档简介
第1章《认识化学科学》单元测试卷
一、单选题
1.三氯化氮(NCl3)易与水反应:2NCl3+3H2O=3HCl+N2↑+3HClO。若NA代表阿伏加德罗常数的值。下列说法正确的是( )
A.0.1 mol NCl3中质子数为6.5NA
B.每生成36.5 g HCl转移电子数为2NA
C.标准状况下,2.24 LN2中含σ键数为0.2NA
D.100 mL1 mol/LHClO溶液中阴、阳离子总数为0.2NA
2.实验室利用NaOH固体配制480mL0.1mol·L-1的NaOH溶液时,以下操作会使溶液的浓度偏高的是
A.用滤纸称量NaOH固体
B.溶解后没有冷却便进行定容
C.定容时仰视刻度线
D.将容量瓶中的溶液转移到试剂瓶的过程中,不慎有少量溶液溅出
3.化学科学与技术在宇宙探索、改进生活、改善环境与促进发展方面均发挥着关键性的作用。下列说法正确的是
A.指南针是我国古代的四大发明之一,制造指南针的磁性物质是FeO
B.湖南苗族银饰和江西景德镇彩瓷是我国特有的文化产品,其主要成分均为金属材料
C.人工合成淀粉不仅有利于解决人类的温饱问题,也有利于实现“碳中和”
D.北斗导航专用ASIC硬件结合国产处理器打造出的一颗真正意义的“中国芯”,其主要成分为SiO2
4.下列实验现象描述不正确的是
A.铁丝在氯气中点燃,剧烈燃烧,产生棕褐色烟,燃烧后产物溶于水,溶液呈棕黄色
B.钠在空气中加热,先熔化成银白色小球,然后燃烧,发出黄色火焰,生成淡黄色固体
C.钠放入氯化铁溶液后,浮在水面,迅速游动,嘶嘶作响,溶液中出现红褐色沉淀
D.将1~2mL水滴入盛有1~2g过氧化钠固体的试管中,滴加酚酞,溶液变红
5.设为阿伏加德罗常数的值,下列叙述正确的是
A.22.4L中含氯原子数目为
B.7.8g苯中含碳碳双键数日为3
C.1mol乙酸与足量乙醇充分反应,所得乙酸乙酯分子数目为
D.28g乙烯和丙烯的混合气体中含共用电子对数目为6
6.相同质量的SO2和SO3,下列关系正确的是
A.含硫原子个数比为1∶1 B.含氧原子个数比为2∶3
C.含硫元素质量比为4∶5 D.含氧元素质量比为5∶6
7.1gO2和1gO3中
A.所含分子数相同 B.在标准状况下的体积相同
C.所含原子数相同 D.1gO3中所含分子数较多
8.将过氧化钠投入下列溶液中,恢复至原温度时,会有白色物质析出的是( )
A.饱和CuSO4溶液 B.饱和石灰水 C.生理盐水 D.稀盐酸
9.下列说法正确的是
A.过氧化钠与二氧化硫反应可生成硫酸钠
B.明矾具有很强的杀菌消毒作用,因此可以用作净水剂
C.用覆铜板制作印刷电路板就是利用铁单质还原性比铜强的原理
D.合金的熔点一定比各成分金属的低
10.NA阿伏加德罗常数的值。下列叙述正确的是
A.22 g D3O+中含有的中子数为10NA
B.1 mol P4S3()分子中含有非极性键的数目为3NA
C.1 L0.1 mol/L草酸(H2C2O4)溶液中含有H+的数目为0.2NA
D.11.2 L(标准状况)氧气与足量钠反应,转移的电子数一定为NA
11.铝分别与足量的稀盐酸和氢氧化钠溶液反应,当两个反应放出的气体在相同状况下体积相同时,反应中消耗的HCl和NaOH的物质的量之比为
A.3:1 B.1:1 C.2:1 D.1:2
12.设NA表示阿伏伽德罗常数,下列叙述中正确的是
A.常温常压下,11.2 L H2O所含原子数为1.5NA
B.常温常压下,92gNO2 和N2O4混合气体中含有原子总数为6NA
C.标准状况下,22.4 L氦气中所含原子数为2NA
D.常温常压下,18gH2O中含有电子数为3NA
13.某学生运用所学知识研究钠的性质:将一粒金属钠和一块不锈钢片分别放在表面皿中,研究它们在空气中的稳定性。该学生采用的研究方法是
①假说法 ②实验法 ③分类法 ④比较法
A.②④ B.①②③④ C.①③ D.①②
14.将金属钠分别投入下列物质的溶液中,有气体放出且溶液质量减轻的是( )
A.HCl B.K2SO4
C.稀NaOH溶液 D.饱和NaOH溶液
15.下列化合物中一般不能通过单质与氯气直接化合制得的是
A.FeCl2 B.FeCl3 C.CuCl2 D.NaCl
二、填空题
16.完成下列填空:
(1)0.25mol 在标准状况下的体积为_________,含有的原子数目为_________。
(2)0.98g物质中的含有个分子,则该物质的物质的量为_________,的摩尔质量为_________,A的相对原子质量为_________。
17.硫酸亚铁铵晶体的化学式为,是常用的还原剂,实验室制备它的原理为.已知几种盐的溶解度(g)如下表所示:
温度/℃ 0 10 20 30 40 50
15.6 20.5 26.5 32.9 40.2 48.6
70.6 73.0 75.4 78.0 81.63 84.4
12.5 17.2 33.0 40.0
回答下列问题:
(1)下列有关的说法错误的是_______(填序号)。A.是硫酸盐 B.是铁盐 C.是含氧酸盐 D.是可溶性盐
(2)实验室制备硫酸亚铁铵晶体时,从混合液中获取该晶体的操作是_______、过滤、洗涤、干燥。
(3)若某次实验中需要使用480mL0.1mol/L硫酸亚铁铵溶液,则实验中需要称取_______g硫酸亚铁铵晶体。配制时所用的水要先用蒸馏法处理,其目的是_______。若定容时仰视容量瓶刻度线,则所配溶液浓度_______(填“偏高”或“偏低”)。
(4)取20mL所配溶液与足量NaOH溶液反应,将所得沉淀充分放置一段时间后过滤、洗涤、灼烧,最终可得到_______g固体。
18.Ⅰ、铝土矿(主要成分为Al2O3,含有少量杂质)是提取铝的原料。提取铝的工艺流程如下:
(1)请用离子方程式表示以上工艺流程中第①步反应:___________。
(2)写出以上工艺流程中第③步反应的化学方程式:___________。
(3)若第①步加入的是盐酸,则发生反应的离子方程式为___________。
Ⅱ、下图为几种物质的转化关系,其中A为金属,B为淡黄色固体粉末,每一物质均含有A元素。
(4)写出下列物质的化学式:
B___________,C___________,E___________,F___________。
(5)写出下列各步反应的化学方程式:
C→E___________;
C→F___________;
F→C___________。
三、计算题
19.含有个HCl分子,物质的量是_______mol,在标准状况下的体积是_______升,溶于水得到50mL盐酸溶液,物质的量浓度是_______,加入足量的粉末,生成的全部通入足量NaOH溶液中,溶液增重_______克。
20.反应完成后得到的混合物处理得到固体NaHCO3和滤液,对固体NaHCO3充分加热,产生的气体先通过足量浓硫酸,再通过足量Na2O2,Na2O2增重0.14g,则固体NaHCO3的质量为_______g。
四、实验题
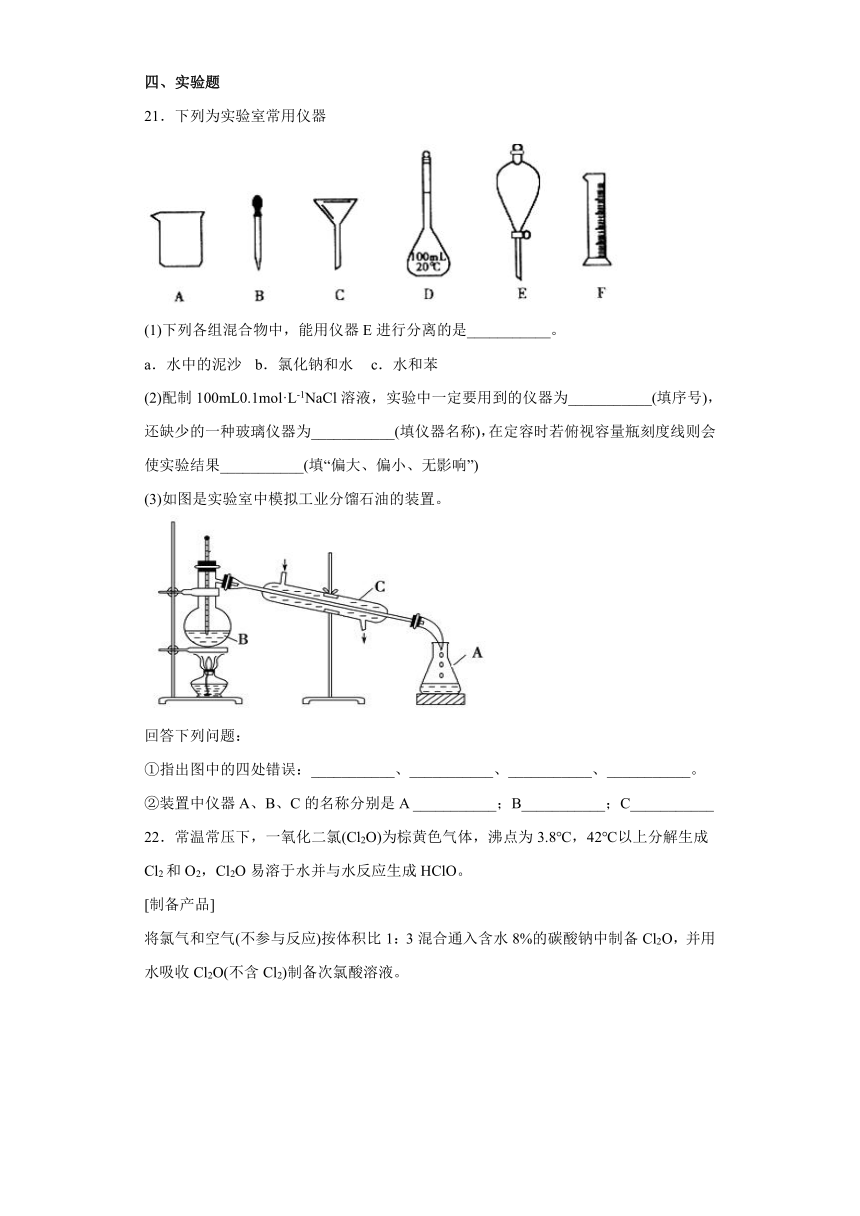
21.下列为实验室常用仪器
(1)下列各组混合物中,能用仪器E进行分离的是___________。
a.水中的泥沙 b.氯化钠和水 c.水和苯
(2)配制100mL0.1mol·L-1NaCl溶液,实验中一定要用到的仪器为___________(填序号),还缺少的一种玻璃仪器为___________(填仪器名称),在定容时若俯视容量瓶刻度线则会使实验结果___________(填“偏大、偏小、无影响”)
(3)如图是实验室中模拟工业分馏石油的装置。
回答下列问题:
①指出图中的四处错误:___________、___________、___________、___________。
②装置中仪器A、B、C的名称分别是A ___________;B___________;C___________
22.常温常压下,一氧化二氯(Cl2O)为棕黄色气体,沸点为3.8℃,42℃以上分解生成Cl2和O2,Cl2O易溶于水并与水反应生成HClO。
[制备产品]
将氯气和空气(不参与反应)按体积比1:3混合通入含水8%的碳酸钠中制备Cl2O,并用水吸收Cl2O(不含Cl2)制备次氯酸溶液。
(1)各装置的连接顺序为_______→______→_____→C→_____;(填字母)
(2)装置B中多孔球泡和搅拌棒的作用是_______;装置C的作用是______;
(3)制备Cl2O的化学方程式为________;
(4)此方法相对于用氯气直接溶于水制备次氯酸溶液的主要优点是_______;
(5)反应过程中,装置B需放在_______中:(选填“冷水”或“热水”)
[测定浓度]
(6)已知次氯酸可被FeSO4等物质还原。用下列实验方案测定装置E所得溶液中次氯酸的物质的量浓度:量取10 mL上述次氯酸溶液,并稀释至100 mL,再从中取出10.00 mL于锥形瓶中,并加入10.00 mL 0.8 mol/L的FeSO4溶液,充分反应后,用0.05000 mol/L的酸性KMnO4溶液滴定至终点,消耗KMnO4溶液24.00 mL,则原次氯酸的物质的量浓度为_______。(保留四位有效数字)
参考答案:
1.B
【详解】A.NCl3分子中含有的质子数是58,则0.1 mol NCl3中含有的质子数为5.8NA,A错误;
B.在反应2NCl3+3H2O=3HCl+N2↑+3HClO中,每反应产生3 mol HCl,转移6 mol电子,反应生成36.5 g HCl的物质的量是1 mol,则转移电子数为2NA,B正确;
C.N2中2个N原子形成共价三键,其中1个σ键,2个π键,标准状况下,2.24 LN2的物质的量是0.1 mol,因此其中含σ键数为0.1NA,C错误;
D.100 mL1 mol/LHClO中含有溶质的物质的量是n(HClO)=1 mol/L×0.1 L=0.1 mol,由于HClO是一元弱酸,主要以电解质分子存在,因此该溶液中离子数目远小于0.2NA,D错误;
故答案为B。
2.B
【详解】A.氢氧化钠易潮解变质,用滤纸称量NaOH固体时,会导致配制的溶液中氢氧化钠的物质的量偏小,配制的溶液浓度偏低,故A错误;
B.NaOH固体溶解时放热,导致溶液温度高,受热膨胀,没有冷却便进行定容会导致溶液体积偏小,浓度偏高,故B正确;
C.定容时仰视刻度线会导致溶液体积偏大,浓度偏低,故C错误;
D.将容量瓶中的溶液转移到试剂瓶的过程中,有少量溶液溅出,会导致所配溶液中溶质的物质的量偏少,浓度偏低,故D错误;
故答案选B。
3.C
【详解】A.制造指南针的磁性物质是Fe3O4,故A错误;
B.苗族银饰和景德镇彩瓷是我国特有的文化产品,苗族银饰的主要成分为金属材料,而景德镇彩瓷的主要成分为无机非金属材料,故B错误;
C.二氧化碳与氢气合成淀粉,可以将二氧化碳回收利用并转化为有机物,因此人工合成淀粉不仅有利于解决人类的温饱问题,也有利于实现“碳中和”,故C正确;
D.硅属于半导体材料,芯片的主要成分为晶体Si,故D错误;
故选C。
4.D
【详解】A.铁丝在氯气中点燃,剧烈燃烧,产生棕褐色烟,产物为FeCl3,溶于水,溶液呈棕黄色,故A正确;
B.钠在空气中加热,先熔化成银白色小球,然后燃烧,发出黄色火焰,生成过氧化钠,为淡黄色固体,故B正确;
C.钠放入氯化铁溶液后,钠与水反应生成氢氧化钠和氢气,则现象为钠浮在水面,迅速游动,嘶嘶作响;生成的氢氧化钠与氯化铁反应生成氢氧化铁,氢氧化铁为红褐色,难溶于水,则现象为溶液中出现红褐色沉淀,故C正确;
D.过氧化钠与水反应生成氢氧化钠和氧气,中间产物具有漂白性,则滴加酚酞,溶液先变红后褪色,故D错误;
答案选D。
5.D
【详解】A.未强调标准状况下,无法计算出含有的氯原子数目,A错误;
B.苯中不含碳碳双键,B错误;
C.乙酸与乙醇生成乙酸乙酯为可逆反应,C错误;
D.每个及中含有1对共用电子对,中含有2对共用电子对,28g乙烯中共用电子对数目为,28g丙烯中共用电子对数目为,则28g混合气体中含共用电子对数目为,D正确;
故答案为:D。
6.D
【详解】SO2和SO3的摩尔质量分别是64g/mol、80g/mol,根据n=m÷M知,相同质量时n与M成反比,所以二者的物质的量之比=80g/mol:64g/mol=5:4,则
A.根据N=nNA知,其分子数与n成正比,所以分子个数之比=5:4,每个分子中都含有一个S原子,所以S原子总数=5:4,故A错误;
B.根据N=nNA知,其分子数与n成正比,所以分子个数之比=5:4,二氧化硫分子中含有两个O原子、三氧化硫分子中含有3个O原子,所以O原子总数=(5×2):(4×3)=5:6,故B错误;
C.二氧化硫和三氧化硫的物质的量之比为5:4,每个分子中都含有一个S原子,所以S元素的物质的量之比为5:4,则根据m=nM知,S元素的质量与n成正比,所以S元素的质量之比=5:4,故C错误;
D.二氧化硫分子中含有两个O原子、三氧化硫分子中含有3个O原子,所以二氧化硫、三氧化硫中O原子的物质的量之比=(5×2):(4×3)=5:6,根据m=nM知,O元素的质量之比等于物质的量之比,所以O元素质量之比=5:6,故D正确;
故选D。
7.C
【分析】n(O2)=,n(O3)=。
【详解】A.结合分析可知二者分子数分别为NA,NA,即二者分子数不相同,A错误;
B.标准状况下,气体的体积之比等于物质的量之比,由分析可知,物质的量不相等,故二者体积不相同,B错误;
C.1gO2中n(原子)=×2mol=mol,1gO3中n(原子)=×3mol=mol,故二者所含原子数相同,C正确;
D.由A可知,1gO3中所含分子数较少,D错误。
答案选C。
8.B
【详解】A.将过氧化钠投入到饱和CuSO4溶液,首先发生反应:2Na2O2+2H2O=4NaOH+O2↑,产生的NaOH再与溶质CuSO4发生反应:CuSO4+2NaOH=Cu(OH)2↓+Na2SO4,因此产生的是Cu(OH)2蓝色沉淀,A不符合题意;
B.将过氧化钠投入到饱和石灰水, 发生反应:2Na2O2+2H2O=4NaOH+O2↑,消耗溶剂水,导致Ca(OH)2溶解量减少,当恢复至原温度时,会有Ca(OH)2白色物质析出,B符合题意;
C.生理盐水是0.9%的NaCl水溶液,向其中加入过氧化钠,发生反应:2Na2O2+2H2O=4NaOH+O2↑,消耗溶剂水,使溶液浓度增大,但由于溶液浓度较小,反应后仍然是不饱和溶液,因此无沉淀析出,C不符合题意;
D.将过氧化钠投入稀盐酸中,会发生反应:2Na2O2+4HCl=4NaCl+2H2O+O2↑,无沉淀析出,D不符合题意;
故合理选项是B。
9.A
【详解】A.过氧化钠具有强氧化性,故过氧化钠与二氧化硫发生氧化还原反应可生成硫酸钠,A正确;
B.明矾不具有杀菌消毒作用,但是可以用作净水剂,B错误;
C.用覆铜板制作印刷电路板,是利用过量的饱和氯化铁溶液与镀铜电路板上金属铜反应,然后用过量铁粉把生成的氯化铜置换得到金属铜。同时把过量的氯化铁溶液转变为氯化亚铁溶液,最后,进行过滤分离出金属铜而回收铜,并把滤液氯化亚铁再转化为氯化铁溶液循环利用,C错误;
D.合金的熔点不一定比各成分金属的低,铪是具有银白色光泽的稀有金属,其熔点为2227℃,而碳化铪为4160℃,D错误;
故选A。
10.B
【详解】A.1个D3O+中含11个中子,22 g D3O+中含有的中子数为11NA,故A错误;
B. 分子中P-P键为非极性键,1 mol P4S3含有非极性键的数目为3NA,故B正确;
C.草酸是弱酸,1 L0.1 mol/L草酸(H2C2O4)溶液中含有H+的数目小于0.2NA,故C错误;
D.11.2 L(标准状况)氧气的物质的量是0.5mol,与足量钠反应,若生成氧化钠,转移2mol电子,若生成过氧化钠,转移1mol电子,故D错误;
选B。
11.A
【详解】Al和稀盐酸、NaOH溶液反应方程式分别为2Al+6HCl=2AlCl3+3H2↑、2Al+2NaOH+2H2O=2NaAlO2+3H2↑,Al与足量稀盐酸、NaOH溶液反应时生成相同条件下的同体积氢气,说明生成氢气的物质的量相等,假设都是生成3mol氢气,消耗稀盐酸6mol、消耗NaOH溶液2mol,所以反应中消耗的HCl和NaOH的物质的量之比=6mol:2mol=3:1,故答案为A。
12.B
【详解】A.常温常压下,H2O为液态,不能用气体的摩尔体积计算物质的量,选项A错误;
B.二氧化氮和四氧化二氮的最简式相同,都为NO2,则92g NO2中含有的原子个数为×3×NAmol—1=6NA,选项B正确;
C.标准状况下,22.4L氦气的物质的量为1mol,氦气为单原子分子,1mol22.4L氦气含有所含的原子数为NA,选项C错误;
D.18 g H2O的物质的量为=1mol,每个水分子中含有10个电子,所以18 g H2O含有10mol电子,个数为10NA,选项D错误;
答案选B。
13.A
【详解】同时研究钠和不锈钢的稳定性,对二者性质进行比较,即采用比较法,通过做实验研究二者稳定性,故采用了实验法,因此②④符合题意,故选A。
14.D
【详解】A.钠和盐酸的反应方程式为:2Na+2HCl═2NaCl+H2↑,根据方程式知,溶液质量增加,溶液增加的质量=m(Na)-m(H2),故A不选;
B.钠与硫酸钾溶液的反应实质是钠与水的反应,钠和水的反应方程式为:2Na+2H2O═2NaOH+H2↑,所以溶液质量增加,溶液增加的质量=m(Na)-m(H2),故B不选;
C.钠和稀NaOH溶液中的水反应的方程式为:2Na+2H2O═2NaOH+H2↑,所以溶液质量增加,溶液增加的质量=m(Na)-m(H2),故C不选;
D.钠和水的反应方程式为:2Na+2H2O═2NaOH+H2↑,水量减少,氢氧化钠会析出,所以溶液质量减少,故D选;
答案选D。
15.A
【详解】A.氯气和铁化合反应得到氯化铁得不到氯化亚铁,A符合题意;
B.氯气和铁化合反应得到氯化铁,B不符合题意;
C.氯气和铜化合反应得到氯化铜,C不符合题意;
D.氯气和钠化合反应得到氯化钠,D不符合题意;
故选A。
16.(1) 5.6L 0.75NA
(2) 0.01mol 98g/mol 32
【详解】(1)0.25mol在标准状况下的体积为0.25mol×22.4L/mol=5.6L;0.25mol含有的原子数目为0.25mol×3×NA=0.75NA;
(2)0.98g物质中的含有个分子,则该物质的物质的量为=0.01mol,的摩尔质量为=98g/mol,A的相对原子质量为98-1×2-16×4=32。
17.(1)B
(2)蒸发浓缩、降温结晶
(3) 19.6 除去溶解在水中的氧气 偏低
(4)0.16
【解析】(1)
是由亚铁离子和硫酸根离子构成的化合物,属于硫酸盐、亚铁盐,硫酸为含氧酸,故属于含氧酸盐,由溶解度表格可知,硫酸亚铁易溶于水,属于可溶性盐;
故选B;
(2)
由溶解度表格可知,硫酸亚铁铵晶体在低温下溶解度较小,从混合液中获取该晶体的操作是蒸发浓缩、降温结晶、过滤、洗涤、干燥。
(3)
配制溶液一定要选择合适的容量瓶,一般容量瓶的规格有100mL,250mL,500mL,1000mL,通常选择大于等于溶液体积的容量瓶;需要使用480mL0.1mol/L硫酸亚铁铵溶液,则实验中需要使用500mL的容量瓶,需要称取0.5L×0.1mol/L×392g/mol=19.6 g硫酸亚铁铵晶体。配制时所用的水要先用蒸馏法处理,其目的是除去溶解在水中的氧气,防止亚铁离子被氧化为铁离子;若定容时仰视容量瓶刻度线,导致溶液体积偏大,所配溶液浓度偏低;
(4)
取20mL所配溶液与足量NaOH溶液反应,得到氢氧化亚铁沉淀,氢氧化亚铁被空气中氧气氧化为氢氧化铁,灼烧氢氧化铁生成氧化铁,根据铁元素守恒可知,最终可得到0.02L×0.1mol/L××160g/mol=0.16g固体。
18.(1)Al2O3+2OH-=2+H2O
(2)NaAlO2+CO2+2H2O=Al(OH)3↓+NaHCO3
(3)Al2O3+6H+=2Al3++3H2O
(4) Na2O2 Na2CO3 NaOH(或NaCl) NaHCO3
(5) Na2CO3+Ba(OH)2=BaCO3↓+2NaOH(或Na2CO3+2HCl=2NaCl+CO2↑+H2O)(答案合理即可) Na2CO3+CO2+H2O=2NaHCO3 2NaHCO3Na2CO3+CO2↑+H2O
【解析】(1)
铝土矿的主要成分为Al2O3,为两性氧化物,与氢氧化钠反应离子方程式为:Al2O3+2OH-=2+H2O;
(2)
为保证把偏铝酸钠溶液种的铝元素完全转化为氢氧化铝沉淀,应通入足量二氧化碳气体,发生的化学反应为:NaAlO2+CO2+2H2O=Al(OH)3↓+NaHCO3;
(3)
铝土矿的主要成分为Al2O3,为两性氧化物,即可与氢氧化钠反应又可与盐酸反应,故若第①步加入的是盐酸,则发生反应的离子方程式:Al2O3+6H+=2Al3++3H2O;
(4)
根据A为金属,B为淡黄色固体粉末,可知A为Na,B为Na2O2,前后联系,可知D、E分别为Na2O、NaCl、NaOH中的一种,由Na2O2的性质可知,C必为Na2CO3,则F为NaHCO3,由Na2CO3→E可知,E为NaOH或NaCl,由D→C知,E为NaOH时,D只能为Na2O;当E为NaCl时,D可以为Na2O或NaOH;
(5)
根据小问(4)可知,C为Na2CO3、E为NaOH或NaCl,故 C→E 反应方程式为:Na2CO3+Ba(OH)2=BaCO3↓+2NaOH(或Na2CO3+2HCl=2NaCl+CO2↑+H2O)(答案合理即可);F为NaHCO3,故C→F反应方程式为:Na2CO3+CO2+H2O=2NaHCO3;F→C反应方程式为:2NaHCO3Na2CO3+CO2↑+H2O。
19. 0.2 4.48 4 4.4
【详解】,标况下,气体摩尔体积为22.4L/mol,故体积为0.2mol×22.4L/mol=44.8L。HCl的物质的量浓度,盐酸与碳酸钠反应:,0.2mol的HCl可以生成0.1mol二氧化碳,故溶液增重的质量即0.1mol二氧化碳的质量为。
20.0.84
【详解】碳酸氢钠受热分解的化学方程式为:2NaHCO3Na2CO3+H2O+CO2↑,产生的气体通过浓硫酸吸水,得到的气体为二氧化碳,过氧化钠与二氧化碳反应,方程式为:2Na2O2+2CO2=2Na2CO3+O2,由方程式可知,每消耗1mol二氧化碳,过氧化钠增重28g,所以当Na2O2增重0.14g时,说明消耗了0.005mol二氧化碳,碳酸氢钠受热分解生成了0.005mol二氧化碳,则碳酸氢钠的物质的量为0.005mol2=0.01mol,碳酸氢钠的质量为0.01mol84g/mol=0.84g。
21. c ABD 玻璃棒 偏大 温度计水银球位置不在支管口处 未加石棉网 未加沸石 冷凝水上进下出 锥形瓶 蒸馏烧瓶 冷凝管
【详解】(1)仪器E为分液漏斗,常用于萃取分液,则:
a.水中的泥沙为固液不相溶混合物,用过滤的方法进行分离,需要用到的仪器为烧杯、普通漏斗和玻璃棒,a不符合;
b.氯化钠和水可采用蒸发结晶的方法进行分离,需要用到的仪器为蒸发皿、玻璃棒,b不符合;
c.水和苯为互不相溶的液体,可采用分液的方法进行分离,需要用到分液漏斗,c符合;
故答案选c;
(2)配制100mL0.1mol·L-1NaCl溶液,要用到的仪器有烧杯、玻璃棒、100mL的容量瓶、胶头滴管和托盘天平等,故选ABD,还缺少的玻璃仪器是玻璃棒,在定容时若俯视容量瓶刻度线,使得最终溶液体积偏小,则浓度偏大;
(3)①该实验装置为蒸馏装置,图中共有以下4点错误:温度计水银球位置不在支管口处、未加石棉网、未加沸石、冷凝水上进下出;
②根据仪器结构可知,A为锥形瓶,B为蒸馏烧瓶,C为冷凝管。
22. A D B E 增大反应物接触面积,加快反应速率,使反应充分进行 除去Cl2O中的Cl2 2Cl2+Na2CO3═Cl2O+2NaCl+CO2(或2Cl2+Na2CO3+H2O═Cl2O+2NaCl+2NaHCO3) 制得的次氯酸溶液纯度较高,浓度较大 冷水 1.000mol/L
【分析】根据实验目的,将氯气和空气(不参与反应)按体积比1:3混合通入含水8%的碳酸钠中制备Cl2O,并用水吸收Cl2O(不含Cl2)制备次氯酸溶液,应先用装置A制备Cl2,再通过装置D除去混合气体中的HCl气体,同时混入空气,将混合气体通入装置B,在装置B中发生制备Cl2O的反应;然后将制取的Cl2O气体先通入装置C,以除去Cl2等杂质气体,最后通过装置E制取次氯酸溶液,以此解答。
【详解】(1)根据实验目的,将氯气和空气(不参与反应)按体积比1:3混合通入含水8%的碳酸钠中制备Cl2O,并用水吸收Cl2O(不含Cl2)制备次氯酸溶液,应先用装置A制备Cl2,再通过装置D除去混合气体中的HCl气体,同时混入空气,将混合气体通入装置B,在装置B中发生制备Cl2O的反应;然后将制取的Cl2O气体先通入装置C,以除去Cl2等杂质气体,最后通过装置E制取次氯酸溶液,装置连接顺序为:A→D→B→C→E,故答案为:A;D;B;E;
(2)多孔球泡和搅拌棒均能使反应物充分接触,增大反应物接触面积,加快反应速率,使反应充分进行;装置B中生成Cl2O的同时还会有多余的Cl2逸出,而Cl2是非极性分子,易溶于非极性溶剂四氯化碳,因此此处装置C使用足量的四氯化碳将Cl2吸收,故答案为:增大反应物接触面积,加快反应速率,使反应充分进行;除去Cl2O中的Cl2;
(3)已知空气不参与反应,则制取Cl2O以Cl2和Na2CO3为反应物,发生歧化反应,其中氯元素从0价变为+1价和 1价,反应的化学方程式为:2Cl2+Na2CO3═Cl2O+2NaCl+CO2(或2Cl2+Na2CO3+H2O═Cl2O+2NaCl+2NaHCO3),故答案为:2Cl2+Na2CO3═Cl2O+2NaCl+CO2(或2Cl2+Na2CO3+H2O═Cl2O+2NaCl+2NaHCO3);
(4)Cl2O与水反应的化学方程式为:Cl2O+H2O=2HClO,Cl2和水反应的化学方程式为:Cl2+H2O=HCl+HClO,Cl2O和水反应只生成HClO且反应不可逆,氯气和水反应除了生成HClO还生成HCl,并且反应可逆,所以用Cl2O与水反应制备次氯酸溶液相对于用氯气溶于水制备次氯酸溶液的主要优点是用Cl2O与水反应制备次氯酸溶液时制得次氯酸溶液纯度较高、浓度也较大,故答案为:制得的次氯酸溶液纯度较高,浓度较大;
(5)由题可知:Cl2O在42℃以上会分解生成Cl2和O2,故为防止反应放热后温度过高导致Cl2O分解,装置B需放在冷水中,故答案为:冷水;
(6)10.00mL 0.80mol L 1的FeSO4溶液中,n(FeSO4)=0.80mol/L×0.01L=0.008mol,24.00mL0.050 00mol L 1的酸性KMnO4溶液中,n(KMnO4)=0.050mol/L×0.024L=0.0012mol,根据反应MnO+5Fe2++8H+=5Fe3++Mn2++4H2O可知,0.0012mol高锰酸钾消耗硫酸亚铁的物质的量为:0.0012mol×5=0.006mol,则稀释后的10.00mLHClO溶液消耗硫酸亚铁的物质的量为:0.008mol 0.006mol=0.002mol,根据反应HClO+2Fe2++H+=2Fe3++Cl +H2O可知,稀释后10.00mLHClO溶液中n(HClO)=×0.002mol=0.001mol,原10mL次氯酸溶液中n(HClO)=0.001mol×=0.01mol,其浓度为:=1.000mol/L,故答案为:1.000mol/L。
一、单选题
1.三氯化氮(NCl3)易与水反应:2NCl3+3H2O=3HCl+N2↑+3HClO。若NA代表阿伏加德罗常数的值。下列说法正确的是( )
A.0.1 mol NCl3中质子数为6.5NA
B.每生成36.5 g HCl转移电子数为2NA
C.标准状况下,2.24 LN2中含σ键数为0.2NA
D.100 mL1 mol/LHClO溶液中阴、阳离子总数为0.2NA
2.实验室利用NaOH固体配制480mL0.1mol·L-1的NaOH溶液时,以下操作会使溶液的浓度偏高的是
A.用滤纸称量NaOH固体
B.溶解后没有冷却便进行定容
C.定容时仰视刻度线
D.将容量瓶中的溶液转移到试剂瓶的过程中,不慎有少量溶液溅出
3.化学科学与技术在宇宙探索、改进生活、改善环境与促进发展方面均发挥着关键性的作用。下列说法正确的是
A.指南针是我国古代的四大发明之一,制造指南针的磁性物质是FeO
B.湖南苗族银饰和江西景德镇彩瓷是我国特有的文化产品,其主要成分均为金属材料
C.人工合成淀粉不仅有利于解决人类的温饱问题,也有利于实现“碳中和”
D.北斗导航专用ASIC硬件结合国产处理器打造出的一颗真正意义的“中国芯”,其主要成分为SiO2
4.下列实验现象描述不正确的是
A.铁丝在氯气中点燃,剧烈燃烧,产生棕褐色烟,燃烧后产物溶于水,溶液呈棕黄色
B.钠在空气中加热,先熔化成银白色小球,然后燃烧,发出黄色火焰,生成淡黄色固体
C.钠放入氯化铁溶液后,浮在水面,迅速游动,嘶嘶作响,溶液中出现红褐色沉淀
D.将1~2mL水滴入盛有1~2g过氧化钠固体的试管中,滴加酚酞,溶液变红
5.设为阿伏加德罗常数的值,下列叙述正确的是
A.22.4L中含氯原子数目为
B.7.8g苯中含碳碳双键数日为3
C.1mol乙酸与足量乙醇充分反应,所得乙酸乙酯分子数目为
D.28g乙烯和丙烯的混合气体中含共用电子对数目为6
6.相同质量的SO2和SO3,下列关系正确的是
A.含硫原子个数比为1∶1 B.含氧原子个数比为2∶3
C.含硫元素质量比为4∶5 D.含氧元素质量比为5∶6
7.1gO2和1gO3中
A.所含分子数相同 B.在标准状况下的体积相同
C.所含原子数相同 D.1gO3中所含分子数较多
8.将过氧化钠投入下列溶液中,恢复至原温度时,会有白色物质析出的是( )
A.饱和CuSO4溶液 B.饱和石灰水 C.生理盐水 D.稀盐酸
9.下列说法正确的是
A.过氧化钠与二氧化硫反应可生成硫酸钠
B.明矾具有很强的杀菌消毒作用,因此可以用作净水剂
C.用覆铜板制作印刷电路板就是利用铁单质还原性比铜强的原理
D.合金的熔点一定比各成分金属的低
10.NA阿伏加德罗常数的值。下列叙述正确的是
A.22 g D3O+中含有的中子数为10NA
B.1 mol P4S3()分子中含有非极性键的数目为3NA
C.1 L0.1 mol/L草酸(H2C2O4)溶液中含有H+的数目为0.2NA
D.11.2 L(标准状况)氧气与足量钠反应,转移的电子数一定为NA
11.铝分别与足量的稀盐酸和氢氧化钠溶液反应,当两个反应放出的气体在相同状况下体积相同时,反应中消耗的HCl和NaOH的物质的量之比为
A.3:1 B.1:1 C.2:1 D.1:2
12.设NA表示阿伏伽德罗常数,下列叙述中正确的是
A.常温常压下,11.2 L H2O所含原子数为1.5NA
B.常温常压下,92gNO2 和N2O4混合气体中含有原子总数为6NA
C.标准状况下,22.4 L氦气中所含原子数为2NA
D.常温常压下,18gH2O中含有电子数为3NA
13.某学生运用所学知识研究钠的性质:将一粒金属钠和一块不锈钢片分别放在表面皿中,研究它们在空气中的稳定性。该学生采用的研究方法是
①假说法 ②实验法 ③分类法 ④比较法
A.②④ B.①②③④ C.①③ D.①②
14.将金属钠分别投入下列物质的溶液中,有气体放出且溶液质量减轻的是( )
A.HCl B.K2SO4
C.稀NaOH溶液 D.饱和NaOH溶液
15.下列化合物中一般不能通过单质与氯气直接化合制得的是
A.FeCl2 B.FeCl3 C.CuCl2 D.NaCl
二、填空题
16.完成下列填空:
(1)0.25mol 在标准状况下的体积为_________,含有的原子数目为_________。
(2)0.98g物质中的含有个分子,则该物质的物质的量为_________,的摩尔质量为_________,A的相对原子质量为_________。
17.硫酸亚铁铵晶体的化学式为,是常用的还原剂,实验室制备它的原理为.已知几种盐的溶解度(g)如下表所示:
温度/℃ 0 10 20 30 40 50
15.6 20.5 26.5 32.9 40.2 48.6
70.6 73.0 75.4 78.0 81.63 84.4
12.5 17.2 33.0 40.0
回答下列问题:
(1)下列有关的说法错误的是_______(填序号)。A.是硫酸盐 B.是铁盐 C.是含氧酸盐 D.是可溶性盐
(2)实验室制备硫酸亚铁铵晶体时,从混合液中获取该晶体的操作是_______、过滤、洗涤、干燥。
(3)若某次实验中需要使用480mL0.1mol/L硫酸亚铁铵溶液,则实验中需要称取_______g硫酸亚铁铵晶体。配制时所用的水要先用蒸馏法处理,其目的是_______。若定容时仰视容量瓶刻度线,则所配溶液浓度_______(填“偏高”或“偏低”)。
(4)取20mL所配溶液与足量NaOH溶液反应,将所得沉淀充分放置一段时间后过滤、洗涤、灼烧,最终可得到_______g固体。
18.Ⅰ、铝土矿(主要成分为Al2O3,含有少量杂质)是提取铝的原料。提取铝的工艺流程如下:
(1)请用离子方程式表示以上工艺流程中第①步反应:___________。
(2)写出以上工艺流程中第③步反应的化学方程式:___________。
(3)若第①步加入的是盐酸,则发生反应的离子方程式为___________。
Ⅱ、下图为几种物质的转化关系,其中A为金属,B为淡黄色固体粉末,每一物质均含有A元素。
(4)写出下列物质的化学式:
B___________,C___________,E___________,F___________。
(5)写出下列各步反应的化学方程式:
C→E___________;
C→F___________;
F→C___________。
三、计算题
19.含有个HCl分子,物质的量是_______mol,在标准状况下的体积是_______升,溶于水得到50mL盐酸溶液,物质的量浓度是_______,加入足量的粉末,生成的全部通入足量NaOH溶液中,溶液增重_______克。
20.反应完成后得到的混合物处理得到固体NaHCO3和滤液,对固体NaHCO3充分加热,产生的气体先通过足量浓硫酸,再通过足量Na2O2,Na2O2增重0.14g,则固体NaHCO3的质量为_______g。
四、实验题
21.下列为实验室常用仪器
(1)下列各组混合物中,能用仪器E进行分离的是___________。
a.水中的泥沙 b.氯化钠和水 c.水和苯
(2)配制100mL0.1mol·L-1NaCl溶液,实验中一定要用到的仪器为___________(填序号),还缺少的一种玻璃仪器为___________(填仪器名称),在定容时若俯视容量瓶刻度线则会使实验结果___________(填“偏大、偏小、无影响”)
(3)如图是实验室中模拟工业分馏石油的装置。
回答下列问题:
①指出图中的四处错误:___________、___________、___________、___________。
②装置中仪器A、B、C的名称分别是A ___________;B___________;C___________
22.常温常压下,一氧化二氯(Cl2O)为棕黄色气体,沸点为3.8℃,42℃以上分解生成Cl2和O2,Cl2O易溶于水并与水反应生成HClO。
[制备产品]
将氯气和空气(不参与反应)按体积比1:3混合通入含水8%的碳酸钠中制备Cl2O,并用水吸收Cl2O(不含Cl2)制备次氯酸溶液。
(1)各装置的连接顺序为_______→______→_____→C→_____;(填字母)
(2)装置B中多孔球泡和搅拌棒的作用是_______;装置C的作用是______;
(3)制备Cl2O的化学方程式为________;
(4)此方法相对于用氯气直接溶于水制备次氯酸溶液的主要优点是_______;
(5)反应过程中,装置B需放在_______中:(选填“冷水”或“热水”)
[测定浓度]
(6)已知次氯酸可被FeSO4等物质还原。用下列实验方案测定装置E所得溶液中次氯酸的物质的量浓度:量取10 mL上述次氯酸溶液,并稀释至100 mL,再从中取出10.00 mL于锥形瓶中,并加入10.00 mL 0.8 mol/L的FeSO4溶液,充分反应后,用0.05000 mol/L的酸性KMnO4溶液滴定至终点,消耗KMnO4溶液24.00 mL,则原次氯酸的物质的量浓度为_______。(保留四位有效数字)
参考答案:
1.B
【详解】A.NCl3分子中含有的质子数是58,则0.1 mol NCl3中含有的质子数为5.8NA,A错误;
B.在反应2NCl3+3H2O=3HCl+N2↑+3HClO中,每反应产生3 mol HCl,转移6 mol电子,反应生成36.5 g HCl的物质的量是1 mol,则转移电子数为2NA,B正确;
C.N2中2个N原子形成共价三键,其中1个σ键,2个π键,标准状况下,2.24 LN2的物质的量是0.1 mol,因此其中含σ键数为0.1NA,C错误;
D.100 mL1 mol/LHClO中含有溶质的物质的量是n(HClO)=1 mol/L×0.1 L=0.1 mol,由于HClO是一元弱酸,主要以电解质分子存在,因此该溶液中离子数目远小于0.2NA,D错误;
故答案为B。
2.B
【详解】A.氢氧化钠易潮解变质,用滤纸称量NaOH固体时,会导致配制的溶液中氢氧化钠的物质的量偏小,配制的溶液浓度偏低,故A错误;
B.NaOH固体溶解时放热,导致溶液温度高,受热膨胀,没有冷却便进行定容会导致溶液体积偏小,浓度偏高,故B正确;
C.定容时仰视刻度线会导致溶液体积偏大,浓度偏低,故C错误;
D.将容量瓶中的溶液转移到试剂瓶的过程中,有少量溶液溅出,会导致所配溶液中溶质的物质的量偏少,浓度偏低,故D错误;
故答案选B。
3.C
【详解】A.制造指南针的磁性物质是Fe3O4,故A错误;
B.苗族银饰和景德镇彩瓷是我国特有的文化产品,苗族银饰的主要成分为金属材料,而景德镇彩瓷的主要成分为无机非金属材料,故B错误;
C.二氧化碳与氢气合成淀粉,可以将二氧化碳回收利用并转化为有机物,因此人工合成淀粉不仅有利于解决人类的温饱问题,也有利于实现“碳中和”,故C正确;
D.硅属于半导体材料,芯片的主要成分为晶体Si,故D错误;
故选C。
4.D
【详解】A.铁丝在氯气中点燃,剧烈燃烧,产生棕褐色烟,产物为FeCl3,溶于水,溶液呈棕黄色,故A正确;
B.钠在空气中加热,先熔化成银白色小球,然后燃烧,发出黄色火焰,生成过氧化钠,为淡黄色固体,故B正确;
C.钠放入氯化铁溶液后,钠与水反应生成氢氧化钠和氢气,则现象为钠浮在水面,迅速游动,嘶嘶作响;生成的氢氧化钠与氯化铁反应生成氢氧化铁,氢氧化铁为红褐色,难溶于水,则现象为溶液中出现红褐色沉淀,故C正确;
D.过氧化钠与水反应生成氢氧化钠和氧气,中间产物具有漂白性,则滴加酚酞,溶液先变红后褪色,故D错误;
答案选D。
5.D
【详解】A.未强调标准状况下,无法计算出含有的氯原子数目,A错误;
B.苯中不含碳碳双键,B错误;
C.乙酸与乙醇生成乙酸乙酯为可逆反应,C错误;
D.每个及中含有1对共用电子对,中含有2对共用电子对,28g乙烯中共用电子对数目为,28g丙烯中共用电子对数目为,则28g混合气体中含共用电子对数目为,D正确;
故答案为:D。
6.D
【详解】SO2和SO3的摩尔质量分别是64g/mol、80g/mol,根据n=m÷M知,相同质量时n与M成反比,所以二者的物质的量之比=80g/mol:64g/mol=5:4,则
A.根据N=nNA知,其分子数与n成正比,所以分子个数之比=5:4,每个分子中都含有一个S原子,所以S原子总数=5:4,故A错误;
B.根据N=nNA知,其分子数与n成正比,所以分子个数之比=5:4,二氧化硫分子中含有两个O原子、三氧化硫分子中含有3个O原子,所以O原子总数=(5×2):(4×3)=5:6,故B错误;
C.二氧化硫和三氧化硫的物质的量之比为5:4,每个分子中都含有一个S原子,所以S元素的物质的量之比为5:4,则根据m=nM知,S元素的质量与n成正比,所以S元素的质量之比=5:4,故C错误;
D.二氧化硫分子中含有两个O原子、三氧化硫分子中含有3个O原子,所以二氧化硫、三氧化硫中O原子的物质的量之比=(5×2):(4×3)=5:6,根据m=nM知,O元素的质量之比等于物质的量之比,所以O元素质量之比=5:6,故D正确;
故选D。
7.C
【分析】n(O2)=,n(O3)=。
【详解】A.结合分析可知二者分子数分别为NA,NA,即二者分子数不相同,A错误;
B.标准状况下,气体的体积之比等于物质的量之比,由分析可知,物质的量不相等,故二者体积不相同,B错误;
C.1gO2中n(原子)=×2mol=mol,1gO3中n(原子)=×3mol=mol,故二者所含原子数相同,C正确;
D.由A可知,1gO3中所含分子数较少,D错误。
答案选C。
8.B
【详解】A.将过氧化钠投入到饱和CuSO4溶液,首先发生反应:2Na2O2+2H2O=4NaOH+O2↑,产生的NaOH再与溶质CuSO4发生反应:CuSO4+2NaOH=Cu(OH)2↓+Na2SO4,因此产生的是Cu(OH)2蓝色沉淀,A不符合题意;
B.将过氧化钠投入到饱和石灰水, 发生反应:2Na2O2+2H2O=4NaOH+O2↑,消耗溶剂水,导致Ca(OH)2溶解量减少,当恢复至原温度时,会有Ca(OH)2白色物质析出,B符合题意;
C.生理盐水是0.9%的NaCl水溶液,向其中加入过氧化钠,发生反应:2Na2O2+2H2O=4NaOH+O2↑,消耗溶剂水,使溶液浓度增大,但由于溶液浓度较小,反应后仍然是不饱和溶液,因此无沉淀析出,C不符合题意;
D.将过氧化钠投入稀盐酸中,会发生反应:2Na2O2+4HCl=4NaCl+2H2O+O2↑,无沉淀析出,D不符合题意;
故合理选项是B。
9.A
【详解】A.过氧化钠具有强氧化性,故过氧化钠与二氧化硫发生氧化还原反应可生成硫酸钠,A正确;
B.明矾不具有杀菌消毒作用,但是可以用作净水剂,B错误;
C.用覆铜板制作印刷电路板,是利用过量的饱和氯化铁溶液与镀铜电路板上金属铜反应,然后用过量铁粉把生成的氯化铜置换得到金属铜。同时把过量的氯化铁溶液转变为氯化亚铁溶液,最后,进行过滤分离出金属铜而回收铜,并把滤液氯化亚铁再转化为氯化铁溶液循环利用,C错误;
D.合金的熔点不一定比各成分金属的低,铪是具有银白色光泽的稀有金属,其熔点为2227℃,而碳化铪为4160℃,D错误;
故选A。
10.B
【详解】A.1个D3O+中含11个中子,22 g D3O+中含有的中子数为11NA,故A错误;
B. 分子中P-P键为非极性键,1 mol P4S3含有非极性键的数目为3NA,故B正确;
C.草酸是弱酸,1 L0.1 mol/L草酸(H2C2O4)溶液中含有H+的数目小于0.2NA,故C错误;
D.11.2 L(标准状况)氧气的物质的量是0.5mol,与足量钠反应,若生成氧化钠,转移2mol电子,若生成过氧化钠,转移1mol电子,故D错误;
选B。
11.A
【详解】Al和稀盐酸、NaOH溶液反应方程式分别为2Al+6HCl=2AlCl3+3H2↑、2Al+2NaOH+2H2O=2NaAlO2+3H2↑,Al与足量稀盐酸、NaOH溶液反应时生成相同条件下的同体积氢气,说明生成氢气的物质的量相等,假设都是生成3mol氢气,消耗稀盐酸6mol、消耗NaOH溶液2mol,所以反应中消耗的HCl和NaOH的物质的量之比=6mol:2mol=3:1,故答案为A。
12.B
【详解】A.常温常压下,H2O为液态,不能用气体的摩尔体积计算物质的量,选项A错误;
B.二氧化氮和四氧化二氮的最简式相同,都为NO2,则92g NO2中含有的原子个数为×3×NAmol—1=6NA,选项B正确;
C.标准状况下,22.4L氦气的物质的量为1mol,氦气为单原子分子,1mol22.4L氦气含有所含的原子数为NA,选项C错误;
D.18 g H2O的物质的量为=1mol,每个水分子中含有10个电子,所以18 g H2O含有10mol电子,个数为10NA,选项D错误;
答案选B。
13.A
【详解】同时研究钠和不锈钢的稳定性,对二者性质进行比较,即采用比较法,通过做实验研究二者稳定性,故采用了实验法,因此②④符合题意,故选A。
14.D
【详解】A.钠和盐酸的反应方程式为:2Na+2HCl═2NaCl+H2↑,根据方程式知,溶液质量增加,溶液增加的质量=m(Na)-m(H2),故A不选;
B.钠与硫酸钾溶液的反应实质是钠与水的反应,钠和水的反应方程式为:2Na+2H2O═2NaOH+H2↑,所以溶液质量增加,溶液增加的质量=m(Na)-m(H2),故B不选;
C.钠和稀NaOH溶液中的水反应的方程式为:2Na+2H2O═2NaOH+H2↑,所以溶液质量增加,溶液增加的质量=m(Na)-m(H2),故C不选;
D.钠和水的反应方程式为:2Na+2H2O═2NaOH+H2↑,水量减少,氢氧化钠会析出,所以溶液质量减少,故D选;
答案选D。
15.A
【详解】A.氯气和铁化合反应得到氯化铁得不到氯化亚铁,A符合题意;
B.氯气和铁化合反应得到氯化铁,B不符合题意;
C.氯气和铜化合反应得到氯化铜,C不符合题意;
D.氯气和钠化合反应得到氯化钠,D不符合题意;
故选A。
16.(1) 5.6L 0.75NA
(2) 0.01mol 98g/mol 32
【详解】(1)0.25mol在标准状况下的体积为0.25mol×22.4L/mol=5.6L;0.25mol含有的原子数目为0.25mol×3×NA=0.75NA;
(2)0.98g物质中的含有个分子,则该物质的物质的量为=0.01mol,的摩尔质量为=98g/mol,A的相对原子质量为98-1×2-16×4=32。
17.(1)B
(2)蒸发浓缩、降温结晶
(3) 19.6 除去溶解在水中的氧气 偏低
(4)0.16
【解析】(1)
是由亚铁离子和硫酸根离子构成的化合物,属于硫酸盐、亚铁盐,硫酸为含氧酸,故属于含氧酸盐,由溶解度表格可知,硫酸亚铁易溶于水,属于可溶性盐;
故选B;
(2)
由溶解度表格可知,硫酸亚铁铵晶体在低温下溶解度较小,从混合液中获取该晶体的操作是蒸发浓缩、降温结晶、过滤、洗涤、干燥。
(3)
配制溶液一定要选择合适的容量瓶,一般容量瓶的规格有100mL,250mL,500mL,1000mL,通常选择大于等于溶液体积的容量瓶;需要使用480mL0.1mol/L硫酸亚铁铵溶液,则实验中需要使用500mL的容量瓶,需要称取0.5L×0.1mol/L×392g/mol=19.6 g硫酸亚铁铵晶体。配制时所用的水要先用蒸馏法处理,其目的是除去溶解在水中的氧气,防止亚铁离子被氧化为铁离子;若定容时仰视容量瓶刻度线,导致溶液体积偏大,所配溶液浓度偏低;
(4)
取20mL所配溶液与足量NaOH溶液反应,得到氢氧化亚铁沉淀,氢氧化亚铁被空气中氧气氧化为氢氧化铁,灼烧氢氧化铁生成氧化铁,根据铁元素守恒可知,最终可得到0.02L×0.1mol/L××160g/mol=0.16g固体。
18.(1)Al2O3+2OH-=2+H2O
(2)NaAlO2+CO2+2H2O=Al(OH)3↓+NaHCO3
(3)Al2O3+6H+=2Al3++3H2O
(4) Na2O2 Na2CO3 NaOH(或NaCl) NaHCO3
(5) Na2CO3+Ba(OH)2=BaCO3↓+2NaOH(或Na2CO3+2HCl=2NaCl+CO2↑+H2O)(答案合理即可) Na2CO3+CO2+H2O=2NaHCO3 2NaHCO3Na2CO3+CO2↑+H2O
【解析】(1)
铝土矿的主要成分为Al2O3,为两性氧化物,与氢氧化钠反应离子方程式为:Al2O3+2OH-=2+H2O;
(2)
为保证把偏铝酸钠溶液种的铝元素完全转化为氢氧化铝沉淀,应通入足量二氧化碳气体,发生的化学反应为:NaAlO2+CO2+2H2O=Al(OH)3↓+NaHCO3;
(3)
铝土矿的主要成分为Al2O3,为两性氧化物,即可与氢氧化钠反应又可与盐酸反应,故若第①步加入的是盐酸,则发生反应的离子方程式:Al2O3+6H+=2Al3++3H2O;
(4)
根据A为金属,B为淡黄色固体粉末,可知A为Na,B为Na2O2,前后联系,可知D、E分别为Na2O、NaCl、NaOH中的一种,由Na2O2的性质可知,C必为Na2CO3,则F为NaHCO3,由Na2CO3→E可知,E为NaOH或NaCl,由D→C知,E为NaOH时,D只能为Na2O;当E为NaCl时,D可以为Na2O或NaOH;
(5)
根据小问(4)可知,C为Na2CO3、E为NaOH或NaCl,故 C→E 反应方程式为:Na2CO3+Ba(OH)2=BaCO3↓+2NaOH(或Na2CO3+2HCl=2NaCl+CO2↑+H2O)(答案合理即可);F为NaHCO3,故C→F反应方程式为:Na2CO3+CO2+H2O=2NaHCO3;F→C反应方程式为:2NaHCO3Na2CO3+CO2↑+H2O。
19. 0.2 4.48 4 4.4
【详解】,标况下,气体摩尔体积为22.4L/mol,故体积为0.2mol×22.4L/mol=44.8L。HCl的物质的量浓度,盐酸与碳酸钠反应:,0.2mol的HCl可以生成0.1mol二氧化碳,故溶液增重的质量即0.1mol二氧化碳的质量为。
20.0.84
【详解】碳酸氢钠受热分解的化学方程式为:2NaHCO3Na2CO3+H2O+CO2↑,产生的气体通过浓硫酸吸水,得到的气体为二氧化碳,过氧化钠与二氧化碳反应,方程式为:2Na2O2+2CO2=2Na2CO3+O2,由方程式可知,每消耗1mol二氧化碳,过氧化钠增重28g,所以当Na2O2增重0.14g时,说明消耗了0.005mol二氧化碳,碳酸氢钠受热分解生成了0.005mol二氧化碳,则碳酸氢钠的物质的量为0.005mol2=0.01mol,碳酸氢钠的质量为0.01mol84g/mol=0.84g。
21. c ABD 玻璃棒 偏大 温度计水银球位置不在支管口处 未加石棉网 未加沸石 冷凝水上进下出 锥形瓶 蒸馏烧瓶 冷凝管
【详解】(1)仪器E为分液漏斗,常用于萃取分液,则:
a.水中的泥沙为固液不相溶混合物,用过滤的方法进行分离,需要用到的仪器为烧杯、普通漏斗和玻璃棒,a不符合;
b.氯化钠和水可采用蒸发结晶的方法进行分离,需要用到的仪器为蒸发皿、玻璃棒,b不符合;
c.水和苯为互不相溶的液体,可采用分液的方法进行分离,需要用到分液漏斗,c符合;
故答案选c;
(2)配制100mL0.1mol·L-1NaCl溶液,要用到的仪器有烧杯、玻璃棒、100mL的容量瓶、胶头滴管和托盘天平等,故选ABD,还缺少的玻璃仪器是玻璃棒,在定容时若俯视容量瓶刻度线,使得最终溶液体积偏小,则浓度偏大;
(3)①该实验装置为蒸馏装置,图中共有以下4点错误:温度计水银球位置不在支管口处、未加石棉网、未加沸石、冷凝水上进下出;
②根据仪器结构可知,A为锥形瓶,B为蒸馏烧瓶,C为冷凝管。
22. A D B E 增大反应物接触面积,加快反应速率,使反应充分进行 除去Cl2O中的Cl2 2Cl2+Na2CO3═Cl2O+2NaCl+CO2(或2Cl2+Na2CO3+H2O═Cl2O+2NaCl+2NaHCO3) 制得的次氯酸溶液纯度较高,浓度较大 冷水 1.000mol/L
【分析】根据实验目的,将氯气和空气(不参与反应)按体积比1:3混合通入含水8%的碳酸钠中制备Cl2O,并用水吸收Cl2O(不含Cl2)制备次氯酸溶液,应先用装置A制备Cl2,再通过装置D除去混合气体中的HCl气体,同时混入空气,将混合气体通入装置B,在装置B中发生制备Cl2O的反应;然后将制取的Cl2O气体先通入装置C,以除去Cl2等杂质气体,最后通过装置E制取次氯酸溶液,以此解答。
【详解】(1)根据实验目的,将氯气和空气(不参与反应)按体积比1:3混合通入含水8%的碳酸钠中制备Cl2O,并用水吸收Cl2O(不含Cl2)制备次氯酸溶液,应先用装置A制备Cl2,再通过装置D除去混合气体中的HCl气体,同时混入空气,将混合气体通入装置B,在装置B中发生制备Cl2O的反应;然后将制取的Cl2O气体先通入装置C,以除去Cl2等杂质气体,最后通过装置E制取次氯酸溶液,装置连接顺序为:A→D→B→C→E,故答案为:A;D;B;E;
(2)多孔球泡和搅拌棒均能使反应物充分接触,增大反应物接触面积,加快反应速率,使反应充分进行;装置B中生成Cl2O的同时还会有多余的Cl2逸出,而Cl2是非极性分子,易溶于非极性溶剂四氯化碳,因此此处装置C使用足量的四氯化碳将Cl2吸收,故答案为:增大反应物接触面积,加快反应速率,使反应充分进行;除去Cl2O中的Cl2;
(3)已知空气不参与反应,则制取Cl2O以Cl2和Na2CO3为反应物,发生歧化反应,其中氯元素从0价变为+1价和 1价,反应的化学方程式为:2Cl2+Na2CO3═Cl2O+2NaCl+CO2(或2Cl2+Na2CO3+H2O═Cl2O+2NaCl+2NaHCO3),故答案为:2Cl2+Na2CO3═Cl2O+2NaCl+CO2(或2Cl2+Na2CO3+H2O═Cl2O+2NaCl+2NaHCO3);
(4)Cl2O与水反应的化学方程式为:Cl2O+H2O=2HClO,Cl2和水反应的化学方程式为:Cl2+H2O=HCl+HClO,Cl2O和水反应只生成HClO且反应不可逆,氯气和水反应除了生成HClO还生成HCl,并且反应可逆,所以用Cl2O与水反应制备次氯酸溶液相对于用氯气溶于水制备次氯酸溶液的主要优点是用Cl2O与水反应制备次氯酸溶液时制得次氯酸溶液纯度较高、浓度也较大,故答案为:制得的次氯酸溶液纯度较高,浓度较大;
(5)由题可知:Cl2O在42℃以上会分解生成Cl2和O2,故为防止反应放热后温度过高导致Cl2O分解,装置B需放在冷水中,故答案为:冷水;
(6)10.00mL 0.80mol L 1的FeSO4溶液中,n(FeSO4)=0.80mol/L×0.01L=0.008mol,24.00mL0.050 00mol L 1的酸性KMnO4溶液中,n(KMnO4)=0.050mol/L×0.024L=0.0012mol,根据反应MnO+5Fe2++8H+=5Fe3++Mn2++4H2O可知,0.0012mol高锰酸钾消耗硫酸亚铁的物质的量为:0.0012mol×5=0.006mol,则稀释后的10.00mLHClO溶液消耗硫酸亚铁的物质的量为:0.008mol 0.006mol=0.002mol,根据反应HClO+2Fe2++H+=2Fe3++Cl +H2O可知,稀释后10.00mLHClO溶液中n(HClO)=×0.002mol=0.001mol,原10mL次氯酸溶液中n(HClO)=0.001mol×=0.01mol,其浓度为:=1.000mol/L,故答案为:1.000mol/L。
