第六章第一节化学反应与能量变化同步练习(含解析)2022-2023学年下学期高一化学人教版(2019)必修第二册
文档属性
| 名称 | 第六章第一节化学反应与能量变化同步练习(含解析)2022-2023学年下学期高一化学人教版(2019)必修第二册 |

|
|
| 格式 | docx | ||
| 文件大小 | 1.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-06-21 00:00:00 | ||
图片预览




文档简介
第六章第一节化学反应与能量变化同步练习
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1.化学反应中的能量变化常表现为热量变化,如有的反应为放热反应,有的为吸热反应,请从下列选项中选出对此解释合理的为
A.旧化学键断裂时吸收的能量高于新化学键形成时所释放的总能量为吸热反应
B.旧化学键断裂时吸收的能量低于新化学键形成时所释放的总能量为吸热反应
C.在化学反应中需要加热的反应就是吸热反应
D.在化学反应中需要使用催化剂的反应为放热反应
2.N2和H2在催化剂表面合成氨的微观历程及能量变化的示意图如图,用 、 、 分别表示N2、H2、NH3,已知:N2(g)+3H2(g)2NH3(g),该反应属于放热反应。下列说法不正确的是
A.②→③过程,是吸热过程
B.③→④过程,N原子和H原子形成了含有极性键的NH3
C.合成氨反应中,反应物断键吸收的能量大于生成物形成新键释放的能量
D.合成氨反应中,反应物总能量大于生成物总能量
3.和在催化剂表面合成氨的微观历程示意图如下,用、、分别表示、、,下列说法正确的是
A.②到③过程中,需要释放能量
B.③到④变化过程中,需要吸收能量
C.因反应中化学键断裂吸收的能量小于形成新化学键放出的能量,故该反应为放热反应
D.N原子和H原子形成了含有非极性键的
4.反应A+B→C(放热反应)分两步进行:①A+B→X(吸热反应),②X→C(放热反应)。下列示意图中,能正确表示总反应过程中能量变化的是
A. B.
C. D.
5.某小组设计如图装置(盐桥中盛有浸泡了KNO3溶液的琼胶)研究电化学原理。下列叙述正确的是
A.银片为负极,发生的反应为:Ag++e-=Ag
B.用稀硫酸代替AgNO3溶液,也可形成原电池
C.进行实验时,琼胶中K+移向Mg(NO3)2溶液
D.取出盐桥,电流表指针依然偏转
6.某科研机构研发的NO—空气质子交换膜酸性电池工作原理如下图所示(已知:Pt电极对电极反应有催化作用):
当该电池工作一段时间后,下列叙述正确的是
A.“多孔"电极对化学反应速率没有影响
B.具有催化作用的电极能提高电极反应的活化能
C.Pt(B)电极的电极反应式为
D.若有生成,则有向Pt(B)电极区域移动
7.有专家指出,如果对燃烧产物如CO2、H2O、N2等利用太阳能使它们重新组合,那么,不仅可以消除对大气的污染,还可以节约燃料,缓解能源危机。如图所示。在此构想的物质循环中太阳能最终转化为
A.化学能 B.热能 C.生物质能 D.电能
8.下图是1 mol 与1 mol CO反应生成1 mol 和1 mol NO过程中的能量变化示意图。下列说法正确的是
A.反应放出的能量为
B.反应放出的能量为
C.反应吸收的能量为
D.反应吸收的能量为
9.下列电池不属于二次电池的是
A B C D
手机用锂电池 电动汽车用电池 铅酸蓄电池 锌锰干电池
A.A B.B C.C D.D
10.某汽车尾气分析仪以燃料电池为工作原理测定CO的浓度,其装置如图所示,该电池中电解质为氧化钇—氧化钠,其中O2-可以在固体介质NASICON中自由移动。下列说法不正确的是
A.工作时电极b作正极,O2-由电极b流向电极a
B.负极的电极反应式为:
C.当传感器中通过2×10-3mol电子时,通过的尾气中含有2.24mLCO
D.传感器中通过的电流越大,尾气中CO的含量越高
11.下列实验方案设计不合理,且不能达到实验目的的是
A B C D
检验氯气是否具有漂白性 探究钠与水的反应是放热反应 证明热稳定性:Na2CO3>NaHCO3 检查装置气密性
A.A B.B C.C D.D
12.下列装置可以形成原电池的是
A. B. C. D.
13.常见的锌锰干电池构造示意图如图所示,下列说法不正确的是
A.该电池属于一次电池
B.电池工作时,锌筒作负极,电极反应式为Zn-2e =Zn2+
C.电池工作时,电子由锌筒流出经过外电路流向石墨棒
D.电池工作时,电能转化为化学能
14.化学键是高中化学中非常重要的一个概念,它与物质变化过程中的能量变化息息相关,下列说法正确的是:
①化学键存在相邻原子间强烈的相互作用
②是离子化合物
③中既存在离子键又存在共价键
④速滑馆“冰丝带”用干冰作为制冷剂,干冰升华过程中破坏了共价键
⑤物理变化也可以有化学键的破坏
⑥化学变化中一定有化学键的断裂和形成,所以一定伴随能量的变化
⑦吸热反应一定需要加热
⑧氢键是化学键中的一种,会影响物质的熔沸点
A.①③⑤⑥ B.③④⑤⑧ C.①②③⑤ D.③⑤⑥⑦
15.2A(g) B(g)该反应正方向为放热反应;下列能量变化示意图正确的是
A. B.
C. D.
二、实验题
16.实验室利用下列装置模拟工业生产制备少量硝酸。
(1)化学实验室中干燥氨气使用的试剂是___________。
(2)B中反应的化学方程式为___________。
(3)实验时先用酒精喷灯预热催化剂,然后通入反应气体,当催化剂红热后撤离酒精喷灯,催化剂始终保持红热,温度可达到700 ℃以上。下列图示中,能够正确表示该反应过程能量变化的是___________(填字母)。
(4)高温时,2NO2(g)=2NO(g)+O2(g),因此氨气与氧气反应难以生成NO2.根据下列数据计算,当2 mol NO2分解时,反应会___________(填“吸收”或“放出”)___________ kJ能量。
NO2(g) N(g)+2O(g)
NO(g) N(g)+O(g)
O2(g) 2O(g)
17.请按要求填空。
(1)一种以葡萄糖为燃料的微生物电池,其工作原理如图所示:
①写出负极电极反应式:_______;
②随着电池不断放电,电解质溶液的酸性_______(填“增大”、“减小”或“不变”)
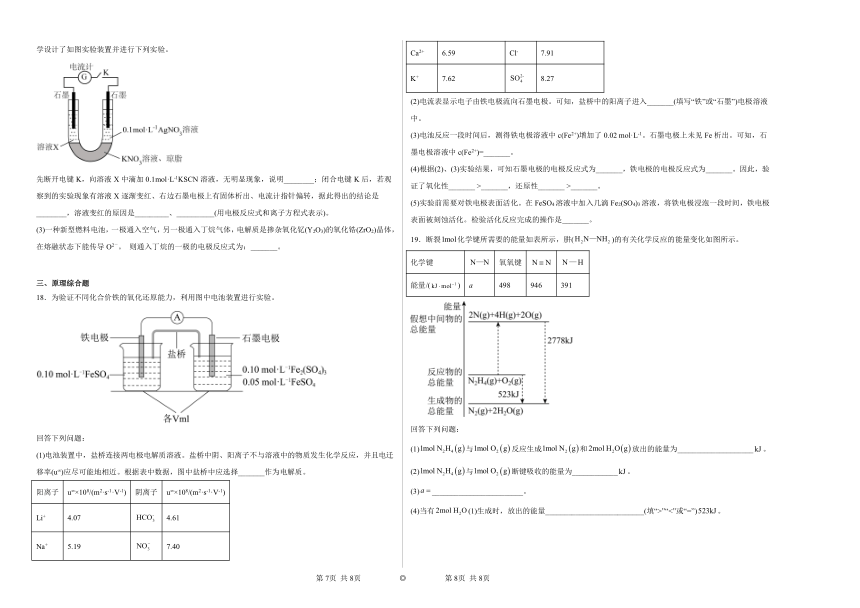
(2)查阅资料发现AgSCN为白色难溶物,Ag+可以氧化SCNˉ和Fe2+。为探究SCNˉ和Fe2+的还原性强弱,某同学设计了如图实验装置并进行下列实验。
先断开电键K,向溶液X中滴加0.1mol·L-1KSCN溶液,无明显现象,说明________;闭合电键K后,若观察到的实验现象有溶液X逐渐变红、右边石墨电极上有固体析出、电流计指针偏转,据此得出的结论是________,溶液变红的原因是_________、__________(用电极反应式和离子方程式表示)。
(3)一种新型燃料电池,一极通入空气,另一极通入丁烷气体,电解质是掺杂氧化钇(Y2O3)的氧化锆(ZrO2)晶体,在熔融状态下能传导O2-。 则通入丁烷的一极的电极反应式为:_______。
三、原理综合题
18.为验证不同化合价铁的氧化还原能力,利用图中电池装置进行实验。
回答下列问题:
(1)电池装置中,盐桥连接两电极电解质溶液。盐桥中阴、阳离子不与溶液中的物质发生化学反应,并且电迁移率(u∞)应尽可能地相近。根据表中数据,图中盐桥中应选择_______作为电解质。
阳离子 u∞×108/(m2·s-1·V-1) 阴离子 u∞×108/(m2·s-1·V-1)
Li+ 4.07 4.61
Na+ 5.19 7.40
Ca2+ 6.59 Cl- 7.91
K+ 7.62 8.27
(2)电流表显示电子由铁电极流向石墨电极。可知,盐桥中的阳离子进入_______(填写“铁”或“石墨”)电极溶液中。
(3)电池反应一段时间后,测得铁电极溶液中c(Fe2+)增加了0.02 mol·L-1。石墨电极上未见Fe析出。可知,石墨电极溶液中c(Fe2+)=_______。
(4)根据(2)、(3)实验结果,可知石墨电极的电极反应式为_______,铁电极的电极反应式为_______。因此,验证了氧化性_______ >_______,还原性_______ >_______。
(5)实验前需要对铁电极表面活化。在FeSO4溶液中加入几滴Fe2(SO4)3溶液,将铁电极浸泡一段时间,铁电极表面被刻蚀活化。检验活化反应完成的操作是_______。
19.断裂化学键所需要的能量如表所示,肼()的有关化学反应的能量变化如图所示。
化学键 氧氧键
能量/() a 498 946 391
回答下列问题:
(1)与反应生成和放出的能量为____________________。
(2)与断键吸收的能量为____________。
(3)________________________。
(4)当有(1)生成时,放出的能量__________________________(填“>”“<”或“=”)。
第1页 共4页 ◎ 第2页 共4页
第1页 共4页 ◎ 第2页 共4页
参考答案:
1.A
【详解】A.在化学反应中,断键吸热,成键放热。若断键吸收的热量大于成键放出的热量,则该反应为吸热反应,A正确;
B.任何化学反应过程中都存在断裂反应物化学键和形成生成物化学键的过程。断裂反应物化学键会吸收热量,形成生成物化学键会释放热量,若旧化学键断裂时吸收的能量低于新化学键形成时所释放的总能量,则该反应为放热反应,B错误;
C.化学反应需在一定条件下进行。反应类型是放热反应还是吸热反应与反应条件是否需要加热无关,有的放热反应也需在加热或高温条件下进行,如铝热反应,C错误;
D.催化剂只能改变反应历程,降低反应的活化能,使化学反应在较低的条件下发生,但不能改变反应热,因此反应发生是否需要使用催化剂与反应类型是放热反应还是吸热反应无关,D错误;
故合理选项是A。
2.C
【详解】A.②→③过程是断开化学键,是吸热过程,故A正确;
B.③→④过程是形成化学键,N原子和H原子形成了含有极性键的NH3,故B正确;
C.合成氨反应是放热反应,则反应物断键吸收的能量小于生成物形成新键释放的能量,故C错误;
D.合成氨反应是放热反应,则反应物总能量大于生成物总能量,故D正确。
综上所述,答案为C。
3.C
【详解】A.②到③过程为化学键的断裂,则需要吸收能量,故A错误;
B.③到④变化过程为化学键的形成,则有能量放出,故B错误;
C.反应物化学键断裂吸收的能量小于形成新化学键放出的能量,该反应为放热反应,故C正确;
D.N原子和H原子形成了含有极性键的NH3,故D错误;
故选:C。
4.A
【详解】第一步反应为吸热反应,说明X的能量比A、B的能量和高;第二步反应为放热反应,则X的能量比生成物C的高,且总反应是放热反应,说明反应物A、B的能量总和比生成物C的高,则只有选项A的图像符合题意,
故选A。
5.B
【详解】A.该装置为MgAg原电池,镁的活泼性大于银,镁作负极,失电子形成镁离子,故A错误;
B.若把硝酸银换成稀硫酸,H+同样在银电极处得到电子析出氢气,可以构成原电池,故B正确;
C.MgAg原电池,镁的活泼性大于银,镁作负极、银为正极,原电池中阳离子移向正极,所以盐桥中的阳离子往右侧硝酸银溶液迁移,故C错误;
D.取出盐桥,由于无法构成闭合回路,不能形成原电池,所以电流表不发生偏转,D错误;
选B。
6.D
【分析】氧气得电子产生OH-,故多孔Pt(B)为正极,NO失电子产生HNO2,故多孔Pt(A)为负极,质子在电池中移动到正极多孔Pt(B);
【详解】A.“多孔”电极有利于增大气体的接触面积,增大反应速率,选项A错误;
B.具有催化作用的电极能降低电极反应的活化能,选项B错误;
C.Pt(B)电极的电极反应式为,选项C错误;
D.Pt(A)电极为负极,失电子发生氧化反应,其电极反应式为:,若有1mol生成,则有向Pt(B)电极区域移动,选项D正确;
答案选D。
7.B
【分析】图中关键信息是利用太阳能使H2O、CO2、N2等重新组合,组合成可燃物,而可燃物燃烧后转化为燃烧产物并放出热量,产物又结合太阳能转化为燃料,如此循环,可知太阳能最终转化为热能。
【详解】A.太阳能转化为化学能,燃烧后转化为热能,A错误;
B.太阳能转化为化学能,燃烧后转化为热能,B正确;
C.生物质能是指自然界有生命的物质提供的能量,此构想未涉及到生物质能,C错误;
D.此构想未涉及电能,D错误;
故答案为:B。
8.A
【详解】A.根据图像可知,该反应为放热反应,放出的能量为,A正确;
B.根据图像可知,该反应为放热反应,放出的能量为,B错误;
C.根据图像可知,该反应为放热反应,C错误;
D.根据图像可知,该反应为放热反应,D错误;
故答案为:A。
9.D
【详解】A.手机用锂电池,可充电,属于二次电池,故A不选;
B.电动汽车用电池,可充电,属于二次电池,故B不选;
C.铅酸蓄电池,可充电,属于二次电池,故C不选;
D.锌锰干电池不可充电,属于一次电池,故D选;
故选D。
10.C
【分析】该电池为燃料电池,燃料为负极,空气为正极。
【详解】A.b为正极,阴离子向负极移动,正确;
B.负极发生氧化反应,正确;
C.通过2×10-3mol电子时,反应的CO为0.001mol,在标准状况下,体积为2.24mL,错误;
D.CO含量高,转移电子多,电流大,正确。
故选C。
11.A
【详解】A.氯气通入湿润有色布条中,氯气先和水反应生成次氯酸,次氯酸有漂白性,因此只能说明次氯酸有漂白性,不能说明氯气有漂白性,该实验不能达到实验目的,故A符合题意;
B. U形管液面左低右高,说明带支管的试管里压强大,则温度高,说明钠与水的反应是放热反应,该实验能达到实验目的,故B不符合题意;
C.外面试管的温度高,里面试管温度低,里面分解,说明里面物质的热稳定性差,能证明热稳定性:Na2CO3>NaHCO3,故C不符合题意;
D.用手捂住试管,有气泡冒出,松开手,形成一段水柱,能检查装置气密性,该实验能达到实验目的,故D不符合题意。
综上所述,答案为A。
12.A
【详解】A.该装置中,两个电极材料Zn、Cu的金属活动性不同,用导线相连接,与电解质溶液稀硫酸相接触,能形成原电池,A符合题意;
B.两个电极材料都为Ag,活动性相同,不能产生电势差,不能形成电流,B不符合题意;
C.虽然具有两个活动性不同的电极,但植物油为非电解质,不能传导电流,C不符合题意;
D.具有两个活动性不同的电极,且稀硫酸为电解质溶液,但不能形成闭合回路,D不符合题意;
故选A。
13.D
【详解】A.锌锰干电池属于一次电池,故A正确;
B.电池工作时,锌筒作负极,电解液呈酸性,电极反应式为Zn-2e =Zn2+,故B正确;
C.电池工作时,锌为负极、碳棒为正极,电子由锌筒流出经过外电路流向石墨棒,故C正确;
D.电池工作时,化学能转化为电能,故D错误;
选D。
14.A
【详解】①化学键是相邻的两个或多个原子之间的强烈的相互作用,这种相互作用既包括吸引力也包括排斥力,故①正确;
②中Al和Cl之间形成共价键,属于共价化合物,故②错误;
③中和Cl-之间以离子键结合,中含有共价键,故③正确;
④干冰属于分子晶体,升华破坏了分子间作用力,故④错误;
⑤物理变化中可能有化学键的断裂,如NaCl溶液水发生电离,离子键被破坏,故⑤正确;
⑥化学反应过程是旧键的断裂与新键的形成过程,化学反应过程中一定有化学键的断裂和形成,断裂化学键吸收能量,形成化学键放出能量,因此化学变化所以一定伴随能量的变化,故⑥正确;
⑦吸热反应不一定需要加热才能发生,如和的反应属于吸热反应,但是不需要加热就可发生,故⑦错误;
⑧氢键属于分子间作用力,不属于化学键,故⑧错误;
说法正确的是①③⑤⑥;
答案选A。
15.B
【详解】2A(g) B(g)该反应正方向为放热反应,说明反应物总能量高于生成物总能量,又因为气态B转化为液态B放热,所以选项B中图像符合。
答案选B。
16. 碱石灰 3NO2+H2O=2HNO3+NO A 吸收 113
【详解】(1)化学实验室中干燥氨气使用的试剂是碱石灰。
(2)B中反应的化学方程式为3NO2+H2O=2HNO3+NO。
(3)实验时先用酒精喷灯预热催化剂,然后通入反应气体,当催化剂红热后撤离酒精喷灯,催化剂始终保持红热,温度可达到700 ℃以上,说明该反应是放热反应。放热反应中反应物的总能量高于生成物的总能量,所以能够正确表示该反应过程能量变化的是A。
(4)2 mol NO2断裂化学键时吸收的总能量为931 kJ×2=1 862 kJ,生成2 mol NO和1 mol O2的化学键放出的总能量是628 kJ×2+493 kJ=1 749 kJ,显然吸收的热量较多,故为吸热反应。因此,当有2 mol NO2分解时吸收的热量为-1749 kJ+1862 kJ =113 kJ。
17. C6H12O6+6H2O-24e-=6CO2↑+24H+ 减小 溶液中无Fe3+ Fe2+的还原性强于SCN- Fe2+-e-=Fe3+ Fe3++3SCN-=Fe(SCN)3 C4H10 -26e-+13O2-=4CO2 ↑+5H2O
【分析】燃料电池中,通入燃料的一极为负极,还原剂失去电子发生氧化反应,电子沿着导线流向正极,通入助燃物的一极为正极,正极上发生还原反应,内电路中阴离子移向负极、阳离子移向正极;
【详解】(1)由工作原理示意图知,以葡萄糖为燃料的微生物电池中,左侧电极上氧气得到电子被还原,正极反应为:O2+4H++4e-=2H2O;右侧电极上葡萄糖失去电子被氧化,右侧区是负极区,则①负极电极反应式:C6H12O6+6H2O-24e-=6CO2↑+24H+;②该电池总反应为:C6H12O6+6 O2=6CO2↑++6H2O,随着电池不断放电,水不断生成、电解质物质的量不变,故电解质溶液的酸性减小;
(2) 先断开电键K,向溶液X中滴加0.1mol·L-1KSCN溶液,无明显现象,说明溶液中无Fe3+;闭合电键K后,若观察到的实验现象有:溶液X逐渐变红即有Fe(SCN)3生成、则负极亚铁离子失去电子被氧化,右边石墨电极上有固体析出、则是银离子得到电子被还原得到银,电流计指针偏转,可见该原电池总反应为:Ag++ Fe2+=Fe3++Ag,则Fe2+被氧化而SCN-没有被氧化,据此得出的结论是Fe2+的还原性强于SCN-,溶液变红的原因是Fe2+-e-=Fe3+、Fe3++3SCN-=Fe(SCN)3;
(3)该丁烷电池总反应为2C4H10+13 O2=8 CO2 ↑+10 H2O,正极反应为:13O2+52e-=26O2-,按电池总反应=正极反应式+负极反应式知,则-通入丁烷的一极的电极反应式为:2C4H10 -52 e-+26O2-=8CO2 ↑+10H2O;即 C4H10 -26 e-+13 O2-=4 CO2 ↑+5 H2O。
18. KCl 石墨 0.09mol/L Fe3++e-=Fe2+ Fe-2e-= Fe2+ Fe3+ Fe2+ Fe Fe2+ 取少量活化后溶液,滴入KSCN溶液,若溶液未变红,证明活化反应完成
【分析】(1)~(4)根据题给信息选择合适的物质,根据原电池工作的原理书写电极反应式,并进行计算,由此判断氧化性、还原性的强弱;
(5)根据刻蚀活化的原理分析作答。
【详解】(1)Fe2+、Fe3+能与反应,Ca2+能与反应,FeSO4、Fe2(SO4)3都属于强酸弱碱盐,水溶液呈酸性,酸性条件下能与Fe2+反应,根据题意“盐桥中阴、阳离子不与溶液中的物质发生化学反应”,盐桥中阴离子不可以选择、,阳离子不可以选择Ca2+,另盐桥中阴、阳离子的迁移率(u∞)应尽可能地相近,根据表中数据,盐桥中应选择KCl作为电解质,故答案为:KCl;
(2)电流表显示电子由铁电极流向石墨电极,则铁电极为负极,石墨电极为正极,盐桥中阳离子向正极移动,则盐桥中的阳离子进入石墨电极溶液中,故答案为:石墨;
(3)根据(2)的分析,铁电极的电极反应式为Fe-2e-=Fe2+,石墨电极上未见Fe析出,石墨电极的电极反应式为Fe3++e-=Fe2+,电池反应一段时间后,测得铁电极溶液中c(Fe2+)增加了0.02mol/L,根据得失电子守恒,石墨电极溶液中c(Fe2+)增加0.04mol/L,石墨电极溶液中c(Fe2+)=0.05mol/L+0.04mol/L=0.09mol/L,故答案为:0.09mol/L;
(4)根据(2)、(3)实验结果,可知石墨电极的电极反应式为Fe3++e-=Fe2+,铁电极的电极反应式为Fe-2e-=Fe2+;电池总反应为Fe+2Fe3+=3Fe2+,根据同一反应中,氧化剂的氧化性强于氧化产物、还原剂的还原性强于还原产物,则验证了Fe3+氧化性大于Fe2+,Fe还原性大于Fe2+,故答案为:Fe3++e-=Fe2+ ,Fe-2e-=Fe2+ ,Fe3+,Fe2+,Fe,Fe2+;
(5)在FeSO4溶液中加入几滴Fe2(SO4)3溶液,将铁电极浸泡一段时间,铁电极表面被刻蚀活化,发生的反应为Fe+ Fe2(SO4)3=3FeSO4,要检验活化反应完成,只要检验溶液中不含Fe3+即可,检验活化反应完成的方法是:取活化后溶液少许于试管中,加入KSCN溶液,若溶液不出现血红色,说明活化反应完成,故答案为:取活化后溶液少许于试管中,加入KSCN溶液,若溶液不变红,说明活化反应完成。
19. 523 2255 193 >
【详解】(1)由题图可知,与反应生成和放出的能量为,故答案为:523;
(2)与断键吸收的能量为,故答案为:2255;
(3)化学键断裂吸收能量,化学键生成释放能量,断裂键所需的能量为,则化学键断裂吸收的能量为,解得,故答案为:193;
(4)据图可知,与反应生成和放出的能量。(1)放出能量,因此当有(1)生成时,放出的能量大于,故答案为:>。
答案第1页,共2页
答案第1页,共2页
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1.化学反应中的能量变化常表现为热量变化,如有的反应为放热反应,有的为吸热反应,请从下列选项中选出对此解释合理的为
A.旧化学键断裂时吸收的能量高于新化学键形成时所释放的总能量为吸热反应
B.旧化学键断裂时吸收的能量低于新化学键形成时所释放的总能量为吸热反应
C.在化学反应中需要加热的反应就是吸热反应
D.在化学反应中需要使用催化剂的反应为放热反应
2.N2和H2在催化剂表面合成氨的微观历程及能量变化的示意图如图,用 、 、 分别表示N2、H2、NH3,已知:N2(g)+3H2(g)2NH3(g),该反应属于放热反应。下列说法不正确的是
A.②→③过程,是吸热过程
B.③→④过程,N原子和H原子形成了含有极性键的NH3
C.合成氨反应中,反应物断键吸收的能量大于生成物形成新键释放的能量
D.合成氨反应中,反应物总能量大于生成物总能量
3.和在催化剂表面合成氨的微观历程示意图如下,用、、分别表示、、,下列说法正确的是
A.②到③过程中,需要释放能量
B.③到④变化过程中,需要吸收能量
C.因反应中化学键断裂吸收的能量小于形成新化学键放出的能量,故该反应为放热反应
D.N原子和H原子形成了含有非极性键的
4.反应A+B→C(放热反应)分两步进行:①A+B→X(吸热反应),②X→C(放热反应)。下列示意图中,能正确表示总反应过程中能量变化的是
A. B.
C. D.
5.某小组设计如图装置(盐桥中盛有浸泡了KNO3溶液的琼胶)研究电化学原理。下列叙述正确的是
A.银片为负极,发生的反应为:Ag++e-=Ag
B.用稀硫酸代替AgNO3溶液,也可形成原电池
C.进行实验时,琼胶中K+移向Mg(NO3)2溶液
D.取出盐桥,电流表指针依然偏转
6.某科研机构研发的NO—空气质子交换膜酸性电池工作原理如下图所示(已知:Pt电极对电极反应有催化作用):
当该电池工作一段时间后,下列叙述正确的是
A.“多孔"电极对化学反应速率没有影响
B.具有催化作用的电极能提高电极反应的活化能
C.Pt(B)电极的电极反应式为
D.若有生成,则有向Pt(B)电极区域移动
7.有专家指出,如果对燃烧产物如CO2、H2O、N2等利用太阳能使它们重新组合,那么,不仅可以消除对大气的污染,还可以节约燃料,缓解能源危机。如图所示。在此构想的物质循环中太阳能最终转化为
A.化学能 B.热能 C.生物质能 D.电能
8.下图是1 mol 与1 mol CO反应生成1 mol 和1 mol NO过程中的能量变化示意图。下列说法正确的是
A.反应放出的能量为
B.反应放出的能量为
C.反应吸收的能量为
D.反应吸收的能量为
9.下列电池不属于二次电池的是
A B C D
手机用锂电池 电动汽车用电池 铅酸蓄电池 锌锰干电池
A.A B.B C.C D.D
10.某汽车尾气分析仪以燃料电池为工作原理测定CO的浓度,其装置如图所示,该电池中电解质为氧化钇—氧化钠,其中O2-可以在固体介质NASICON中自由移动。下列说法不正确的是
A.工作时电极b作正极,O2-由电极b流向电极a
B.负极的电极反应式为:
C.当传感器中通过2×10-3mol电子时,通过的尾气中含有2.24mLCO
D.传感器中通过的电流越大,尾气中CO的含量越高
11.下列实验方案设计不合理,且不能达到实验目的的是
A B C D
检验氯气是否具有漂白性 探究钠与水的反应是放热反应 证明热稳定性:Na2CO3>NaHCO3 检查装置气密性
A.A B.B C.C D.D
12.下列装置可以形成原电池的是
A. B. C. D.
13.常见的锌锰干电池构造示意图如图所示,下列说法不正确的是
A.该电池属于一次电池
B.电池工作时,锌筒作负极,电极反应式为Zn-2e =Zn2+
C.电池工作时,电子由锌筒流出经过外电路流向石墨棒
D.电池工作时,电能转化为化学能
14.化学键是高中化学中非常重要的一个概念,它与物质变化过程中的能量变化息息相关,下列说法正确的是:
①化学键存在相邻原子间强烈的相互作用
②是离子化合物
③中既存在离子键又存在共价键
④速滑馆“冰丝带”用干冰作为制冷剂,干冰升华过程中破坏了共价键
⑤物理变化也可以有化学键的破坏
⑥化学变化中一定有化学键的断裂和形成,所以一定伴随能量的变化
⑦吸热反应一定需要加热
⑧氢键是化学键中的一种,会影响物质的熔沸点
A.①③⑤⑥ B.③④⑤⑧ C.①②③⑤ D.③⑤⑥⑦
15.2A(g) B(g)该反应正方向为放热反应;下列能量变化示意图正确的是
A. B.
C. D.
二、实验题
16.实验室利用下列装置模拟工业生产制备少量硝酸。
(1)化学实验室中干燥氨气使用的试剂是___________。
(2)B中反应的化学方程式为___________。
(3)实验时先用酒精喷灯预热催化剂,然后通入反应气体,当催化剂红热后撤离酒精喷灯,催化剂始终保持红热,温度可达到700 ℃以上。下列图示中,能够正确表示该反应过程能量变化的是___________(填字母)。
(4)高温时,2NO2(g)=2NO(g)+O2(g),因此氨气与氧气反应难以生成NO2.根据下列数据计算,当2 mol NO2分解时,反应会___________(填“吸收”或“放出”)___________ kJ能量。
NO2(g) N(g)+2O(g)
NO(g) N(g)+O(g)
O2(g) 2O(g)
17.请按要求填空。
(1)一种以葡萄糖为燃料的微生物电池,其工作原理如图所示:
①写出负极电极反应式:_______;
②随着电池不断放电,电解质溶液的酸性_______(填“增大”、“减小”或“不变”)
(2)查阅资料发现AgSCN为白色难溶物,Ag+可以氧化SCNˉ和Fe2+。为探究SCNˉ和Fe2+的还原性强弱,某同学设计了如图实验装置并进行下列实验。
先断开电键K,向溶液X中滴加0.1mol·L-1KSCN溶液,无明显现象,说明________;闭合电键K后,若观察到的实验现象有溶液X逐渐变红、右边石墨电极上有固体析出、电流计指针偏转,据此得出的结论是________,溶液变红的原因是_________、__________(用电极反应式和离子方程式表示)。
(3)一种新型燃料电池,一极通入空气,另一极通入丁烷气体,电解质是掺杂氧化钇(Y2O3)的氧化锆(ZrO2)晶体,在熔融状态下能传导O2-。 则通入丁烷的一极的电极反应式为:_______。
三、原理综合题
18.为验证不同化合价铁的氧化还原能力,利用图中电池装置进行实验。
回答下列问题:
(1)电池装置中,盐桥连接两电极电解质溶液。盐桥中阴、阳离子不与溶液中的物质发生化学反应,并且电迁移率(u∞)应尽可能地相近。根据表中数据,图中盐桥中应选择_______作为电解质。
阳离子 u∞×108/(m2·s-1·V-1) 阴离子 u∞×108/(m2·s-1·V-1)
Li+ 4.07 4.61
Na+ 5.19 7.40
Ca2+ 6.59 Cl- 7.91
K+ 7.62 8.27
(2)电流表显示电子由铁电极流向石墨电极。可知,盐桥中的阳离子进入_______(填写“铁”或“石墨”)电极溶液中。
(3)电池反应一段时间后,测得铁电极溶液中c(Fe2+)增加了0.02 mol·L-1。石墨电极上未见Fe析出。可知,石墨电极溶液中c(Fe2+)=_______。
(4)根据(2)、(3)实验结果,可知石墨电极的电极反应式为_______,铁电极的电极反应式为_______。因此,验证了氧化性_______ >_______,还原性_______ >_______。
(5)实验前需要对铁电极表面活化。在FeSO4溶液中加入几滴Fe2(SO4)3溶液,将铁电极浸泡一段时间,铁电极表面被刻蚀活化。检验活化反应完成的操作是_______。
19.断裂化学键所需要的能量如表所示,肼()的有关化学反应的能量变化如图所示。
化学键 氧氧键
能量/() a 498 946 391
回答下列问题:
(1)与反应生成和放出的能量为____________________。
(2)与断键吸收的能量为____________。
(3)________________________。
(4)当有(1)生成时,放出的能量__________________________(填“>”“<”或“=”)。
第1页 共4页 ◎ 第2页 共4页
第1页 共4页 ◎ 第2页 共4页
参考答案:
1.A
【详解】A.在化学反应中,断键吸热,成键放热。若断键吸收的热量大于成键放出的热量,则该反应为吸热反应,A正确;
B.任何化学反应过程中都存在断裂反应物化学键和形成生成物化学键的过程。断裂反应物化学键会吸收热量,形成生成物化学键会释放热量,若旧化学键断裂时吸收的能量低于新化学键形成时所释放的总能量,则该反应为放热反应,B错误;
C.化学反应需在一定条件下进行。反应类型是放热反应还是吸热反应与反应条件是否需要加热无关,有的放热反应也需在加热或高温条件下进行,如铝热反应,C错误;
D.催化剂只能改变反应历程,降低反应的活化能,使化学反应在较低的条件下发生,但不能改变反应热,因此反应发生是否需要使用催化剂与反应类型是放热反应还是吸热反应无关,D错误;
故合理选项是A。
2.C
【详解】A.②→③过程是断开化学键,是吸热过程,故A正确;
B.③→④过程是形成化学键,N原子和H原子形成了含有极性键的NH3,故B正确;
C.合成氨反应是放热反应,则反应物断键吸收的能量小于生成物形成新键释放的能量,故C错误;
D.合成氨反应是放热反应,则反应物总能量大于生成物总能量,故D正确。
综上所述,答案为C。
3.C
【详解】A.②到③过程为化学键的断裂,则需要吸收能量,故A错误;
B.③到④变化过程为化学键的形成,则有能量放出,故B错误;
C.反应物化学键断裂吸收的能量小于形成新化学键放出的能量,该反应为放热反应,故C正确;
D.N原子和H原子形成了含有极性键的NH3,故D错误;
故选:C。
4.A
【详解】第一步反应为吸热反应,说明X的能量比A、B的能量和高;第二步反应为放热反应,则X的能量比生成物C的高,且总反应是放热反应,说明反应物A、B的能量总和比生成物C的高,则只有选项A的图像符合题意,
故选A。
5.B
【详解】A.该装置为MgAg原电池,镁的活泼性大于银,镁作负极,失电子形成镁离子,故A错误;
B.若把硝酸银换成稀硫酸,H+同样在银电极处得到电子析出氢气,可以构成原电池,故B正确;
C.MgAg原电池,镁的活泼性大于银,镁作负极、银为正极,原电池中阳离子移向正极,所以盐桥中的阳离子往右侧硝酸银溶液迁移,故C错误;
D.取出盐桥,由于无法构成闭合回路,不能形成原电池,所以电流表不发生偏转,D错误;
选B。
6.D
【分析】氧气得电子产生OH-,故多孔Pt(B)为正极,NO失电子产生HNO2,故多孔Pt(A)为负极,质子在电池中移动到正极多孔Pt(B);
【详解】A.“多孔”电极有利于增大气体的接触面积,增大反应速率,选项A错误;
B.具有催化作用的电极能降低电极反应的活化能,选项B错误;
C.Pt(B)电极的电极反应式为,选项C错误;
D.Pt(A)电极为负极,失电子发生氧化反应,其电极反应式为:,若有1mol生成,则有向Pt(B)电极区域移动,选项D正确;
答案选D。
7.B
【分析】图中关键信息是利用太阳能使H2O、CO2、N2等重新组合,组合成可燃物,而可燃物燃烧后转化为燃烧产物并放出热量,产物又结合太阳能转化为燃料,如此循环,可知太阳能最终转化为热能。
【详解】A.太阳能转化为化学能,燃烧后转化为热能,A错误;
B.太阳能转化为化学能,燃烧后转化为热能,B正确;
C.生物质能是指自然界有生命的物质提供的能量,此构想未涉及到生物质能,C错误;
D.此构想未涉及电能,D错误;
故答案为:B。
8.A
【详解】A.根据图像可知,该反应为放热反应,放出的能量为,A正确;
B.根据图像可知,该反应为放热反应,放出的能量为,B错误;
C.根据图像可知,该反应为放热反应,C错误;
D.根据图像可知,该反应为放热反应,D错误;
故答案为:A。
9.D
【详解】A.手机用锂电池,可充电,属于二次电池,故A不选;
B.电动汽车用电池,可充电,属于二次电池,故B不选;
C.铅酸蓄电池,可充电,属于二次电池,故C不选;
D.锌锰干电池不可充电,属于一次电池,故D选;
故选D。
10.C
【分析】该电池为燃料电池,燃料为负极,空气为正极。
【详解】A.b为正极,阴离子向负极移动,正确;
B.负极发生氧化反应,正确;
C.通过2×10-3mol电子时,反应的CO为0.001mol,在标准状况下,体积为2.24mL,错误;
D.CO含量高,转移电子多,电流大,正确。
故选C。
11.A
【详解】A.氯气通入湿润有色布条中,氯气先和水反应生成次氯酸,次氯酸有漂白性,因此只能说明次氯酸有漂白性,不能说明氯气有漂白性,该实验不能达到实验目的,故A符合题意;
B. U形管液面左低右高,说明带支管的试管里压强大,则温度高,说明钠与水的反应是放热反应,该实验能达到实验目的,故B不符合题意;
C.外面试管的温度高,里面试管温度低,里面分解,说明里面物质的热稳定性差,能证明热稳定性:Na2CO3>NaHCO3,故C不符合题意;
D.用手捂住试管,有气泡冒出,松开手,形成一段水柱,能检查装置气密性,该实验能达到实验目的,故D不符合题意。
综上所述,答案为A。
12.A
【详解】A.该装置中,两个电极材料Zn、Cu的金属活动性不同,用导线相连接,与电解质溶液稀硫酸相接触,能形成原电池,A符合题意;
B.两个电极材料都为Ag,活动性相同,不能产生电势差,不能形成电流,B不符合题意;
C.虽然具有两个活动性不同的电极,但植物油为非电解质,不能传导电流,C不符合题意;
D.具有两个活动性不同的电极,且稀硫酸为电解质溶液,但不能形成闭合回路,D不符合题意;
故选A。
13.D
【详解】A.锌锰干电池属于一次电池,故A正确;
B.电池工作时,锌筒作负极,电解液呈酸性,电极反应式为Zn-2e =Zn2+,故B正确;
C.电池工作时,锌为负极、碳棒为正极,电子由锌筒流出经过外电路流向石墨棒,故C正确;
D.电池工作时,化学能转化为电能,故D错误;
选D。
14.A
【详解】①化学键是相邻的两个或多个原子之间的强烈的相互作用,这种相互作用既包括吸引力也包括排斥力,故①正确;
②中Al和Cl之间形成共价键,属于共价化合物,故②错误;
③中和Cl-之间以离子键结合,中含有共价键,故③正确;
④干冰属于分子晶体,升华破坏了分子间作用力,故④错误;
⑤物理变化中可能有化学键的断裂,如NaCl溶液水发生电离,离子键被破坏,故⑤正确;
⑥化学反应过程是旧键的断裂与新键的形成过程,化学反应过程中一定有化学键的断裂和形成,断裂化学键吸收能量,形成化学键放出能量,因此化学变化所以一定伴随能量的变化,故⑥正确;
⑦吸热反应不一定需要加热才能发生,如和的反应属于吸热反应,但是不需要加热就可发生,故⑦错误;
⑧氢键属于分子间作用力,不属于化学键,故⑧错误;
说法正确的是①③⑤⑥;
答案选A。
15.B
【详解】2A(g) B(g)该反应正方向为放热反应,说明反应物总能量高于生成物总能量,又因为气态B转化为液态B放热,所以选项B中图像符合。
答案选B。
16. 碱石灰 3NO2+H2O=2HNO3+NO A 吸收 113
【详解】(1)化学实验室中干燥氨气使用的试剂是碱石灰。
(2)B中反应的化学方程式为3NO2+H2O=2HNO3+NO。
(3)实验时先用酒精喷灯预热催化剂,然后通入反应气体,当催化剂红热后撤离酒精喷灯,催化剂始终保持红热,温度可达到700 ℃以上,说明该反应是放热反应。放热反应中反应物的总能量高于生成物的总能量,所以能够正确表示该反应过程能量变化的是A。
(4)2 mol NO2断裂化学键时吸收的总能量为931 kJ×2=1 862 kJ,生成2 mol NO和1 mol O2的化学键放出的总能量是628 kJ×2+493 kJ=1 749 kJ,显然吸收的热量较多,故为吸热反应。因此,当有2 mol NO2分解时吸收的热量为-1749 kJ+1862 kJ =113 kJ。
17. C6H12O6+6H2O-24e-=6CO2↑+24H+ 减小 溶液中无Fe3+ Fe2+的还原性强于SCN- Fe2+-e-=Fe3+ Fe3++3SCN-=Fe(SCN)3 C4H10 -26e-+13O2-=4CO2 ↑+5H2O
【分析】燃料电池中,通入燃料的一极为负极,还原剂失去电子发生氧化反应,电子沿着导线流向正极,通入助燃物的一极为正极,正极上发生还原反应,内电路中阴离子移向负极、阳离子移向正极;
【详解】(1)由工作原理示意图知,以葡萄糖为燃料的微生物电池中,左侧电极上氧气得到电子被还原,正极反应为:O2+4H++4e-=2H2O;右侧电极上葡萄糖失去电子被氧化,右侧区是负极区,则①负极电极反应式:C6H12O6+6H2O-24e-=6CO2↑+24H+;②该电池总反应为:C6H12O6+6 O2=6CO2↑++6H2O,随着电池不断放电,水不断生成、电解质物质的量不变,故电解质溶液的酸性减小;
(2) 先断开电键K,向溶液X中滴加0.1mol·L-1KSCN溶液,无明显现象,说明溶液中无Fe3+;闭合电键K后,若观察到的实验现象有:溶液X逐渐变红即有Fe(SCN)3生成、则负极亚铁离子失去电子被氧化,右边石墨电极上有固体析出、则是银离子得到电子被还原得到银,电流计指针偏转,可见该原电池总反应为:Ag++ Fe2+=Fe3++Ag,则Fe2+被氧化而SCN-没有被氧化,据此得出的结论是Fe2+的还原性强于SCN-,溶液变红的原因是Fe2+-e-=Fe3+、Fe3++3SCN-=Fe(SCN)3;
(3)该丁烷电池总反应为2C4H10+13 O2=8 CO2 ↑+10 H2O,正极反应为:13O2+52e-=26O2-,按电池总反应=正极反应式+负极反应式知,则-通入丁烷的一极的电极反应式为:2C4H10 -52 e-+26O2-=8CO2 ↑+10H2O;即 C4H10 -26 e-+13 O2-=4 CO2 ↑+5 H2O。
18. KCl 石墨 0.09mol/L Fe3++e-=Fe2+ Fe-2e-= Fe2+ Fe3+ Fe2+ Fe Fe2+ 取少量活化后溶液,滴入KSCN溶液,若溶液未变红,证明活化反应完成
【分析】(1)~(4)根据题给信息选择合适的物质,根据原电池工作的原理书写电极反应式,并进行计算,由此判断氧化性、还原性的强弱;
(5)根据刻蚀活化的原理分析作答。
【详解】(1)Fe2+、Fe3+能与反应,Ca2+能与反应,FeSO4、Fe2(SO4)3都属于强酸弱碱盐,水溶液呈酸性,酸性条件下能与Fe2+反应,根据题意“盐桥中阴、阳离子不与溶液中的物质发生化学反应”,盐桥中阴离子不可以选择、,阳离子不可以选择Ca2+,另盐桥中阴、阳离子的迁移率(u∞)应尽可能地相近,根据表中数据,盐桥中应选择KCl作为电解质,故答案为:KCl;
(2)电流表显示电子由铁电极流向石墨电极,则铁电极为负极,石墨电极为正极,盐桥中阳离子向正极移动,则盐桥中的阳离子进入石墨电极溶液中,故答案为:石墨;
(3)根据(2)的分析,铁电极的电极反应式为Fe-2e-=Fe2+,石墨电极上未见Fe析出,石墨电极的电极反应式为Fe3++e-=Fe2+,电池反应一段时间后,测得铁电极溶液中c(Fe2+)增加了0.02mol/L,根据得失电子守恒,石墨电极溶液中c(Fe2+)增加0.04mol/L,石墨电极溶液中c(Fe2+)=0.05mol/L+0.04mol/L=0.09mol/L,故答案为:0.09mol/L;
(4)根据(2)、(3)实验结果,可知石墨电极的电极反应式为Fe3++e-=Fe2+,铁电极的电极反应式为Fe-2e-=Fe2+;电池总反应为Fe+2Fe3+=3Fe2+,根据同一反应中,氧化剂的氧化性强于氧化产物、还原剂的还原性强于还原产物,则验证了Fe3+氧化性大于Fe2+,Fe还原性大于Fe2+,故答案为:Fe3++e-=Fe2+ ,Fe-2e-=Fe2+ ,Fe3+,Fe2+,Fe,Fe2+;
(5)在FeSO4溶液中加入几滴Fe2(SO4)3溶液,将铁电极浸泡一段时间,铁电极表面被刻蚀活化,发生的反应为Fe+ Fe2(SO4)3=3FeSO4,要检验活化反应完成,只要检验溶液中不含Fe3+即可,检验活化反应完成的方法是:取活化后溶液少许于试管中,加入KSCN溶液,若溶液不出现血红色,说明活化反应完成,故答案为:取活化后溶液少许于试管中,加入KSCN溶液,若溶液不变红,说明活化反应完成。
19. 523 2255 193 >
【详解】(1)由题图可知,与反应生成和放出的能量为,故答案为:523;
(2)与断键吸收的能量为,故答案为:2255;
(3)化学键断裂吸收能量,化学键生成释放能量,断裂键所需的能量为,则化学键断裂吸收的能量为,解得,故答案为:193;
(4)据图可知,与反应生成和放出的能量。(1)放出能量,因此当有(1)生成时,放出的能量大于,故答案为:>。
答案第1页,共2页
答案第1页,共2页
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
