第五章第一节硫及其化合物同步练习(含解析)2022-2023学年下学期高一化学人教版(2019)必修第二册
文档属性
| 名称 | 第五章第一节硫及其化合物同步练习(含解析)2022-2023学年下学期高一化学人教版(2019)必修第二册 |

|
|
| 格式 | docx | ||
| 文件大小 | 1.4MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-06-21 00:00:00 | ||
图片预览




文档简介
第五章第一节硫及其化合物同步练习
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1.下列物质的检验中,其结论一定正确的是
A.向某溶液中加入溶液,产生白色沉淀,加入稀后,白色沉淀不溶解,也无其他现象,说明原溶液中一定含有
B.向某溶液中加入盐酸产生无色气体,该气体能使澄清的石灰水变浑浊,说明该溶液中一定含有或
C.取少量久置的样品于试管中加水溶解,再加足量盐酸酸化,然后加溶液,若加盐酸时有气体产生,加溶液时有白色沉淀产生,说明样品已部分被氧化
D.将某气体通入品红溶液中,品红溶液褪色,该气体一定是
2.如图所示是一系列含硫化合物的转化关系(反应中生成的水已略去),其中说法正确的是
A.反应①说明SO2具有氧化性,反应②说明SO2具有酸性
B.反应②中生成物n(Na2SO3)∶n(NaHSO3)=1∶1时,则反应物n(SO2)∶n(NaOH)=1∶2
C.反应③④⑤均属于氧化还原反应
D.工业上可利用反应②和反应④回收SO2
3.下列说法正确的是
A.因为SO2具有漂白性,所以它能使品红溶液、溴水、KMnO4(H+)、石蕊溶液褪色
B.能使品红溶液褪色的不一定是SO2
C.SO2、漂白粉、活性炭、Na2O2都能使红墨水褪色,其原理相同
D.等物质的量的SO2和Cl2相遇在溶液中具有漂白能力
4.下列反应中,硫酸既表现出强氧化性,又表现出酸性的是
A.氯化钠固体与浓硫酸反应 B.铜与浓硫酸反应
C.碳与浓硫酸反应 D.CuO与稀硫酸反应
5.现有两瓶无色溶液,分别是稀硫酸和浓硫酸。下列方法不能将它们鉴别出来的是
A.分别取少量两种溶液加水稀释,比较热效应
B.分别取少量两种溶液滴加到纸张上,观察纸张是否变黑
C.分别取少量两种溶液滴加BaCl2溶液,观察是否产生白色沉淀
D.分别取足量两种溶液向其中加入铁片,一段时间后观察铁片是否溶解
6.下列变化的本质相似的是
A.浓硫酸和浓盐酸在空气中敞口放置时浓度均减小
B.SO2和Cl2均能能使品红溶液褪色
C.浓H2SO4和稀H2SO4与金属反应时均有气体放出
D.H2S和HI气体均不能用浓硫酸干燥
7.如图W、X、Y、Z为四种物质,若箭头表示能一步转化的常见反应,其中常温下能实现图示转化关系的是
选项 W X Y Z
A S SO2 SO3 H2SO4
B Na Na2O2 NaOH NaCl
C Fe FeCl3 Fe(OH)2 FeCl2
D Al AlCl3 NaAlO2 Al2(SO4)3
A.A B.B C.C D.D
8.固硫剂能把含硫燃料燃烧生成的二氧化硫转化成盐的形式固定在炉渣中。下列选项的物质组合中,各种试剂均可用作固硫剂的是
① ② ③ ④
A.① B.②③ C.①③ D.①②③④
9.为了除去二氧化碳气体中的二氧化硫气体,下列仪器和药品组合合理的是
仪器:①洗气瓶、②干燥管;
药品:③固态生石灰、④苏打溶液、⑤饱和小苏打溶液。
A.①⑤ B.②⑤ C.①③ D.①④
10.下列说法正确的是
A.向HClO溶液中通入SO2,生成H2SO4,证明H2SO4的酸性比HClO强
B.SO2、H2S为含硫化合物,都可用浓硫酸干燥
C.将SO2通入品红溶液,溶液褪色后加热恢复原色
D.蔗糖遇浓H2SO4后变黑,膨胀,最后产生刺激性气味气体,说明浓H2SO4具有脱水性、酸性和强氧化性
11.硫元素在自然界中的循环如图所示,下列说法错误的是
A.硫是组成某些蛋白质的生命元素
B.地壳中化合态的硫主要以硫化物和硫酸盐的形式存在
C.硫粉在过量的纯氧中燃烧可以生成SO3
D.化石燃料的燃烧以及含硫矿物的冶炼是大气SO2污染的主要来源
12.在可能含有、的溶液中,要检验是否存在,下列实验方法正确的是
A.取样,加溶液,有白色沉淀生成,则有
B.取样,加足量溶液,过滤后再加溶液,有白色沉淀,则有
C.取样,加入足量溶液,过滤后再加溶液,有白色沉淀,则有
D.取样,加入和混合溶液,有白色沉淀,则有
13.下列实验对应的化学用语正确的是
A.溶液中滴加溶液,静置一段时间后:
B.酸性氯化亚铁溶液中加入双氧水:
C.足量二氧化硫与氢氧化钠溶液反应:
D.澄清石灰水中加入过量溶液:
14.能正确表示下列反应的离子方程式的是
A.向澄清的石灰水中通入SO2气体:+SO2=CaSO3↓
B.过量SO2气体通入氢氧化钠溶液中:SO2+OH-=HSO
C.SO2气体通入溴水中:SO2+Br2+H2O=2H++2Br-+SO
D.向氢硫酸(H2S)中通入氯气:
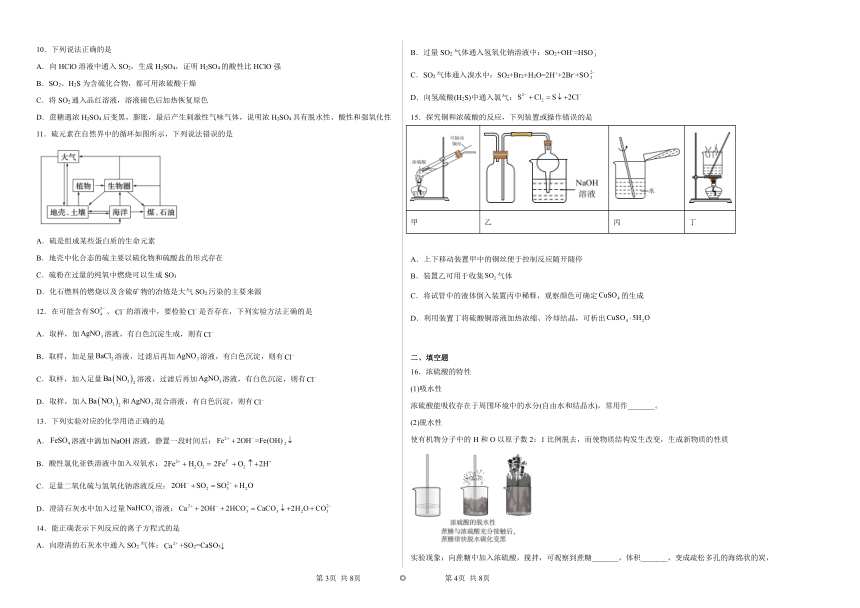
15.探究铜和浓硫酸的反应,下列装置或操作错误的是
甲 乙 丙 丁
A.上下移动装置甲中的铜丝便于控制反应随开随停
B.装置乙可用于收集气体
C.将试管中的液体倒入装置丙中稀释,观察颜色可确定的生成
D.利用装置丁将硫酸铜溶液加热浓缩、冷却结晶,可析出
二、填空题
16.浓硫酸的特性
(1)吸水性
浓硫酸能吸收存在于周围环境中的水分(自由水和结晶水),常用作_______。
(2)脱水性
使有机物分子中的H和O以原子数2:1比例脱去,而使物质结构发生改变,生成新物质的性质
实验现象:向蔗糖中加入浓硫酸,搅拌,可观察到蔗糖_______,体积_______,变成疏松多孔的海绵状的炭,并放出有_______气味的气体。反应化学方程式_______。
(3)强氧化性
①浓硫酸与Cu反应
实验操作
实验现象 铜丝表面_______,溶液中产生_______色固体;试管中的溶液有气泡冒出;品红溶液_______;冷却后将a试管里的物质慢慢倒入水中,溶液呈_______。
实验结论 在反应中,浓硫酸体现_______和酸性
化学方程式 _______
②浓硫酸与非金属反应
碳与浓硫酸反应_______。
③浓硫酸与金属反应
a.常温下,Fe、Al与浓H2SO4发生钝化,生成了致密的氧化膜。
b.氢前的活泼金属(如Zn):常温下与浓硫酸反应先产生_______,后产生_______。
c.氢后的活泼金属(如铜):加热下与浓硫酸反应先产生_______,后反应停止。
17.浓硫酸在常温下为黏稠状液体,且具有吸水性、脱水性和强氧化性。
(1)将浓硫酸敞口放置在空气中其质量会_______,溶质的质量分数会_______,本过程中浓硫酸表现出_______性。
(2)浓硫酸表现吸水性时,可作干燥剂,下列物质可用浓硫酸干燥的是_______。
A.NH3 B.H2S C.H2 D.SO2 E.O2 F.HI G.HBr
(3)用蘸有浓硫酸的玻璃棒在木板上写字,字迹一会儿就变黑。浓硫酸表现出_______性。
(4)在加热条件下,浓硫酸能与Cu、C等单质反应,表现强氧化性。请写出这两个化学反应的化学方程式,并指出与Cu反应时,浓硫酸除表现强氧化性外,还表现什么性质:_______。
(5)稀硫酸常用来洗涤金属表面的铁锈和铜锈,这是利用了硫酸的_______性,请写出有关反应的化学方程式:_______。
三、工业流程题
18.以高硫铝土矿(主要成分为、、少量和金属硫酸盐)为原料,生产氧化铝并获得的部分工艺流程如图所示,能溶于NaOH溶液,与NaOH溶液不反应。
(1)焙烧过程均会产生,用NaOH溶液吸收过量的离子方程式为_____________________。
(2)添加1%和不添加的矿粉焙烧,其硫去除率随温度变化曲线如图所示。
已知:多数金属硫酸盐的分解温度都高于;
。
①不添加CaO的矿粉在低于焙烧时,去除的硫元素主要来源于____________(填化学式)。
②焙烧时,添加1%的矿粉硫去除率比不添加的矿粉硫去除率低,其主要原因是_________________________。
19.焦亚硫酸钠(Na2S2O5)是葡萄酒中常用的抗氧化剂。一种以硫黄为原料制取Na2S2O5的生产工艺如下:
已知:结晶脱水发生的反应:
回答下列问题:
(1)Na2S2O5中硫元素的化合价为________。
(2)焚烧炉中反应的化学方程式为________________。
(3)反应器中发生反应的离子方程式为________________。
(4)葡萄酒酿造过程中添加Na2S2O5会放出一种有刺激性气味的气体,该气体是一种食品添加剂。实验室中检验该气体的常用试剂是________________。
(5)废水中的硫单质(S8)能与碱反应,化学反应:,反应中氧化剂与还原剂的物质的量之比为________。
第1页 共4页 ◎ 第2页 共4页
第1页 共4页 ◎ 第2页 共4页
参考答案:
1.C
【详解】A.若溶液中含有Ag+,同样的操作会看到相同的现象,A错误;
B.也有可能是或,B错误;
C.加足量盐酸时有气体产生说明含,再加溶液时有白色沉淀产生,说明有,则样品已部分被氧化,C正确;
D.使品红溶液褪色也可能是Cl2,D错误;
故选C。
2.D
【详解】A.反应①中先变蓝后褪色,说明KIO3先转化为I2后转化为I-,SO2体现还原性,A错误;
B.根据原子守恒,当n(Na2SO3)∶n(NaHSO3)=1∶1时,n(SO2)∶n(NaOH)=2∶3,B错误;
C.反应④不是氧化还原反应因为元素没有化合价变化,C错误;
D.利用反应②④,可以吸收SO2并回收利用,②中SO2作反应物,⑤中SO2为产物,D正确;
故选D。
3.B
【分析】常见漂白剂的漂白原理:Cl2、Na2O2、H2O2、O3等是因强氧化性而具有漂白性;SO2是能和有机色质化合生成无色物质;活性炭是因吸附有机色质而漂白。
【详解】A.SO2使溴水、酸性KMnO4溶液褪色是因为SO2具有还原性,能使品红褪色是因其具有漂白性,SO2不能使指示剂褪色,A错误;
B.因为能使品红褪色的物质很多,不仅仅是SO2,B正确;
C.因为这些漂白剂的漂白原理不相同,SO2漂白属于化合型,活性炭属于吸附型,漂白粉、Na2O2属于氧化型,C错误;
D.等物质的量的SO2和Cl2相遇在溶液中反应生成H2SO4和HCl,从而失去漂白能力,D错误;
故选B。
4.B
【详解】A.氯化钠固体与浓硫酸混合加热反应产生Na2SO4、HCl,反应类型是复分解反应,硫酸仅表现出酸性,A不符合题意;
B.铜与浓硫酸混合加热反应产生CuSO4、SO2、H2O,浓硫酸既表现出强氧化性,又表现出酸性,B符合题意;
C.碳与浓硫酸混合加热发生反应,产生CO2、SO2、H2O,浓硫酸仅表现强氧化性,C不符合题意;
D.CuO与稀硫酸反应产生CuSO4、H2O,浓硫酸仅表现出酸性,D不符合题意;
故合理选项是B。
5.C
【详解】A.浓硫酸溶于水会放出大量热量使溶液温度升高;而稀硫酸溶于水,没有明显的热量变化,温度几乎不变,因此可以通过分别取少量两种溶液加水稀释,比较热效应进行鉴别,A正确;
B.浓硫酸具有脱水性,能够使有机物脱水炭黑,而稀硫酸不具有脱水性,因此分别取少量两种溶液滴加到纸张上,观察纸张是否变黑,变黑的是浓硫酸,不能变黑的是稀硫酸,B正确;
C.二者溶于BaCl2溶液中都会电离产生,因此能够与溶液中的Ba2+结合形成BaSO4白色沉淀,因此不能使用BaCl2溶液进行鉴别,C错误;
D.在室温下铁遇浓硫酸会发生钝化现象而不能进一步反应,而铁加入稀硫酸中,会发生反应使铁片溶解,溶液变为浅绿色,同时产生气泡,二者现象不同,可以进行鉴别,D正确;
故合理选项是C。
6.D
【详解】A.浓硫酸具有吸水性,敞口放置时浓度减小,浓盐酸易挥发,敞口放置时浓度减小,二者本质不同,A错误;
B.SO2和有色物质生成不稳定无色物质而使品红溶液褪色,Cl2与水反应生成的次氯酸具有强氧化性而使品红溶液褪色,二者本质不同,B错误;
C.浓H2SO4与金属反应放出气体体现酸性和强氧化性,生成二氧化硫气体,稀H2SO4与金属反应生成氢气,二者本质不同,C错误;
D.H2S和HI气体均具有还原性,会被浓硫酸氧化而不能用浓硫酸干燥,二者本质相似,D正确;
故选D。
7.D
【详解】A.S燃烧生成二氧化硫, S不能一步转化为 SO3、H2SO4,则常温下不能发生图中转化,A错误;
B.Na在氧气中燃烧生成Na2O2,Na在常温下反应生成 Na2O,则常温下不能发生图中转化,故B错误;
C.Fe在氯气中点燃生成FeCl3,Fe在常温下不能一步生成 Fe(OH)2。,则常温下不能发生图中转化,故C错误;
D.常温下,Al溶于盐酸生成AlCl3,溶于氢氧化钠生成NaAlO2,溶于硫酸生成Al2(SO4)3,AlCl3和过量NaOH生成NaAlO2,NaAlO2和过量硫酸生成Al2(SO4)3,Al2(SO4)3和BaCl2生成AlCl3,常温下能实现图示转化,D正确;
故答案选D。
8.C
【详解】二氧化硫为酸性氧化物,在一定条件下二氧化硫能和、等反应生成硫酸银,达到固硫作用;硝酸铵、氯化镁不与二氧化硫反应,不能作固硫剂;
故选C。
9.A
【详解】洗气瓶与液态试剂对应,干燥管与固体试剂对应,小苏打是碳酸氢钠,苏打是碳酸钠;SO2既能与NaHCO3溶液反应,又能与Na2CO3溶液反应生成二氧化碳气体;CO2能与Na2CO3溶液反应,不能与NaHCO3溶液反应,所以可以利用饱和碳酸氢钠溶液除去二氧化硫;生石灰是固体,在干燥管中用来干燥气体,但二氧化硫和二氧化碳气体都和生石灰反应。综上所述,除去CO2气体中的SO2气体,下列对于仪器和药品为①⑤。
答案选A。
10.C
【详解】A.HClO具有强氧化性,SO2具有还原性,向HClO溶液中通入SO2,会发生氧化还原反应:HClO+SO2+H2O=H2SO4+HCl,生成H2SO4不能证明H2SO4的酸性比HClO强,A项错误;
B.H2S具有还原性,会与浓硫酸发生氧化还原反应,不可以用浓硫酸干燥,B项错误;
C.SO2漂白性是与有色物质不稳定的无色物质,故将SO2通入品红溶液,溶液褪色后加热恢复原色,C项正确;
D.蔗糖遇浓H2SO4后变黑,膨胀,说明浓H2SO4具有脱水性,产生刺激性气味气体SO2说明浓H2SO4具有强氧化性,该过程没有体现浓硫酸的酸性,D项错误;
答案选C。
11.C
【详解】A.蛋白质的组成元素主要有C、H、O、N,某些蛋白质还含有P、S等元素,A正确;
B.大多数硫化物和硫酸盐比较稳定,地壳中化合态的硫主要以硫化物和硫酸盐的形式存在,B正确;
C.硫粉在过量的纯氧中燃烧生成SO2,不能直接得到SO3,SO2进一步氧化得到SO3,C错误;
D.化石燃料、含硫矿物均含有硫元素,高温下与空气反应生成SO2,是大气SO2污染的主要来源,D正确;
故选C。
12.C
【分析】一般情况下,检验需要用溶液和溶液,但是的存在会干扰的检验,所以先用除去,再检验;此时已经没有其他的干扰离子,所以可以省略溶液;
【详解】A.直接加入溶液,生成的白色沉淀可能是,也可能是,无法确定是否含有,A错误;
B.加足量溶液,虽然可以除去,但是同时也加入了,干扰检验,B错误;
C.先加足量溶液,可除去,从而排除的干扰,过滤后再加溶液,产生了白色沉淀,可表明溶液中含有,C正确;
D.加入和混合溶液,可能生成、、白色沉淀,无法确定是否含有,D错误;
故合理选项为C。
13.D
【详解】A.Fe2+不稳定,易被空气中氧气氧化,正确反应式为:4Fe2++O2+2H2O+8OH-=4Fe(OH)3,A选项错误;
B.离子方程式要满足电荷守恒,正确反应式为:2Fe2++H2O2+2H+=2Fe3++2H2O,B选项错误;
C.足量SO2与碱反应生成酸式盐,正确反应式为:SO2+OH-=HSO,C选项错误;
D.依照“定少为1”,氢氧化钙不足,NaHCO3过量,D选项正确;
答案选D。
14.B
【详解】A.向澄清的石灰水中通入少量SO2气体,离子方程式是,向澄清的石灰水中通入过量SO2气体,离子方程式是,A项错误;
B.过量SO2气体通入氢氧化钠溶液中,离子方程式是,B项正确;
C.SO2气体通入溴水中,SO2化合价升高具有还原性,Br2具有氧化性,则离子方程式是,C项错误;
D.氢硫酸为弱电解质,通入氯气后发生氧化还原反应,则离子方程式是,D项错误;
答案选B。
15.B
【详解】A.Cu和浓硫酸在加热条件下反应可产生二氧化硫,上下移动装置甲中的铜丝可控制反应的发生和停止,从而控制SO2的生成,A正确;
B.SO2的的密度比空气大,可用向上排空气法收集,应采用长管进短管出,B错误;
C.含铜离子的溶液呈蓝色,可以将试管中的液体倒入水中稀释,根据溶液是否呈蓝色确定是否有CuSO4生成,C正确;;
D.结晶水合物加热时容易失去结晶水,不宜采取蒸发结晶的方法,硫酸铜溶液加热浓缩、冷却结晶可析出CuSO4 5H2O,D正确;
答案选B。
16.(1)干燥剂
(2) 变黑 膨胀 刺激性 C12H22O1112C+11H2O、C+2H2SO4(浓)CO2+2SO2+2H2O
(3) 有气泡产生 白 逐渐变为无色 蓝色 强氧化性 Cu+2H2SO4(浓)CuSO4+SO2+2H2O C+2H2SO4(浓)CO2+2SO2+2H2O SO2 H2 SO2
【详解】(1)浓硫酸能吸收存在于周围环境中的水分(自由水和结晶水),常用作干燥剂;
(2)浓硫酸具有脱水性和强氧化性:C12H22O1112C+11H2O、C+2H2SO4(浓)CO2+2SO2+2H2O,故向蔗糖中加入浓硫酸,搅拌,可观察到蔗糖变黑,体积膨胀,变成疏松多孔的海绵状的炭,并放出有有刺激性气味的气体;
(3)铜丝表面产生气泡,溶液中产生白色固体;试管中的溶液有气泡冒出;品红溶液褪色;冷却后将a试管里的物质慢慢倒入水中,溶液呈蓝色,Cu+2H2SO4(浓)CuSO4+SO2+2H2O,浓硫酸体现了强氧化性和酸性;浓硫酸还可以与非金属反应:C+2H2SO4(浓)CO2+2SO2+2H2O;量变引发质量,浓硫酸在反应中逐渐变稀,与氢前的活泼金属(如Zn):常温下与浓硫酸反应先产生二氧化硫,后产生氢气;与氢后的活泼金属(如铜):加热下与浓硫酸反应先产生二氧化硫,后反应停止。
17.(1) 增加 减小 吸水
(2)CDE
(3)脱水
(4)Cu+2H2SO4(浓) CuSO4+SO2↑+2H2O,C+2H2SO4(浓) CO2↑+2SO2↑+2H2O;与 Cu反应时,浓硫酸还表现酸性
(5) 酸 3H2SO4+Fe2O3=Fe2(SO4)3+3H2O,2H2SO4+Cu2(OH)2CO3=2CuSO4+CO2↑+3H2O
【详解】(1)由于浓硫酸具有吸水性,所以将其敞口放置在空气中溶液质量会增加,溶质质量分数会减小。
(2)浓硫酸具有酸性和强氧化性,因此,A、B、F、G均不能用浓硫酸进行干燥,故选CDE。
(3)因浓硫酸具有脱水性,它能按水的组成夺取木材中的氢元素和氧元素,所以,字迹一会儿就变黑。
(4)浓硫酸在加热的条件下与金属铜和非金属C发生反应,Cu+2H2SO4(浓) CuSO4+SO2↑+2H2O,C+2H2SO4(浓) CO2↑+2SO2↑+2H2O;均体现了浓硫酸的强氧化性,但与Cu发生反应时,浓硫酸还表现出了酸性。
(5)铜锈的主要成分是Cu2(OH)2CO3,铁锈的主要成分是Fe2O3,稀硫酸具有酸性;与二者反应生成可溶性物质3H2SO4+Fe2O3=Fe2(SO4)3+3H2O,2H2SO4+Cu2(OH)2CO3=2CuSO4+CO2↑+3H2O。
18. 硫元素转化为而留在矿粉中
【分析】高硫铝土矿(主要成分为、、少量和金属硫酸盐)焙烧时发生反应,生成的在空气中与反应生成,碱浸时转化为溶于水的NaAlO2,过滤得到,与混合后在缺氧条件下生成和。
【详解】(1)二氧化硫是酸性氧化物,少量二氧化硫与NaOH溶液反应可生成,过量二氧化硫与NaOH溶液反应可生成,离子方程式为。
(2)①高硫铝土矿的成分中含和金属硫酸盐,而已知多数金属硫酸盐的分解温度都高于,如果不添加CaO的矿粉在低于焙烧,则去除的硫元素主要来源于,具体的反应原理为。
②添加的CaO吸收生成,易被空气中的氧气氧化为,根据“多数金属硫酸盐的分解温度都高于”,可知时可能未分解或未完全分解而留在矿粉中,从而导致添加1%的矿粉硫去除率比不添加的矿粉硫去除率低,故答案为硫元素转化为而留在矿粉中。
19. +4 品红溶液 2:1
【分析】硫磺在空气中燃烧生成,在洗涤塔中溶于水得到亚硫酸,经除杂后与反应得到,再经题目给出的反应式结晶脱水即可得到产物。
【详解】(1)钠为+1价,氧为-2价,则硫只能是+4价;
(2)焚烧炉里实际就是硫在空气中燃烧:;
(3)根据分析,反应器中实际上是亚硫酸和的反应:;
(4)这种刺激性气味的气体就是,实验室中可用品红溶液来检验,若能使品红褪色且加热后能复原,即可证明是;
(5)不难看出这是一个硫的歧化反应,有16个硫的化合价从0价降低到-2价,有8个硫的化合价从0价升高到+4价,因此氧化剂与还原剂的物质的量之比为16:8,即2:1。
答案第1页,共2页
答案第1页,共2页
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1.下列物质的检验中,其结论一定正确的是
A.向某溶液中加入溶液,产生白色沉淀,加入稀后,白色沉淀不溶解,也无其他现象,说明原溶液中一定含有
B.向某溶液中加入盐酸产生无色气体,该气体能使澄清的石灰水变浑浊,说明该溶液中一定含有或
C.取少量久置的样品于试管中加水溶解,再加足量盐酸酸化,然后加溶液,若加盐酸时有气体产生,加溶液时有白色沉淀产生,说明样品已部分被氧化
D.将某气体通入品红溶液中,品红溶液褪色,该气体一定是
2.如图所示是一系列含硫化合物的转化关系(反应中生成的水已略去),其中说法正确的是
A.反应①说明SO2具有氧化性,反应②说明SO2具有酸性
B.反应②中生成物n(Na2SO3)∶n(NaHSO3)=1∶1时,则反应物n(SO2)∶n(NaOH)=1∶2
C.反应③④⑤均属于氧化还原反应
D.工业上可利用反应②和反应④回收SO2
3.下列说法正确的是
A.因为SO2具有漂白性,所以它能使品红溶液、溴水、KMnO4(H+)、石蕊溶液褪色
B.能使品红溶液褪色的不一定是SO2
C.SO2、漂白粉、活性炭、Na2O2都能使红墨水褪色,其原理相同
D.等物质的量的SO2和Cl2相遇在溶液中具有漂白能力
4.下列反应中,硫酸既表现出强氧化性,又表现出酸性的是
A.氯化钠固体与浓硫酸反应 B.铜与浓硫酸反应
C.碳与浓硫酸反应 D.CuO与稀硫酸反应
5.现有两瓶无色溶液,分别是稀硫酸和浓硫酸。下列方法不能将它们鉴别出来的是
A.分别取少量两种溶液加水稀释,比较热效应
B.分别取少量两种溶液滴加到纸张上,观察纸张是否变黑
C.分别取少量两种溶液滴加BaCl2溶液,观察是否产生白色沉淀
D.分别取足量两种溶液向其中加入铁片,一段时间后观察铁片是否溶解
6.下列变化的本质相似的是
A.浓硫酸和浓盐酸在空气中敞口放置时浓度均减小
B.SO2和Cl2均能能使品红溶液褪色
C.浓H2SO4和稀H2SO4与金属反应时均有气体放出
D.H2S和HI气体均不能用浓硫酸干燥
7.如图W、X、Y、Z为四种物质,若箭头表示能一步转化的常见反应,其中常温下能实现图示转化关系的是
选项 W X Y Z
A S SO2 SO3 H2SO4
B Na Na2O2 NaOH NaCl
C Fe FeCl3 Fe(OH)2 FeCl2
D Al AlCl3 NaAlO2 Al2(SO4)3
A.A B.B C.C D.D
8.固硫剂能把含硫燃料燃烧生成的二氧化硫转化成盐的形式固定在炉渣中。下列选项的物质组合中,各种试剂均可用作固硫剂的是
① ② ③ ④
A.① B.②③ C.①③ D.①②③④
9.为了除去二氧化碳气体中的二氧化硫气体,下列仪器和药品组合合理的是
仪器:①洗气瓶、②干燥管;
药品:③固态生石灰、④苏打溶液、⑤饱和小苏打溶液。
A.①⑤ B.②⑤ C.①③ D.①④
10.下列说法正确的是
A.向HClO溶液中通入SO2,生成H2SO4,证明H2SO4的酸性比HClO强
B.SO2、H2S为含硫化合物,都可用浓硫酸干燥
C.将SO2通入品红溶液,溶液褪色后加热恢复原色
D.蔗糖遇浓H2SO4后变黑,膨胀,最后产生刺激性气味气体,说明浓H2SO4具有脱水性、酸性和强氧化性
11.硫元素在自然界中的循环如图所示,下列说法错误的是
A.硫是组成某些蛋白质的生命元素
B.地壳中化合态的硫主要以硫化物和硫酸盐的形式存在
C.硫粉在过量的纯氧中燃烧可以生成SO3
D.化石燃料的燃烧以及含硫矿物的冶炼是大气SO2污染的主要来源
12.在可能含有、的溶液中,要检验是否存在,下列实验方法正确的是
A.取样,加溶液,有白色沉淀生成,则有
B.取样,加足量溶液,过滤后再加溶液,有白色沉淀,则有
C.取样,加入足量溶液,过滤后再加溶液,有白色沉淀,则有
D.取样,加入和混合溶液,有白色沉淀,则有
13.下列实验对应的化学用语正确的是
A.溶液中滴加溶液,静置一段时间后:
B.酸性氯化亚铁溶液中加入双氧水:
C.足量二氧化硫与氢氧化钠溶液反应:
D.澄清石灰水中加入过量溶液:
14.能正确表示下列反应的离子方程式的是
A.向澄清的石灰水中通入SO2气体:+SO2=CaSO3↓
B.过量SO2气体通入氢氧化钠溶液中:SO2+OH-=HSO
C.SO2气体通入溴水中:SO2+Br2+H2O=2H++2Br-+SO
D.向氢硫酸(H2S)中通入氯气:
15.探究铜和浓硫酸的反应,下列装置或操作错误的是
甲 乙 丙 丁
A.上下移动装置甲中的铜丝便于控制反应随开随停
B.装置乙可用于收集气体
C.将试管中的液体倒入装置丙中稀释,观察颜色可确定的生成
D.利用装置丁将硫酸铜溶液加热浓缩、冷却结晶,可析出
二、填空题
16.浓硫酸的特性
(1)吸水性
浓硫酸能吸收存在于周围环境中的水分(自由水和结晶水),常用作_______。
(2)脱水性
使有机物分子中的H和O以原子数2:1比例脱去,而使物质结构发生改变,生成新物质的性质
实验现象:向蔗糖中加入浓硫酸,搅拌,可观察到蔗糖_______,体积_______,变成疏松多孔的海绵状的炭,并放出有_______气味的气体。反应化学方程式_______。
(3)强氧化性
①浓硫酸与Cu反应
实验操作
实验现象 铜丝表面_______,溶液中产生_______色固体;试管中的溶液有气泡冒出;品红溶液_______;冷却后将a试管里的物质慢慢倒入水中,溶液呈_______。
实验结论 在反应中,浓硫酸体现_______和酸性
化学方程式 _______
②浓硫酸与非金属反应
碳与浓硫酸反应_______。
③浓硫酸与金属反应
a.常温下,Fe、Al与浓H2SO4发生钝化,生成了致密的氧化膜。
b.氢前的活泼金属(如Zn):常温下与浓硫酸反应先产生_______,后产生_______。
c.氢后的活泼金属(如铜):加热下与浓硫酸反应先产生_______,后反应停止。
17.浓硫酸在常温下为黏稠状液体,且具有吸水性、脱水性和强氧化性。
(1)将浓硫酸敞口放置在空气中其质量会_______,溶质的质量分数会_______,本过程中浓硫酸表现出_______性。
(2)浓硫酸表现吸水性时,可作干燥剂,下列物质可用浓硫酸干燥的是_______。
A.NH3 B.H2S C.H2 D.SO2 E.O2 F.HI G.HBr
(3)用蘸有浓硫酸的玻璃棒在木板上写字,字迹一会儿就变黑。浓硫酸表现出_______性。
(4)在加热条件下,浓硫酸能与Cu、C等单质反应,表现强氧化性。请写出这两个化学反应的化学方程式,并指出与Cu反应时,浓硫酸除表现强氧化性外,还表现什么性质:_______。
(5)稀硫酸常用来洗涤金属表面的铁锈和铜锈,这是利用了硫酸的_______性,请写出有关反应的化学方程式:_______。
三、工业流程题
18.以高硫铝土矿(主要成分为、、少量和金属硫酸盐)为原料,生产氧化铝并获得的部分工艺流程如图所示,能溶于NaOH溶液,与NaOH溶液不反应。
(1)焙烧过程均会产生,用NaOH溶液吸收过量的离子方程式为_____________________。
(2)添加1%和不添加的矿粉焙烧,其硫去除率随温度变化曲线如图所示。
已知:多数金属硫酸盐的分解温度都高于;
。
①不添加CaO的矿粉在低于焙烧时,去除的硫元素主要来源于____________(填化学式)。
②焙烧时,添加1%的矿粉硫去除率比不添加的矿粉硫去除率低,其主要原因是_________________________。
19.焦亚硫酸钠(Na2S2O5)是葡萄酒中常用的抗氧化剂。一种以硫黄为原料制取Na2S2O5的生产工艺如下:
已知:结晶脱水发生的反应:
回答下列问题:
(1)Na2S2O5中硫元素的化合价为________。
(2)焚烧炉中反应的化学方程式为________________。
(3)反应器中发生反应的离子方程式为________________。
(4)葡萄酒酿造过程中添加Na2S2O5会放出一种有刺激性气味的气体,该气体是一种食品添加剂。实验室中检验该气体的常用试剂是________________。
(5)废水中的硫单质(S8)能与碱反应,化学反应:,反应中氧化剂与还原剂的物质的量之比为________。
第1页 共4页 ◎ 第2页 共4页
第1页 共4页 ◎ 第2页 共4页
参考答案:
1.C
【详解】A.若溶液中含有Ag+,同样的操作会看到相同的现象,A错误;
B.也有可能是或,B错误;
C.加足量盐酸时有气体产生说明含,再加溶液时有白色沉淀产生,说明有,则样品已部分被氧化,C正确;
D.使品红溶液褪色也可能是Cl2,D错误;
故选C。
2.D
【详解】A.反应①中先变蓝后褪色,说明KIO3先转化为I2后转化为I-,SO2体现还原性,A错误;
B.根据原子守恒,当n(Na2SO3)∶n(NaHSO3)=1∶1时,n(SO2)∶n(NaOH)=2∶3,B错误;
C.反应④不是氧化还原反应因为元素没有化合价变化,C错误;
D.利用反应②④,可以吸收SO2并回收利用,②中SO2作反应物,⑤中SO2为产物,D正确;
故选D。
3.B
【分析】常见漂白剂的漂白原理:Cl2、Na2O2、H2O2、O3等是因强氧化性而具有漂白性;SO2是能和有机色质化合生成无色物质;活性炭是因吸附有机色质而漂白。
【详解】A.SO2使溴水、酸性KMnO4溶液褪色是因为SO2具有还原性,能使品红褪色是因其具有漂白性,SO2不能使指示剂褪色,A错误;
B.因为能使品红褪色的物质很多,不仅仅是SO2,B正确;
C.因为这些漂白剂的漂白原理不相同,SO2漂白属于化合型,活性炭属于吸附型,漂白粉、Na2O2属于氧化型,C错误;
D.等物质的量的SO2和Cl2相遇在溶液中反应生成H2SO4和HCl,从而失去漂白能力,D错误;
故选B。
4.B
【详解】A.氯化钠固体与浓硫酸混合加热反应产生Na2SO4、HCl,反应类型是复分解反应,硫酸仅表现出酸性,A不符合题意;
B.铜与浓硫酸混合加热反应产生CuSO4、SO2、H2O,浓硫酸既表现出强氧化性,又表现出酸性,B符合题意;
C.碳与浓硫酸混合加热发生反应,产生CO2、SO2、H2O,浓硫酸仅表现强氧化性,C不符合题意;
D.CuO与稀硫酸反应产生CuSO4、H2O,浓硫酸仅表现出酸性,D不符合题意;
故合理选项是B。
5.C
【详解】A.浓硫酸溶于水会放出大量热量使溶液温度升高;而稀硫酸溶于水,没有明显的热量变化,温度几乎不变,因此可以通过分别取少量两种溶液加水稀释,比较热效应进行鉴别,A正确;
B.浓硫酸具有脱水性,能够使有机物脱水炭黑,而稀硫酸不具有脱水性,因此分别取少量两种溶液滴加到纸张上,观察纸张是否变黑,变黑的是浓硫酸,不能变黑的是稀硫酸,B正确;
C.二者溶于BaCl2溶液中都会电离产生,因此能够与溶液中的Ba2+结合形成BaSO4白色沉淀,因此不能使用BaCl2溶液进行鉴别,C错误;
D.在室温下铁遇浓硫酸会发生钝化现象而不能进一步反应,而铁加入稀硫酸中,会发生反应使铁片溶解,溶液变为浅绿色,同时产生气泡,二者现象不同,可以进行鉴别,D正确;
故合理选项是C。
6.D
【详解】A.浓硫酸具有吸水性,敞口放置时浓度减小,浓盐酸易挥发,敞口放置时浓度减小,二者本质不同,A错误;
B.SO2和有色物质生成不稳定无色物质而使品红溶液褪色,Cl2与水反应生成的次氯酸具有强氧化性而使品红溶液褪色,二者本质不同,B错误;
C.浓H2SO4与金属反应放出气体体现酸性和强氧化性,生成二氧化硫气体,稀H2SO4与金属反应生成氢气,二者本质不同,C错误;
D.H2S和HI气体均具有还原性,会被浓硫酸氧化而不能用浓硫酸干燥,二者本质相似,D正确;
故选D。
7.D
【详解】A.S燃烧生成二氧化硫, S不能一步转化为 SO3、H2SO4,则常温下不能发生图中转化,A错误;
B.Na在氧气中燃烧生成Na2O2,Na在常温下反应生成 Na2O,则常温下不能发生图中转化,故B错误;
C.Fe在氯气中点燃生成FeCl3,Fe在常温下不能一步生成 Fe(OH)2。,则常温下不能发生图中转化,故C错误;
D.常温下,Al溶于盐酸生成AlCl3,溶于氢氧化钠生成NaAlO2,溶于硫酸生成Al2(SO4)3,AlCl3和过量NaOH生成NaAlO2,NaAlO2和过量硫酸生成Al2(SO4)3,Al2(SO4)3和BaCl2生成AlCl3,常温下能实现图示转化,D正确;
故答案选D。
8.C
【详解】二氧化硫为酸性氧化物,在一定条件下二氧化硫能和、等反应生成硫酸银,达到固硫作用;硝酸铵、氯化镁不与二氧化硫反应,不能作固硫剂;
故选C。
9.A
【详解】洗气瓶与液态试剂对应,干燥管与固体试剂对应,小苏打是碳酸氢钠,苏打是碳酸钠;SO2既能与NaHCO3溶液反应,又能与Na2CO3溶液反应生成二氧化碳气体;CO2能与Na2CO3溶液反应,不能与NaHCO3溶液反应,所以可以利用饱和碳酸氢钠溶液除去二氧化硫;生石灰是固体,在干燥管中用来干燥气体,但二氧化硫和二氧化碳气体都和生石灰反应。综上所述,除去CO2气体中的SO2气体,下列对于仪器和药品为①⑤。
答案选A。
10.C
【详解】A.HClO具有强氧化性,SO2具有还原性,向HClO溶液中通入SO2,会发生氧化还原反应:HClO+SO2+H2O=H2SO4+HCl,生成H2SO4不能证明H2SO4的酸性比HClO强,A项错误;
B.H2S具有还原性,会与浓硫酸发生氧化还原反应,不可以用浓硫酸干燥,B项错误;
C.SO2漂白性是与有色物质不稳定的无色物质,故将SO2通入品红溶液,溶液褪色后加热恢复原色,C项正确;
D.蔗糖遇浓H2SO4后变黑,膨胀,说明浓H2SO4具有脱水性,产生刺激性气味气体SO2说明浓H2SO4具有强氧化性,该过程没有体现浓硫酸的酸性,D项错误;
答案选C。
11.C
【详解】A.蛋白质的组成元素主要有C、H、O、N,某些蛋白质还含有P、S等元素,A正确;
B.大多数硫化物和硫酸盐比较稳定,地壳中化合态的硫主要以硫化物和硫酸盐的形式存在,B正确;
C.硫粉在过量的纯氧中燃烧生成SO2,不能直接得到SO3,SO2进一步氧化得到SO3,C错误;
D.化石燃料、含硫矿物均含有硫元素,高温下与空气反应生成SO2,是大气SO2污染的主要来源,D正确;
故选C。
12.C
【分析】一般情况下,检验需要用溶液和溶液,但是的存在会干扰的检验,所以先用除去,再检验;此时已经没有其他的干扰离子,所以可以省略溶液;
【详解】A.直接加入溶液,生成的白色沉淀可能是,也可能是,无法确定是否含有,A错误;
B.加足量溶液,虽然可以除去,但是同时也加入了,干扰检验,B错误;
C.先加足量溶液,可除去,从而排除的干扰,过滤后再加溶液,产生了白色沉淀,可表明溶液中含有,C正确;
D.加入和混合溶液,可能生成、、白色沉淀,无法确定是否含有,D错误;
故合理选项为C。
13.D
【详解】A.Fe2+不稳定,易被空气中氧气氧化,正确反应式为:4Fe2++O2+2H2O+8OH-=4Fe(OH)3,A选项错误;
B.离子方程式要满足电荷守恒,正确反应式为:2Fe2++H2O2+2H+=2Fe3++2H2O,B选项错误;
C.足量SO2与碱反应生成酸式盐,正确反应式为:SO2+OH-=HSO,C选项错误;
D.依照“定少为1”,氢氧化钙不足,NaHCO3过量,D选项正确;
答案选D。
14.B
【详解】A.向澄清的石灰水中通入少量SO2气体,离子方程式是,向澄清的石灰水中通入过量SO2气体,离子方程式是,A项错误;
B.过量SO2气体通入氢氧化钠溶液中,离子方程式是,B项正确;
C.SO2气体通入溴水中,SO2化合价升高具有还原性,Br2具有氧化性,则离子方程式是,C项错误;
D.氢硫酸为弱电解质,通入氯气后发生氧化还原反应,则离子方程式是,D项错误;
答案选B。
15.B
【详解】A.Cu和浓硫酸在加热条件下反应可产生二氧化硫,上下移动装置甲中的铜丝可控制反应的发生和停止,从而控制SO2的生成,A正确;
B.SO2的的密度比空气大,可用向上排空气法收集,应采用长管进短管出,B错误;
C.含铜离子的溶液呈蓝色,可以将试管中的液体倒入水中稀释,根据溶液是否呈蓝色确定是否有CuSO4生成,C正确;;
D.结晶水合物加热时容易失去结晶水,不宜采取蒸发结晶的方法,硫酸铜溶液加热浓缩、冷却结晶可析出CuSO4 5H2O,D正确;
答案选B。
16.(1)干燥剂
(2) 变黑 膨胀 刺激性 C12H22O1112C+11H2O、C+2H2SO4(浓)CO2+2SO2+2H2O
(3) 有气泡产生 白 逐渐变为无色 蓝色 强氧化性 Cu+2H2SO4(浓)CuSO4+SO2+2H2O C+2H2SO4(浓)CO2+2SO2+2H2O SO2 H2 SO2
【详解】(1)浓硫酸能吸收存在于周围环境中的水分(自由水和结晶水),常用作干燥剂;
(2)浓硫酸具有脱水性和强氧化性:C12H22O1112C+11H2O、C+2H2SO4(浓)CO2+2SO2+2H2O,故向蔗糖中加入浓硫酸,搅拌,可观察到蔗糖变黑,体积膨胀,变成疏松多孔的海绵状的炭,并放出有有刺激性气味的气体;
(3)铜丝表面产生气泡,溶液中产生白色固体;试管中的溶液有气泡冒出;品红溶液褪色;冷却后将a试管里的物质慢慢倒入水中,溶液呈蓝色,Cu+2H2SO4(浓)CuSO4+SO2+2H2O,浓硫酸体现了强氧化性和酸性;浓硫酸还可以与非金属反应:C+2H2SO4(浓)CO2+2SO2+2H2O;量变引发质量,浓硫酸在反应中逐渐变稀,与氢前的活泼金属(如Zn):常温下与浓硫酸反应先产生二氧化硫,后产生氢气;与氢后的活泼金属(如铜):加热下与浓硫酸反应先产生二氧化硫,后反应停止。
17.(1) 增加 减小 吸水
(2)CDE
(3)脱水
(4)Cu+2H2SO4(浓) CuSO4+SO2↑+2H2O,C+2H2SO4(浓) CO2↑+2SO2↑+2H2O;与 Cu反应时,浓硫酸还表现酸性
(5) 酸 3H2SO4+Fe2O3=Fe2(SO4)3+3H2O,2H2SO4+Cu2(OH)2CO3=2CuSO4+CO2↑+3H2O
【详解】(1)由于浓硫酸具有吸水性,所以将其敞口放置在空气中溶液质量会增加,溶质质量分数会减小。
(2)浓硫酸具有酸性和强氧化性,因此,A、B、F、G均不能用浓硫酸进行干燥,故选CDE。
(3)因浓硫酸具有脱水性,它能按水的组成夺取木材中的氢元素和氧元素,所以,字迹一会儿就变黑。
(4)浓硫酸在加热的条件下与金属铜和非金属C发生反应,Cu+2H2SO4(浓) CuSO4+SO2↑+2H2O,C+2H2SO4(浓) CO2↑+2SO2↑+2H2O;均体现了浓硫酸的强氧化性,但与Cu发生反应时,浓硫酸还表现出了酸性。
(5)铜锈的主要成分是Cu2(OH)2CO3,铁锈的主要成分是Fe2O3,稀硫酸具有酸性;与二者反应生成可溶性物质3H2SO4+Fe2O3=Fe2(SO4)3+3H2O,2H2SO4+Cu2(OH)2CO3=2CuSO4+CO2↑+3H2O。
18. 硫元素转化为而留在矿粉中
【分析】高硫铝土矿(主要成分为、、少量和金属硫酸盐)焙烧时发生反应,生成的在空气中与反应生成,碱浸时转化为溶于水的NaAlO2,过滤得到,与混合后在缺氧条件下生成和。
【详解】(1)二氧化硫是酸性氧化物,少量二氧化硫与NaOH溶液反应可生成,过量二氧化硫与NaOH溶液反应可生成,离子方程式为。
(2)①高硫铝土矿的成分中含和金属硫酸盐,而已知多数金属硫酸盐的分解温度都高于,如果不添加CaO的矿粉在低于焙烧,则去除的硫元素主要来源于,具体的反应原理为。
②添加的CaO吸收生成,易被空气中的氧气氧化为,根据“多数金属硫酸盐的分解温度都高于”,可知时可能未分解或未完全分解而留在矿粉中,从而导致添加1%的矿粉硫去除率比不添加的矿粉硫去除率低,故答案为硫元素转化为而留在矿粉中。
19. +4 品红溶液 2:1
【分析】硫磺在空气中燃烧生成,在洗涤塔中溶于水得到亚硫酸,经除杂后与反应得到,再经题目给出的反应式结晶脱水即可得到产物。
【详解】(1)钠为+1价,氧为-2价,则硫只能是+4价;
(2)焚烧炉里实际就是硫在空气中燃烧:;
(3)根据分析,反应器中实际上是亚硫酸和的反应:;
(4)这种刺激性气味的气体就是,实验室中可用品红溶液来检验,若能使品红褪色且加热后能复原,即可证明是;
(5)不难看出这是一个硫的歧化反应,有16个硫的化合价从0价降低到-2价,有8个硫的化合价从0价升高到+4价,因此氧化剂与还原剂的物质的量之比为16:8,即2:1。
答案第1页,共2页
答案第1页,共2页
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
