第五章第二节氮及其化合物同步练习 (含解析)2022-2023学年下学期高一化学人教版(2019)必修第二册
文档属性
| 名称 | 第五章第二节氮及其化合物同步练习 (含解析)2022-2023学年下学期高一化学人教版(2019)必修第二册 |

|
|
| 格式 | docx | ||
| 文件大小 | 262.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-06-21 00:00:00 | ||
图片预览



文档简介
第五章第二节氮及其化合物同步练习
一、单选题
1. 下列说法错误的是( )
A. 氯气使溶液变黄,被还原
B. 将铁屑放入稀中证明比活泼
C. 、的某些单质或两元素之间形成的某些化合物可作水的消毒剂
D. 使溴水褪色与乙烯使溶液褪色的原理相同
2. 对于和的混合溶液,若和物质的量浓度存在如下关系:,理论上最多能溶解铜的物质的量为 ( )
A. B. C. D.
3. 将等物质的量的铁和铜的混合物与稀硝酸恰好完全反应,生成标准状况,向反应后的溶液中加入溶液使金属离子恰好沉淀,过滤。下列有关说法错误的是
A. 混合物溶解后的溶液中 B. 稀硝酸的物质的量浓度是
C. 需加入溶液 D. 最后所得沉淀在空气中充分加热可得固体
4. 下列说法不正确的是( )
A. 工业盐酸呈黄色是溶解在其中的的颜色
B. 可作为潜水艇的供氧剂
C. 二氧化硫是酸性氧化物,可用作食品添加剂
D. 硝酸浓度不同,与金属反应的产物也不同
5. 下列关于氮及其化合物说法,不正确的是( )
A. 氮气在通常情况下不燃烧,也不支持燃烧,不能供给呼吸
B. 可用作航天飞机的燃料
C. 碳酸氢铵常用作氮肥,可与碱性肥料混用
D. 硝酸可用于制造染料、炸药等
6. 如图是某元素的价一类二维图。其中正盐与反应可生成,的相对分子质量比大。下列说法正确的是
A. 可经催化氧化生成
B. 和都可用排水法收集
C. 的浓溶液具有吸水性,可用来干燥气体
D. 实验室制备时,可以将其浓溶液滴入碱石灰中进行制取
7. 下列叙述 正 确的有( )
、、都是形成酸雨的因素,都能和水反应生成酸
、均不能用浓硫酸干燥
水晶的主要成分是
与都属于酸性氧化物,都不能与酸反应
实验室可用溶液处理和废气
只能用排水集气法收集,不能用排空气法收集;而只能用排空气法收集,不能用排水集气法.
A. 项 B. 项 C. 项 D. 项
8. 将一包由、和组成的混合物均分成两份:一份混合物在加热条件下与充分反应,将固体全部转化成铜粉时固体质量减少了;向另一份混合物中加入溶液恰好完全反应生成和假设不产生其他还原产物,这些和标准状况混合并通入足量水中,气体全部被吸收生成。则该硝酸的物质的量浓度为( )
A. B. C. D.
9. 谚语“雷雨发庄稼”不包括下列哪个化学反应 反应条件已忽略
A. B.
C. D.
10. 下列关于含氮化合物的性质叙述正确的是( )
A. 与水发生化合反应生成
B. 与气体反应生成属于氮的固定
C. 实验室可用加热固体的方法制备
D. 见光易分解,实验室用棕色试剂瓶盛放浓
11. 下列关于氮及其化合物的说法正确的是( )
A. 实验中常用排水法收集气体
B. 久置的浓硝酸会变为稀硝酸
C. 与空气中的氧气反应生成属于氮的固定
D. 稀硝酸与铁反应而浓硝酸不与铁反应
12. 探究氨气及铵盐性质中,下列根据实验现象得出的结论不正确的是( )
A. 将有氨气的试管倒扣水中,液体迅速充满试管,说明氨气极易溶于水
B. 将红热的丝伸入如上图所示的锥形瓶中,瓶口出现少量的红棕色气体,说明氨气催化氧化的产物中有
C. 加热固体,观察到固体逐渐减少,试管口有液滴产生,说明具有热不稳定性
D. 充分反应后,锥形瓶内有存在
13. 某实验过程如图所示,则试管中的现象是。( )
A. 无明显现象,因稀不与铜反应
B. 铜片溶解,产生无色气体,该气体遇到空气不变色
C. 铜片溶解,产生红棕色、有刺激性气味的气体
D. 铜片溶解,产生无色气体,该气体在液面上方变为红棕色
14. 探究氨气及铵盐性质的过程中,下列根据实验现象得出的结论不正确的是 ( )
A. 将集有氨气的试管倒扣于水槽中,液体迅速充满试管,说明氨气极易溶于水
B. 将湿润的红色石蕊试纸放入集有氨气的集气瓶中,试纸由红色变为蓝色,说明氨水呈碱性
C. 加热固体,观察到固体逐渐减少,试管口有液滴产生,说明受热不稳定
D. 将红热的丝伸入如图所示的锥形瓶中,瓶口出现少量红棕色气体,说明氨气的直接氧化产物为2
15. 研究氮及其化合物的性质,可以有效改善人类的生存环境。氮元素化合价物质类别关系图如下,图中、、和分别代表一种含氮化合物。
下列说法中正确的是( )
A. 催化氧化可以生成
B. 从化合价角度分析,与能发生氧化还原反应。
C. 从物质类别角度分析,可以和、、发生反应
D. 转化过程中物质类别和化合价均发生变化
二、实验题
16. 装置Ⅰ和装置Ⅱ是有关硝酸和铜反应的实验装置示意图。
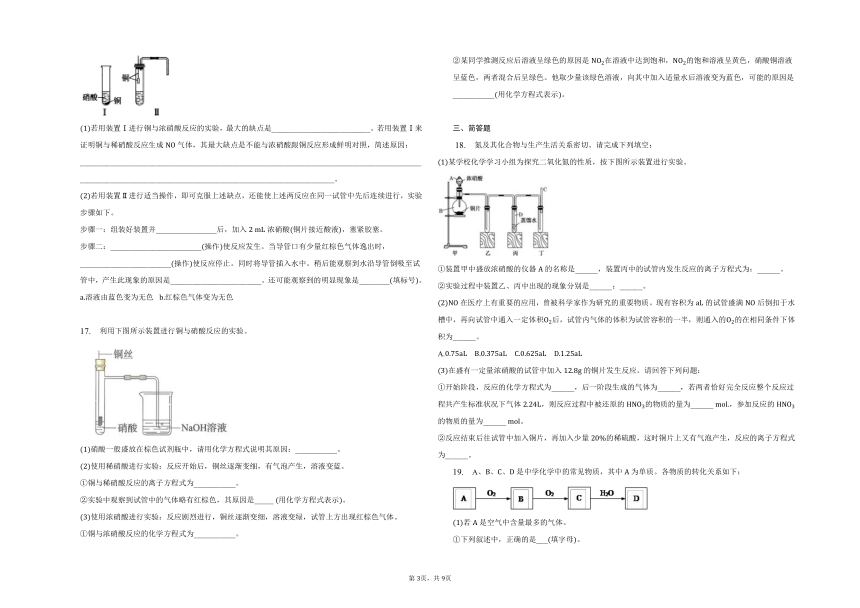
若用装置Ⅰ进行铜与浓硝酸反应的实验,最大的缺点是__________________________。若用装置Ⅰ来证明铜与稀硝酸反应生成气体,其最大缺点是不能与浓硝酸跟铜反应形成鲜明对照,简述原因:_____________________________________________________________________________________________________________________________________________________________。
若用装置Ⅱ进行适当操作,即可克服上述缺点,还能使上述两反应在同一试管中先后连续进行,实验步骤如下。
步骤一:组装好装置并________________后,加入浓硝酸铜片接近酸液,塞紧胶塞。
步骤二:________________________操作使反应发生。当导管口有少量红棕色气体逸出时,________________________操作使反应停止。同时将导管插入水中。稍后能观察到水沿导管倒吸至试管中,产生此现象的原因是________________________。还可能观察到的明显现象是________填标号。
溶液由蓝色变为无色 红棕色气体变为无色
17. 利用下图所示装置进行铜与硝酸反应的实验。
硝酸一般盛放在棕色试剂瓶中,请用化学方程式说明其原因:___________。
使用稀硝酸进行实验:反应开始后,铜丝逐渐变细,有气泡产生,溶液变蓝。
铜与稀硝酸反应的离子方程式为___________。
实验中观察到试管中的气体略有红棕色,其原因是_____用化学方程式表示。
使用浓硝酸进行实验:反应剧烈进行,铜丝逐渐变细,溶液变绿,试管上方出现红棕色气体。
铜与浓硝酸反应的化学方程式为___________。
某同学推测反应后溶液呈绿色的原因是在溶液中达到饱和,的饱和溶液呈黄色,硝酸铜溶液呈蓝色,两者混合后呈绿色。他取少量该绿色溶液,向其中加入适量水后溶液变为蓝色,可能的原因是___________用化学方程式表示。
简答题
18. 氮及其化合物与生产生活关系密切。请完成下列填空:
某学校化学学习小组为探究二氧化氮的性质,按下图所示装置进行实验。
装置甲中盛放浓硝酸的仪器的名称是______,装置丙中的试管内发生反应的离子方程式为:______。
实验过程中装置乙、丙中出现的现象分别是______;______。
在医疗上有重要的应用,曾被科学家作为研究的重要物质。现有容积为的试管盛满后倒扣于水槽中,再向试管中通入一定体积后,试管内气体的体积为试管容积的一半,则通入的的在相同条件下体积为______。
A.
在盛有一定量浓硝酸的试管中加入的铜片发生反应。请回答下列问题:
开始阶段,反应的化学方程式为______,后一阶段生成的气体为______,若两者恰好完全反应整个反应过程共产生标准状况下气体,则反应过程中被还原的的物质的量为______ ,参加反应的的物质的量为______ 。
反应结束后往试管中加入铜片,再加入少量的稀硫酸,这时铜片上又有气泡产生,反应的离子方程式为______。
19. A、、、是中学化学中的常见物质,其中为单质。各物质的转化关系如下:
若是空气中含量最多的气体。
下列叙述中,正确的是___填字母。
可用向上排空气法收集 的基本反应类型为化合反应
的浓溶液见光易分解,一般保存在棕色试剂瓶中
写出与水反应的化学方程式_____________________________
实验室制取的最简单氢化物装置如图所示,回答下列问题
试管中的试剂为_________________;装置的作用是___________。
若、、、的焰色反应均为黄色,为淡黄色固体,在加热条件下可直接转化为。
的化学方程式是_______________________________________
、、均能与水发生反应。与水反应的实验现象中,能说明该反应放热、的熔点低的是___。若单质与水反应。产生的气体在标准状况下的体积为_______.
答案和解析
1.【答案】
【解析】A.发生反应,氯气中由价降到价,被还原,A正确;
B.将铁屑放入稀中会生成,不能生成,不能证明比活泼,B错误;
C.、、等均可作水的消毒剂,C正确;
D.使溴水褪色与乙烯使溶液褪色,都是氧化还原反应,和都具有还原性,D正确;
故选B。
2.【答案】
【解析】
【分析】
本题考查混合物的计算,涉及化学方程式的计算,关键是利用离子方程式解答,避免方程式的繁琐,试题培养了学生的分析能力、化学计算能力,难度较大。
【解答】
稀硫酸不与铜反应,但能提供氢离子,硝酸与铜反应,生成硝酸铜,硝酸根离子与硫酸提供的氢离子可以继续反应,反应离子方程式如下:,硝酸根离子的浓度与氢离子的浓度比为:时,溶解的铜最多,设硫酸的物质的量为,硝酸的物质的量为,则,::,解得,,设参加反应的铜的最大物质的量是,
,解得:,即理论上最多能溶解铜的物质的量为。
故选B。
3.【答案】
【解析】
【分析】
本题考查混合金属与硝酸反应的计算,通过原子守恒思想是计算的关键,难度一般。
【解答】
A. 等物质的量的铁和铜混合,平均摩尔质量为,铁和铜的混合物,物质的量之和为,即其中含有铁和铜,标准状况的物质的量为,所以的铁和铜的混合物共转移电子,即需氢氧化钠。如果铁全部变成三价铁,共转移电子,所以有一部分铁转化为亚铁离子,设亚铁离子的物质的量为 ,则铁离子为,根据得失电子守恒,可知 ,所以,所以混合物溶解后的溶液中,项正确;
B. 反应后生成硝酸亚铁、硝酸铁、硝酸铜、气体、,根据氮原子守恒,硝酸的物质的量浓度是,项正确;
C. 需加入溶液的体积为,项正确;
D. 最后所得沉淀在空气中充分加热可得氧化铁和氧化铜的固体混合物,质量为,项错误。
4.【答案】
【解析】
【分析】
略
【解答】
A.工业盐酸呈现黄色是因为含有少量杂质,不正确;
B.,,所以过氧化钠可作为潜艇工作人员的供氧剂,B正确;
C.二氧化硫是国内外允许使用的一种食品添加剂,二氧化硫有显著的杀菌作用,二氧化硫有显著的抗氧化作用,二氧化硫创造了酸性环境,其溶于水生成的溶液呈酸性,帮助植物细胞溶解,促进其中的色素、风味物质和多酚成分进入到果汁中,C正确;
D.不同的硝酸浓度,不同活泼性的金属与硝酸反应产物不同,稀硝酸产物主要是一氧化氮,浓硝酸是二氧化氮,极稀硝酸与活泼金属反应产物是硝酸铵,D正确;
故选A。
5.【答案】
【解析】
【分析】
本题主要考查氮及其化合物的有关知识,涉及氮气、铵盐、硝酸等,难度不大。
【解答】
A.氮气的化学性质很稳定,在通常情况下不燃烧,也不支持燃烧,不能供给呼吸,故A正确;
B.在二氧化氮中燃烧放出大量的热量,所以可用作航天飞机的燃料,故B正确;
C.铵态氮肥能与碱性物质反应生成氨气,使肥效降低,所以铵态氮肥应避免和碱性肥料混合使用,故C错误;
D.硝酸常用来制造染料、氮肥、塑料、炸药、硝酸盐等物质,硝酸是一种重要的化工原料,故D正确。
6.【答案】
【解析】
【分析】
本题考查元素的价一类二维图,“盐与碱反应生成氢化物以及氢化物连续反应生成氧化物”等是推断的突破口,难度不大。
【解答】
正盐与反应可生成,则为铵盐、为,的相对分子质量比大,则为、为,为,为,为硝酸盐。
A.氨气催化氧化生成一氧化氮,故A错误;
B.为、为,不溶于水,可以用排水法收集;与水反应,不能用排水法收集,故B错误;
C.为,其浓溶液没有吸水性,故C错误;
D.为,实验室制备氨气时,可以将浓氨水滴入碱石灰中进行制取,故D正确。
7.【答案】
【解析】
【分析】
本题考查了元素化合物知识,难度不大,熟悉相关物质的性质是解题关键,注意对基础知识的巩固.
【解答】
一氧化氮不溶于水,与水不反应,故错误;
氨气为碱性气体,硫化氢具有强的还原性,二者都不能用浓硫酸干燥,故正确;
水晶的主要成分是二氧化硅,故正确;
二氧化硅常温下能够与氢氟酸反应生成四氟化硅和水,故错误;
氯气、二氧化硫都能够与氢氧化钠反应,被氢氧化钠溶液吸收,故正确;
一氧化氮能够被空气中氧气氧化,所以只能用排水集气法收集,不能用排空气法收集;而二氧化氮与水反应,所以只能用排空气法收集,不能用排水集气法,故正确;
故选:。
8.【答案】
【解析】
【分析】
本题考查根据化学方程式的计算、氮的氧化物的性质、氧化还原反应的计算等,题目难度中等。
【解答】
将拆分为、,原混合物看做、的混合物,其中一份用足量的氢气还原,反应后固体质量减少为拆分后、的混合物中元素的质量,原子的物质的量为:,根据元素守恒可知;另一份中加入硝酸,固体恰好完全溶解,溶液中溶质为,且同时收集到,标准状况下的物质的量为:,由可知,,根据电子转移守恒可知拆分后、的混合物中,,由铜元素守恒可知,根据氮元素守恒可知,硝酸的浓度为:,选项B符合题意。
故选B。
9.【答案】
【解析】
【分析】
本题主要考查了雷雨肥田原理,氮气、一氧化氮、二氧化氮的化学性质,理解反应原理、正确书写化学方程式是解答的关键,题目难度不大。
【解答】
“雷雨发庄稼”,空气中的在放电条件下与直接化合生成无色且不溶于水的一氧化氮气体:;一氧化氮常温下易与空气中的反应生成红棕色的二氧化氮气体:;二氧化氮与水反应生成硝酸和一氧化氮:,生成的硝酸随雨水淋洒到大地上,同土壤中的矿物相互作用,生成可溶于水的硝酸盐可作氮肥,植物生长得更好。“雷雨发庄稼”不包括氮气和氢气合成氨的反应,故B符合题意。
故选B。
10.【答案】
【解析】
【分析】
本题考查含氮化合物的性质和转化,难度不大,掌握物质的性质即可解答。
【解答】
A.与水发生氧化还原反应生成和,不属于化合反应,故A错误;
B.与气体反应生成,但不属于氮的固定,氮的固定为游离态的氮元素转化为化合态,故B错误;
C.实验室不能用加热固体的方法制备,氯化铵受热分解生成氨气和氯化氢,遇冷会立即化合生成氯化铵,故C错误;
D.见光易分解,实验室用棕色试剂瓶盛放浓,避光保存,故D正确。
11.【答案】
【解析】
【分析】
本题主要考查氮及其化合物的性质,属于基本知识的考查,难度不大。
【解答】
A.与水反应,不能用排水法收集,故A错误;
B.浓硝酸有挥发性,久置的浓硝酸会变为稀硝酸,故B正确;
C.氮的固定是指游离态的氮转化为含氮化合物,故C错误;
D.稀硝酸与铁反应,浓硝酸与铁发生钝化,钝化是化学变化,故D错误。
故选B。
12.【答案】
【解析】
【分析】
本题考查氨气的性质与铵盐的性质,题目难度中等,解题关键是理解氨气、铵盐的性质及含氮物质的相互转化。
【解答】
A.将集有氨气的试管倒扣于水槽中,液体迅速充满试管,说明氨气极易溶于水,使试管内的压强迅速减小,水充满试管,故A正确;
B.挥发的氨气在红热的铂丝作催化剂的条件下与氧气发生催化氧化反应生成,遇氧气又生成红棕色的二氧化氮,所以瓶口出现红棕色气体,故B错误;
C.加热碳酸氢铵,固体逐渐减少,有液滴产生,说明有水生成,所以可以说明碳酸氢铵受热不稳定,分解为氨气、二氧化碳、水,故C正确;
D.氨气在红热的铂丝作催化剂的条件下与氧气发生催化氧化反应生成,遇氧气生成红棕色的二氧化氮,二氧化氮与水反应生成硝酸和一氧化氮,所以锥形瓶内有存在,故D正确。
13.【答案】
【解析】
【分析】
本题考查铜和稀硝酸反应的现象,掌握铜和稀硝酸的反应即可解答,题目较为简单。
【解答】
A.加入稀硫酸,提供了氢离子,反应继续进行,即铜片继续溶解,产生无色气体,该气体在液面上方变为红棕色,故A错误;
B.铜片溶解,产生无色气体,该气体在液面上方变为红棕色,故B错误;
C.铜片溶解,先产生无色气体,该气体在液面上方变为红棕色,故C错误;
D.铜片溶解,产生无色气体,该气体在液面上方变为红棕色,故D正确。
14.【答案】
【解析】
【分析】
本题考查氨气及铵盐性质探究,熟悉氨气的物理性质、化学性质是解题关键,题目难度中等。
【解答】
A.氨气极易溶于水,使试管内压强迅速降低,液体迅速充满试管,故A正确;
B.将湿润的红色石蕊试纸放入集有氨气的集气瓶中,试纸由红色变为蓝色,说明氨水呈碱性,故B正确;
C.加热固体,观察到固体逐渐减少,试管口有液滴产生,说明受热分解,不稳定,故C正确;
D.氨气催化氧化生成一氧化氮,一氧化氮与空气中氧气反应生成二氧化氮,故D错误。
故选D。
15.【答案】
【解析】
【分析】
本题考查氮及其化合物性质分析,为高频考点,侧重考查学生的分析能力以及元素化合物知识的综合理解和运用,注意把握化学方程式书写,氧化还原反应电子转移的计算等,题目难度中等。
【解答】
根据图中氮元素化合价与物质类别分析可知,为氨气,为二氧化氮,为硝酸,为一水合氨,据此分析作答。
A. 为氨气,催化氧化可生成和水,而不是,故A错误;
B.的元素化合价为价,的化合价为价,存在中间价态,可发生歧化反应,即两者能发生氧化还原反应,故 B正确;
C. 从物质类别角度分析,一水合氨为碱,可以与二氧化氮、硝酸反应,但不能和氨气反应,故C错误;
D. 转化过程中,一水合氨分解可生成氨气和水,各元素化合价并未发生变化,故D错误。
故选B。
16.【答案】生成的或氮的氧化物扩散到大气中,污染环境;生成的与空气相接触,被氧化成红棕色的气体;
检验气密性;将铜片插入溶液中或向左侧倾斜试管,使铜片浸在浓硝酸中;抽动铜片使其和溶液脱离接触;与水反应,气体体积减小,使导管内压强减小,气压差将水压入试管中;
【解析】略
17.【答案】
;
浓;
【解析】硝酸一般盛放在棕色试剂瓶中,因为硝酸见光易分解,化学方程式:。
铜与稀硝酸反应生成一氧化氮,离子方程式为:;
实验中观察到试管中的气体略有红棕色,因为反应生成的无色气体与试管内氧气反应生成红棕色的,化学方程式:。
铜与浓硝酸反应生成二氧化氮,化学方程式为:浓;
加入适量水后与水发生反应生成了硝酸和一氧化氮,原溶液中饱和溶液的黄色褪去,显现出硝酸铜溶液的蓝色,化学方程式:。
18.【答案】分液漏斗;
产生红棕色气体 蒸馏水中有气泡,生成无色气体
浓;;;
【解析】
【分析】
本题考查性质方案的设计,题目难度中等,明确氮元素及其化合物性质为解答关键,注意掌握守恒书写在化学计算中的应用,试题培养了学生的分析能力及综合应用能力。
【解答】
装置甲中盛放浓硝酸的仪器的名称是分液漏斗;
二氧化氮经导管进入丙装置和水反应生成硝酸和,该反应的离子方程式为:,
故答案为:分液漏斗; ;
铜和浓硝酸在装置甲中反应浓,生成红棕色的二氧化氮气体进入乙装置,所以装置乙中出现的现象为生成红棕色气体;二氧化氮经导管进入丙装置和水反应,所以装置丙中出现的现象蒸馏水中有气泡产生,生成无色气体,
故答案为:产生红棕色气体;蒸馏水中有气泡,生成无色气体;
、和水反应生成硝酸,化学方程式为:,
若剩余气体为,反应消耗的体积为:,则通入的体积;
若剩余气体为,完全反应,同时消耗的氧气的体积为:,则通入的体积为:,
根据分析可知,则通入的的在相同条件下体积可能为,
故答案为:;
开始时与浓硝酸反应生成二氧化氮,发生反应为:浓,随着反应的进行,浓硝酸浓度逐渐减小,当变为稀硝酸后,稀硝酸与反应生成气体;
若两者恰好完全反应整个反应过程共产生标准状况下气体,即生成和的混合气体,根据原子守恒,反应过程中被还原的的物质的量为;反应后生成硝酸铜中含有的物质的量为:,则参加反应的的物质的量为:,
故答案为:浓;;;;
与稀释反应生成硝酸铜,反应后溶液中氢离子消耗完毕,但硝酸根离子有剩余,若再加入少量的稀硫酸,相当于稀硝酸溶液,铜与稀硝酸反应生成硝酸铜、和水,发生反应的离子方程式为:,
故答案为:。
19.【答案】;
;
、;干燥氨气;
;
融化成小球;。
【解析】
【分析】
本题主要考查化学方程式的书写,难度不大,需要学生熟练掌握。
【解答】
空气中含量最多的气体是氮气,
,是氮气与氧气反应生成一氧化氮,是一氧化氮与氧气反应生成二氧化氮,是二氧化氮与水反应生成硝酸,
下列叙述中,正确的是
一氧化氮容易被空气氧化,不能用排空气法收集,故错误;
的基本反应类型为化合反应,故正确;
浓硝酸见光易分解,一般保存在棕色试剂瓶中,故正确;
故选;
二氧化氮与水反应的化学方程式为:,
故答案为:;
实验室制取氨气所需试剂为:、,装置的作用是干燥氨气,
故答案为:、;干燥氨气;
若、、、的焰色反应均为黄色,说明含有钠,为淡黄色固体,说明为过氧化钠,在加热条件下可直接转化为,说明是金属钠。
是过氧化钠与水反应,化学方程式是:,
故答案为:;
与水反应的实验现象中,能说明该反应放热、的熔点低的是:融化成小球,单质钠与水反应生成氢气,在标准状况下的体积为。
故答案为:融化成小球;。
第1页,共1页
一、单选题
1. 下列说法错误的是( )
A. 氯气使溶液变黄,被还原
B. 将铁屑放入稀中证明比活泼
C. 、的某些单质或两元素之间形成的某些化合物可作水的消毒剂
D. 使溴水褪色与乙烯使溶液褪色的原理相同
2. 对于和的混合溶液,若和物质的量浓度存在如下关系:,理论上最多能溶解铜的物质的量为 ( )
A. B. C. D.
3. 将等物质的量的铁和铜的混合物与稀硝酸恰好完全反应,生成标准状况,向反应后的溶液中加入溶液使金属离子恰好沉淀,过滤。下列有关说法错误的是
A. 混合物溶解后的溶液中 B. 稀硝酸的物质的量浓度是
C. 需加入溶液 D. 最后所得沉淀在空气中充分加热可得固体
4. 下列说法不正确的是( )
A. 工业盐酸呈黄色是溶解在其中的的颜色
B. 可作为潜水艇的供氧剂
C. 二氧化硫是酸性氧化物,可用作食品添加剂
D. 硝酸浓度不同,与金属反应的产物也不同
5. 下列关于氮及其化合物说法,不正确的是( )
A. 氮气在通常情况下不燃烧,也不支持燃烧,不能供给呼吸
B. 可用作航天飞机的燃料
C. 碳酸氢铵常用作氮肥,可与碱性肥料混用
D. 硝酸可用于制造染料、炸药等
6. 如图是某元素的价一类二维图。其中正盐与反应可生成,的相对分子质量比大。下列说法正确的是
A. 可经催化氧化生成
B. 和都可用排水法收集
C. 的浓溶液具有吸水性,可用来干燥气体
D. 实验室制备时,可以将其浓溶液滴入碱石灰中进行制取
7. 下列叙述 正 确的有( )
、、都是形成酸雨的因素,都能和水反应生成酸
、均不能用浓硫酸干燥
水晶的主要成分是
与都属于酸性氧化物,都不能与酸反应
实验室可用溶液处理和废气
只能用排水集气法收集,不能用排空气法收集;而只能用排空气法收集,不能用排水集气法.
A. 项 B. 项 C. 项 D. 项
8. 将一包由、和组成的混合物均分成两份:一份混合物在加热条件下与充分反应,将固体全部转化成铜粉时固体质量减少了;向另一份混合物中加入溶液恰好完全反应生成和假设不产生其他还原产物,这些和标准状况混合并通入足量水中,气体全部被吸收生成。则该硝酸的物质的量浓度为( )
A. B. C. D.
9. 谚语“雷雨发庄稼”不包括下列哪个化学反应 反应条件已忽略
A. B.
C. D.
10. 下列关于含氮化合物的性质叙述正确的是( )
A. 与水发生化合反应生成
B. 与气体反应生成属于氮的固定
C. 实验室可用加热固体的方法制备
D. 见光易分解,实验室用棕色试剂瓶盛放浓
11. 下列关于氮及其化合物的说法正确的是( )
A. 实验中常用排水法收集气体
B. 久置的浓硝酸会变为稀硝酸
C. 与空气中的氧气反应生成属于氮的固定
D. 稀硝酸与铁反应而浓硝酸不与铁反应
12. 探究氨气及铵盐性质中,下列根据实验现象得出的结论不正确的是( )
A. 将有氨气的试管倒扣水中,液体迅速充满试管,说明氨气极易溶于水
B. 将红热的丝伸入如上图所示的锥形瓶中,瓶口出现少量的红棕色气体,说明氨气催化氧化的产物中有
C. 加热固体,观察到固体逐渐减少,试管口有液滴产生,说明具有热不稳定性
D. 充分反应后,锥形瓶内有存在
13. 某实验过程如图所示,则试管中的现象是。( )
A. 无明显现象,因稀不与铜反应
B. 铜片溶解,产生无色气体,该气体遇到空气不变色
C. 铜片溶解,产生红棕色、有刺激性气味的气体
D. 铜片溶解,产生无色气体,该气体在液面上方变为红棕色
14. 探究氨气及铵盐性质的过程中,下列根据实验现象得出的结论不正确的是 ( )
A. 将集有氨气的试管倒扣于水槽中,液体迅速充满试管,说明氨气极易溶于水
B. 将湿润的红色石蕊试纸放入集有氨气的集气瓶中,试纸由红色变为蓝色,说明氨水呈碱性
C. 加热固体,观察到固体逐渐减少,试管口有液滴产生,说明受热不稳定
D. 将红热的丝伸入如图所示的锥形瓶中,瓶口出现少量红棕色气体,说明氨气的直接氧化产物为2
15. 研究氮及其化合物的性质,可以有效改善人类的生存环境。氮元素化合价物质类别关系图如下,图中、、和分别代表一种含氮化合物。
下列说法中正确的是( )
A. 催化氧化可以生成
B. 从化合价角度分析,与能发生氧化还原反应。
C. 从物质类别角度分析,可以和、、发生反应
D. 转化过程中物质类别和化合价均发生变化
二、实验题
16. 装置Ⅰ和装置Ⅱ是有关硝酸和铜反应的实验装置示意图。
若用装置Ⅰ进行铜与浓硝酸反应的实验,最大的缺点是__________________________。若用装置Ⅰ来证明铜与稀硝酸反应生成气体,其最大缺点是不能与浓硝酸跟铜反应形成鲜明对照,简述原因:_____________________________________________________________________________________________________________________________________________________________。
若用装置Ⅱ进行适当操作,即可克服上述缺点,还能使上述两反应在同一试管中先后连续进行,实验步骤如下。
步骤一:组装好装置并________________后,加入浓硝酸铜片接近酸液,塞紧胶塞。
步骤二:________________________操作使反应发生。当导管口有少量红棕色气体逸出时,________________________操作使反应停止。同时将导管插入水中。稍后能观察到水沿导管倒吸至试管中,产生此现象的原因是________________________。还可能观察到的明显现象是________填标号。
溶液由蓝色变为无色 红棕色气体变为无色
17. 利用下图所示装置进行铜与硝酸反应的实验。
硝酸一般盛放在棕色试剂瓶中,请用化学方程式说明其原因:___________。
使用稀硝酸进行实验:反应开始后,铜丝逐渐变细,有气泡产生,溶液变蓝。
铜与稀硝酸反应的离子方程式为___________。
实验中观察到试管中的气体略有红棕色,其原因是_____用化学方程式表示。
使用浓硝酸进行实验:反应剧烈进行,铜丝逐渐变细,溶液变绿,试管上方出现红棕色气体。
铜与浓硝酸反应的化学方程式为___________。
某同学推测反应后溶液呈绿色的原因是在溶液中达到饱和,的饱和溶液呈黄色,硝酸铜溶液呈蓝色,两者混合后呈绿色。他取少量该绿色溶液,向其中加入适量水后溶液变为蓝色,可能的原因是___________用化学方程式表示。
简答题
18. 氮及其化合物与生产生活关系密切。请完成下列填空:
某学校化学学习小组为探究二氧化氮的性质,按下图所示装置进行实验。
装置甲中盛放浓硝酸的仪器的名称是______,装置丙中的试管内发生反应的离子方程式为:______。
实验过程中装置乙、丙中出现的现象分别是______;______。
在医疗上有重要的应用,曾被科学家作为研究的重要物质。现有容积为的试管盛满后倒扣于水槽中,再向试管中通入一定体积后,试管内气体的体积为试管容积的一半,则通入的的在相同条件下体积为______。
A.
在盛有一定量浓硝酸的试管中加入的铜片发生反应。请回答下列问题:
开始阶段,反应的化学方程式为______,后一阶段生成的气体为______,若两者恰好完全反应整个反应过程共产生标准状况下气体,则反应过程中被还原的的物质的量为______ ,参加反应的的物质的量为______ 。
反应结束后往试管中加入铜片,再加入少量的稀硫酸,这时铜片上又有气泡产生,反应的离子方程式为______。
19. A、、、是中学化学中的常见物质,其中为单质。各物质的转化关系如下:
若是空气中含量最多的气体。
下列叙述中,正确的是___填字母。
可用向上排空气法收集 的基本反应类型为化合反应
的浓溶液见光易分解,一般保存在棕色试剂瓶中
写出与水反应的化学方程式_____________________________
实验室制取的最简单氢化物装置如图所示,回答下列问题
试管中的试剂为_________________;装置的作用是___________。
若、、、的焰色反应均为黄色,为淡黄色固体,在加热条件下可直接转化为。
的化学方程式是_______________________________________
、、均能与水发生反应。与水反应的实验现象中,能说明该反应放热、的熔点低的是___。若单质与水反应。产生的气体在标准状况下的体积为_______.
答案和解析
1.【答案】
【解析】A.发生反应,氯气中由价降到价,被还原,A正确;
B.将铁屑放入稀中会生成,不能生成,不能证明比活泼,B错误;
C.、、等均可作水的消毒剂,C正确;
D.使溴水褪色与乙烯使溶液褪色,都是氧化还原反应,和都具有还原性,D正确;
故选B。
2.【答案】
【解析】
【分析】
本题考查混合物的计算,涉及化学方程式的计算,关键是利用离子方程式解答,避免方程式的繁琐,试题培养了学生的分析能力、化学计算能力,难度较大。
【解答】
稀硫酸不与铜反应,但能提供氢离子,硝酸与铜反应,生成硝酸铜,硝酸根离子与硫酸提供的氢离子可以继续反应,反应离子方程式如下:,硝酸根离子的浓度与氢离子的浓度比为:时,溶解的铜最多,设硫酸的物质的量为,硝酸的物质的量为,则,::,解得,,设参加反应的铜的最大物质的量是,
,解得:,即理论上最多能溶解铜的物质的量为。
故选B。
3.【答案】
【解析】
【分析】
本题考查混合金属与硝酸反应的计算,通过原子守恒思想是计算的关键,难度一般。
【解答】
A. 等物质的量的铁和铜混合,平均摩尔质量为,铁和铜的混合物,物质的量之和为,即其中含有铁和铜,标准状况的物质的量为,所以的铁和铜的混合物共转移电子,即需氢氧化钠。如果铁全部变成三价铁,共转移电子,所以有一部分铁转化为亚铁离子,设亚铁离子的物质的量为 ,则铁离子为,根据得失电子守恒,可知 ,所以,所以混合物溶解后的溶液中,项正确;
B. 反应后生成硝酸亚铁、硝酸铁、硝酸铜、气体、,根据氮原子守恒,硝酸的物质的量浓度是,项正确;
C. 需加入溶液的体积为,项正确;
D. 最后所得沉淀在空气中充分加热可得氧化铁和氧化铜的固体混合物,质量为,项错误。
4.【答案】
【解析】
【分析】
略
【解答】
A.工业盐酸呈现黄色是因为含有少量杂质,不正确;
B.,,所以过氧化钠可作为潜艇工作人员的供氧剂,B正确;
C.二氧化硫是国内外允许使用的一种食品添加剂,二氧化硫有显著的杀菌作用,二氧化硫有显著的抗氧化作用,二氧化硫创造了酸性环境,其溶于水生成的溶液呈酸性,帮助植物细胞溶解,促进其中的色素、风味物质和多酚成分进入到果汁中,C正确;
D.不同的硝酸浓度,不同活泼性的金属与硝酸反应产物不同,稀硝酸产物主要是一氧化氮,浓硝酸是二氧化氮,极稀硝酸与活泼金属反应产物是硝酸铵,D正确;
故选A。
5.【答案】
【解析】
【分析】
本题主要考查氮及其化合物的有关知识,涉及氮气、铵盐、硝酸等,难度不大。
【解答】
A.氮气的化学性质很稳定,在通常情况下不燃烧,也不支持燃烧,不能供给呼吸,故A正确;
B.在二氧化氮中燃烧放出大量的热量,所以可用作航天飞机的燃料,故B正确;
C.铵态氮肥能与碱性物质反应生成氨气,使肥效降低,所以铵态氮肥应避免和碱性肥料混合使用,故C错误;
D.硝酸常用来制造染料、氮肥、塑料、炸药、硝酸盐等物质,硝酸是一种重要的化工原料,故D正确。
6.【答案】
【解析】
【分析】
本题考查元素的价一类二维图,“盐与碱反应生成氢化物以及氢化物连续反应生成氧化物”等是推断的突破口,难度不大。
【解答】
正盐与反应可生成,则为铵盐、为,的相对分子质量比大,则为、为,为,为,为硝酸盐。
A.氨气催化氧化生成一氧化氮,故A错误;
B.为、为,不溶于水,可以用排水法收集;与水反应,不能用排水法收集,故B错误;
C.为,其浓溶液没有吸水性,故C错误;
D.为,实验室制备氨气时,可以将浓氨水滴入碱石灰中进行制取,故D正确。
7.【答案】
【解析】
【分析】
本题考查了元素化合物知识,难度不大,熟悉相关物质的性质是解题关键,注意对基础知识的巩固.
【解答】
一氧化氮不溶于水,与水不反应,故错误;
氨气为碱性气体,硫化氢具有强的还原性,二者都不能用浓硫酸干燥,故正确;
水晶的主要成分是二氧化硅,故正确;
二氧化硅常温下能够与氢氟酸反应生成四氟化硅和水,故错误;
氯气、二氧化硫都能够与氢氧化钠反应,被氢氧化钠溶液吸收,故正确;
一氧化氮能够被空气中氧气氧化,所以只能用排水集气法收集,不能用排空气法收集;而二氧化氮与水反应,所以只能用排空气法收集,不能用排水集气法,故正确;
故选:。
8.【答案】
【解析】
【分析】
本题考查根据化学方程式的计算、氮的氧化物的性质、氧化还原反应的计算等,题目难度中等。
【解答】
将拆分为、,原混合物看做、的混合物,其中一份用足量的氢气还原,反应后固体质量减少为拆分后、的混合物中元素的质量,原子的物质的量为:,根据元素守恒可知;另一份中加入硝酸,固体恰好完全溶解,溶液中溶质为,且同时收集到,标准状况下的物质的量为:,由可知,,根据电子转移守恒可知拆分后、的混合物中,,由铜元素守恒可知,根据氮元素守恒可知,硝酸的浓度为:,选项B符合题意。
故选B。
9.【答案】
【解析】
【分析】
本题主要考查了雷雨肥田原理,氮气、一氧化氮、二氧化氮的化学性质,理解反应原理、正确书写化学方程式是解答的关键,题目难度不大。
【解答】
“雷雨发庄稼”,空气中的在放电条件下与直接化合生成无色且不溶于水的一氧化氮气体:;一氧化氮常温下易与空气中的反应生成红棕色的二氧化氮气体:;二氧化氮与水反应生成硝酸和一氧化氮:,生成的硝酸随雨水淋洒到大地上,同土壤中的矿物相互作用,生成可溶于水的硝酸盐可作氮肥,植物生长得更好。“雷雨发庄稼”不包括氮气和氢气合成氨的反应,故B符合题意。
故选B。
10.【答案】
【解析】
【分析】
本题考查含氮化合物的性质和转化,难度不大,掌握物质的性质即可解答。
【解答】
A.与水发生氧化还原反应生成和,不属于化合反应,故A错误;
B.与气体反应生成,但不属于氮的固定,氮的固定为游离态的氮元素转化为化合态,故B错误;
C.实验室不能用加热固体的方法制备,氯化铵受热分解生成氨气和氯化氢,遇冷会立即化合生成氯化铵,故C错误;
D.见光易分解,实验室用棕色试剂瓶盛放浓,避光保存,故D正确。
11.【答案】
【解析】
【分析】
本题主要考查氮及其化合物的性质,属于基本知识的考查,难度不大。
【解答】
A.与水反应,不能用排水法收集,故A错误;
B.浓硝酸有挥发性,久置的浓硝酸会变为稀硝酸,故B正确;
C.氮的固定是指游离态的氮转化为含氮化合物,故C错误;
D.稀硝酸与铁反应,浓硝酸与铁发生钝化,钝化是化学变化,故D错误。
故选B。
12.【答案】
【解析】
【分析】
本题考查氨气的性质与铵盐的性质,题目难度中等,解题关键是理解氨气、铵盐的性质及含氮物质的相互转化。
【解答】
A.将集有氨气的试管倒扣于水槽中,液体迅速充满试管,说明氨气极易溶于水,使试管内的压强迅速减小,水充满试管,故A正确;
B.挥发的氨气在红热的铂丝作催化剂的条件下与氧气发生催化氧化反应生成,遇氧气又生成红棕色的二氧化氮,所以瓶口出现红棕色气体,故B错误;
C.加热碳酸氢铵,固体逐渐减少,有液滴产生,说明有水生成,所以可以说明碳酸氢铵受热不稳定,分解为氨气、二氧化碳、水,故C正确;
D.氨气在红热的铂丝作催化剂的条件下与氧气发生催化氧化反应生成,遇氧气生成红棕色的二氧化氮,二氧化氮与水反应生成硝酸和一氧化氮,所以锥形瓶内有存在,故D正确。
13.【答案】
【解析】
【分析】
本题考查铜和稀硝酸反应的现象,掌握铜和稀硝酸的反应即可解答,题目较为简单。
【解答】
A.加入稀硫酸,提供了氢离子,反应继续进行,即铜片继续溶解,产生无色气体,该气体在液面上方变为红棕色,故A错误;
B.铜片溶解,产生无色气体,该气体在液面上方变为红棕色,故B错误;
C.铜片溶解,先产生无色气体,该气体在液面上方变为红棕色,故C错误;
D.铜片溶解,产生无色气体,该气体在液面上方变为红棕色,故D正确。
14.【答案】
【解析】
【分析】
本题考查氨气及铵盐性质探究,熟悉氨气的物理性质、化学性质是解题关键,题目难度中等。
【解答】
A.氨气极易溶于水,使试管内压强迅速降低,液体迅速充满试管,故A正确;
B.将湿润的红色石蕊试纸放入集有氨气的集气瓶中,试纸由红色变为蓝色,说明氨水呈碱性,故B正确;
C.加热固体,观察到固体逐渐减少,试管口有液滴产生,说明受热分解,不稳定,故C正确;
D.氨气催化氧化生成一氧化氮,一氧化氮与空气中氧气反应生成二氧化氮,故D错误。
故选D。
15.【答案】
【解析】
【分析】
本题考查氮及其化合物性质分析,为高频考点,侧重考查学生的分析能力以及元素化合物知识的综合理解和运用,注意把握化学方程式书写,氧化还原反应电子转移的计算等,题目难度中等。
【解答】
根据图中氮元素化合价与物质类别分析可知,为氨气,为二氧化氮,为硝酸,为一水合氨,据此分析作答。
A. 为氨气,催化氧化可生成和水,而不是,故A错误;
B.的元素化合价为价,的化合价为价,存在中间价态,可发生歧化反应,即两者能发生氧化还原反应,故 B正确;
C. 从物质类别角度分析,一水合氨为碱,可以与二氧化氮、硝酸反应,但不能和氨气反应,故C错误;
D. 转化过程中,一水合氨分解可生成氨气和水,各元素化合价并未发生变化,故D错误。
故选B。
16.【答案】生成的或氮的氧化物扩散到大气中,污染环境;生成的与空气相接触,被氧化成红棕色的气体;
检验气密性;将铜片插入溶液中或向左侧倾斜试管,使铜片浸在浓硝酸中;抽动铜片使其和溶液脱离接触;与水反应,气体体积减小,使导管内压强减小,气压差将水压入试管中;
【解析】略
17.【答案】
;
浓;
【解析】硝酸一般盛放在棕色试剂瓶中,因为硝酸见光易分解,化学方程式:。
铜与稀硝酸反应生成一氧化氮,离子方程式为:;
实验中观察到试管中的气体略有红棕色,因为反应生成的无色气体与试管内氧气反应生成红棕色的,化学方程式:。
铜与浓硝酸反应生成二氧化氮,化学方程式为:浓;
加入适量水后与水发生反应生成了硝酸和一氧化氮,原溶液中饱和溶液的黄色褪去,显现出硝酸铜溶液的蓝色,化学方程式:。
18.【答案】分液漏斗;
产生红棕色气体 蒸馏水中有气泡,生成无色气体
浓;;;
【解析】
【分析】
本题考查性质方案的设计,题目难度中等,明确氮元素及其化合物性质为解答关键,注意掌握守恒书写在化学计算中的应用,试题培养了学生的分析能力及综合应用能力。
【解答】
装置甲中盛放浓硝酸的仪器的名称是分液漏斗;
二氧化氮经导管进入丙装置和水反应生成硝酸和,该反应的离子方程式为:,
故答案为:分液漏斗; ;
铜和浓硝酸在装置甲中反应浓,生成红棕色的二氧化氮气体进入乙装置,所以装置乙中出现的现象为生成红棕色气体;二氧化氮经导管进入丙装置和水反应,所以装置丙中出现的现象蒸馏水中有气泡产生,生成无色气体,
故答案为:产生红棕色气体;蒸馏水中有气泡,生成无色气体;
、和水反应生成硝酸,化学方程式为:,
若剩余气体为,反应消耗的体积为:,则通入的体积;
若剩余气体为,完全反应,同时消耗的氧气的体积为:,则通入的体积为:,
根据分析可知,则通入的的在相同条件下体积可能为,
故答案为:;
开始时与浓硝酸反应生成二氧化氮,发生反应为:浓,随着反应的进行,浓硝酸浓度逐渐减小,当变为稀硝酸后,稀硝酸与反应生成气体;
若两者恰好完全反应整个反应过程共产生标准状况下气体,即生成和的混合气体,根据原子守恒,反应过程中被还原的的物质的量为;反应后生成硝酸铜中含有的物质的量为:,则参加反应的的物质的量为:,
故答案为:浓;;;;
与稀释反应生成硝酸铜,反应后溶液中氢离子消耗完毕,但硝酸根离子有剩余,若再加入少量的稀硫酸,相当于稀硝酸溶液,铜与稀硝酸反应生成硝酸铜、和水,发生反应的离子方程式为:,
故答案为:。
19.【答案】;
;
、;干燥氨气;
;
融化成小球;。
【解析】
【分析】
本题主要考查化学方程式的书写,难度不大,需要学生熟练掌握。
【解答】
空气中含量最多的气体是氮气,
,是氮气与氧气反应生成一氧化氮,是一氧化氮与氧气反应生成二氧化氮,是二氧化氮与水反应生成硝酸,
下列叙述中,正确的是
一氧化氮容易被空气氧化,不能用排空气法收集,故错误;
的基本反应类型为化合反应,故正确;
浓硝酸见光易分解,一般保存在棕色试剂瓶中,故正确;
故选;
二氧化氮与水反应的化学方程式为:,
故答案为:;
实验室制取氨气所需试剂为:、,装置的作用是干燥氨气,
故答案为:、;干燥氨气;
若、、、的焰色反应均为黄色,说明含有钠,为淡黄色固体,说明为过氧化钠,在加热条件下可直接转化为,说明是金属钠。
是过氧化钠与水反应,化学方程式是:,
故答案为:;
与水反应的实验现象中,能说明该反应放热、的熔点低的是:融化成小球,单质钠与水反应生成氢气,在标准状况下的体积为。
故答案为:融化成小球;。
第1页,共1页
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
