化学人教版(2019)选择性必修3 2.3芳香烃 课件(共23张ppt)
文档属性
| 名称 | 化学人教版(2019)选择性必修3 2.3芳香烃 课件(共23张ppt) |  | |
| 格式 | pptx | ||
| 文件大小 | 526.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-06-22 10:44:40 | ||
图片预览



文档简介
(共23张PPT)
芳香烃
第二章第三节
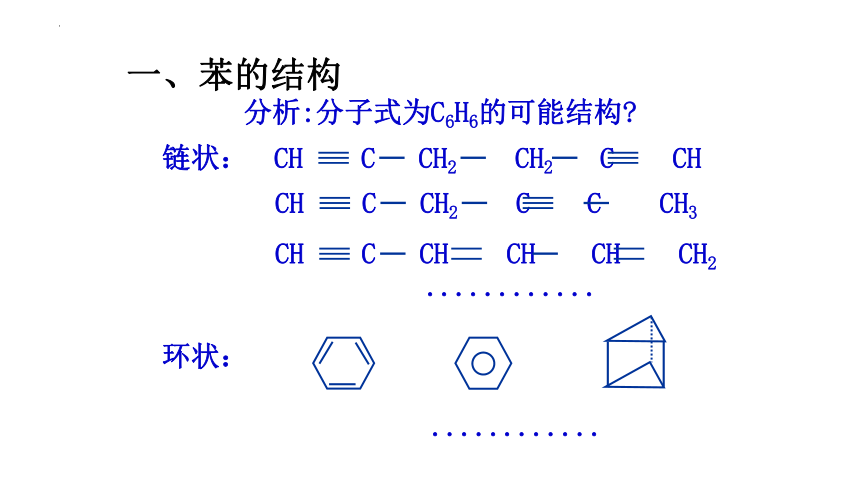
分析:分子式为C6H6的可能结构
链状:
环状:
CH C CH2 CH2 C CH
CH C CH2 C C CH3
CH C CH CH CH CH2
............
............
一、苯的结构
1、苯不能使酸性高锰酸钾溶液褪色,也不能使溴水褪色
2、苯的一氯代物只有一种,二氯代物有三种
3、苯的邻二代物只有一种
4、苯的氢核磁共振谱图只有一个峰
有关苯的一些实验事实
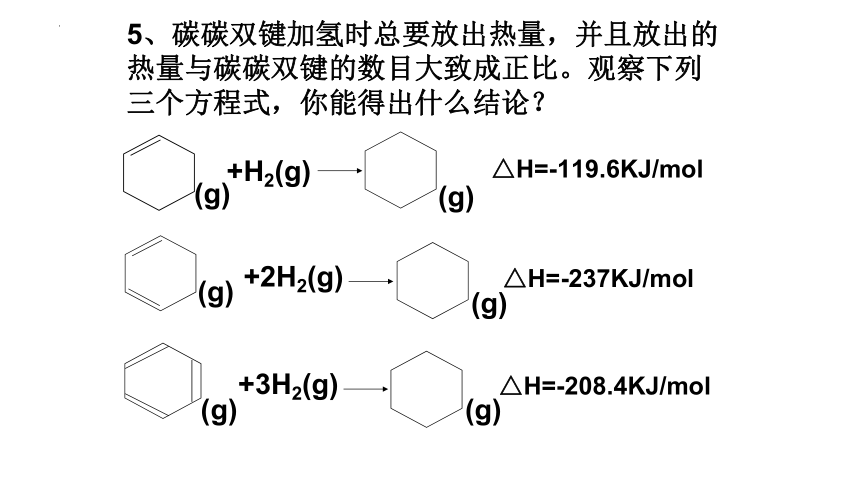
5、碳碳双键加氢时总要放出热量,并且放出的热量与碳碳双键的数目大致成正比。观察下列三个方程式,你能得出什么结论?
+H2(g)
(g)
(g)
△H=-119.6KJ/mol
(g)
+3H2(g)
(g)
△H=-208.4KJ/mol
(g)
+2H2(g)
(g)
△H=-237KJ/mol
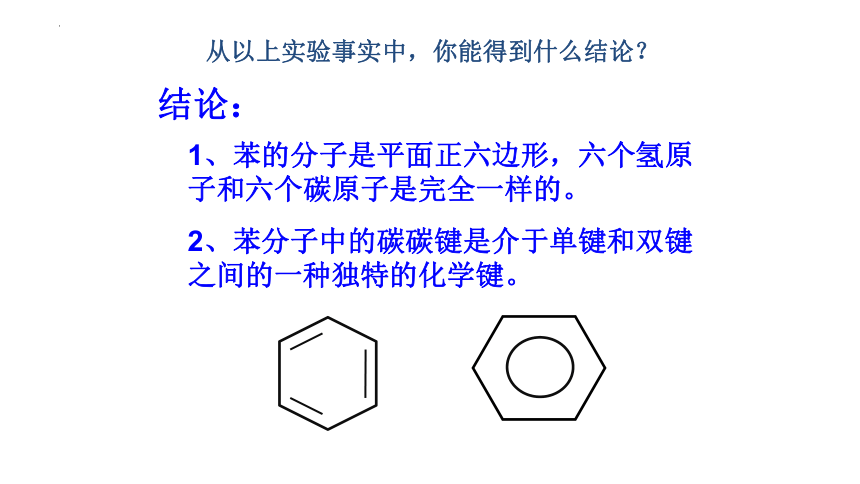
结论:
1、苯的分子是平面正六边形,六个氢原子和六个碳原子是完全一样的。
2、苯分子中的碳碳键是介于单键和双键之间的一种独特的化学键。
从以上实验事实中,你能得到什么结论?
二、苯的性质
苯的特殊结构
苯的特殊性质
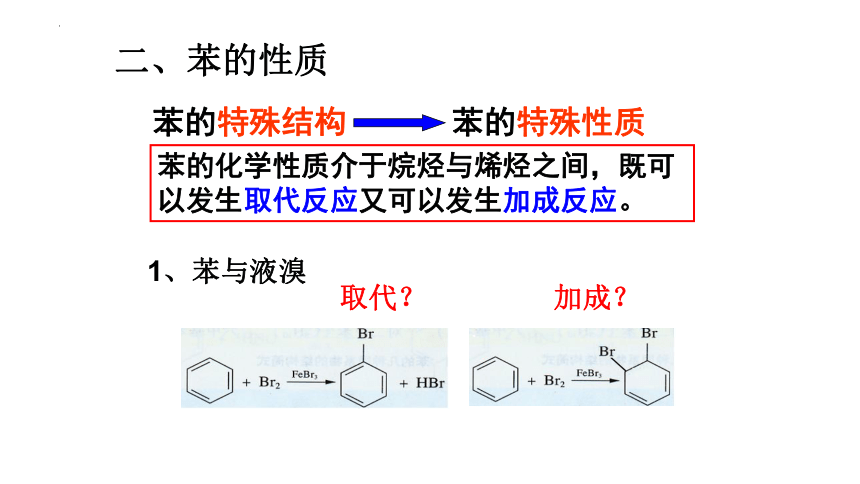
苯的化学性质介于烷烃与烯烃之间,既可以发生取代反应又可以发生加成反应。
1、苯与液溴
取代? 加成?
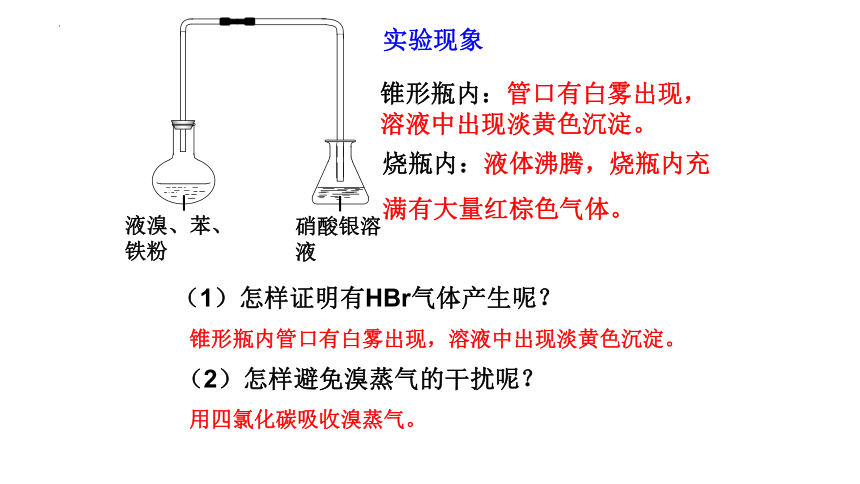
液溴、苯、铁粉
硝酸银溶液
实验现象
烧瓶内:液体沸腾,烧瓶内充
满有大量红棕色气体。
锥形瓶内:管口有白雾出现,溶液中出现淡黄色沉淀。
(1)怎样证明有HBr气体产生呢?
(2)怎样避免溴蒸气的干扰呢?
锥形瓶内管口有白雾出现,溶液中出现淡黄色沉淀。
用四氯化碳吸收溴蒸气。
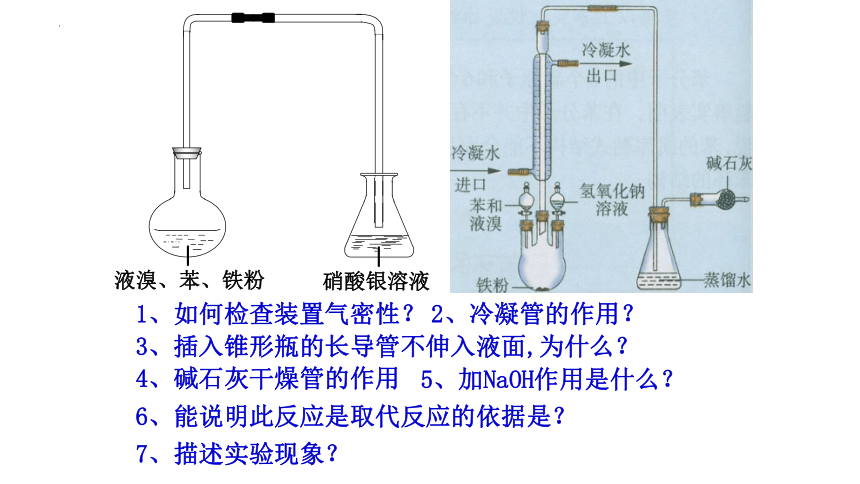
液溴、苯、铁粉
硝酸银溶液
1、如何检查装置气密性?
2、冷凝管的作用?
3、插入锥形瓶的长导管不伸入液面,为什么?
7、描述实验现象?
4、碱石灰干燥管的作用
5、加NaOH作用是什么?
6、能说明此反应是取代反应的依据是?
2、冷凝管的作用:冷凝。
3、插入锥形瓶的长导管不伸入液面:防止倒吸。
7、描述实验现象:三颈瓶中液体沸腾,烧瓶内充满有大量红棕色气体。
4、碱石灰干燥管的作用:吸收HBr,防止污染空气。
5、加NaOH作用:吸收溴苯中的溴和溴化氢。
6、能说明此反应是取代反应的依据:向锥形瓶中加入硝酸银或石蕊试液,检验HBr生成,从而证明为取代反应。
1、检查气密性:把右侧的干燥管接一导管,插到盛有水的水槽中,用酒精灯加热三颈烧瓶,若观察到插入水槽中的导管口有气泡冒出,撤去酒精灯后,导管中有一段液注上升,一段时间不变,则气密性良好。
两者相比,后一装置有哪些优点?
(1)冷凝效果更好。
(3)NaOH溶液吸收溴苯中的溴和溴化氢,使现象更明显。
液溴、苯、铁粉
硝酸银溶液
(2)有尾气吸收装置,能防止污染。
(4)试管中液面低于烧杯中,为什么?
二、苯的性质
1、苯与液溴
2、苯与浓硝酸
(1)如何混合浓硫酸和浓硝酸?
(3)怎样控制反应温度在60℃左右
(5)长导管的作用
(6)生成物状态 怎样除去其中的杂质
(2)为何要在不断振荡下,逐滴加苯?
在一支大试管中先加入1.5mL浓硝酸,再慢慢加入2mL浓硫酸,摇匀,并使混合液温度冷却到60摄氏度以下。
因为反应放热,温度过高,苯易挥发,且硝酸也会分解。
水浴加热。
使试管内的混合液受热均匀。
冷凝回流作用,防止未反应的苯和硝酸挥发。使反应体系与外界大气想通,防止试管内压强增大发生事故。
纯硝基苯为无色的油状液体,密度大于水,实验中可将粗产品依次用蒸馏水和NaOH溶液洗涤,最后再用蒸馏水洗涤(将用无水CaCl2干燥后的粗硝基苯进行蒸馏,可得纯硝基苯)。
当把温度升高到100 ~ 110℃,产物还一样吗?
试写出方程式。
3、苯与氢气
+ 3H2
Ni
18MPa 180~250℃
总结苯的性质:
易取代,难加成。
+ HNO3
— NO2
+ H2O
浓硫酸
60℃
一、芳香烃的来源与应用
起初源于:煤焦油。
现代来源:石油化学工业中的催化重整和裂化。
有机原料应用最多的芳烃:苯、乙苯、对二甲苯等。
重要有机化合物的原料。
苯
苯酚
硝基苯
苯胺
环己烷
二氯苯
氯苯
苯乙烯
……
合成树脂
合成纤维
合成塑料
染料
医药
洗剂剂
炸药
……
二、苯的同系物
1、含义:只有一个苯环,苯环上氢原子被烷基
代替而得到的芳烃。
CH3
|
CH2CH3
|
CH3
|
|
CH3
|
CH3
CH3
|
CH3
CH3
H3C
H3C
甲苯(C7H8) 乙苯( C8H10) 对二甲苯(C8H10) 六甲基苯(C12H18)
2、苯的同系物化学性质
甲苯+高锰酸钾酸性溶液
二甲苯+高锰酸钾酸性溶液
用力振荡,必要时加热
现象:紫红色褪去
①氧化反应
反应机理:
|
—C—H
|
O
||
C—OH
|
酸性高锰酸钾溶液
烷基上与苯环直接相连的碳原子上
一定要直接连氢原子。
H
|
—C—H
|
H
H
| |
—C—C—
| |
H
CH3
|
—C—CH3
|
CH3
×
CH3
|
—C—CH3
|
CH3
CH3
|
|
CH2—R
CH3
|
CH3—CH—
CH3
|
—C—CH3
|
CH3
HOOC
|
|
COOH
HOOC—
KMnO4/H+
②取代反应
CH3
|
|
NO2
CH3
|
NO2
O2N
+ 3HO-NO2
+ 3H2O
浓硫酸
100℃
2,4,6—三硝基甲苯
三硝基甲苯
(TNT)
不溶于水的淡黄色针状晶体
黄色烈性炸药
如果把100℃改为30℃呢?
生成邻硝基甲苯和对硝基甲苯两种一取代物
苯环性质:
烷基性质:
共同性质:
卤代反应、硝化反应、加成反应
氧化反应(燃烧)
卤代反应
你还能说出苯的同系物具有的性质吗?
3、常见的苯的同系物的获得
CH2CH3
|
+ CH2=CH2
催化剂
△
乙苯
两种生产异丙苯工艺的对比
多苯代脂烃:苯环通过脂肪烃连在一起
联苯或多联苯:苯环之间通过碳碳单键直接相连
稠环芳烃:苯环之间通过共用苯环的若干环边而形成
—CH2—
—
二苯甲烷(C13H12)
联苯(C12H10)
萘(C10H8)
蒽(C14H10)
二、多环芳烃
芳香烃对健康的危害
苯
稠环
芳烃
是黏合剂、油性涂料、油墨等的常用有机溶剂
操作车间空气中苯的浓度≤40mg·m-3
居室内空气中苯含量平均每小时≤0.09mg·m-3
制鞋、皮革、箱包、家具、喷漆、油漆等工作
引起急性中毒或慢性中毒,诱发白血病
致癌物质
萘——过去卫生球的主要成分
秸秆、树叶等不完全燃烧形成的烟雾中
香烟的烟雾中
脂肪烃与芳香烃的比较
烃 碳碳键结构特点 化学性质
烷烃
烯烃
炔烃
芳香烃
碳碳单键
碳碳双键
碳碳三键
介于单双键间的碳碳键
芳香烃
第二章第三节
分析:分子式为C6H6的可能结构
链状:
环状:
CH C CH2 CH2 C CH
CH C CH2 C C CH3
CH C CH CH CH CH2
............
............
一、苯的结构
1、苯不能使酸性高锰酸钾溶液褪色,也不能使溴水褪色
2、苯的一氯代物只有一种,二氯代物有三种
3、苯的邻二代物只有一种
4、苯的氢核磁共振谱图只有一个峰
有关苯的一些实验事实
5、碳碳双键加氢时总要放出热量,并且放出的热量与碳碳双键的数目大致成正比。观察下列三个方程式,你能得出什么结论?
+H2(g)
(g)
(g)
△H=-119.6KJ/mol
(g)
+3H2(g)
(g)
△H=-208.4KJ/mol
(g)
+2H2(g)
(g)
△H=-237KJ/mol
结论:
1、苯的分子是平面正六边形,六个氢原子和六个碳原子是完全一样的。
2、苯分子中的碳碳键是介于单键和双键之间的一种独特的化学键。
从以上实验事实中,你能得到什么结论?
二、苯的性质
苯的特殊结构
苯的特殊性质
苯的化学性质介于烷烃与烯烃之间,既可以发生取代反应又可以发生加成反应。
1、苯与液溴
取代? 加成?
液溴、苯、铁粉
硝酸银溶液
实验现象
烧瓶内:液体沸腾,烧瓶内充
满有大量红棕色气体。
锥形瓶内:管口有白雾出现,溶液中出现淡黄色沉淀。
(1)怎样证明有HBr气体产生呢?
(2)怎样避免溴蒸气的干扰呢?
锥形瓶内管口有白雾出现,溶液中出现淡黄色沉淀。
用四氯化碳吸收溴蒸气。
液溴、苯、铁粉
硝酸银溶液
1、如何检查装置气密性?
2、冷凝管的作用?
3、插入锥形瓶的长导管不伸入液面,为什么?
7、描述实验现象?
4、碱石灰干燥管的作用
5、加NaOH作用是什么?
6、能说明此反应是取代反应的依据是?
2、冷凝管的作用:冷凝。
3、插入锥形瓶的长导管不伸入液面:防止倒吸。
7、描述实验现象:三颈瓶中液体沸腾,烧瓶内充满有大量红棕色气体。
4、碱石灰干燥管的作用:吸收HBr,防止污染空气。
5、加NaOH作用:吸收溴苯中的溴和溴化氢。
6、能说明此反应是取代反应的依据:向锥形瓶中加入硝酸银或石蕊试液,检验HBr生成,从而证明为取代反应。
1、检查气密性:把右侧的干燥管接一导管,插到盛有水的水槽中,用酒精灯加热三颈烧瓶,若观察到插入水槽中的导管口有气泡冒出,撤去酒精灯后,导管中有一段液注上升,一段时间不变,则气密性良好。
两者相比,后一装置有哪些优点?
(1)冷凝效果更好。
(3)NaOH溶液吸收溴苯中的溴和溴化氢,使现象更明显。
液溴、苯、铁粉
硝酸银溶液
(2)有尾气吸收装置,能防止污染。
(4)试管中液面低于烧杯中,为什么?
二、苯的性质
1、苯与液溴
2、苯与浓硝酸
(1)如何混合浓硫酸和浓硝酸?
(3)怎样控制反应温度在60℃左右
(5)长导管的作用
(6)生成物状态 怎样除去其中的杂质
(2)为何要在不断振荡下,逐滴加苯?
在一支大试管中先加入1.5mL浓硝酸,再慢慢加入2mL浓硫酸,摇匀,并使混合液温度冷却到60摄氏度以下。
因为反应放热,温度过高,苯易挥发,且硝酸也会分解。
水浴加热。
使试管内的混合液受热均匀。
冷凝回流作用,防止未反应的苯和硝酸挥发。使反应体系与外界大气想通,防止试管内压强增大发生事故。
纯硝基苯为无色的油状液体,密度大于水,实验中可将粗产品依次用蒸馏水和NaOH溶液洗涤,最后再用蒸馏水洗涤(将用无水CaCl2干燥后的粗硝基苯进行蒸馏,可得纯硝基苯)。
当把温度升高到100 ~ 110℃,产物还一样吗?
试写出方程式。
3、苯与氢气
+ 3H2
Ni
18MPa 180~250℃
总结苯的性质:
易取代,难加成。
+ HNO3
— NO2
+ H2O
浓硫酸
60℃
一、芳香烃的来源与应用
起初源于:煤焦油。
现代来源:石油化学工业中的催化重整和裂化。
有机原料应用最多的芳烃:苯、乙苯、对二甲苯等。
重要有机化合物的原料。
苯
苯酚
硝基苯
苯胺
环己烷
二氯苯
氯苯
苯乙烯
……
合成树脂
合成纤维
合成塑料
染料
医药
洗剂剂
炸药
……
二、苯的同系物
1、含义:只有一个苯环,苯环上氢原子被烷基
代替而得到的芳烃。
CH3
|
CH2CH3
|
CH3
|
|
CH3
|
CH3
CH3
|
CH3
CH3
H3C
H3C
甲苯(C7H8) 乙苯( C8H10) 对二甲苯(C8H10) 六甲基苯(C12H18)
2、苯的同系物化学性质
甲苯+高锰酸钾酸性溶液
二甲苯+高锰酸钾酸性溶液
用力振荡,必要时加热
现象:紫红色褪去
①氧化反应
反应机理:
|
—C—H
|
O
||
C—OH
|
酸性高锰酸钾溶液
烷基上与苯环直接相连的碳原子上
一定要直接连氢原子。
H
|
—C—H
|
H
H
| |
—C—C—
| |
H
CH3
|
—C—CH3
|
CH3
×
CH3
|
—C—CH3
|
CH3
CH3
|
|
CH2—R
CH3
|
CH3—CH—
CH3
|
—C—CH3
|
CH3
HOOC
|
|
COOH
HOOC—
KMnO4/H+
②取代反应
CH3
|
|
NO2
CH3
|
NO2
O2N
+ 3HO-NO2
+ 3H2O
浓硫酸
100℃
2,4,6—三硝基甲苯
三硝基甲苯
(TNT)
不溶于水的淡黄色针状晶体
黄色烈性炸药
如果把100℃改为30℃呢?
生成邻硝基甲苯和对硝基甲苯两种一取代物
苯环性质:
烷基性质:
共同性质:
卤代反应、硝化反应、加成反应
氧化反应(燃烧)
卤代反应
你还能说出苯的同系物具有的性质吗?
3、常见的苯的同系物的获得
CH2CH3
|
+ CH2=CH2
催化剂
△
乙苯
两种生产异丙苯工艺的对比
多苯代脂烃:苯环通过脂肪烃连在一起
联苯或多联苯:苯环之间通过碳碳单键直接相连
稠环芳烃:苯环之间通过共用苯环的若干环边而形成
—CH2—
—
二苯甲烷(C13H12)
联苯(C12H10)
萘(C10H8)
蒽(C14H10)
二、多环芳烃
芳香烃对健康的危害
苯
稠环
芳烃
是黏合剂、油性涂料、油墨等的常用有机溶剂
操作车间空气中苯的浓度≤40mg·m-3
居室内空气中苯含量平均每小时≤0.09mg·m-3
制鞋、皮革、箱包、家具、喷漆、油漆等工作
引起急性中毒或慢性中毒,诱发白血病
致癌物质
萘——过去卫生球的主要成分
秸秆、树叶等不完全燃烧形成的烟雾中
香烟的烟雾中
脂肪烃与芳香烃的比较
烃 碳碳键结构特点 化学性质
烷烃
烯烃
炔烃
芳香烃
碳碳单键
碳碳双键
碳碳三键
介于单双键间的碳碳键
