第一章第二节原子结构与元素的性质同步练习 (含解析)2022-2023学年下学期高二化学人教版(2019)选择性必修2
文档属性
| 名称 | 第一章第二节原子结构与元素的性质同步练习 (含解析)2022-2023学年下学期高二化学人教版(2019)选择性必修2 |  | |
| 格式 | docx | ||
| 文件大小 | 715.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-06-21 20:17:58 | ||
图片预览




文档简介
第一章第二节原子结构与元素的性质同步练习
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1.当汽车遭受一定碰撞力量以后,安全气囊中的物质会发生剧烈的反应:
NaN3+ KNO3= K2O + Na2O + N2↑(未配平),生成大量气体。下列说法正确的是
A.半径大小:r(Na+) < r(N3-) B.电负性大小:χ(N) > χ(O)
C.第一电离能:I1(K) > I1(Na) D.碱性强弱:KOH < NaOH
2.下表列出了某短周期元素R的各级电离能数据(用I1、I2…^表示,单位kJ/mol)。
I1 I2 I3 I4 ……
740 1500 7700 10500
下列关于元素R的判断正确的是
A.R的最高正价为+1价
B.R元素位于元素周期表中第ⅢA族
C.R元素第一电离能大于同周期相邻元素
D.R元素基态原子的电子排布式为1s22s22p1
3.下列说法不正确的是
A.某外围电子排布为基态原子,该元素位于周期表中第六周期第IIIB族
B.在元素周期表中,d区和ds区的元素都是金属元素
C.当碳原子的核外电子排布由 转变为 时,吸收能量,由基态转化成激发态
D.非金属元素形成的共价化合物中,原子的最外层电子数不一定是2或8
4.已知号元素的离子、、、都具有相同电子层结构,下列关系正确的是
A.质子数:,离子的还原性:
B.电负性:
C.氢化物的稳定性:
D.原子半径:,第一电离能:
5.2017年5月9日中国科学院正式向社会发布113号、115号、117号和118号元素的中文名称。已知117号元素有多种原子,如、等。下列说法正确的是
A.和的化学性质完全不同
B.Ts位于周期表的第七周期ⅦA族
C.在Ts原子中,最后填入电子的轨道能级符号是f,故Ts位于周期表的f区
D.在周期表中,假设第八周期按现有规则填满,则117号元素的正下方是149号元素
6.1817年,瑞典的贝采利乌斯从硫酸厂的铅室底部的红色粉状物质中制得硒。硒在元素周期表中的数据如图所示,下列关于硒元素及其基态原子的说法错误的是
A.属于非金属元素 B.位于周期表p区
C.有34种不同运动状态的电子 D.价层电子排布式为3d104s24p4
7.的原子结构示意图为,下列关于的描述正确的是
A.位于第五周期,第Ⅴ族 B.属于金属元素
C.酸性: D.稳定性:
8.下列选项中,所叙述的粒子按半径由大到小排列时,顺序正确的是
①基态X的原子结构示意图为
②基态Y原子的价电子排布式为
③基态的轨道表示式为
④基态T原子有2个电子层,电子式为
A.①②③④ B.③④①②
C.③①②④ D.①②④③
9.下列各选项中,按元素的电负性由大到小排列,顺序正确的是
A. B.
C. D.
10.下列各组元素中,第一电离能大小次序不正确的是
A. B. C. D.
11.“飞秒()化学”使运用激光光谱技术观测化学反应时分子中原子的运动成为可能,你认为利用该技术不能观察到的是
A.原子中原子核的内部结构 B.化学反应中原子的运动
C.化学反应中生成物分子的形成 D.化学反应中反应物分子的分解
12.核外电子层结构相同的是
A.、、、Ar B.、、、
C.、、、Ar D.、、、
13.短周期主族元素A、B、C、D、E、F的原子序数依次增大,A的某种核素没有中子,B、C、D、E在周期表中的相对位置如图,且四种元素原子序数之和为37。下列说法不正确的是
B C D
E
A.B的某种核素可用来判定文物的年代
B.A、C、D三种元素可组成可溶于水的盐
C.原子半径由大到小顺序:E>F>C>A
D.最简单气态氢化物的稳定性:D14.下列性质的比较正确的是
A.单质的熔点:Li>Na>K> Rb B.电负性: P>N>O>C
C.第一电离能: Na15.具有下列电子排布的原子中,半径最大的为
A.1s22s22p63s1 B.1s22s22p63s23p64s1
C.1s22s22p63s2 D.1s22s22p63s23p64s2
二、填空题
16.分析下列图表,回答问题。
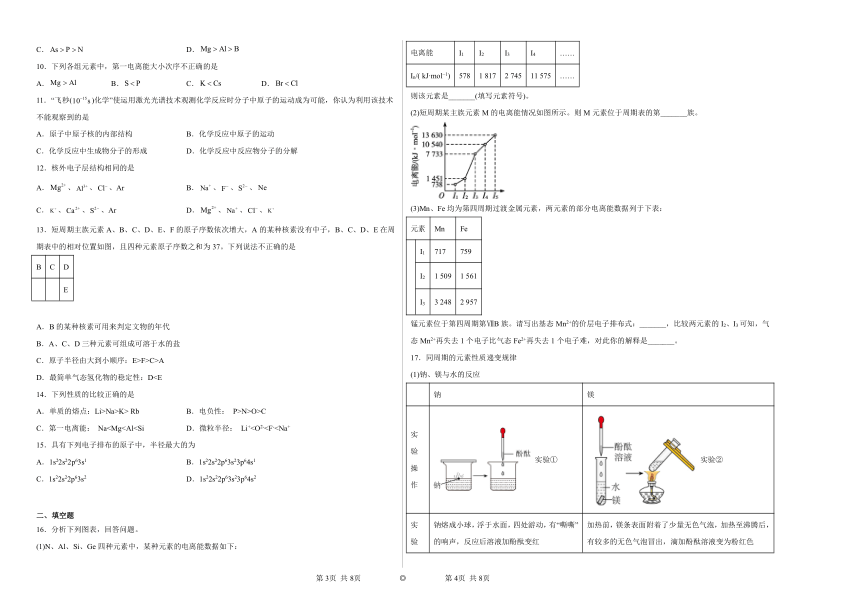
(1)N、Al、Si、Ge四种元素中,某种元素的电离能数据如下:
电离能 I1 I2 I3 I4 ……
In/( kJ mol 1) 578 1 817 2 745 11 575 ……
则该元素是_______(填写元素符号)。
(2)短周期某主族元素M的电离能情况如图所示。则M元素位于周期表的第_______族。
(3)Mn、Fe均为第四周期过渡金属元素,两元素的部分电离能数据列于下表:
元素 Mn Fe
I1 717 759
I2 1 509 1 561
I3 3 248 2 957
锰元素位于第四周期第ⅦB族。请写出基态Mn2+的价层电子排布式:_______,比较两元素的I2、I3可知,气态Mn2+再失去1个电子比气态Fe2+再失去1个电子难,对此你的解释是_______。
17.同周期的元素性质递变规律
(1)钠、镁与水的反应
钠 镁
实验操作 实验① 实验②
实验现象 钠熔成小球,浮于水面,四处游动,有“嘶嘶”的响声,反应后溶液加酚酞变红 加热前,镁条表面附着了少量无色气泡,加热至沸腾后,有较多的无色气泡冒出,滴加酚酞溶液变为粉红色
反应原理 ____________ ____________
结论 钠、镁均能与水反应,钠比镁活泼,金属性:_____________。
(2)Al(OH)3的制备与性质
实验探究:
①向AlCl3溶液中加入足量氨水,现象为__________,反应的离子方程式为__________;
②将①实验得到的沉淀分装两支试管中,一支试管中加入盐酸,现象为__________,离子方程式为_________;另一支试管中加入NaOH溶液,现象为________,离子方程式为______________。
③向MgCl2溶液加入过量NaOH溶液,现象_________,离子方程式为_____________。
两性氢氧化物:既能与酸反应又能与强碱反应,且均生成盐和水的氢氧化物。如 Al(OH)3。
(3)第三周期递变规律
①第三周期的Na、Mg、Al的金属性逐渐__________,NaOH、Mg(OH)2、Al(OH)3的碱性逐渐__________,NaOH为强碱,Mg(OH)2为中强碱,Al(OH)3为两性氢氧化物。
②第三周期的Si、P、S、Cl的非金属性逐渐__________,H3SiO3、H3PO4、H2SO4、HClO4的酸性逐渐__________。HClO4是最强的含氧酸,H2SiO3为难溶的弱酸,H3PO4为中强酸,H2SO4为强酸。
③同一周期从左到右,原子半径逐渐__________,失电子能力逐渐__________,得电子能力逐渐__________,金属性逐渐__________,非金属性逐渐__________。
三、结构与性质
18.回答下列问题:
(1)Mn位于元素周期表中第四周期_______族。
(2)比较离子半径:F-_______O2-(填“大于”“等于”或“小于”)。
(3)Li+与H-具有相同的电子构型,r(Li+)小于r(H-),原因是_______。
(4)光催化还原CO2制备CH4反应中,带状纳米Zn2GeO4是该反应的良好催化剂。Zn、Ge、O电负性由大至小的顺序是_______。
(5)在周期表中,与Li的化学性质最相似的邻族元素是_______。
(6)下列状态的镁中,电离最外层一个电子所需能量最大的是_______(填标号)。
A. B. C. D.
(7)黄铜是人类最早使用的合金之一,主要由Zn和Cu组成。第一电离能I1(Zn)_______I1(Cu)(填“大于”或“小于”)。原因是_______。
(8)元素Mn与O中,第一电离能较大的是_______。
(9)元素的基态气态原子得到一个电子形成气态负一价离子时所放出的能量称作第一电子亲和能(E1)。第二周期部分元素的E1变化趋势如图所示,其中除氮元素外,其他元素的E1自左而右依次增大的原因是_______;氮元素的E1呈现异常的原因是_______。
19.已知A、B、C、D、E、F是原子序数依次增大的前四周期元素。其中A是宇宙中含量最多的元素;B元素原子最高能级的不同轨道都有电子,并且自旋方向相同;C元素原子的价层电子排布是;D元素原子中只有两种形状的电子云,最外层只有一种自旋方向的电子;E与D的最高能层数相同,但其价层电子数等于其电子层数。F元素原子的最外层只有一个电子,其次外层内的所有轨道的电子均成对。
(1)请用元素符号完成下列空白:
①元素:A_______、B_______、C_______、D______、E______、F______。
②A、B、C三种元素的电负性大小顺序是:___________。
③B、C、D、E四种元素的第一电离能大小顺序是:___________。
(2)如图是A~F元素中某种元素的部分电离能,由此可判断该元素是___________。F元素位于周期表的___________区,此区元素的价电子层结构特点是___________。
第1页 共4页 ◎ 第2页 共4页
第1页 共4页 ◎ 第2页 共4页
参考答案:
1.A
【详解】A.钠离子和氮离子电子层数相同,但氮离子的核电荷数更小,半径更大,A正确;
B.非金属性O>N,所以电负性大小:χ(N)<χ(O),B错误;
C.最外层电子数相同,电子层数越多,第一电离能越小,所以电离能大小:I1(Na)>I1(K),C错误;
D.同主族自上而下金属性增强,最高价氧化物对应的水化物的碱性增强,所以碱性:KOH>NaOH,D错误;
综上所述答案为A。
2.C
【分析】根据第一至第四电离能分析该元素的电离能可知:第三电离能剧增,说明该元素容易失去2个电子,则该元素原子形成离子的化合价为+ 2价,即最外层应有2个电子,应为第ⅡA族元素,由此分析解答。
【详解】A.元素R最外层应有2个电子,所以R的最高正价为+2价,A错误;
B.元素R第一、第二电离能相差不大,元素的第三电离能剧增说明R元素位于元素周期表中第ⅡA族元素,B错误;
C.R元素的原子最外层共有2个电子,处于原子轨道的全充满的稳定状态,因此其第一电离能大于同一周期相邻元素,C正确;
D.R元素可能是Be或Mg,基态Be核外电子排布是1s22s2;基态Mg基态原子的电子排布式为ls2s2p63s2,D错误;
故合理选项是C。
3.C
【详解】A.由外围电子排布为4f75d16s2基态原子,判断此元素位于周期表中第六周期第ⅢB族,A正确;
B. d区和ds区的元素包括副族元素除镧系元素和锕系元素,全部是金属元素,B正确;
C.碳原子的核外电子排布为:1s22s22p2,该原子处于基态,当核外电子排布为1s22s12p3,该原子处于激发态,所以由碳原子的核外电子排布由转变为的过程为由激发态变为基态,释放能量,C错误;
D.非金属元素形成的共价化合物中,原子的最外层电子数除了2或8外,像一氧化碳、一氧化氮、二氧化硫等均不符合2或8电子结构,D正确;
答案为C。
4.B
【分析】元素周期表前三周期元素的离子aW3+、bX+、cY2-、dZ-具有相同电子层结构,核外电子数相等,所以a-3=b-1=c+2=d+1,Y、Z为非金属,应处于第二周期,故Y为O元素,Z为F元素,W、X为金属,应处于第三周期,W为Al元素,X为Na元素,即X为Na元素,Y为O元素,Z为F元素,W为Al元素,结合元素周期律分析解答。
【详解】A.由以上分析可知c=8,d=9,则质子数c<d,非金属性F>O,非金属性越强,对应的单质的氧化性越强,则阴离子的还原性越弱,则离子还原性O2->F-,故A错误;
B.同周期自左而右,电负性增大,同主族自上而下,电负性减小,故电负性:Z(F)>Y(O)>W(Al)>X(Na),故B正确;
C.非金属性F>O,非金属性越强,氢化物越稳定,氢化物的稳定性为HF>H2O,故C错误;
C.W为Al元素,X为Na元素,同周期中随原子序数增大,原子半径减小,第一电离能呈增大趋势,故原子半径Na>Al,第一电离能Na故答案选B。
5.B
【详解】A.和是Ts元素的两种同位素,质子数为117,核外电子数为117,最外层电子数为7,化学性质相同,A错误;
B.117号元素Ts位于周期表稀有气体118号前,位于第七周期第ⅦA族,B正确;
C.Ts为第七周期第ⅦA族元素,最后填入的能级为7p能级,位于p区,C错误;
D.按照现有规则,第八周期的元素种类数应为50种,则117号元素的正下方应为167号元素,D错误;
故选B。
6.D
【分析】硒元素原子的核电荷数为34,核外电子排布为:1s22s22p63s23p63d104s24p4。
【详解】A.硒元素位于元素周期表第四周期第VIA族,是非金属元素,A正确;
B.硒元素位于元素周期表第四周期第VIA族,位于周期表p区,B正确;
C.硒原子核外有34个电子,则有34种不同运动状态的电子,C正确;
D.硒原子的价电子排布式为,D错误。
答案选D。
7.D
【详解】A.周期数等于电子层数,主族元素最外层电子数等于主族序数,电子层数是4,最外层5个电子,所以As位于第四周期,第ⅤA族,故A错误;
B.As是非金属元素,故B错误;
C.非金属性越强最高价氧化物对应水化物的酸性越强,非金属性:P>As,所以酸性:H3AsO4>H3PO4,故C错误;
D.非金属性越强氢化物越稳定,非金属性:P>As,所以稳定性:AsH3<PH3,故D正确;
故选D。
8.C
【详解】①基态X的原子结构示意图为,X为S原子;
②基态Y原子的价电子排布式为,Y为Cl原子;
③基态的轨道表示式为,Z2-原子为S2-;
④基态T原子有2个电子层,电子式为,T为O原子;
电子层数越多半径越大,电子层数相同,质子数越多半径越小,S、S2-的电子层数相同、质子数相等,S2-的电子数多,S原子的半径小于S2-,所以半径由大到小排列顺序为③①②④,故选C。
9.B
【详解】A.同主族元素从上到下电负性减小,所以电负性,故A错误;
B.同主族元素从上到下电负性减小,同周期元素从左到右电负性增大,所以电负性,故B正确;
C.同主族元素从上到下电负性减小,所以电负性,故C错误;
D.同主族元素从上到下电负性减小,同周期元素从左到右电负性增大,所以电负性,故D错误;
选B。
10.C
【详解】A.同一周期随着原子序数变大,第一电离能变大,但是镁原子价电子为3s2全满稳定状态,电离能较大,故Al的第一电离能比Mg小;,A正确;
B.同一周期随着原子序数变大,第一电离能变大,P的3p轨道为半充满稳定状态,第一电离能大于同周期相邻元素,故P、S的第一电离能由大到小的顺序为P、S;B正确;
C.同一主族随原子序数变大,原子半径变大,第一电离能变小;,C错误;
D.同一主族随原子序数变大,原子半径变大,第一电离能变小;,D正确;
故选C。
11.A
【详解】运用激光光谱技术观测的是化学反应时分子中原子的运动,分子的形成和分解都是由原子的运动完成的,化学反应的最小粒子是原子,原子参与反应,原子核不参与反应;
故答案为:A。
12.C
【详解】A.镁离子、铝离子的电子层结构相同,比氯离子和氩原子少一个电子层,A错误;
B.钠离子、氟离子和氖原子电子层结构相同,比硫离子少一个电子层,B错误;
C.钾离子、钙离子、硫离子和氩核外都是18个电子,所以电子层结构相同,C正确;
D.钠离子和镁离子电子层结构相同,氯离子和钾离子电子层结构相同,但钠离子和镁离子比氯离子和钾离子少一个电子层,D错误;
故选C。
13.D
【分析】A的某种核素没有中子,故A为H元素;全部为短周期元素,根据图示位置关系,B 、C、 D第二周期,E、F为第三周期,且D、E同族。B、 C、 D、 E四种元素原子序数之和为37,则设D的原子序数为x,则x-2+x-1+x+x+8=37,则x=8,故B为C元素,C为N元素,D为O元素,E为S元素,都为主族元素,所以F为Cl元素;
【详解】A.B元素为碳,含碳的化合物在自然界中种类最多,A正确;
B.A、C、D三元素可组成化合物硝酸铵,可溶于水,B正确;
C.E、F第三周期,C为第二周期,A为第一周期,周期数越大,电子层数越多,半径越大,故,E、F半径大于C,C半径大于A;E、F同周期且F原子序数大于E,从左至右,原子半径依次减小,因此E半径大于F;所以原子半径由大到小顺序:E>F>C>A,C正确;
D.非金属性:D>E,非金属越强,气态氢化物的稳定性越强,因此氢化物的稳定性:D>E,D错误;
故选D。
14.A
【详解】A.同主族的金属元素从上到下,金属原子的价层电子数不变,原子半径逐渐增大,金属键逐渐减弱,金属熔点逐渐降低,故A正确;
B.元素的非金属性越强,电负性越大,电负性O>N>P>C,故B错误;
C.同周期元素第一电离能呈增大趋势,但IIA和VA族为全满和半满稳定状态,第一电离能反常的比相邻下一主族大,故第一电离能NaD.微粒的电子层数越多原子半径越大,电子层数相同时,核电荷数越多半径越小,微粒半径Li+故选:A。
15.B
【详解】1s22s22p63s1为Na,1s22s22p63s23p64s1为K,1s22s22p63s2为Mg,1s22s22p63s23p64s2为Ca;同周期自左而右原子半径减小,同主族自上而下原子半径增大,故原子半径:K>Na>Mg,K>Ca,故K原子半径最大,即B的原子半径最大;
故选B。
16.(1)Al
(2)ⅡA
(3) 3d5 由Mn2+转化为Mn3+时,3d能级由较稳定的3d5半充满状态转变为不稳定的3d4状态需要的能量较多;而Fe2+转化为Fe3+时,3d能级由不稳定的3d6状态转变为较稳定的3d5半充满状态需要的能量相对要少
【详解】(1)因为I4 I3,所以该元素原子最外层有3个电子,为铝元素;故答案为:Al。
(2)元素M的各级电离能逐渐增大,I1和I2差别较小,但I3 I2>I1,I3突跃式变大,即失去2个电子后,再失去电子变为+3价阳离子却非常困难,说明元素M失去2个电子后达到稳定结构,M元素位于周期表的第ⅡA族元素;故答案为:ⅡA。
(3)第ⅦB族元素的族序数=价层电子数,周期序数=电子层数,所以基态Mn原子价层电子排布式为3d54s2,Mn2+的3d能级电子排布式为3d5,Mn2+的3d能级电子为3d5,是半充满状态,很难失去电子,而Fe2+的3d能级电子排布式为3d6,失去一个电子,即变为半充满的3d5状态,所以气态Mn2+再失去一个电子比气态Fe2+再失去一个电子难;故答案为:3d5;由Mn2+转化为Mn3+时,3d能级由较稳定的3d5半充满状态转变为不稳定的3d4状态需要的能量较多;而Fe2+转化为Fe3+时,3d能级由不稳定的3d6状态转变为较稳定的3d5半充满状态需要的能量相对要少。
17.(1) 2Na+2H2O=2NaOH+H2↑ Mg+2H2OMg(OH)2↓+H2↑ 金属性:Na>Mg
(2) 产生白色沉淀 Al3++3NH3·H2O=Al(OH)3↓+3NH 白色沉淀逐渐溶解 Al(OH)3+3H+=Al3++3H2O 白色沉淀逐渐溶解 Al(OH)3+OH-=AlO+2H2O 产生白色沉淀 Mg2++2OH-=Mg(OH)2↓
(3) 减弱 减弱 增强 增强 减小 减弱 增强 减弱 增强
【详解】(1)钠和水常温下剧烈反应生成碱和气体,化学方程式2Na+2H2O=2NaOH+H2↑,镁常温下和水不反应,加热时剧烈反应,生成碱和气体,化学方程式Mg+2H2OMg(OH)2↓+H2↑,金属单质和水或酸反应越剧烈,金属的金属性越强,所以金属性:Na>Mg,答案:2Na+2H2O=2NaOH+H2↑;Mg+2H2OMg(OH)2↓+H2↑;金属性:Na>Mg;
(2)向AlCl3溶液中加入足量氨水,生成白色沉淀,Al3++3NH3·H2O=Al(OH)3↓+3 ,氢氧化铝不溶于氨水。实验得到的沉淀分装两支试管中,一支试管中加入盐酸,白色沉淀逐渐溶解,生成盐和水,离子方程式为Al(OH)3+3H+=Al3++3H2O;另一支试管中加入NaOH溶液,白色沉淀逐渐溶解,生成偏铝酸盐和水,离子方程式为Al(OH)3+OH-=AlO+2H2O。向MgCl2溶液加入过量NaOH溶液,产生白色沉淀,离子方程式为Mg2++2OH-=Mg(OH)2↓。答案:产生白色沉淀;Al3++3NH3·H2O=Al(OH)3↓+3NH;白色沉淀逐渐溶解;Al(OH)3+3H+=Al3++3H2O;白色沉淀逐渐溶解;Al(OH)3+OH-=AlO+2H2O;产生白色沉淀;Mg2++2OH-=Mg(OH)2↓;
(3)第三周期的Na、Mg、Al的金属性逐渐减弱,最高价氧化物的水化物NaOH、Mg(OH)2、Al(OH)3的碱性逐渐减弱,NaOH为强碱,Mg(OH)2为中强碱,Al(OH)3为两性氢氧化物。第三周期的Si、P、S、Cl的非金属性逐渐增强,最高价氧化物的水化物H2SiO3、H3PO4、H2SO4、HClO4的酸性逐渐增强。HClO4是最强的含氧酸,H2SiO3为难溶的弱酸,H3PO4为中强酸,H2SO4为强酸。同一周期从左到右,原子半径逐渐减小,失电子能力逐渐减弱,得电子能力逐渐增强,金属性逐渐减弱,非金属性逐渐增强。答案:减弱;减弱;增强;增强;减小;减弱;增强;减弱; 增强。
18.(1)ⅦB
(2)小于
(3)由于锂的核电荷数较大,原子核对最外层电子的吸引力较大,因此Li+半径小于H-
(4)O>Ge>Zn
(5)Mg
(6)A
(7) 大于 Zn核外电子排布为全满稳定结构,较难失去电子
(8)氧
(9) 同周期随着核电荷数依次增大,原子半径逐渐变小,故结合一个电子释放出的能量依次增大 N的2p能级处于半充满状态,相对稳定,不易结合一个电子
【详解】(1)Mn是25号元素,根据原子序数与元素周期表的位置判断其位置;
(2)F-和O2-的核外电子排布相同,核电荷数越大,则半径越小,故半径:F-(3)由于锂的核电荷数较大,原子核对最外层电子的吸引力较大,因此Li+半径小于H-;
(4)元素的非金属性越强,其吸引电子的能力就越强,元素的电负性就越大。元素Zn、Ge、O的非金属性强弱顺序是:O>Ge>Zn,所以这三种元素的电负性由大至小的顺序是O>Ge>Zn;
(5)根据元素周期表和对角线原则可知与锂化学性质相似的是镁;
(6)[Ne]3s1属于基态的Mg+,由于Mg的第二电离能高于其第一电离能,故其再失去一个电子所需能量较高;[Ne] 3s2属于基态Mg原子,其失去一个电子变为基态Mg+;[Ne] 3s13p1属于激发态Mg原子,其失去一个电子所需能量低于基态Mg原子;[Ne] 3p1属于激发态Mg+,其失去一个电子所需能量低于基态Mg+,综上所述,电离最外层一个电子所需能量最大的是[Ne]3s1,答案选A;
(7)Zn的第一电离能应该高于Cu的第一电离能,原因是,Zn的核外电子排布已经达到了每个能级都是全满的稳定结构,所以失电子比较困难。同时也可以考虑到Zn最外层上是一对电子,而Cu的最外层是一个电子,Zn电离最外层一个电子还要拆开电子对,额外吸收能量;
(8)元素Mn与O中,由于O元素是非金属而Mn是过渡元素,所以第一电离能较大的是O;
(9)根据图,同周期随着核电荷数依次增大,原子半径逐渐变小,故结合一个电子释放出的能量依次增大;氮元素的2p能级达到半满状态,原子相对稳定,不易失去电子。
19.(1) H N O Na Al Cu O >N>H N>O>Al>Na
(2) Al ds 价电子构型是(n-1)d10ns1~2,即次外层d轨道是满的,最外层轨道上有1-2个电子
【分析】由题干信息可知,A、B、C、D、E、F是原子序数依次增大的前四周期元素。其中A是宇宙中含量最多的元素,故A为H;C元素原子的价层电子排布是,n=2,即1s22s22p4,故为O;B元素原子最高能级的不同轨道都有电子,并且自旋方向相同,即2p3,故B为N;D元素原子中只有两种形状的电子云即s、p能级,最外层只有一种自旋方向的电子即3s1,故D为Na;E与D的最高能层数相同,但其价层电子数等于其电子层数,故E为Al,F元素原子的最外层只有一个电子,其次外层内的所有轨道的电子均成对即价电子排布为3d104s1,故F为Cu,综上分析可知,A、B、C、D、E、F分别是H、N、O、Na、Al、Cu,据此分析解题。
【详解】(1)①由分析可知,元素A、B、C、D、E、F分别是H,N,O,Na,Al,Cu,故答案为: H;N;O;Na;Al;Cu;
②由分析可知,A、B、C三种元素分别为H,N,O,根据同一周期从左往右元素的电负性依次增大,同一主族从上往下元素的电负性依次减小,故其电负性大小顺序是:O >N>H,故答案为:O >N>H;
③由分析可知,B、C、D、E四种元素分别为N、O、Na、Al,根据同一周期从左往右元素的第一电离能呈增大趋势,IIA与IIIA、VA与VIA反常,同一主族从上往下元素的第一电离能依次减小,故其第一电离能大小顺序是:N>O>Al>Na,故答案为:N>O>Al>Na;
(2)由图可知,该元素的第一至第三电离能变化比较平稳,而第四电离能比第三电离能突然增大很多,故说明该元素的最外层上只有3个电子,由此可判断该元素是Al,已知F元素为Cu,Cu位于周期表的ds区,此区元素的价电子层结构特点是价电子构型是(n-1)d10ns1~2,即次外层d轨道是满的,最外层轨道上有1-2个电子,故答案为:Al;ds;价电子构型是(n-1)d10ns1~2,即次外层d轨道是满的,最外层轨道上有1-2个电子。
答案第1页,共2页
答案第1页,共2页
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1.当汽车遭受一定碰撞力量以后,安全气囊中的物质会发生剧烈的反应:
NaN3+ KNO3= K2O + Na2O + N2↑(未配平),生成大量气体。下列说法正确的是
A.半径大小:r(Na+) < r(N3-) B.电负性大小:χ(N) > χ(O)
C.第一电离能:I1(K) > I1(Na) D.碱性强弱:KOH < NaOH
2.下表列出了某短周期元素R的各级电离能数据(用I1、I2…^表示,单位kJ/mol)。
I1 I2 I3 I4 ……
740 1500 7700 10500
下列关于元素R的判断正确的是
A.R的最高正价为+1价
B.R元素位于元素周期表中第ⅢA族
C.R元素第一电离能大于同周期相邻元素
D.R元素基态原子的电子排布式为1s22s22p1
3.下列说法不正确的是
A.某外围电子排布为基态原子,该元素位于周期表中第六周期第IIIB族
B.在元素周期表中,d区和ds区的元素都是金属元素
C.当碳原子的核外电子排布由 转变为 时,吸收能量,由基态转化成激发态
D.非金属元素形成的共价化合物中,原子的最外层电子数不一定是2或8
4.已知号元素的离子、、、都具有相同电子层结构,下列关系正确的是
A.质子数:,离子的还原性:
B.电负性:
C.氢化物的稳定性:
D.原子半径:,第一电离能:
5.2017年5月9日中国科学院正式向社会发布113号、115号、117号和118号元素的中文名称。已知117号元素有多种原子,如、等。下列说法正确的是
A.和的化学性质完全不同
B.Ts位于周期表的第七周期ⅦA族
C.在Ts原子中,最后填入电子的轨道能级符号是f,故Ts位于周期表的f区
D.在周期表中,假设第八周期按现有规则填满,则117号元素的正下方是149号元素
6.1817年,瑞典的贝采利乌斯从硫酸厂的铅室底部的红色粉状物质中制得硒。硒在元素周期表中的数据如图所示,下列关于硒元素及其基态原子的说法错误的是
A.属于非金属元素 B.位于周期表p区
C.有34种不同运动状态的电子 D.价层电子排布式为3d104s24p4
7.的原子结构示意图为,下列关于的描述正确的是
A.位于第五周期,第Ⅴ族 B.属于金属元素
C.酸性: D.稳定性:
8.下列选项中,所叙述的粒子按半径由大到小排列时,顺序正确的是
①基态X的原子结构示意图为
②基态Y原子的价电子排布式为
③基态的轨道表示式为
④基态T原子有2个电子层,电子式为
A.①②③④ B.③④①②
C.③①②④ D.①②④③
9.下列各选项中,按元素的电负性由大到小排列,顺序正确的是
A. B.
C. D.
10.下列各组元素中,第一电离能大小次序不正确的是
A. B. C. D.
11.“飞秒()化学”使运用激光光谱技术观测化学反应时分子中原子的运动成为可能,你认为利用该技术不能观察到的是
A.原子中原子核的内部结构 B.化学反应中原子的运动
C.化学反应中生成物分子的形成 D.化学反应中反应物分子的分解
12.核外电子层结构相同的是
A.、、、Ar B.、、、
C.、、、Ar D.、、、
13.短周期主族元素A、B、C、D、E、F的原子序数依次增大,A的某种核素没有中子,B、C、D、E在周期表中的相对位置如图,且四种元素原子序数之和为37。下列说法不正确的是
B C D
E
A.B的某种核素可用来判定文物的年代
B.A、C、D三种元素可组成可溶于水的盐
C.原子半径由大到小顺序:E>F>C>A
D.最简单气态氢化物的稳定性:D
A.单质的熔点:Li>Na>K> Rb B.电负性: P>N>O>C
C.第一电离能: Na
A.1s22s22p63s1 B.1s22s22p63s23p64s1
C.1s22s22p63s2 D.1s22s22p63s23p64s2
二、填空题
16.分析下列图表,回答问题。
(1)N、Al、Si、Ge四种元素中,某种元素的电离能数据如下:
电离能 I1 I2 I3 I4 ……
In/( kJ mol 1) 578 1 817 2 745 11 575 ……
则该元素是_______(填写元素符号)。
(2)短周期某主族元素M的电离能情况如图所示。则M元素位于周期表的第_______族。
(3)Mn、Fe均为第四周期过渡金属元素,两元素的部分电离能数据列于下表:
元素 Mn Fe
I1 717 759
I2 1 509 1 561
I3 3 248 2 957
锰元素位于第四周期第ⅦB族。请写出基态Mn2+的价层电子排布式:_______,比较两元素的I2、I3可知,气态Mn2+再失去1个电子比气态Fe2+再失去1个电子难,对此你的解释是_______。
17.同周期的元素性质递变规律
(1)钠、镁与水的反应
钠 镁
实验操作 实验① 实验②
实验现象 钠熔成小球,浮于水面,四处游动,有“嘶嘶”的响声,反应后溶液加酚酞变红 加热前,镁条表面附着了少量无色气泡,加热至沸腾后,有较多的无色气泡冒出,滴加酚酞溶液变为粉红色
反应原理 ____________ ____________
结论 钠、镁均能与水反应,钠比镁活泼,金属性:_____________。
(2)Al(OH)3的制备与性质
实验探究:
①向AlCl3溶液中加入足量氨水,现象为__________,反应的离子方程式为__________;
②将①实验得到的沉淀分装两支试管中,一支试管中加入盐酸,现象为__________,离子方程式为_________;另一支试管中加入NaOH溶液,现象为________,离子方程式为______________。
③向MgCl2溶液加入过量NaOH溶液,现象_________,离子方程式为_____________。
两性氢氧化物:既能与酸反应又能与强碱反应,且均生成盐和水的氢氧化物。如 Al(OH)3。
(3)第三周期递变规律
①第三周期的Na、Mg、Al的金属性逐渐__________,NaOH、Mg(OH)2、Al(OH)3的碱性逐渐__________,NaOH为强碱,Mg(OH)2为中强碱,Al(OH)3为两性氢氧化物。
②第三周期的Si、P、S、Cl的非金属性逐渐__________,H3SiO3、H3PO4、H2SO4、HClO4的酸性逐渐__________。HClO4是最强的含氧酸,H2SiO3为难溶的弱酸,H3PO4为中强酸,H2SO4为强酸。
③同一周期从左到右,原子半径逐渐__________,失电子能力逐渐__________,得电子能力逐渐__________,金属性逐渐__________,非金属性逐渐__________。
三、结构与性质
18.回答下列问题:
(1)Mn位于元素周期表中第四周期_______族。
(2)比较离子半径:F-_______O2-(填“大于”“等于”或“小于”)。
(3)Li+与H-具有相同的电子构型,r(Li+)小于r(H-),原因是_______。
(4)光催化还原CO2制备CH4反应中,带状纳米Zn2GeO4是该反应的良好催化剂。Zn、Ge、O电负性由大至小的顺序是_______。
(5)在周期表中,与Li的化学性质最相似的邻族元素是_______。
(6)下列状态的镁中,电离最外层一个电子所需能量最大的是_______(填标号)。
A. B. C. D.
(7)黄铜是人类最早使用的合金之一,主要由Zn和Cu组成。第一电离能I1(Zn)_______I1(Cu)(填“大于”或“小于”)。原因是_______。
(8)元素Mn与O中,第一电离能较大的是_______。
(9)元素的基态气态原子得到一个电子形成气态负一价离子时所放出的能量称作第一电子亲和能(E1)。第二周期部分元素的E1变化趋势如图所示,其中除氮元素外,其他元素的E1自左而右依次增大的原因是_______;氮元素的E1呈现异常的原因是_______。
19.已知A、B、C、D、E、F是原子序数依次增大的前四周期元素。其中A是宇宙中含量最多的元素;B元素原子最高能级的不同轨道都有电子,并且自旋方向相同;C元素原子的价层电子排布是;D元素原子中只有两种形状的电子云,最外层只有一种自旋方向的电子;E与D的最高能层数相同,但其价层电子数等于其电子层数。F元素原子的最外层只有一个电子,其次外层内的所有轨道的电子均成对。
(1)请用元素符号完成下列空白:
①元素:A_______、B_______、C_______、D______、E______、F______。
②A、B、C三种元素的电负性大小顺序是:___________。
③B、C、D、E四种元素的第一电离能大小顺序是:___________。
(2)如图是A~F元素中某种元素的部分电离能,由此可判断该元素是___________。F元素位于周期表的___________区,此区元素的价电子层结构特点是___________。
第1页 共4页 ◎ 第2页 共4页
第1页 共4页 ◎ 第2页 共4页
参考答案:
1.A
【详解】A.钠离子和氮离子电子层数相同,但氮离子的核电荷数更小,半径更大,A正确;
B.非金属性O>N,所以电负性大小:χ(N)<χ(O),B错误;
C.最外层电子数相同,电子层数越多,第一电离能越小,所以电离能大小:I1(Na)>I1(K),C错误;
D.同主族自上而下金属性增强,最高价氧化物对应的水化物的碱性增强,所以碱性:KOH>NaOH,D错误;
综上所述答案为A。
2.C
【分析】根据第一至第四电离能分析该元素的电离能可知:第三电离能剧增,说明该元素容易失去2个电子,则该元素原子形成离子的化合价为+ 2价,即最外层应有2个电子,应为第ⅡA族元素,由此分析解答。
【详解】A.元素R最外层应有2个电子,所以R的最高正价为+2价,A错误;
B.元素R第一、第二电离能相差不大,元素的第三电离能剧增说明R元素位于元素周期表中第ⅡA族元素,B错误;
C.R元素的原子最外层共有2个电子,处于原子轨道的全充满的稳定状态,因此其第一电离能大于同一周期相邻元素,C正确;
D.R元素可能是Be或Mg,基态Be核外电子排布是1s22s2;基态Mg基态原子的电子排布式为ls2s2p63s2,D错误;
故合理选项是C。
3.C
【详解】A.由外围电子排布为4f75d16s2基态原子,判断此元素位于周期表中第六周期第ⅢB族,A正确;
B. d区和ds区的元素包括副族元素除镧系元素和锕系元素,全部是金属元素,B正确;
C.碳原子的核外电子排布为:1s22s22p2,该原子处于基态,当核外电子排布为1s22s12p3,该原子处于激发态,所以由碳原子的核外电子排布由转变为的过程为由激发态变为基态,释放能量,C错误;
D.非金属元素形成的共价化合物中,原子的最外层电子数除了2或8外,像一氧化碳、一氧化氮、二氧化硫等均不符合2或8电子结构,D正确;
答案为C。
4.B
【分析】元素周期表前三周期元素的离子aW3+、bX+、cY2-、dZ-具有相同电子层结构,核外电子数相等,所以a-3=b-1=c+2=d+1,Y、Z为非金属,应处于第二周期,故Y为O元素,Z为F元素,W、X为金属,应处于第三周期,W为Al元素,X为Na元素,即X为Na元素,Y为O元素,Z为F元素,W为Al元素,结合元素周期律分析解答。
【详解】A.由以上分析可知c=8,d=9,则质子数c<d,非金属性F>O,非金属性越强,对应的单质的氧化性越强,则阴离子的还原性越弱,则离子还原性O2->F-,故A错误;
B.同周期自左而右,电负性增大,同主族自上而下,电负性减小,故电负性:Z(F)>Y(O)>W(Al)>X(Na),故B正确;
C.非金属性F>O,非金属性越强,氢化物越稳定,氢化物的稳定性为HF>H2O,故C错误;
C.W为Al元素,X为Na元素,同周期中随原子序数增大,原子半径减小,第一电离能呈增大趋势,故原子半径Na>Al,第一电离能Na
5.B
【详解】A.和是Ts元素的两种同位素,质子数为117,核外电子数为117,最外层电子数为7,化学性质相同,A错误;
B.117号元素Ts位于周期表稀有气体118号前,位于第七周期第ⅦA族,B正确;
C.Ts为第七周期第ⅦA族元素,最后填入的能级为7p能级,位于p区,C错误;
D.按照现有规则,第八周期的元素种类数应为50种,则117号元素的正下方应为167号元素,D错误;
故选B。
6.D
【分析】硒元素原子的核电荷数为34,核外电子排布为:1s22s22p63s23p63d104s24p4。
【详解】A.硒元素位于元素周期表第四周期第VIA族,是非金属元素,A正确;
B.硒元素位于元素周期表第四周期第VIA族,位于周期表p区,B正确;
C.硒原子核外有34个电子,则有34种不同运动状态的电子,C正确;
D.硒原子的价电子排布式为,D错误。
答案选D。
7.D
【详解】A.周期数等于电子层数,主族元素最外层电子数等于主族序数,电子层数是4,最外层5个电子,所以As位于第四周期,第ⅤA族,故A错误;
B.As是非金属元素,故B错误;
C.非金属性越强最高价氧化物对应水化物的酸性越强,非金属性:P>As,所以酸性:H3AsO4>H3PO4,故C错误;
D.非金属性越强氢化物越稳定,非金属性:P>As,所以稳定性:AsH3<PH3,故D正确;
故选D。
8.C
【详解】①基态X的原子结构示意图为,X为S原子;
②基态Y原子的价电子排布式为,Y为Cl原子;
③基态的轨道表示式为,Z2-原子为S2-;
④基态T原子有2个电子层,电子式为,T为O原子;
电子层数越多半径越大,电子层数相同,质子数越多半径越小,S、S2-的电子层数相同、质子数相等,S2-的电子数多,S原子的半径小于S2-,所以半径由大到小排列顺序为③①②④,故选C。
9.B
【详解】A.同主族元素从上到下电负性减小,所以电负性,故A错误;
B.同主族元素从上到下电负性减小,同周期元素从左到右电负性增大,所以电负性,故B正确;
C.同主族元素从上到下电负性减小,所以电负性,故C错误;
D.同主族元素从上到下电负性减小,同周期元素从左到右电负性增大,所以电负性,故D错误;
选B。
10.C
【详解】A.同一周期随着原子序数变大,第一电离能变大,但是镁原子价电子为3s2全满稳定状态,电离能较大,故Al的第一电离能比Mg小;,A正确;
B.同一周期随着原子序数变大,第一电离能变大,P的3p轨道为半充满稳定状态,第一电离能大于同周期相邻元素,故P、S的第一电离能由大到小的顺序为P、S;B正确;
C.同一主族随原子序数变大,原子半径变大,第一电离能变小;,C错误;
D.同一主族随原子序数变大,原子半径变大,第一电离能变小;,D正确;
故选C。
11.A
【详解】运用激光光谱技术观测的是化学反应时分子中原子的运动,分子的形成和分解都是由原子的运动完成的,化学反应的最小粒子是原子,原子参与反应,原子核不参与反应;
故答案为:A。
12.C
【详解】A.镁离子、铝离子的电子层结构相同,比氯离子和氩原子少一个电子层,A错误;
B.钠离子、氟离子和氖原子电子层结构相同,比硫离子少一个电子层,B错误;
C.钾离子、钙离子、硫离子和氩核外都是18个电子,所以电子层结构相同,C正确;
D.钠离子和镁离子电子层结构相同,氯离子和钾离子电子层结构相同,但钠离子和镁离子比氯离子和钾离子少一个电子层,D错误;
故选C。
13.D
【分析】A的某种核素没有中子,故A为H元素;全部为短周期元素,根据图示位置关系,B 、C、 D第二周期,E、F为第三周期,且D、E同族。B、 C、 D、 E四种元素原子序数之和为37,则设D的原子序数为x,则x-2+x-1+x+x+8=37,则x=8,故B为C元素,C为N元素,D为O元素,E为S元素,都为主族元素,所以F为Cl元素;
【详解】A.B元素为碳,含碳的化合物在自然界中种类最多,A正确;
B.A、C、D三元素可组成化合物硝酸铵,可溶于水,B正确;
C.E、F第三周期,C为第二周期,A为第一周期,周期数越大,电子层数越多,半径越大,故,E、F半径大于C,C半径大于A;E、F同周期且F原子序数大于E,从左至右,原子半径依次减小,因此E半径大于F;所以原子半径由大到小顺序:E>F>C>A,C正确;
D.非金属性:D>E,非金属越强,气态氢化物的稳定性越强,因此氢化物的稳定性:D>E,D错误;
故选D。
14.A
【详解】A.同主族的金属元素从上到下,金属原子的价层电子数不变,原子半径逐渐增大,金属键逐渐减弱,金属熔点逐渐降低,故A正确;
B.元素的非金属性越强,电负性越大,电负性O>N>P>C,故B错误;
C.同周期元素第一电离能呈增大趋势,但IIA和VA族为全满和半满稳定状态,第一电离能反常的比相邻下一主族大,故第一电离能Na
15.B
【详解】1s22s22p63s1为Na,1s22s22p63s23p64s1为K,1s22s22p63s2为Mg,1s22s22p63s23p64s2为Ca;同周期自左而右原子半径减小,同主族自上而下原子半径增大,故原子半径:K>Na>Mg,K>Ca,故K原子半径最大,即B的原子半径最大;
故选B。
16.(1)Al
(2)ⅡA
(3) 3d5 由Mn2+转化为Mn3+时,3d能级由较稳定的3d5半充满状态转变为不稳定的3d4状态需要的能量较多;而Fe2+转化为Fe3+时,3d能级由不稳定的3d6状态转变为较稳定的3d5半充满状态需要的能量相对要少
【详解】(1)因为I4 I3,所以该元素原子最外层有3个电子,为铝元素;故答案为:Al。
(2)元素M的各级电离能逐渐增大,I1和I2差别较小,但I3 I2>I1,I3突跃式变大,即失去2个电子后,再失去电子变为+3价阳离子却非常困难,说明元素M失去2个电子后达到稳定结构,M元素位于周期表的第ⅡA族元素;故答案为:ⅡA。
(3)第ⅦB族元素的族序数=价层电子数,周期序数=电子层数,所以基态Mn原子价层电子排布式为3d54s2,Mn2+的3d能级电子排布式为3d5,Mn2+的3d能级电子为3d5,是半充满状态,很难失去电子,而Fe2+的3d能级电子排布式为3d6,失去一个电子,即变为半充满的3d5状态,所以气态Mn2+再失去一个电子比气态Fe2+再失去一个电子难;故答案为:3d5;由Mn2+转化为Mn3+时,3d能级由较稳定的3d5半充满状态转变为不稳定的3d4状态需要的能量较多;而Fe2+转化为Fe3+时,3d能级由不稳定的3d6状态转变为较稳定的3d5半充满状态需要的能量相对要少。
17.(1) 2Na+2H2O=2NaOH+H2↑ Mg+2H2OMg(OH)2↓+H2↑ 金属性:Na>Mg
(2) 产生白色沉淀 Al3++3NH3·H2O=Al(OH)3↓+3NH 白色沉淀逐渐溶解 Al(OH)3+3H+=Al3++3H2O 白色沉淀逐渐溶解 Al(OH)3+OH-=AlO+2H2O 产生白色沉淀 Mg2++2OH-=Mg(OH)2↓
(3) 减弱 减弱 增强 增强 减小 减弱 增强 减弱 增强
【详解】(1)钠和水常温下剧烈反应生成碱和气体,化学方程式2Na+2H2O=2NaOH+H2↑,镁常温下和水不反应,加热时剧烈反应,生成碱和气体,化学方程式Mg+2H2OMg(OH)2↓+H2↑,金属单质和水或酸反应越剧烈,金属的金属性越强,所以金属性:Na>Mg,答案:2Na+2H2O=2NaOH+H2↑;Mg+2H2OMg(OH)2↓+H2↑;金属性:Na>Mg;
(2)向AlCl3溶液中加入足量氨水,生成白色沉淀,Al3++3NH3·H2O=Al(OH)3↓+3 ,氢氧化铝不溶于氨水。实验得到的沉淀分装两支试管中,一支试管中加入盐酸,白色沉淀逐渐溶解,生成盐和水,离子方程式为Al(OH)3+3H+=Al3++3H2O;另一支试管中加入NaOH溶液,白色沉淀逐渐溶解,生成偏铝酸盐和水,离子方程式为Al(OH)3+OH-=AlO+2H2O。向MgCl2溶液加入过量NaOH溶液,产生白色沉淀,离子方程式为Mg2++2OH-=Mg(OH)2↓。答案:产生白色沉淀;Al3++3NH3·H2O=Al(OH)3↓+3NH;白色沉淀逐渐溶解;Al(OH)3+3H+=Al3++3H2O;白色沉淀逐渐溶解;Al(OH)3+OH-=AlO+2H2O;产生白色沉淀;Mg2++2OH-=Mg(OH)2↓;
(3)第三周期的Na、Mg、Al的金属性逐渐减弱,最高价氧化物的水化物NaOH、Mg(OH)2、Al(OH)3的碱性逐渐减弱,NaOH为强碱,Mg(OH)2为中强碱,Al(OH)3为两性氢氧化物。第三周期的Si、P、S、Cl的非金属性逐渐增强,最高价氧化物的水化物H2SiO3、H3PO4、H2SO4、HClO4的酸性逐渐增强。HClO4是最强的含氧酸,H2SiO3为难溶的弱酸,H3PO4为中强酸,H2SO4为强酸。同一周期从左到右,原子半径逐渐减小,失电子能力逐渐减弱,得电子能力逐渐增强,金属性逐渐减弱,非金属性逐渐增强。答案:减弱;减弱;增强;增强;减小;减弱;增强;减弱; 增强。
18.(1)ⅦB
(2)小于
(3)由于锂的核电荷数较大,原子核对最外层电子的吸引力较大,因此Li+半径小于H-
(4)O>Ge>Zn
(5)Mg
(6)A
(7) 大于 Zn核外电子排布为全满稳定结构,较难失去电子
(8)氧
(9) 同周期随着核电荷数依次增大,原子半径逐渐变小,故结合一个电子释放出的能量依次增大 N的2p能级处于半充满状态,相对稳定,不易结合一个电子
【详解】(1)Mn是25号元素,根据原子序数与元素周期表的位置判断其位置;
(2)F-和O2-的核外电子排布相同,核电荷数越大,则半径越小,故半径:F-
(4)元素的非金属性越强,其吸引电子的能力就越强,元素的电负性就越大。元素Zn、Ge、O的非金属性强弱顺序是:O>Ge>Zn,所以这三种元素的电负性由大至小的顺序是O>Ge>Zn;
(5)根据元素周期表和对角线原则可知与锂化学性质相似的是镁;
(6)[Ne]3s1属于基态的Mg+,由于Mg的第二电离能高于其第一电离能,故其再失去一个电子所需能量较高;[Ne] 3s2属于基态Mg原子,其失去一个电子变为基态Mg+;[Ne] 3s13p1属于激发态Mg原子,其失去一个电子所需能量低于基态Mg原子;[Ne] 3p1属于激发态Mg+,其失去一个电子所需能量低于基态Mg+,综上所述,电离最外层一个电子所需能量最大的是[Ne]3s1,答案选A;
(7)Zn的第一电离能应该高于Cu的第一电离能,原因是,Zn的核外电子排布已经达到了每个能级都是全满的稳定结构,所以失电子比较困难。同时也可以考虑到Zn最外层上是一对电子,而Cu的最外层是一个电子,Zn电离最外层一个电子还要拆开电子对,额外吸收能量;
(8)元素Mn与O中,由于O元素是非金属而Mn是过渡元素,所以第一电离能较大的是O;
(9)根据图,同周期随着核电荷数依次增大,原子半径逐渐变小,故结合一个电子释放出的能量依次增大;氮元素的2p能级达到半满状态,原子相对稳定,不易失去电子。
19.(1) H N O Na Al Cu O >N>H N>O>Al>Na
(2) Al ds 价电子构型是(n-1)d10ns1~2,即次外层d轨道是满的,最外层轨道上有1-2个电子
【分析】由题干信息可知,A、B、C、D、E、F是原子序数依次增大的前四周期元素。其中A是宇宙中含量最多的元素,故A为H;C元素原子的价层电子排布是,n=2,即1s22s22p4,故为O;B元素原子最高能级的不同轨道都有电子,并且自旋方向相同,即2p3,故B为N;D元素原子中只有两种形状的电子云即s、p能级,最外层只有一种自旋方向的电子即3s1,故D为Na;E与D的最高能层数相同,但其价层电子数等于其电子层数,故E为Al,F元素原子的最外层只有一个电子,其次外层内的所有轨道的电子均成对即价电子排布为3d104s1,故F为Cu,综上分析可知,A、B、C、D、E、F分别是H、N、O、Na、Al、Cu,据此分析解题。
【详解】(1)①由分析可知,元素A、B、C、D、E、F分别是H,N,O,Na,Al,Cu,故答案为: H;N;O;Na;Al;Cu;
②由分析可知,A、B、C三种元素分别为H,N,O,根据同一周期从左往右元素的电负性依次增大,同一主族从上往下元素的电负性依次减小,故其电负性大小顺序是:O >N>H,故答案为:O >N>H;
③由分析可知,B、C、D、E四种元素分别为N、O、Na、Al,根据同一周期从左往右元素的第一电离能呈增大趋势,IIA与IIIA、VA与VIA反常,同一主族从上往下元素的第一电离能依次减小,故其第一电离能大小顺序是:N>O>Al>Na,故答案为:N>O>Al>Na;
(2)由图可知,该元素的第一至第三电离能变化比较平稳,而第四电离能比第三电离能突然增大很多,故说明该元素的最外层上只有3个电子,由此可判断该元素是Al,已知F元素为Cu,Cu位于周期表的ds区,此区元素的价电子层结构特点是价电子构型是(n-1)d10ns1~2,即次外层d轨道是满的,最外层轨道上有1-2个电子,故答案为:Al;ds;价电子构型是(n-1)d10ns1~2,即次外层d轨道是满的,最外层轨道上有1-2个电子。
答案第1页,共2页
答案第1页,共2页
