第三章第五节有机合成同步练习(含解析)2022-2023学年下学期高二化学人教版(2019)选择性必修3
文档属性
| 名称 | 第三章第五节有机合成同步练习(含解析)2022-2023学年下学期高二化学人教版(2019)选择性必修3 |
|
|
| 格式 | docx | ||
| 文件大小 | 1.5MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-06-21 00:00:00 | ||
图片预览




文档简介
第三章第五节有机合成同步练习
学校:___________姓名:___________班级:___________考号:___________
一、单选题
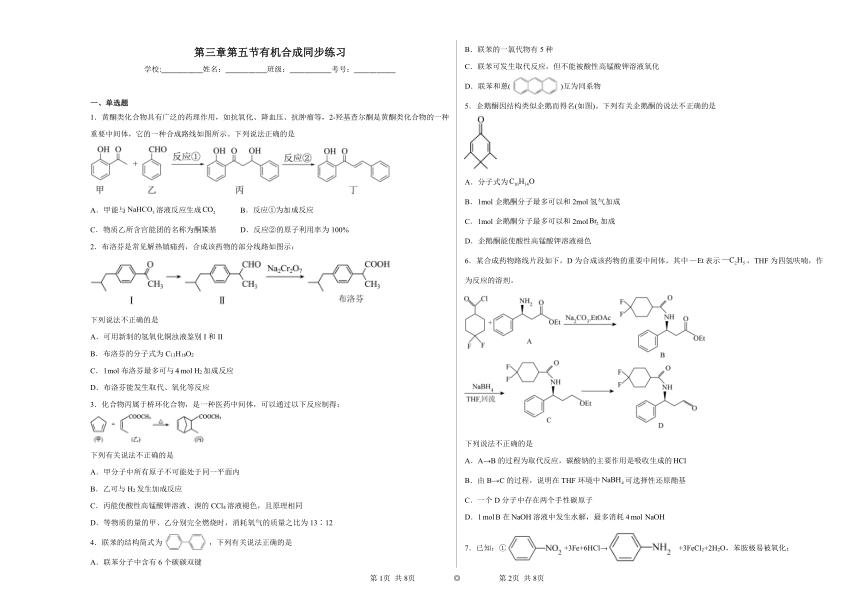
1.黄酮类化合物具有广泛的药理作用,如抗氧化、降血压、抗肿瘤等,2-羟基查尔酮是黄酮类化合物的一种重要中间体,它的一种合成路线如图所示。下列说法正确的是
A.甲能与溶液反应生成 B.反应①为加成反应
C.物质乙所含官能团的名称为酮羰基 D.反应②的原子利用率为100%
2.布洛芬是常见解热镇痛药,合成该药物的部分线路如图示:
下列说法不正确的是
A.可用新制的氢氧化铜浊液鉴别I和II
B.布洛芬的分子式为C13H18O2
C.mol布洛芬最多可与mol H2加成反应
D.布洛芬能发生取代、氧化等反应
3.化合物丙属于桥环化合物,是一种医药中间体,可以通过以下反应制得:
下列有关说法不正确的是
A.甲分子中所有原子不可能处于同一平面内
B.乙可与H2发生加成反应
C.丙能使酸性高锰酸钾溶液、溴的CCl4溶液褪色,且原理相同
D.等物质的量的甲、乙分别完全燃烧时,消耗氧气的质量之比为13∶12
4.联苯的结构简式为,下列有关说法正确的是
A.联苯分子中含有6个碳碳双键
B.联苯的一氯代物有5种
C.联苯可发生取代反应,但不能被酸性高锰酸钾溶液氧化
D.联苯和蒽()互为同系物
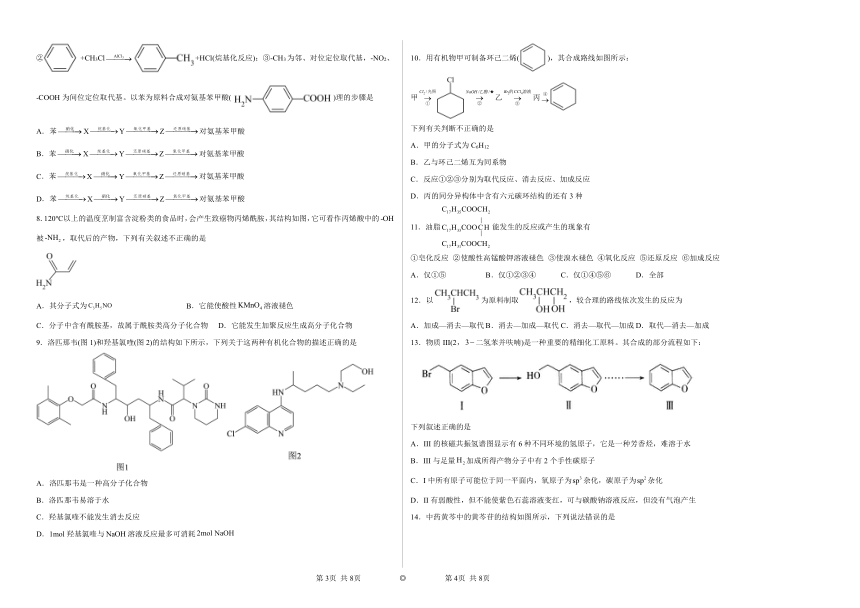
5.企鹅酮因结构类似企鹅而得名(如图)。下列有关企鹅酮的说法不正确的是
A.分子式为
B.1mol企鹅酮分子最多可以和2mol氢气加成
C.1mol企鹅酮分子最多可以和2mol加成
D.企鹅酮能使酸性高锰酸钾溶液褪色
6.某合成药物路线片段如下,D为合成该药物的重要中间体,其中表示,THF为四氢呋喃,作为反应的溶剂。
下列说法不正确的是
A.A→B的过程为取代反应,碳酸钠的主要作用是吸收生成的
B.由B→C的过程,说明在THF环境中可选择性还原酯基
C.一个D分子中存在两个手性碳原子
D.1B在溶液中发生水解,最多消耗4
7.已知:①+3Fe+6HCl→ +3FeCl2+2H2O,苯胺极易被氧化;②+CH3Cl+HCl(烷基化反应);③-CH3为邻、对位定位取代基,-NO2、-COOH为间位定位取代基。以苯为原料合成对氨基苯甲酸()理的步骤是
A.苯XYZ对氨基苯甲酸
B.苯XYZ对氨基苯甲酸
C.苯XYZ对氨基苯甲酸
D.苯XYZ对氨基苯甲酸
8.120℃以上的温度烹制富含淀粉类的食品时,会产生致癌物丙烯酰胺,其结构如图,它可看作丙烯酸中的被,取代后的产物,下列有关叙述不正确的是
A.其分子式为 B.它能使酸性溶液褪色
C.分子中含有酰胺基,故属于酰胺类高分子化合物 D.它能发生加聚反应生成高分子化合物
9.洛匹那韦(图1)和羟基氯喹(图2)的结构如下所示,下列关于这两种有机化合物的描述正确的是
A.洛匹那韦是一种高分子化合物
B.洛匹那韦易溶于水
C.羟基氯喹不能发生消去反应
D.1mol羟基氯喹与溶液反应最多可消耗
10.用有机物甲可制备环己二烯(),其合成路线如图所示:
甲乙丙
下列有关判断不正确的是
A.甲的分子式为C6H12
B.乙与环己二烯互为同系物
C.反应①②③分别为取代反应、消去反应、加成反应
D.丙的同分异构体中含有六元碳环结构的还有3种
11.油脂能发生的反应或产生的现象有
①皂化反应 ②使酸性高锰酸钾溶液褪色 ③使溴水褪色 ④氧化反应 ⑤还原反应 ⑥加成反应
A.仅①⑤ B.仅①②③④ C.仅①④⑤⑥ D.全部
12.以为原料制取,较合理的路线依次发生的反应为
A.加成—消去—取代 B.消去—加成—取代 C.消去—取代—加成 D.取代—消去—加成
13.物质III(2,二氢苯并呋喃)是一种重要的精细化工原料。其合成的部分流程如下:
下列叙述正确的是
A.III的核磁共振氢谱图显示有6种不同环境的氢原子,它是一种芳香烃,难溶于水
B.III与足量加成所得产物分子中有2个手性碳原子
C.I中所有原子可能位于同一平面内,氧原子为杂化,碳原子为杂化
D.II有弱酸性,但不能使紫色石蕊溶液变红,可与碳酸钠溶液反应,但没有气泡产生
14.中药黄芩中的黄芩苷的结构如图所示,下列说法错误的是
A.黄芩苷是芳香族化合物,其分子式为
B.黄芩苷可发生取代、加成、氧化反应
C.黄芩苷分子中苯环上的一氯代物(不考虑立体异构)有3种
D.1黄芩苷与足量钠反应,所得的体积在标准状况下为67.2L
15.国际奥委会在兴奋剂药检中检测出的两种兴奋剂的结构如下,关于它们的说法中正确的是
A.1Y与足量的反应,最多生成3
B.1X与足量的氢气反应,最多消耗4
C.Y能与足量的饱和溴水反应产生白色沉淀
D.Y不能发生加聚反应
二、实验题
16.如图所示,形管的左端是被水和胶塞封闭的甲烷和氯气(体积比为)的混合气体,假设氯气在水中的溶解度可以忽略。将封闭有甲烷和氯气混合气体的一端放置在有光的地方,让混合气体缓慢地反应一段时间。
(1)假设甲烷与氯气充分反应,且只产生一种有机物,请写出其化学方程式_______。
(2)若题目中甲烷与氯气体积之比为,则得到的产物为_______(填序号,下同)。
A.
B.
C.
D.
(3)经过几个小时的反应后,形管右端的水面变化是_______。
A.升高 B.降低 C.不变 D.无法确定
(4)若水中含有,则在形管左端会观察到的现象是_______。
(5)右端玻璃管的作用是_______。
17.醇与氢卤酸反应是制备卤代烃的重要方法。实验室制备溴乙烷和1-溴丁烷的反应如下:
NaBr+H2SO4=HBr+NaHSO4①
R—OH+HBrR—Br+H2O②
可能存在的副反应有:醇在浓硫酸的存在下脱水生成烯和醚,Br-被浓硫酸氧化为Br2等。有关数据见下表:
乙醇 溴乙烷 正丁醇 1-溴丁烷
密度/g.cm 3 0.7893 1.4604 0.8098 1.2758
沸点/℃ 78.5 38.4 117.2 101.6
请回答下列问题:
(1)溴乙烷和1 溴丁烷的制备实验中,下列仪器最不可能用到的是________(填字母)。
a.圆底烧瓶 b.量筒 c.锥形瓶 d.布氏漏斗
(2)溴代烃的水溶性________(填“大于”、“等于”或“小于”)相应的醇,其原因是______________________________________________________________。
(3)将1 溴丁烷粗产品置于分液漏斗中加水,振荡后静置,产物在________(填“上层”“下层”或“不分层”)。
(4)制备操作中,加入的浓硫酸必须进行稀释,其目的是________(填字母)。
a.减少副产物烯和醚的生成 b.减少Br2的生成
c.减少HBr的挥发 d.水是反应的催化剂
(5)欲除去溴乙烷中的少量杂质Br2,下列物质中最适合的是________(填字母)。
a.NaI b.NaOH c.NaHSO3 d.KCl
(6)在制备溴乙烷时,采用边反应边蒸出产物的方法,其有利于___________________,但在制备1 溴丁烷时却不能边反应边蒸出产物,其原因是___________________________。
三、有机推断题
18.化合物A最早发现于酸牛奶中,它是人体内糖代谢的中间体,可由马铃薯、玉米淀粉等发酵制得,A的钙盐是人们喜爱的补钙剂之一、A在某种催化剂的存在下进行氧化,其产物不能发生银镜反应。在浓硫酸存在下,A可发生如图所示的反应。完成下面各小题:
(1)化合物A、B、D的结构简式:_________、_________、_________。
(2)化学方程式:
A→E_________,_________反应;
A→F_________,_________反应。
(3)在一定条件下,若干个A分子在浓硫酸作用下,可以反应生成一种链状的高分子化合物(聚酯),写出三分子A相互反应生成链状物质的结构简式:_________,并根据得到的结构简式分析该高分子化合物最小的重复单元(链节)可表示为_________。
19.已知:①A是石油裂解气的主要成分,A的产量通常用来衡量一个国家的石油化工水平;②2CH3CHO+O22CH3COOH。现以A为主要原料合成乙酸乙酯,其合成路线如图所示。
回答下列问题:
(1)写出A的结构式_______。
(2)B、D分子中的官能团名称分别是_______、_______。
(3)写出下列反应的反应类型:①_______,②_______,④_______。
(4)写出下列反应的化学方程式:
①_______;
②_______;
④_______。
第1页 共4页 ◎ 第2页 共4页
第1页 共4页 ◎ 第2页 共4页
参考答案:
1.B
【详解】A.甲中含有酚羟基和酮羰基,二者都不能与溶液反应生成,故A错误;
B.由甲、乙和丙的结构简式可以推知反应①为加成反应,故B正确;
C.物质乙所含官能团的名称为醛基,故C错误;
D.由丙和丁的结构简式可以推知丙发生消去反应生成丁,同时还有H2O生成,反应②的原子利用率不是100%,故D错误;
故选B。
2.C
【详解】A.II中含有醛基,I中没有醛基,因此可用新制的氢氧化铜浊液鉴别I和II,故A正确;
B.根据布洛芬的结构简式得到分子式为C13H18O2,故B正确;
C.布洛芬含有苯环,能与氢气发生加成反应,羧基不能与氢气发生加成反应,因此mol布洛芬最多可与3mol H2加成反应,故C错误;
D.布洛芬含有羧基,能发生置换反应,又叫取代反应,布洛芬能被酸性高锰酸钾溶液氧化,故D正确。
综上所述,答案为C。
3.C
【详解】A.甲分子中含有饱和碳原子,饱和碳原子与其相连原子构成四面体结构,所有原子不可能都在同一平面内,A正确;
B.乙分子中含有碳碳双键,可与H2发生加成反应,B正确;
C.丙分子中含有碳碳双键,可以被酸性高锰酸钾溶液氧化而使溶液褪色,也可以与溴的CCl4溶液中的Br2发生加成反应而使溶液褪色,褪色原理不同,C不正确;
D.甲的分子式是C5H6,1mol甲完全燃烧消耗O2的物质的量为6.5mol,乙的分子式为C5H8O2,1mol乙完全燃烧消耗O2的物质的量为6mol,所以等物质的量的甲、乙分别完全燃烧时,消耗氧气的质量之比为13∶12,D正确;
故选C。
4.C
【详解】A.苯分子不是单双键交替的结构,所以联苯分子中不含有碳碳双键,A错误;
B.联苯中不同化学环境的氢原子有3种,则一氯代物有3种,B错误;
C.联苯由两个苯环相连而成,与苯的性质相似,可发生取代反应,但不能被酸性高锰酸钾溶液氧化,C正确;
D.联苯和蒽()的结构不相似,组成上也不是相差若干个CH2,二者不互为同系物,D错误。
故选C。
5.B
【详解】A.由企鹅酮的结构可知其分子式为,故A项正确;
B.企鹅酮分子中碳碳双键、羰基都能与氢气发生加成反应,因此1mol企鹅酮分子最多能与3mol氢气发生加成反应,故B项错误;
C.企鹅酮分子中碳碳双键能与溴单质发生加成反应,因此1mol企鹅酮分子最多可以和2mol加成,故C项正确;
D.企鹅酮分子中碳碳双键能被酸性高锰酸钾溶液氧化,从而使酸性高锰酸钾溶液褪色,故D项正确;
故选B。
6.C
【详解】A.由A和B的结构可知A→B的反应属于取代反应,根据元素守恒分析,该反应除生成B外,还生成,碳酸钠的作用是吸收生成的,A正确;
B.分析B、C的结构可知,没有发生变化,酯基变成了醇羟基,说明在THF环境中可选择性还原酯基,B正确;
C.D分子中只有与亚氨基和苯环同时相连的碳原子是手性碳原子,C错误;
D.1B在溶液中发生水解,和各消耗1,2mol氟原子共消耗2,因此1B在溶液中发生水解,最多消耗4,D正确。
故选C。
7.C
【详解】若苯先发生硝化反应,由于硝基是间位定位取代基,再引入甲基时会进入硝基的间位,故应先发生烷基化反应,得到的甲苯发生硝化反应,生成对硝基甲苯;对硝基甲苯先发生氧化反应,将甲基氧化为羧基,若先将硝基还原为氨基,则氧化甲基时氨基容易被氧化。最后再将硝基还原为氨基。所以合理步骤为:苯甲苯对硝基甲苯对硝基苯甲酸对氨基苯甲酸,故选C。
8.C
【详解】A.根据有机物的结构,推出该物质的分子式为,选项A正确;
B.该有机物分子中含有碳碳双键,可使酸性溶液褪色,选项B正确;
C.该有机物不属于高分子化合物,选项C错误;
D.该有机物含有碳碳双键,可以发生加聚反应生成高分子化合物,选项D正确;
答案选C。
9.D
【详解】A.高分子化合物的相对分子质量通常在1万以上,洛匹那韦不是高分子化合物,选项A错误;
B.洛匹那韦的憎水基团比重远大于亲水基团,故其易溶于有机溶剂,难溶于水,选项B错误;
C.羟基氯喹分子中含有羟基,且和羟基相连的碳原子的邻位碳原子上有氢原子,所以能发生消去反应,选项C错误;
D.羟基氯喹分子中含有与苯环相连的氯原子,水解产生的酚羟基和均能与反应,所以羟基氯喹最多可与反应,选项D正确;
答案选D。
10.B
【详解】由流程图可知,甲与Cl2在光照条件下发生取代反应生成,则甲为 ; 与氢氧化钠的醇溶液共热发生消去反应生成乙,则乙为 ;乙与Br2的CCl4溶液发生加成反应生成丙,则丙为 ;丙发生消去反应生成。
A.甲为 ,其分子式为C6H12,选项A正确;
B.乙为 ,与环己二烯的结构不相似,二者不互为同系物,选项B不正确;
C.反应①为取代反应,反应②为消去反应,反应③为加成反应,选项C正确;
D.丙的同分异构体中含有六元碳环结构的有,共3种,选项D正确;
答案选B。
11.D
【详解】根据该物质结构,可知其分子中含有碳碳不饱和键,所以可以使酸性高锰酸钾溶液褪色,即发生氧化反应;可使溴水褪色,即发生加成反应;可与氢气发生加成反应,即还原反应;油脂可发生皂化反应;该物质可以和氧气燃烧发生氧化反应。
故选D。
12.B
【详解】由逆合成法可知,二卤代烃水解可制备二元醇,烯烃加成可制备二卤代烃,则以2-溴丙烷为原料制取1,2-丙二醇,步骤为:①2-溴丙烷与NaOH醇溶液共热发生消去反应生成丙烯;②丙烯与溴单质发生加成反应生成1,2-二溴丙烷;③1,2-二溴丙烷与NaOH水溶液共热发生取代反应生成1,2-丙二醇,故选B。
13.B
【详解】A.III的结构不对称,III的核磁共振氢谱显示有6种不同化学环境的氢原子,该分子中含有C、H、O三种元素且含有苯环,该分子不属于芳香烃,属于芳香族化合物,没有亲水基,只有憎水基,故不易溶于水,A错误;
B.III与足量的H2加成后产物的结构简式为:,两个环连接的碳原子为手性碳原子,共2个手性碳原子,B正确;
C.I中亚甲基具有甲烷结构特点,故所有原子不可能位于同一平面内,亚甲基上的碳原子、氧原子的价层电子对数均为4,则杂化方式均为sp3杂化,苯环上的碳原子杂化方式为sp2杂化,C错误;
D.II中含醇羟基,不含羧基和酚羟基,该物质无酸性,不能使紫色石蕊试液变红,不能与碳酸钠溶液反应,D错误;
故选B。
14.C
【详解】A.黄芩苷分子中含有苯环,是芳香族化合物,根据结构可知其分子式为,故A正确;
B.黄芩苷中含有羧基可以发生取代反应,含有碳碳双键,能发生加成反应和氧化反应,故B正确;
C.黄芩苷分子中苯环上的一氯代物有4种,如图: ,故C错误;
D.1黄芩苷分子中含有2酚羟基,3醇羟基,1羧基,因此与足量钠反应,得到3,所得的体积在标准状况下为67.2L,故D正确;
故选C。
15.C
【详解】A.1Y与足量的反应,可消耗3,生成氢气的物质的量最多为1.5,故A错误;
B.1X与足量的氢气反应,苯环和碳碳双键都能和氢气反应,最多消耗5,故B错误;
C.Y中含有酚羟基且酚羟基邻、对位上有H,可与饱和溴水发生取代反应生成白色沉淀,故C正确;
D.Y中含有碳碳双键,可发生加聚反应,故D错误。
故选C。
16. D B 有白色胶状沉淀生成 平衡气压
【分析】本题考查了甲烷的取代反应,以及反应产物HCl酸性的检验。要熟悉其方程式。
【详解】(1)因足量,若充分反应且只产生一种有机物,则中的四个H原子可完全被取代,生成和。
(2)甲烷与氯气的取代反应,会同时发生四步反应,得到四种氯代产物和。
(3)甲烷和氯气在光照条件下发生取代反应生成的一氯甲烷为气体,难溶于水,其他三种有机产物均为油状液滴,生成的氯化氢气体易溶于水,故生成气体的物质的量减少,压强减小,U形管右端液面下降,左端液面上升。
(4)因U形管左侧生成的溶于水后发生反应:,所以会观察到有白色胶状沉淀生成。
(5)在U形管右侧插入一支玻璃管的目的是连通大气,平衡气压。
17.(1)d (2)小于 醇分子可与水分子形成氢键,溴代烃分子不能与水分子形成氢键
(3)下层 (4)abc (5)c
(6)平衡向生成溴乙烷的方向移动(或反应②向右移动),产物1 溴丁烷的沸点与反应物正丁醇的沸点相差很小,在蒸出产物时反应物也一块被蒸出
【详解】试题分析:(1)布氏漏斗主要用于抽滤操作(即有晶体析出时),但溴乙烷和1 溴丁烷均不是晶体,则无需使用。
(2)醇比卤代烃更易溶于水,是由于醇中含有氧原子可以与水形成氢键,以增加其在水中的溶解性。
(3)1 溴丁烷的密度大于水,应沉于水底。
(4)根据题目所提供的信息知,浓硫酸可使醇脱水生成烯和醚;可以将Br-氧化成单质Br2;浓硫酸与水溶液接触会放热,而导致HBr的挥发,以上三点促使硫酸应稀释。
(5)除溴,则必须与溴反应,可排除d;a可以反应,但生成新杂质I2;b可以将溴反应掉,但也可使溴乙烷水解;只有c正确,HSO可以将Br2还原进入水溶液,然后再分液处理即可。(6)制溴乙烷时,利用反应②,蒸出反应物,可促使平衡正向移动;但制1 溴丁烷时,由于它与正丁醇的沸点相差很小,在蒸出产物时也蒸出反应物,不妥。
考点:考查卤代烃制备的实验设计、仪器的选择、条件控制以及基本实验操作
点评:该题是高考中的常见题型,属于中等难度的试题。试题综合性强,难易适中,侧重对学生基础知识的巩固与训练,旨在考查学生灵活运用基础知识解决实际问题的能力,同时也注重对学生答题能力的培养和方法指导,有利于培养学生的逻辑思维能力和发散思维能力以及严谨规范的实验设计能力和知识的迁移能力。该类试题是一类综合性较强的试题,它不仅可考查学生对化学知识的理解程度,更重要的是培养学生的综合分析能力和思维方法,提升学生的学科素养。
18.(1)
(2) H2C=CHCOOH+H2O 消去反应 取代反应(或酯化反应)
(3)
【分析】A在浓硫酸存在下既能和乙醇反应,又能和乙酸反应,说明A中既有羧基又有羟基,A催化氧化的产物不能产生银镜反应,说明羟基不在碳链的端点,根据A的化学式,可推知A的结构简式为,根据反应条件可知B为、D为,E能使溴水褪色,说明其分子结构中含碳碳双键,A发生消去反应,E为H2C=CHCOOH、;F为六元环状化合物,结合F的分子式可知,F是由2分子A发生酯化反应生成的,F为。A分子中既有羧基又有羟基,可以发生酯化反应生成链状的高分子化合物,其链节为最小的重复单元,据此分析解题。
【详解】(1)由分析可知,化合物A的结构简式为:,B的结构简式为:,D的结构简式为:,故答案为:;;;
(2)由分析可知,A的的结构简式为:,E的结构简式为H2C=CHCOOH,故A到E的反应方程式为:H2C=CHCOOH+H2O,反应类型属于消去反应,F的结构简式为:,故A到F的反应方程式为:,反应类型为取代反应或酯化反应,故答案为:H2C=CHCOOH+H2O;消去反应;;取代反应或酯化反应;
(3)A分子中既有羧基又有羟基,可以发生酯化反应生成链状的高分子化合物,其链节为最小的重复单元,在一定条件下,若干个A分子在浓硫酸作用下,可以反应生成一种链状的高分子化合物(聚酯),则三分子A相互反应生成链状物质的结构简式:,并根据得到的结构简式分析该高分子化合物最小的重复单元(链节)可表示为:故答案为:;。
19.(1)
(2) 羟基 羧基
(3) 加成反应 氧化反应 酯化反应(或取代反应)
(4) CH2CH2+H2OCH3CH2OH 2CH3CH2OH+O22CH3CHO+2H2O CH3COOH+CH3CH2OHCH3COOCH2CH3+H2O
【分析】A的产量通常用来衡量一个国家的石油化工水平,则A为CH2=CH2,乙烯与水发生加成反应生成乙醇,B为CH3CH2OH,B发生催化氧化生成乙醛,C为CH3CHO,C进一步发生氧化反应生成乙酸,D为CH3COOH,乙醇与乙酸发生酯化反应得到乙酸乙酯;
【详解】(1)由分析可知,A为乙烯,结构为;
(2)B为乙醇,含有官能团为羟基,D为乙酸,含有官能团为羧基;
(3)反应①是乙烯与水发生加成反应生成乙醇,反应②是乙醇发生氧化反应生成乙醛,反应④为乙酸和乙醇发生酯化反应生成乙酸乙酯;
(4)反应①乙烯与水发生加成反应生成乙醇,化学反应方程式为:CH2=CH2+H2OCH3CH2OH;
反应②乙醇发生氧化反应生成乙醛,化学反应方程式为:2CH3CH2OH+O22CH3CHO+2H2O;
反应④是乙醇和乙酸制备乙酸乙酯的反应,反应方程式为:CH3COOH+C2H5OHCH3COOC2H5+H2O。
答案第1页,共2页
答案第1页,共2页
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1.黄酮类化合物具有广泛的药理作用,如抗氧化、降血压、抗肿瘤等,2-羟基查尔酮是黄酮类化合物的一种重要中间体,它的一种合成路线如图所示。下列说法正确的是
A.甲能与溶液反应生成 B.反应①为加成反应
C.物质乙所含官能团的名称为酮羰基 D.反应②的原子利用率为100%
2.布洛芬是常见解热镇痛药,合成该药物的部分线路如图示:
下列说法不正确的是
A.可用新制的氢氧化铜浊液鉴别I和II
B.布洛芬的分子式为C13H18O2
C.mol布洛芬最多可与mol H2加成反应
D.布洛芬能发生取代、氧化等反应
3.化合物丙属于桥环化合物,是一种医药中间体,可以通过以下反应制得:
下列有关说法不正确的是
A.甲分子中所有原子不可能处于同一平面内
B.乙可与H2发生加成反应
C.丙能使酸性高锰酸钾溶液、溴的CCl4溶液褪色,且原理相同
D.等物质的量的甲、乙分别完全燃烧时,消耗氧气的质量之比为13∶12
4.联苯的结构简式为,下列有关说法正确的是
A.联苯分子中含有6个碳碳双键
B.联苯的一氯代物有5种
C.联苯可发生取代反应,但不能被酸性高锰酸钾溶液氧化
D.联苯和蒽()互为同系物
5.企鹅酮因结构类似企鹅而得名(如图)。下列有关企鹅酮的说法不正确的是
A.分子式为
B.1mol企鹅酮分子最多可以和2mol氢气加成
C.1mol企鹅酮分子最多可以和2mol加成
D.企鹅酮能使酸性高锰酸钾溶液褪色
6.某合成药物路线片段如下,D为合成该药物的重要中间体,其中表示,THF为四氢呋喃,作为反应的溶剂。
下列说法不正确的是
A.A→B的过程为取代反应,碳酸钠的主要作用是吸收生成的
B.由B→C的过程,说明在THF环境中可选择性还原酯基
C.一个D分子中存在两个手性碳原子
D.1B在溶液中发生水解,最多消耗4
7.已知:①+3Fe+6HCl→ +3FeCl2+2H2O,苯胺极易被氧化;②+CH3Cl+HCl(烷基化反应);③-CH3为邻、对位定位取代基,-NO2、-COOH为间位定位取代基。以苯为原料合成对氨基苯甲酸()理的步骤是
A.苯XYZ对氨基苯甲酸
B.苯XYZ对氨基苯甲酸
C.苯XYZ对氨基苯甲酸
D.苯XYZ对氨基苯甲酸
8.120℃以上的温度烹制富含淀粉类的食品时,会产生致癌物丙烯酰胺,其结构如图,它可看作丙烯酸中的被,取代后的产物,下列有关叙述不正确的是
A.其分子式为 B.它能使酸性溶液褪色
C.分子中含有酰胺基,故属于酰胺类高分子化合物 D.它能发生加聚反应生成高分子化合物
9.洛匹那韦(图1)和羟基氯喹(图2)的结构如下所示,下列关于这两种有机化合物的描述正确的是
A.洛匹那韦是一种高分子化合物
B.洛匹那韦易溶于水
C.羟基氯喹不能发生消去反应
D.1mol羟基氯喹与溶液反应最多可消耗
10.用有机物甲可制备环己二烯(),其合成路线如图所示:
甲乙丙
下列有关判断不正确的是
A.甲的分子式为C6H12
B.乙与环己二烯互为同系物
C.反应①②③分别为取代反应、消去反应、加成反应
D.丙的同分异构体中含有六元碳环结构的还有3种
11.油脂能发生的反应或产生的现象有
①皂化反应 ②使酸性高锰酸钾溶液褪色 ③使溴水褪色 ④氧化反应 ⑤还原反应 ⑥加成反应
A.仅①⑤ B.仅①②③④ C.仅①④⑤⑥ D.全部
12.以为原料制取,较合理的路线依次发生的反应为
A.加成—消去—取代 B.消去—加成—取代 C.消去—取代—加成 D.取代—消去—加成
13.物质III(2,二氢苯并呋喃)是一种重要的精细化工原料。其合成的部分流程如下:
下列叙述正确的是
A.III的核磁共振氢谱图显示有6种不同环境的氢原子,它是一种芳香烃,难溶于水
B.III与足量加成所得产物分子中有2个手性碳原子
C.I中所有原子可能位于同一平面内,氧原子为杂化,碳原子为杂化
D.II有弱酸性,但不能使紫色石蕊溶液变红,可与碳酸钠溶液反应,但没有气泡产生
14.中药黄芩中的黄芩苷的结构如图所示,下列说法错误的是
A.黄芩苷是芳香族化合物,其分子式为
B.黄芩苷可发生取代、加成、氧化反应
C.黄芩苷分子中苯环上的一氯代物(不考虑立体异构)有3种
D.1黄芩苷与足量钠反应,所得的体积在标准状况下为67.2L
15.国际奥委会在兴奋剂药检中检测出的两种兴奋剂的结构如下,关于它们的说法中正确的是
A.1Y与足量的反应,最多生成3
B.1X与足量的氢气反应,最多消耗4
C.Y能与足量的饱和溴水反应产生白色沉淀
D.Y不能发生加聚反应
二、实验题
16.如图所示,形管的左端是被水和胶塞封闭的甲烷和氯气(体积比为)的混合气体,假设氯气在水中的溶解度可以忽略。将封闭有甲烷和氯气混合气体的一端放置在有光的地方,让混合气体缓慢地反应一段时间。
(1)假设甲烷与氯气充分反应,且只产生一种有机物,请写出其化学方程式_______。
(2)若题目中甲烷与氯气体积之比为,则得到的产物为_______(填序号,下同)。
A.
B.
C.
D.
(3)经过几个小时的反应后,形管右端的水面变化是_______。
A.升高 B.降低 C.不变 D.无法确定
(4)若水中含有,则在形管左端会观察到的现象是_______。
(5)右端玻璃管的作用是_______。
17.醇与氢卤酸反应是制备卤代烃的重要方法。实验室制备溴乙烷和1-溴丁烷的反应如下:
NaBr+H2SO4=HBr+NaHSO4①
R—OH+HBrR—Br+H2O②
可能存在的副反应有:醇在浓硫酸的存在下脱水生成烯和醚,Br-被浓硫酸氧化为Br2等。有关数据见下表:
乙醇 溴乙烷 正丁醇 1-溴丁烷
密度/g.cm 3 0.7893 1.4604 0.8098 1.2758
沸点/℃ 78.5 38.4 117.2 101.6
请回答下列问题:
(1)溴乙烷和1 溴丁烷的制备实验中,下列仪器最不可能用到的是________(填字母)。
a.圆底烧瓶 b.量筒 c.锥形瓶 d.布氏漏斗
(2)溴代烃的水溶性________(填“大于”、“等于”或“小于”)相应的醇,其原因是______________________________________________________________。
(3)将1 溴丁烷粗产品置于分液漏斗中加水,振荡后静置,产物在________(填“上层”“下层”或“不分层”)。
(4)制备操作中,加入的浓硫酸必须进行稀释,其目的是________(填字母)。
a.减少副产物烯和醚的生成 b.减少Br2的生成
c.减少HBr的挥发 d.水是反应的催化剂
(5)欲除去溴乙烷中的少量杂质Br2,下列物质中最适合的是________(填字母)。
a.NaI b.NaOH c.NaHSO3 d.KCl
(6)在制备溴乙烷时,采用边反应边蒸出产物的方法,其有利于___________________,但在制备1 溴丁烷时却不能边反应边蒸出产物,其原因是___________________________。
三、有机推断题
18.化合物A最早发现于酸牛奶中,它是人体内糖代谢的中间体,可由马铃薯、玉米淀粉等发酵制得,A的钙盐是人们喜爱的补钙剂之一、A在某种催化剂的存在下进行氧化,其产物不能发生银镜反应。在浓硫酸存在下,A可发生如图所示的反应。完成下面各小题:
(1)化合物A、B、D的结构简式:_________、_________、_________。
(2)化学方程式:
A→E_________,_________反应;
A→F_________,_________反应。
(3)在一定条件下,若干个A分子在浓硫酸作用下,可以反应生成一种链状的高分子化合物(聚酯),写出三分子A相互反应生成链状物质的结构简式:_________,并根据得到的结构简式分析该高分子化合物最小的重复单元(链节)可表示为_________。
19.已知:①A是石油裂解气的主要成分,A的产量通常用来衡量一个国家的石油化工水平;②2CH3CHO+O22CH3COOH。现以A为主要原料合成乙酸乙酯,其合成路线如图所示。
回答下列问题:
(1)写出A的结构式_______。
(2)B、D分子中的官能团名称分别是_______、_______。
(3)写出下列反应的反应类型:①_______,②_______,④_______。
(4)写出下列反应的化学方程式:
①_______;
②_______;
④_______。
第1页 共4页 ◎ 第2页 共4页
第1页 共4页 ◎ 第2页 共4页
参考答案:
1.B
【详解】A.甲中含有酚羟基和酮羰基,二者都不能与溶液反应生成,故A错误;
B.由甲、乙和丙的结构简式可以推知反应①为加成反应,故B正确;
C.物质乙所含官能团的名称为醛基,故C错误;
D.由丙和丁的结构简式可以推知丙发生消去反应生成丁,同时还有H2O生成,反应②的原子利用率不是100%,故D错误;
故选B。
2.C
【详解】A.II中含有醛基,I中没有醛基,因此可用新制的氢氧化铜浊液鉴别I和II,故A正确;
B.根据布洛芬的结构简式得到分子式为C13H18O2,故B正确;
C.布洛芬含有苯环,能与氢气发生加成反应,羧基不能与氢气发生加成反应,因此mol布洛芬最多可与3mol H2加成反应,故C错误;
D.布洛芬含有羧基,能发生置换反应,又叫取代反应,布洛芬能被酸性高锰酸钾溶液氧化,故D正确。
综上所述,答案为C。
3.C
【详解】A.甲分子中含有饱和碳原子,饱和碳原子与其相连原子构成四面体结构,所有原子不可能都在同一平面内,A正确;
B.乙分子中含有碳碳双键,可与H2发生加成反应,B正确;
C.丙分子中含有碳碳双键,可以被酸性高锰酸钾溶液氧化而使溶液褪色,也可以与溴的CCl4溶液中的Br2发生加成反应而使溶液褪色,褪色原理不同,C不正确;
D.甲的分子式是C5H6,1mol甲完全燃烧消耗O2的物质的量为6.5mol,乙的分子式为C5H8O2,1mol乙完全燃烧消耗O2的物质的量为6mol,所以等物质的量的甲、乙分别完全燃烧时,消耗氧气的质量之比为13∶12,D正确;
故选C。
4.C
【详解】A.苯分子不是单双键交替的结构,所以联苯分子中不含有碳碳双键,A错误;
B.联苯中不同化学环境的氢原子有3种,则一氯代物有3种,B错误;
C.联苯由两个苯环相连而成,与苯的性质相似,可发生取代反应,但不能被酸性高锰酸钾溶液氧化,C正确;
D.联苯和蒽()的结构不相似,组成上也不是相差若干个CH2,二者不互为同系物,D错误。
故选C。
5.B
【详解】A.由企鹅酮的结构可知其分子式为,故A项正确;
B.企鹅酮分子中碳碳双键、羰基都能与氢气发生加成反应,因此1mol企鹅酮分子最多能与3mol氢气发生加成反应,故B项错误;
C.企鹅酮分子中碳碳双键能与溴单质发生加成反应,因此1mol企鹅酮分子最多可以和2mol加成,故C项正确;
D.企鹅酮分子中碳碳双键能被酸性高锰酸钾溶液氧化,从而使酸性高锰酸钾溶液褪色,故D项正确;
故选B。
6.C
【详解】A.由A和B的结构可知A→B的反应属于取代反应,根据元素守恒分析,该反应除生成B外,还生成,碳酸钠的作用是吸收生成的,A正确;
B.分析B、C的结构可知,没有发生变化,酯基变成了醇羟基,说明在THF环境中可选择性还原酯基,B正确;
C.D分子中只有与亚氨基和苯环同时相连的碳原子是手性碳原子,C错误;
D.1B在溶液中发生水解,和各消耗1,2mol氟原子共消耗2,因此1B在溶液中发生水解,最多消耗4,D正确。
故选C。
7.C
【详解】若苯先发生硝化反应,由于硝基是间位定位取代基,再引入甲基时会进入硝基的间位,故应先发生烷基化反应,得到的甲苯发生硝化反应,生成对硝基甲苯;对硝基甲苯先发生氧化反应,将甲基氧化为羧基,若先将硝基还原为氨基,则氧化甲基时氨基容易被氧化。最后再将硝基还原为氨基。所以合理步骤为:苯甲苯对硝基甲苯对硝基苯甲酸对氨基苯甲酸,故选C。
8.C
【详解】A.根据有机物的结构,推出该物质的分子式为,选项A正确;
B.该有机物分子中含有碳碳双键,可使酸性溶液褪色,选项B正确;
C.该有机物不属于高分子化合物,选项C错误;
D.该有机物含有碳碳双键,可以发生加聚反应生成高分子化合物,选项D正确;
答案选C。
9.D
【详解】A.高分子化合物的相对分子质量通常在1万以上,洛匹那韦不是高分子化合物,选项A错误;
B.洛匹那韦的憎水基团比重远大于亲水基团,故其易溶于有机溶剂,难溶于水,选项B错误;
C.羟基氯喹分子中含有羟基,且和羟基相连的碳原子的邻位碳原子上有氢原子,所以能发生消去反应,选项C错误;
D.羟基氯喹分子中含有与苯环相连的氯原子,水解产生的酚羟基和均能与反应,所以羟基氯喹最多可与反应,选项D正确;
答案选D。
10.B
【详解】由流程图可知,甲与Cl2在光照条件下发生取代反应生成,则甲为 ; 与氢氧化钠的醇溶液共热发生消去反应生成乙,则乙为 ;乙与Br2的CCl4溶液发生加成反应生成丙,则丙为 ;丙发生消去反应生成。
A.甲为 ,其分子式为C6H12,选项A正确;
B.乙为 ,与环己二烯的结构不相似,二者不互为同系物,选项B不正确;
C.反应①为取代反应,反应②为消去反应,反应③为加成反应,选项C正确;
D.丙的同分异构体中含有六元碳环结构的有,共3种,选项D正确;
答案选B。
11.D
【详解】根据该物质结构,可知其分子中含有碳碳不饱和键,所以可以使酸性高锰酸钾溶液褪色,即发生氧化反应;可使溴水褪色,即发生加成反应;可与氢气发生加成反应,即还原反应;油脂可发生皂化反应;该物质可以和氧气燃烧发生氧化反应。
故选D。
12.B
【详解】由逆合成法可知,二卤代烃水解可制备二元醇,烯烃加成可制备二卤代烃,则以2-溴丙烷为原料制取1,2-丙二醇,步骤为:①2-溴丙烷与NaOH醇溶液共热发生消去反应生成丙烯;②丙烯与溴单质发生加成反应生成1,2-二溴丙烷;③1,2-二溴丙烷与NaOH水溶液共热发生取代反应生成1,2-丙二醇,故选B。
13.B
【详解】A.III的结构不对称,III的核磁共振氢谱显示有6种不同化学环境的氢原子,该分子中含有C、H、O三种元素且含有苯环,该分子不属于芳香烃,属于芳香族化合物,没有亲水基,只有憎水基,故不易溶于水,A错误;
B.III与足量的H2加成后产物的结构简式为:,两个环连接的碳原子为手性碳原子,共2个手性碳原子,B正确;
C.I中亚甲基具有甲烷结构特点,故所有原子不可能位于同一平面内,亚甲基上的碳原子、氧原子的价层电子对数均为4,则杂化方式均为sp3杂化,苯环上的碳原子杂化方式为sp2杂化,C错误;
D.II中含醇羟基,不含羧基和酚羟基,该物质无酸性,不能使紫色石蕊试液变红,不能与碳酸钠溶液反应,D错误;
故选B。
14.C
【详解】A.黄芩苷分子中含有苯环,是芳香族化合物,根据结构可知其分子式为,故A正确;
B.黄芩苷中含有羧基可以发生取代反应,含有碳碳双键,能发生加成反应和氧化反应,故B正确;
C.黄芩苷分子中苯环上的一氯代物有4种,如图: ,故C错误;
D.1黄芩苷分子中含有2酚羟基,3醇羟基,1羧基,因此与足量钠反应,得到3,所得的体积在标准状况下为67.2L,故D正确;
故选C。
15.C
【详解】A.1Y与足量的反应,可消耗3,生成氢气的物质的量最多为1.5,故A错误;
B.1X与足量的氢气反应,苯环和碳碳双键都能和氢气反应,最多消耗5,故B错误;
C.Y中含有酚羟基且酚羟基邻、对位上有H,可与饱和溴水发生取代反应生成白色沉淀,故C正确;
D.Y中含有碳碳双键,可发生加聚反应,故D错误。
故选C。
16. D B 有白色胶状沉淀生成 平衡气压
【分析】本题考查了甲烷的取代反应,以及反应产物HCl酸性的检验。要熟悉其方程式。
【详解】(1)因足量,若充分反应且只产生一种有机物,则中的四个H原子可完全被取代,生成和。
(2)甲烷与氯气的取代反应,会同时发生四步反应,得到四种氯代产物和。
(3)甲烷和氯气在光照条件下发生取代反应生成的一氯甲烷为气体,难溶于水,其他三种有机产物均为油状液滴,生成的氯化氢气体易溶于水,故生成气体的物质的量减少,压强减小,U形管右端液面下降,左端液面上升。
(4)因U形管左侧生成的溶于水后发生反应:,所以会观察到有白色胶状沉淀生成。
(5)在U形管右侧插入一支玻璃管的目的是连通大气,平衡气压。
17.(1)d (2)小于 醇分子可与水分子形成氢键,溴代烃分子不能与水分子形成氢键
(3)下层 (4)abc (5)c
(6)平衡向生成溴乙烷的方向移动(或反应②向右移动),产物1 溴丁烷的沸点与反应物正丁醇的沸点相差很小,在蒸出产物时反应物也一块被蒸出
【详解】试题分析:(1)布氏漏斗主要用于抽滤操作(即有晶体析出时),但溴乙烷和1 溴丁烷均不是晶体,则无需使用。
(2)醇比卤代烃更易溶于水,是由于醇中含有氧原子可以与水形成氢键,以增加其在水中的溶解性。
(3)1 溴丁烷的密度大于水,应沉于水底。
(4)根据题目所提供的信息知,浓硫酸可使醇脱水生成烯和醚;可以将Br-氧化成单质Br2;浓硫酸与水溶液接触会放热,而导致HBr的挥发,以上三点促使硫酸应稀释。
(5)除溴,则必须与溴反应,可排除d;a可以反应,但生成新杂质I2;b可以将溴反应掉,但也可使溴乙烷水解;只有c正确,HSO可以将Br2还原进入水溶液,然后再分液处理即可。(6)制溴乙烷时,利用反应②,蒸出反应物,可促使平衡正向移动;但制1 溴丁烷时,由于它与正丁醇的沸点相差很小,在蒸出产物时也蒸出反应物,不妥。
考点:考查卤代烃制备的实验设计、仪器的选择、条件控制以及基本实验操作
点评:该题是高考中的常见题型,属于中等难度的试题。试题综合性强,难易适中,侧重对学生基础知识的巩固与训练,旨在考查学生灵活运用基础知识解决实际问题的能力,同时也注重对学生答题能力的培养和方法指导,有利于培养学生的逻辑思维能力和发散思维能力以及严谨规范的实验设计能力和知识的迁移能力。该类试题是一类综合性较强的试题,它不仅可考查学生对化学知识的理解程度,更重要的是培养学生的综合分析能力和思维方法,提升学生的学科素养。
18.(1)
(2) H2C=CHCOOH+H2O 消去反应 取代反应(或酯化反应)
(3)
【分析】A在浓硫酸存在下既能和乙醇反应,又能和乙酸反应,说明A中既有羧基又有羟基,A催化氧化的产物不能产生银镜反应,说明羟基不在碳链的端点,根据A的化学式,可推知A的结构简式为,根据反应条件可知B为、D为,E能使溴水褪色,说明其分子结构中含碳碳双键,A发生消去反应,E为H2C=CHCOOH、;F为六元环状化合物,结合F的分子式可知,F是由2分子A发生酯化反应生成的,F为。A分子中既有羧基又有羟基,可以发生酯化反应生成链状的高分子化合物,其链节为最小的重复单元,据此分析解题。
【详解】(1)由分析可知,化合物A的结构简式为:,B的结构简式为:,D的结构简式为:,故答案为:;;;
(2)由分析可知,A的的结构简式为:,E的结构简式为H2C=CHCOOH,故A到E的反应方程式为:H2C=CHCOOH+H2O,反应类型属于消去反应,F的结构简式为:,故A到F的反应方程式为:,反应类型为取代反应或酯化反应,故答案为:H2C=CHCOOH+H2O;消去反应;;取代反应或酯化反应;
(3)A分子中既有羧基又有羟基,可以发生酯化反应生成链状的高分子化合物,其链节为最小的重复单元,在一定条件下,若干个A分子在浓硫酸作用下,可以反应生成一种链状的高分子化合物(聚酯),则三分子A相互反应生成链状物质的结构简式:,并根据得到的结构简式分析该高分子化合物最小的重复单元(链节)可表示为:故答案为:;。
19.(1)
(2) 羟基 羧基
(3) 加成反应 氧化反应 酯化反应(或取代反应)
(4) CH2CH2+H2OCH3CH2OH 2CH3CH2OH+O22CH3CHO+2H2O CH3COOH+CH3CH2OHCH3COOCH2CH3+H2O
【分析】A的产量通常用来衡量一个国家的石油化工水平,则A为CH2=CH2,乙烯与水发生加成反应生成乙醇,B为CH3CH2OH,B发生催化氧化生成乙醛,C为CH3CHO,C进一步发生氧化反应生成乙酸,D为CH3COOH,乙醇与乙酸发生酯化反应得到乙酸乙酯;
【详解】(1)由分析可知,A为乙烯,结构为;
(2)B为乙醇,含有官能团为羟基,D为乙酸,含有官能团为羧基;
(3)反应①是乙烯与水发生加成反应生成乙醇,反应②是乙醇发生氧化反应生成乙醛,反应④为乙酸和乙醇发生酯化反应生成乙酸乙酯;
(4)反应①乙烯与水发生加成反应生成乙醇,化学反应方程式为:CH2=CH2+H2OCH3CH2OH;
反应②乙醇发生氧化反应生成乙醛,化学反应方程式为:2CH3CH2OH+O22CH3CHO+2H2O;
反应④是乙醇和乙酸制备乙酸乙酯的反应,反应方程式为:CH3COOH+C2H5OHCH3COOC2H5+H2O。
答案第1页,共2页
答案第1页,共2页
