第五章第一节合成高分子的基本方法同步练习(含解析)2022-2023学年下学期高二化学人教版(2019)选择性必修3
文档属性
| 名称 | 第五章第一节合成高分子的基本方法同步练习(含解析)2022-2023学年下学期高二化学人教版(2019)选择性必修3 |

|
|
| 格式 | docx | ||
| 文件大小 | 5.8MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-06-22 00:00:00 | ||
图片预览



文档简介
第五章第一节合成高分子的基本方法同步练习
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1.材料是人类赖以生存和发展的物质基础。下列说法错误的是
A.可用于飞机与舰艇等的隐形涂料的聚乙炔、聚苯胺等属于导电高分子材料
B.聚酰胺纤维中的锦纶是较早通过加聚反应合成的纤维
C.高纯度的单晶硅、二氧化硅属于新型无机非金属材料
D.华为公司首创的液冷散热技术所用的石墨烯材料是无机高分子材料
2.聚合物商品Kodel的结构简式(假设为理想单一结构)如下:
下列有关该聚合物的叙述错误的是
A.属于线性高分子,具有热塑性 B.属于合成纤维,可降解
C.可通过缩聚反应制得 D.聚合单体有3种
3.化学用语可以表达化学过程,下列化学用语的表达错误的是
A.用电子式表示的形成:
B.用离子方程式表示溶于烧碱溶液:
C.用电子云轮廓图表示H-H的s-sσ键形成的示意图:
D.用化学方程式表示尿素与甲醛制备线型脲醛树脂:
4.光学性能优良的高分子材料聚碳酸异山梨醇酯可由如下反应制备。
下列说法错误的是
A.该高分子材料可降解 B.异山梨醇分子中有3个手性碳
C.反应式中化合物X为甲醇 D.该聚合反应为缩聚反应
5.高分子树脂X的合成路线如下。
下列说法不正确的是
A.高分子X中存在氢键
B.甲的结构简式为
C.①的反应中有水生成
D.高分子X水解可得到乙
6.某种超分子聚合物网络生物电极的制备原料CB和PDMA的结构如下图。下列说法正确的是
A.CB中核磁共振氢谱有两组峰 B.单体的化学式为
C.CB与PDMA均为高分子 D.CB与PDMA都具有良好的耐酸碱性
7.下图是制备生物降解塑料(PHB)的部分合成步骤。下列有关说法正确的是
A.A→B为加成反应,B→C为加聚反应
B.B的同分异构体中,与B含有相同官能团的结构有4种
C.为纯净物
D.易溶于水
8.一种自修复材料在外力破坏后能够复原,其结构简式(图1)和修复原理(图2)如下图所示,下列说法正确的是
A.自修复过程中“-COOCH2CH2CH2CH3”基团之间形成了化学键
B.该材料可以接触强酸或强碱
C.合成该高分子的两种单体在水中溶解度较大
D.该高分子可通过加聚反应合成
9.2022年北京成功举办了第24届冬奥会,大量有机材料亮相冬奥。下列材料中主要成分不属于有机高分子的是
A.(聚氯乙烯)制作的“冰墩墩”钥匙扣
B.(双向拉伸聚丙烯薄膜)制成的冬奥纪念钞
C.颁奖礼服中的石墨烯发热内胆
D.“冰立方”的(乙烯-四氟乙烯共聚物)膜结构
10.葫芦脲是近年来超分子领域发展迅速的大环主体分子之一,具有疏水的刚性空腔。葫芦[6]脲的结构简式如图所示,对位取代的苯的衍生物恰好可以进入葫芦[6]的空腔,下列关于葫芦[6]脲的说法正确的是
已知
A.属于高分子化合物
B.能与4molNaOH发生水解反应
C.由乙二醛和尿素两种有机物合成
D.4—甲基苯甲醛可进入葫芦[6]脲的空腔
11.某光刻胶(ESCAP)由三种单体共聚而成,ESCAP在芯片表面曝光时发生如下反应:下列叙述不正确的是
A.合成ESCAP的一种单体为苯乙烯 B.曝光时发生了取代反应和消去反应
C.X的酸性比ESCAP的酸性强 D.Y分子碳原子共平面且存在顺反异构
12.卡塔尔足球世界杯处处体现“化学元素”,下列有关描述正确的是
A.局部麻醉剂中的氯乙烷有2种同分异构体
B.人造草坪中的聚乙烯和聚丙烯互为同系物
C.看台材料中的聚碳酸酯可通过缩聚反应制得
D.运动衣的主要材料,其两种单体的核磁共振氢谱峰数、峰面积均相同
13.脱落酸是抑制植物生长的激素,因能促使叶子脱落而得名,其结构简式如图所示,下列说法正确的是
A.脱落酸分子式为C15H18O4
B.脱落酸通过聚合反应能生成高分子化合物
C.1 mol脱落酸最多可与5 mol氢气发生加成反应
D.脱落酸与等物质的量的Br2加成的产物只有3种
14.化学在国防领域发挥着重要作用。关于下列装备涉及材料的说法不正确的是
A 防弹衣的主要材料: 聚合物分子内含有酰胺基
B 隐形飞机的微波吸收材料: 单体不能使溴水褪色
C 潜艇的消声瓦: 可由和合成
D 潜艇的耐压球壳:钛合金 钛合金中存在金属键
A.A B.B C.C D.D
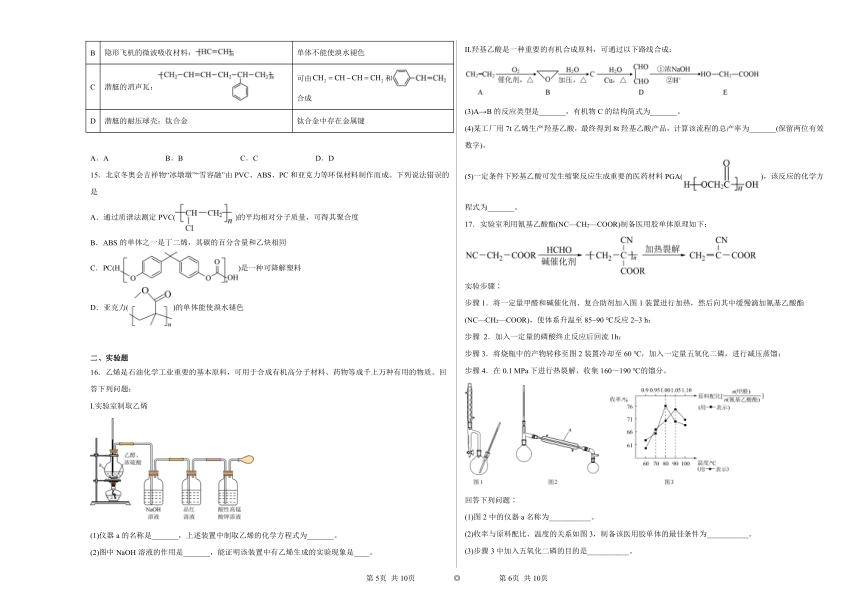
15.北京冬奥会吉祥物“冰墩墩”“雪容融”由PVC、ABS、PC和亚克力等环保材料制作而成。下列说法错误的是
A.通过质谱法测定PVC()的平均相对分子质量,可得其聚合度
B.ABS的单体之一是丁二烯,其碳的百分含量和乙炔相同
C.PC()是一种可降解塑料
D.亚克力()的单体能使溴水褪色
二、实验题
16.乙烯是石油化学工业重要的基本原料,可用于合成有机高分子材料、药物等成千上万种有用的物质。回答下列问题:
I.实验室制取乙烯
(1)仪器a的名称是_______,上述装置中制取乙烯的化学方程式为_______。
(2)图中NaOH溶液的作用是_______,能证明该装置中有乙烯生成的实验现象是____。
II.羟基乙酸是一种重要的有机合成原料,可通过以下路线合成:
(3)A→B的反应类型是_______,有机物C的结构简式为_______。
(4)某工厂用7t乙烯生产羟基乙酸,最终得到8t羟基乙酸产品,计算该流程的总产率为_______(保留两位有效数字)。
(5)一定条件下羟基乙酸可发生缩聚反应生成重要的医药材料PGA(),该反应的化学方程式为_______。
17.实验室利用氰基乙酸酯(NC—CH2—COOR)制备医用胶单体原理如下:
实验步骤∶
步骤1.将一定量甲醛和碱催化剂、复合助剂加入图1装置进行加热,然后向其中缓慢滴加氰基乙酸酯(NC—CH2—COOR),使体系升温至85~90 ℃反应2~3 h;
步骤 2.加入一定量的磷酸终止反应后回流1h;
步骤3.将烧瓶中的产物转移至图2装置冷却至60 ℃,加入一定量五氧化二磷,进行减压蒸馏;
步骤4.在0.1 MPa下进行热裂解,收集160~190 ℃的馏分。
回答下列问题∶
(1)图2中的仪器a名称为___________。
(2)收率与原料配比、温度的关系如图3,制备该医用胶单体的最佳条件为___________。
(3)步骤3中加入五氧化二磷的目的是___________。
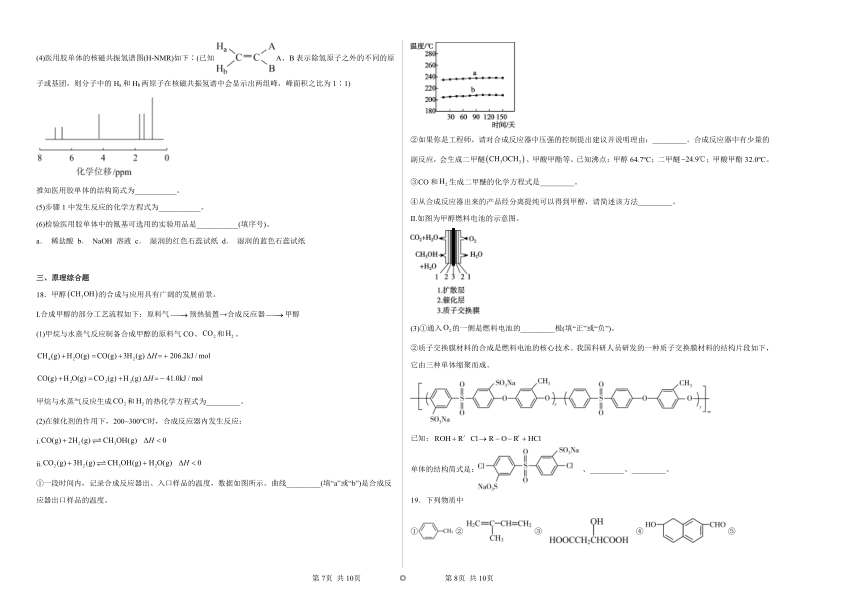
(4)医用胶单体的核磁共振氢谱图(H-NMR)如下∶(已知A、B表示除氢原子之外的不同的原子或基团,则分子中的Ha和Hb两原子在核磁共振氢谱中会显示出两组峰,峰面积之比为1∶1)
推知医用胶单体的结构简式为___________。
(5)步骤1中发生反应的化学方程式为___________。
(6)检验医用胶单体中的氰基可选用的实验用品是___________(填序号)。
a. 稀盐酸 b. NaOH 溶液 c. 湿润的红色石蕊试纸 d. 湿润的蓝色石蕊试纸
三、原理综合题
18.甲醇的合成与应用具有广阔的发展前景。
Ⅰ.合成甲醇的部分工艺流程如下:原料气预热装置→合成反应器甲醇
(1)甲烷与水蒸气反应制备合成甲醇的原料气CO、和。
甲烷与水蒸气反应生成和的热化学方程式为_________。
(2)在催化剂的作用下,200~300℃时,合成反应器内发生反应:
ⅰ.
ⅱ.
①一段时间内,记录合成反应器出、入口样品的温度,数据如图所示。曲线_________(填“a”或“b”)是合成反应器出口样品的温度。
②如果你是工程师,请对合成反应器中压强的控制提出建议并说明理由:_________。合成反应器中有少量的副反应,会生成二甲醚、甲酸甲酯等。已知沸点:甲醇64.7℃;二甲醚;甲酸甲酯32.0℃。
③CO和生成二甲醚的化学方程式是_________。
④从合成反应器出来的产品经分离提纯可以得到甲醇,请简述该方法_________。
Ⅱ.如图为甲醇燃料电池的示意图。
(3)①通入的一侧是燃料电池的_________极(填“正”或“负”)。
②质子交换膜材料的合成是燃料电池的核心技术。我国科研人员研发的一种质子交换膜材料的结构片段如下,它由三种单体缩聚而成。
已知:
单体的结构简式是: 、_________、_________。
19.下列物质中①②③④⑤(填写编号)
(1)常温下①和②都是液体,实验室可选用_______(填试剂名称,下同)进行鉴别,用一种试剂鉴别有机物③和有机物⑤:_______。写出③与乙醇发生酯化反应的化学方程式:_______。
(2)有机物④中含氧官能团的名称为_______,1mol有机物⑤最多可消耗_______mol H2,写出实验室检验④中醛基的实验过程:_______。
(3)有机物⑤与丙酮()反应可制取某种高聚物树脂,这种树脂的结构简式为_______。
(4)有机物⑤制取的流程如下图:
①反应(1)和反应(3)的目的为_______。
②若需完成如下转化:,选用试剂为_______。
第1页 共4页 ◎ 第2页 共4页
第1页 共4页 ◎ 第2页 共4页
参考答案:
1.B
【详解】A.聚乙炔、聚苯胺链节上存在自由移动的电子,可以导电,属于导电高分子材料,故A正确;
B.聚酰胺纤维是通过缩聚反应合成的,故B错误;
C.高纯度的单晶硅、二氧化硅属于新型无机非金属材料,故C正确;
D.石墨烯材料是单层石墨结构,属于无机高分子材料,故D正确;
故选:B。
2.D
【详解】A.由Kodel的结构简式可知,该聚合物属于线性高分子,具有热塑性,故A正确;
B.该聚合物属于合成纤维,其中含有酯基,可以发生水解反应而降解,故B正确;
C.由Kodel的结构简式可知,该聚合物可通过缩聚反应制得,故C正确;
D.由Kodel的结构简式可知,该聚合物的单体为和共2种,故D错误;
故选D。
3.D
【详解】A.钾原子失去电子,硫原子得到电子形成硫化钾,硫化钾为离子化合物,用电子式表示的形成:,A正确;
B.氢氧化铝为两性氢氧化物,可以和强碱反应生成四羟基合铝酸根离子,离子方程式为:,B正确;
C.H的s能级为球形,两个氢原子形成氢气的时候,是两个s能级的原子轨道相互靠近,形成新的轨道,则用电子云轮廓图表示H-H的s-sσ键形成的示意图:,C正确;
D.用化学方程式表示尿素与甲醛制备线型脲醛树脂为,D错误;
故选D。
4.B
【详解】A.该高分子材料中含有酯基,可以降解,A正确;
B.异山梨醇中四处的碳原子为手性碳原子,故异山梨醇分子中有4个手性碳,B错误;
C.反应式中异山梨醇释放出一个羟基与碳酸二甲酯释放出的甲基结合生成甲醇,故反应式中X为甲醇,C正确;
D.该反应在生产高聚物的同时还有小分子的物质生成,属于缩聚反应,D正确;
故答案选B。
5.D
【分析】CH2=CHCN与H2O、H+加热条件下反应生成甲为CH2=CHCOOH,根据高分子X的结构简式,乙的分子式可知,乙的结构简式为,甲与乙发生加聚反应生成高分子X。
【详解】A.根据高分子X的结构简式可知,其内部存在-NH-结构,存在氢键,A正确;
B.根据分析可知,甲的结构简式为CH2=CHCOOH,B正确;
C.反应①为2个与HCHO反应生成,根据原子守恒可知,该反应中有水生成,C正确;
D.甲和乙发生加聚反应生成高分子X,而不是缩聚反应,因此高分子X水解无法得到乙,D错误;
故答案选D。
6.A
【详解】A.根据等效氢原理可知,中核磁共振氢谱有二组峰如图所示 ,A正确;
B.由题干图示信息可知,单体为: ,则其化学式为C5H9NO,B错误;
C.高分子是指相对分子质量成千上万的物质,由题干可知,的相对分子质量为1328,不是高分子化合物,为高分子 ,C错误;
D.由题干信息可知,CB与PDMA中都含有酰胺键,在酸性和碱性条件下均能发生水解,故CB与PDMA都不耐酸碱性,D错误;
故答案为:A。
7.B
【分析】H2可以还原酮羰基为羟基,不能还原羧基,则B为 。
【详解】A.A→B为加成反应,B→C为缩聚反应,A项错误;
B.B的同分异构体中与B含有相同官能团的结构有、 、 、 ,共4种,B项正确;
C.高聚物由于n的不确定,组成的物质是混合物,C项错误;
D.为聚酯,难溶于水,D项错误。
答案选B。
8.D
【详解】A.由图2可知,自修复过程中“-COOCH2CH2CH2CH3”基团之间没有形成化学键,故A错误;
B.该高分子化合物中含有酯基,所以能和酸、碱反应,使用时应避免接触强酸或强碱;故B错误;
C.合成该高分子化合物的单体分别为CH2=C(CH3)COOCH3和CH2=CHCOOCH2CH2CH2CH3,在水中溶解度较小,故B错误;
D.该高分子由CH2=C(CH3)COOCH3和CH2=CHCOOCH2CH2CH2CH3加聚反应得到;故D正确;
故答案选D。
9.C
【详解】聚氯乙烯、双向拉伸聚丙烯薄膜、乙烯 四氟乙烯共聚物都属于有机高分子,石墨烯是碳单质,不属于有机物,故C符合题意。
综上所述,答案为C。
10.D
【详解】A.由结构简式可知,葫芦[6]脲的相对分子质量小于一万,不属于高分子化合物,故A错误;
B.由结构简式可知,葫芦[6]脲分子中含有的酰胺基能在氢氧化钠溶液中发生水解反应,1mol葫芦[6]脲分子能与24mol氢氧化钠发生水解反应,故B错误;
C.由结构简式可知,葫芦[6]脲分子是由乙二醛、尿素和甲醛三种有机物合成而得,故C错误;
D.由对位取代的苯的衍生物恰好可以进入葫芦[6]的空腔可知,4—甲基苯甲醛可进入葫芦[6]脲的空腔,故D正确;
故选D。
11.D
【详解】A.由图可知,合成ESCAP的单体为,故其中一种单体为苯乙烯,故A正确;
B.曝光时ESCAP支链上酯基发生取代反应生成羧基和羟基,羟基又发生消去反应生成碳碳双键得到,故发生了取代反应和消去反应,故B正确;
C.X中含有羧基,故其酸性比ESCAP的酸性强,故C正确;
D.Y分子中碳碳双键两端的基团相同,不存在顺反异构,故D错误;
答案选D。
12.C
【详解】A.氯乙烷只有1种结构,不存在同分异构体,故A错误;
B.聚乙烯和聚丙烯的聚合度n值为不确定值,都属于混合物,不可能互为同系物,故B错误;
C.由结构简式可知,聚碳酸酯属于聚酯类高分子化合物,可通过缩聚反应制得,故C正确;
D.由结构简式可知,合成高分子化合物的单体为对苯二甲酸和对苯二胺,两种单体的核磁共振氢谱峰数相同,但羧基和氨基的氢原子数目不同,所以峰面积不同,故D错误;
故选C。
13.B
【详解】A.脱落酸的分子式为C15H20O4,A项错误;
B.脱落酸含有碳碳双键,可发生加聚反应;含有羧基和羟基,可发生缩聚反应,B项正确;
C.羧基不能和H2发生加成反应,1 mol脱落酸最多可与4 mol氢气发生加成反应,C项错误;
D.脱落酸分子中含有3个碳碳双键,其中右侧的2个双键通过一个碳碳单键连接,具有共轭二烯烃的性质,则脱落酸分子与等物质的量的Br2加成的产物有4种(不考虑顺反异构),D项错误。
答案选B。
14.B
【详解】A.由单体和通过缩聚反应生成,聚合物分子内含有酰胺基,故A正确;
B.单体为乙炔,含碳碳三键,能与溴单质发生加成反应,从而使溴水褪色,故B错误;
C.由结构可知的单体为:CH2=CH CH=CH2和,两者通过加聚反应生成消声瓦,故C正确;
D.合金中存在金属键,故D正确;
故选:B。
15.B
【详解】A.单体的相对分子质量为68,则聚合度等于,选项A正确;
B.ABS的单体之一是丁二烯,分子式为C4H6,与乙炔的最简式不相同,其碳的百分含量和乙炔不相同,选项B错误;
C.PC是一种可降解的聚碳酸酯类高分子材料,选项C正确;
D.亚克力材料的单体是,名称为甲基丙烯酸甲酯,能使溴水褪色,选项D正确;
答案选B。
16.(1) 圆底烧瓶 CH3CH2OHCH2=CH2↑+H2O
(2) 除去乙烯中混有的SO2、CO2等酸性气体 品红溶液不褪色,酸性KMnO4溶液紫色褪去
(3) 氧化反应 HOCH2CH2OH
(4)42%
(5)nHOCH2COOH+(n-1)H2O
【分析】I.乙醇与浓硫酸反应生成乙烯的同时浓H2SO4易将乙醇氧化为C或CO和CO2,浓H2SO4被还原为SO2,乙烯具有还原性,可根据酸性KMnO4溶液褪色来证明有乙烯生成,由于SO2也具有还原性,能使酸性KMnO4溶液褪色,会干扰乙烯的检验,所以检验乙烯之前必须除净SO2,则NaOH溶液的作用是除去乙烯中混有的SO2、CO2等酸性气体,品红溶液可检验是否除净。
II.由合成路线可知,乙烯催化氧化生成环氧乙烷,环氧乙烷和水反应得到C,C发生催化氧化得到乙二醛,可推知C为乙二醇,乙二醛先与浓NaOH作用,再酸化得到羟基乙酸。
【详解】(1)由仪器构造可知,仪器a的名称是圆底烧瓶,实验室用乙醇与浓硫酸加热到170反应生成乙烯和水,反应的化学方程式为CH3CH2OHCH2=CH2↑+H2O,故答案为:圆底烧瓶;CH3CH2OHCH2=CH2↑+H2O;
(2)由分析可知,制取乙烯时同时生成了SO2、CO2等酸性气体,为防止干扰乙烯的检验,用NaOH溶液除去乙烯中混有的SO2、CO2等酸性气体;乙烯和二氧化硫都能使酸性KMnO4溶液褪色,所以能证明该装置中有乙烯生成的实验现象是品红溶液不褪色,排除的干扰,酸性KMnO4溶液紫色褪去,故答案为:除去乙烯中混有的SO2、CO2等酸性气体;品红溶液不褪色,酸性KMnO4溶液紫色褪去;
(3)有机物加氧去氢的反应为氧化反应,A→B过程中为加氧反应,故反应类型是氧化反应,由分析可知,乙二醇催化氧化生成乙二醛,则有机物C为乙二醇,结构简式为HOCH2CH2OH,故答案为:氧化反应;HOCH2CH2OH;
(4)由转化关系可知,理论上乙烯反应得到等物质的量的羟基乙酸,则用7t乙烯生产羟基乙酸,理论上得到羟基乙酸的质量为76=19t,则该流程的总产率为100%=42%,故答案为:42%。
(5)羟基乙酸分子中含有羟基和羧基,在一定条件下发生缩聚反应生成高聚物,反应的化学方程式为nHOCH2COOH+(n-1)H2O故答案为:nHOCH2COOH+(n-1)H2O。
17. 直形冷凝管 甲醛和氨基乙酸酯的配比为1.00、温度为80℃ 干燥有机物 nNC—CH2—COOCH2CH2CH2CH3+nHCHO+nH2O ad
【分析】氰基乙酸酯(NC—CH2—COOR)和甲醛在碱催化下发生聚合反应生成和水,,再裂解得到最终产物。
【详解】(1)根据仪器构造可知,图2中的仪器a名称为直形冷凝管。
(2)根据图3可知,当甲醛和氨基乙酸酯的物质的量之比为1.00、温度为80℃时,收率最高,所以制备该医用胶单体的最佳条件为甲醛和氨基乙酸酯的配比为1.00、温度为80℃。
(3)发生第一步反应时生成了水,步骤3中加入五氧化二磷的目的是除去中间产物中的水。
(4)根据核磁共振氢谱图(H-NMR)可知,该医用胶单体有6种不同化学环境的氢原子,个数比为1:1:2:2:2:3,所以该有机物的结构简式为。
(5)步骤1是氰基乙酸丁酯(NC—CH2—COOCH2CH2CH2CH3)和甲醛在碱催化下发生聚合反应,发生反应的化学方程式为:nNC—CH2—COOCH2CH2CH2CH3+nHCHO+nH2O。
(6)氰基能发生水解生成羧基,所以可以用稀盐酸和湿润湿润的蓝色石蕊试纸检验医用胶单体中的氰基,故选用的实验用品是ad。
18.(1)CH4(g) + 2H2O(g) =CO2(g) + 4H2(g) H = +165.2kJ·mol-1
(2) a 适当加压。加压能使该反应速率增大、原料转化率升高,也会增加设备和动力成本 降温冷凝得到液态甲醇粗品再蒸馏提纯
(3) 正
【详解】(1)根据盖斯定律,将两个热化学方程式加起来得:CH4(g)+2H2O(g)=CO2(g)+4H2(g) H=+165.2kJ·mol-1;
(2)①两个反应都是放热反应,合成反应器出口样品的温度更高一些,故选a;
②两个反应都是气体体积减小的反应,从平衡的角度来看,增大压强,能使该反应速率增大、原料转化率升高,但是压强高,意味着设备要好,这就需要加大成本的投入,因此需要适当加压;
③CO和H2生成二甲醚的化学方程式为:2CO+4H2CH3OCH3+H2O;
④题中给出了几个物质的沸点,甲醇的沸点较高,且和其他物质的沸点相差较大,可以通过降温冷凝的方法得到甲醇粗品,再经过蒸馏提纯;
(3)①根据燃料电池的构造,通入O2的一侧是燃料电池的正极;
②结合题中给出的化学方程式,可以推出另外两种单体分别为: 、 。
19.(1) 溴水 浓溴水or三氯化铁溶液or水or碳酸氢钠溶液 +2CH3CH2OH +2H2O
(2) 羟基和醛基 3 取样,加入新制氢氧化铜,加热,有砖红色沉淀生成
(3)
(4) 保护酚羟基,防止其被KMnO4(H+)氧化 NaHCO3
【详解】(1)甲苯和烯烃在常温下可以通过加入溴水进行鉴别,能使溴水褪色的是烯烃;③中含有羟基和羧基,⑤中含有酚羟基,加入碳酸氢钠,可以产生气泡的说明含有羧基;加入浓溴水,产生白色沉淀的说明含有酚羟基;加入三氯化铁溶液变成紫色的,说明有酚羟基;③与乙醇发生酯化反应;
故答案为:溴水;浓溴水或三氯化铁溶液或碳酸氢钠溶液; +C2H5OH +2H2O;
(2)④中的含氧官能团为羟基和醛基;⑤中因含有苯环,1个苯环能与3个H2发生加成反应;检验醛基可以通过加入新制的氢氧化铜并加热,观察是否有砖红色沉淀生成;
故答案为:羟基和醛基;3;取样,加入新制氢氧化铜,加热,有砖红色沉淀生成;
(3)⑤与丙酮发生缩聚反应,生成 ;
故答案为: ;
(4)①酚羟基具有还原性,通过对比物质的结构式可知,反应(1)和反应(3)的目的为保护酚羟基,防止其被KMnO4(H+)氧化;
故答案为:保护酚羟基,防止其被KMnO4(H+)氧化;
②羧基与碳酸氢钠反应生成羧酸钠,故需要加碳酸氢钠;
故答案为:碳酸氢钠。
答案第1页,共2页
答案第1页,共2页
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1.材料是人类赖以生存和发展的物质基础。下列说法错误的是
A.可用于飞机与舰艇等的隐形涂料的聚乙炔、聚苯胺等属于导电高分子材料
B.聚酰胺纤维中的锦纶是较早通过加聚反应合成的纤维
C.高纯度的单晶硅、二氧化硅属于新型无机非金属材料
D.华为公司首创的液冷散热技术所用的石墨烯材料是无机高分子材料
2.聚合物商品Kodel的结构简式(假设为理想单一结构)如下:
下列有关该聚合物的叙述错误的是
A.属于线性高分子,具有热塑性 B.属于合成纤维,可降解
C.可通过缩聚反应制得 D.聚合单体有3种
3.化学用语可以表达化学过程,下列化学用语的表达错误的是
A.用电子式表示的形成:
B.用离子方程式表示溶于烧碱溶液:
C.用电子云轮廓图表示H-H的s-sσ键形成的示意图:
D.用化学方程式表示尿素与甲醛制备线型脲醛树脂:
4.光学性能优良的高分子材料聚碳酸异山梨醇酯可由如下反应制备。
下列说法错误的是
A.该高分子材料可降解 B.异山梨醇分子中有3个手性碳
C.反应式中化合物X为甲醇 D.该聚合反应为缩聚反应
5.高分子树脂X的合成路线如下。
下列说法不正确的是
A.高分子X中存在氢键
B.甲的结构简式为
C.①的反应中有水生成
D.高分子X水解可得到乙
6.某种超分子聚合物网络生物电极的制备原料CB和PDMA的结构如下图。下列说法正确的是
A.CB中核磁共振氢谱有两组峰 B.单体的化学式为
C.CB与PDMA均为高分子 D.CB与PDMA都具有良好的耐酸碱性
7.下图是制备生物降解塑料(PHB)的部分合成步骤。下列有关说法正确的是
A.A→B为加成反应,B→C为加聚反应
B.B的同分异构体中,与B含有相同官能团的结构有4种
C.为纯净物
D.易溶于水
8.一种自修复材料在外力破坏后能够复原,其结构简式(图1)和修复原理(图2)如下图所示,下列说法正确的是
A.自修复过程中“-COOCH2CH2CH2CH3”基团之间形成了化学键
B.该材料可以接触强酸或强碱
C.合成该高分子的两种单体在水中溶解度较大
D.该高分子可通过加聚反应合成
9.2022年北京成功举办了第24届冬奥会,大量有机材料亮相冬奥。下列材料中主要成分不属于有机高分子的是
A.(聚氯乙烯)制作的“冰墩墩”钥匙扣
B.(双向拉伸聚丙烯薄膜)制成的冬奥纪念钞
C.颁奖礼服中的石墨烯发热内胆
D.“冰立方”的(乙烯-四氟乙烯共聚物)膜结构
10.葫芦脲是近年来超分子领域发展迅速的大环主体分子之一,具有疏水的刚性空腔。葫芦[6]脲的结构简式如图所示,对位取代的苯的衍生物恰好可以进入葫芦[6]的空腔,下列关于葫芦[6]脲的说法正确的是
已知
A.属于高分子化合物
B.能与4molNaOH发生水解反应
C.由乙二醛和尿素两种有机物合成
D.4—甲基苯甲醛可进入葫芦[6]脲的空腔
11.某光刻胶(ESCAP)由三种单体共聚而成,ESCAP在芯片表面曝光时发生如下反应:下列叙述不正确的是
A.合成ESCAP的一种单体为苯乙烯 B.曝光时发生了取代反应和消去反应
C.X的酸性比ESCAP的酸性强 D.Y分子碳原子共平面且存在顺反异构
12.卡塔尔足球世界杯处处体现“化学元素”,下列有关描述正确的是
A.局部麻醉剂中的氯乙烷有2种同分异构体
B.人造草坪中的聚乙烯和聚丙烯互为同系物
C.看台材料中的聚碳酸酯可通过缩聚反应制得
D.运动衣的主要材料,其两种单体的核磁共振氢谱峰数、峰面积均相同
13.脱落酸是抑制植物生长的激素,因能促使叶子脱落而得名,其结构简式如图所示,下列说法正确的是
A.脱落酸分子式为C15H18O4
B.脱落酸通过聚合反应能生成高分子化合物
C.1 mol脱落酸最多可与5 mol氢气发生加成反应
D.脱落酸与等物质的量的Br2加成的产物只有3种
14.化学在国防领域发挥着重要作用。关于下列装备涉及材料的说法不正确的是
A 防弹衣的主要材料: 聚合物分子内含有酰胺基
B 隐形飞机的微波吸收材料: 单体不能使溴水褪色
C 潜艇的消声瓦: 可由和合成
D 潜艇的耐压球壳:钛合金 钛合金中存在金属键
A.A B.B C.C D.D
15.北京冬奥会吉祥物“冰墩墩”“雪容融”由PVC、ABS、PC和亚克力等环保材料制作而成。下列说法错误的是
A.通过质谱法测定PVC()的平均相对分子质量,可得其聚合度
B.ABS的单体之一是丁二烯,其碳的百分含量和乙炔相同
C.PC()是一种可降解塑料
D.亚克力()的单体能使溴水褪色
二、实验题
16.乙烯是石油化学工业重要的基本原料,可用于合成有机高分子材料、药物等成千上万种有用的物质。回答下列问题:
I.实验室制取乙烯
(1)仪器a的名称是_______,上述装置中制取乙烯的化学方程式为_______。
(2)图中NaOH溶液的作用是_______,能证明该装置中有乙烯生成的实验现象是____。
II.羟基乙酸是一种重要的有机合成原料,可通过以下路线合成:
(3)A→B的反应类型是_______,有机物C的结构简式为_______。
(4)某工厂用7t乙烯生产羟基乙酸,最终得到8t羟基乙酸产品,计算该流程的总产率为_______(保留两位有效数字)。
(5)一定条件下羟基乙酸可发生缩聚反应生成重要的医药材料PGA(),该反应的化学方程式为_______。
17.实验室利用氰基乙酸酯(NC—CH2—COOR)制备医用胶单体原理如下:
实验步骤∶
步骤1.将一定量甲醛和碱催化剂、复合助剂加入图1装置进行加热,然后向其中缓慢滴加氰基乙酸酯(NC—CH2—COOR),使体系升温至85~90 ℃反应2~3 h;
步骤 2.加入一定量的磷酸终止反应后回流1h;
步骤3.将烧瓶中的产物转移至图2装置冷却至60 ℃,加入一定量五氧化二磷,进行减压蒸馏;
步骤4.在0.1 MPa下进行热裂解,收集160~190 ℃的馏分。
回答下列问题∶
(1)图2中的仪器a名称为___________。
(2)收率与原料配比、温度的关系如图3,制备该医用胶单体的最佳条件为___________。
(3)步骤3中加入五氧化二磷的目的是___________。
(4)医用胶单体的核磁共振氢谱图(H-NMR)如下∶(已知A、B表示除氢原子之外的不同的原子或基团,则分子中的Ha和Hb两原子在核磁共振氢谱中会显示出两组峰,峰面积之比为1∶1)
推知医用胶单体的结构简式为___________。
(5)步骤1中发生反应的化学方程式为___________。
(6)检验医用胶单体中的氰基可选用的实验用品是___________(填序号)。
a. 稀盐酸 b. NaOH 溶液 c. 湿润的红色石蕊试纸 d. 湿润的蓝色石蕊试纸
三、原理综合题
18.甲醇的合成与应用具有广阔的发展前景。
Ⅰ.合成甲醇的部分工艺流程如下:原料气预热装置→合成反应器甲醇
(1)甲烷与水蒸气反应制备合成甲醇的原料气CO、和。
甲烷与水蒸气反应生成和的热化学方程式为_________。
(2)在催化剂的作用下,200~300℃时,合成反应器内发生反应:
ⅰ.
ⅱ.
①一段时间内,记录合成反应器出、入口样品的温度,数据如图所示。曲线_________(填“a”或“b”)是合成反应器出口样品的温度。
②如果你是工程师,请对合成反应器中压强的控制提出建议并说明理由:_________。合成反应器中有少量的副反应,会生成二甲醚、甲酸甲酯等。已知沸点:甲醇64.7℃;二甲醚;甲酸甲酯32.0℃。
③CO和生成二甲醚的化学方程式是_________。
④从合成反应器出来的产品经分离提纯可以得到甲醇,请简述该方法_________。
Ⅱ.如图为甲醇燃料电池的示意图。
(3)①通入的一侧是燃料电池的_________极(填“正”或“负”)。
②质子交换膜材料的合成是燃料电池的核心技术。我国科研人员研发的一种质子交换膜材料的结构片段如下,它由三种单体缩聚而成。
已知:
单体的结构简式是: 、_________、_________。
19.下列物质中①②③④⑤(填写编号)
(1)常温下①和②都是液体,实验室可选用_______(填试剂名称,下同)进行鉴别,用一种试剂鉴别有机物③和有机物⑤:_______。写出③与乙醇发生酯化反应的化学方程式:_______。
(2)有机物④中含氧官能团的名称为_______,1mol有机物⑤最多可消耗_______mol H2,写出实验室检验④中醛基的实验过程:_______。
(3)有机物⑤与丙酮()反应可制取某种高聚物树脂,这种树脂的结构简式为_______。
(4)有机物⑤制取的流程如下图:
①反应(1)和反应(3)的目的为_______。
②若需完成如下转化:,选用试剂为_______。
第1页 共4页 ◎ 第2页 共4页
第1页 共4页 ◎ 第2页 共4页
参考答案:
1.B
【详解】A.聚乙炔、聚苯胺链节上存在自由移动的电子,可以导电,属于导电高分子材料,故A正确;
B.聚酰胺纤维是通过缩聚反应合成的,故B错误;
C.高纯度的单晶硅、二氧化硅属于新型无机非金属材料,故C正确;
D.石墨烯材料是单层石墨结构,属于无机高分子材料,故D正确;
故选:B。
2.D
【详解】A.由Kodel的结构简式可知,该聚合物属于线性高分子,具有热塑性,故A正确;
B.该聚合物属于合成纤维,其中含有酯基,可以发生水解反应而降解,故B正确;
C.由Kodel的结构简式可知,该聚合物可通过缩聚反应制得,故C正确;
D.由Kodel的结构简式可知,该聚合物的单体为和共2种,故D错误;
故选D。
3.D
【详解】A.钾原子失去电子,硫原子得到电子形成硫化钾,硫化钾为离子化合物,用电子式表示的形成:,A正确;
B.氢氧化铝为两性氢氧化物,可以和强碱反应生成四羟基合铝酸根离子,离子方程式为:,B正确;
C.H的s能级为球形,两个氢原子形成氢气的时候,是两个s能级的原子轨道相互靠近,形成新的轨道,则用电子云轮廓图表示H-H的s-sσ键形成的示意图:,C正确;
D.用化学方程式表示尿素与甲醛制备线型脲醛树脂为,D错误;
故选D。
4.B
【详解】A.该高分子材料中含有酯基,可以降解,A正确;
B.异山梨醇中四处的碳原子为手性碳原子,故异山梨醇分子中有4个手性碳,B错误;
C.反应式中异山梨醇释放出一个羟基与碳酸二甲酯释放出的甲基结合生成甲醇,故反应式中X为甲醇,C正确;
D.该反应在生产高聚物的同时还有小分子的物质生成,属于缩聚反应,D正确;
故答案选B。
5.D
【分析】CH2=CHCN与H2O、H+加热条件下反应生成甲为CH2=CHCOOH,根据高分子X的结构简式,乙的分子式可知,乙的结构简式为,甲与乙发生加聚反应生成高分子X。
【详解】A.根据高分子X的结构简式可知,其内部存在-NH-结构,存在氢键,A正确;
B.根据分析可知,甲的结构简式为CH2=CHCOOH,B正确;
C.反应①为2个与HCHO反应生成,根据原子守恒可知,该反应中有水生成,C正确;
D.甲和乙发生加聚反应生成高分子X,而不是缩聚反应,因此高分子X水解无法得到乙,D错误;
故答案选D。
6.A
【详解】A.根据等效氢原理可知,中核磁共振氢谱有二组峰如图所示 ,A正确;
B.由题干图示信息可知,单体为: ,则其化学式为C5H9NO,B错误;
C.高分子是指相对分子质量成千上万的物质,由题干可知,的相对分子质量为1328,不是高分子化合物,为高分子 ,C错误;
D.由题干信息可知,CB与PDMA中都含有酰胺键,在酸性和碱性条件下均能发生水解,故CB与PDMA都不耐酸碱性,D错误;
故答案为:A。
7.B
【分析】H2可以还原酮羰基为羟基,不能还原羧基,则B为 。
【详解】A.A→B为加成反应,B→C为缩聚反应,A项错误;
B.B的同分异构体中与B含有相同官能团的结构有、 、 、 ,共4种,B项正确;
C.高聚物由于n的不确定,组成的物质是混合物,C项错误;
D.为聚酯,难溶于水,D项错误。
答案选B。
8.D
【详解】A.由图2可知,自修复过程中“-COOCH2CH2CH2CH3”基团之间没有形成化学键,故A错误;
B.该高分子化合物中含有酯基,所以能和酸、碱反应,使用时应避免接触强酸或强碱;故B错误;
C.合成该高分子化合物的单体分别为CH2=C(CH3)COOCH3和CH2=CHCOOCH2CH2CH2CH3,在水中溶解度较小,故B错误;
D.该高分子由CH2=C(CH3)COOCH3和CH2=CHCOOCH2CH2CH2CH3加聚反应得到;故D正确;
故答案选D。
9.C
【详解】聚氯乙烯、双向拉伸聚丙烯薄膜、乙烯 四氟乙烯共聚物都属于有机高分子,石墨烯是碳单质,不属于有机物,故C符合题意。
综上所述,答案为C。
10.D
【详解】A.由结构简式可知,葫芦[6]脲的相对分子质量小于一万,不属于高分子化合物,故A错误;
B.由结构简式可知,葫芦[6]脲分子中含有的酰胺基能在氢氧化钠溶液中发生水解反应,1mol葫芦[6]脲分子能与24mol氢氧化钠发生水解反应,故B错误;
C.由结构简式可知,葫芦[6]脲分子是由乙二醛、尿素和甲醛三种有机物合成而得,故C错误;
D.由对位取代的苯的衍生物恰好可以进入葫芦[6]的空腔可知,4—甲基苯甲醛可进入葫芦[6]脲的空腔,故D正确;
故选D。
11.D
【详解】A.由图可知,合成ESCAP的单体为,故其中一种单体为苯乙烯,故A正确;
B.曝光时ESCAP支链上酯基发生取代反应生成羧基和羟基,羟基又发生消去反应生成碳碳双键得到,故发生了取代反应和消去反应,故B正确;
C.X中含有羧基,故其酸性比ESCAP的酸性强,故C正确;
D.Y分子中碳碳双键两端的基团相同,不存在顺反异构,故D错误;
答案选D。
12.C
【详解】A.氯乙烷只有1种结构,不存在同分异构体,故A错误;
B.聚乙烯和聚丙烯的聚合度n值为不确定值,都属于混合物,不可能互为同系物,故B错误;
C.由结构简式可知,聚碳酸酯属于聚酯类高分子化合物,可通过缩聚反应制得,故C正确;
D.由结构简式可知,合成高分子化合物的单体为对苯二甲酸和对苯二胺,两种单体的核磁共振氢谱峰数相同,但羧基和氨基的氢原子数目不同,所以峰面积不同,故D错误;
故选C。
13.B
【详解】A.脱落酸的分子式为C15H20O4,A项错误;
B.脱落酸含有碳碳双键,可发生加聚反应;含有羧基和羟基,可发生缩聚反应,B项正确;
C.羧基不能和H2发生加成反应,1 mol脱落酸最多可与4 mol氢气发生加成反应,C项错误;
D.脱落酸分子中含有3个碳碳双键,其中右侧的2个双键通过一个碳碳单键连接,具有共轭二烯烃的性质,则脱落酸分子与等物质的量的Br2加成的产物有4种(不考虑顺反异构),D项错误。
答案选B。
14.B
【详解】A.由单体和通过缩聚反应生成,聚合物分子内含有酰胺基,故A正确;
B.单体为乙炔,含碳碳三键,能与溴单质发生加成反应,从而使溴水褪色,故B错误;
C.由结构可知的单体为:CH2=CH CH=CH2和,两者通过加聚反应生成消声瓦,故C正确;
D.合金中存在金属键,故D正确;
故选:B。
15.B
【详解】A.单体的相对分子质量为68,则聚合度等于,选项A正确;
B.ABS的单体之一是丁二烯,分子式为C4H6,与乙炔的最简式不相同,其碳的百分含量和乙炔不相同,选项B错误;
C.PC是一种可降解的聚碳酸酯类高分子材料,选项C正确;
D.亚克力材料的单体是,名称为甲基丙烯酸甲酯,能使溴水褪色,选项D正确;
答案选B。
16.(1) 圆底烧瓶 CH3CH2OHCH2=CH2↑+H2O
(2) 除去乙烯中混有的SO2、CO2等酸性气体 品红溶液不褪色,酸性KMnO4溶液紫色褪去
(3) 氧化反应 HOCH2CH2OH
(4)42%
(5)nHOCH2COOH+(n-1)H2O
【分析】I.乙醇与浓硫酸反应生成乙烯的同时浓H2SO4易将乙醇氧化为C或CO和CO2,浓H2SO4被还原为SO2,乙烯具有还原性,可根据酸性KMnO4溶液褪色来证明有乙烯生成,由于SO2也具有还原性,能使酸性KMnO4溶液褪色,会干扰乙烯的检验,所以检验乙烯之前必须除净SO2,则NaOH溶液的作用是除去乙烯中混有的SO2、CO2等酸性气体,品红溶液可检验是否除净。
II.由合成路线可知,乙烯催化氧化生成环氧乙烷,环氧乙烷和水反应得到C,C发生催化氧化得到乙二醛,可推知C为乙二醇,乙二醛先与浓NaOH作用,再酸化得到羟基乙酸。
【详解】(1)由仪器构造可知,仪器a的名称是圆底烧瓶,实验室用乙醇与浓硫酸加热到170反应生成乙烯和水,反应的化学方程式为CH3CH2OHCH2=CH2↑+H2O,故答案为:圆底烧瓶;CH3CH2OHCH2=CH2↑+H2O;
(2)由分析可知,制取乙烯时同时生成了SO2、CO2等酸性气体,为防止干扰乙烯的检验,用NaOH溶液除去乙烯中混有的SO2、CO2等酸性气体;乙烯和二氧化硫都能使酸性KMnO4溶液褪色,所以能证明该装置中有乙烯生成的实验现象是品红溶液不褪色,排除的干扰,酸性KMnO4溶液紫色褪去,故答案为:除去乙烯中混有的SO2、CO2等酸性气体;品红溶液不褪色,酸性KMnO4溶液紫色褪去;
(3)有机物加氧去氢的反应为氧化反应,A→B过程中为加氧反应,故反应类型是氧化反应,由分析可知,乙二醇催化氧化生成乙二醛,则有机物C为乙二醇,结构简式为HOCH2CH2OH,故答案为:氧化反应;HOCH2CH2OH;
(4)由转化关系可知,理论上乙烯反应得到等物质的量的羟基乙酸,则用7t乙烯生产羟基乙酸,理论上得到羟基乙酸的质量为76=19t,则该流程的总产率为100%=42%,故答案为:42%。
(5)羟基乙酸分子中含有羟基和羧基,在一定条件下发生缩聚反应生成高聚物,反应的化学方程式为nHOCH2COOH+(n-1)H2O故答案为:nHOCH2COOH+(n-1)H2O。
17. 直形冷凝管 甲醛和氨基乙酸酯的配比为1.00、温度为80℃ 干燥有机物 nNC—CH2—COOCH2CH2CH2CH3+nHCHO+nH2O ad
【分析】氰基乙酸酯(NC—CH2—COOR)和甲醛在碱催化下发生聚合反应生成和水,,再裂解得到最终产物。
【详解】(1)根据仪器构造可知,图2中的仪器a名称为直形冷凝管。
(2)根据图3可知,当甲醛和氨基乙酸酯的物质的量之比为1.00、温度为80℃时,收率最高,所以制备该医用胶单体的最佳条件为甲醛和氨基乙酸酯的配比为1.00、温度为80℃。
(3)发生第一步反应时生成了水,步骤3中加入五氧化二磷的目的是除去中间产物中的水。
(4)根据核磁共振氢谱图(H-NMR)可知,该医用胶单体有6种不同化学环境的氢原子,个数比为1:1:2:2:2:3,所以该有机物的结构简式为。
(5)步骤1是氰基乙酸丁酯(NC—CH2—COOCH2CH2CH2CH3)和甲醛在碱催化下发生聚合反应,发生反应的化学方程式为:nNC—CH2—COOCH2CH2CH2CH3+nHCHO+nH2O。
(6)氰基能发生水解生成羧基,所以可以用稀盐酸和湿润湿润的蓝色石蕊试纸检验医用胶单体中的氰基,故选用的实验用品是ad。
18.(1)CH4(g) + 2H2O(g) =CO2(g) + 4H2(g) H = +165.2kJ·mol-1
(2) a 适当加压。加压能使该反应速率增大、原料转化率升高,也会增加设备和动力成本 降温冷凝得到液态甲醇粗品再蒸馏提纯
(3) 正
【详解】(1)根据盖斯定律,将两个热化学方程式加起来得:CH4(g)+2H2O(g)=CO2(g)+4H2(g) H=+165.2kJ·mol-1;
(2)①两个反应都是放热反应,合成反应器出口样品的温度更高一些,故选a;
②两个反应都是气体体积减小的反应,从平衡的角度来看,增大压强,能使该反应速率增大、原料转化率升高,但是压强高,意味着设备要好,这就需要加大成本的投入,因此需要适当加压;
③CO和H2生成二甲醚的化学方程式为:2CO+4H2CH3OCH3+H2O;
④题中给出了几个物质的沸点,甲醇的沸点较高,且和其他物质的沸点相差较大,可以通过降温冷凝的方法得到甲醇粗品,再经过蒸馏提纯;
(3)①根据燃料电池的构造,通入O2的一侧是燃料电池的正极;
②结合题中给出的化学方程式,可以推出另外两种单体分别为: 、 。
19.(1) 溴水 浓溴水or三氯化铁溶液or水or碳酸氢钠溶液 +2CH3CH2OH +2H2O
(2) 羟基和醛基 3 取样,加入新制氢氧化铜,加热,有砖红色沉淀生成
(3)
(4) 保护酚羟基,防止其被KMnO4(H+)氧化 NaHCO3
【详解】(1)甲苯和烯烃在常温下可以通过加入溴水进行鉴别,能使溴水褪色的是烯烃;③中含有羟基和羧基,⑤中含有酚羟基,加入碳酸氢钠,可以产生气泡的说明含有羧基;加入浓溴水,产生白色沉淀的说明含有酚羟基;加入三氯化铁溶液变成紫色的,说明有酚羟基;③与乙醇发生酯化反应;
故答案为:溴水;浓溴水或三氯化铁溶液或碳酸氢钠溶液; +C2H5OH +2H2O;
(2)④中的含氧官能团为羟基和醛基;⑤中因含有苯环,1个苯环能与3个H2发生加成反应;检验醛基可以通过加入新制的氢氧化铜并加热,观察是否有砖红色沉淀生成;
故答案为:羟基和醛基;3;取样,加入新制氢氧化铜,加热,有砖红色沉淀生成;
(3)⑤与丙酮发生缩聚反应,生成 ;
故答案为: ;
(4)①酚羟基具有还原性,通过对比物质的结构式可知,反应(1)和反应(3)的目的为保护酚羟基,防止其被KMnO4(H+)氧化;
故答案为:保护酚羟基,防止其被KMnO4(H+)氧化;
②羧基与碳酸氢钠反应生成羧酸钠,故需要加碳酸氢钠;
故答案为:碳酸氢钠。
答案第1页,共2页
答案第1页,共2页
