专题4第一单元醇和酚同步练习 (含解析)2022——2023学年下学期高二化学苏教版(2019)选择性必修3
文档属性
| 名称 | 专题4第一单元醇和酚同步练习 (含解析)2022——2023学年下学期高二化学苏教版(2019)选择性必修3 |

|
|
| 格式 | docx | ||
| 文件大小 | 1.3MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-06-22 00:00:00 | ||
图片预览



文档简介
专题4第一单元醇和酚同步练习
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1.A、B、C三种醇分别与足量的金属钠完全反应,在相同条件下产生相同的体积H2,消耗这三种醇的物质的量之比为3:6:2,则A、B、C三种醇分子中所含羟基的个数之比为
A.3:2:1 B.2:6:3 C.3:1:2 D.2:1:3
2.有机物分子中的原子(团)之间会相互影响,导致相同的原子(团)表现不同的性质。下列各项事实不能说明上述观点的是
A.甲苯能使高锰酸钾酸性溶液褪色,而甲基环己烷不能使高锰酸钾酸性溶液褪色
B.苯酚可以与NaOH反应,而乙醇不能与NaOH反应
C.乙烯能与溴水发生加成反应,而乙烷不能发生加成反应
D.苯酚与溴水可直接反应,而苯与液溴反应则需要FeBr3作催化剂
3.某种聚碳酸酯的透光性好,可制成车、船的挡风玻璃,以及眼镜镜片、光盘等,其结构可表示为: ,原来合成聚碳酸酯的一种原料是有毒的光气(,又称碳酰氯)。为贯彻绿色化学理念,可以改用碳酸二甲酯()与什么缩合聚合生产聚碳酸酯
A.二卤化物 B.二酚类物质 C.二醇类物质 D.二烯类物质
4.某实验小组学习了乙醇的化学性质后,在老师的指导下设计了如下实验验证课堂所学的乙醇的化学性质。下列说法错误的是
A.甲、乙烧杯中均为78℃以上的热水 B.铜网降低了乙醇和氧气反应的活化能
C.试管a中得到的溶液可能使锌粒溶解 D.铜网上出现红色和黑色交替现象
5.我国科研人员发现中药成分黄芩素能明显抑制新冠病毒的活性。下列关于黄芩素的说法不正确的是
A.能和Br2发生取代反应和加成反应 B.能与Na2CO3溶液反应
C.在空气中可发生氧化反应 D.分子中有3种官能团
6.金合欢醇广泛应用于多种香型的香精中,其结构简式如图所示。下列说法不正确的是
A.金合欢醇与乙醇互为同系物
B.金合欢醇既可发生加成反应,又可发生取代反应
C.1 mol金合欢醇能与3 mol H2发生加成反应,也能与3 mol Br2发生加成反应
D.1 mol金合欢醇与足量Na反应生成0.5 mol H2
7.乙醇分子中的各种化学键如图所示,关于乙醇在各种反应中断裂键的说法不正确的是
A.和金属钠反应时键①断裂
B.与卤化氢反应时断裂②键
C.在铜催化共热下与O2反应时断裂①和②键
D.在空气中完全燃烧时断裂①②③④⑤键
8.能与金属钠反应,并放出氢气的有机物是
A. B.
C. D.
9.五倍子是一种常见的中草药,其有效成分为X,在一定条件下X可分别转化为Y、Z。
下列说法正确的是
A.1 mol Z最多能与7 mol NaOH发生反应
B.1 mol X最多能与2 mol Br2发生取代反应
C.Y分子结构中所有碳原子共平面
D.Y不能发生消去反应
10.中药莪术有行气破血,消积止痛之功效,莪术二醇是莪术挥发油主要成分之一,其结构简式如图。下列说法错误的是
A.莪术二醇的分子式为
B.莪术二醇可以使酸性溶液变色
C.莪术二醇含有两个醇羟基可以催化氧化得到二元醛
D.一定条件下莪术二醇可发生加聚反应得到高聚物
11.生漆涂在物品表面,在空气中干燥时会产生漆膜。漆酚是生漆的主要化学成分,某种漆酚的结构简式为:
漆酚不具有的化学性质是
A.可与烧碱溶液反应 B.可与溴水发生取代反应
C.可与酸性溶液反应 D.可与溶液反应放出二氧化碳
12.有机化合物分子中基团之间的相互影响会导致物质化学性质的不同。下列事实中,不能说明上述观点的是
A.甲苯能使酸性溶液褪色,而苯和甲烷不能使酸性溶液褪色
B.乙烯能发生加成反应,而乙烷不能发生加成反应
C.苯酚能与溶液反应,而乙醇不能与溶液反应
D.苯酚苯环上的氢原子比苯分子中的氢原子更容易被卤素原子取代
13.某物质可溶于水、乙醇,熔点为209.5℃,其分子的结构简式如图所示,下列说法不正确的是
A.该分子易溶于水、乙醇,可能是因为他们结构相似
B.该分子中含有大π键
C.该分子中只含有1个手性碳原子
D.该分子中所有C原子可能在同一平面
14.下列物质属于酚类的是
A. B.
C. D.
15.氯乙烷(沸点:12.5℃,熔点:-138.7℃)有如图转化关系:
氯乙烷乙醇乙醛;
设NA表示阿伏加德罗常数的值。下列叙述正确的是
A.标准状况下,22.4 L氯乙烷所含分子数为NA
B.25℃时,1.0 mol·L-1的NaOH溶液中阴阳离子总数为2NA
C.若有46 g乙醇转化为乙醛时,乙醇得到的电子数为2NA
D.若38 g乙醛和甲醇的混合物中含有4 g氢元素,则碳原子数目为1.5NA
二、实验题
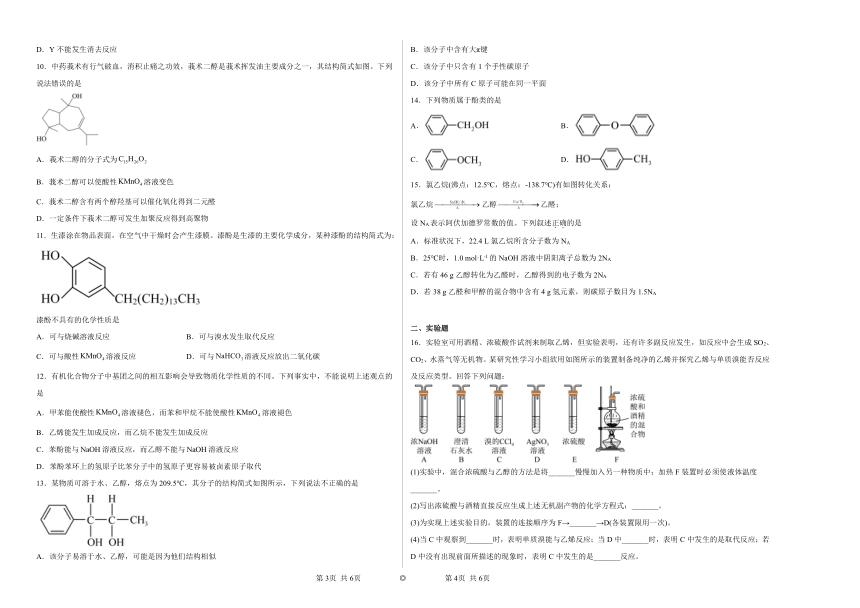
16.实验室可用酒精、浓硫酸作试剂来制取乙烯,但实验表明,还有许多副反应发生,如反应中会生成SO2、CO2、水蒸气等无机物。某研究性学习小组欲用如图所示的装置制备纯净的乙烯并探究乙烯与单质溴能否反应及反应类型。回答下列问题:
(1)实验中,混合浓硫酸与乙醇的方法是将_______慢慢加入另一种物质中;加热F装置时必须使液体温度_______。
(2)写出浓硫酸与酒精直接反应生成上述无机副产物的化学方程式:_______。
(3)为实现上述实验目的,装置的连接顺序为F→_______→D(各装置限用一次)。
(4)当C中观察到_______时,表明单质溴能与乙烯反应;当D中_______时,表明C中发生的是取代反应;若D中没有出现前面所描述的现象时,表明C中发生的是_______反应。
(5)关于浓硫酸和乙醇混合加热制取乙烯的实验装置F中,下列说法正确的个数有_______个。
①浓硫酸的作用是作催化剂
②在反应容器中放入几片碎瓷片防止混合液暴沸
③圆底烧瓶中装的是乙醇和3mol·L-1H2SO4的混合液
④温度计应插入反应溶液液面下,以便控制温度
⑤若出口出来的气体能使酸性KMnO4溶液褪色,说明有乙烯生成
⑥反应过程中溶液的颜色会逐渐变黑
⑦生成的乙烯气体中混有带刺激性气味的气体
17.溴乙烷是一种重要的有机合成原料,为无色液体,难溶于水,沸点,熔点,密度。某实验小组用下图所示装置制取溴苯和溴乙烷。
主要实验步骤如下:
①检查装置的气密性后,向装置A中加入一定量的苯和液溴。
②向B处锥形瓶中加入乙醇和浓的混合液至浸没导管口。
③将A装置中的纯铁丝小心向下插入混合液中。
④点燃B装置中的酒精灯,用小火缓缓对锥形瓶加热10min。回答下列问题:
(1)仪器a的名称_______。装置A中生成的有机产物结构简式为_______。
(2)已知B装置中主要反应的反应类型为取代反应,其化学方程式为_______。浓硫酸的作用是_______。
(3)C装置中U形管浸在冰水中的目的是_______。
(4)步骤④中不能用大火加热,理由是_______。
三、工业流程题
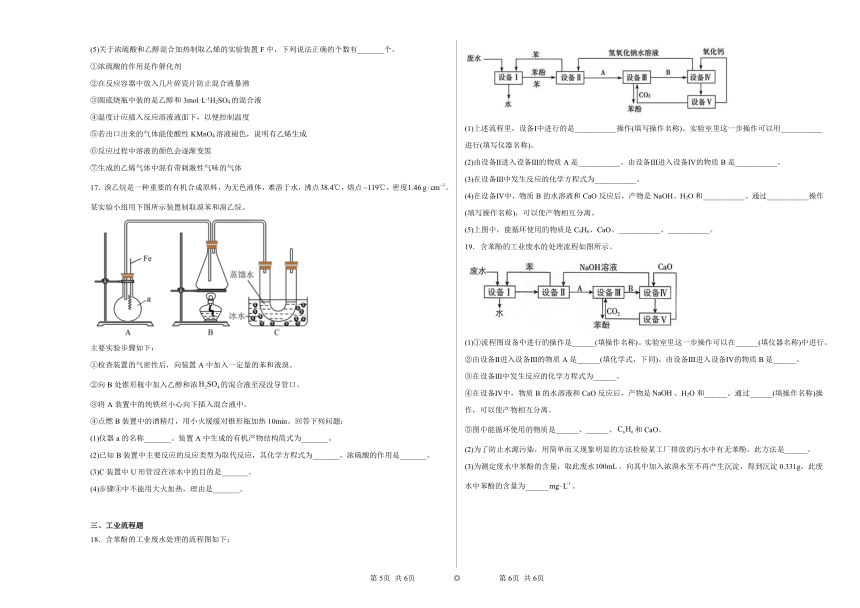
18.含苯酚的工业废水处理的流程图如下:
(1)上述流程里,设备Ⅰ中进行的是___________操作(填写操作名称)。实验室里这一步操作可以用___________进行(填写仪器名称)。
(2)由设备Ⅱ进入设备Ⅲ的物质A是___________。由设备Ⅲ进入设备Ⅳ的物质B是___________。
(3)在设备Ⅲ中发生反应的化学方程式为___________。
(4)在设备Ⅳ中,物质B的水溶液和CaO反应后,产物是NaOH、H2O和___________。通过___________操作(填写操作名称),可以使产物相互分离。
(5)上图中,能循环使用的物质是C6H6、CaO、___________、___________。
19.含苯酚的工业废水的处理流程如图所示。
(1)①流程图设备中进行的操作是______(填操作名称)。实验室里这一步操作可以在______(填仪器名称)中进行。
②由设备Ⅱ进入设备Ⅲ的物质A是______(填化学式,下同)。由设备Ⅲ进入设备Ⅳ的物质B是______。
③在设备Ⅲ中发生反应的化学方程式为______。
④在设备Ⅳ中,物质B的水溶液和CaO反应后,产物是、H2O和______。通过______(填操作名称)操作,可以使产物相互分离。
⑤图中能循环使用的物质是______、______、和CaO。
(2)为了防止水源污染,用简单而又现象明显的方法检验某工厂排放的污水中有无苯酚,此方法是______。
(3)为测定废水中苯酚的含量,取此废水,向其中加入浓溴水至不再产生沉淀,得到沉淀0.331g,此废水中苯酚的含量为______。
第1页 共4页 ◎ 第2页 共4页
第1页 共4页 ◎ 第2页 共4页
参考答案:
1.D
【详解】相同条件下相同体积的氢气的物质的量相等,设生成氢气6mol,根据2-OH~2Na~H2↑可知参加反应的羟基均为12mol,三种醇的物质的量之比为3:6:2,故A、B、C三种分子里羟基数目之比为=2:1:3。
故选D。
2.C
【详解】A.甲苯中由于苯环对甲基的影响,使甲苯中甲基易被高锰酸钾酸性溶液氧化,而甲基环己烷不能,可说明原子与原子团间的相互影响导致物质的化学性质不同,A与题意不符;
B.苯酚中由于苯环对羟基的影响,使羟基中氢原子更易电离,表现出弱酸性,乙醇为中性,-OH连接的烃基不同,可说明原子与原子团间的相互影响导致物质的化学性质不同,B与题意不符;
C.乙烯含有碳碳双键,能与溴水发生加成反应,乙烷属于烷经,不含不饱和结构,不能发生加成反应,性质不同是由于官能团不同,与原子团的影响无关,C符合题意;
D.苯酚中由于羟基对苯环的影响,使苯酚分子中处于羟基邻、对位的苯环氢原子更活泼,更易被取代,可说明原子与原子团间的相互影响导致物质的化学性质不同,D与题意不符;
答案选C。
3.B
【详解】由结构简式可知,碳酸二甲酯一定条件下能与 发生缩聚反应生成聚碳酸酯, 分子中含有2个酚羟基,属于二酚类物质,故选B。
4.A
【分析】该实验的原理为在铜的催化作用下,乙醇被氧气氧化成乙醛,乙醛可能继续被氧化成乙酸。甲烧杯内是高于乙醇沸点的热水,目的是使乙醇汽化,然后和氧气按照一定体积比混合,在硬质玻璃管中,铜被氧化成黑色CuO,CuO被乙醇还原成Cu,总体上铜作催化剂,降低了乙醇被氧气氧化成乙醛的活化能。反应生成的乙醛(可能含有乙酸及未被氧化的乙醇)进入置于乙烧杯冷水中的试管a中被冷凝,得到含有乙醛、可能含有乙酸及未被氧化的乙醇的溶液,乙酸和活泼金属Zn能反应;
【详解】A.甲烧杯内是高于乙醇沸点的热水,乙烧杯冷水,选项A错误;
B.铜网降低了乙醇和氧气反应的活化能,选项B正确;
C.反应生成的乙醛,可能含有乙酸,进入置于乙烧杯冷水中的试管a中可能使锌粒溶解,选项C正确;
D.铜被氧化成黑色CuO,CuO被乙醇还原成Cu,出现红色和黑色交替现象,选项D正确;
答案选A。
5.D
【详解】A.该分子中含有酚羟基的邻对位易与溴发生取代反应,而分子中C=C易于溴发生加成反应,A项正确;
B.酚羟基能表现酸性,可以与Na2CO3反应生成酚钠和NaHCO3,B项正确;
C.酚羟基在空气中易被氧化,C项正确;
D.分子中的官能团为酚羟基、羰基、醚键、碳碳双键,D项错误;
故选D。
6.A
【详解】A.乙醇为饱和一元醇,而金合欢醇分子中含有碳碳双键,二者的结构不相似,所以不是同系物,故A错误;
B.金合欢醇分子中含有碳碳双键可发生加成反应,同时含有羟基,所以能发生取代反应,故B正确;
C.金合欢醇含有3个碳碳双键,所以1 mol金合欢醇能与3 mol H2发生加成反应,也能与3 mol Br2发生加成反应,故C正确;
D.金合欢醇分子中含有3个碳碳双键,醇羟基与产生H2的物质的量之比为2∶1,故D正确;
故选A。
7.C
【详解】A.乙醇与钠反应生成乙醇钠,是羟基中的O—H键断裂,A项正确;
B.乙醇与卤化氢反应时生成卤代烃,断裂②化学键,B项正确,
C.乙醇催化氧化成乙醛时,断裂①和③化学键,C项错误;
D.乙醇完全燃烧时生成二氧化碳和水,化学键①②③④⑤全部断裂,D项正确;
故选C。
8.B
【详解】A.水是无机物,故A不符合题意;
B.甲醇是有机物,含有羟基和钠生成氢气,故B符合题意;
C.乙醛和钠不反应,故C不符合题意;
D.乙酸甲酯和钠不反应,故D不符合题意;
故选B。
9.B
【详解】A.1 mol Z中含有5 mol酚羟基、1 mol羧基、1 mol酚酯基,1 mol酚酯基可消耗2 mol NaOH,故1 mol Z最多能与8 mol NaOH发生反应,A项错误;
B.X中苯环上有2个氢原子处于酚羟基的邻位,1 mol X最多能与2 mol Br2发生取代反应,B项正确;
C.Y分子中碳原子构成的六元环不是苯环,所有碳原子不能共平面,C项错误;
D.Y分子中与羟基相连碳原子的相邻碳原子上有氢原子,能发生消去反应,D项错误;
故答案为:B。
10.C
【详解】A.由其结构简式可知莪术二醇的分子式为,故A正确;
B.由其结构简式可知其含有官能团醇羟基,具有还原性,含有碳碳双键,极易被氧化,酸性溶液具有强氧化性,两者发生氧化还原反应,故莪术二醇可以使酸性溶液变色,故B正确;
C.只有与羟基相连的碳原子上有两个氢原子时,羟基才能氧化成醛基,而莪术二醇羟基相连的碳原子上并没有氢原子,则莪术二醇含有两个醇羟基不能被催化氧化,故C错误;
D.由其结构简式可知该分子含有碳碳双键,在一定条件下可发生加聚反应,在一定条件下莪术二醇可发生加聚反应得到高聚物,故D正确;
故答案为C。
11.D
【详解】A.该有机物中的羟基直接连在苯环上,属于酚类化合物,具有酸性,能与烧碱溶液发生中和反应,故A不符合题意;
B.该有机物属于酚,能与溴水发生取代反应,故B不符合题意;
C.该有机物含有羟基且苯环有烃基的侧链,都能被酸性高锰酸钾溶液氧化,故C不符合题意;
D.酚具有酸性,但其酸性比碳酸的酸性弱,因此该有机物不能与碳酸氢钠溶液反应,故D符合题意;
故选D。
12.B
【详解】A.苯和甲烷不能使酸性溶液褪色,甲基连接在苯环上,可被氧化,说明苯环对甲基影响,能说明上述观点,故A不选;
B.因为乙烯的结构中含有碳碳双键,能与氢气发生加成反应,而烷烃中则没有,是自身的官能团性质,不是原子团间的相互影响导致的化学性质,故B选;
C.受苯环的影响,苯酚中的羟基氢原子变得比较活泼,所以苯酚能与NaOH溶液反应,而乙醇不能,是有机物分子中基团间的相互影响会导致化学性质不同,故C不选;
D.苯酚苯环上的氢比苯分子中的氢更容易被卤原子取代,说明苯酚苯环上H原子更活泼,说明酚-OH对苯环的影响,故D不选;
故选B。
13.C
【详解】A.由结构简式可知,该有机物与水、乙醇都是极性分子,由相似相溶原理可知,该分子易溶于水、乙醇,故A正确;
B.由结构简式可知,有机物分子含有苯环,苯环中含有大π键,故B正确;
C.由结构简式可知,有机物分子与羟基相连的2个碳原子都是连有4个不同原子或原子团的手性碳原子,故C错误;
D.苯环是平面结构,苯环上的碳原子和与苯环相连的碳原子共平面,由三点成面的原理可知,该分子中所有碳原子可能在同一平面,故D正确;
故选C。
14.D
【详解】A.的羟基连接在测链上,属于芳香醇,名称为苯甲醇,A不符合题意;
B.中2个苯基通过O原子相连,该物质属于醚,B不符合题意;
C.O原子分别连接苯基、甲基,属于醚,C不符合题意;
D.中羟基与苯环直接相连,属于酚,D符合题意;
故合理选项是D。
15.D
【分析】氯乙烷转化为乙醇的反应为;乙醇转化为一圈的反应为;
【详解】A.标准状况下,氯乙烷为液态,不能用进行计算,故A错误;
B.根据,NaOH溶液的体积未知,无法计算NaOH的量,故B错误;
C.对于反应,乙醇被氧化,失去电子,转移电子总数为4,若有46 g乙醇转化为乙醛时,乙醇失去的电子数为,故C错误;
D.设,,则根据题意有,,解得,,则38 g乙醛和甲醇的混合物中碳原子数目为,故D正确;
故选D。
16.(1) 浓硫酸 迅速升到170℃
(2)CH3CH2OH+6H2SO4(浓)=2CO2↑+6SO2↑+9H2O
(3)A→B→E→C
(4) 溶液褪色 有淡黄色沉淀生成 加成
(5)4
【分析】装置F是乙醇和浓H2SO4在170℃下反应制备乙烯,生成的乙烯气体中会混有SO2、CO2、乙醇蒸汽等物质,为实现实验目的,应用装置A中的NaOH溶液除去SO2、CO2,并用装置B中的澄清石灰水检验是否除尽,然后用装置E中的浓硫酸干燥,得到纯净干燥的乙烯,乙烯通入装有溴的CCl4溶液的装置C中,探究乙烯与单质溴能否反应,最后用装置D验证是否有HBr产生,以确定反应类型。
【详解】(1)混合浓硫酸与乙醇,与稀释浓硫酸相似,应将浓硫酸缓慢加入乙醇中,边加边搅拌;为了避免副反应发生,加热时应使溶液迅速升温到170 ℃;
(2)浓硫酸具有强氧化性,加热条件下,乙醇可与浓硫酸反应生成CO2、SO2等物质,其化学方程式为CH3CH2OH+6H2SO4(浓)=2CO2↑+6SO2↑+9H2O;
(3)为实现上述实验目的,应用装置A中的NaOH溶液除去SO2、CO2,并用装置B中的澄清石灰水检验是否除尽,然后用装置E中的浓硫酸干燥,得到纯净干燥的乙烯,乙烯通入装有溴的CCl4溶液的装置C中,探究乙烯与单质溴能否反应,最后用装置D验证是否有HBr产生,以确定反应类型,故装置的连接顺序为F→A→B→E→C→D;
(4)当C中观察到溴的CCl4溶液褪色时,乙烯与单质溴之间可能发生加成反应,也可能发生取代反应;若是取代反应,则会有HBr生成,HBr遇AgNO3溶液会产生淡黄色沉淀,若D中没有出现前面所描述的现象时,表明C中发生的是加成反应;
(5)①.浓硫酸的作用是催化剂、脱水剂,故错误;
②.在反应容器中放入几片碎瓷片是防止混合液暴沸,故正确;
③.圆底烧瓶中装的是乙醇和浓H2SO4的混合液,故错误;
④.需要控制溶液的温度为170℃,所以温度计应插入反应溶液液面下,以便控制温度,故正确;
⑤.乙烯、SO2、乙醇蒸汽等都能使酸性KMnO4溶液褪色,不能说明有乙烯生成,故错误;
⑥.制备乙烯时,伴随有乙醇和浓硫酸的氧化还原反应,由于生成黑色的C单质,溶液的颜色会逐渐变黑,故正确;
⑦.制备乙烯时,伴随有乙醇和浓硫酸的氧化还原反应,生成带刺激性气味的SO2气体,故正确;
故说法正确的个数有4个。
17.(1) 圆底烧瓶
(2) 催化剂
(3)收集溴乙烷
(4)易发生副反应生成乙醚、乙烯等
【分析】A装置中铁与溴发生反应生成溴化铁,溴化铁作为催化剂催化溴与苯的反应,其中生成的溴化氢和挥发的溴单质通过导管a进入到装置B中与乙醇发生取代反应,由溴乙烷数据可知,在冰水浴中溴乙烷液化,故装置C为溴乙烷的收集装置,装置C底部用蒸馏水液封,作用是吸收生成的溴化氢;
【详解】(1)仪器a的名称是圆底烧瓶;装置A中铁与溴发生反应生成溴化铁,溴化铁作为催化剂催化溴与苯反应生成溴苯,生成的有机产物结构简式为;
(2)生成的溴化氢和挥发的溴单质通过导管a进入到装置B中与乙醇发生取代反应,反应方程式为;浓硫酸的作用是催化剂;
(3)C装置中U形管浸在冰水中的目的是收集溴乙烷;
(4)在温度较高的情况下浓H2SO4存在条件下发生副反应生成乙醚、乙烯等,故答案为:易发生副反应生成乙醚、乙烯等。
18.(1) 萃取、分液 分液漏斗
(2) C6H5ONa NaHCO3
(3)C6H5ONa+CO2+H2O→C6H5OH+NaHCO3
(4) CaCO3 过滤
(5) NaOH溶液 CO2
【分析】由流程图和每一步新加的试剂进行分析可知:用苯萃取出设备Ⅰ中的苯酚进入设备Ⅱ,然后用NaOH溶液将设备Ⅱ中的苯酚转化为苯酚钠而进入设备Ⅲ,向设备Ⅲ中通入CO2将苯酚钠转化为苯酚,同时生成NaHCO3而进入设备Ⅳ,向设备Ⅳ中加入CaO时,生成CaCO3进入设备Ⅴ,NaOH进入设备Ⅱ循环使用。
【详解】(1)根据上述分析,设备Ⅰ中进行的是萃取、分液,实验室里这一步操作可以用分液漏斗进行;
(2)根据上述分析,由设备Ⅱ进入设备Ⅲ的物质A是苯酚钠,由设备Ⅲ进入设备Ⅳ的物质B是NaHCO3;
(3)根据上述分析,在设备Ⅲ中发生反应的化学方程式为C6H5ONa+CO2+H2O→C6H5OH+NaHCO3;
(4)在设备Ⅳ中,物质B的水溶液和CaO反应后,产物是NaOH、H2O和CaCO3,CaCO3难溶于水,通过过滤,可以使产物相互分离;
(5)上图中,能循环使用的物质是C6H6、CaO、NaOH溶液、CO2。
19. 萃取、分液 分液漏斗 过滤 溶液 向污水中滴加溶液,若溶液呈紫色,则表明污水中有苯酚 940
【分析】由流程可知,设备I中中含有苯和工业废水,可经萃取、分液得到苯酚的苯溶液混合物,进入设备Ⅱ;设备Ⅱ中加入溶液,可得到苯酚钠溶液;在设备Ⅲ中通入,分离出苯酚;在设备Ⅳ中主要物质是,溶液中加入,可生成、、,通过过滤操作分离出;在设备V中高温分解可得和,据此分析解答。
【详解】(1)①设备I中废水和苯混合后分离出水,进行的操作是萃取、分液,实验室中可以用分液漏斗进行分液操作,故答案为:萃取、分液;分液漏斗;
②设备Ⅱ中向苯酚和苯的混合液中加入NaOH溶液,目的是分离出苯,故物质A是苯酚钠溶液;在设备Ⅲ中通入CO2,分离出苯酚,故物质B是NaHCO3溶液;故答案为:;NaHCO3;
③在盛有苯酚钠溶液的设备Ⅲ中,通入过量的二氧化碳气体,发生反应生成苯酚和碳酸氢钠,反应的化学方程式为,故答案为:;
④在设备Ⅳ中向NaHCO3溶液中加入CaO,生成NaOH、H2O、CaCO3,可通过过滤操作分离出CaCO3,故答案为:CaCO3;过滤;
⑤在设备V中CaCO3高温分解可得CO2和CaO,所以图中能循环使用的物质是NaOH溶液、CO2、C6H6和CaO,故答案为:NaOH溶液;CO2;
(2)苯酚和氯化铁溶液之间会发生显色反应,向溶液中滴加氯化铁溶液,若溶液呈紫色,则表明污水中有苯酚,故答案为:向污水中滴加FeCl3溶液,若溶液呈紫色,则表明污水中有苯酚;
(3) )设每升废水中含苯酚,
,根据反应关系可知:94:331=xg:0.331g,解得,所以此废水中苯酚的含量为:==,故答案为:940。
答案第1页,共2页
答案第1页,共2页
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1.A、B、C三种醇分别与足量的金属钠完全反应,在相同条件下产生相同的体积H2,消耗这三种醇的物质的量之比为3:6:2,则A、B、C三种醇分子中所含羟基的个数之比为
A.3:2:1 B.2:6:3 C.3:1:2 D.2:1:3
2.有机物分子中的原子(团)之间会相互影响,导致相同的原子(团)表现不同的性质。下列各项事实不能说明上述观点的是
A.甲苯能使高锰酸钾酸性溶液褪色,而甲基环己烷不能使高锰酸钾酸性溶液褪色
B.苯酚可以与NaOH反应,而乙醇不能与NaOH反应
C.乙烯能与溴水发生加成反应,而乙烷不能发生加成反应
D.苯酚与溴水可直接反应,而苯与液溴反应则需要FeBr3作催化剂
3.某种聚碳酸酯的透光性好,可制成车、船的挡风玻璃,以及眼镜镜片、光盘等,其结构可表示为: ,原来合成聚碳酸酯的一种原料是有毒的光气(,又称碳酰氯)。为贯彻绿色化学理念,可以改用碳酸二甲酯()与什么缩合聚合生产聚碳酸酯
A.二卤化物 B.二酚类物质 C.二醇类物质 D.二烯类物质
4.某实验小组学习了乙醇的化学性质后,在老师的指导下设计了如下实验验证课堂所学的乙醇的化学性质。下列说法错误的是
A.甲、乙烧杯中均为78℃以上的热水 B.铜网降低了乙醇和氧气反应的活化能
C.试管a中得到的溶液可能使锌粒溶解 D.铜网上出现红色和黑色交替现象
5.我国科研人员发现中药成分黄芩素能明显抑制新冠病毒的活性。下列关于黄芩素的说法不正确的是
A.能和Br2发生取代反应和加成反应 B.能与Na2CO3溶液反应
C.在空气中可发生氧化反应 D.分子中有3种官能团
6.金合欢醇广泛应用于多种香型的香精中,其结构简式如图所示。下列说法不正确的是
A.金合欢醇与乙醇互为同系物
B.金合欢醇既可发生加成反应,又可发生取代反应
C.1 mol金合欢醇能与3 mol H2发生加成反应,也能与3 mol Br2发生加成反应
D.1 mol金合欢醇与足量Na反应生成0.5 mol H2
7.乙醇分子中的各种化学键如图所示,关于乙醇在各种反应中断裂键的说法不正确的是
A.和金属钠反应时键①断裂
B.与卤化氢反应时断裂②键
C.在铜催化共热下与O2反应时断裂①和②键
D.在空气中完全燃烧时断裂①②③④⑤键
8.能与金属钠反应,并放出氢气的有机物是
A. B.
C. D.
9.五倍子是一种常见的中草药,其有效成分为X,在一定条件下X可分别转化为Y、Z。
下列说法正确的是
A.1 mol Z最多能与7 mol NaOH发生反应
B.1 mol X最多能与2 mol Br2发生取代反应
C.Y分子结构中所有碳原子共平面
D.Y不能发生消去反应
10.中药莪术有行气破血,消积止痛之功效,莪术二醇是莪术挥发油主要成分之一,其结构简式如图。下列说法错误的是
A.莪术二醇的分子式为
B.莪术二醇可以使酸性溶液变色
C.莪术二醇含有两个醇羟基可以催化氧化得到二元醛
D.一定条件下莪术二醇可发生加聚反应得到高聚物
11.生漆涂在物品表面,在空气中干燥时会产生漆膜。漆酚是生漆的主要化学成分,某种漆酚的结构简式为:
漆酚不具有的化学性质是
A.可与烧碱溶液反应 B.可与溴水发生取代反应
C.可与酸性溶液反应 D.可与溶液反应放出二氧化碳
12.有机化合物分子中基团之间的相互影响会导致物质化学性质的不同。下列事实中,不能说明上述观点的是
A.甲苯能使酸性溶液褪色,而苯和甲烷不能使酸性溶液褪色
B.乙烯能发生加成反应,而乙烷不能发生加成反应
C.苯酚能与溶液反应,而乙醇不能与溶液反应
D.苯酚苯环上的氢原子比苯分子中的氢原子更容易被卤素原子取代
13.某物质可溶于水、乙醇,熔点为209.5℃,其分子的结构简式如图所示,下列说法不正确的是
A.该分子易溶于水、乙醇,可能是因为他们结构相似
B.该分子中含有大π键
C.该分子中只含有1个手性碳原子
D.该分子中所有C原子可能在同一平面
14.下列物质属于酚类的是
A. B.
C. D.
15.氯乙烷(沸点:12.5℃,熔点:-138.7℃)有如图转化关系:
氯乙烷乙醇乙醛;
设NA表示阿伏加德罗常数的值。下列叙述正确的是
A.标准状况下,22.4 L氯乙烷所含分子数为NA
B.25℃时,1.0 mol·L-1的NaOH溶液中阴阳离子总数为2NA
C.若有46 g乙醇转化为乙醛时,乙醇得到的电子数为2NA
D.若38 g乙醛和甲醇的混合物中含有4 g氢元素,则碳原子数目为1.5NA
二、实验题
16.实验室可用酒精、浓硫酸作试剂来制取乙烯,但实验表明,还有许多副反应发生,如反应中会生成SO2、CO2、水蒸气等无机物。某研究性学习小组欲用如图所示的装置制备纯净的乙烯并探究乙烯与单质溴能否反应及反应类型。回答下列问题:
(1)实验中,混合浓硫酸与乙醇的方法是将_______慢慢加入另一种物质中;加热F装置时必须使液体温度_______。
(2)写出浓硫酸与酒精直接反应生成上述无机副产物的化学方程式:_______。
(3)为实现上述实验目的,装置的连接顺序为F→_______→D(各装置限用一次)。
(4)当C中观察到_______时,表明单质溴能与乙烯反应;当D中_______时,表明C中发生的是取代反应;若D中没有出现前面所描述的现象时,表明C中发生的是_______反应。
(5)关于浓硫酸和乙醇混合加热制取乙烯的实验装置F中,下列说法正确的个数有_______个。
①浓硫酸的作用是作催化剂
②在反应容器中放入几片碎瓷片防止混合液暴沸
③圆底烧瓶中装的是乙醇和3mol·L-1H2SO4的混合液
④温度计应插入反应溶液液面下,以便控制温度
⑤若出口出来的气体能使酸性KMnO4溶液褪色,说明有乙烯生成
⑥反应过程中溶液的颜色会逐渐变黑
⑦生成的乙烯气体中混有带刺激性气味的气体
17.溴乙烷是一种重要的有机合成原料,为无色液体,难溶于水,沸点,熔点,密度。某实验小组用下图所示装置制取溴苯和溴乙烷。
主要实验步骤如下:
①检查装置的气密性后,向装置A中加入一定量的苯和液溴。
②向B处锥形瓶中加入乙醇和浓的混合液至浸没导管口。
③将A装置中的纯铁丝小心向下插入混合液中。
④点燃B装置中的酒精灯,用小火缓缓对锥形瓶加热10min。回答下列问题:
(1)仪器a的名称_______。装置A中生成的有机产物结构简式为_______。
(2)已知B装置中主要反应的反应类型为取代反应,其化学方程式为_______。浓硫酸的作用是_______。
(3)C装置中U形管浸在冰水中的目的是_______。
(4)步骤④中不能用大火加热,理由是_______。
三、工业流程题
18.含苯酚的工业废水处理的流程图如下:
(1)上述流程里,设备Ⅰ中进行的是___________操作(填写操作名称)。实验室里这一步操作可以用___________进行(填写仪器名称)。
(2)由设备Ⅱ进入设备Ⅲ的物质A是___________。由设备Ⅲ进入设备Ⅳ的物质B是___________。
(3)在设备Ⅲ中发生反应的化学方程式为___________。
(4)在设备Ⅳ中,物质B的水溶液和CaO反应后,产物是NaOH、H2O和___________。通过___________操作(填写操作名称),可以使产物相互分离。
(5)上图中,能循环使用的物质是C6H6、CaO、___________、___________。
19.含苯酚的工业废水的处理流程如图所示。
(1)①流程图设备中进行的操作是______(填操作名称)。实验室里这一步操作可以在______(填仪器名称)中进行。
②由设备Ⅱ进入设备Ⅲ的物质A是______(填化学式,下同)。由设备Ⅲ进入设备Ⅳ的物质B是______。
③在设备Ⅲ中发生反应的化学方程式为______。
④在设备Ⅳ中,物质B的水溶液和CaO反应后,产物是、H2O和______。通过______(填操作名称)操作,可以使产物相互分离。
⑤图中能循环使用的物质是______、______、和CaO。
(2)为了防止水源污染,用简单而又现象明显的方法检验某工厂排放的污水中有无苯酚,此方法是______。
(3)为测定废水中苯酚的含量,取此废水,向其中加入浓溴水至不再产生沉淀,得到沉淀0.331g,此废水中苯酚的含量为______。
第1页 共4页 ◎ 第2页 共4页
第1页 共4页 ◎ 第2页 共4页
参考答案:
1.D
【详解】相同条件下相同体积的氢气的物质的量相等,设生成氢气6mol,根据2-OH~2Na~H2↑可知参加反应的羟基均为12mol,三种醇的物质的量之比为3:6:2,故A、B、C三种分子里羟基数目之比为=2:1:3。
故选D。
2.C
【详解】A.甲苯中由于苯环对甲基的影响,使甲苯中甲基易被高锰酸钾酸性溶液氧化,而甲基环己烷不能,可说明原子与原子团间的相互影响导致物质的化学性质不同,A与题意不符;
B.苯酚中由于苯环对羟基的影响,使羟基中氢原子更易电离,表现出弱酸性,乙醇为中性,-OH连接的烃基不同,可说明原子与原子团间的相互影响导致物质的化学性质不同,B与题意不符;
C.乙烯含有碳碳双键,能与溴水发生加成反应,乙烷属于烷经,不含不饱和结构,不能发生加成反应,性质不同是由于官能团不同,与原子团的影响无关,C符合题意;
D.苯酚中由于羟基对苯环的影响,使苯酚分子中处于羟基邻、对位的苯环氢原子更活泼,更易被取代,可说明原子与原子团间的相互影响导致物质的化学性质不同,D与题意不符;
答案选C。
3.B
【详解】由结构简式可知,碳酸二甲酯一定条件下能与 发生缩聚反应生成聚碳酸酯, 分子中含有2个酚羟基,属于二酚类物质,故选B。
4.A
【分析】该实验的原理为在铜的催化作用下,乙醇被氧气氧化成乙醛,乙醛可能继续被氧化成乙酸。甲烧杯内是高于乙醇沸点的热水,目的是使乙醇汽化,然后和氧气按照一定体积比混合,在硬质玻璃管中,铜被氧化成黑色CuO,CuO被乙醇还原成Cu,总体上铜作催化剂,降低了乙醇被氧气氧化成乙醛的活化能。反应生成的乙醛(可能含有乙酸及未被氧化的乙醇)进入置于乙烧杯冷水中的试管a中被冷凝,得到含有乙醛、可能含有乙酸及未被氧化的乙醇的溶液,乙酸和活泼金属Zn能反应;
【详解】A.甲烧杯内是高于乙醇沸点的热水,乙烧杯冷水,选项A错误;
B.铜网降低了乙醇和氧气反应的活化能,选项B正确;
C.反应生成的乙醛,可能含有乙酸,进入置于乙烧杯冷水中的试管a中可能使锌粒溶解,选项C正确;
D.铜被氧化成黑色CuO,CuO被乙醇还原成Cu,出现红色和黑色交替现象,选项D正确;
答案选A。
5.D
【详解】A.该分子中含有酚羟基的邻对位易与溴发生取代反应,而分子中C=C易于溴发生加成反应,A项正确;
B.酚羟基能表现酸性,可以与Na2CO3反应生成酚钠和NaHCO3,B项正确;
C.酚羟基在空气中易被氧化,C项正确;
D.分子中的官能团为酚羟基、羰基、醚键、碳碳双键,D项错误;
故选D。
6.A
【详解】A.乙醇为饱和一元醇,而金合欢醇分子中含有碳碳双键,二者的结构不相似,所以不是同系物,故A错误;
B.金合欢醇分子中含有碳碳双键可发生加成反应,同时含有羟基,所以能发生取代反应,故B正确;
C.金合欢醇含有3个碳碳双键,所以1 mol金合欢醇能与3 mol H2发生加成反应,也能与3 mol Br2发生加成反应,故C正确;
D.金合欢醇分子中含有3个碳碳双键,醇羟基与产生H2的物质的量之比为2∶1,故D正确;
故选A。
7.C
【详解】A.乙醇与钠反应生成乙醇钠,是羟基中的O—H键断裂,A项正确;
B.乙醇与卤化氢反应时生成卤代烃,断裂②化学键,B项正确,
C.乙醇催化氧化成乙醛时,断裂①和③化学键,C项错误;
D.乙醇完全燃烧时生成二氧化碳和水,化学键①②③④⑤全部断裂,D项正确;
故选C。
8.B
【详解】A.水是无机物,故A不符合题意;
B.甲醇是有机物,含有羟基和钠生成氢气,故B符合题意;
C.乙醛和钠不反应,故C不符合题意;
D.乙酸甲酯和钠不反应,故D不符合题意;
故选B。
9.B
【详解】A.1 mol Z中含有5 mol酚羟基、1 mol羧基、1 mol酚酯基,1 mol酚酯基可消耗2 mol NaOH,故1 mol Z最多能与8 mol NaOH发生反应,A项错误;
B.X中苯环上有2个氢原子处于酚羟基的邻位,1 mol X最多能与2 mol Br2发生取代反应,B项正确;
C.Y分子中碳原子构成的六元环不是苯环,所有碳原子不能共平面,C项错误;
D.Y分子中与羟基相连碳原子的相邻碳原子上有氢原子,能发生消去反应,D项错误;
故答案为:B。
10.C
【详解】A.由其结构简式可知莪术二醇的分子式为,故A正确;
B.由其结构简式可知其含有官能团醇羟基,具有还原性,含有碳碳双键,极易被氧化,酸性溶液具有强氧化性,两者发生氧化还原反应,故莪术二醇可以使酸性溶液变色,故B正确;
C.只有与羟基相连的碳原子上有两个氢原子时,羟基才能氧化成醛基,而莪术二醇羟基相连的碳原子上并没有氢原子,则莪术二醇含有两个醇羟基不能被催化氧化,故C错误;
D.由其结构简式可知该分子含有碳碳双键,在一定条件下可发生加聚反应,在一定条件下莪术二醇可发生加聚反应得到高聚物,故D正确;
故答案为C。
11.D
【详解】A.该有机物中的羟基直接连在苯环上,属于酚类化合物,具有酸性,能与烧碱溶液发生中和反应,故A不符合题意;
B.该有机物属于酚,能与溴水发生取代反应,故B不符合题意;
C.该有机物含有羟基且苯环有烃基的侧链,都能被酸性高锰酸钾溶液氧化,故C不符合题意;
D.酚具有酸性,但其酸性比碳酸的酸性弱,因此该有机物不能与碳酸氢钠溶液反应,故D符合题意;
故选D。
12.B
【详解】A.苯和甲烷不能使酸性溶液褪色,甲基连接在苯环上,可被氧化,说明苯环对甲基影响,能说明上述观点,故A不选;
B.因为乙烯的结构中含有碳碳双键,能与氢气发生加成反应,而烷烃中则没有,是自身的官能团性质,不是原子团间的相互影响导致的化学性质,故B选;
C.受苯环的影响,苯酚中的羟基氢原子变得比较活泼,所以苯酚能与NaOH溶液反应,而乙醇不能,是有机物分子中基团间的相互影响会导致化学性质不同,故C不选;
D.苯酚苯环上的氢比苯分子中的氢更容易被卤原子取代,说明苯酚苯环上H原子更活泼,说明酚-OH对苯环的影响,故D不选;
故选B。
13.C
【详解】A.由结构简式可知,该有机物与水、乙醇都是极性分子,由相似相溶原理可知,该分子易溶于水、乙醇,故A正确;
B.由结构简式可知,有机物分子含有苯环,苯环中含有大π键,故B正确;
C.由结构简式可知,有机物分子与羟基相连的2个碳原子都是连有4个不同原子或原子团的手性碳原子,故C错误;
D.苯环是平面结构,苯环上的碳原子和与苯环相连的碳原子共平面,由三点成面的原理可知,该分子中所有碳原子可能在同一平面,故D正确;
故选C。
14.D
【详解】A.的羟基连接在测链上,属于芳香醇,名称为苯甲醇,A不符合题意;
B.中2个苯基通过O原子相连,该物质属于醚,B不符合题意;
C.O原子分别连接苯基、甲基,属于醚,C不符合题意;
D.中羟基与苯环直接相连,属于酚,D符合题意;
故合理选项是D。
15.D
【分析】氯乙烷转化为乙醇的反应为;乙醇转化为一圈的反应为;
【详解】A.标准状况下,氯乙烷为液态,不能用进行计算,故A错误;
B.根据,NaOH溶液的体积未知,无法计算NaOH的量,故B错误;
C.对于反应,乙醇被氧化,失去电子,转移电子总数为4,若有46 g乙醇转化为乙醛时,乙醇失去的电子数为,故C错误;
D.设,,则根据题意有,,解得,,则38 g乙醛和甲醇的混合物中碳原子数目为,故D正确;
故选D。
16.(1) 浓硫酸 迅速升到170℃
(2)CH3CH2OH+6H2SO4(浓)=2CO2↑+6SO2↑+9H2O
(3)A→B→E→C
(4) 溶液褪色 有淡黄色沉淀生成 加成
(5)4
【分析】装置F是乙醇和浓H2SO4在170℃下反应制备乙烯,生成的乙烯气体中会混有SO2、CO2、乙醇蒸汽等物质,为实现实验目的,应用装置A中的NaOH溶液除去SO2、CO2,并用装置B中的澄清石灰水检验是否除尽,然后用装置E中的浓硫酸干燥,得到纯净干燥的乙烯,乙烯通入装有溴的CCl4溶液的装置C中,探究乙烯与单质溴能否反应,最后用装置D验证是否有HBr产生,以确定反应类型。
【详解】(1)混合浓硫酸与乙醇,与稀释浓硫酸相似,应将浓硫酸缓慢加入乙醇中,边加边搅拌;为了避免副反应发生,加热时应使溶液迅速升温到170 ℃;
(2)浓硫酸具有强氧化性,加热条件下,乙醇可与浓硫酸反应生成CO2、SO2等物质,其化学方程式为CH3CH2OH+6H2SO4(浓)=2CO2↑+6SO2↑+9H2O;
(3)为实现上述实验目的,应用装置A中的NaOH溶液除去SO2、CO2,并用装置B中的澄清石灰水检验是否除尽,然后用装置E中的浓硫酸干燥,得到纯净干燥的乙烯,乙烯通入装有溴的CCl4溶液的装置C中,探究乙烯与单质溴能否反应,最后用装置D验证是否有HBr产生,以确定反应类型,故装置的连接顺序为F→A→B→E→C→D;
(4)当C中观察到溴的CCl4溶液褪色时,乙烯与单质溴之间可能发生加成反应,也可能发生取代反应;若是取代反应,则会有HBr生成,HBr遇AgNO3溶液会产生淡黄色沉淀,若D中没有出现前面所描述的现象时,表明C中发生的是加成反应;
(5)①.浓硫酸的作用是催化剂、脱水剂,故错误;
②.在反应容器中放入几片碎瓷片是防止混合液暴沸,故正确;
③.圆底烧瓶中装的是乙醇和浓H2SO4的混合液,故错误;
④.需要控制溶液的温度为170℃,所以温度计应插入反应溶液液面下,以便控制温度,故正确;
⑤.乙烯、SO2、乙醇蒸汽等都能使酸性KMnO4溶液褪色,不能说明有乙烯生成,故错误;
⑥.制备乙烯时,伴随有乙醇和浓硫酸的氧化还原反应,由于生成黑色的C单质,溶液的颜色会逐渐变黑,故正确;
⑦.制备乙烯时,伴随有乙醇和浓硫酸的氧化还原反应,生成带刺激性气味的SO2气体,故正确;
故说法正确的个数有4个。
17.(1) 圆底烧瓶
(2) 催化剂
(3)收集溴乙烷
(4)易发生副反应生成乙醚、乙烯等
【分析】A装置中铁与溴发生反应生成溴化铁,溴化铁作为催化剂催化溴与苯的反应,其中生成的溴化氢和挥发的溴单质通过导管a进入到装置B中与乙醇发生取代反应,由溴乙烷数据可知,在冰水浴中溴乙烷液化,故装置C为溴乙烷的收集装置,装置C底部用蒸馏水液封,作用是吸收生成的溴化氢;
【详解】(1)仪器a的名称是圆底烧瓶;装置A中铁与溴发生反应生成溴化铁,溴化铁作为催化剂催化溴与苯反应生成溴苯,生成的有机产物结构简式为;
(2)生成的溴化氢和挥发的溴单质通过导管a进入到装置B中与乙醇发生取代反应,反应方程式为;浓硫酸的作用是催化剂;
(3)C装置中U形管浸在冰水中的目的是收集溴乙烷;
(4)在温度较高的情况下浓H2SO4存在条件下发生副反应生成乙醚、乙烯等,故答案为:易发生副反应生成乙醚、乙烯等。
18.(1) 萃取、分液 分液漏斗
(2) C6H5ONa NaHCO3
(3)C6H5ONa+CO2+H2O→C6H5OH+NaHCO3
(4) CaCO3 过滤
(5) NaOH溶液 CO2
【分析】由流程图和每一步新加的试剂进行分析可知:用苯萃取出设备Ⅰ中的苯酚进入设备Ⅱ,然后用NaOH溶液将设备Ⅱ中的苯酚转化为苯酚钠而进入设备Ⅲ,向设备Ⅲ中通入CO2将苯酚钠转化为苯酚,同时生成NaHCO3而进入设备Ⅳ,向设备Ⅳ中加入CaO时,生成CaCO3进入设备Ⅴ,NaOH进入设备Ⅱ循环使用。
【详解】(1)根据上述分析,设备Ⅰ中进行的是萃取、分液,实验室里这一步操作可以用分液漏斗进行;
(2)根据上述分析,由设备Ⅱ进入设备Ⅲ的物质A是苯酚钠,由设备Ⅲ进入设备Ⅳ的物质B是NaHCO3;
(3)根据上述分析,在设备Ⅲ中发生反应的化学方程式为C6H5ONa+CO2+H2O→C6H5OH+NaHCO3;
(4)在设备Ⅳ中,物质B的水溶液和CaO反应后,产物是NaOH、H2O和CaCO3,CaCO3难溶于水,通过过滤,可以使产物相互分离;
(5)上图中,能循环使用的物质是C6H6、CaO、NaOH溶液、CO2。
19. 萃取、分液 分液漏斗 过滤 溶液 向污水中滴加溶液,若溶液呈紫色,则表明污水中有苯酚 940
【分析】由流程可知,设备I中中含有苯和工业废水,可经萃取、分液得到苯酚的苯溶液混合物,进入设备Ⅱ;设备Ⅱ中加入溶液,可得到苯酚钠溶液;在设备Ⅲ中通入,分离出苯酚;在设备Ⅳ中主要物质是,溶液中加入,可生成、、,通过过滤操作分离出;在设备V中高温分解可得和,据此分析解答。
【详解】(1)①设备I中废水和苯混合后分离出水,进行的操作是萃取、分液,实验室中可以用分液漏斗进行分液操作,故答案为:萃取、分液;分液漏斗;
②设备Ⅱ中向苯酚和苯的混合液中加入NaOH溶液,目的是分离出苯,故物质A是苯酚钠溶液;在设备Ⅲ中通入CO2,分离出苯酚,故物质B是NaHCO3溶液;故答案为:;NaHCO3;
③在盛有苯酚钠溶液的设备Ⅲ中,通入过量的二氧化碳气体,发生反应生成苯酚和碳酸氢钠,反应的化学方程式为,故答案为:;
④在设备Ⅳ中向NaHCO3溶液中加入CaO,生成NaOH、H2O、CaCO3,可通过过滤操作分离出CaCO3,故答案为:CaCO3;过滤;
⑤在设备V中CaCO3高温分解可得CO2和CaO,所以图中能循环使用的物质是NaOH溶液、CO2、C6H6和CaO,故答案为:NaOH溶液;CO2;
(2)苯酚和氯化铁溶液之间会发生显色反应,向溶液中滴加氯化铁溶液,若溶液呈紫色,则表明污水中有苯酚,故答案为:向污水中滴加FeCl3溶液,若溶液呈紫色,则表明污水中有苯酚;
(3) )设每升废水中含苯酚,
,根据反应关系可知:94:331=xg:0.331g,解得,所以此废水中苯酚的含量为:==,故答案为:940。
答案第1页,共2页
答案第1页,共2页
