化学人教版(2019)选择性必修3 1.2.1有机物的分离提纯 课件(共19张ppt)
文档属性
| 名称 | 化学人教版(2019)选择性必修3 1.2.1有机物的分离提纯 课件(共19张ppt) |

|
|
| 格式 | pptx | ||
| 文件大小 | 15.6MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-06-22 00:00:00 | ||
图片预览




文档简介
(共19张PPT)
第一章
第二节 研究有机化合物的一般方法
第1课时 《 分离、提纯》
分离、提纯
确定实验式
确定分子式
确定分子结构
研究有机物结构的一般步骤
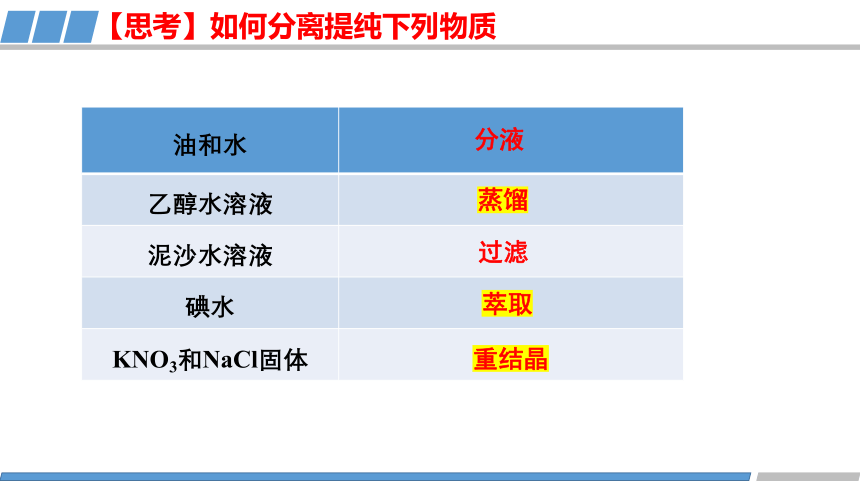
油和水
乙醇水溶液
泥沙水溶液
碘水
KNO3和NaCl固体
【思考】如何分离提纯下列物质
分液
蒸馏
过滤
萃取
重结晶
蒸馏
3.条件:
被提纯物质热稳定性较高
与杂质的沸点相差较大(一般大于30℃)
1.原理:
根据混合物沸点不同
互溶液态混合物
2.适用范围:
蒸馏烧瓶
石棉网
温度计
直形冷凝管
锥形瓶
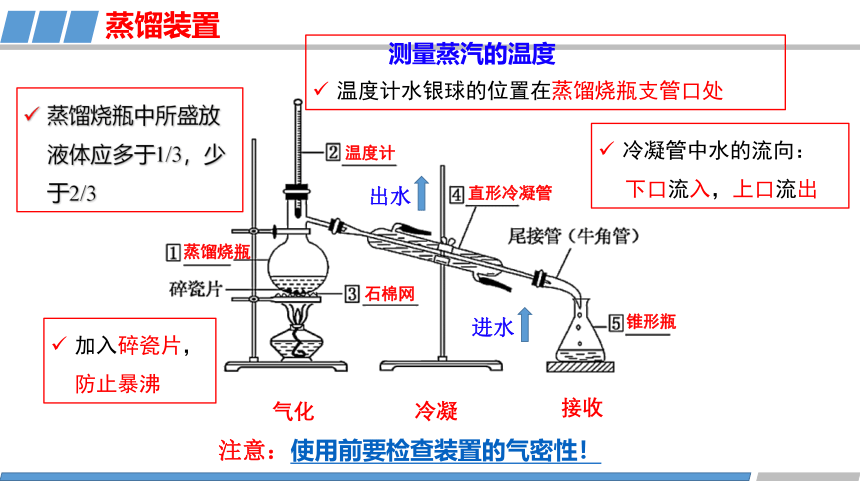
蒸馏装置
气化
冷凝
接收
测量蒸汽的温度
温度计水银球的位置在蒸馏烧瓶支管口处
出水
进水
冷凝管中水的流向:
下口流入,上口流出
加入碎瓷片,防止暴沸
蒸馏烧瓶中所盛放液体应多于1/3,少于2/3
注意:使用前要检查装置的气密性!
利用蒸馏方法提纯工业乙醇
已知工业乙醇(主要成分是乙醇,含有水、甲醇杂质),通过蒸馏可获得95.6%乙醇和4.4%水的共沸混合物(沸点78.15℃)。
物质 乙醇 水
沸点/℃ 78.5 100
沸点差距小
蒸馏法的应用
含杂质的乙醇
95.6%乙醇 和4.4%水
无水乙醇99.5%
蒸馏
如何获得无水乙醇?
加CaO
蒸馏
?
CaO+H2O=Ca(OH)2
萃取
1. 定义:
待分离组分在两种互不相溶溶剂中溶解性不同,将其从一种溶剂转移到另一种溶剂中的过程。
【思考】如何提取碘水中的碘单质?
水(H2O) 苯(C6H6) 四氯化碳 (CCl4)
碘(I2) 棕黄 紫红色 紫红色
表1:碘溶解在不同溶剂中的颜色
水(H2O) 苯(C6H6) 四氯化碳 (CCl4)
碘(I2) 0.029g 14.1g 2.9g
表2:碘在不同溶剂中的溶解度(25℃)
溶解性:水不溶于四氯化碳、苯
密 度:水1.0g/ml;苯0.88g/ml(密度比水小);四氯化碳1.59g/ml(密度比水大)
萃取的应用
萃取剂
萃取
1. 定义:
待分离组分在两种互不相溶溶剂中溶解性不同,将其从一种溶剂转移到另一种溶剂中的过程。
2. 萃取剂的选择:
①和原溶剂不相溶,不反应
②溶质溶解度:萃取剂中比原溶剂中大
③萃取剂与被萃取物质要易于分离
【思考】如何分离碘的CCl4溶液?
蒸馏
萃取碘水中的碘单质
分液
静置
装液
振荡
分液:将两种互不相溶的液体分开的操作
萃取的操作
检漏
04
重结晶
被提纯物和杂质为固态
1.原理:
被提纯物与杂质在同一溶剂中的溶解度不同而将其杂质除去。
2.适用范围:
某粗苯甲酸样品中含有少量氯化钠和泥沙,如何提纯苯甲酸?
【资料】苯甲酸可用作食品防腐剂,纯净的
苯甲酸为无色结晶,其结构可表示为 ,
熔点122℃,沸点249℃,苯甲酸微溶于水,易溶于乙醇等有机溶剂。苯甲酸、氯化钠在水中的溶解度如下:
温度 25℃ 50℃ 95℃
苯甲酸 0.34g 0.85g 6.8g
NaCl 36.0 37.0 39.1
重结晶法提纯苯甲酸
【实验过程】
(1)观察粗苯甲酸样品的状态。
(2)将1g粗苯甲酸放入100mL烧杯,加入50mL蒸馏水。加热,搅拌,使粗苯甲酸充分溶解。
(3)使用漏斗趁热将溶液过滤至另一烧杯中,将滤液静置,使其缓慢冷却结晶。
(4)待滤液完全冷却后滤出晶体,并用少量蒸馏水洗涤。将晶体铺在干燥的滤纸上,晾干后称其质量。
①加热溶解
②趁热过滤
③冷却结晶
④过滤洗涤
⑤干燥称量
重结晶法提纯苯甲酸
重结晶法提纯苯甲酸
2、溶解粗苯甲酸时加热的作用是什么?趁热过滤的目的是什么?
3、实验操作中多次使用了玻璃棒,分别起到哪些作用?
4、如何检验提纯后的苯甲酸中氯化钠已被除净?
增大苯甲酸在水中的溶解度
防止苯甲酸晶体析出
溶解时搅拌,加快溶解速度;过滤和洗涤时引流。
取最后一次洗涤液于试管中,加入足量稀硝酸,再加少量硝酸银溶液,无明显现象,说明氯化钠已经除净。
【思考交流】
1、重结晶法提纯苯甲酸的原理是什么?有哪些主要操作步骤?
被提纯物与杂质在同一溶剂中的溶解度不同而将其杂质除去。
①加热溶解
②趁热过滤
③冷却结晶
④过滤洗涤
⑤干燥称量
根据右图信息,下列实验的步骤是什么?
(1)提纯KNO3(NaCl)
(2)提纯NaCl、(KNO3)
溶解,蒸发结晶,趁热过滤
溶解,蒸发浓缩,冷却结晶
过滤得到KNO3晶体,杂质NaCl留在滤液中。
这样首先析出的是NaCl,少量的KNO3仍残留在热的溶液中。
重结晶
总结归纳
第一章
第二节 研究有机化合物的一般方法
第1课时 《 分离、提纯》
分离、提纯
确定实验式
确定分子式
确定分子结构
研究有机物结构的一般步骤
油和水
乙醇水溶液
泥沙水溶液
碘水
KNO3和NaCl固体
【思考】如何分离提纯下列物质
分液
蒸馏
过滤
萃取
重结晶
蒸馏
3.条件:
被提纯物质热稳定性较高
与杂质的沸点相差较大(一般大于30℃)
1.原理:
根据混合物沸点不同
互溶液态混合物
2.适用范围:
蒸馏烧瓶
石棉网
温度计
直形冷凝管
锥形瓶
蒸馏装置
气化
冷凝
接收
测量蒸汽的温度
温度计水银球的位置在蒸馏烧瓶支管口处
出水
进水
冷凝管中水的流向:
下口流入,上口流出
加入碎瓷片,防止暴沸
蒸馏烧瓶中所盛放液体应多于1/3,少于2/3
注意:使用前要检查装置的气密性!
利用蒸馏方法提纯工业乙醇
已知工业乙醇(主要成分是乙醇,含有水、甲醇杂质),通过蒸馏可获得95.6%乙醇和4.4%水的共沸混合物(沸点78.15℃)。
物质 乙醇 水
沸点/℃ 78.5 100
沸点差距小
蒸馏法的应用
含杂质的乙醇
95.6%乙醇 和4.4%水
无水乙醇99.5%
蒸馏
如何获得无水乙醇?
加CaO
蒸馏
?
CaO+H2O=Ca(OH)2
萃取
1. 定义:
待分离组分在两种互不相溶溶剂中溶解性不同,将其从一种溶剂转移到另一种溶剂中的过程。
【思考】如何提取碘水中的碘单质?
水(H2O) 苯(C6H6) 四氯化碳 (CCl4)
碘(I2) 棕黄 紫红色 紫红色
表1:碘溶解在不同溶剂中的颜色
水(H2O) 苯(C6H6) 四氯化碳 (CCl4)
碘(I2) 0.029g 14.1g 2.9g
表2:碘在不同溶剂中的溶解度(25℃)
溶解性:水不溶于四氯化碳、苯
密 度:水1.0g/ml;苯0.88g/ml(密度比水小);四氯化碳1.59g/ml(密度比水大)
萃取的应用
萃取剂
萃取
1. 定义:
待分离组分在两种互不相溶溶剂中溶解性不同,将其从一种溶剂转移到另一种溶剂中的过程。
2. 萃取剂的选择:
①和原溶剂不相溶,不反应
②溶质溶解度:萃取剂中比原溶剂中大
③萃取剂与被萃取物质要易于分离
【思考】如何分离碘的CCl4溶液?
蒸馏
萃取碘水中的碘单质
分液
静置
装液
振荡
分液:将两种互不相溶的液体分开的操作
萃取的操作
检漏
04
重结晶
被提纯物和杂质为固态
1.原理:
被提纯物与杂质在同一溶剂中的溶解度不同而将其杂质除去。
2.适用范围:
某粗苯甲酸样品中含有少量氯化钠和泥沙,如何提纯苯甲酸?
【资料】苯甲酸可用作食品防腐剂,纯净的
苯甲酸为无色结晶,其结构可表示为 ,
熔点122℃,沸点249℃,苯甲酸微溶于水,易溶于乙醇等有机溶剂。苯甲酸、氯化钠在水中的溶解度如下:
温度 25℃ 50℃ 95℃
苯甲酸 0.34g 0.85g 6.8g
NaCl 36.0 37.0 39.1
重结晶法提纯苯甲酸
【实验过程】
(1)观察粗苯甲酸样品的状态。
(2)将1g粗苯甲酸放入100mL烧杯,加入50mL蒸馏水。加热,搅拌,使粗苯甲酸充分溶解。
(3)使用漏斗趁热将溶液过滤至另一烧杯中,将滤液静置,使其缓慢冷却结晶。
(4)待滤液完全冷却后滤出晶体,并用少量蒸馏水洗涤。将晶体铺在干燥的滤纸上,晾干后称其质量。
①加热溶解
②趁热过滤
③冷却结晶
④过滤洗涤
⑤干燥称量
重结晶法提纯苯甲酸
重结晶法提纯苯甲酸
2、溶解粗苯甲酸时加热的作用是什么?趁热过滤的目的是什么?
3、实验操作中多次使用了玻璃棒,分别起到哪些作用?
4、如何检验提纯后的苯甲酸中氯化钠已被除净?
增大苯甲酸在水中的溶解度
防止苯甲酸晶体析出
溶解时搅拌,加快溶解速度;过滤和洗涤时引流。
取最后一次洗涤液于试管中,加入足量稀硝酸,再加少量硝酸银溶液,无明显现象,说明氯化钠已经除净。
【思考交流】
1、重结晶法提纯苯甲酸的原理是什么?有哪些主要操作步骤?
被提纯物与杂质在同一溶剂中的溶解度不同而将其杂质除去。
①加热溶解
②趁热过滤
③冷却结晶
④过滤洗涤
⑤干燥称量
根据右图信息,下列实验的步骤是什么?
(1)提纯KNO3(NaCl)
(2)提纯NaCl、(KNO3)
溶解,蒸发结晶,趁热过滤
溶解,蒸发浓缩,冷却结晶
过滤得到KNO3晶体,杂质NaCl留在滤液中。
这样首先析出的是NaCl,少量的KNO3仍残留在热的溶液中。
重结晶
总结归纳
