化学人教版(2019)选择性必修3 3.4.1羧酸 课件(共20张ppt)
文档属性
| 名称 | 化学人教版(2019)选择性必修3 3.4.1羧酸 课件(共20张ppt) |

|
|
| 格式 | pptx | ||
| 文件大小 | 5.4MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-06-22 00:00:00 | ||
图片预览








文档简介
(共20张PPT)
第三章 第四节 第1课时
《羧酸》
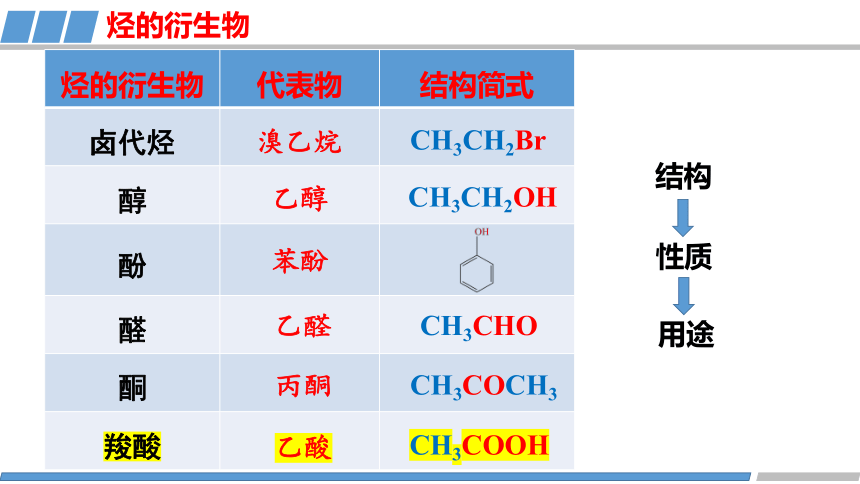
烃的衍生物 代表物 结构简式
卤代烃
醇
酚
醛
酮
羧酸
溴乙烷
乙醇
乙醛
丙酮
结构
性质
烃的衍生物
CH3CH2Br
CH3CH2OH
CH3CHO
CH3COCH3
乙酸
CH3COOH
苯酚
用途
生活中的羧酸
(2)官能团:
1.组成与结构
(1)定义:
分子中烃基(或氢原子)和羧基(—COOH)相连的有机化合物
CnH2n+1COOH 或 CnH2nO2( n ≥ 1)
(3)饱和一元羧酸通式:
任务一:羧酸的定义和分类
羧基
2.羧酸的分类
羧酸
分类
根据与羧基相连的
烃基不同
根据羧酸分子中的
羧基数目
芳香酸
脂肪酸
一元羧酸
二元羧酸
多元羧酸
CH3-COOH
C15H31-COOH
软脂酸
C17H35-COOH
硬脂酸
C17H33-COOH
油酸
CH2=CH-COOH
丙烯酸
H-COOH
甲酸(蚁酸)
COOH
苯甲酸(安息香酸)
COOH
COOH
草酸
柠檬酸
任务一:羧酸的定义和分类
物质 结构简式 性质 用途
甲酸 (蚁酸)
苯甲酸 (安息香酸)
乙二酸 (草酸)
认识几种常见的羧酸
①无色有刺激性的液体,可与水混溶,有腐蚀性。
HCOOH
在工业上可用作还原剂,也是合成医药、农药和染料等的原料。
苯甲酸是一种无色晶体,易升华,微溶于水,易溶于乙醇。
用于合成香料、药物等,它的钠盐是常用的食品防腐剂。
无色透明晶体,可溶于水和乙醇
常用于化学分析的还原剂,是重要的化工原料。
②具有醛和羧酸的性质;
能和新制Cu(OH)2和银氨溶液反应
(1)状态:
任务二:羧酸的物理性质
液体或固体
强烈刺激性气味
①甲酸、乙酸等分子中碳原子数较少的羧酸能够与水互溶。
(2)气味:
(3)溶解性:
②随着分子中碳原子数的增加,一元羧酸在水中的溶解度迅速减小,甚至不溶于水。
③高级脂肪酸是不溶于水的蜡状固体。
3.物理性质
(4)熔沸点:
名称 结构简式 熔点/℃ 沸点/℃
甲酸 HCOOH 8 101
乙酸 CH3COOH 17 118
丙酸 CH3CH2COOH -21 141
正丁酸 CH3CH2CH2COOH -5 166
十八酸 (硬脂酸) CH3(CH2)16COOH 70 383
苯甲酸 122 249
COOH
3.物理性质
随碳原子数的增加,
熔、沸点逐渐升高。
任务二:羧酸的物理性质
表3-4 几种羧酸的熔点和沸点
思考:结构决定性质,请从键的极性角度分析羧酸可能的断键位置以及所具有的化学性质?
断键方式:
C—O易断裂
﹒取代反应
O—H易断裂
﹒酸性
O
C
O
H
R
任务三:羧酸的化学性质——乙酸为例
元素符号 C H O
电负性 2.5 2.1 3.5
(1)酸性(以乙酸为例)
任务三:羧酸的化学性质
非金属单质
酸性氧化物
酸
盐
金属单质
碱性氧化物
碱
盐
2CH3COOH + Zn = (CH3COO)2Zn+H2↑
2CH3COOH + CuO =(CH3COO)2Cu + H2O
CH3COOH + NaOH= CH3COONa+ H2O
2CH3COOH + CaCO3 = (CH3COO)2Ca+H2O+CO2↑
该盐对应酸的酸性弱于醋酸
羧酸是一类弱酸,具有酸的通性。
【问题】羧酸的化学性质与乙酸的相似,如何通过实验证明其他
羧酸也具有酸性?
(1)设计实验证明羧酸具有酸性(提供的羧酸有甲酸、苯甲酸和乙二酸)
实验内容 实验现象 结论
分别取0.01 mol·L-1三种酸
溶液,滴入紫色石蕊溶液
分别取0.01 mol·L-1三种酸溶液,测pH
紫色石蕊溶液
变红色
pH大于2
甲酸、苯甲酸
和乙二酸具有
弱酸性
任务三:羧酸的化学性质
【设计与实验】
(2)利用下图所示仪器和药品,设计一个简单的一次性完成的实验装置,比较乙酸、碳酸和苯酚的酸性强弱。
任务三:羧酸的化学性质
装置连接顺序:
对应的化学方程式?
乙酸与碳酸钠产生气体,苯酚钠溶液变浑浊
A→D→E→B→C→F→G→H→I→J
预期实验现象?
【实验装置】
如何除去乙酸呢?
在两个装置间添加盛有饱和NaHCO3溶液的洗气瓶,除去CO2中的乙酸蒸气,防止对碳酸酸性大于苯酚酸性的检验产生干扰。
√
任务三:羧酸的化学性质
苯酚钠溶液变浑浊是否一定是与CO2的反应导致的呢?
不一定。乙酸易挥发,也会和苯酚钠反应
写出各装置中反应的化学方程式:
ONa
+CO2+H2O → +NaHCO3
OH
任务三:羧酸的化学性质
【实验结论】
酸性:乙酸 > 碳酸 > 苯酚
②CH3COOH+NaHCO3→CH3COONa+CO2↑+H2O
①2CH3COOH+Na2CO3→2CH3COONa+CO2↑+H2O
③
①
②
③
代表物 结构简式 羟基氢的活泼性 酸性 (与碳酸相比) 与Na反应 与NaOH的 反应 与Na2CO3的 反应 与NaHCO3的
反应
乙醇 CH3CH2OH
苯酚 C6H5OH
乙酸 CH3COOH
【小结】比较醇、酚、羧酸中O-H键的活泼性
增强
中性
比碳酸弱
比碳酸强
能
能
能
能
能
能
能
不能
不能
不能
不能
能
例题.某有机物A的结构简式为 ,取Na、NaOH、NaHCO3、Na2CO3分别与
等物质的量的该物质充分反应(反应时可加热煮沸),则消耗Na、NaOH、NaHCO3、Na2CO3四种物质的物质的量之比为
3∶2∶1:2
⑵酯化反应(以乙酸为例)
【思考与讨论】乙酸与乙醇的酯化反应,从形式上看是羧基与羟基之间脱去一个水分子。脱水时有哪些可能的方式,你能设计一个实验方案来证明是哪一种吗?
同位素示踪法
碳氧键易断裂
﹒取代反应
δ+
δ+
δ-
δ-
O
C
O
H
R
任务三:羧酸的化学性质
酯化反应(取代反应):乙酸分子中羧基的羟基与乙醇分子中羟基的氢原子结合成水,其余部分相互结合成酯。
【思考与讨论】在制取乙酸乙酯的实验中,如果要提高
乙酸乙酯的产率,你认为应当采取哪些措施?请结合化学
反应原理的有关知识进行说明。
现象:饱和碳酸钠溶液的液面上有透明的油状液体,并可闻到香味。
任务三:羧酸的化学性质
根据化学平衡原理,提高乙酸乙酯产率的措施有:
①由于乙酸乙酯的沸点比乙酸、乙醇都低,因此从反应物中不断蒸出乙酸乙酯
可提高其产率。
②使用过量的乙醇,可提高乙酸转化率。
③使用浓H2SO4作吸水剂,提高反应转化率。
④冷凝回流,提高产率。
任务三:羧酸的化学性质
【小结】羧酸的化学性质
(1)酸性
碳氧键易断裂
﹒取代反应
δ+
δ-
δ+
δ-
氧氢键易断裂
﹒酸性
O
C
O
H
R
O O
CH3—C—O—H+H—O— C2H5 CH3—C—O—C2H5 + H2O
浓H2SO4
①使酸碱指示剂变色
②与活泼金属反应
③与碱性氧化物反应
④与碱反应
⑤与弱酸(其对应酸的酸性弱于羧酸)盐反应
(2)酯化反应(取代反应)
第三章 第四节 第1课时
《羧酸》
烃的衍生物 代表物 结构简式
卤代烃
醇
酚
醛
酮
羧酸
溴乙烷
乙醇
乙醛
丙酮
结构
性质
烃的衍生物
CH3CH2Br
CH3CH2OH
CH3CHO
CH3COCH3
乙酸
CH3COOH
苯酚
用途
生活中的羧酸
(2)官能团:
1.组成与结构
(1)定义:
分子中烃基(或氢原子)和羧基(—COOH)相连的有机化合物
CnH2n+1COOH 或 CnH2nO2( n ≥ 1)
(3)饱和一元羧酸通式:
任务一:羧酸的定义和分类
羧基
2.羧酸的分类
羧酸
分类
根据与羧基相连的
烃基不同
根据羧酸分子中的
羧基数目
芳香酸
脂肪酸
一元羧酸
二元羧酸
多元羧酸
CH3-COOH
C15H31-COOH
软脂酸
C17H35-COOH
硬脂酸
C17H33-COOH
油酸
CH2=CH-COOH
丙烯酸
H-COOH
甲酸(蚁酸)
COOH
苯甲酸(安息香酸)
COOH
COOH
草酸
柠檬酸
任务一:羧酸的定义和分类
物质 结构简式 性质 用途
甲酸 (蚁酸)
苯甲酸 (安息香酸)
乙二酸 (草酸)
认识几种常见的羧酸
①无色有刺激性的液体,可与水混溶,有腐蚀性。
HCOOH
在工业上可用作还原剂,也是合成医药、农药和染料等的原料。
苯甲酸是一种无色晶体,易升华,微溶于水,易溶于乙醇。
用于合成香料、药物等,它的钠盐是常用的食品防腐剂。
无色透明晶体,可溶于水和乙醇
常用于化学分析的还原剂,是重要的化工原料。
②具有醛和羧酸的性质;
能和新制Cu(OH)2和银氨溶液反应
(1)状态:
任务二:羧酸的物理性质
液体或固体
强烈刺激性气味
①甲酸、乙酸等分子中碳原子数较少的羧酸能够与水互溶。
(2)气味:
(3)溶解性:
②随着分子中碳原子数的增加,一元羧酸在水中的溶解度迅速减小,甚至不溶于水。
③高级脂肪酸是不溶于水的蜡状固体。
3.物理性质
(4)熔沸点:
名称 结构简式 熔点/℃ 沸点/℃
甲酸 HCOOH 8 101
乙酸 CH3COOH 17 118
丙酸 CH3CH2COOH -21 141
正丁酸 CH3CH2CH2COOH -5 166
十八酸 (硬脂酸) CH3(CH2)16COOH 70 383
苯甲酸 122 249
COOH
3.物理性质
随碳原子数的增加,
熔、沸点逐渐升高。
任务二:羧酸的物理性质
表3-4 几种羧酸的熔点和沸点
思考:结构决定性质,请从键的极性角度分析羧酸可能的断键位置以及所具有的化学性质?
断键方式:
C—O易断裂
﹒取代反应
O—H易断裂
﹒酸性
O
C
O
H
R
任务三:羧酸的化学性质——乙酸为例
元素符号 C H O
电负性 2.5 2.1 3.5
(1)酸性(以乙酸为例)
任务三:羧酸的化学性质
非金属单质
酸性氧化物
酸
盐
金属单质
碱性氧化物
碱
盐
2CH3COOH + Zn = (CH3COO)2Zn+H2↑
2CH3COOH + CuO =(CH3COO)2Cu + H2O
CH3COOH + NaOH= CH3COONa+ H2O
2CH3COOH + CaCO3 = (CH3COO)2Ca+H2O+CO2↑
该盐对应酸的酸性弱于醋酸
羧酸是一类弱酸,具有酸的通性。
【问题】羧酸的化学性质与乙酸的相似,如何通过实验证明其他
羧酸也具有酸性?
(1)设计实验证明羧酸具有酸性(提供的羧酸有甲酸、苯甲酸和乙二酸)
实验内容 实验现象 结论
分别取0.01 mol·L-1三种酸
溶液,滴入紫色石蕊溶液
分别取0.01 mol·L-1三种酸溶液,测pH
紫色石蕊溶液
变红色
pH大于2
甲酸、苯甲酸
和乙二酸具有
弱酸性
任务三:羧酸的化学性质
【设计与实验】
(2)利用下图所示仪器和药品,设计一个简单的一次性完成的实验装置,比较乙酸、碳酸和苯酚的酸性强弱。
任务三:羧酸的化学性质
装置连接顺序:
对应的化学方程式?
乙酸与碳酸钠产生气体,苯酚钠溶液变浑浊
A→D→E→B→C→F→G→H→I→J
预期实验现象?
【实验装置】
如何除去乙酸呢?
在两个装置间添加盛有饱和NaHCO3溶液的洗气瓶,除去CO2中的乙酸蒸气,防止对碳酸酸性大于苯酚酸性的检验产生干扰。
√
任务三:羧酸的化学性质
苯酚钠溶液变浑浊是否一定是与CO2的反应导致的呢?
不一定。乙酸易挥发,也会和苯酚钠反应
写出各装置中反应的化学方程式:
ONa
+CO2+H2O → +NaHCO3
OH
任务三:羧酸的化学性质
【实验结论】
酸性:乙酸 > 碳酸 > 苯酚
②CH3COOH+NaHCO3→CH3COONa+CO2↑+H2O
①2CH3COOH+Na2CO3→2CH3COONa+CO2↑+H2O
③
①
②
③
代表物 结构简式 羟基氢的活泼性 酸性 (与碳酸相比) 与Na反应 与NaOH的 反应 与Na2CO3的 反应 与NaHCO3的
反应
乙醇 CH3CH2OH
苯酚 C6H5OH
乙酸 CH3COOH
【小结】比较醇、酚、羧酸中O-H键的活泼性
增强
中性
比碳酸弱
比碳酸强
能
能
能
能
能
能
能
不能
不能
不能
不能
能
例题.某有机物A的结构简式为 ,取Na、NaOH、NaHCO3、Na2CO3分别与
等物质的量的该物质充分反应(反应时可加热煮沸),则消耗Na、NaOH、NaHCO3、Na2CO3四种物质的物质的量之比为
3∶2∶1:2
⑵酯化反应(以乙酸为例)
【思考与讨论】乙酸与乙醇的酯化反应,从形式上看是羧基与羟基之间脱去一个水分子。脱水时有哪些可能的方式,你能设计一个实验方案来证明是哪一种吗?
同位素示踪法
碳氧键易断裂
﹒取代反应
δ+
δ+
δ-
δ-
O
C
O
H
R
任务三:羧酸的化学性质
酯化反应(取代反应):乙酸分子中羧基的羟基与乙醇分子中羟基的氢原子结合成水,其余部分相互结合成酯。
【思考与讨论】在制取乙酸乙酯的实验中,如果要提高
乙酸乙酯的产率,你认为应当采取哪些措施?请结合化学
反应原理的有关知识进行说明。
现象:饱和碳酸钠溶液的液面上有透明的油状液体,并可闻到香味。
任务三:羧酸的化学性质
根据化学平衡原理,提高乙酸乙酯产率的措施有:
①由于乙酸乙酯的沸点比乙酸、乙醇都低,因此从反应物中不断蒸出乙酸乙酯
可提高其产率。
②使用过量的乙醇,可提高乙酸转化率。
③使用浓H2SO4作吸水剂,提高反应转化率。
④冷凝回流,提高产率。
任务三:羧酸的化学性质
【小结】羧酸的化学性质
(1)酸性
碳氧键易断裂
﹒取代反应
δ+
δ-
δ+
δ-
氧氢键易断裂
﹒酸性
O
C
O
H
R
O O
CH3—C—O—H+H—O— C2H5 CH3—C—O—C2H5 + H2O
浓H2SO4
①使酸碱指示剂变色
②与活泼金属反应
③与碱性氧化物反应
④与碱反应
⑤与弱酸(其对应酸的酸性弱于羧酸)盐反应
(2)酯化反应(取代反应)
