3.4 物质组成的表示式第三课时课件(共27张PPT)
文档属性
| 名称 | 3.4 物质组成的表示式第三课时课件(共27张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 1.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 科粤版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-06-22 00:00:00 | ||
图片预览







文档简介
(共27张PPT)
3.4 物质组成的表示式(课时3)
第三章 维持生命之气—氧气
学习目标
1.了解相对分子质量的涵义,并能利用相对原子质量、相对分子质量进行物质组成的简单计算。
2.通过对物质相对分子质量的计算,让学生熟悉计算的过程。
3.通过交流讨论、活动探究,培养学生善于合作、勤于思考、勇于实践的精神。
新课导入
【回顾】相对原子质量的算法你还记得吗?
相对原子质量=
原子的实际质量
碳12原子质量的1/12
氢原子的相对原子质量
≈ 1
碳原子的相对原子质量
=12
氧原子的相对原子质量
≈ 16
其它元素的相对原子质量可以在元素周期表查询。
一、计算相对分子质量
新课讲解
(1)定义:相对分子质量是化学式中各原子的相对原子
质量总和。
(2)公式:相对分子质量=各原子的相对原子质量的总和
新课讲解
1.计算相对分子质量
相对分子质量:化学式中各原子的相对原子质量总和。
例1计算水的相对分子质量。
解:Mr(H2O)
= 18
= 1×2+16×1
例2计算 NH4NO3 的相对分子质量。
解:Mr(NH4NO3 )
= 14×2+1×4+16×3
= 80
例3计算硫酸铝 Al2(SO4)3 的相对分子质量
解:Mr[Al2(SO4)3 ]
= 27×2+(32×1+16×4)×3
= 342
注意:相对分子质量也是比值,单位为1!!!
新课讲解
计算下列物质的相对分子质量或相对分子质量总和。
(1)水(H2O)
水(H2O)的相对分子质量
=1×2+16
=18
(2)碳酸氢铵(NH4HCO3)
NH4HCO3的相对分子质量
=14+1×5+12 +16×3
=79
典例分析
例
新课讲解
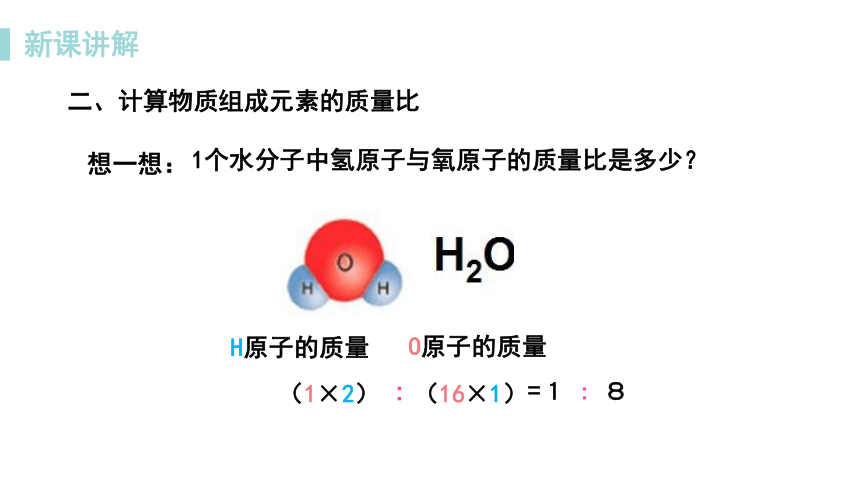
二、计算物质组成元素的质量比
H原子的质量
O原子的质量
(1×2)
(16×1)
=1 : 8
:
1个水分子中氢原子与氧原子的质量比是多少?
想一想:
新课讲解
试计算水中各元素的质量比。
H原子的质量
O原子的质量
2个H2O分子中
=1 : 8
(1×2)x 2
(16×1)x 2
:
2个、10个、100个、n个水分子中氢原子与氧原子的质量比是多少?
n个H2O分子中
=1 : 8
(1×2)x n
(16×1)x n
:
新课讲解
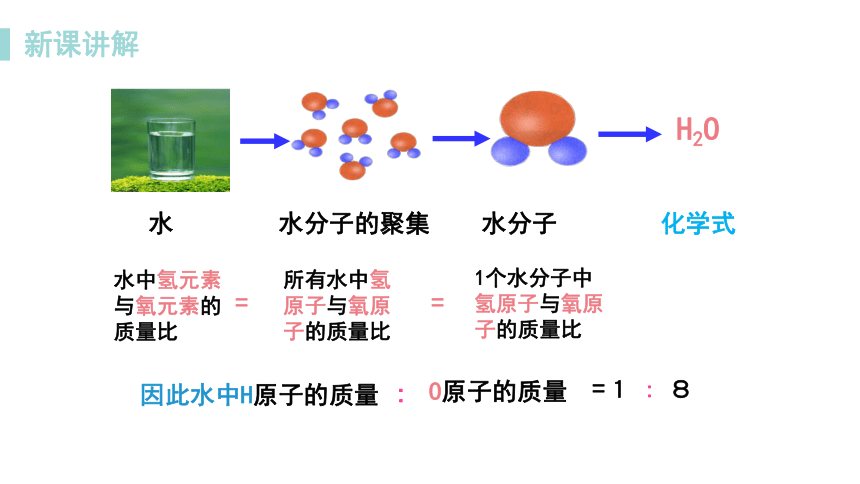
水
H2O
水分子的聚集
水分子
化学式
水中氢元素
与氧元素的
质量比
所有水中氢原子与氧原子的质量比
1个水分子中氢原子与氧原子的质量比
=
=
因此水中H原子的质量
:
O原子的质量
=1 : 8
新课讲解
归纳总结
计算物质组成各元素质量比:化合物中各元素的质量比等于各元素原子的相对原子质量总和之比。
新课讲解
典例分析
例1
(1)计算水( H2O )组成元素的质量比。
解:在H2O中,氢和氧的原子个数比为2:1,则氢元素的质量:氧元素的质量=(1×2)∶16 = 1∶8
新课讲解
解:在H2SO4中,氢、硫、氧的原子个数比为2:1:4。
则氢元素的质量:硫元素的质量:氧元素的质量
=(1×2)∶32∶(16×4)=1∶16∶32
(2)计算硫酸(H2SO4)中各元素的质量比。
新课讲解
三、计算物质中某元素的质量分数
物质中某元素的质量分数,就是该元素的质量与物质总质量之比。
某元素的质量分数=
该元素的相对原子质量×该原子的个数
化合物的相对分子质量
×100%
新课讲解
典例分析
例
计算水( H2O )中氧元素的质量分数。
答:水中氧元素的质量分数为88.9%。
课堂小结
有关化学式的简单计算
当堂小练
1.吸烟危害健康。吸烟时人会吸人多种有害气体,其中有一种是氧化物,它所含的氧元素与另一种元素的质量比为4:3,这种气体是( )
A.CO B.NO
C.CO2 D.SO2
A
D
当堂小练
2.某地1000kg化肥的市场价格如下:CO(NH2)2 1080元,NH4NO3 810元,NH4HCO3(碳酸氢铵)330元。分别用10000元采购上述化肥,则购得化肥中含氮元素最多的是哪一种?
解:用10000元采购上述化肥中氮元素的质量分别为:
1.“达菲”是治疗甲型HINI流感的一种特效药,该药对治疗HN9禽流感也很有疗效。其主要成分是一种化学式为C16H31N2PO8的物质。关于该物质的说法不正确的是( ) 。
A.组成该物质的元素有C、H、N、P、0
B.碳元素和氧元素的质量之比是2 :1
C.相对分子质量为410
D.一个分子中含有58个原子
教材习题
B
教材习题
2.吸烟危害健康。吸烟时人会吸人多种有害气体,其中有一种是氧化物,它所含的氧元素与另一种元素的质量比为4:3,这种气体是( ) 。
A.CO B.NO C.CO2 D.SO2
A
3.“H2SO4” 表示的意义是:
(1)表示物质 。
(2)表示该物质的1个 。
(3)表示该物质由 , 和 元素结合而形成。
(4) 表示该物质的每个分子中含有 个 , 个 ,
个 。
教材习题
硫酸
分子
氢
硫
氧
氢原子
硫原子
氧原子
2
1
4
(5)该物质的相对分子质量是 。
(6)该物质中 , , 元素的质量比为 。
(7).该物质中几种元素的质量分数分别为 , ,
。
教材习题
98
1∶16∶32
O:65.31%
氢
硫
氧
H:2.04%
S:32.65%
4.硫酸铵曾经是广为使用的一种化肥,但施用后会造成土壤板结,目前已较少生产和使用,取而代之的是肥效更高的尿素等。计算尿素[CO(NH)2] 和硫酸铵[(NH,)2S04]中氮元素的质量分数,多少吨硫酸铵的含氮量与1吨尿素的含氮量相当
教材习题
答案:尿素中氮元素的质量分=14×212+16+(14+1×2)×2×100%≈46.7%,
硫酸铵中氮元素的质量分数=14×2(14+4)×2+32+16×4×100%≈21.2%。
设与1 t尿素含氮量相当的硫酸铵的质量为x。
21.2%·x=1 t×46.7%x≈2.2 t
答:2.2吨硫酸铵的含氮量与1吨尿素的含氮量相当。
教材习题
5.有某生产化学肥料碳酸氢铵的企业,在一个公共场所的围墙上做了大型户外广告,局部如下页图:
教材习题
(1)碳酸氢铵的有效成分是氮元素(N),碳酸氢铵氮含量的理论值就是氮元素的质量分数,它等于 。
17.72%
(3)请质量检测部门化验该企业的碳酸氢铵,发现其氮含量仅为12.0%,据此可知该企业生产的“优质碳酸氢铵”产品中,每100kg实际含纯净的碳酸氢铵的质量只有 。
教材习题
(2)该广告宣称其氮含量为20.1%,比理论值高出 ,因此它是 广告。
2.38%
虚假
67.72 kg
教材习题
(4)据调查,此企业广告未经有关管理部门许可,为擅自宣传,且有虚假坑农之嫌。同时,在公共场所乱涂乱画,影响环境。对此,你认为应怎样处理
答案:环卫部门清除非法广告;工商部门依法处理乱涂乱画企业(答案合理即可)。
THANKS
3.4 物质组成的表示式(课时3)
第三章 维持生命之气—氧气
学习目标
1.了解相对分子质量的涵义,并能利用相对原子质量、相对分子质量进行物质组成的简单计算。
2.通过对物质相对分子质量的计算,让学生熟悉计算的过程。
3.通过交流讨论、活动探究,培养学生善于合作、勤于思考、勇于实践的精神。
新课导入
【回顾】相对原子质量的算法你还记得吗?
相对原子质量=
原子的实际质量
碳12原子质量的1/12
氢原子的相对原子质量
≈ 1
碳原子的相对原子质量
=12
氧原子的相对原子质量
≈ 16
其它元素的相对原子质量可以在元素周期表查询。
一、计算相对分子质量
新课讲解
(1)定义:相对分子质量是化学式中各原子的相对原子
质量总和。
(2)公式:相对分子质量=各原子的相对原子质量的总和
新课讲解
1.计算相对分子质量
相对分子质量:化学式中各原子的相对原子质量总和。
例1计算水的相对分子质量。
解:Mr(H2O)
= 18
= 1×2+16×1
例2计算 NH4NO3 的相对分子质量。
解:Mr(NH4NO3 )
= 14×2+1×4+16×3
= 80
例3计算硫酸铝 Al2(SO4)3 的相对分子质量
解:Mr[Al2(SO4)3 ]
= 27×2+(32×1+16×4)×3
= 342
注意:相对分子质量也是比值,单位为1!!!
新课讲解
计算下列物质的相对分子质量或相对分子质量总和。
(1)水(H2O)
水(H2O)的相对分子质量
=1×2+16
=18
(2)碳酸氢铵(NH4HCO3)
NH4HCO3的相对分子质量
=14+1×5+12 +16×3
=79
典例分析
例
新课讲解
二、计算物质组成元素的质量比
H原子的质量
O原子的质量
(1×2)
(16×1)
=1 : 8
:
1个水分子中氢原子与氧原子的质量比是多少?
想一想:
新课讲解
试计算水中各元素的质量比。
H原子的质量
O原子的质量
2个H2O分子中
=1 : 8
(1×2)x 2
(16×1)x 2
:
2个、10个、100个、n个水分子中氢原子与氧原子的质量比是多少?
n个H2O分子中
=1 : 8
(1×2)x n
(16×1)x n
:
新课讲解
水
H2O
水分子的聚集
水分子
化学式
水中氢元素
与氧元素的
质量比
所有水中氢原子与氧原子的质量比
1个水分子中氢原子与氧原子的质量比
=
=
因此水中H原子的质量
:
O原子的质量
=1 : 8
新课讲解
归纳总结
计算物质组成各元素质量比:化合物中各元素的质量比等于各元素原子的相对原子质量总和之比。
新课讲解
典例分析
例1
(1)计算水( H2O )组成元素的质量比。
解:在H2O中,氢和氧的原子个数比为2:1,则氢元素的质量:氧元素的质量=(1×2)∶16 = 1∶8
新课讲解
解:在H2SO4中,氢、硫、氧的原子个数比为2:1:4。
则氢元素的质量:硫元素的质量:氧元素的质量
=(1×2)∶32∶(16×4)=1∶16∶32
(2)计算硫酸(H2SO4)中各元素的质量比。
新课讲解
三、计算物质中某元素的质量分数
物质中某元素的质量分数,就是该元素的质量与物质总质量之比。
某元素的质量分数=
该元素的相对原子质量×该原子的个数
化合物的相对分子质量
×100%
新课讲解
典例分析
例
计算水( H2O )中氧元素的质量分数。
答:水中氧元素的质量分数为88.9%。
课堂小结
有关化学式的简单计算
当堂小练
1.吸烟危害健康。吸烟时人会吸人多种有害气体,其中有一种是氧化物,它所含的氧元素与另一种元素的质量比为4:3,这种气体是( )
A.CO B.NO
C.CO2 D.SO2
A
D
当堂小练
2.某地1000kg化肥的市场价格如下:CO(NH2)2 1080元,NH4NO3 810元,NH4HCO3(碳酸氢铵)330元。分别用10000元采购上述化肥,则购得化肥中含氮元素最多的是哪一种?
解:用10000元采购上述化肥中氮元素的质量分别为:
1.“达菲”是治疗甲型HINI流感的一种特效药,该药对治疗HN9禽流感也很有疗效。其主要成分是一种化学式为C16H31N2PO8的物质。关于该物质的说法不正确的是( ) 。
A.组成该物质的元素有C、H、N、P、0
B.碳元素和氧元素的质量之比是2 :1
C.相对分子质量为410
D.一个分子中含有58个原子
教材习题
B
教材习题
2.吸烟危害健康。吸烟时人会吸人多种有害气体,其中有一种是氧化物,它所含的氧元素与另一种元素的质量比为4:3,这种气体是( ) 。
A.CO B.NO C.CO2 D.SO2
A
3.“H2SO4” 表示的意义是:
(1)表示物质 。
(2)表示该物质的1个 。
(3)表示该物质由 , 和 元素结合而形成。
(4) 表示该物质的每个分子中含有 个 , 个 ,
个 。
教材习题
硫酸
分子
氢
硫
氧
氢原子
硫原子
氧原子
2
1
4
(5)该物质的相对分子质量是 。
(6)该物质中 , , 元素的质量比为 。
(7).该物质中几种元素的质量分数分别为 , ,
。
教材习题
98
1∶16∶32
O:65.31%
氢
硫
氧
H:2.04%
S:32.65%
4.硫酸铵曾经是广为使用的一种化肥,但施用后会造成土壤板结,目前已较少生产和使用,取而代之的是肥效更高的尿素等。计算尿素[CO(NH)2] 和硫酸铵[(NH,)2S04]中氮元素的质量分数,多少吨硫酸铵的含氮量与1吨尿素的含氮量相当
教材习题
答案:尿素中氮元素的质量分=14×212+16+(14+1×2)×2×100%≈46.7%,
硫酸铵中氮元素的质量分数=14×2(14+4)×2+32+16×4×100%≈21.2%。
设与1 t尿素含氮量相当的硫酸铵的质量为x。
21.2%·x=1 t×46.7%x≈2.2 t
答:2.2吨硫酸铵的含氮量与1吨尿素的含氮量相当。
教材习题
5.有某生产化学肥料碳酸氢铵的企业,在一个公共场所的围墙上做了大型户外广告,局部如下页图:
教材习题
(1)碳酸氢铵的有效成分是氮元素(N),碳酸氢铵氮含量的理论值就是氮元素的质量分数,它等于 。
17.72%
(3)请质量检测部门化验该企业的碳酸氢铵,发现其氮含量仅为12.0%,据此可知该企业生产的“优质碳酸氢铵”产品中,每100kg实际含纯净的碳酸氢铵的质量只有 。
教材习题
(2)该广告宣称其氮含量为20.1%,比理论值高出 ,因此它是 广告。
2.38%
虚假
67.72 kg
教材习题
(4)据调查,此企业广告未经有关管理部门许可,为擅自宣传,且有虚假坑农之嫌。同时,在公共场所乱涂乱画,影响环境。对此,你认为应怎样处理
答案:环卫部门清除非法广告;工商部门依法处理乱涂乱画企业(答案合理即可)。
THANKS
同课章节目录
- 第一章 大家都来学化学
- 1.1 身边的化学
- 1.2 化学实验室之旅
- 1.3 物质的变化
- 1.4 物质性质的探究
- 第二章 空气、物质的构成
- 2.1 空气的成分
- 2.2 构成物质的微粒(Ⅰ)——分子
- 2.3 构成物质的微粒(Ⅱ)——原子和离子
- 2.4 辨别物质的元素组成
- 第三章 维持生命之气——氧气
- 3.1 氧气的性质和用途
- 3.2 制取氧气
- 3.3 燃烧条件与灭火原理
- 3.4 物质构成的表示式
- 第四章 生命之源——水
- 4.1 我们的水资源
- 4.2 水的组成
- 4.3 质量守恒定律
- 4.4 化学方程式
- 第五章 燃料
- 5.1 洁净的燃料——氢气
- 5.2 组成燃料的主要元素——碳
- 5.3 二氧化碳的性质和制法
- 5.4 古生物的“遗产”——化石燃料
