5.2 化学反应的表示 课件(共25张PPT)-初中化学鲁教版九年级上册
文档属性
| 名称 | 5.2 化学反应的表示 课件(共25张PPT)-初中化学鲁教版九年级上册 |

|
|
| 格式 | pptx | ||
| 文件大小 | 1.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-06-23 00:00:00 | ||
图片预览







文档简介
(共25张PPT)
初中化学
九年级上 鲁教版
第五单元 定量研究化学反应
第二节 化学反应的表示
目
录
CONTENTS
1
学习目标
新课导入
2
新课讲解
3
课堂小结
4
当堂小练
5
课后习题
6
学习目标
返回
1. 知道化学方程式的定义,能说出化学方程式的基本含义,特别是各物质之间的质量关系;
2. 知道书写化学方程式应遵守的原则;
3. 学会化学方程式的读法;
新课导入
之前我们学习过元素及化合价等内容,知道化学式是如何书写的,而化学式又是怎样表示物质的。今天我们一起学习化学方程式的知识!
返回
一、化学方程式及其意义
新课讲解
定义:用元素符号和分子式来表示化学反应的式子叫化学方程式。
书写原则:
(1)以客观事实为依据,反应是真实存在的
(2)符合质量守恒定律
磷在氧气中燃烧的化学方程式如下,判断正误
(1)P + O2 PO2
(2)P2 + O5 P2O5
(3)P + O2 P2O5
凭空臆造成生成物PO2 ,与事实不符
任意改动氧气化学式,也与事实不符,应为O2
反应前后各原子个数不相等,违背了质量守恒定律
思 考
新课讲解
在左右两边写出反应物和生成物的化学式,并在左右两边之间画一条短线。
配平化学方程式,使遵守质量守恒定律。
表明化学反应发生的条件,把短线改成等号。
写
配
标
【书写化学方程式的步骤】
新课讲解
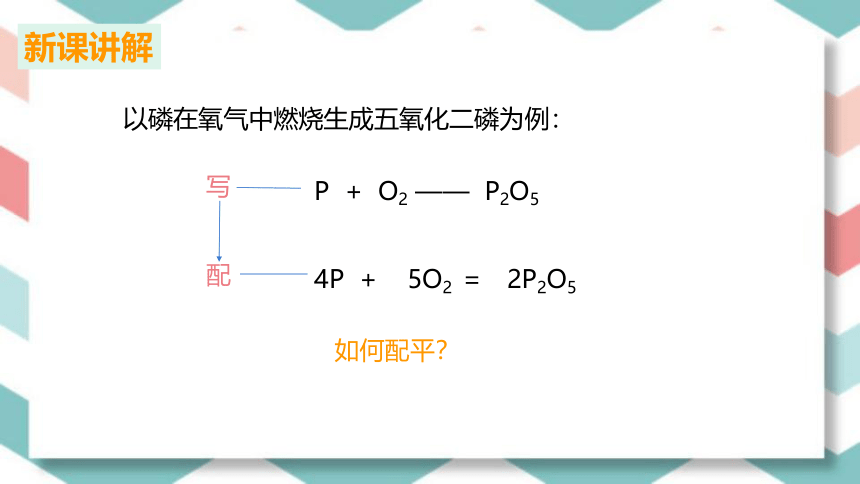
P + O2 —— P2O5
4P + 5O2 = 2P2O5
写
配
以磷在氧气中燃烧生成五氧化二磷为例:
如何配平?
新课讲解
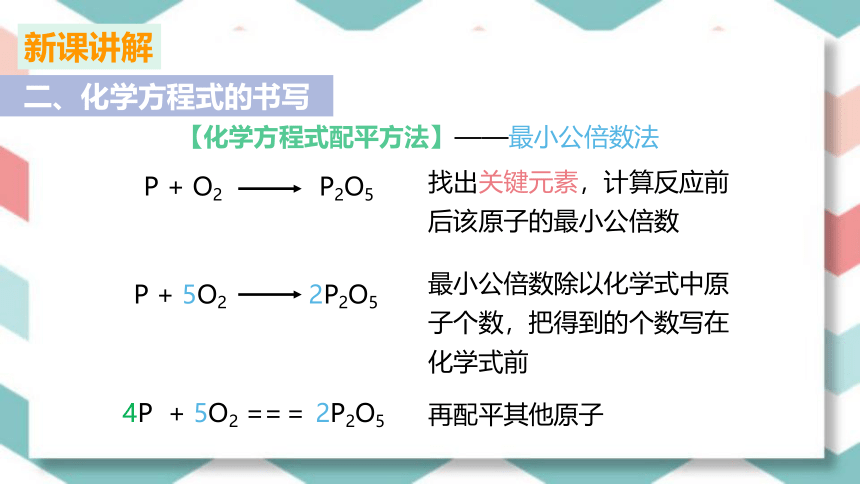
P + O2 P2O5
P + 5O2 2P2O5
找出关键元素,计算反应前后该原子的最小公倍数
最小公倍数除以化学式中原子个数,把得到的个数写在化学式前
4P + 5O2 === 2P2O5
再配平其他原子
新课讲解
【化学方程式配平方法】——最小公倍数法
二、化学方程式的书写
奇偶配平法
C2H2+O2 —— CO2+H2O
1.从先出现次数最多的氧原子配起。O2内有2个氧原子,无论化学式前系数为几,氧原子总数应为偶数。
C2H2+O2 —— CO2+2H2O
2.推知C2H2前2,式子变为:
2C2H2+O2 ——CO2+2H2O
3.配平其他原子,最终结果为:
2C2H2+5O2=== 4CO2+2H2O
新课讲解
观察法
Fe+H2O Fe3O4+H2
1. Fe3O4化学式较复杂,Fe3O4中Fe来源于单质Fe,O来自于H2O,则Fe前配3,H2O前配4,则式子为 3Fe+4H2O Fe3O4+H2
2. 由此推出H2系数为4,写明条件,短线改为等号即可: 3Fe+4H2O ==== Fe3O4+4H2
新课讲解
新课讲解
归 纳
通过上述配平方法,你有什么认识?
奇偶配平法:这种方法适用于化学方程式两边某一元素多次出现,并且两边的该元素原子总数有一奇一偶。
观察法:有时方程式中会出现一种化学式比较复杂的物质,我们可通过这个复杂的分子去推其他化学式的系数
化学方程式配平注意要点
①若生成物中有气体,在气体物质的化学式右边要注“↑”号;若生成物有固体,在固体物质的化学式右边要注“↓”。
②若反应物和生成物中都有气体,在气体物质的化学式右边就不注“↑”号;若反应物和生成物都有固体,在固体物质的化学式右边也不注“↓”。
新课讲解
A、B在反应中的生成物是C,若C的化学式为A2B,则该反应的化学方程式为 ( )
A. A2+B2=2C
B. 2AB+B2=2C
C. 2AB+A2=2C
D. 2A2B+B=2C
新课讲解
典例分析
例
C
新课讲解
解析:A中由A2+B2=2C,将C的化学式AB2,代入方程式中A2+B2=2A2B,可知A原子个数前后不相等,故A错误.B中根据2AB+B2=2C,将C的化学式AB2,代入方程式中得2AB+B2=2A2B,可知A、B原子个数前后不相等,故B错误.C中根据2AB+A2=2C,将C的化学式AB2,代入方程式中得2AB+A2=2A2B,可知A和B原子在反应前后都不变,符合质量守恒定律,故C正确.D中根据2A2B+B=2C,将C的化学式AB2,代入方程式中得2A2B+B=2A2B,可知B原子在反应前后不相等,故D错误.故选C
返回
课堂小结
返回
化
学反应方程式
定义
化学反应式的意义
书写原则
书写步骤
配平方法
1. 只根据化学方程式不能知道的是( )
A.反应物、生成物
B.反应条件
C.各物质之间的质量之比
D.各物质的物理性质
D
当堂小练
D
2.下列关于S+O2===SO2的理解不正确的是 ( )
A.表示硫与氧气在点燃条件下反应生成二氧化硫
B.参加反应的硫与氧气的质量比是2 : 1
C.反应前后硫原子.氧原子的个数均不变
D.参加反应的氧气与生成的二氧化硫的分子个数比为1 : 1
当堂小练
B
点燃
3. 化学方程式2CO+O2 ===== 2CO2的读法不正确的是 ( )
A.一氧化碳和氧气在点燃的条件下生成二氧化碳
B.一氧化碳加氧气等于二氧化碳
C.在点燃条件下,每2个一氧化碳分子与1个氧分子反应生成2个二氧化碳分子
D.每56份质量的一氧化碳和32份质量的氧气在点燃的条件下生成88份质量的二氧化碳
D
当堂小练
B
返回
点燃
1.下列关于化学方程式 含义的叙述中,正确的是( )。
A.可表示双氧水是由水和氧气化合而成的
B.双氧水在催化剂的存在下分解生成水和氧气
C.2个双氧水分解生成2个水和1个氧气
D.在催化剂存在的条件下,每34份质量的双氧水分解生成16份质量的氧气和18份质量的水
课后习题
答案:BD
解析:由化学方程式可知,在催化剂作用下,每68份质量的双氧水分解生成36份质量的水和32份质量的氧气;每2个过氧化氢分子分解生成2个水分子和1个氧分子。
课后习题
2. 某化合物X在氧气中完全燃烧,反应的化学方程式为:
试写出X的化学式。
答案: C2H4
解析:根据质量守恒定律,反应前后原子种类和数目不发生改变,推知X的化学式为C2H4。
课后习题
3.下列化学方程式书写是否正确 若不正确,请改正。
(1)氢气在氧气中燃烧:
(2)铁在氧气中燃烧:
答案: (1)不正确;正确的写法应为
(2)不正确;正确的写法应为
课后习题
4.写出下列反应的化学方程式,计算反应中各物质间的质量比。
( 1 )镁在氧气中燃烧;
(2)氧化铜和碳在加热条件下反应生成铜和二氧化碳;
(3)乙醇(化学式为C2H6O)在氧气中燃烧生成二氧化碳和水。
课后习题
答案:(1)
反应中镁、氧气和氧化镁的质量比为48:32:80。
(2)
反应中氧化铜、碳、铜和二氧化碳的质量比为160:12:128:44
(3)
反应中乙醇、氧气、二氧化碳和水的质量比为46:96:88:54。
课后习题
初中化学
九年级上 鲁教版
第五单元 定量研究化学反应
第二节 化学反应的表示
目
录
CONTENTS
1
学习目标
新课导入
2
新课讲解
3
课堂小结
4
当堂小练
5
课后习题
6
学习目标
返回
1. 知道化学方程式的定义,能说出化学方程式的基本含义,特别是各物质之间的质量关系;
2. 知道书写化学方程式应遵守的原则;
3. 学会化学方程式的读法;
新课导入
之前我们学习过元素及化合价等内容,知道化学式是如何书写的,而化学式又是怎样表示物质的。今天我们一起学习化学方程式的知识!
返回
一、化学方程式及其意义
新课讲解
定义:用元素符号和分子式来表示化学反应的式子叫化学方程式。
书写原则:
(1)以客观事实为依据,反应是真实存在的
(2)符合质量守恒定律
磷在氧气中燃烧的化学方程式如下,判断正误
(1)P + O2 PO2
(2)P2 + O5 P2O5
(3)P + O2 P2O5
凭空臆造成生成物PO2 ,与事实不符
任意改动氧气化学式,也与事实不符,应为O2
反应前后各原子个数不相等,违背了质量守恒定律
思 考
新课讲解
在左右两边写出反应物和生成物的化学式,并在左右两边之间画一条短线。
配平化学方程式,使遵守质量守恒定律。
表明化学反应发生的条件,把短线改成等号。
写
配
标
【书写化学方程式的步骤】
新课讲解
P + O2 —— P2O5
4P + 5O2 = 2P2O5
写
配
以磷在氧气中燃烧生成五氧化二磷为例:
如何配平?
新课讲解
P + O2 P2O5
P + 5O2 2P2O5
找出关键元素,计算反应前后该原子的最小公倍数
最小公倍数除以化学式中原子个数,把得到的个数写在化学式前
4P + 5O2 === 2P2O5
再配平其他原子
新课讲解
【化学方程式配平方法】——最小公倍数法
二、化学方程式的书写
奇偶配平法
C2H2+O2 —— CO2+H2O
1.从先出现次数最多的氧原子配起。O2内有2个氧原子,无论化学式前系数为几,氧原子总数应为偶数。
C2H2+O2 —— CO2+2H2O
2.推知C2H2前2,式子变为:
2C2H2+O2 ——CO2+2H2O
3.配平其他原子,最终结果为:
2C2H2+5O2=== 4CO2+2H2O
新课讲解
观察法
Fe+H2O Fe3O4+H2
1. Fe3O4化学式较复杂,Fe3O4中Fe来源于单质Fe,O来自于H2O,则Fe前配3,H2O前配4,则式子为 3Fe+4H2O Fe3O4+H2
2. 由此推出H2系数为4,写明条件,短线改为等号即可: 3Fe+4H2O ==== Fe3O4+4H2
新课讲解
新课讲解
归 纳
通过上述配平方法,你有什么认识?
奇偶配平法:这种方法适用于化学方程式两边某一元素多次出现,并且两边的该元素原子总数有一奇一偶。
观察法:有时方程式中会出现一种化学式比较复杂的物质,我们可通过这个复杂的分子去推其他化学式的系数
化学方程式配平注意要点
①若生成物中有气体,在气体物质的化学式右边要注“↑”号;若生成物有固体,在固体物质的化学式右边要注“↓”。
②若反应物和生成物中都有气体,在气体物质的化学式右边就不注“↑”号;若反应物和生成物都有固体,在固体物质的化学式右边也不注“↓”。
新课讲解
A、B在反应中的生成物是C,若C的化学式为A2B,则该反应的化学方程式为 ( )
A. A2+B2=2C
B. 2AB+B2=2C
C. 2AB+A2=2C
D. 2A2B+B=2C
新课讲解
典例分析
例
C
新课讲解
解析:A中由A2+B2=2C,将C的化学式AB2,代入方程式中A2+B2=2A2B,可知A原子个数前后不相等,故A错误.B中根据2AB+B2=2C,将C的化学式AB2,代入方程式中得2AB+B2=2A2B,可知A、B原子个数前后不相等,故B错误.C中根据2AB+A2=2C,将C的化学式AB2,代入方程式中得2AB+A2=2A2B,可知A和B原子在反应前后都不变,符合质量守恒定律,故C正确.D中根据2A2B+B=2C,将C的化学式AB2,代入方程式中得2A2B+B=2A2B,可知B原子在反应前后不相等,故D错误.故选C
返回
课堂小结
返回
化
学反应方程式
定义
化学反应式的意义
书写原则
书写步骤
配平方法
1. 只根据化学方程式不能知道的是( )
A.反应物、生成物
B.反应条件
C.各物质之间的质量之比
D.各物质的物理性质
D
当堂小练
D
2.下列关于S+O2===SO2的理解不正确的是 ( )
A.表示硫与氧气在点燃条件下反应生成二氧化硫
B.参加反应的硫与氧气的质量比是2 : 1
C.反应前后硫原子.氧原子的个数均不变
D.参加反应的氧气与生成的二氧化硫的分子个数比为1 : 1
当堂小练
B
点燃
3. 化学方程式2CO+O2 ===== 2CO2的读法不正确的是 ( )
A.一氧化碳和氧气在点燃的条件下生成二氧化碳
B.一氧化碳加氧气等于二氧化碳
C.在点燃条件下,每2个一氧化碳分子与1个氧分子反应生成2个二氧化碳分子
D.每56份质量的一氧化碳和32份质量的氧气在点燃的条件下生成88份质量的二氧化碳
D
当堂小练
B
返回
点燃
1.下列关于化学方程式 含义的叙述中,正确的是( )。
A.可表示双氧水是由水和氧气化合而成的
B.双氧水在催化剂的存在下分解生成水和氧气
C.2个双氧水分解生成2个水和1个氧气
D.在催化剂存在的条件下,每34份质量的双氧水分解生成16份质量的氧气和18份质量的水
课后习题
答案:BD
解析:由化学方程式可知,在催化剂作用下,每68份质量的双氧水分解生成36份质量的水和32份质量的氧气;每2个过氧化氢分子分解生成2个水分子和1个氧分子。
课后习题
2. 某化合物X在氧气中完全燃烧,反应的化学方程式为:
试写出X的化学式。
答案: C2H4
解析:根据质量守恒定律,反应前后原子种类和数目不发生改变,推知X的化学式为C2H4。
课后习题
3.下列化学方程式书写是否正确 若不正确,请改正。
(1)氢气在氧气中燃烧:
(2)铁在氧气中燃烧:
答案: (1)不正确;正确的写法应为
(2)不正确;正确的写法应为
课后习题
4.写出下列反应的化学方程式,计算反应中各物质间的质量比。
( 1 )镁在氧气中燃烧;
(2)氧化铜和碳在加热条件下反应生成铜和二氧化碳;
(3)乙醇(化学式为C2H6O)在氧气中燃烧生成二氧化碳和水。
课后习题
答案:(1)
反应中镁、氧气和氧化镁的质量比为48:32:80。
(2)
反应中氧化铜、碳、铜和二氧化碳的质量比为160:12:128:44
(3)
反应中乙醇、氧气、二氧化碳和水的质量比为46:96:88:54。
课后习题
同课章节目录
- 第一单元 步入化学殿堂
- 第一节 化学真奇妙
- 第二节 体验化学探究
- 到实验室去:化学实验基本技能训练(一)
- 第二单元 探秘水世界
- 第一节 运动的水分子
- 第二节 水分子的变化
- 第三节 原子的构成
- 第四节 元素
- 到实验室去:化学实验基本技能训练(二)
- 第三单元 溶液
- 第一节 溶液的形成
- 第二节 溶液组成的定量表示
- 到实验室去:配制一定溶质质量分数的溶液
- 第四单元 我们周围的空气
- 第一节 空气的成分
- 第二节 物质组成的表示
- 第三节 氧气
- 到实验室去:氧气的实验室制取与性质
- 第五单元 定量研究化学反应
- 第一节 化学反应中的质量守恒
- 第二节 化学反应的表示
- 第三节 化学反应中的有关计算
- 到实验室去:探究燃烧的条件
- 第六单元 燃烧与燃料
- 第一节 燃烧与灭火
- 第二节 化石燃料的利用
- 第三节 大自然中的二氧化碳
- 到实验室去:二氧化碳的实验室制取与性质
