6.3 大自然中的二氧化碳 课件(共29张PPT)-初中化学鲁教版九年级上册
文档属性
| 名称 | 6.3 大自然中的二氧化碳 课件(共29张PPT)-初中化学鲁教版九年级上册 |

|
|
| 格式 | pptx | ||
| 文件大小 | 2.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-06-23 00:00:00 | ||
图片预览








文档简介
(共29张PPT)
初中化学
九年级上 鲁教版
第六单元 燃烧与燃料
第三节 大气中的二氧化碳
目
录
CONTENTS
1
学习目标
新课导入
2
新课讲解
3
课堂小结
4
当堂小练
5
课后习题
6
学习目标
返回
1. 认识二氧化碳的主要物理性质和化学性质;了解二氧化碳在自然界碳循环中的作用,以及对人类生产生活的意义。
2. 初步学会运用各种媒体获取信息;初步学会用归纳,概括等方法对获取的信息进行加工处理。
新课导入
近一百多年来,人类对化石燃料持续进行的大规模开采和利用,使其储量急剧减少,同时导致地球大气中二氧化碳含量持续升高。如此一来,二氧化碳在大自然中的循环还能够保持平衡吗 二氧化碳在大气中的含量升高会对自然环境产生怎样的影响
返回
一、二氧化碳的循环
新课讲解
请你根据已有的知识和日常生活经验,完成下列表格。
想一想
新课讲解
大气中二氧化碳的产生途径
大气中二氧化碳的消耗途径
1、动物的呼吸
2、植物的呼吸
3、微生物的分解作用
4、燃烧产生
5、工业废气
植物的呼吸
新课讲解
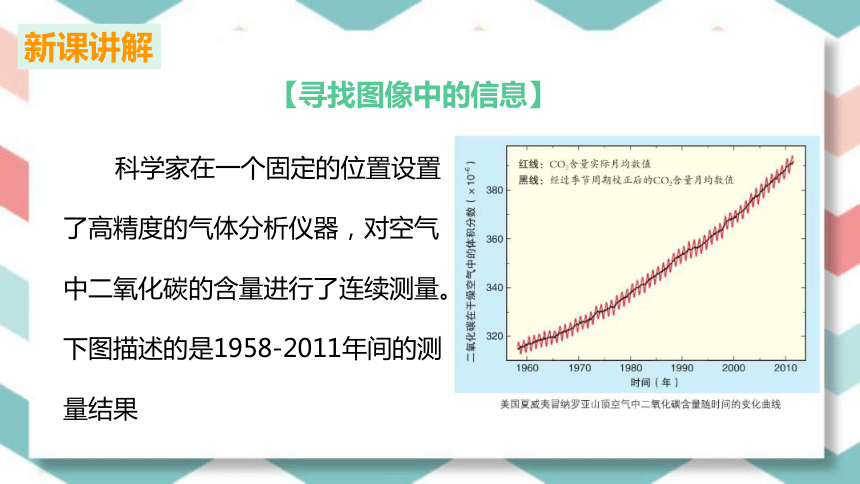
【寻找图像中的信息】
科学家在一个固定的位置设置了高精度的气体分析仪器,对空气中二氧化碳的含量进行了连续测量。下图描述的是1958-2011年间的测量结果
新课讲解
【寻找图像中的信息】
1.认真观察上页图中曲线的形状和走势,想一想:
图中红色曲线反映出的同一年度内空气中二氧化碳含量是如何变化的 是不是每一年都在重复同样的变化规律 原因是什么
在不同年度,空气中二氧化碳含量的变化呈现了怎样的趋势
(3) 你还能从这幅图中获得哪些信息
新课讲解
【寻找图像中的信息】
2.观察下图,分析二氧化碳产生和消耗的途径,试讨论:
二氧化碳是怎样循环的
(2)二氧化碳的循环对自然界和人类社会有什么意义
(3) 导致大气中二氧化碳含量逐年升高的可能原因是什么 ( 图中数字表示通过不同途径产生或消耗碳量的相对值)
新课讲解
【寻找图像中的信息】
新课讲解
【二氧化碳对环境的影响】
随着工业生产的发展和人们生活水平的提高,煤、石油和天然气的消耗量急剧增加,释放的二氧化碳越来越多,而吸收二氧化碳的森林因为天灾和被滥砍乱伐而不断减少,使得空气中二氧化碳的含量呈上升趋势。当大气中二氧化碳等气体的含量升高时,会增强大气对太阳光中红外线辐射的吸收,阻止地球表面的热量向外散发,使地球表面的平均气温上升,这就是所谓的“温室效应“
自然界中二氧化碳的循环如图6-3-1所示,下列过程放在X处
不合理的是 ( )
A.人和动物的呼吸
B.植物的呼吸作用
C.化石燃料的燃烧
D.利用太阳能发电
新课讲解
典例分析
例
D
新课讲解
解析:从图示中可以看出X处产生二氧化碳,我们都知道人和动植物的呼吸能产生二氧化碳,化石燃料的大量使用也能产生二氧化碳,而利用太阳能发电不产生二氧化碳。
新课讲解
在通常情况下,1L水中大约溶解1L二氧化碳气体,生产汽水就利用了二氧化碳这一性质,在加压条件下将二氧化碳溶解在饮料中。但为什么汽水又叫“碳酸饮料”呢?
二、二氧化碳的性质
新课讲解
【二氧化碳的物理性质】
在通常状况下,二氧化碳是一种无色、能溶于水的气体,密度约为空气的1.5倍。二氧化碳气体在-定压强和低温条件下能够变成白色块状或片状固体俗称“干冰”。
新课讲解
干冰不融化成液体,直接升华为二氧化碳气体,升华时会吸收大量的热。所以干冰是一种环保型制冷剂,可用于人工降雨、食物储运、制造舞台烟雾效果等。
新课讲解
【二氧化碳的化学性质】
1.二氧化碳是一种常见的气体,实验室里可以用大理石或石灰石 (主要成分都为CaCO ) 和稀盐酸(HCl)反应来制取,反应的化学方程式为:
新课讲解
【二氧化碳的化学性质】
2.二.氧化碳溶于水后,部分和水反应,生成了碳酸。
反应的化学方程式为:
碳酸的水溶液能使紫色石蕊试液变成红色。
3.二氧化碳还能与氢氧化钙[Ca(OH) ]的水溶液( 俗称石灰水)反应,生成碳酸钙和水。
反应的化学方程式为:
这一反应可用于检验二氧化碳的存在。
新课讲解
【二氧化碳的用途】
下列有关二氧化碳的实验中,只能证明二氧化碳物理性质的是 ( )
新课讲解
典例分析
例
B
新课讲解
解析:(1)解析:二氧化碳使蜡烛由下到上依次熄灭,证明了二氧化碳的密度比空气大(物理性质),且不助燃、不可燃(化学性质),A错误;二氧化碳倾倒后,后端下沉,只能证明二氧化碳的密度比空气的大(物理性质) ,B正确;二氧化碳与水反应生成的碳酸,使紫色石蕊溶液变红,验证了二氧化碳的化学性质,C错误;瓶子变瘪,澄清石灰水变浑浊,验证的是二氧化碳的化学性质,D错误。
课堂小结
返回
大
自然
中的二氧化碳
二氧化碳的循环及环境的影响
二氧化碳的性质
物理性质
化学性质
1.下列操作中只发生物理变化的是( )
A.将二氧化碳通入水中
B.将二氧化碳通入澄清石灰水中
C.将二氧化碳倾倒入盛有燃着蜡烛的烧杯中
D.将二氧化碳加压降温压缩成干冰
D
当堂小练
D
2.将二氧化碳气体通入紫色石蕊试液中,再加热溶液,颜色变化过程为( )
A.红色---红色----无色
B.紫色----红色----无色
C.紫色----红色----紫色
D.红色----蓝色----无色
D
当堂小练
C
3.下列反应既不属于化合反应,也不属于分解反应的是 ( )
A、硫 + 氧气 → 二氧化硫
B、氧化钙 + 水 → 氢氧化钙
C、甲烷 + 氧气 → 二氧化碳 + 水
D、高锰酸钾→锰酸钾 + 二氧化锰 + 氧气
D
当堂小练
C
1.大气中的二氧化碳有哪些来源 大自然通过哪些途径消耗二氧化碳
提示:可从教材P132“自然界中二氧化碳的循环”图中寻找答案。
课后习题
2. 有两个集气瓶,分别盛满了氧气和二氧化碳,用哪些方法可以区别这两种气体
答案: (1)用带火星的木条分别放人两个集气瓶中,使木条复燃的是O2,使木条熄灭的是CO2 ;(2)分别向两个集气瓶中加人紫色石蕊试液,使其变红的是CO2 ,不变红的是02;(3)分别向两个集气瓶中加入少量澄清石灰水,变浑浊的是CO2 ,不变浑浊的是02。
课后习题
3.用化学知识解释下列现象:
(1)用石灰浆[主要成分是Ca(OH)2]涂抹的墙壁,往往表面已干燥一段时间之后,又会出现水珠。
(2)实验室中长期盛放石灰水的玻璃试剂瓶内壁上会附着一层白色固体物质,用水难以去除,需用稀盐酸清洗。
课后习题
答案:(1)石灰浆的主要成分是Ca(0H)2,涂抹墙壁上后会与空气中的二氧化碳反应,生成白色的碳酸钙和水,反应的化学方程式为Ca(OH)2+CO2 =CaCO3↓+H2O。
(2)长期盛放石灰水的玻璃试剂瓶内壁会附着一层白色固体,白色固体是碳酸钙,难溶于水。所以,用水难以去除,需用稀盐酸清洗,这是因为白色碳酸钙沉淀与稀盐酸反应生成可以溶解的氯化钙、水和二氧化碳。反应的化学方程式为CaCO3 +2HCl= CaCl2+H2O+CO2↑。
课后习题
初中化学
九年级上 鲁教版
第六单元 燃烧与燃料
第三节 大气中的二氧化碳
目
录
CONTENTS
1
学习目标
新课导入
2
新课讲解
3
课堂小结
4
当堂小练
5
课后习题
6
学习目标
返回
1. 认识二氧化碳的主要物理性质和化学性质;了解二氧化碳在自然界碳循环中的作用,以及对人类生产生活的意义。
2. 初步学会运用各种媒体获取信息;初步学会用归纳,概括等方法对获取的信息进行加工处理。
新课导入
近一百多年来,人类对化石燃料持续进行的大规模开采和利用,使其储量急剧减少,同时导致地球大气中二氧化碳含量持续升高。如此一来,二氧化碳在大自然中的循环还能够保持平衡吗 二氧化碳在大气中的含量升高会对自然环境产生怎样的影响
返回
一、二氧化碳的循环
新课讲解
请你根据已有的知识和日常生活经验,完成下列表格。
想一想
新课讲解
大气中二氧化碳的产生途径
大气中二氧化碳的消耗途径
1、动物的呼吸
2、植物的呼吸
3、微生物的分解作用
4、燃烧产生
5、工业废气
植物的呼吸
新课讲解
【寻找图像中的信息】
科学家在一个固定的位置设置了高精度的气体分析仪器,对空气中二氧化碳的含量进行了连续测量。下图描述的是1958-2011年间的测量结果
新课讲解
【寻找图像中的信息】
1.认真观察上页图中曲线的形状和走势,想一想:
图中红色曲线反映出的同一年度内空气中二氧化碳含量是如何变化的 是不是每一年都在重复同样的变化规律 原因是什么
在不同年度,空气中二氧化碳含量的变化呈现了怎样的趋势
(3) 你还能从这幅图中获得哪些信息
新课讲解
【寻找图像中的信息】
2.观察下图,分析二氧化碳产生和消耗的途径,试讨论:
二氧化碳是怎样循环的
(2)二氧化碳的循环对自然界和人类社会有什么意义
(3) 导致大气中二氧化碳含量逐年升高的可能原因是什么 ( 图中数字表示通过不同途径产生或消耗碳量的相对值)
新课讲解
【寻找图像中的信息】
新课讲解
【二氧化碳对环境的影响】
随着工业生产的发展和人们生活水平的提高,煤、石油和天然气的消耗量急剧增加,释放的二氧化碳越来越多,而吸收二氧化碳的森林因为天灾和被滥砍乱伐而不断减少,使得空气中二氧化碳的含量呈上升趋势。当大气中二氧化碳等气体的含量升高时,会增强大气对太阳光中红外线辐射的吸收,阻止地球表面的热量向外散发,使地球表面的平均气温上升,这就是所谓的“温室效应“
自然界中二氧化碳的循环如图6-3-1所示,下列过程放在X处
不合理的是 ( )
A.人和动物的呼吸
B.植物的呼吸作用
C.化石燃料的燃烧
D.利用太阳能发电
新课讲解
典例分析
例
D
新课讲解
解析:从图示中可以看出X处产生二氧化碳,我们都知道人和动植物的呼吸能产生二氧化碳,化石燃料的大量使用也能产生二氧化碳,而利用太阳能发电不产生二氧化碳。
新课讲解
在通常情况下,1L水中大约溶解1L二氧化碳气体,生产汽水就利用了二氧化碳这一性质,在加压条件下将二氧化碳溶解在饮料中。但为什么汽水又叫“碳酸饮料”呢?
二、二氧化碳的性质
新课讲解
【二氧化碳的物理性质】
在通常状况下,二氧化碳是一种无色、能溶于水的气体,密度约为空气的1.5倍。二氧化碳气体在-定压强和低温条件下能够变成白色块状或片状固体俗称“干冰”。
新课讲解
干冰不融化成液体,直接升华为二氧化碳气体,升华时会吸收大量的热。所以干冰是一种环保型制冷剂,可用于人工降雨、食物储运、制造舞台烟雾效果等。
新课讲解
【二氧化碳的化学性质】
1.二氧化碳是一种常见的气体,实验室里可以用大理石或石灰石 (主要成分都为CaCO ) 和稀盐酸(HCl)反应来制取,反应的化学方程式为:
新课讲解
【二氧化碳的化学性质】
2.二.氧化碳溶于水后,部分和水反应,生成了碳酸。
反应的化学方程式为:
碳酸的水溶液能使紫色石蕊试液变成红色。
3.二氧化碳还能与氢氧化钙[Ca(OH) ]的水溶液( 俗称石灰水)反应,生成碳酸钙和水。
反应的化学方程式为:
这一反应可用于检验二氧化碳的存在。
新课讲解
【二氧化碳的用途】
下列有关二氧化碳的实验中,只能证明二氧化碳物理性质的是 ( )
新课讲解
典例分析
例
B
新课讲解
解析:(1)解析:二氧化碳使蜡烛由下到上依次熄灭,证明了二氧化碳的密度比空气大(物理性质),且不助燃、不可燃(化学性质),A错误;二氧化碳倾倒后,后端下沉,只能证明二氧化碳的密度比空气的大(物理性质) ,B正确;二氧化碳与水反应生成的碳酸,使紫色石蕊溶液变红,验证了二氧化碳的化学性质,C错误;瓶子变瘪,澄清石灰水变浑浊,验证的是二氧化碳的化学性质,D错误。
课堂小结
返回
大
自然
中的二氧化碳
二氧化碳的循环及环境的影响
二氧化碳的性质
物理性质
化学性质
1.下列操作中只发生物理变化的是( )
A.将二氧化碳通入水中
B.将二氧化碳通入澄清石灰水中
C.将二氧化碳倾倒入盛有燃着蜡烛的烧杯中
D.将二氧化碳加压降温压缩成干冰
D
当堂小练
D
2.将二氧化碳气体通入紫色石蕊试液中,再加热溶液,颜色变化过程为( )
A.红色---红色----无色
B.紫色----红色----无色
C.紫色----红色----紫色
D.红色----蓝色----无色
D
当堂小练
C
3.下列反应既不属于化合反应,也不属于分解反应的是 ( )
A、硫 + 氧气 → 二氧化硫
B、氧化钙 + 水 → 氢氧化钙
C、甲烷 + 氧气 → 二氧化碳 + 水
D、高锰酸钾→锰酸钾 + 二氧化锰 + 氧气
D
当堂小练
C
1.大气中的二氧化碳有哪些来源 大自然通过哪些途径消耗二氧化碳
提示:可从教材P132“自然界中二氧化碳的循环”图中寻找答案。
课后习题
2. 有两个集气瓶,分别盛满了氧气和二氧化碳,用哪些方法可以区别这两种气体
答案: (1)用带火星的木条分别放人两个集气瓶中,使木条复燃的是O2,使木条熄灭的是CO2 ;(2)分别向两个集气瓶中加人紫色石蕊试液,使其变红的是CO2 ,不变红的是02;(3)分别向两个集气瓶中加入少量澄清石灰水,变浑浊的是CO2 ,不变浑浊的是02。
课后习题
3.用化学知识解释下列现象:
(1)用石灰浆[主要成分是Ca(OH)2]涂抹的墙壁,往往表面已干燥一段时间之后,又会出现水珠。
(2)实验室中长期盛放石灰水的玻璃试剂瓶内壁上会附着一层白色固体物质,用水难以去除,需用稀盐酸清洗。
课后习题
答案:(1)石灰浆的主要成分是Ca(0H)2,涂抹墙壁上后会与空气中的二氧化碳反应,生成白色的碳酸钙和水,反应的化学方程式为Ca(OH)2+CO2 =CaCO3↓+H2O。
(2)长期盛放石灰水的玻璃试剂瓶内壁会附着一层白色固体,白色固体是碳酸钙,难溶于水。所以,用水难以去除,需用稀盐酸清洗,这是因为白色碳酸钙沉淀与稀盐酸反应生成可以溶解的氯化钙、水和二氧化碳。反应的化学方程式为CaCO3 +2HCl= CaCl2+H2O+CO2↑。
课后习题
同课章节目录
- 第一单元 步入化学殿堂
- 第一节 化学真奇妙
- 第二节 体验化学探究
- 到实验室去:化学实验基本技能训练(一)
- 第二单元 探秘水世界
- 第一节 运动的水分子
- 第二节 水分子的变化
- 第三节 原子的构成
- 第四节 元素
- 到实验室去:化学实验基本技能训练(二)
- 第三单元 溶液
- 第一节 溶液的形成
- 第二节 溶液组成的定量表示
- 到实验室去:配制一定溶质质量分数的溶液
- 第四单元 我们周围的空气
- 第一节 空气的成分
- 第二节 物质组成的表示
- 第三节 氧气
- 到实验室去:氧气的实验室制取与性质
- 第五单元 定量研究化学反应
- 第一节 化学反应中的质量守恒
- 第二节 化学反应的表示
- 第三节 化学反应中的有关计算
- 到实验室去:探究燃烧的条件
- 第六单元 燃烧与燃料
- 第一节 燃烧与灭火
- 第二节 化石燃料的利用
- 第三节 大自然中的二氧化碳
- 到实验室去:二氧化碳的实验室制取与性质
