到实验室 配制一定溶质质量分数的溶液-初中化学鲁教版九年级上册(共19张PPT)
文档属性
| 名称 | 到实验室 配制一定溶质质量分数的溶液-初中化学鲁教版九年级上册(共19张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 1.9MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-06-23 00:00:00 | ||
图片预览






文档简介
(共19张PPT)
初中化学
九年级上 鲁教版
第三单元 溶液
到实验室去:配制一定溶质质量分数的溶液
目
录
CONTENTS
1
学习目标
新课导入
2
新课讲解
3
课堂小结
4
当堂小练
5
学习目标
返回
1.会进行溶质质量分数相关的简单计算。
2.会配制一定溶质质量分数的溶液。
新课导入
上图信息中0.9%是什么含义呢?这些溶液是如何得到的呢?在实验室你能配制这样的溶液吗?要使用到哪些仪器呢?具体的操作步骤是什么呢?
返回
一、配制一定溶质质量分数的溶液
新课讲解
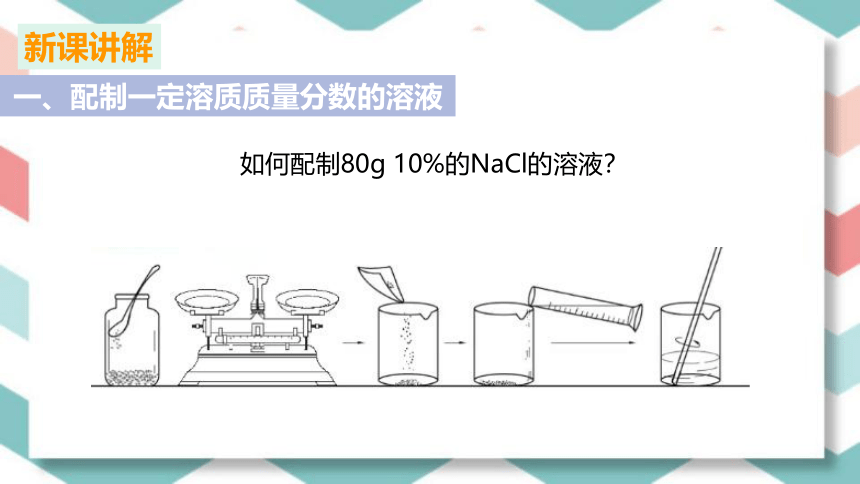
如何配制80g 10%的NaCl的溶液?
新课讲解
【实验前分析】
实验药品:氯化钠、蒸馏水
实验仪器:托盘天平 、药匙 、量筒、 胶头 滴管、烧杯 、玻璃棒 、细口瓶
实验原理:溶质质量分数=溶质质量/溶液质量*100%
实验方法:计算出溶质溶剂的量,用天平和量筒分别测出溶质溶剂的量,按要求配制
新课讲解
【托盘天平使用】
注意事项:
(1)使用前要调零
(2)两个托盘上各放一张大小相同的称量纸
(3)称量时遵循左物右码的原则
(4)用镊子夹取砝码应按照从大到小的顺序
(5)称量完毕应将砝码放回盒中,游码归零
新课讲解
液体的量取
用量简量取液体时,先向量简里倾倒液体至接近所需刻度,然后将量简平放在桌面上,再用胶头滴管滴加液体至该刻度。
【量筒的使用】
新课讲解
俯视——读数偏大
平视——读数与真实值一致
仰视——读数偏小
( 1 )计算: NaCl ____g H2O g
( 2 )称量、量取:用_________称量2.5g食盐,用__________量取47.5mL水
( 3 )溶解:将溶质和溶剂在烧杯中混合,搅拌至溶质完全溶解。
实验步骤:
2.5
47.5
托盘天平
量筒
新课讲解
( 4 ) 装瓶:(盖好瓶塞贴上标签)
按上图所示步骤完成实验并将表格中各项内容补充完整。
步骤名称 操作方法
计算
2、
3、
4、
新课讲解
新课讲解
注意事项
用玻璃棒搅拌时,要注意尽量不要使玻璃棒碰触容器的器壁。
新课讲解
【误差分析】
1. 造成实际值偏小的可能原因
①溶质溶解的量变少了:溶质本身不纯 ;左码右物称量;溶质有撒落;溶质没有完全溶解就装瓶存放了
②溶剂的量增多了:仰视量取;烧杯内壁上有水;试剂瓶内壁上有水
2. 造成实际值偏大的可能原因
①溶剂的量减少了: 俯视量取溶剂;量取的水没有完全转移到烧杯中
②溶质溶解的量变多了:称量时,所用砝码已生锈或沾有油污
欲配制 100 g 质量分数为 10%的氯化钠溶液,需要的仪器组合是 ( )
①托盘天平;②烧杯;③玻璃棒;④100 mL 量筒
A.①②
B.①②③
C.①②③④
D.①②④
新课讲解
典例分析
例
C
新课讲解
解析:配制溶质质量分数一定的溶液的基本步骤:计算、
称量、量取、溶解、装瓶存放,其中需要用到的仪器有:
烧杯、玻璃棒、量筒、胶头滴管、天平、药匙,答案选C。
返回
课堂小结
返回
配制一定溶质质量分数的溶液
溶液配制的步骤
1.计算
2.称量、量取
3.溶解
2.装瓶
1.欲配制 100 g 质量分数为 10%的氯化钠溶液,需要的仪器组合是①托盘天平;②烧杯;③玻璃棒;④100 mL 量筒。( )
A.①②
B.①②③
C.①②③④
D.①②④
当堂小练
C
2.配制2000g生理盐水(溶质质量分数为0.9%)需要称取 NaCl 的质量为( )
A. 9g
B. 18g
C.90g
D. 180g
当堂小练
B
3.在配制一定溶质质量分数的氯化钠溶液的实验中,下列实验操作不正确的是 ( )
D
当堂小练
C
返回
初中化学
九年级上 鲁教版
第三单元 溶液
到实验室去:配制一定溶质质量分数的溶液
目
录
CONTENTS
1
学习目标
新课导入
2
新课讲解
3
课堂小结
4
当堂小练
5
学习目标
返回
1.会进行溶质质量分数相关的简单计算。
2.会配制一定溶质质量分数的溶液。
新课导入
上图信息中0.9%是什么含义呢?这些溶液是如何得到的呢?在实验室你能配制这样的溶液吗?要使用到哪些仪器呢?具体的操作步骤是什么呢?
返回
一、配制一定溶质质量分数的溶液
新课讲解
如何配制80g 10%的NaCl的溶液?
新课讲解
【实验前分析】
实验药品:氯化钠、蒸馏水
实验仪器:托盘天平 、药匙 、量筒、 胶头 滴管、烧杯 、玻璃棒 、细口瓶
实验原理:溶质质量分数=溶质质量/溶液质量*100%
实验方法:计算出溶质溶剂的量,用天平和量筒分别测出溶质溶剂的量,按要求配制
新课讲解
【托盘天平使用】
注意事项:
(1)使用前要调零
(2)两个托盘上各放一张大小相同的称量纸
(3)称量时遵循左物右码的原则
(4)用镊子夹取砝码应按照从大到小的顺序
(5)称量完毕应将砝码放回盒中,游码归零
新课讲解
液体的量取
用量简量取液体时,先向量简里倾倒液体至接近所需刻度,然后将量简平放在桌面上,再用胶头滴管滴加液体至该刻度。
【量筒的使用】
新课讲解
俯视——读数偏大
平视——读数与真实值一致
仰视——读数偏小
( 1 )计算: NaCl ____g H2O g
( 2 )称量、量取:用_________称量2.5g食盐,用__________量取47.5mL水
( 3 )溶解:将溶质和溶剂在烧杯中混合,搅拌至溶质完全溶解。
实验步骤:
2.5
47.5
托盘天平
量筒
新课讲解
( 4 ) 装瓶:(盖好瓶塞贴上标签)
按上图所示步骤完成实验并将表格中各项内容补充完整。
步骤名称 操作方法
计算
2、
3、
4、
新课讲解
新课讲解
注意事项
用玻璃棒搅拌时,要注意尽量不要使玻璃棒碰触容器的器壁。
新课讲解
【误差分析】
1. 造成实际值偏小的可能原因
①溶质溶解的量变少了:溶质本身不纯 ;左码右物称量;溶质有撒落;溶质没有完全溶解就装瓶存放了
②溶剂的量增多了:仰视量取;烧杯内壁上有水;试剂瓶内壁上有水
2. 造成实际值偏大的可能原因
①溶剂的量减少了: 俯视量取溶剂;量取的水没有完全转移到烧杯中
②溶质溶解的量变多了:称量时,所用砝码已生锈或沾有油污
欲配制 100 g 质量分数为 10%的氯化钠溶液,需要的仪器组合是 ( )
①托盘天平;②烧杯;③玻璃棒;④100 mL 量筒
A.①②
B.①②③
C.①②③④
D.①②④
新课讲解
典例分析
例
C
新课讲解
解析:配制溶质质量分数一定的溶液的基本步骤:计算、
称量、量取、溶解、装瓶存放,其中需要用到的仪器有:
烧杯、玻璃棒、量筒、胶头滴管、天平、药匙,答案选C。
返回
课堂小结
返回
配制一定溶质质量分数的溶液
溶液配制的步骤
1.计算
2.称量、量取
3.溶解
2.装瓶
1.欲配制 100 g 质量分数为 10%的氯化钠溶液,需要的仪器组合是①托盘天平;②烧杯;③玻璃棒;④100 mL 量筒。( )
A.①②
B.①②③
C.①②③④
D.①②④
当堂小练
C
2.配制2000g生理盐水(溶质质量分数为0.9%)需要称取 NaCl 的质量为( )
A. 9g
B. 18g
C.90g
D. 180g
当堂小练
B
3.在配制一定溶质质量分数的氯化钠溶液的实验中,下列实验操作不正确的是 ( )
D
当堂小练
C
返回
同课章节目录
- 第一单元 步入化学殿堂
- 第一节 化学真奇妙
- 第二节 体验化学探究
- 到实验室去:化学实验基本技能训练(一)
- 第二单元 探秘水世界
- 第一节 运动的水分子
- 第二节 水分子的变化
- 第三节 原子的构成
- 第四节 元素
- 到实验室去:化学实验基本技能训练(二)
- 第三单元 溶液
- 第一节 溶液的形成
- 第二节 溶液组成的定量表示
- 到实验室去:配制一定溶质质量分数的溶液
- 第四单元 我们周围的空气
- 第一节 空气的成分
- 第二节 物质组成的表示
- 第三节 氧气
- 到实验室去:氧气的实验室制取与性质
- 第五单元 定量研究化学反应
- 第一节 化学反应中的质量守恒
- 第二节 化学反应的表示
- 第三节 化学反应中的有关计算
- 到实验室去:探究燃烧的条件
- 第六单元 燃烧与燃料
- 第一节 燃烧与灭火
- 第二节 化石燃料的利用
- 第三节 大自然中的二氧化碳
- 到实验室去:二氧化碳的实验室制取与性质
