专题5药物合成的重要原料-卤代烃胺酰胺基础巩固(含解析)2022--2023学年下学期高二化学苏教版(2019)选择性必修3
文档属性
| 名称 | 专题5药物合成的重要原料-卤代烃胺酰胺基础巩固(含解析)2022--2023学年下学期高二化学苏教版(2019)选择性必修3 |

|
|
| 格式 | docx | ||
| 文件大小 | 498.4KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-06-24 00:00:00 | ||
图片预览




文档简介
专题5药物合成的重要原料-卤代烃胺酰胺基础巩固
一、单选题
1.下列各组有机化合物,不管它们以何种比例混合,只要总物质的量一定,则完全燃烧时消耗O2量为一恒量的是
①和 ②和 ③和 ④和 ⑤和
A.②③⑤ B.①④ C.③⑤ D.全部
2.有机物可用于治疗大出血、创伤、外科手术引起的低血压,其部分合成路线如图所示。下列说法正确的是
A.的过程属于消去反应
B.分子的同分异构体中,苯环上有2个取代基并能使溶液显紫色的物质有9种
C.分子中存在醚键和酰胺键
D.物质中有2个手性碳原子,含有共价键和离子键
3.2020年12月,Nutrients 报道了《唾液中维生素A,维生素B12和维生素D结合蛋白的起源》。维生素A的结构简式如下图所示。下列关于维生素A的说法错误的是
A.溶解度比乙醇小
B.分子中不可能所有碳原子共平面
C.一定条件下能发生酯化反应
D.1 mol维生素A最多与7 mol H2发生加成反应
4.下列化学方程式正确的是
A.1-溴丙烷与氢氧化钾的乙醇溶液共热:CH3CH2CH2Br+KOHCH3CH2CH2OH+KBr
B.乙酸乙酯的制备:CH3CO18OH+CH3CH2OHCH3CO18OCH2CH3+H2O
C.用银氨溶液检验乙醛中的醛基CH3CHO+2+2OH-CH3COO-++3NH3+2Ag↓+H2O
D.实验室用液溴和苯在催化剂作用下制溴苯:2+Br22+H2↑
5.水杨酸 和对羟基苯甲酸,下列关于上述物质的说法正确的是
A.分子式不同 B.互为同分异构体 C.化学性质相同 D.物理性质相同
6.下列物质中,在一定条件下既能发生银镜反应,又能发生水解和氧化反应的是
A.溴乙烯 B.乙酸甲酯 C.甲酸乙酯 D.苯甲醛
7.下列说法正确的是
A.烷烃分子中均只含单键,均符合分子通式CnH2n+2
B.烷烃是一类饱和链烃,其分子都是直线型的
C.正戊烷、异戊烷和新戊烷互为同分异构体,沸点依次升高
D.相同质量的烃完全燃烧,耗氧量最大的是CH4
8.将有机化合物完全燃烧,生成CO2和H2O。将12g该有机化合物的完全燃烧产物通过浓硫酸,浓硫酸增重14.4g,再通过碱石灰,碱石灰增重26.4g。则该有机化合物的分子式为
A.C4H10 B.C2H6O C.C3H8O D.C2H4O2
9.下列说法中正确的是
A.正戊烷、异戊烷、新戊烷的沸点逐渐降低
B.等质量的A、B两种烃分别完全燃烧后,生成的与消耗的的物质的量均相同,则A和B一定互为同系物
C.和的最简式相同
D.依据间二甲苯只有一种结构可判断苯分子中不存在碳碳单键与碳碳双键交替结构
10.如图是天冬酰苯丙氨酸甲酯(aspartame)的结构简式。下列关于aspartame的说法不正确的是
A.是芳香族化合物 B.分子中只含有氨基、羧基、酯基官能团
C.既能与NaOH反应,也能与HCl反应 D.1molaspartame最多能与3molNaOH反应
二、填空题
11.现有以下几种有机物:
① ② ③ ④ ⑤ ⑥ ⑦ ⑧ ⑨
请利用上述给出的物质按要求回答下列问题:
(1)③的系统命名是_______。
(2)用“>”表示①③④⑧熔沸点高低顺序:_______(填序号)。
(3)⑨的一氯代物同分异构体数目有_______种。
(4)在120℃,条件下,某种气态烃与足量的完全反应后,测得反应前后气体的体积没有发生改变,则该烃是_______(填序号)。
(5)写出⑥在铁作催化剂的条件下与液溴发生取代反应的化学方程式_______。
12.下图中A、B、C分别是三种有机物的结构模型:
请回答下列问题:
(1)A、B两种模型分别是有机物的___________模型和___________模型。
(2)A及其同系物的分子式符合通式___________(用n表示)。当n=___________时,烷烃开始出现同分异构体。
(3)A、B、C三种有机物中,所有原子均共面的是___________ (填名称)。结构简式为CH2=CHCH2CH2CH3的有机物中,处于同一平面内的碳原子数最多为___________个。
(4)有机物C具有的结构或性质是___________(填字母)。
A.是碳碳双键和碳碳单键交替的结构 B.有毒、不溶于水、密度比水小
C.不能由于化学反应使酸性KMnO4溶液和溴水褪色 D.一定条件下能与氢气或氧气反应
(5)等质量的上述三种有机物完全燃烧生成H2O和CO2,消耗氧气的体积(相同状况下)最大的是___________(填分子式)。
13.根据要求答下列有关问题。
Ⅰ.由乙烷和乙烯都能制得一氯乙烷。
(1) 由乙烷制一氯乙烷的化学方程式为____________,反应类型为______________。
(2)由乙烯制一氯乙烷的化学方程式为____________,反应类型为______________。
(3)以上两种方法中_________【填“(1) ”或“(2 ) ” 】更适合用来制取一氯乙烷,原因是_________________。
Ⅱ.分别用一个化学方程式解释下列问题。
(4)甲烷与氯气的混合物在漫射光下—段时间,出现白雾:__________________。
(5)溴水中通入乙烯,溴水颜色退去:_________________________。
(6)工业上通过乙烯水化获得乙醇:______________________________。
Ⅲ.(7)下列关于苯的叙述正确的是__________(填序号)。
A.苯的分子式为C6H6,它不能使酸性KmnO4溶液褪色,属于饱和烃
B.从苯的凯库勒式()看,苯分子中含有碳碳双键,应属于烯烃
C.二甲苯和的结构不同,互为同分异构体
D.苯分子中的12个原子都在同一平面上
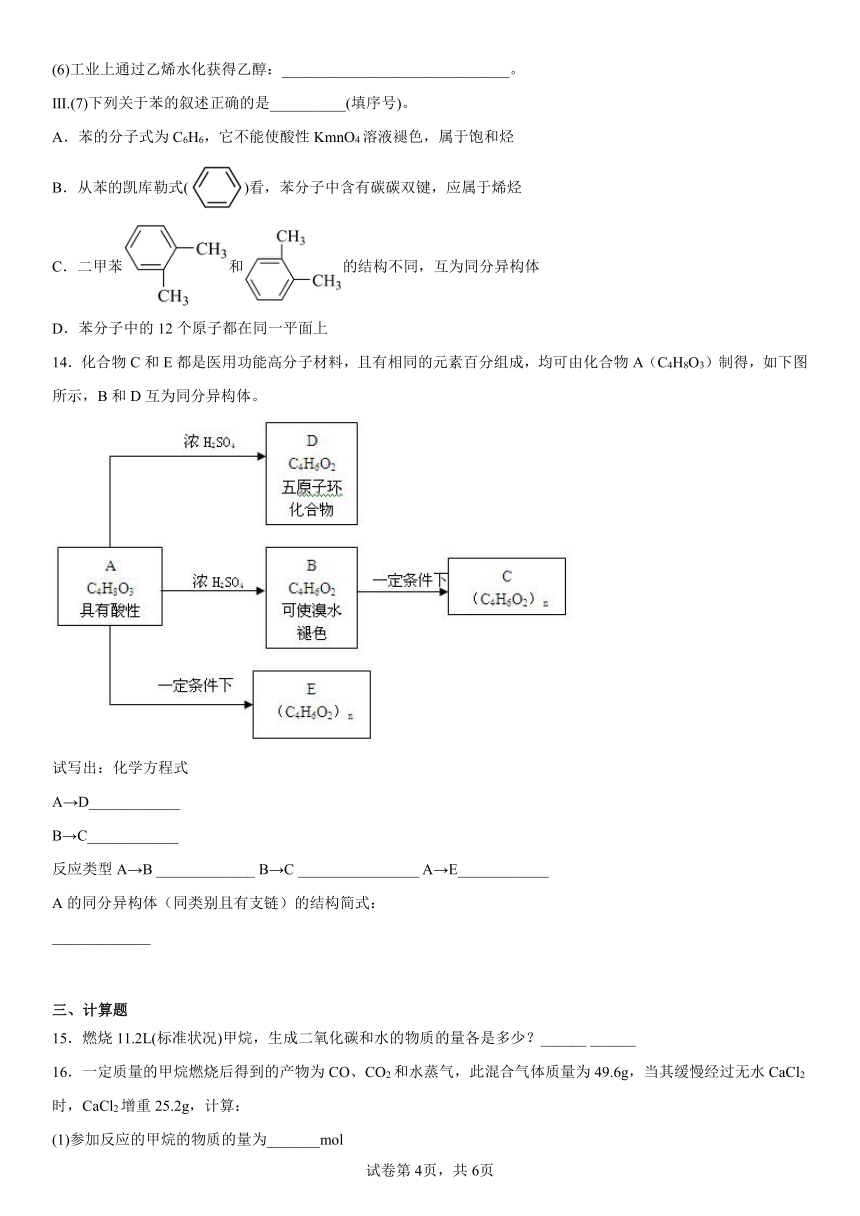
14.化合物C和E都是医用功能高分子材料,且有相同的元素百分组成,均可由化合物A(C4H8O3)制得,如下图所示,B和D互为同分异构体。
试写出:化学方程式
A→D____________
B→C____________
反应类型A→B _____________ B→C ________________ A→E____________
A的同分异构体(同类别且有支链)的结构简式:
_____________
三、计算题
15.燃烧11.2L(标准状况)甲烷,生成二氧化碳和水的物质的量各是多少?______ ______
16.一定质量的甲烷燃烧后得到的产物为CO、CO2和水蒸气,此混合气体质量为49.6g,当其缓慢经过无水CaCl2时,CaCl2增重25.2g,计算:
(1)参加反应的甲烷的物质的量为_______mol
(2)生成的CO的质量为_______g。
17.已知A为烃,B为烃的含氧衍生物,由等物质的量的A和B组成的混合物0.05 mol在0.125 mol的氧气中恰好完全燃烧,生成0.1 mol的CO2和0.1 mol H2O,试通过计算回答下列问题:
(1)从分子式的角度看,等物质的量A和B组成的混合物平均组成可用化学式表示为_________;
(2)另取一定量的A和B完全燃烧,将其以任意物质的量比混合,且物质的量之和一定,则:
①若耗氧量一定,则A和B的分子式分别为:
A_____________________________; B____________________________。
②若生成的CO2和H2O的物质的量一定,则A和B的分子式为:
A_____________________________; B____________________________。
四、有机推断题
18.按以下步骤可以用原料合成有机物(部分试剂和反应条件已略去)。试回答下列问题:
(1)B、F的结构简式分别为_______、_______。
(2)反应① ⑦中属于消去反应的有_______(填序号)。
(3)根据反应+Br2→,写出与等物质的量的发生类似加成反应的化学方程式:_______。
(4)写出反应④的化学方程式:_______。
(5)与4个不同的原子或原子团相连的碳原子称为手性碳原子,A~G这七种有机物分子中含有手性碳原子的有_______(填序号)。
(6)下列有机物分子的核磁共振氢谱中有3个峰,且峰面积之比为的有_______(填序号)。
A. B. C. D.
19.碳纤维质轻、耐高温、有很高的抗拉强度与弹性,它与树脂、金属或陶瓷基体形成的复合材料广泛运用于航天飞机、火箭、导弹的外壳以及体育器具等。碳纤维的合成方法一般经历以下过程:
请回答下列问题:
(1)反应①的化学方程式:________________________________________________。
(2)反应②属于__________;反应④属于____________。(请选a、b、c、d填空)
a.加聚反应 b.缩聚反应 c.氧化反应 d.还原反应
(3)在化合物A、B、C、D、E中,所有原子可能在同一平面上的是____________。
(4)化合物E中碳元素的质量分数接近于________%。(保留1位小数)
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.A
【分析】根据题意可知,要求混合物中的各有机化合物耗氧量相等,根据反应方程式:,即的值相等。
【详解】①、;②,;③,;④,;⑤,;故②③⑤满足条件,A项正确。
故选A。
2.D
【详解】A.由题干信息可知,的过程属于取代反应,A错误;
B.能使溶液显紫色说明分子中含有酚羟基,分子的同分异构体又知苯环上有2个取代基,则两个取代基分别为-OH,-CH2CH2OH或者-OH,-CH2OCH3或-OH,-OCH2CH3或者-OH,-CH(OH)CH3四种组合,而每一组合又有邻、间、对三种位置关系,故符合条件的的物质有3×4=12种,B错误;
C.由D的结构简式可知分子中存在醚键和羰基、氨基,但不存在酰胺键,C错误;
D.由E的结构简式可知,物质中有2个手性碳原子如图所示 ,分子中存在阴阳离子,故含有共价键和离子键,D正确;
故答案为:D。
3.D
【详解】A.分子中碳链较长,亲水基较少,不易溶于水,而乙醇能与水互溶,A项正确;
B.分子中存在饱和烷烃结构,即四个碳原子直接连接在一个碳上,则不可能所有碳原子共平面,B项正确;
C.分子中存在羟基,能发生酯化反应,C项正确;
D.维生素A中存在5个碳碳双键,则1mol维生素A最多与5mol H2发生加成反应,D项错误;
答案选D。
4.C
【详解】A.1-溴丙烷与氢氧化钾的乙醇溶液共热时,发生消去反应:CH3CH2CH2Br+KOHCH3CH=CH2↑+KBr+H2O,A不正确;
B.乙酸与乙醇制备乙酸乙酯时,乙酸脱去羟基,乙醇脱去羟基上的氢原子,发生酯化反应:CH3CO18OH+CH3CH2OHCH3COOCH2CH3+H218O,B不正确;
C.用银氨溶液检验乙醛中的醛基时,乙醛被氧化为乙酸铵,同时生成Ag等,离子方程式为:CH3CHO+2+2OH-CH3COO-++3NH3+2Ag↓+H2O,C正确;
D.实验室用液溴和苯在催化剂作用下制溴苯时,发生取代反应,生成溴苯和溴化氢:+Br2+HBr,D不正确;
故选C。
5.B
【详解】A.观察水杨酸和对羟基苯甲酸结构简式可知,两者的分子式相同,A错误;
B.水杨酸和对羟基苯甲酸分子式相同,结构不同,互为同分异构体,B正确;
C.水杨酸和对羟基苯甲酸结构不同,化学性质不同,C错误;
D.水杨酸和对羟基苯甲酸的结构不同,物理性质也有所差异,D错误;
故答案选B。
6.C
【详解】A.溴乙烯含有溴原子,能发生水解反应,不含醛基不能发生银镜反应,故不选A;
B.乙酸甲酯结构简式为CH3COOCH3,不含醛基不能发生银镜反应,故不选B;
C.甲酸乙酯结构简式为HCOOCH2CH3,含有醛基能发生银镜反应,含有酯基能发生水解反应,可以发生氧化反应,故选C;
D.苯甲醛含有醛基能发生银镜反应,不能发生水解反应,故不选D;
选C。
7.D
【详解】A.烷烃分子中碳碳以单键连成链,碳的其它键都与H相连,环烷烃的通式不符合CnH2n+2,故A错误;
B.烷烃是一类饱和链烃,其分子为锯齿形,故B错误;
C.碳原子数相同,支链越多沸点越低,正戊烷、异戊烷和新戊烷互为同分异构体,沸点依次降低,故C错误;
D.相同质量的烃完全燃烧,氢元素质量分数越大,耗氧量越多,耗氧量最大的是CH4,故D正确;
选D。
8.C
【详解】由浓硫酸增重14.4 g,可知水的质量为14.4 g,可计算出n(H2O)==0.8 mol,n(H)=1.6 mol,m(H)=1.6 g;使碱石灰增重26.4 g,可知二氧化碳质量为26.4 g,n(C)=n(CO2)==0.6 mol,m(C)=7.2 g;m(C)+m(H)=8.8 g,有机化合物的质量为12 g,所以有机化合物中氧元素的质量为3.2 g,n(O)==0.2 mol;n(C)∶n(H)∶n(O)=0.6 mol∶1.6 mol∶0.2 mol=3∶8∶1,即实验式为C3H8O,由于C3H8O中碳原子已经饱和,所以分子式也为C3H8O。
答案选C。
9.A
【详解】A.正戊烷、异戊烷、新戊烷随着支链增加,沸点逐渐降低,A正确;
B.同系物是指结构相似、分子组成相差若干个“CH2”原子团的有机化合物;烃燃烧通式为CxHy+(x+y)O2xCO2+y H2O,等质量的A、B两种烃分别完全燃烧后,生成的与消耗的的物质的量均相同,A和B可能实验式相同,但不一定互为同系物,B错误;
C.和分别为C8H8、C6H12,最简式分别为CH、CH2,不相同,C错误;
D.若苯分子存在碳碳单键与碳碳双键交替结构、或碳碳之间化学键完全相同时,其间二甲苯均只有一种结构,不能依据间二甲苯只有一种结构可判断苯分子中不存在碳碳单键与碳碳双键交替结构,D错误;
故选A。
10.B
【详解】A.由于分子中含有苯环,所以属芳香族化合物,A正确;
B.根据该有机物结构简式可知,分子中含有氨基、羧基、酯基和酰胺基四种官能团,B错误;
C.羧基能与NaOH反应,氨基能与HCl反应,C正确;
D.羧基、酯基和酰胺基都能与NaOH反应,1 mol aspartame最多能与3 mol NaOH反应,D正确;
故选B。
11.(1)2,2-二甲基丁烷
(2)③>⑧>④>①
(3)4
(4)①
(5)+Br2+HBr
【解析】(1)
③为烷烃,烷烃的系统命名法是先找主链,取最长的碳链为主链,则主链有4个碳原子,编号的原则是从取代基离链端最近的一端开始编号,所以其系统命名是2,2-二甲基丁烷。
(2)
碳原子个数越多,沸点越大,相同碳原子个数的烷烃中支链多的沸点低,故①CH4③④⑧,熔沸点高低顺序:③>⑧>④>①。
(3)
⑨具有对称性,有四种位置的氢,因此其一氯代物同分异构体数目有4种。
(4)
在120℃, 1.01×105Pa 条件下,某种气态烃与足量的 O2完全反应。根据烃的燃烧通式:CxHy+(x+)O2xCO2+H2O可知,若测得反应前后气体的体积没有发生改变,则1+x+= x+,计算可得y=4,即当氢原子数为4的时候,燃烧后气体的体积没有改变,因此该烃是①。
(5)
苯在铁作催化剂的条件下与液溴发生取代反应的化学方程式为:+Br2+HBr。
12.(1) 球棍 空间填充
(2) CnH2n+2 4
(3) 乙烯和苯 5
(4)BCD
(5)CH4
【解析】(1)
A、B两种模型分别是有机物的球棍模型和比例模型,空间填充模型突出的是原子之间的成键的情况及空间结构,比例模型突出的是原子之间相等大小以及原子的大致连接顺序、空间结构,不能体现原子之间的成键的情况,故答案为:球棍;空间填充;
(2)
A属于烷烃,其通式为CnH2n+2,从丁烷烃开始出现同分异构体,所以从n=4开始出现同分异构体,故答案为:CnH2n+2;4;
(3)
A是甲烷、B是乙烯、C是苯,甲烷是正四面体结构,乙烯和苯属于平面结构,所以乙烯和苯中所有原子共平面,CH2=CHCH2CH2CH3的有机物中与碳碳双键直接相连的C一定共面,由于单键可以旋转,则处于同一平面内的碳原子数最多为5个,故答案为:乙烯和苯;5;
(4)
有机物C是苯:
A.该分子中不存在碳碳单键和双键,是介于单键和双键之间的特殊键大π键,故A错误;
B.苯有毒、不溶于水、密度比水小,所以和水混合分层,水在下层,故B正确;
C.苯性质较稳定,和酸性KMnO4溶液和溴水不反应,故C正确;
D.一定条件下能与氢气发生加成反应,能和氧气发生氧化反应,故D正确;
故选:BCD;
(5)
等质量时,有机物含氢量越大,燃烧时消耗氧气越多;三种物质的最简式分别为CH4、CH2、CH,显然CH4含氢量最大,等质量时,消耗O2最多,故答案为:CH4 。
13. 取代反应 加成反应 (2) 产物纯净,没有副产物生成 (答案合理即可) D
【分析】Ⅰ.(1)联系甲烷与Cl2的反应,结合烷烃性质的相似性,可知利用乙烷在光照条件下与Cl2发生取代反应可制备氯乙烷;
(2)利用乙烯与HCl发生加成反应可制备氯乙烷;
(3)用乙烷与Cl2制备氯乙烷时,副产物较多,目标物质不纯净,而乙烯与HCl的加成反应,只生成氯乙烷;
Ⅱ. (4)CH4与Cl2在光照条件下生成氯代甲烷(CH3Cl、CH2Cl2等)和HCl,HCl在空气中可形成白雾;
(5)CH2=CH2与Br2发生加成反应生成CH2BrCH2Br,使溴水褪色;
(6)CH2=CH2与水发生加成反应生成 CH3CH2OH;
Ⅲ.(7)苯的分子结构比较特殊,其碳碳键既不是单键,也不是双键,是一种介于单键和双键之间的独特的键,6 个碳碳键完全相同,因此邻二甲苯不存在同分异构体;苯分子是平面正六边形结构,12个原子都在一个平面上。
【详解】Ⅰ.(1)联系甲烷与Cl2的反应,结合烷烃性质的相似性,可知利用乙烷在光照条件下与Cl2发生取代反应可制备氯乙烷,化学方程式为:,故答案为:;取代反应;
(2)利用乙烯与HCl发生加成反应可制备氯乙烷,化学方程式为:,故答案为:;加成反应;
(3)用乙烷与Cl2制备氯乙烷时,副产物较多,目标物质不纯净,而乙烯与HCl的加成反应,只生成氯乙烷,故答案为:(2);产物纯净,没有副产物生成;
Ⅱ. (4)CH4与Cl2在光照条件下生成氯代甲烷(CH3Cl、CH2Cl2等)和HCl,HCl在空气中可形成白雾,化学方程式为:(答案合理即可),故答案为:(答案合理即可);
(5)CH2=CH2与Br2发生加成反应生成CH2BrCH2Br,使溴水褪色,化学方程式为:,故答案为:;
(6)CH2=CH2与水发生加成反应生成 CH3CH2OH,化学方程式为:,故答案为:;
Ⅲ.(7) A. 苯的分子结构比较特殊,其碳碳键既不是单键,也不是双键,是一种介于单键和双键之间的独特的键,苯可与氢气发生加成反应生成环己烷,为不饱和烃,A项错误;
B. 苯的分子结构比较特殊,其碳碳键既不是单键,也不是双键,是一种介于单键和双键之间的独特的键,B项错误;
C. 苯的6 个碳碳键完全相同,因此邻二甲苯不存在同分异构体,C项错误;
D. 苯分子是平面正六边形结构,12个原子都在一个平面上,D项正确;
答案选D。
14. \ 消去反应 加聚反应 缩聚反应 、
【分析】A的分子式为C4H8O3,具有酸性,含有-COOH,A在浓硫酸的作用下生成B,B可以使溴水褪色,由A、B分子式可知,A分子内脱去1分子水发生消去反应生成B,则A中还含有-OH,D是分子式为C4H6O2的五元环化合物,应是A发生酯化反应形成的环酯,则A的结构简式为HOCH2CH2CH2COOH,所以D为,B为CH2=CHCH2COOH,B发生加聚反应得到高分子C为,比较A、E的分子式可知,A发生缩聚反应得到E,E为。
【详解】A→D的反应方程式为:,
B→C的反应方程式为:;
A→B属于消去反应;
B→C属于加聚反应;
A→E属于缩聚反应;
A为HOCH2CH2CH2COOH,其同分异构体(同类别且有支链)的结构简式为:、。
15. 0.5mol 1mol
【详解】n(CH4)=V÷Vm=11.2L÷22.4L/mol=0.5mol,根据C元素守恒可知:n(CO2)=n(CH4)=0.5mol,n(H2O)=2n(CH4)= 1mol。
16. 0.7 11.2
【分析】CH4燃烧产物为CO、CO2,和水蒸气,产物通过无水CaCl2时,无水CaCl2的作用是吸收水分,无水CaCl2增重25.2g为水的质量,根据氢原子守恒可计算CH4的物质的量,根据碳原子守恒可计算CO和CO2的总物质的量。
【详解】(1)产物通过无水CaCl2时,无水CaCl2增重25.2g为水的质量,所以n(H2O)==1.4mol,根据H原子守恒,可以知道:n(CH4)=n(H2O)=×1.4mol=0.7mol;
(2)根据C原子守恒,n(CO)+n(CO2)=0.7mol,m(CO)+m(CO2)=49.6g 25.2g=24.4g,所以[0.7mol n(CO2)]×28g/mol+n(CO2)×44g/mol=24.4g,解得n(CO2)=0.3mol,n(CO)=0.4mol,生成CO的质量为0.4mol×28g/mol=11.2g。
17. C2H4O C2H2 C2H6O2 C2H4 C2H4O2
【详解】(1)等物质的量的A和B组成的混合物0.05 mol在0.125 mol的氧气中恰好完全燃烧,生成0.1 mol的CO2和0.1 mol H2O,说明0.05 mol A和B组成的混合物中含有0.1 mol C、0.2 mol H,根据氧原子个数守恒::0.1 mol×2+0.1 mol-0.125 mol×2=0.05 mol,可得在0.05 mol A和B组成的混合物中含有0.05 mol O;因此等物质的量A和B组成的混合物平均组成可用化学式表示为C2H4O;
(2)①若耗氧量一定,A的分子式表示为CxHy,那么B的分子式应满足CxHy(H2O)m或CxHy(CO2)n。若A为CH4,则B应为CH4(CO2)n,且n≥2。若n=2,则B为C3H4O4,平均碳原子数为2,则要求两者物质的量之比为1:1,但若两者1:1,则平均氧原子数为2,不满足平均分子组成C2H4O,故舍去;其他亦不满足。若A为C2H2,则B应为C2H2(H2O)m,且m≥2。若m=2,则B为C2H6O2,C2H2和C2H6O2两者1:1可满足平均分子组成C2H4O,因此物质A为的分子式为:C2H2,物质B的分子式为:C2H6O2;
②若生成的CO2和H2O的物质的量一定,则要求A和B的分子中碳和氢的原子个数相同。所以A一定为C2H4,B一定为C2H4Oz,z≥2。当z=2时,B为C2H4O2,C2H4和C2H4O2两者1:1可满足平均分子组成C2H4O,因此物质A为的分子式为:C2H4,物质B的分子式为:C2H4O2;
18. ②④ +2NaOH+2NaBr+2H2O CE BD
【分析】由有机物的转化关系可知,与足量氢气发生加成反应生成,则A为;在浓硫酸作用下,共热发生消去反应生成,则B为;与溴发生加成反应生成,则C为;在氢氧化钠醇溶液共热发生消去反应生成, 与溴水发生1,4—加成生成, 与氢气发生加成反应生成,则F为;在氢氧化钠水溶液中共热发生水解反应生成。
【详解】(1)由分析可知,B的结构简式为,F的结构简式为,故答案为:;;
(2) 由分析可知,反应①③⑤⑥属于加成反应,反应②④属于消去反应,反应⑦属于取代反应,故答案为:②④;
(4)反应④发生的反应为在氢氧化钠醇溶液共热发生消去反应生成和水,反应的的化学方程式为+2NaOH+2NaBr+2H2O,故答案为:+2NaOH+2NaBr+2H2O;
(5)手性碳原子为含有4个不同原子或原子团的饱和碳原子,则A~G这七种有机物分子中含有手性碳原子的是和,故答案为:CE;
(6) A.的结构对称,分子中含有3类氢原子,核磁共振氢谱中有三个峰,且峰面积之比为,故错误;
B.的结构对称,分子中含有3类氢原子,核磁共振氢谱中有3个峰,且峰面积之比为,故正确;
C.的结构对称,分子中含有4类氢原子,核磁共振氢谱中有4个峰,且峰面积之比为,故错误;
D.的结构对称,分子中含有3类氢原子,核磁共振氢谱中有3个峰,且峰面积之比为,故正确;
BD正确,故答案为:BD。
19. 2CH2=CH—CH3+2NH3+3O22CH2=CH-CN+6H2O a c BE 70.6%(70.5%~70.7%均给分)
【详解】(1)反应①中生成物是丙烯、氨气和氧气,生成物是CH2=CH-CN,根据原子守恒可知还有H2O生成,因此反应的化学方程式为2CH2=CH—CH3+2NH3+3O22CH2=CH-CN+6H2O。
(2)B分子中含有碳碳双键,发生加聚反应生成C,则反应②属于加聚反应;根据D与E的结构简式可判断D生成E是去氢的反应,因此反应④属于氧化反应。
(3)由于碳碳双键、苯环均是平面形结构,三键是直线形结构,则在化合物A、B、C、D、E中,所有原子可能在同一平面上的是B与E。
(4)由于D转化为E是去氢的反应,则根据B的结构简式可知化合物E中碳元素的质量分数接近于。
答案第1页,共2页
答案第1页,共2页
一、单选题
1.下列各组有机化合物,不管它们以何种比例混合,只要总物质的量一定,则完全燃烧时消耗O2量为一恒量的是
①和 ②和 ③和 ④和 ⑤和
A.②③⑤ B.①④ C.③⑤ D.全部
2.有机物可用于治疗大出血、创伤、外科手术引起的低血压,其部分合成路线如图所示。下列说法正确的是
A.的过程属于消去反应
B.分子的同分异构体中,苯环上有2个取代基并能使溶液显紫色的物质有9种
C.分子中存在醚键和酰胺键
D.物质中有2个手性碳原子,含有共价键和离子键
3.2020年12月,Nutrients 报道了《唾液中维生素A,维生素B12和维生素D结合蛋白的起源》。维生素A的结构简式如下图所示。下列关于维生素A的说法错误的是
A.溶解度比乙醇小
B.分子中不可能所有碳原子共平面
C.一定条件下能发生酯化反应
D.1 mol维生素A最多与7 mol H2发生加成反应
4.下列化学方程式正确的是
A.1-溴丙烷与氢氧化钾的乙醇溶液共热:CH3CH2CH2Br+KOHCH3CH2CH2OH+KBr
B.乙酸乙酯的制备:CH3CO18OH+CH3CH2OHCH3CO18OCH2CH3+H2O
C.用银氨溶液检验乙醛中的醛基CH3CHO+2+2OH-CH3COO-++3NH3+2Ag↓+H2O
D.实验室用液溴和苯在催化剂作用下制溴苯:2+Br22+H2↑
5.水杨酸 和对羟基苯甲酸,下列关于上述物质的说法正确的是
A.分子式不同 B.互为同分异构体 C.化学性质相同 D.物理性质相同
6.下列物质中,在一定条件下既能发生银镜反应,又能发生水解和氧化反应的是
A.溴乙烯 B.乙酸甲酯 C.甲酸乙酯 D.苯甲醛
7.下列说法正确的是
A.烷烃分子中均只含单键,均符合分子通式CnH2n+2
B.烷烃是一类饱和链烃,其分子都是直线型的
C.正戊烷、异戊烷和新戊烷互为同分异构体,沸点依次升高
D.相同质量的烃完全燃烧,耗氧量最大的是CH4
8.将有机化合物完全燃烧,生成CO2和H2O。将12g该有机化合物的完全燃烧产物通过浓硫酸,浓硫酸增重14.4g,再通过碱石灰,碱石灰增重26.4g。则该有机化合物的分子式为
A.C4H10 B.C2H6O C.C3H8O D.C2H4O2
9.下列说法中正确的是
A.正戊烷、异戊烷、新戊烷的沸点逐渐降低
B.等质量的A、B两种烃分别完全燃烧后,生成的与消耗的的物质的量均相同,则A和B一定互为同系物
C.和的最简式相同
D.依据间二甲苯只有一种结构可判断苯分子中不存在碳碳单键与碳碳双键交替结构
10.如图是天冬酰苯丙氨酸甲酯(aspartame)的结构简式。下列关于aspartame的说法不正确的是
A.是芳香族化合物 B.分子中只含有氨基、羧基、酯基官能团
C.既能与NaOH反应,也能与HCl反应 D.1molaspartame最多能与3molNaOH反应
二、填空题
11.现有以下几种有机物:
① ② ③ ④ ⑤ ⑥ ⑦ ⑧ ⑨
请利用上述给出的物质按要求回答下列问题:
(1)③的系统命名是_______。
(2)用“>”表示①③④⑧熔沸点高低顺序:_______(填序号)。
(3)⑨的一氯代物同分异构体数目有_______种。
(4)在120℃,条件下,某种气态烃与足量的完全反应后,测得反应前后气体的体积没有发生改变,则该烃是_______(填序号)。
(5)写出⑥在铁作催化剂的条件下与液溴发生取代反应的化学方程式_______。
12.下图中A、B、C分别是三种有机物的结构模型:
请回答下列问题:
(1)A、B两种模型分别是有机物的___________模型和___________模型。
(2)A及其同系物的分子式符合通式___________(用n表示)。当n=___________时,烷烃开始出现同分异构体。
(3)A、B、C三种有机物中,所有原子均共面的是___________ (填名称)。结构简式为CH2=CHCH2CH2CH3的有机物中,处于同一平面内的碳原子数最多为___________个。
(4)有机物C具有的结构或性质是___________(填字母)。
A.是碳碳双键和碳碳单键交替的结构 B.有毒、不溶于水、密度比水小
C.不能由于化学反应使酸性KMnO4溶液和溴水褪色 D.一定条件下能与氢气或氧气反应
(5)等质量的上述三种有机物完全燃烧生成H2O和CO2,消耗氧气的体积(相同状况下)最大的是___________(填分子式)。
13.根据要求答下列有关问题。
Ⅰ.由乙烷和乙烯都能制得一氯乙烷。
(1) 由乙烷制一氯乙烷的化学方程式为____________,反应类型为______________。
(2)由乙烯制一氯乙烷的化学方程式为____________,反应类型为______________。
(3)以上两种方法中_________【填“(1) ”或“(2 ) ” 】更适合用来制取一氯乙烷,原因是_________________。
Ⅱ.分别用一个化学方程式解释下列问题。
(4)甲烷与氯气的混合物在漫射光下—段时间,出现白雾:__________________。
(5)溴水中通入乙烯,溴水颜色退去:_________________________。
(6)工业上通过乙烯水化获得乙醇:______________________________。
Ⅲ.(7)下列关于苯的叙述正确的是__________(填序号)。
A.苯的分子式为C6H6,它不能使酸性KmnO4溶液褪色,属于饱和烃
B.从苯的凯库勒式()看,苯分子中含有碳碳双键,应属于烯烃
C.二甲苯和的结构不同,互为同分异构体
D.苯分子中的12个原子都在同一平面上
14.化合物C和E都是医用功能高分子材料,且有相同的元素百分组成,均可由化合物A(C4H8O3)制得,如下图所示,B和D互为同分异构体。
试写出:化学方程式
A→D____________
B→C____________
反应类型A→B _____________ B→C ________________ A→E____________
A的同分异构体(同类别且有支链)的结构简式:
_____________
三、计算题
15.燃烧11.2L(标准状况)甲烷,生成二氧化碳和水的物质的量各是多少?______ ______
16.一定质量的甲烷燃烧后得到的产物为CO、CO2和水蒸气,此混合气体质量为49.6g,当其缓慢经过无水CaCl2时,CaCl2增重25.2g,计算:
(1)参加反应的甲烷的物质的量为_______mol
(2)生成的CO的质量为_______g。
17.已知A为烃,B为烃的含氧衍生物,由等物质的量的A和B组成的混合物0.05 mol在0.125 mol的氧气中恰好完全燃烧,生成0.1 mol的CO2和0.1 mol H2O,试通过计算回答下列问题:
(1)从分子式的角度看,等物质的量A和B组成的混合物平均组成可用化学式表示为_________;
(2)另取一定量的A和B完全燃烧,将其以任意物质的量比混合,且物质的量之和一定,则:
①若耗氧量一定,则A和B的分子式分别为:
A_____________________________; B____________________________。
②若生成的CO2和H2O的物质的量一定,则A和B的分子式为:
A_____________________________; B____________________________。
四、有机推断题
18.按以下步骤可以用原料合成有机物(部分试剂和反应条件已略去)。试回答下列问题:
(1)B、F的结构简式分别为_______、_______。
(2)反应① ⑦中属于消去反应的有_______(填序号)。
(3)根据反应+Br2→,写出与等物质的量的发生类似加成反应的化学方程式:_______。
(4)写出反应④的化学方程式:_______。
(5)与4个不同的原子或原子团相连的碳原子称为手性碳原子,A~G这七种有机物分子中含有手性碳原子的有_______(填序号)。
(6)下列有机物分子的核磁共振氢谱中有3个峰,且峰面积之比为的有_______(填序号)。
A. B. C. D.
19.碳纤维质轻、耐高温、有很高的抗拉强度与弹性,它与树脂、金属或陶瓷基体形成的复合材料广泛运用于航天飞机、火箭、导弹的外壳以及体育器具等。碳纤维的合成方法一般经历以下过程:
请回答下列问题:
(1)反应①的化学方程式:________________________________________________。
(2)反应②属于__________;反应④属于____________。(请选a、b、c、d填空)
a.加聚反应 b.缩聚反应 c.氧化反应 d.还原反应
(3)在化合物A、B、C、D、E中,所有原子可能在同一平面上的是____________。
(4)化合物E中碳元素的质量分数接近于________%。(保留1位小数)
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.A
【分析】根据题意可知,要求混合物中的各有机化合物耗氧量相等,根据反应方程式:,即的值相等。
【详解】①、;②,;③,;④,;⑤,;故②③⑤满足条件,A项正确。
故选A。
2.D
【详解】A.由题干信息可知,的过程属于取代反应,A错误;
B.能使溶液显紫色说明分子中含有酚羟基,分子的同分异构体又知苯环上有2个取代基,则两个取代基分别为-OH,-CH2CH2OH或者-OH,-CH2OCH3或-OH,-OCH2CH3或者-OH,-CH(OH)CH3四种组合,而每一组合又有邻、间、对三种位置关系,故符合条件的的物质有3×4=12种,B错误;
C.由D的结构简式可知分子中存在醚键和羰基、氨基,但不存在酰胺键,C错误;
D.由E的结构简式可知,物质中有2个手性碳原子如图所示 ,分子中存在阴阳离子,故含有共价键和离子键,D正确;
故答案为:D。
3.D
【详解】A.分子中碳链较长,亲水基较少,不易溶于水,而乙醇能与水互溶,A项正确;
B.分子中存在饱和烷烃结构,即四个碳原子直接连接在一个碳上,则不可能所有碳原子共平面,B项正确;
C.分子中存在羟基,能发生酯化反应,C项正确;
D.维生素A中存在5个碳碳双键,则1mol维生素A最多与5mol H2发生加成反应,D项错误;
答案选D。
4.C
【详解】A.1-溴丙烷与氢氧化钾的乙醇溶液共热时,发生消去反应:CH3CH2CH2Br+KOHCH3CH=CH2↑+KBr+H2O,A不正确;
B.乙酸与乙醇制备乙酸乙酯时,乙酸脱去羟基,乙醇脱去羟基上的氢原子,发生酯化反应:CH3CO18OH+CH3CH2OHCH3COOCH2CH3+H218O,B不正确;
C.用银氨溶液检验乙醛中的醛基时,乙醛被氧化为乙酸铵,同时生成Ag等,离子方程式为:CH3CHO+2+2OH-CH3COO-++3NH3+2Ag↓+H2O,C正确;
D.实验室用液溴和苯在催化剂作用下制溴苯时,发生取代反应,生成溴苯和溴化氢:+Br2+HBr,D不正确;
故选C。
5.B
【详解】A.观察水杨酸和对羟基苯甲酸结构简式可知,两者的分子式相同,A错误;
B.水杨酸和对羟基苯甲酸分子式相同,结构不同,互为同分异构体,B正确;
C.水杨酸和对羟基苯甲酸结构不同,化学性质不同,C错误;
D.水杨酸和对羟基苯甲酸的结构不同,物理性质也有所差异,D错误;
故答案选B。
6.C
【详解】A.溴乙烯含有溴原子,能发生水解反应,不含醛基不能发生银镜反应,故不选A;
B.乙酸甲酯结构简式为CH3COOCH3,不含醛基不能发生银镜反应,故不选B;
C.甲酸乙酯结构简式为HCOOCH2CH3,含有醛基能发生银镜反应,含有酯基能发生水解反应,可以发生氧化反应,故选C;
D.苯甲醛含有醛基能发生银镜反应,不能发生水解反应,故不选D;
选C。
7.D
【详解】A.烷烃分子中碳碳以单键连成链,碳的其它键都与H相连,环烷烃的通式不符合CnH2n+2,故A错误;
B.烷烃是一类饱和链烃,其分子为锯齿形,故B错误;
C.碳原子数相同,支链越多沸点越低,正戊烷、异戊烷和新戊烷互为同分异构体,沸点依次降低,故C错误;
D.相同质量的烃完全燃烧,氢元素质量分数越大,耗氧量越多,耗氧量最大的是CH4,故D正确;
选D。
8.C
【详解】由浓硫酸增重14.4 g,可知水的质量为14.4 g,可计算出n(H2O)==0.8 mol,n(H)=1.6 mol,m(H)=1.6 g;使碱石灰增重26.4 g,可知二氧化碳质量为26.4 g,n(C)=n(CO2)==0.6 mol,m(C)=7.2 g;m(C)+m(H)=8.8 g,有机化合物的质量为12 g,所以有机化合物中氧元素的质量为3.2 g,n(O)==0.2 mol;n(C)∶n(H)∶n(O)=0.6 mol∶1.6 mol∶0.2 mol=3∶8∶1,即实验式为C3H8O,由于C3H8O中碳原子已经饱和,所以分子式也为C3H8O。
答案选C。
9.A
【详解】A.正戊烷、异戊烷、新戊烷随着支链增加,沸点逐渐降低,A正确;
B.同系物是指结构相似、分子组成相差若干个“CH2”原子团的有机化合物;烃燃烧通式为CxHy+(x+y)O2xCO2+y H2O,等质量的A、B两种烃分别完全燃烧后,生成的与消耗的的物质的量均相同,A和B可能实验式相同,但不一定互为同系物,B错误;
C.和分别为C8H8、C6H12,最简式分别为CH、CH2,不相同,C错误;
D.若苯分子存在碳碳单键与碳碳双键交替结构、或碳碳之间化学键完全相同时,其间二甲苯均只有一种结构,不能依据间二甲苯只有一种结构可判断苯分子中不存在碳碳单键与碳碳双键交替结构,D错误;
故选A。
10.B
【详解】A.由于分子中含有苯环,所以属芳香族化合物,A正确;
B.根据该有机物结构简式可知,分子中含有氨基、羧基、酯基和酰胺基四种官能团,B错误;
C.羧基能与NaOH反应,氨基能与HCl反应,C正确;
D.羧基、酯基和酰胺基都能与NaOH反应,1 mol aspartame最多能与3 mol NaOH反应,D正确;
故选B。
11.(1)2,2-二甲基丁烷
(2)③>⑧>④>①
(3)4
(4)①
(5)+Br2+HBr
【解析】(1)
③为烷烃,烷烃的系统命名法是先找主链,取最长的碳链为主链,则主链有4个碳原子,编号的原则是从取代基离链端最近的一端开始编号,所以其系统命名是2,2-二甲基丁烷。
(2)
碳原子个数越多,沸点越大,相同碳原子个数的烷烃中支链多的沸点低,故①CH4③④⑧,熔沸点高低顺序:③>⑧>④>①。
(3)
⑨具有对称性,有四种位置的氢,因此其一氯代物同分异构体数目有4种。
(4)
在120℃, 1.01×105Pa 条件下,某种气态烃与足量的 O2完全反应。根据烃的燃烧通式:CxHy+(x+)O2xCO2+H2O可知,若测得反应前后气体的体积没有发生改变,则1+x+= x+,计算可得y=4,即当氢原子数为4的时候,燃烧后气体的体积没有改变,因此该烃是①。
(5)
苯在铁作催化剂的条件下与液溴发生取代反应的化学方程式为:+Br2+HBr。
12.(1) 球棍 空间填充
(2) CnH2n+2 4
(3) 乙烯和苯 5
(4)BCD
(5)CH4
【解析】(1)
A、B两种模型分别是有机物的球棍模型和比例模型,空间填充模型突出的是原子之间的成键的情况及空间结构,比例模型突出的是原子之间相等大小以及原子的大致连接顺序、空间结构,不能体现原子之间的成键的情况,故答案为:球棍;空间填充;
(2)
A属于烷烃,其通式为CnH2n+2,从丁烷烃开始出现同分异构体,所以从n=4开始出现同分异构体,故答案为:CnH2n+2;4;
(3)
A是甲烷、B是乙烯、C是苯,甲烷是正四面体结构,乙烯和苯属于平面结构,所以乙烯和苯中所有原子共平面,CH2=CHCH2CH2CH3的有机物中与碳碳双键直接相连的C一定共面,由于单键可以旋转,则处于同一平面内的碳原子数最多为5个,故答案为:乙烯和苯;5;
(4)
有机物C是苯:
A.该分子中不存在碳碳单键和双键,是介于单键和双键之间的特殊键大π键,故A错误;
B.苯有毒、不溶于水、密度比水小,所以和水混合分层,水在下层,故B正确;
C.苯性质较稳定,和酸性KMnO4溶液和溴水不反应,故C正确;
D.一定条件下能与氢气发生加成反应,能和氧气发生氧化反应,故D正确;
故选:BCD;
(5)
等质量时,有机物含氢量越大,燃烧时消耗氧气越多;三种物质的最简式分别为CH4、CH2、CH,显然CH4含氢量最大,等质量时,消耗O2最多,故答案为:CH4 。
13. 取代反应 加成反应 (2) 产物纯净,没有副产物生成 (答案合理即可) D
【分析】Ⅰ.(1)联系甲烷与Cl2的反应,结合烷烃性质的相似性,可知利用乙烷在光照条件下与Cl2发生取代反应可制备氯乙烷;
(2)利用乙烯与HCl发生加成反应可制备氯乙烷;
(3)用乙烷与Cl2制备氯乙烷时,副产物较多,目标物质不纯净,而乙烯与HCl的加成反应,只生成氯乙烷;
Ⅱ. (4)CH4与Cl2在光照条件下生成氯代甲烷(CH3Cl、CH2Cl2等)和HCl,HCl在空气中可形成白雾;
(5)CH2=CH2与Br2发生加成反应生成CH2BrCH2Br,使溴水褪色;
(6)CH2=CH2与水发生加成反应生成 CH3CH2OH;
Ⅲ.(7)苯的分子结构比较特殊,其碳碳键既不是单键,也不是双键,是一种介于单键和双键之间的独特的键,6 个碳碳键完全相同,因此邻二甲苯不存在同分异构体;苯分子是平面正六边形结构,12个原子都在一个平面上。
【详解】Ⅰ.(1)联系甲烷与Cl2的反应,结合烷烃性质的相似性,可知利用乙烷在光照条件下与Cl2发生取代反应可制备氯乙烷,化学方程式为:,故答案为:;取代反应;
(2)利用乙烯与HCl发生加成反应可制备氯乙烷,化学方程式为:,故答案为:;加成反应;
(3)用乙烷与Cl2制备氯乙烷时,副产物较多,目标物质不纯净,而乙烯与HCl的加成反应,只生成氯乙烷,故答案为:(2);产物纯净,没有副产物生成;
Ⅱ. (4)CH4与Cl2在光照条件下生成氯代甲烷(CH3Cl、CH2Cl2等)和HCl,HCl在空气中可形成白雾,化学方程式为:(答案合理即可),故答案为:(答案合理即可);
(5)CH2=CH2与Br2发生加成反应生成CH2BrCH2Br,使溴水褪色,化学方程式为:,故答案为:;
(6)CH2=CH2与水发生加成反应生成 CH3CH2OH,化学方程式为:,故答案为:;
Ⅲ.(7) A. 苯的分子结构比较特殊,其碳碳键既不是单键,也不是双键,是一种介于单键和双键之间的独特的键,苯可与氢气发生加成反应生成环己烷,为不饱和烃,A项错误;
B. 苯的分子结构比较特殊,其碳碳键既不是单键,也不是双键,是一种介于单键和双键之间的独特的键,B项错误;
C. 苯的6 个碳碳键完全相同,因此邻二甲苯不存在同分异构体,C项错误;
D. 苯分子是平面正六边形结构,12个原子都在一个平面上,D项正确;
答案选D。
14. \ 消去反应 加聚反应 缩聚反应 、
【分析】A的分子式为C4H8O3,具有酸性,含有-COOH,A在浓硫酸的作用下生成B,B可以使溴水褪色,由A、B分子式可知,A分子内脱去1分子水发生消去反应生成B,则A中还含有-OH,D是分子式为C4H6O2的五元环化合物,应是A发生酯化反应形成的环酯,则A的结构简式为HOCH2CH2CH2COOH,所以D为,B为CH2=CHCH2COOH,B发生加聚反应得到高分子C为,比较A、E的分子式可知,A发生缩聚反应得到E,E为。
【详解】A→D的反应方程式为:,
B→C的反应方程式为:;
A→B属于消去反应;
B→C属于加聚反应;
A→E属于缩聚反应;
A为HOCH2CH2CH2COOH,其同分异构体(同类别且有支链)的结构简式为:、。
15. 0.5mol 1mol
【详解】n(CH4)=V÷Vm=11.2L÷22.4L/mol=0.5mol,根据C元素守恒可知:n(CO2)=n(CH4)=0.5mol,n(H2O)=2n(CH4)= 1mol。
16. 0.7 11.2
【分析】CH4燃烧产物为CO、CO2,和水蒸气,产物通过无水CaCl2时,无水CaCl2的作用是吸收水分,无水CaCl2增重25.2g为水的质量,根据氢原子守恒可计算CH4的物质的量,根据碳原子守恒可计算CO和CO2的总物质的量。
【详解】(1)产物通过无水CaCl2时,无水CaCl2增重25.2g为水的质量,所以n(H2O)==1.4mol,根据H原子守恒,可以知道:n(CH4)=n(H2O)=×1.4mol=0.7mol;
(2)根据C原子守恒,n(CO)+n(CO2)=0.7mol,m(CO)+m(CO2)=49.6g 25.2g=24.4g,所以[0.7mol n(CO2)]×28g/mol+n(CO2)×44g/mol=24.4g,解得n(CO2)=0.3mol,n(CO)=0.4mol,生成CO的质量为0.4mol×28g/mol=11.2g。
17. C2H4O C2H2 C2H6O2 C2H4 C2H4O2
【详解】(1)等物质的量的A和B组成的混合物0.05 mol在0.125 mol的氧气中恰好完全燃烧,生成0.1 mol的CO2和0.1 mol H2O,说明0.05 mol A和B组成的混合物中含有0.1 mol C、0.2 mol H,根据氧原子个数守恒::0.1 mol×2+0.1 mol-0.125 mol×2=0.05 mol,可得在0.05 mol A和B组成的混合物中含有0.05 mol O;因此等物质的量A和B组成的混合物平均组成可用化学式表示为C2H4O;
(2)①若耗氧量一定,A的分子式表示为CxHy,那么B的分子式应满足CxHy(H2O)m或CxHy(CO2)n。若A为CH4,则B应为CH4(CO2)n,且n≥2。若n=2,则B为C3H4O4,平均碳原子数为2,则要求两者物质的量之比为1:1,但若两者1:1,则平均氧原子数为2,不满足平均分子组成C2H4O,故舍去;其他亦不满足。若A为C2H2,则B应为C2H2(H2O)m,且m≥2。若m=2,则B为C2H6O2,C2H2和C2H6O2两者1:1可满足平均分子组成C2H4O,因此物质A为的分子式为:C2H2,物质B的分子式为:C2H6O2;
②若生成的CO2和H2O的物质的量一定,则要求A和B的分子中碳和氢的原子个数相同。所以A一定为C2H4,B一定为C2H4Oz,z≥2。当z=2时,B为C2H4O2,C2H4和C2H4O2两者1:1可满足平均分子组成C2H4O,因此物质A为的分子式为:C2H4,物质B的分子式为:C2H4O2;
18. ②④ +2NaOH+2NaBr+2H2O CE BD
【分析】由有机物的转化关系可知,与足量氢气发生加成反应生成,则A为;在浓硫酸作用下,共热发生消去反应生成,则B为;与溴发生加成反应生成,则C为;在氢氧化钠醇溶液共热发生消去反应生成, 与溴水发生1,4—加成生成, 与氢气发生加成反应生成,则F为;在氢氧化钠水溶液中共热发生水解反应生成。
【详解】(1)由分析可知,B的结构简式为,F的结构简式为,故答案为:;;
(2) 由分析可知,反应①③⑤⑥属于加成反应,反应②④属于消去反应,反应⑦属于取代反应,故答案为:②④;
(4)反应④发生的反应为在氢氧化钠醇溶液共热发生消去反应生成和水,反应的的化学方程式为+2NaOH+2NaBr+2H2O,故答案为:+2NaOH+2NaBr+2H2O;
(5)手性碳原子为含有4个不同原子或原子团的饱和碳原子,则A~G这七种有机物分子中含有手性碳原子的是和,故答案为:CE;
(6) A.的结构对称,分子中含有3类氢原子,核磁共振氢谱中有三个峰,且峰面积之比为,故错误;
B.的结构对称,分子中含有3类氢原子,核磁共振氢谱中有3个峰,且峰面积之比为,故正确;
C.的结构对称,分子中含有4类氢原子,核磁共振氢谱中有4个峰,且峰面积之比为,故错误;
D.的结构对称,分子中含有3类氢原子,核磁共振氢谱中有3个峰,且峰面积之比为,故正确;
BD正确,故答案为:BD。
19. 2CH2=CH—CH3+2NH3+3O22CH2=CH-CN+6H2O a c BE 70.6%(70.5%~70.7%均给分)
【详解】(1)反应①中生成物是丙烯、氨气和氧气,生成物是CH2=CH-CN,根据原子守恒可知还有H2O生成,因此反应的化学方程式为2CH2=CH—CH3+2NH3+3O22CH2=CH-CN+6H2O。
(2)B分子中含有碳碳双键,发生加聚反应生成C,则反应②属于加聚反应;根据D与E的结构简式可判断D生成E是去氢的反应,因此反应④属于氧化反应。
(3)由于碳碳双键、苯环均是平面形结构,三键是直线形结构,则在化合物A、B、C、D、E中,所有原子可能在同一平面上的是B与E。
(4)由于D转化为E是去氢的反应,则根据B的结构简式可知化合物E中碳元素的质量分数接近于。
答案第1页,共2页
答案第1页,共2页
