专题3 石油化工的基础物质—烃 检测题 (含解析)高二下学期化学苏教版(2019)选择性必修3
文档属性
| 名称 | 专题3 石油化工的基础物质—烃 检测题 (含解析)高二下学期化学苏教版(2019)选择性必修3 |  | |
| 格式 | docx | ||
| 文件大小 | 710.3KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-06-24 10:32:53 | ||
图片预览




文档简介
专题3《石油化工的基础物质—烃》检测题
一、单选题
1.设阿伏加德罗常数的值为NA,下列说法中正确的是
A.1mol苯乙烯中含有的C=C数为4NA
B.2.8g乙烯和丙烯的混合气体中所含碳原子数为0.2NA
C.标准状况下,22.4L乙醛完全燃烧所耗的氧气分子数为2.5NA
D.1L0.1mol·L-1的乙酸溶液中H+数为0.1NA
2.下列说法不正确的是
A.乙烯可以发生加成反应,乙苯也可以
B.苯和四氯化碳可以用酸性高锰酸钾溶液鉴别
C.正丁烷与异丁烷的一氯取代物都只有两种,它们的沸点都相同
D.石蜡在高温催化下反应能生成使酸性高锰酸钾溶液褪色的气体
3.下列说法正确的是(NA 表示阿伏加德罗常数)
A.1 mol 聚乙烯含有的原子数目为 6NA
B.20℃时,1 L 己烷完全燃烧后恢复至原状态,生成气态物质分子数为 6NA/22.4
C.2.8 g 乙烯和丙烯的混合气体中所含碳原子数为 0.2NA
D.1 mol 甲基含 10 NA 个电子
4.设NA为阿伏加德罗常数的值。下列叙述正确的是
A.标准状况下,11.2LCH4与11.2LCl2在光照下充分反应后,气体分子数为NA
B.46g乙醇中含有的C-H键的数目为5NA
C.1mol·L-1的NaClO溶液中含有的ClO-数目小于NA
D.1molAl3+完全转化为转移电子数为4NA
5.设NA为阿伏加德罗常数的值。下列说法正确的是
A.标准状况下,NA个分子所占的体积约为22.4L
B.14 g环丙烷中含共用电子对数为3NA
C.1 mol HClO中含有H-Cl键数为NA
D.将2.24 L (标准状况下)通入水中,溶液中的分子数为0.1NA
6.从苔藓中提取的半月苔酸对研究植物活化石——苔藓的进化关系起重要作用。半月苔酸的分子结构简式如图所示,关于该化合物,下列说法错误的是
A.分子式为C15H14O4 B.难溶于水
C.可发生取代反应 D.所有碳原子一定共平面
7.下列叙述正确的是
A.乙烷、丙烷和丁烷都没有同分异构体
B.在一定条件下,苯与液溴、硝酸作用生成溴苯、硝基苯的反应都属于加成反应
C.乙烯和聚氯乙烯都能使溴的四氯化碳溶液褪色
D.甲烷与足量氯气在光照条件下反应可生成难溶于水的油状液体
8.下列分子中只有σ键没有π键的是
A.2 -甲基丁烷 B.2 -丁烯 C.苯 D.乙炔
9.“新基建”成为2020年的网络热词,包括5G基站建设、特高压、城际高速铁路和城际轨道交通等领域,其中涉及到各类材料。下列说法不正确的是
A.高铁列车使用的不锈钢属于合金
B.基础设施建设所用水泥属于硅酸盐
C.5G通信网络所用的光纤光缆材料是SiO2
D.电缆绝缘层所用聚氯乙烯可发生加成反应
10.硅橡胶是一种兼具有机和无机物性质、热稳定性好的高分子材料.两种硅橡胶L和M的结构片段如图(图中 表示链延长)。二甲基硅橡胶L:;甲基乙烯基硅橡胶M:
X为 Y为
已知:的性质与C相似,L可由在酸催化下水解、聚合制得。下列关于硅橡胶的说法不正确的是
A.L、M的热稳定性好与键键能大有关
B.由制得L的过程中,有产生
C.M可通过加成反应交联改性
D.硅橡胶的抗氧化性:
11.下列说法中正确的是
A.炔烃既易发生加成反应,又易发生取代反应
B.分子组成符合通式的链烃,一定是炔烃
C.烯烃既可使溴水褪色,又可使酸性溶液褪色
D.分子中所有的碳原子都在同一条直线上
12.下列说法正确的是
A.乙烯的电子式为
B.乙烯的球棍模型为
C.乙烯分子是平面结构
D.乙烯的结构简式为CH2CH2
13.利用某些有机物之间的转化可贮存太阳能,如降冰片二烯(NBD)经太阳光照射转化成四环烷(Q)的反应如图所示,下列叙述错误的是
(NBD) (Q)
A.NBD和Q互为同分异构体 B.NBD属于不饱和烃,Q属于饱和烃
C.Q的一氯代物只有3种 D.Q可使溴水褪色
14.对于苯乙烯()的下列叙述:①能使KMnO4酸性溶液褪色②可发生加聚反应③可溶于水④可溶于苯中⑤能与浓硝酸发生取代反应⑥所有的原子一定全部共平面,其中正确的是
A.①②④⑤ B.①②⑤⑥ C.①②④⑥ D.①②④⑤⑥
15.下列反应不属于加成反应的是
A.乙炔与氯化氢反应生成氯乙烯
B.常温下丙烯与溴的四氯化碳溶液反应
C.乙醛与HCN反应生成羟基乙腈
D.顺酐()与水反应生成顺丁烯二酸
二、填空题
16.烯烃中碳碳双键是重要的官能团,烯烃与高锰酸钾酸性溶液反应的氧化产物有如图的反应关系:
已知某烯烃的质谱图中最大质荷比为70,则该烯烃的化学式为_______,该烯烃的某种同分异构体可能存在顺反应异构,写出其顺式结构的结构简式_______。若该烯烃的一种同分异构体与酸性高锰酸钾溶液反应得到的产物为二氧化碳和丁酮(),则此烯烃的结构简式为_______,名称为_______;丁酮中官能团的名称为_______。
17.1834年,德国科学家米希尔里希通过蒸馏安息香酸(苯甲酸)和石灰的混合物得到一种液体物质,将其命名为苯。
(1)分子式为的有机化合物有多种同分异构体,由于苯的碳氢个数比与乙炔相同,人们曾认为它是一种不饱和烃。请写出分子式为的一种含碳碳三键且无支链的链烃的结构简式______。
(2)苯乙烯()在常温下用镍作为催化剂与氢气加成通常得到乙苯,很难得到乙基环己烷,这说明__________________________________________________。
(3)苯乙烯加成聚合可得到的产物为_________________________(用结构简式表示)。
三、实验题
18.I.乙炔是一种无色、无臭的气体,微溶于水,易溶于有机溶剂。实验室常用如图所示装置,利用电石(CaC2)和水反应制取乙炔,并验证乙炔的性质。回答下列问题:
(1)利用电石制备乙炔的方程式:______。
(2)装置A的作用是_____。
(3)装置C发生的反应的方程式______。
(4)若称取ag电石,反应完全后,将生成的乙炔全部通入足量溴的CCl4溶液中,溶液增重bg,则电石的纯度为______(用含有a、b的式子表示)。
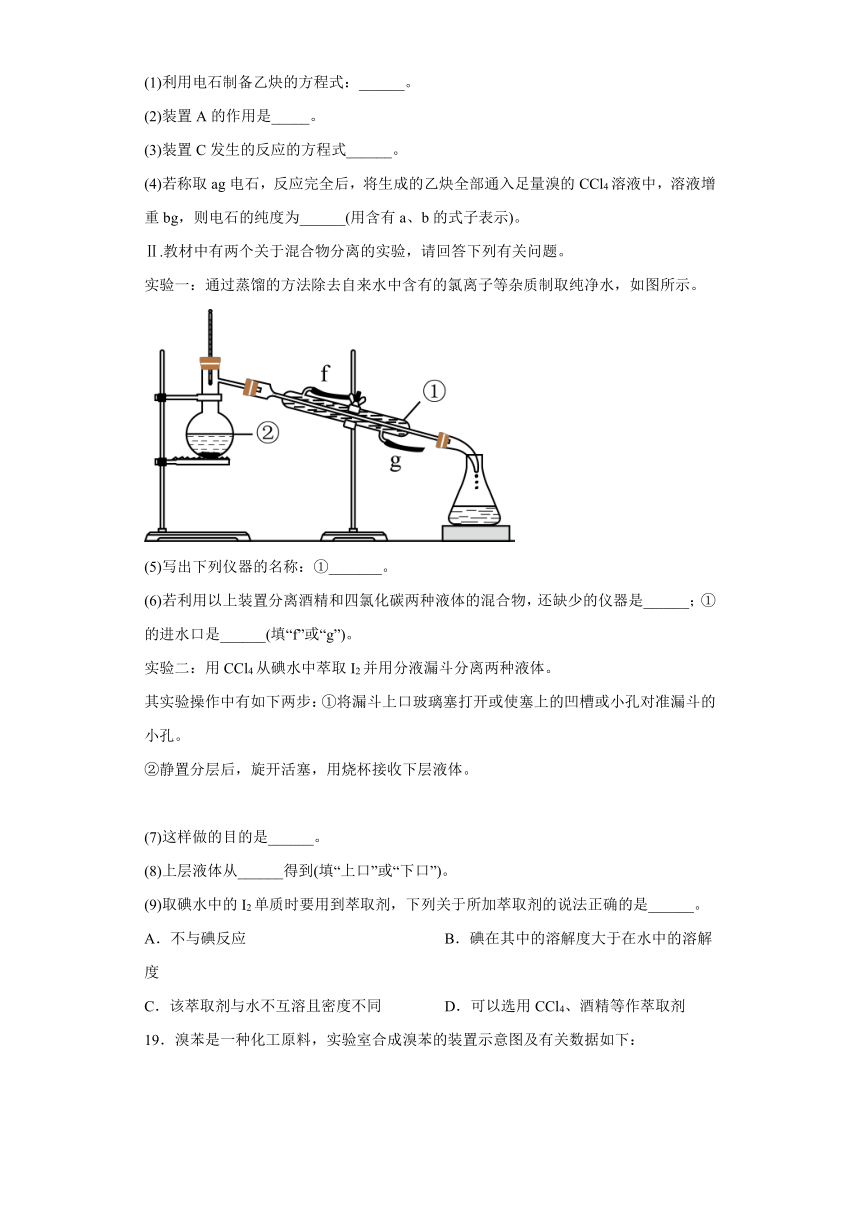
Ⅱ.教材中有两个关于混合物分离的实验,请回答下列有关问题。
实验一:通过蒸馏的方法除去自来水中含有的氯离子等杂质制取纯净水,如图所示。
(5)写出下列仪器的名称:①_______。
(6)若利用以上装置分离酒精和四氯化碳两种液体的混合物,还缺少的仪器是______;①的进水口是______(填“f”或“g”)。
实验二:用CCl4从碘水中萃取I2并用分液漏斗分离两种液体。
其实验操作中有如下两步:①将漏斗上口玻璃塞打开或使塞上的凹槽或小孔对准漏斗的小孔。
②静置分层后,旋开活塞,用烧杯接收下层液体。
(7)这样做的目的是______。
(8)上层液体从______得到(填“上口”或“下口”)。
(9)取碘水中的I2单质时要用到萃取剂,下列关于所加萃取剂的说法正确的是______。
A.不与碘反应 B.碘在其中的溶解度大于在水中的溶解度
C.该萃取剂与水不互溶且密度不同 D.可以选用CCl4、酒精等作萃取剂
19.溴苯是一种化工原料,实验室合成溴苯的装置示意图及有关数据如下:
苯 溴 溴苯
密度/g·cm-3 0.88 3.10 1.50
沸点/℃ 80 59 156
水中溶解度 微溶 微溶 微溶
按以下合成步骤回答问题:
(1)在a中加入15 mL无水苯和少量铁屑。在b中小心加入4.0 mL 液溴。向a中滴入几滴液溴,有白雾产生,写出产生白雾的化学方程式_________________。继续滴加至液溴滴完。装置d中NaOH溶液的作用是_______________。
(2)反应过程中,a外壁温度升高,为提高原料利用率,需利用温度计控制温度,适宜的温度范围为(填序号)_________。
A.>156℃ B.59℃-80℃ C.<59℃
(3)液溴滴完后,经过下列步骤分离提纯:
①向a中加入10 mL水,然后过滤除去未反应的铁屑;
②滤液依次用10 mL水、8 mL10%的NaOH溶液、10 mL水洗涤。
此操作所需要的玻璃仪器除烧杯外,还需__________,用NaOH溶液洗涤的作用是______;
③向分离出的粗溴苯中加入少量的无水氯化钙,静置、过滤。加入氯化钙的目的是_____________。
(4)经过上述分离操作后,粗溴苯中还含有的主要杂质为_________,要进一步提纯,下列操作中必须的是________(填入字母)。
A.重结晶 B.过滤 C.蒸馏 D.萃取
四、计算题
20.计算。
(1)蚂蚁分泌的信息素中含有十一烷,其分子中碳、氢两元素质量比为_______。
(2)在标准状况下的密度为2.59g·L-1的烷烃,相对分子质量为_______,写出其带有支链的同分异构体的结构简式。_______。
21.某混合气体由一种气态烷烃和一种气态烯烃组成,在同温同压下,混合气体对氢气的相对密度为13,在标准状况下,将56.0L混合气体通入足量溴水,溴水质量增重35.0g,通过计算回答:
(1)推出混合气体中气态烷烃的化学式:
依据题意知混合气体的平均相对分子质量为_____________,则烷烃一定为___________。
(2)混合气体中两种气体的物质的量之比:____________________。
(3)写出混合气体中气态烯烃可能的结构简式:__________________。
参考答案:
1.B
【详解】A.苯环不含双键,1mol苯乙烯分子()中只有NA个碳碳双键,A错误;
B.乙烯和丙烯的最简式相同,都是CH2,则2.8 g乙烯和丙烯的混合气体中所含碳原子的物质的量是 0.2mol,碳原子数为0.2NA,B 正确;
C.标准状况下,乙醛(沸点20.8℃)为液体,无法计算22.4L乙醛的体积,也无法计算该条件下乙醛燃烧消耗的氧气分子的数目,C错误;
D.1L 0.1mol·L-1的乙酸溶液中,n(CH3COOH)=cV=0.1mol·L-11L=0.1mol,CH3COOH是弱酸,在水中部分电离,故溶液中H+的数目小于0.1NA,D错误;
故选B。
2.C
【详解】A.乙烯含有碳碳双键可以发生加成反应,乙苯在一定条件下能与氢气等发生加成反应,A说法正确;
B.苯和四氯化碳都不能与高锰酸钾反应,但苯的密度比水小,四氯化碳比水大,可以鉴别,B说法正确;
C.正丁烷与异丁烷的一氯取代物都只有两种,同分异构体的物理性质不同,则它们的沸点不相同,C说法错误;
D.石蜡在高温催化下反应生成含有碳碳双键的物质,使酸性高锰酸钾溶液褪色,D说法正确;
答案为C。
3.C
【详解】A.聚乙烯是高分子化合物,聚合度不知道,无法计算原子数目,A错误;
B.20℃时,己烷为液态,不能使用气体摩尔体积,B错误;
C.乙烯和丙烯的最简式为CH2,2.8g乙烯和丙烯的混合气体中所含碳原子物质的量为,所以含碳原子数为0.2NA,C正确;
D.1个甲基中含有9个电子,1 mol甲基含9NA个电子,D错误;
答案选C。
4.B
【详解】A.CH4与Cl2在光照下充分反应后生成一氯甲烷、二氯甲烷、三氯甲烷、四氯甲烷、氯化氢的混合物,故气体分子数不是NA,A项错误;
B.乙醇的相对分子质量为46g/mol,46g乙醇的物质的量为1mol,1mol乙醇分子中含有5molC-H键,故46g乙醇中含有C-H键数目为5NA,B项正确;
C.不知道溶液的体积,无法计算物质的量,C项错误;
D.Al3+完全转化为,并没有化合价变化,无电子转移,D项错误;
答案选B。
5.B
【详解】A.NA个气态分子物质的量为,标准状况下所占的体积约为22.4L,若该物质不是气体,则体积不是22.4L,A错误;
B.一分子环丙烷中含共用电子对数为9,14g环丙烷物质的量为,含共用电子对数为3 mol,B项正确;
C.结构式为H-O-Cl,不含有,C项错误;
D.和水反应是可逆反应,溶液中的分子数小于,D项错误;
故选:B。
6.D
【详解】A.根据该物质的结构简式可知其分子式为C15H14O4,A正确;
B.该物质中烃基占比较大,烃基为憎水基,所以该物质难溶于水,B正确;
C.该物质含有羧基、羟基,可以发生酯化反应,属于取代反应,C正确;
D.该物质中两个苯环均以单键和饱和碳原子相连,单键可以旋转,所以所有碳原子不一定共面,D错误;
综上所述答案为D。
7.D
【详解】A.乙烷、丙烷都没有同分异构体,而丁烷有正丁烷、异丁烷两种同分异构体,故A错误;
B.在催化剂作用下苯与液溴、硝酸反应生成溴苯、硝基苯的反应都属于取代反应,故B错误;
C.聚氯乙烯不存在碳碳双键,不能使溴的四氯化碳溶液褪色,故C错误;
D.甲烷与足量氯气在光照下反应可生成四氯化碳,四氯化碳是难溶于水的油状液体,故D正确;
故选:D。
8.A
【详解】A.2 -甲基丁烷中只有σ键没有π键,A正确;
B.2 -丁烯中含有碳碳双键,分子中既有σ键又有π键,B错误;
C.苯中含有不饱和键,分子中既有σ键又有π键,C错误;
D.乙炔中含有碳碳三键,分子中既有σ键又有π键,D错误;
答案选A。
9.D
【详解】A.不锈钢是铁合金,属于金属材料,故A正确;
B.水泥是传统的无机非金属材料,主要成分为硅酸盐,故B正确;
C.光导纤维的主要成分是二氧化硅,有良好的导光性,故C正确;
D.聚氯乙烯结构中没有不饱和键,不能发生加成反应,故D错误;
故选D。
10.D
【详解】A.L、M中构成高分子的链节是通过硅氧键连接起来的,其热稳定性好与Si-O键键能大有关,故A正确;
B.L可由在酸催化水解,聚合制得,水解会生成和HCl,故B正确;
C.M中还含有碳碳双键,可通过碳碳双键的加成反应实现交联,得到网状结构,故C正确;
D.M中含有碳碳双键,碳碳双键容易被氧化,硅橡胶的抗氧化性:L>M,故D错误;
故选D。
11.C
【详解】A.炔烃含有碳碳叁键,易发生加成反应,不易发生取代反应,故A错误;
B.分子组成符合通式的链烃,可能是炔烃或二烯烃,故BC错误;
C.烯烃含有碳碳双键,既可使溴水褪色,又可使酸性溶液褪色,故C正确;
D.乙炔是直线分子,分子中有3个碳原子在同一条直线上,故D错误;
选C。
12.C
【详解】A.乙烯的电子式为,A错误;
B.乙烯的球棍模型中,要注意碳原子和氢原子的相对大小,应该是H原子小于C原子,故B错误;
C.乙烯为平面型分子,故C正确;
D.乙烯的结构简式为,D错误。
答案选C。
13.D
【详解】A.NBD和Q互为同分异构体的分子式均是C7H8,结构不同,互为同分异构体,A正确;
B.NBD含有碳碳双键属于不饱和烃,Q中的碳原子均连接四个单键属于饱和烃,B正确;
C.Q的不同环境氢原子有三种,则一氯代物只有3种,C正确;
D.Q中碳原子均达到饱和状态,不能与溴水反应,不能使溴水褪色,D错误;
故选D。
14.A
【详解】①苯乙烯中含有碳碳双键,则能使酸性KMnO4溶液褪色,①项正确;
②苯乙烯中含有碳碳双键,则可发生加聚反应,②项正确;
③苯乙烯为有机物,不溶于水,③项错误;
④根据相似相溶可知,苯乙烯可溶于苯中,④项正确;
⑤苯环能与浓硝酸发生取代反应,则苯乙烯能与浓硝酸发生取代反应,⑤项正确;
⑥苯环为平面结构、乙烯为平面结构,且苯环中的C原子与乙烯中的碳原子直接相连,单键可以旋转,所有的原子可能共面,⑥项错误;
答案选A。
15.D
【详解】A.乙炔中有碳碳三键,可以与氯化氢发生加成反应,生成氯乙烯,A错误;
B.丙烯中有碳碳双键,可以与溴发生加成反应,生成1,2-二溴丙烯,B错误;
C.乙醛中有醛基可以与HCN发生加成反应,生成羟基乙腈C错误;
D.工业上生产顺丁烯二酸是在五氧化二钒催化下,于450~500℃用空气氧化苯,先生成顺丁烯二酸酐,经水解即得顺丁烯二酸,D错误;
故选D。
16. C5H10 2-甲基-1-丁烯 羰基
【详解】烯烃的质谱图中最大质荷比为70,即相对分子质量为70,70÷14=5,则该烯烃的化学式为C5H10;此烯烃有多种同分异构体,其中存在顺反应异构的顺式结构的结构简式为;氧化产物为二氧化碳和丁酮(,依据烯烃与高锰酸钾酸性溶液反应的氧化产物的规律可知该烯烃的结构简式为:CH2=C(CH3)C2H5,名称为2-甲基-1-丁烯;丁酮中官能团的名称为羰基;故答案为:C5H10;;;2-甲基-1-丁烯;羰基。
17. HCC-CC-CH2-CH3、HCC-CH2-CC-CH3、HCC-CH2-CH2-CCH、CH3-CC-CC-CH3 苯环中碳碳键比碳碳双键稳定的多
【详解】(1) 比饱和链烃 (C6H14) 少8个H,结构中可能含有两个碳碳三键、1个碳碳三键和2个碳碳双键、也可能成环等,根据题意,结构中含有碳碳三键的可能的结构简式为:HCC-CC-CH2-CH3、HCC-CH2-CC-CH3、HCC-CH2-CH2-CCH、CH3-CC-CC-CH3;
(2) 苯乙烯在常温下用镍做催化剂与氢气加成得到乙苯,很难得到乙基环己烷,说明苯环中的碳碳键不是碳碳双键且苯环中碳碳键比碳碳双键稳定的多;
(3)苯乙烯发生加聚反应得到聚苯乙烯,聚苯乙烯的结构简式为:。
18.(1)CaC2+2H2O→CH≡CH↑+Ca(OH)2
(2)除去乙炔中的杂质气体
(3)CH≡CH+2Br2→CHBr2CHBr2
(4)×100%
(5)直形冷凝管
(6) 酒精灯 g
(7)平衡分液漏斗内外气压,使下层液体顺利流下
(8)上口
(9)ABC
【详解】(1)电石(碳化钙CaC2)与水反应制取乙炔的化学方程式为:CaC2+2H2O→Ca(OH)2+HC≡CH↑。
(2)硫酸铜和H2S可以发生复分解反应从而除去H2S,方程式为H2S+CuSO4=CuS↓+H2SO4,则作用为除去乙炔中的杂质气体。
(3)装置C乙炔和溴的四氯化碳溶液发生加成反应,化学方程式为。
(4)乙炔全部通入足量溴的CCl4溶液中,乙炔和溴发生加成反应,溶液增重的bg即为生成的乙炔的质量,所以乙炔的物质的量为mol,根据反应方程式CaC2+2H2O→Ca(OH)2+HC≡CH↑,乙炔和碳化钙的物质的量相等,所以碳化钙的质量为×64g,则CaC2的纯度为。
(5)仪器①的名称为直形冷凝管。
(6)酒精和四氯化碳是互溶的沸点不同的液体,采用蒸馏法分离。若利用以上装置分离酒精和四氯化碳两种溶液的混合物,还缺少的仪器是酒精灯;为了冷凝效果好、冷凝水的流向是“下进上出”,①的进水口是g。
(7)分液操作中,由步骤将漏斗上口玻璃塞打开或使塞上的凹槽或小孔对准漏斗的小孔,这样做的目的是平衡分液漏斗内外气压,使下层液体顺利流下。
(8)为了防止污染、上层液体从上口得到。
(9)A.萃取剂不与碘反应,故A正确;
B.碘在其中的溶解度大于在水中的溶解度,保证萃取效果,故B正确;
C.该萃取剂与水不互溶且密度不同,保证液体显著分层,故C正确;
D.酒精溶于水,不能用作萃取剂,故D错误;
说法正确的是ABC。
19.(1) 吸收HBr和Br2
(2)C
(3) 分液漏斗 除去未反应的Br2 干燥或除去粗溴苯中的水
(4) 苯 C
【详解】(1)在催化剂的作用下苯与液溴反应生成溴苯和溴化氢,溴化氢易挥发而产生白雾,反应的方程式为。由于生成的溴苯中含有液溴和溴化氢,所以氢氧化钠溶液的作用是吸收HBr和Br2。故答案为:;吸收HBr和Br2;
(2)溴的沸点最低,是59℃,所以为防止液溴挥发温度不能超过59℃,答案选C。故答案为:C;
(3)②分液时除需要的玻璃仪器除烧杯外,还需分液漏斗。用NaOH溶液洗涤的作用是进一步除去未反应的Br2。故答案为:分液漏斗;除去未反应的Br2;
③无水氯化钙常用作干燥机,所以加入无水氯化钙的作用是干燥或除去粗溴苯中的水。故答案为:干燥或除去粗溴苯中的水;
(4)溴苯易溶在有机溶剂苯中,所以粗溴苯中还含有的主要杂质为苯。苯和溴苯互溶蒸馏可以实现分离。故答案为:苯;C。
20.(1)11:2
(2) 58 CH3CH(CH3)2
【详解】(1)十一烷的分子式为C11H24,其中碳元素和氢元素的质量比为(12×11):24=11:2。
(2)标准状况下密度为2.59g/L的烷烃,其相对分子质量为2.59g/L×22.4L/mol=58g/mol,则其相对分子质量为58,因其为烷烃,则其分子式为C4H10,其带有支链的同分异构体的结构简式为CH3CH(CH3)2。
21.(1) 26 CH4
(2)烷烃:烯烃=3:1
(3)CH2=CH-CH2CH3、CH3-CH=CH-CH3,、CH2=C(CH3)2
【详解】(1)同温同压下,气体相对密度之比等于其相对分子质量之比,故混合气体的相对分子质量为13×2=26,最简单的烯烃为乙烯,相对分质量为28,大于26,则烷烃的相对分子质量一定小于26,小于26的只有甲烷,所以烷烃为甲烷,分子式为CH4;
(2)气体的物质的量为2.5mol,气体的总质量为26g/mol×2.5mol=65g,溴水质量增重35.0g此为烯烃质量,则甲烷的质量为65g-35g=30g;n(CH4)=1.875mol,烯烃的物质的量为2.5mol-1.875mol=0.625mol,则烷烃与烯烃的物质的量之比为1.875mol:0.625mol=3:1。
(3)烯烃的相对分子质量为56;设分子式为CnH2n ,则12n+2n=56,解得n=4,烯烃为C4H8,其结构简式可能为CH2═CH-CH2-CH3、CH3-CH═CH-CH3、CH2═C(CH3)2。
一、单选题
1.设阿伏加德罗常数的值为NA,下列说法中正确的是
A.1mol苯乙烯中含有的C=C数为4NA
B.2.8g乙烯和丙烯的混合气体中所含碳原子数为0.2NA
C.标准状况下,22.4L乙醛完全燃烧所耗的氧气分子数为2.5NA
D.1L0.1mol·L-1的乙酸溶液中H+数为0.1NA
2.下列说法不正确的是
A.乙烯可以发生加成反应,乙苯也可以
B.苯和四氯化碳可以用酸性高锰酸钾溶液鉴别
C.正丁烷与异丁烷的一氯取代物都只有两种,它们的沸点都相同
D.石蜡在高温催化下反应能生成使酸性高锰酸钾溶液褪色的气体
3.下列说法正确的是(NA 表示阿伏加德罗常数)
A.1 mol 聚乙烯含有的原子数目为 6NA
B.20℃时,1 L 己烷完全燃烧后恢复至原状态,生成气态物质分子数为 6NA/22.4
C.2.8 g 乙烯和丙烯的混合气体中所含碳原子数为 0.2NA
D.1 mol 甲基含 10 NA 个电子
4.设NA为阿伏加德罗常数的值。下列叙述正确的是
A.标准状况下,11.2LCH4与11.2LCl2在光照下充分反应后,气体分子数为NA
B.46g乙醇中含有的C-H键的数目为5NA
C.1mol·L-1的NaClO溶液中含有的ClO-数目小于NA
D.1molAl3+完全转化为转移电子数为4NA
5.设NA为阿伏加德罗常数的值。下列说法正确的是
A.标准状况下,NA个分子所占的体积约为22.4L
B.14 g环丙烷中含共用电子对数为3NA
C.1 mol HClO中含有H-Cl键数为NA
D.将2.24 L (标准状况下)通入水中,溶液中的分子数为0.1NA
6.从苔藓中提取的半月苔酸对研究植物活化石——苔藓的进化关系起重要作用。半月苔酸的分子结构简式如图所示,关于该化合物,下列说法错误的是
A.分子式为C15H14O4 B.难溶于水
C.可发生取代反应 D.所有碳原子一定共平面
7.下列叙述正确的是
A.乙烷、丙烷和丁烷都没有同分异构体
B.在一定条件下,苯与液溴、硝酸作用生成溴苯、硝基苯的反应都属于加成反应
C.乙烯和聚氯乙烯都能使溴的四氯化碳溶液褪色
D.甲烷与足量氯气在光照条件下反应可生成难溶于水的油状液体
8.下列分子中只有σ键没有π键的是
A.2 -甲基丁烷 B.2 -丁烯 C.苯 D.乙炔
9.“新基建”成为2020年的网络热词,包括5G基站建设、特高压、城际高速铁路和城际轨道交通等领域,其中涉及到各类材料。下列说法不正确的是
A.高铁列车使用的不锈钢属于合金
B.基础设施建设所用水泥属于硅酸盐
C.5G通信网络所用的光纤光缆材料是SiO2
D.电缆绝缘层所用聚氯乙烯可发生加成反应
10.硅橡胶是一种兼具有机和无机物性质、热稳定性好的高分子材料.两种硅橡胶L和M的结构片段如图(图中 表示链延长)。二甲基硅橡胶L:;甲基乙烯基硅橡胶M:
X为 Y为
已知:的性质与C相似,L可由在酸催化下水解、聚合制得。下列关于硅橡胶的说法不正确的是
A.L、M的热稳定性好与键键能大有关
B.由制得L的过程中,有产生
C.M可通过加成反应交联改性
D.硅橡胶的抗氧化性:
11.下列说法中正确的是
A.炔烃既易发生加成反应,又易发生取代反应
B.分子组成符合通式的链烃,一定是炔烃
C.烯烃既可使溴水褪色,又可使酸性溶液褪色
D.分子中所有的碳原子都在同一条直线上
12.下列说法正确的是
A.乙烯的电子式为
B.乙烯的球棍模型为
C.乙烯分子是平面结构
D.乙烯的结构简式为CH2CH2
13.利用某些有机物之间的转化可贮存太阳能,如降冰片二烯(NBD)经太阳光照射转化成四环烷(Q)的反应如图所示,下列叙述错误的是
(NBD) (Q)
A.NBD和Q互为同分异构体 B.NBD属于不饱和烃,Q属于饱和烃
C.Q的一氯代物只有3种 D.Q可使溴水褪色
14.对于苯乙烯()的下列叙述:①能使KMnO4酸性溶液褪色②可发生加聚反应③可溶于水④可溶于苯中⑤能与浓硝酸发生取代反应⑥所有的原子一定全部共平面,其中正确的是
A.①②④⑤ B.①②⑤⑥ C.①②④⑥ D.①②④⑤⑥
15.下列反应不属于加成反应的是
A.乙炔与氯化氢反应生成氯乙烯
B.常温下丙烯与溴的四氯化碳溶液反应
C.乙醛与HCN反应生成羟基乙腈
D.顺酐()与水反应生成顺丁烯二酸
二、填空题
16.烯烃中碳碳双键是重要的官能团,烯烃与高锰酸钾酸性溶液反应的氧化产物有如图的反应关系:
已知某烯烃的质谱图中最大质荷比为70,则该烯烃的化学式为_______,该烯烃的某种同分异构体可能存在顺反应异构,写出其顺式结构的结构简式_______。若该烯烃的一种同分异构体与酸性高锰酸钾溶液反应得到的产物为二氧化碳和丁酮(),则此烯烃的结构简式为_______,名称为_______;丁酮中官能团的名称为_______。
17.1834年,德国科学家米希尔里希通过蒸馏安息香酸(苯甲酸)和石灰的混合物得到一种液体物质,将其命名为苯。
(1)分子式为的有机化合物有多种同分异构体,由于苯的碳氢个数比与乙炔相同,人们曾认为它是一种不饱和烃。请写出分子式为的一种含碳碳三键且无支链的链烃的结构简式______。
(2)苯乙烯()在常温下用镍作为催化剂与氢气加成通常得到乙苯,很难得到乙基环己烷,这说明__________________________________________________。
(3)苯乙烯加成聚合可得到的产物为_________________________(用结构简式表示)。
三、实验题
18.I.乙炔是一种无色、无臭的气体,微溶于水,易溶于有机溶剂。实验室常用如图所示装置,利用电石(CaC2)和水反应制取乙炔,并验证乙炔的性质。回答下列问题:
(1)利用电石制备乙炔的方程式:______。
(2)装置A的作用是_____。
(3)装置C发生的反应的方程式______。
(4)若称取ag电石,反应完全后,将生成的乙炔全部通入足量溴的CCl4溶液中,溶液增重bg,则电石的纯度为______(用含有a、b的式子表示)。
Ⅱ.教材中有两个关于混合物分离的实验,请回答下列有关问题。
实验一:通过蒸馏的方法除去自来水中含有的氯离子等杂质制取纯净水,如图所示。
(5)写出下列仪器的名称:①_______。
(6)若利用以上装置分离酒精和四氯化碳两种液体的混合物,还缺少的仪器是______;①的进水口是______(填“f”或“g”)。
实验二:用CCl4从碘水中萃取I2并用分液漏斗分离两种液体。
其实验操作中有如下两步:①将漏斗上口玻璃塞打开或使塞上的凹槽或小孔对准漏斗的小孔。
②静置分层后,旋开活塞,用烧杯接收下层液体。
(7)这样做的目的是______。
(8)上层液体从______得到(填“上口”或“下口”)。
(9)取碘水中的I2单质时要用到萃取剂,下列关于所加萃取剂的说法正确的是______。
A.不与碘反应 B.碘在其中的溶解度大于在水中的溶解度
C.该萃取剂与水不互溶且密度不同 D.可以选用CCl4、酒精等作萃取剂
19.溴苯是一种化工原料,实验室合成溴苯的装置示意图及有关数据如下:
苯 溴 溴苯
密度/g·cm-3 0.88 3.10 1.50
沸点/℃ 80 59 156
水中溶解度 微溶 微溶 微溶
按以下合成步骤回答问题:
(1)在a中加入15 mL无水苯和少量铁屑。在b中小心加入4.0 mL 液溴。向a中滴入几滴液溴,有白雾产生,写出产生白雾的化学方程式_________________。继续滴加至液溴滴完。装置d中NaOH溶液的作用是_______________。
(2)反应过程中,a外壁温度升高,为提高原料利用率,需利用温度计控制温度,适宜的温度范围为(填序号)_________。
A.>156℃ B.59℃-80℃ C.<59℃
(3)液溴滴完后,经过下列步骤分离提纯:
①向a中加入10 mL水,然后过滤除去未反应的铁屑;
②滤液依次用10 mL水、8 mL10%的NaOH溶液、10 mL水洗涤。
此操作所需要的玻璃仪器除烧杯外,还需__________,用NaOH溶液洗涤的作用是______;
③向分离出的粗溴苯中加入少量的无水氯化钙,静置、过滤。加入氯化钙的目的是_____________。
(4)经过上述分离操作后,粗溴苯中还含有的主要杂质为_________,要进一步提纯,下列操作中必须的是________(填入字母)。
A.重结晶 B.过滤 C.蒸馏 D.萃取
四、计算题
20.计算。
(1)蚂蚁分泌的信息素中含有十一烷,其分子中碳、氢两元素质量比为_______。
(2)在标准状况下的密度为2.59g·L-1的烷烃,相对分子质量为_______,写出其带有支链的同分异构体的结构简式。_______。
21.某混合气体由一种气态烷烃和一种气态烯烃组成,在同温同压下,混合气体对氢气的相对密度为13,在标准状况下,将56.0L混合气体通入足量溴水,溴水质量增重35.0g,通过计算回答:
(1)推出混合气体中气态烷烃的化学式:
依据题意知混合气体的平均相对分子质量为_____________,则烷烃一定为___________。
(2)混合气体中两种气体的物质的量之比:____________________。
(3)写出混合气体中气态烯烃可能的结构简式:__________________。
参考答案:
1.B
【详解】A.苯环不含双键,1mol苯乙烯分子()中只有NA个碳碳双键,A错误;
B.乙烯和丙烯的最简式相同,都是CH2,则2.8 g乙烯和丙烯的混合气体中所含碳原子的物质的量是 0.2mol,碳原子数为0.2NA,B 正确;
C.标准状况下,乙醛(沸点20.8℃)为液体,无法计算22.4L乙醛的体积,也无法计算该条件下乙醛燃烧消耗的氧气分子的数目,C错误;
D.1L 0.1mol·L-1的乙酸溶液中,n(CH3COOH)=cV=0.1mol·L-11L=0.1mol,CH3COOH是弱酸,在水中部分电离,故溶液中H+的数目小于0.1NA,D错误;
故选B。
2.C
【详解】A.乙烯含有碳碳双键可以发生加成反应,乙苯在一定条件下能与氢气等发生加成反应,A说法正确;
B.苯和四氯化碳都不能与高锰酸钾反应,但苯的密度比水小,四氯化碳比水大,可以鉴别,B说法正确;
C.正丁烷与异丁烷的一氯取代物都只有两种,同分异构体的物理性质不同,则它们的沸点不相同,C说法错误;
D.石蜡在高温催化下反应生成含有碳碳双键的物质,使酸性高锰酸钾溶液褪色,D说法正确;
答案为C。
3.C
【详解】A.聚乙烯是高分子化合物,聚合度不知道,无法计算原子数目,A错误;
B.20℃时,己烷为液态,不能使用气体摩尔体积,B错误;
C.乙烯和丙烯的最简式为CH2,2.8g乙烯和丙烯的混合气体中所含碳原子物质的量为,所以含碳原子数为0.2NA,C正确;
D.1个甲基中含有9个电子,1 mol甲基含9NA个电子,D错误;
答案选C。
4.B
【详解】A.CH4与Cl2在光照下充分反应后生成一氯甲烷、二氯甲烷、三氯甲烷、四氯甲烷、氯化氢的混合物,故气体分子数不是NA,A项错误;
B.乙醇的相对分子质量为46g/mol,46g乙醇的物质的量为1mol,1mol乙醇分子中含有5molC-H键,故46g乙醇中含有C-H键数目为5NA,B项正确;
C.不知道溶液的体积,无法计算物质的量,C项错误;
D.Al3+完全转化为,并没有化合价变化,无电子转移,D项错误;
答案选B。
5.B
【详解】A.NA个气态分子物质的量为,标准状况下所占的体积约为22.4L,若该物质不是气体,则体积不是22.4L,A错误;
B.一分子环丙烷中含共用电子对数为9,14g环丙烷物质的量为,含共用电子对数为3 mol,B项正确;
C.结构式为H-O-Cl,不含有,C项错误;
D.和水反应是可逆反应,溶液中的分子数小于,D项错误;
故选:B。
6.D
【详解】A.根据该物质的结构简式可知其分子式为C15H14O4,A正确;
B.该物质中烃基占比较大,烃基为憎水基,所以该物质难溶于水,B正确;
C.该物质含有羧基、羟基,可以发生酯化反应,属于取代反应,C正确;
D.该物质中两个苯环均以单键和饱和碳原子相连,单键可以旋转,所以所有碳原子不一定共面,D错误;
综上所述答案为D。
7.D
【详解】A.乙烷、丙烷都没有同分异构体,而丁烷有正丁烷、异丁烷两种同分异构体,故A错误;
B.在催化剂作用下苯与液溴、硝酸反应生成溴苯、硝基苯的反应都属于取代反应,故B错误;
C.聚氯乙烯不存在碳碳双键,不能使溴的四氯化碳溶液褪色,故C错误;
D.甲烷与足量氯气在光照下反应可生成四氯化碳,四氯化碳是难溶于水的油状液体,故D正确;
故选:D。
8.A
【详解】A.2 -甲基丁烷中只有σ键没有π键,A正确;
B.2 -丁烯中含有碳碳双键,分子中既有σ键又有π键,B错误;
C.苯中含有不饱和键,分子中既有σ键又有π键,C错误;
D.乙炔中含有碳碳三键,分子中既有σ键又有π键,D错误;
答案选A。
9.D
【详解】A.不锈钢是铁合金,属于金属材料,故A正确;
B.水泥是传统的无机非金属材料,主要成分为硅酸盐,故B正确;
C.光导纤维的主要成分是二氧化硅,有良好的导光性,故C正确;
D.聚氯乙烯结构中没有不饱和键,不能发生加成反应,故D错误;
故选D。
10.D
【详解】A.L、M中构成高分子的链节是通过硅氧键连接起来的,其热稳定性好与Si-O键键能大有关,故A正确;
B.L可由在酸催化水解,聚合制得,水解会生成和HCl,故B正确;
C.M中还含有碳碳双键,可通过碳碳双键的加成反应实现交联,得到网状结构,故C正确;
D.M中含有碳碳双键,碳碳双键容易被氧化,硅橡胶的抗氧化性:L>M,故D错误;
故选D。
11.C
【详解】A.炔烃含有碳碳叁键,易发生加成反应,不易发生取代反应,故A错误;
B.分子组成符合通式的链烃,可能是炔烃或二烯烃,故BC错误;
C.烯烃含有碳碳双键,既可使溴水褪色,又可使酸性溶液褪色,故C正确;
D.乙炔是直线分子,分子中有3个碳原子在同一条直线上,故D错误;
选C。
12.C
【详解】A.乙烯的电子式为,A错误;
B.乙烯的球棍模型中,要注意碳原子和氢原子的相对大小,应该是H原子小于C原子,故B错误;
C.乙烯为平面型分子,故C正确;
D.乙烯的结构简式为,D错误。
答案选C。
13.D
【详解】A.NBD和Q互为同分异构体的分子式均是C7H8,结构不同,互为同分异构体,A正确;
B.NBD含有碳碳双键属于不饱和烃,Q中的碳原子均连接四个单键属于饱和烃,B正确;
C.Q的不同环境氢原子有三种,则一氯代物只有3种,C正确;
D.Q中碳原子均达到饱和状态,不能与溴水反应,不能使溴水褪色,D错误;
故选D。
14.A
【详解】①苯乙烯中含有碳碳双键,则能使酸性KMnO4溶液褪色,①项正确;
②苯乙烯中含有碳碳双键,则可发生加聚反应,②项正确;
③苯乙烯为有机物,不溶于水,③项错误;
④根据相似相溶可知,苯乙烯可溶于苯中,④项正确;
⑤苯环能与浓硝酸发生取代反应,则苯乙烯能与浓硝酸发生取代反应,⑤项正确;
⑥苯环为平面结构、乙烯为平面结构,且苯环中的C原子与乙烯中的碳原子直接相连,单键可以旋转,所有的原子可能共面,⑥项错误;
答案选A。
15.D
【详解】A.乙炔中有碳碳三键,可以与氯化氢发生加成反应,生成氯乙烯,A错误;
B.丙烯中有碳碳双键,可以与溴发生加成反应,生成1,2-二溴丙烯,B错误;
C.乙醛中有醛基可以与HCN发生加成反应,生成羟基乙腈C错误;
D.工业上生产顺丁烯二酸是在五氧化二钒催化下,于450~500℃用空气氧化苯,先生成顺丁烯二酸酐,经水解即得顺丁烯二酸,D错误;
故选D。
16. C5H10 2-甲基-1-丁烯 羰基
【详解】烯烃的质谱图中最大质荷比为70,即相对分子质量为70,70÷14=5,则该烯烃的化学式为C5H10;此烯烃有多种同分异构体,其中存在顺反应异构的顺式结构的结构简式为;氧化产物为二氧化碳和丁酮(,依据烯烃与高锰酸钾酸性溶液反应的氧化产物的规律可知该烯烃的结构简式为:CH2=C(CH3)C2H5,名称为2-甲基-1-丁烯;丁酮中官能团的名称为羰基;故答案为:C5H10;;;2-甲基-1-丁烯;羰基。
17. HCC-CC-CH2-CH3、HCC-CH2-CC-CH3、HCC-CH2-CH2-CCH、CH3-CC-CC-CH3 苯环中碳碳键比碳碳双键稳定的多
【详解】(1) 比饱和链烃 (C6H14) 少8个H,结构中可能含有两个碳碳三键、1个碳碳三键和2个碳碳双键、也可能成环等,根据题意,结构中含有碳碳三键的可能的结构简式为:HCC-CC-CH2-CH3、HCC-CH2-CC-CH3、HCC-CH2-CH2-CCH、CH3-CC-CC-CH3;
(2) 苯乙烯在常温下用镍做催化剂与氢气加成得到乙苯,很难得到乙基环己烷,说明苯环中的碳碳键不是碳碳双键且苯环中碳碳键比碳碳双键稳定的多;
(3)苯乙烯发生加聚反应得到聚苯乙烯,聚苯乙烯的结构简式为:。
18.(1)CaC2+2H2O→CH≡CH↑+Ca(OH)2
(2)除去乙炔中的杂质气体
(3)CH≡CH+2Br2→CHBr2CHBr2
(4)×100%
(5)直形冷凝管
(6) 酒精灯 g
(7)平衡分液漏斗内外气压,使下层液体顺利流下
(8)上口
(9)ABC
【详解】(1)电石(碳化钙CaC2)与水反应制取乙炔的化学方程式为:CaC2+2H2O→Ca(OH)2+HC≡CH↑。
(2)硫酸铜和H2S可以发生复分解反应从而除去H2S,方程式为H2S+CuSO4=CuS↓+H2SO4,则作用为除去乙炔中的杂质气体。
(3)装置C乙炔和溴的四氯化碳溶液发生加成反应,化学方程式为。
(4)乙炔全部通入足量溴的CCl4溶液中,乙炔和溴发生加成反应,溶液增重的bg即为生成的乙炔的质量,所以乙炔的物质的量为mol,根据反应方程式CaC2+2H2O→Ca(OH)2+HC≡CH↑,乙炔和碳化钙的物质的量相等,所以碳化钙的质量为×64g,则CaC2的纯度为。
(5)仪器①的名称为直形冷凝管。
(6)酒精和四氯化碳是互溶的沸点不同的液体,采用蒸馏法分离。若利用以上装置分离酒精和四氯化碳两种溶液的混合物,还缺少的仪器是酒精灯;为了冷凝效果好、冷凝水的流向是“下进上出”,①的进水口是g。
(7)分液操作中,由步骤将漏斗上口玻璃塞打开或使塞上的凹槽或小孔对准漏斗的小孔,这样做的目的是平衡分液漏斗内外气压,使下层液体顺利流下。
(8)为了防止污染、上层液体从上口得到。
(9)A.萃取剂不与碘反应,故A正确;
B.碘在其中的溶解度大于在水中的溶解度,保证萃取效果,故B正确;
C.该萃取剂与水不互溶且密度不同,保证液体显著分层,故C正确;
D.酒精溶于水,不能用作萃取剂,故D错误;
说法正确的是ABC。
19.(1) 吸收HBr和Br2
(2)C
(3) 分液漏斗 除去未反应的Br2 干燥或除去粗溴苯中的水
(4) 苯 C
【详解】(1)在催化剂的作用下苯与液溴反应生成溴苯和溴化氢,溴化氢易挥发而产生白雾,反应的方程式为。由于生成的溴苯中含有液溴和溴化氢,所以氢氧化钠溶液的作用是吸收HBr和Br2。故答案为:;吸收HBr和Br2;
(2)溴的沸点最低,是59℃,所以为防止液溴挥发温度不能超过59℃,答案选C。故答案为:C;
(3)②分液时除需要的玻璃仪器除烧杯外,还需分液漏斗。用NaOH溶液洗涤的作用是进一步除去未反应的Br2。故答案为:分液漏斗;除去未反应的Br2;
③无水氯化钙常用作干燥机,所以加入无水氯化钙的作用是干燥或除去粗溴苯中的水。故答案为:干燥或除去粗溴苯中的水;
(4)溴苯易溶在有机溶剂苯中,所以粗溴苯中还含有的主要杂质为苯。苯和溴苯互溶蒸馏可以实现分离。故答案为:苯;C。
20.(1)11:2
(2) 58 CH3CH(CH3)2
【详解】(1)十一烷的分子式为C11H24,其中碳元素和氢元素的质量比为(12×11):24=11:2。
(2)标准状况下密度为2.59g/L的烷烃,其相对分子质量为2.59g/L×22.4L/mol=58g/mol,则其相对分子质量为58,因其为烷烃,则其分子式为C4H10,其带有支链的同分异构体的结构简式为CH3CH(CH3)2。
21.(1) 26 CH4
(2)烷烃:烯烃=3:1
(3)CH2=CH-CH2CH3、CH3-CH=CH-CH3,、CH2=C(CH3)2
【详解】(1)同温同压下,气体相对密度之比等于其相对分子质量之比,故混合气体的相对分子质量为13×2=26,最简单的烯烃为乙烯,相对分质量为28,大于26,则烷烃的相对分子质量一定小于26,小于26的只有甲烷,所以烷烃为甲烷,分子式为CH4;
(2)气体的物质的量为2.5mol,气体的总质量为26g/mol×2.5mol=65g,溴水质量增重35.0g此为烯烃质量,则甲烷的质量为65g-35g=30g;n(CH4)=1.875mol,烯烃的物质的量为2.5mol-1.875mol=0.625mol,则烷烃与烯烃的物质的量之比为1.875mol:0.625mol=3:1。
(3)烯烃的相对分子质量为56;设分子式为CnH2n ,则12n+2n=56,解得n=4,烯烃为C4H8,其结构简式可能为CH2═CH-CH2-CH3、CH3-CH═CH-CH3、CH2═C(CH3)2。
