1.1 物质的分类及转化 同步练习题(含解析) 高一上学期化学人教版(2019)必修第一册
文档属性
| 名称 | 1.1 物质的分类及转化 同步练习题(含解析) 高一上学期化学人教版(2019)必修第一册 |

|
|
| 格式 | docx | ||
| 文件大小 | 848.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-06-24 00:00:00 | ||
图片预览



文档简介
1.1 物质的分类及转化 同步练习题
一、选择题
1.关于胶体和溶液的区别,下列叙述中正确的是
A.溶液中溶质粒子有规律的运动,而胶体粒子无规律的运动
B.溶液和胶体粒子均能透过滤纸,胶体粒子还可以透过半透膜
C.溶液中溶质粒子一定带电,且通电后溶质粒子向两极移动
D.一束光通过胶体时有光亮的“通路”,通过溶液时无此现象
2.家庭日常生活经常用到的下列物质中,属于纯净物的是
A.调味用的食醋 B.纯水降温得到的冰水混合物
C.消毒用的漂白粉 D.餐饮用的啤酒
3.分类是认识和改造世界的重要方法,运用它可以发现物质及其变化规律。下列分类描述合理的是
A.根据物质组成元素的种类可知由同一种元素组成的物质一定是纯净物
B.根据反应中是否有离子参加或生成,将化学反应分为离子反应和非离子反应
C.根据氧化物中是否含金属元素,把非金属氧化物归为酸性氧化物,金属氧化物归为碱性氧化物
D.纯碱、烧碱两种物质的水溶液均为碱性,故纯碱、烧碱均属于碱
4.下列各组物质中,按化合物、单质、混合物顺序排列的是
A.氯水、氨气、胆矾 B.碘酒、铁、有色玻璃
C.干冰、液氯、汽油 D.生石灰、臭氧、熟石灰
5.《本草纲目》记载“冬灰,乃冬月灶中所烧薪柴之灰也”,这里的“灰”中含有K2CO3,K2CO3属于
A.酸 B.碱 C.盐 D.氧化物
6.用图1所示装置制备Fe(OH)3胶体,用图2所示装置进行提纯。下列说法正确的是
A.为加快Fe(OH)3胶体的生成,可用玻璃棒不断搅拌
B.用含1molFeCl3的饱和溶液制得的胶体中,含有的Fe(OH)3胶粒数为NA
C.图1中用激光笔照射液体,根据有无“光亮的通路”判断Fe(OH)3胶体是否生成
D.取图2中半透膜内的液体少许于试管中,向其中逐滴滴加稀硫酸,可观察到液体由红褐色直接变为黄色
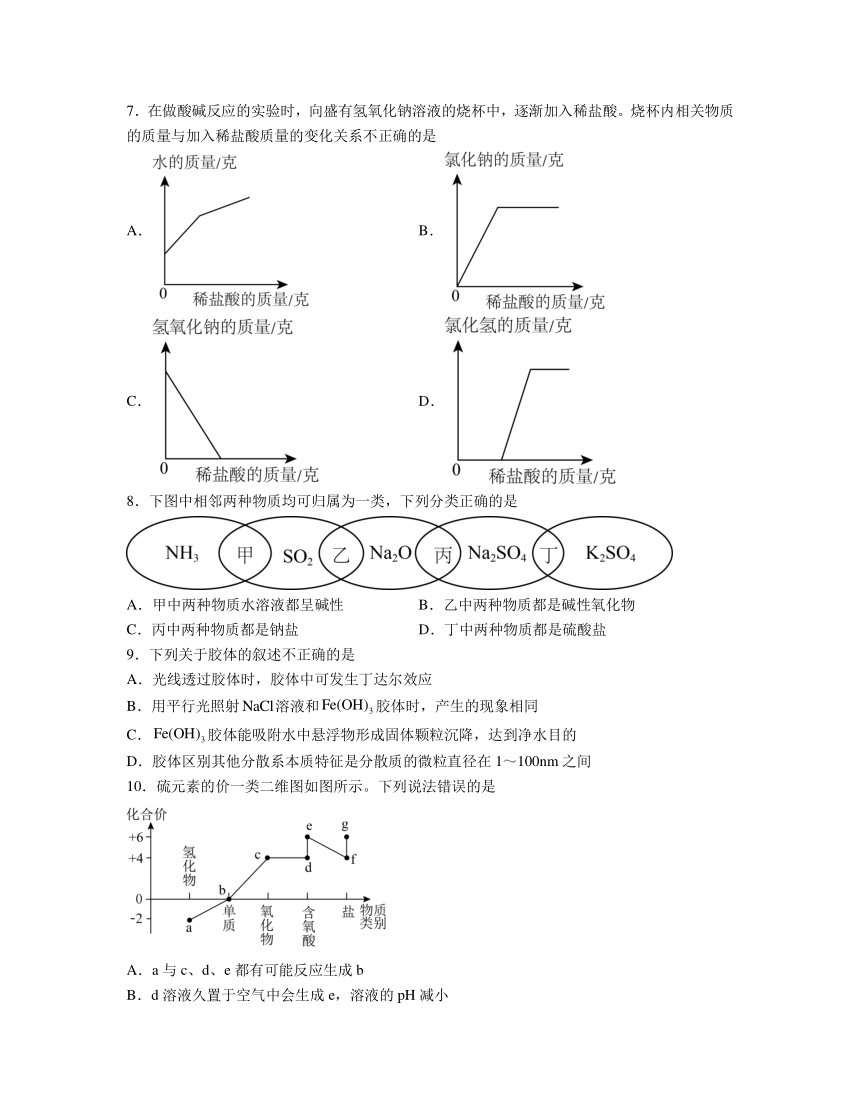
7.在做酸碱反应的实验时,向盛有氢氧化钠溶液的烧杯中,逐渐加入稀盐酸。烧杯内相关物质的质量与加入稀盐酸质量的变化关系不正确的是
A. B.
C. D.
8.下图中相邻两种物质均可归属为一类,下列分类正确的是
A.甲中两种物质水溶液都呈碱性 B.乙中两种物质都是碱性氧化物
C.丙中两种物质都是钠盐 D.丁中两种物质都是硫酸盐
9.下列关于胶体的叙述不正确的是
A.光线透过胶体时,胶体中可发生丁达尔效应
B.用平行光照射溶液和胶体时,产生的现象相同
C.胶体能吸附水中悬浮物形成固体颗粒沉降,达到净水目的
D.胶体区别其他分散系本质特征是分散质的微粒直径在1~100nm之间
10.硫元素的价一类二维图如图所示。下列说法错误的是
A.a与c、d、e都有可能反应生成b
B.d溶液久置于空气中会生成e,溶液的pH减小
C.g与f均是正盐
D.铜与e的浓溶液共热产生的气体通入溶液中,无明显现象
11.下列有关物质的分类正确的是
A.混合物:稀硫酸 B.碱:Cu2(OH)2CO3 C.盐:NH3.H2O D.氧化物:HCOOH
12.下列制备物质的转化关系不合理的是
A.制:
B.制:
C.制NaOH:海水NaCl溶液NaOH
D.制Mg:海水溶液
13.下列关于胶体的说法不正确的是
A.按照分散剂的不同,胶体可分为液溶胶、气溶胶和固溶胶
B.可以用丁达尔效应区别氯化铁溶液和氢氧化铁胶体
C.向氯化铁溶液中加入少量的NaOH溶液制取氢氧化铁胶体
D.胶体、溶液、浊液的分类依据是分散质粒子的直径大小
14.“纳米磁性固体材料”是当今材料科学研究的前沿,若将纳米磁性固态材料分散到水中,当一束光通过时,可以看到一条光亮的“通路”,下列有关该分散系的说法不正确的是
A.该分散系中的分散质粒子直径小于1nm
B.该分散系具有丁达尔效应
C.该分散系属于混合物
D.该分散系属于液溶胶
15.分类是学习和研究化学的一种重要方法,下列分类合理的是
A.K2CO3和K2O都属于盐 B.H2SO4和HNO3都属于酸
C.KOH和Na2CO3都属于碱 D.Na2O和Na2SiO3都属于氧化物
二、填空题
16.运用所学知识回答问题:
(1)按要求从氧气、氢氧化铜、氧化钙、硫酸中选择合适的物质,将其化学式填写在下列横线上。
①可供给呼吸的气体_______。
②一种金属氧化物_______。
③一种不易挥发的酸 _______。
④一种难溶性的碱_______。
(2)科技兴则民族兴,科技强则国家强。回首中国百年征程,科技为中国发展插上了腾飞的翅膀。试回答下列问题:
①淀粉合成,国际首创。2021年,中国科学家在国际上首次实现了二氧化碳到淀粉的从头合成,为淀粉工业制造和二氧化碳利用打开了一扇窗。淀粉是粮食最主要的成分,从物质分类的角度来说,淀粉[化学式为]属于_______(填“氧化物”“无机物”“有机物”之一),它是由_______种元素组成的。
②中国高铁,世界第一、中国高铁已成为中国走向世界的一张“国家名片”。高铁轨道施工过程中常用乙炔()燃烧的火焰来焊接金属,乙炔在氧气中充分燃烧的化学方程式为_______。乙炔分子中,碳原子与氢原子的个数比_______(填最简整数比)。
③“神箭”巡天,筑梦天宫。被誉为“神箭”的长征二号F运载火箭,已成功地完成了神舟系列飞船的发射任务,并圆满将天宫一号和天宫二号送入了太空。发射所用的常规推进剂包括偏二甲肼()和四氧化二氮(),它们反应的化学方程式为,则X的化学式为_______。
17.有下列物质:①氧气 ②二氧化碳 ③臭氧(O3) ④盐酸 ⑤铁 ⑥碳酸钠 ⑦空气⑧氢氧化钠⑨冰、水混合物 ⑩金刚石(用序号填空)其中:
(1)属于氧化物的有:_______;
(2)属于碱的有: _______ ;
(3)属于单质的有:_______;
(4)属于化合物的有: _______;
(5)属于混合物的有: _______ 。
18.现有10种物质:①空气;②金刚石;③生石灰;④无水酒精;⑤稀硫酸;⑥干冰;⑦铜;⑧高锰酸钾;⑨水;⑩碳酸钠。用物质的序号填空:
(1)属于混合物的有___________。
(2)属于单质的有___________,属于盐类的有___________。
(3)属于氧化物的有___________,属于溶液的有___________。
(4)属于有机物的是___________。
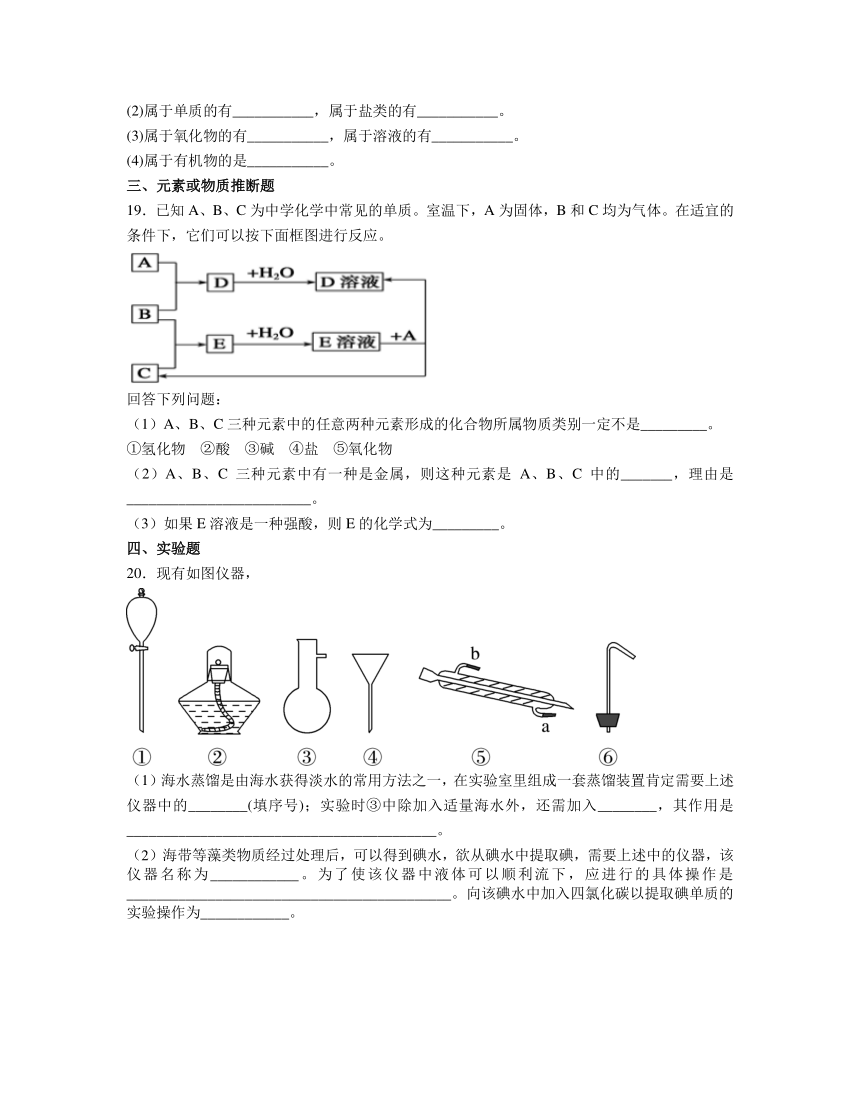
三、元素或物质推断题
19.已知A、B、C为中学化学中常见的单质。室温下,A为固体,B和C均为气体。在适宜的条件下,它们可以按下面框图进行反应。
回答下列问题:
(1)A、B、C三种元素中的任意两种元素形成的化合物所属物质类别一定不是_________。
①氢化物 ②酸 ③碱 ④盐 ⑤氧化物
(2)A、B、C三种元素中有一种是金属,则这种元素是A、B、C中的_______,理由是_________________________。
(3)如果E溶液是一种强酸,则E的化学式为_________。
四、实验题
20.现有如图仪器,
(1)海水蒸馏是由海水获得淡水的常用方法之一,在实验室里组成一套蒸馏装置肯定需要上述仪器中的________(填序号);实验时③中除加入适量海水外,还需加入________,其作用是__________________________________________。
(2)海带等藻类物质经过处理后,可以得到碘水,欲从碘水中提取碘,需要上述中的仪器,该仪器名称为____________。为了使该仪器中液体可以顺利流下,应进行的具体操作是____________________________________________。向该碘水中加入四氯化碳以提取碘单质的实验操作为____________。
【参考答案】
一、选择题
1.D
解析:A.在没有外加电场的作用下,溶液中溶质粒子和胶体粒子都作无规律的运动,A不正确;
B.溶液中的溶质、溶剂粒子、胶体粒子,都比滤纸的孔隙直径小,均能透过滤纸,而胶体粒子的直径比半透膜孔隙直径大,不能透过半透膜,B不正确;
C.溶液中溶质粒子不一定带电,如葡萄糖溶于水,溶质为葡萄糖分子,通电后葡萄糖分子不向两极移动,C不正确;
D.胶粒直径介于10-9~10-7m之间,能使光发生散射,当一束光通过胶体时有光亮的“通路”,而通过溶液时无此现象,D正确;
故选D。
2.B
解析:A. 调味用的食醋是水溶液,属于混合物,故A不符;
B. 纯水降温得到的冰水混合物,只含有水分子,属于纯净物,故B符合;
C. 消毒用的漂白粉由氯化钙、次氯酸钙组成,属于混合物,故C不符;
D. 餐饮用的啤酒是酒精、麦芽糖等的水溶液,属于混合物,故D不符;
故选B。
3.B
解析:A.只含氧元素的物质,可能是O2,也可能是O3,还可能是O2与O3组成的混合物,A错误;
B.有离子参加或有离子生成的反应称为离子反应,没有离子参加和生成的反应称为非离子反应,B正确;
C.非金属氧化物不一定是酸性氧化物,如CO和 NO属于不成盐氧化物,金属氧化物不一定是碱性氧化物,如氧化铝属于两性氧化物,C错误;
D.烧碱是氢氧化钠的俗名,它属于碱,纯碱是碳酸钠的俗名,它属于盐,D错误;
故选B。
4.C
解析:A.氯水是氯气的水溶液,为混合物,氨气是化合物,胆矾是化合物,A不符合题意;
B.碘酒是碘单质的酒精溶液,为混合物,铁是单质,有色玻璃是混合物,B不符合题意;
C.干冰是固态二氧化碳,为化合物,液液氯是液态的氯气为单质,汽油是混合物,C符合题意;
D.生石灰是氧化钙,为化合物,臭氧是单质,熟石灰是氢氧化钙,为纯净物,D不符合题意;
故答案为:C。
5.C
解析:K2CO3属于盐,故选C。
6.C
解析:A.胶体是介稳体系,用玻璃棒不断搅拌会导致胶体发生聚沉,A错误;
B.Fe(OH)3胶体中的胶体粒子是多个Fe(OH)3形成的聚合体,含1molFeCl3的饱和溶液制得的胶体中,含有的Fe(OH)3胶粒数少于NA,B错误;
C.胶体具有丁达尔效应,因此可根据有无“光亮的通路”判断Fe(OH)3胶体是否生成,C正确;
D.向Fe(OH)3胶体中逐滴滴加稀硫酸,胶体先发生聚沉,生成红褐色沉淀,然后发生酸碱中和反应,沉淀溶解,溶液变为黄色,D错误;
故选C。
7.D
解析:A.氢氧化钠溶液中本身含有一定量的水,随着稀盐酸的加入,反应生成的水和稀盐酸中的水都使得烧杯中水的质量不断增大,一段时间后NaOH消耗完全不再生成水,增加水的质量仅为稀盐酸中的水,A正确;
B.滴入盐酸前,烧杯中不含氯化钠,其起始质量为0,随着盐酸的加入,反应生成的氯化钠逐渐增多,但氢氧化钠完全反应后,氯化钠的质量不再变化,B正确;
C.烧杯溶液原有的溶质是氢氧化钠,加入盐酸后,氢氧化钠与盐酸反应,其质量逐渐减少,直至完全反应后其质量变为0,C正确;
D.氢氧化钠未完全反应前,滴入的盐酸中的氯化氢都被反应掉,氢氧化钠反应完全后,氯化氢不再与其他物质反应,溶液中含有的氯化氢会随着滴入盐酸质量的增多而持续增加,D错误。
故选D。
8.D
解析:A.甲中NH3的水溶液呈碱性,但SO2的水溶液呈酸性,A不正确;
B.乙中Na2O为碱性氧化物,但SO2为酸性氧化物,B不正确;
C.丙中两种物质,前者是钠的氧化物,后者是钠盐,C不正确;
D.丁中两种物质都是硫酸盐,前者是硫酸的钠盐,后者是硫酸的钾盐,D正确;
故选D。
9.B
解析:A.丁达尔现象是胶体的性质,光线透过胶体时,胶体中可发生丁达尔效应,故A正确;
B.胶体具有丁达尔现象,溶液无此性质,用聚光手电筒照射NaCl溶液和Fe(OH)3胶体时,产生的现象不相同,故B错误;
C.Fe(OH)3胶体具有较大的表面积,具有吸附悬浮杂质的作用,Fe(OH)3胶体能够吸附水中悬浮的固体颗粒并沉降,达到净水目的,故C正确;
D.分散质微粒直径大小是分散系的本质区别,胶体区别于其他分散系的本质特征是分散质的微粒直径在1~100nm之间,故D正确。
故答案选:B。
10.C
【分析】根据化合价以及物质的类别可知a为H2S、b为S、c为SO2、d为H2SO3、e为H2SO4、f含有或、g含有或。
解析:A.a为H2S,可以和SO2、H2SO3、H2SO4发生归中反应生成硫单质,A正确;
B.H2SO3具有较强的还原性,在空气久置会被氧气氧化成硫酸,硫酸酸性更强,pH更小,B正确;
C.由分析可知,f含有或、g含有或,g与f不一定是正盐,C错误;
D.铜与浓硫酸共热产生的气体SO2,由于HCl的酸性强于H2SO3,SO2通入溶液中不能生成亚硫酸钡沉淀,D正确;
故选C。
11.A
解析:A.稀硫酸是硫酸的水溶液,属于混合物,故A正确;
B.Cu2(OH)2CO3能电离出碳酸根离子、铜离子、氢氧根离子,属于盐,故B错误;
C.NH3·H2O电离出的阴离子全是氢氧根离子,NH3·H2O属于碱,故C错误;
D.氧化物中只含两种元素,HCOOH含有C、H、O三种元素,HCOOH不是氧化物,故D错误;
选A。
12.D
解析:A.氮气和氢气生成NH3,氨和空气的混合气通入灼热的铂铑合金网,在合金网的催化下,氨被氧化成一氧化氮。生成的一氧化氮利用反应后残余的氧气继续氧化为二氧化氮,随后将二氧化氮通入水中制取硝酸,转化关系合理,故A不符合题意;
B.S通过和氧气生成SO2,SO2在催化剂条件下生成SO3,SO3通入水中得到,转化关系合理,故B不符合题意;
C.海水提纯可获得NaCl溶液,电解NaCl溶液可制备NaOH,转化关系合理,故C不符合题意;
D.电解饱和氯化镁溶液,在阳极处产生氯气,阴极处产生氢气和氢氧化镁,因此不能用这种方法获得镁,转化关系不合理,故D符合题意;
故答案选D。
13.C
解析:A.按照分散剂的不同,胶体可分为:分散剂为液体的分散系为液溶胶、分散剂为气体的分散系为气溶胶,分散剂为固体的分散系为固溶胶,故A正确;
B.丁达尔效应是胶体特有的性质,因此可以用丁达尔效应区别氯化铁溶液和氢氧化铁胶体,故B正确;
C.向氯化铁溶液中加入少量的NaOH溶液反应生成氢氧化铁沉淀,不能制备氢氧化铁胶体,故C错误;
D.根据分散质粒子直径大小把分散系划分为:溶液(小于1nm)、胶体(1nm 100nm)、浊液(大于100nm),故D正确;
故答案选C。
14.A
解析:A.将纳米磁性固体材料分散到水中,当光路通过时,可以看到一条光亮的“通路”,所得的分散系属于胶体,具有丁达尔效应。故其分散质直径在1~100nm之间,故A错误;
B.由选项A分析可知,该分散系为胶体,故当一束光通过时,可以看到一条光亮的“通路”,该现象就是丁达尔效应,故B正确;
C.由选项A分析可知,该分散系为胶体,属于混合物,故C正确;
D.所得的分散系中分散剂为液体,属于液溶胶,故D正确;
故选A。
15.B
解析:A.K2O属于氧化物,故A错误;
B.H2SO4和HNO3都属于酸,故B正确;
C.Na2CO3属于盐,故C错误;
D.Na2SiO3属于盐,故D错误;
故选B。
二、填空题
16.(1) CaO
(2) 有机物 三/3 1:1
解析:(1)①氧气可供给呼吸,化学式为:;
②氧化钙是由Ca、O元素组成的化合物,属于金属氧化物,化学式为:CaO;
③硫酸是电离时产生的阳离子都是氢离子的化合物,属于酸,且硫酸不易挥发,故填:;
④氢氧化铜是电离时产生的阴离子都是氢氧根离子的化合物,属于碱,且氢氧化铜难溶于水,故填:;
(2)①淀粉含碳元素,属于有机物;由化学式可知,淀粉由C、H、O三种元素组成;
②乙炔在氧气中充分燃烧生成二氧化碳和水,该反应的化学方程式为:;乙炔分子中,碳原子与氢原子的个数比:2:2=1:1;
③根据质量守恒定律,化学反应前后,原子的种类和数目不变,反应物中含C、H、N、O的个数分别是2、8、6、8,生成物中含C、H、N、O的个数分别是2、8、0、8,故生成物中还应含6个N,故X的化学式为:。
17.(1)②⑨(2)⑧(3)①③⑤⑩(4)②⑥⑧⑨(5)④⑦
【分析】冰、水混合物的成分只有水,是纯净物;
解析:(1)氧化物是指一种元素与氧元素组成的化合物。符合定义的有②⑨;
(2)碱是指电离出的阴离子只有OH-的化合物,一般是氢氧化物的形式,符合定义的有⑧;
(3)单质是只由一种元素组成的纯净物,符合定义的有①③⑤⑩;
(4)化合物是只由两种或两种以上元素组成的纯净物,符合定义的有②⑥⑧⑨;
(5)混合物是由两种或两种以上的物质混合而得,符合定义的有④⑦。
18. ①⑤ ②⑦ ⑧⑩ ③⑥⑨ ⑤ ④
解析:①空气中主要有氮气、氧气,还有二氧化碳、氢气等,属于混合物;
②金刚石为碳元素形成的单质;
③生石灰成分为CaO,属于氧化物;
④无水酒精的成分为C2H5OH,属于有机化合物;
⑤稀硫酸是硫酸的水溶液,属于混合物;
⑥干冰是固体的二氧化碳,属于氧化物;
⑦铜是金属单质;
⑧高锰酸钾的化学式为KMnO4,属于盐类;
⑨水的化学式为H2O,属于氧化物;
⑩碳酸钠的化学式为Na2CO3,属于盐类;
(1)属于混合物的有①⑤;
(2)属于单质的有②⑦;属于盐类的有⑧⑩;
(3)属于氧化物的有③⑥⑨;属于溶液的有⑤;
(4)属于有机物的是④。
三、元素或物质推断题
19. ③⑤ A 金属单质在室温下不是气态物质 HCl
【分析】A、B、C是中学化学中常见的单质,室温下A为固体,A可能为C、Si、S、常见的金属单质如Na、Mg、Al、Fe、Cu、Zn等;B和C均为气体,B、C可能为H2、N2、O2、Cl2等;化合物D、E溶于水分别得到D溶液、E溶液,“A+E溶液→C+D溶液”为置换反应,即固体单质在溶液中能置换出气体单质,根据置换反应的规律,C为H2,E为HCl,B为Cl2,A为金属单质;A与B、E溶液反应都生成D,则A为Na或Mg或Al或Zn,根据上述分析作答。
解析:A、B、C是中学化学中常见的单质,室温下A为固体,A可能为C、Si、S、常见的金属单质如Na、Mg、Al、Fe、Cu、Zn等;B和C均为气体,B、C可能为H2、N2、O2、Cl2等;化合物D、E溶于水分别得到D溶液、E溶液,“A+E溶液→C+D溶液”为置换反应,即固体单质在溶液中能置换出气体单质,根据置换反应的规律,C为H2,E为HCl,B为Cl2,A为金属单质;A与B、E溶液反应都生成D,则A为Na或Mg或Al或Zn。
(1)A为Na或Mg或Al或Zn,B为Cl2,C为H2,A、B、C三种元素中的任意两种元素形成的化合物可能是氢化物、酸、盐;形成的化合物由两种元素组成,不可能为碱,因为没有O元素且化合物D、E溶于水分别得到D溶液、E溶液,不可能为氧化物;答案为:③⑤
(2)A、B、C三种元素中有一种是金属,这种元素是A、B、C中的A,因为金属单质在室温下不是气态物质。答案为:A 金属单质在室温下不是气态物质
(3)如果E溶液是一种强酸,E的化学式为HCl。答案为:HCl
四、实验题
20. ②③⑤⑥ 碎瓷片或沸石 防止溶液暴沸 分液漏斗 打开分液漏斗上口玻璃塞或者使玻璃塞上的凹槽对准分液漏斗小孔 萃取
【分析】本题考查最基本的蒸馏和萃取操作。
解析:(1)由蒸馏装置可知,必需的仪器为②③⑤⑥,还需加入碎瓷片或沸石,防止溶液暴沸,故答案为;②③⑤⑥,碎瓷片或沸石,防止溶液暴沸;
(2)由萃取装置可知,需要的仪器名称为分液漏斗,为了使该仪器中液体可以顺利流下,应进行的具体操作是打开分液漏斗上口玻璃塞或者使玻璃塞上的凹槽对准分液漏斗小孔,故答案为:分液漏斗,打开分液漏斗上口玻璃塞或者使玻璃塞上的凹槽对准分液漏斗小孔,萃取;
一、选择题
1.关于胶体和溶液的区别,下列叙述中正确的是
A.溶液中溶质粒子有规律的运动,而胶体粒子无规律的运动
B.溶液和胶体粒子均能透过滤纸,胶体粒子还可以透过半透膜
C.溶液中溶质粒子一定带电,且通电后溶质粒子向两极移动
D.一束光通过胶体时有光亮的“通路”,通过溶液时无此现象
2.家庭日常生活经常用到的下列物质中,属于纯净物的是
A.调味用的食醋 B.纯水降温得到的冰水混合物
C.消毒用的漂白粉 D.餐饮用的啤酒
3.分类是认识和改造世界的重要方法,运用它可以发现物质及其变化规律。下列分类描述合理的是
A.根据物质组成元素的种类可知由同一种元素组成的物质一定是纯净物
B.根据反应中是否有离子参加或生成,将化学反应分为离子反应和非离子反应
C.根据氧化物中是否含金属元素,把非金属氧化物归为酸性氧化物,金属氧化物归为碱性氧化物
D.纯碱、烧碱两种物质的水溶液均为碱性,故纯碱、烧碱均属于碱
4.下列各组物质中,按化合物、单质、混合物顺序排列的是
A.氯水、氨气、胆矾 B.碘酒、铁、有色玻璃
C.干冰、液氯、汽油 D.生石灰、臭氧、熟石灰
5.《本草纲目》记载“冬灰,乃冬月灶中所烧薪柴之灰也”,这里的“灰”中含有K2CO3,K2CO3属于
A.酸 B.碱 C.盐 D.氧化物
6.用图1所示装置制备Fe(OH)3胶体,用图2所示装置进行提纯。下列说法正确的是
A.为加快Fe(OH)3胶体的生成,可用玻璃棒不断搅拌
B.用含1molFeCl3的饱和溶液制得的胶体中,含有的Fe(OH)3胶粒数为NA
C.图1中用激光笔照射液体,根据有无“光亮的通路”判断Fe(OH)3胶体是否生成
D.取图2中半透膜内的液体少许于试管中,向其中逐滴滴加稀硫酸,可观察到液体由红褐色直接变为黄色
7.在做酸碱反应的实验时,向盛有氢氧化钠溶液的烧杯中,逐渐加入稀盐酸。烧杯内相关物质的质量与加入稀盐酸质量的变化关系不正确的是
A. B.
C. D.
8.下图中相邻两种物质均可归属为一类,下列分类正确的是
A.甲中两种物质水溶液都呈碱性 B.乙中两种物质都是碱性氧化物
C.丙中两种物质都是钠盐 D.丁中两种物质都是硫酸盐
9.下列关于胶体的叙述不正确的是
A.光线透过胶体时,胶体中可发生丁达尔效应
B.用平行光照射溶液和胶体时,产生的现象相同
C.胶体能吸附水中悬浮物形成固体颗粒沉降,达到净水目的
D.胶体区别其他分散系本质特征是分散质的微粒直径在1~100nm之间
10.硫元素的价一类二维图如图所示。下列说法错误的是
A.a与c、d、e都有可能反应生成b
B.d溶液久置于空气中会生成e,溶液的pH减小
C.g与f均是正盐
D.铜与e的浓溶液共热产生的气体通入溶液中,无明显现象
11.下列有关物质的分类正确的是
A.混合物:稀硫酸 B.碱:Cu2(OH)2CO3 C.盐:NH3.H2O D.氧化物:HCOOH
12.下列制备物质的转化关系不合理的是
A.制:
B.制:
C.制NaOH:海水NaCl溶液NaOH
D.制Mg:海水溶液
13.下列关于胶体的说法不正确的是
A.按照分散剂的不同,胶体可分为液溶胶、气溶胶和固溶胶
B.可以用丁达尔效应区别氯化铁溶液和氢氧化铁胶体
C.向氯化铁溶液中加入少量的NaOH溶液制取氢氧化铁胶体
D.胶体、溶液、浊液的分类依据是分散质粒子的直径大小
14.“纳米磁性固体材料”是当今材料科学研究的前沿,若将纳米磁性固态材料分散到水中,当一束光通过时,可以看到一条光亮的“通路”,下列有关该分散系的说法不正确的是
A.该分散系中的分散质粒子直径小于1nm
B.该分散系具有丁达尔效应
C.该分散系属于混合物
D.该分散系属于液溶胶
15.分类是学习和研究化学的一种重要方法,下列分类合理的是
A.K2CO3和K2O都属于盐 B.H2SO4和HNO3都属于酸
C.KOH和Na2CO3都属于碱 D.Na2O和Na2SiO3都属于氧化物
二、填空题
16.运用所学知识回答问题:
(1)按要求从氧气、氢氧化铜、氧化钙、硫酸中选择合适的物质,将其化学式填写在下列横线上。
①可供给呼吸的气体_______。
②一种金属氧化物_______。
③一种不易挥发的酸 _______。
④一种难溶性的碱_______。
(2)科技兴则民族兴,科技强则国家强。回首中国百年征程,科技为中国发展插上了腾飞的翅膀。试回答下列问题:
①淀粉合成,国际首创。2021年,中国科学家在国际上首次实现了二氧化碳到淀粉的从头合成,为淀粉工业制造和二氧化碳利用打开了一扇窗。淀粉是粮食最主要的成分,从物质分类的角度来说,淀粉[化学式为]属于_______(填“氧化物”“无机物”“有机物”之一),它是由_______种元素组成的。
②中国高铁,世界第一、中国高铁已成为中国走向世界的一张“国家名片”。高铁轨道施工过程中常用乙炔()燃烧的火焰来焊接金属,乙炔在氧气中充分燃烧的化学方程式为_______。乙炔分子中,碳原子与氢原子的个数比_______(填最简整数比)。
③“神箭”巡天,筑梦天宫。被誉为“神箭”的长征二号F运载火箭,已成功地完成了神舟系列飞船的发射任务,并圆满将天宫一号和天宫二号送入了太空。发射所用的常规推进剂包括偏二甲肼()和四氧化二氮(),它们反应的化学方程式为,则X的化学式为_______。
17.有下列物质:①氧气 ②二氧化碳 ③臭氧(O3) ④盐酸 ⑤铁 ⑥碳酸钠 ⑦空气⑧氢氧化钠⑨冰、水混合物 ⑩金刚石(用序号填空)其中:
(1)属于氧化物的有:_______;
(2)属于碱的有: _______ ;
(3)属于单质的有:_______;
(4)属于化合物的有: _______;
(5)属于混合物的有: _______ 。
18.现有10种物质:①空气;②金刚石;③生石灰;④无水酒精;⑤稀硫酸;⑥干冰;⑦铜;⑧高锰酸钾;⑨水;⑩碳酸钠。用物质的序号填空:
(1)属于混合物的有___________。
(2)属于单质的有___________,属于盐类的有___________。
(3)属于氧化物的有___________,属于溶液的有___________。
(4)属于有机物的是___________。
三、元素或物质推断题
19.已知A、B、C为中学化学中常见的单质。室温下,A为固体,B和C均为气体。在适宜的条件下,它们可以按下面框图进行反应。
回答下列问题:
(1)A、B、C三种元素中的任意两种元素形成的化合物所属物质类别一定不是_________。
①氢化物 ②酸 ③碱 ④盐 ⑤氧化物
(2)A、B、C三种元素中有一种是金属,则这种元素是A、B、C中的_______,理由是_________________________。
(3)如果E溶液是一种强酸,则E的化学式为_________。
四、实验题
20.现有如图仪器,
(1)海水蒸馏是由海水获得淡水的常用方法之一,在实验室里组成一套蒸馏装置肯定需要上述仪器中的________(填序号);实验时③中除加入适量海水外,还需加入________,其作用是__________________________________________。
(2)海带等藻类物质经过处理后,可以得到碘水,欲从碘水中提取碘,需要上述中的仪器,该仪器名称为____________。为了使该仪器中液体可以顺利流下,应进行的具体操作是____________________________________________。向该碘水中加入四氯化碳以提取碘单质的实验操作为____________。
【参考答案】
一、选择题
1.D
解析:A.在没有外加电场的作用下,溶液中溶质粒子和胶体粒子都作无规律的运动,A不正确;
B.溶液中的溶质、溶剂粒子、胶体粒子,都比滤纸的孔隙直径小,均能透过滤纸,而胶体粒子的直径比半透膜孔隙直径大,不能透过半透膜,B不正确;
C.溶液中溶质粒子不一定带电,如葡萄糖溶于水,溶质为葡萄糖分子,通电后葡萄糖分子不向两极移动,C不正确;
D.胶粒直径介于10-9~10-7m之间,能使光发生散射,当一束光通过胶体时有光亮的“通路”,而通过溶液时无此现象,D正确;
故选D。
2.B
解析:A. 调味用的食醋是水溶液,属于混合物,故A不符;
B. 纯水降温得到的冰水混合物,只含有水分子,属于纯净物,故B符合;
C. 消毒用的漂白粉由氯化钙、次氯酸钙组成,属于混合物,故C不符;
D. 餐饮用的啤酒是酒精、麦芽糖等的水溶液,属于混合物,故D不符;
故选B。
3.B
解析:A.只含氧元素的物质,可能是O2,也可能是O3,还可能是O2与O3组成的混合物,A错误;
B.有离子参加或有离子生成的反应称为离子反应,没有离子参加和生成的反应称为非离子反应,B正确;
C.非金属氧化物不一定是酸性氧化物,如CO和 NO属于不成盐氧化物,金属氧化物不一定是碱性氧化物,如氧化铝属于两性氧化物,C错误;
D.烧碱是氢氧化钠的俗名,它属于碱,纯碱是碳酸钠的俗名,它属于盐,D错误;
故选B。
4.C
解析:A.氯水是氯气的水溶液,为混合物,氨气是化合物,胆矾是化合物,A不符合题意;
B.碘酒是碘单质的酒精溶液,为混合物,铁是单质,有色玻璃是混合物,B不符合题意;
C.干冰是固态二氧化碳,为化合物,液液氯是液态的氯气为单质,汽油是混合物,C符合题意;
D.生石灰是氧化钙,为化合物,臭氧是单质,熟石灰是氢氧化钙,为纯净物,D不符合题意;
故答案为:C。
5.C
解析:K2CO3属于盐,故选C。
6.C
解析:A.胶体是介稳体系,用玻璃棒不断搅拌会导致胶体发生聚沉,A错误;
B.Fe(OH)3胶体中的胶体粒子是多个Fe(OH)3形成的聚合体,含1molFeCl3的饱和溶液制得的胶体中,含有的Fe(OH)3胶粒数少于NA,B错误;
C.胶体具有丁达尔效应,因此可根据有无“光亮的通路”判断Fe(OH)3胶体是否生成,C正确;
D.向Fe(OH)3胶体中逐滴滴加稀硫酸,胶体先发生聚沉,生成红褐色沉淀,然后发生酸碱中和反应,沉淀溶解,溶液变为黄色,D错误;
故选C。
7.D
解析:A.氢氧化钠溶液中本身含有一定量的水,随着稀盐酸的加入,反应生成的水和稀盐酸中的水都使得烧杯中水的质量不断增大,一段时间后NaOH消耗完全不再生成水,增加水的质量仅为稀盐酸中的水,A正确;
B.滴入盐酸前,烧杯中不含氯化钠,其起始质量为0,随着盐酸的加入,反应生成的氯化钠逐渐增多,但氢氧化钠完全反应后,氯化钠的质量不再变化,B正确;
C.烧杯溶液原有的溶质是氢氧化钠,加入盐酸后,氢氧化钠与盐酸反应,其质量逐渐减少,直至完全反应后其质量变为0,C正确;
D.氢氧化钠未完全反应前,滴入的盐酸中的氯化氢都被反应掉,氢氧化钠反应完全后,氯化氢不再与其他物质反应,溶液中含有的氯化氢会随着滴入盐酸质量的增多而持续增加,D错误。
故选D。
8.D
解析:A.甲中NH3的水溶液呈碱性,但SO2的水溶液呈酸性,A不正确;
B.乙中Na2O为碱性氧化物,但SO2为酸性氧化物,B不正确;
C.丙中两种物质,前者是钠的氧化物,后者是钠盐,C不正确;
D.丁中两种物质都是硫酸盐,前者是硫酸的钠盐,后者是硫酸的钾盐,D正确;
故选D。
9.B
解析:A.丁达尔现象是胶体的性质,光线透过胶体时,胶体中可发生丁达尔效应,故A正确;
B.胶体具有丁达尔现象,溶液无此性质,用聚光手电筒照射NaCl溶液和Fe(OH)3胶体时,产生的现象不相同,故B错误;
C.Fe(OH)3胶体具有较大的表面积,具有吸附悬浮杂质的作用,Fe(OH)3胶体能够吸附水中悬浮的固体颗粒并沉降,达到净水目的,故C正确;
D.分散质微粒直径大小是分散系的本质区别,胶体区别于其他分散系的本质特征是分散质的微粒直径在1~100nm之间,故D正确。
故答案选:B。
10.C
【分析】根据化合价以及物质的类别可知a为H2S、b为S、c为SO2、d为H2SO3、e为H2SO4、f含有或、g含有或。
解析:A.a为H2S,可以和SO2、H2SO3、H2SO4发生归中反应生成硫单质,A正确;
B.H2SO3具有较强的还原性,在空气久置会被氧气氧化成硫酸,硫酸酸性更强,pH更小,B正确;
C.由分析可知,f含有或、g含有或,g与f不一定是正盐,C错误;
D.铜与浓硫酸共热产生的气体SO2,由于HCl的酸性强于H2SO3,SO2通入溶液中不能生成亚硫酸钡沉淀,D正确;
故选C。
11.A
解析:A.稀硫酸是硫酸的水溶液,属于混合物,故A正确;
B.Cu2(OH)2CO3能电离出碳酸根离子、铜离子、氢氧根离子,属于盐,故B错误;
C.NH3·H2O电离出的阴离子全是氢氧根离子,NH3·H2O属于碱,故C错误;
D.氧化物中只含两种元素,HCOOH含有C、H、O三种元素,HCOOH不是氧化物,故D错误;
选A。
12.D
解析:A.氮气和氢气生成NH3,氨和空气的混合气通入灼热的铂铑合金网,在合金网的催化下,氨被氧化成一氧化氮。生成的一氧化氮利用反应后残余的氧气继续氧化为二氧化氮,随后将二氧化氮通入水中制取硝酸,转化关系合理,故A不符合题意;
B.S通过和氧气生成SO2,SO2在催化剂条件下生成SO3,SO3通入水中得到,转化关系合理,故B不符合题意;
C.海水提纯可获得NaCl溶液,电解NaCl溶液可制备NaOH,转化关系合理,故C不符合题意;
D.电解饱和氯化镁溶液,在阳极处产生氯气,阴极处产生氢气和氢氧化镁,因此不能用这种方法获得镁,转化关系不合理,故D符合题意;
故答案选D。
13.C
解析:A.按照分散剂的不同,胶体可分为:分散剂为液体的分散系为液溶胶、分散剂为气体的分散系为气溶胶,分散剂为固体的分散系为固溶胶,故A正确;
B.丁达尔效应是胶体特有的性质,因此可以用丁达尔效应区别氯化铁溶液和氢氧化铁胶体,故B正确;
C.向氯化铁溶液中加入少量的NaOH溶液反应生成氢氧化铁沉淀,不能制备氢氧化铁胶体,故C错误;
D.根据分散质粒子直径大小把分散系划分为:溶液(小于1nm)、胶体(1nm 100nm)、浊液(大于100nm),故D正确;
故答案选C。
14.A
解析:A.将纳米磁性固体材料分散到水中,当光路通过时,可以看到一条光亮的“通路”,所得的分散系属于胶体,具有丁达尔效应。故其分散质直径在1~100nm之间,故A错误;
B.由选项A分析可知,该分散系为胶体,故当一束光通过时,可以看到一条光亮的“通路”,该现象就是丁达尔效应,故B正确;
C.由选项A分析可知,该分散系为胶体,属于混合物,故C正确;
D.所得的分散系中分散剂为液体,属于液溶胶,故D正确;
故选A。
15.B
解析:A.K2O属于氧化物,故A错误;
B.H2SO4和HNO3都属于酸,故B正确;
C.Na2CO3属于盐,故C错误;
D.Na2SiO3属于盐,故D错误;
故选B。
二、填空题
16.(1) CaO
(2) 有机物 三/3 1:1
解析:(1)①氧气可供给呼吸,化学式为:;
②氧化钙是由Ca、O元素组成的化合物,属于金属氧化物,化学式为:CaO;
③硫酸是电离时产生的阳离子都是氢离子的化合物,属于酸,且硫酸不易挥发,故填:;
④氢氧化铜是电离时产生的阴离子都是氢氧根离子的化合物,属于碱,且氢氧化铜难溶于水,故填:;
(2)①淀粉含碳元素,属于有机物;由化学式可知,淀粉由C、H、O三种元素组成;
②乙炔在氧气中充分燃烧生成二氧化碳和水,该反应的化学方程式为:;乙炔分子中,碳原子与氢原子的个数比:2:2=1:1;
③根据质量守恒定律,化学反应前后,原子的种类和数目不变,反应物中含C、H、N、O的个数分别是2、8、6、8,生成物中含C、H、N、O的个数分别是2、8、0、8,故生成物中还应含6个N,故X的化学式为:。
17.(1)②⑨(2)⑧(3)①③⑤⑩(4)②⑥⑧⑨(5)④⑦
【分析】冰、水混合物的成分只有水,是纯净物;
解析:(1)氧化物是指一种元素与氧元素组成的化合物。符合定义的有②⑨;
(2)碱是指电离出的阴离子只有OH-的化合物,一般是氢氧化物的形式,符合定义的有⑧;
(3)单质是只由一种元素组成的纯净物,符合定义的有①③⑤⑩;
(4)化合物是只由两种或两种以上元素组成的纯净物,符合定义的有②⑥⑧⑨;
(5)混合物是由两种或两种以上的物质混合而得,符合定义的有④⑦。
18. ①⑤ ②⑦ ⑧⑩ ③⑥⑨ ⑤ ④
解析:①空气中主要有氮气、氧气,还有二氧化碳、氢气等,属于混合物;
②金刚石为碳元素形成的单质;
③生石灰成分为CaO,属于氧化物;
④无水酒精的成分为C2H5OH,属于有机化合物;
⑤稀硫酸是硫酸的水溶液,属于混合物;
⑥干冰是固体的二氧化碳,属于氧化物;
⑦铜是金属单质;
⑧高锰酸钾的化学式为KMnO4,属于盐类;
⑨水的化学式为H2O,属于氧化物;
⑩碳酸钠的化学式为Na2CO3,属于盐类;
(1)属于混合物的有①⑤;
(2)属于单质的有②⑦;属于盐类的有⑧⑩;
(3)属于氧化物的有③⑥⑨;属于溶液的有⑤;
(4)属于有机物的是④。
三、元素或物质推断题
19. ③⑤ A 金属单质在室温下不是气态物质 HCl
【分析】A、B、C是中学化学中常见的单质,室温下A为固体,A可能为C、Si、S、常见的金属单质如Na、Mg、Al、Fe、Cu、Zn等;B和C均为气体,B、C可能为H2、N2、O2、Cl2等;化合物D、E溶于水分别得到D溶液、E溶液,“A+E溶液→C+D溶液”为置换反应,即固体单质在溶液中能置换出气体单质,根据置换反应的规律,C为H2,E为HCl,B为Cl2,A为金属单质;A与B、E溶液反应都生成D,则A为Na或Mg或Al或Zn,根据上述分析作答。
解析:A、B、C是中学化学中常见的单质,室温下A为固体,A可能为C、Si、S、常见的金属单质如Na、Mg、Al、Fe、Cu、Zn等;B和C均为气体,B、C可能为H2、N2、O2、Cl2等;化合物D、E溶于水分别得到D溶液、E溶液,“A+E溶液→C+D溶液”为置换反应,即固体单质在溶液中能置换出气体单质,根据置换反应的规律,C为H2,E为HCl,B为Cl2,A为金属单质;A与B、E溶液反应都生成D,则A为Na或Mg或Al或Zn。
(1)A为Na或Mg或Al或Zn,B为Cl2,C为H2,A、B、C三种元素中的任意两种元素形成的化合物可能是氢化物、酸、盐;形成的化合物由两种元素组成,不可能为碱,因为没有O元素且化合物D、E溶于水分别得到D溶液、E溶液,不可能为氧化物;答案为:③⑤
(2)A、B、C三种元素中有一种是金属,这种元素是A、B、C中的A,因为金属单质在室温下不是气态物质。答案为:A 金属单质在室温下不是气态物质
(3)如果E溶液是一种强酸,E的化学式为HCl。答案为:HCl
四、实验题
20. ②③⑤⑥ 碎瓷片或沸石 防止溶液暴沸 分液漏斗 打开分液漏斗上口玻璃塞或者使玻璃塞上的凹槽对准分液漏斗小孔 萃取
【分析】本题考查最基本的蒸馏和萃取操作。
解析:(1)由蒸馏装置可知,必需的仪器为②③⑤⑥,还需加入碎瓷片或沸石,防止溶液暴沸,故答案为;②③⑤⑥,碎瓷片或沸石,防止溶液暴沸;
(2)由萃取装置可知,需要的仪器名称为分液漏斗,为了使该仪器中液体可以顺利流下,应进行的具体操作是打开分液漏斗上口玻璃塞或者使玻璃塞上的凹槽对准分液漏斗小孔,故答案为:分液漏斗,打开分液漏斗上口玻璃塞或者使玻璃塞上的凹槽对准分液漏斗小孔,萃取;
