1.1物质的分类及转化点对点训练(含解析)高一上学期化学人教版(2019)必修第一册
文档属性
| 名称 | 1.1物质的分类及转化点对点训练(含解析)高一上学期化学人教版(2019)必修第一册 |

|
|
| 格式 | docx | ||
| 文件大小 | 491.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-06-25 00:00:00 | ||
图片预览




文档简介
1.1 物质的分类及转化—2 人教版(2019) 必修第一册高中化学
学校:___________姓名:___________班级:___________考号:___________
知识点一;化学物质的分类方法
1.下列关于物质分类的叙述中不正确的是
A.纯碱既是钠盐又是碳酸盐
B.胶体的分散剂可以是固体、液体或气体
C.能电离出的化合物不一定属于酸
D.和都属于氧化物
2.下列关于物质分类的组合正确的是
分类组合 混合物 酸 碱 盐 酸性氧化物
A 汽油
B 盐酸
C 硫酸 HClO CaO
D 漂白粉 HBr KOH CO
A.A B.B C.C D.D
3.按物质的组成进行分类,NO属于
A.碱 B.氧化物 C.盐 D.单质
知识点二:单一分类法
4.下列各组物质,按单质、化合物、混合物顺序排列的是
A.烧碱、液态氨、碘酒 B.白磷、烧碱、豆浆
C.铁、干冰、氯化氢 D.氮气、空气、胆矾
5.下列物质:①纯碱②食盐水③浓盐酸④烧碱⑤液态氧⑥氯酸钾,分类全部正确的是
A.碱——①④ B.纯净物——③④⑤
C.混合物——②⑤ D.盐——①⑥
6.牙齿的主要成分是[Ca5(PO4)3OH]。从物质的分类角度上考虑,Ca5(PO4)3OH不属于
A.碱 B.盐 C.电解质 D.化合物
知识点三:交叉分类法
7.下列有关钠的各项符合图示阴影部分条件要求的是
A B C D
溶液
A.A B.B C.C D.D
8.下图中相邻两种物质均可归属为一类,下列分类正确的是
A.甲中两种物质水溶液都呈碱性 B.乙中两种物质都是碱性氧化物
C.丙中两种物质都是钠盐 D.丁中两种物质都是硫酸盐
9.下列选项中物质的类别属于图中阴影部分的是
A.Na2SO4 B.K2SO4 C.KHSO4 D.NaCl
知识点四:树状分类法
10.下列各组物质,从物质分类的角度看,后者从属前者的一组是
A.金属氧化物、氧化物 B.含氧酸、酸
C.盐、酸式盐 D.钠盐、含钠化合物
11.下列关于物质分类的叙述中,不正确的是
A.属于酸性氧化物 B.属于酸
C.属于碱 D.属于盐
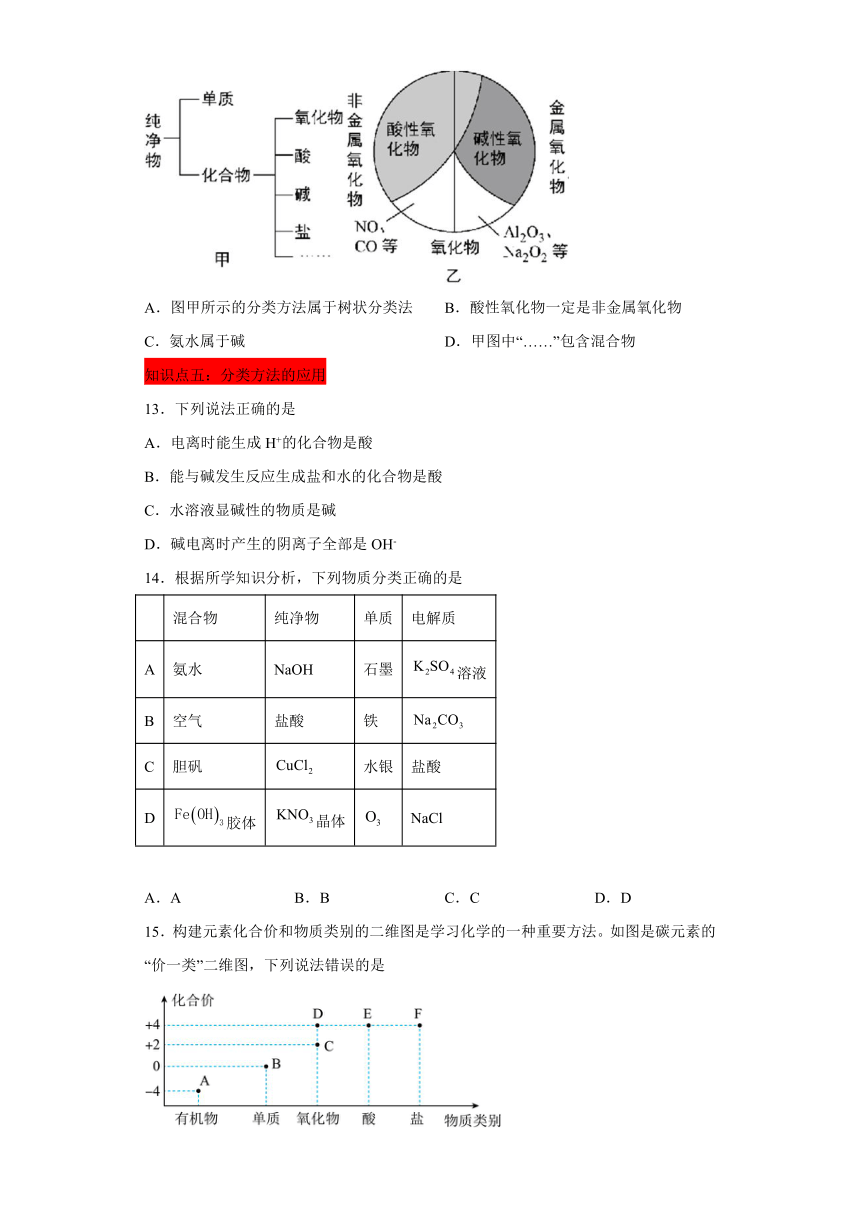
12.分类是一种重要的学习方法。物质的分类如图所示,下列说法中正确的是
A.图甲所示的分类方法属于树状分类法 B.酸性氧化物一定是非金属氧化物
C.氨水属于碱 D.甲图中“……”包含混合物
知识点五:分类方法的应用
13.下列说法正确的是
A.电离时能生成H+的化合物是酸
B.能与碱发生反应生成盐和水的化合物是酸
C.水溶液显碱性的物质是碱
D.碱电离时产生的阴离子全部是OH-
14.根据所学知识分析,下列物质分类正确的是
混合物 纯净物 单质 电解质
A 氨水 NaOH 石墨 溶液
B 空气 盐酸 铁
C 胆矾 水银 盐酸
D 胶体 晶体 NaCl
A.A B.B C.C D.D
15.构建元素化合价和物质类别的二维图是学习化学的一种重要方法。如图是碳元素的“价一类”二维图,下列说法错误的是
A.A点可能是
B.B点对应的物质充分燃烧可能得到D点对应的物质
C.某化合物的化学式为,它对应的点是F
D.C点对应的物质与水反应可能得到E点对应的物质
能力提升
16.对下列物质分类,并完善表格内容
① ② ③ ④ ⑤ ⑥ ⑦ ⑧ ⑨ ⑩
物质 分类依据 物质类型 实例
酸 根据酸根离子是否含有氧元素 含氧酸 _______
无氧酸 _______
根据一定条件下能电离出的数目 一元酸 _______
二元酸 _______
三元酸 _______
根据电离程度 强酸 _______
弱酸 _______
根据沸点高低 高沸点酸 _______
低沸点酸 _______
盐 根据生成盐时酸、碱中和反应进行的程度 正盐 _______
酸式盐 _______
碱式盐 _______
根据生成盐的酸或碱的强弱 强酸强碱盐 _______
强酸弱碱盐 _______
弱酸强碱盐 _______
根据溶解性 易溶性盐 _______
难溶性盐 _______
17.对于数以千万计的化学物质和十分丰富的化学变化,分类法的作用几乎是无可替代。某化学兴趣小组对下列四组物质进行研究:
A.HCl、H2SO4、H2CO3、HNO3 B.、NaNO3、AgNO3、Ba(NO3)2
C.FeCl3溶液、蒸馏水、CaCO3悬浊液、Fe(OH)3胶体 D.NaOH、KOH、Ba(OH)2、Fe2O3
(1)填写下列空白:
A组 B组 C组 D组
分类标准 含氧酸 ②_______ 分散系 ④_______
不属于该类别的物质 ①_______ Na2CO3 ③_______ Fe2O3
(2)写出(1)表中“不属于该类别的物质”发生反应的化学方程式。
A(足量)+B→气体:_______;
A+D:_______
(3)取一小烧杯加入20ml蒸馏水,加热至沸腾后,向沸水中滴入几滴_______溶液,继续煮沸直至溶液呈_______色,即制得Fe(OH)3胶体,将制得的胶体放置于暗处用激光笔照射,可以产生_______效应。这个实验可以用来区别_______ 。
18.下列四组物质中,均有一种物质的类别与其它三种不同。
①MgO、Na2O、CO2、CuO
②NaHCO3、NaHSO4、NaNO3、NaHS
③NaOH、Na2CO3、KOH、SO2
④氯化钠溶液、硫酸铜溶液、氢氧化铁胶体、硫酸铁溶液
(1)四种物质依次是(填化学式):① _________ , ② _________ ③ _________ ,④ _________。
(2)写出满足下列条件要求对应的化学方程式。①反应物从以上各组物质中任选两种;②要求能体现出酸性氧化物的性质_________。
(3)实验室制取氢氧化铁胶体应将饱和溶液逐滴滴入沸水中,继续加热至_________色时,停止加热。
19.下表中有三组物质,每组四种物质中有一种物质与其它三种物质属于不同的类别。请选出该物质,并把该物质及选择该物质的依据填在下表相应的空格中。
序号 物质 被选出的物质 选择依据
(1) O2、H2、C、N2
(2) Fe、Na、Al、Si
(3) NO、CO2、SO2、Fe3O4
(1)________________,___________________;
(2)_________________,______________________;
(3)_______________________,_______________________。
20.回答下列问题:
(1)(树状分类法)填写有关物质分类空格:_______、_______、_______、_______、_______、_______、_______。
(2)(交叉分类法)把“物质”与“物质类别”连接起来:_______。
物质 物质类别
Na2CO3 钠盐
Na2SO4 钾盐
K2SO4 硫酸盐
K2CO3 碳酸盐
参考答案:
1.D
【详解】A.纯碱是碳酸钠的俗称,从组成上看,碳酸钠既是钠盐又是碳酸盐,故A正确;
B.胶体种类很多,胶体的分散剂可以是液体、气体和固体,所以胶体分为液溶胶,气溶胶和固溶胶三大类,故B正确;
C.电离出的阳离子全部是氢离子的化合物属于酸,能电离出氢离子的化合物不一定属于酸,如硫酸氢钠是在溶液中能电离出氢离子的酸式盐,故C正确;
D.乙醇分子中含有氢元素、碳元素、氧元素,属于烃的衍生物,不属于氧化物,故D错误;
故选D。
2.B
【详解】A.C2H5OH为有机化合物中的醇,不属于碱,A项错误;
B.B组内物质分类都正确,B项正确;
C.酸性氧化物能与水作用生成酸或与碱作用生成盐和水,CaO和水反应生成碱Ca(OH)2,属于碱性氧化物,不属于酸性氧化物,C项错误;
D.CO既不能与酸作用生成盐和水,也不能与碱作用生成盐和水,没有相应的氢氧化物,属于中性氧化物(也称为不成盐氧化物),不属于酸性氧化物,D项错误。
答案选B。
3.B
【详解】NO由两种元素组成,其中一种元素为O元素,故NO为氧化物,综上所述故选B。
4.B
【详解】A.烧碱、液态氧、碘酒分别是化合物、单质和混合物,A错误;
B.白磷、烧碱、豆浆分别是单质、化合物和混合物,B正确;
C.铁、干冰、氯化氢分别是单质、化合物和化合物,C错误;
D.氮气、空气、胆矾分别是单质、混合物和化合物,D错误;
故选B。
5.D
【详解】A.纯碱是碳酸钠,属于盐,故A错误;
B.浓硫酸是混合物,故B错误;
C.液态氧中只含氧分子,液态氧属于纯净物,浓硫酸属于混合物,故C错误;
D.纯碱是碳酸钠,属于盐;氯酸钾由K+、构成,氯酸钾属于盐,故D正确;
故选D。
6.A
【详解】Ca5(PO4)3OH可以电离出钙离子、磷酸根离子、氢氧根离子,由金属离子和酸根离子组成,属于盐;故选:A。
7.B
【详解】A.为亚硫酸盐,钠盐,A错误;
B.是化合反应,是氧化还原反应,B正确;
C.溶液焰色试验为黄色,但不是电解质,C错误;
D.是离子反应,是置换反应,D错误;
故选B。
8.D
【详解】A.甲中NH3的水溶液呈碱性,但SO2的水溶液呈酸性,A不正确;
B.乙中Na2O为碱性氧化物,但SO2为酸性氧化物,B不正确;
C.丙中两种物质,前者是钠的氧化物,后者是钠盐,C不正确;
D.丁中两种物质都是硫酸盐,前者是硫酸的钠盐,后者是硫酸的钾盐,D正确;
故选D。
9.B
【详解】A.Na2SO4电离产生的金属阳离子是Na+,而不是K+,因此不属于钾盐,A不符合题意;
B.K2SO4电离产生的金属阳离子是K+,阴离子是SO,无其它离子产生,因此该盐属于正盐、硫酸盐、钾盐,B符合题意;
C.KHSO4电离产生的阳离子中,除了K+外,还有H+,因此属于酸式盐,而不属于正盐,C不符合题意;
D.NaCl电离产生的阴离子是Cl-,而不是SO,因此不属于硫酸盐,阳离子是Na+,不是钾盐,D不符合题意;
故合理选项是B。
10.C
【详解】A.金属氧化物属于氧化物,A错误;
B.含氧酸属于酸,B错误;
C.盐包括酸式盐,C正确;
D.钠盐属于含钠化合物,D错误;
故选C。
11.D
【详解】A.是非金属氧化物,属于酸性氧化物,故A正确;
B.属于中强酸,故B正确;
C.电离出的阴离子全部是氢氧根,属于碱,故C正确;
D.是氢化物,不属于盐,故D错误。
综上所述,答案为D。
12.A
【详解】A.树状分类法含义:对同一类事物按照某些属性进行分类的分类法,从甲图形看应属于树状分类法,故A正确;
B.酸性氧化物不一定是非金属氧化物,如金属氧化物为酸性氧化物,故B错误;
C.氨水为混合物,故C错误;
D.甲图中“……”是化合物的分类,不包含混合物,故D错误;
故答案为A。
13.D
【详解】A.电离时能生成H+的化合物不一定是酸,如NaHSO4是盐类,A错误;
B.能与碱反应生成水的化合物可能是酸、酸性氧化物等,B错误;
C.水溶液呈碱性的物质不一定是碱,如Na2CO3是盐类,C错误;
D.电离产生的阴离子全是OH-的化合物为碱,D正确;
故选D。
14.D
【详解】A.K2SO4溶液为混合物,不是电解质,A错误;
B.盐酸为混合物不是纯净物,B错误;
C.胆矾是五水硫酸铜,是纯净物不是混合物,盐酸是混合物不是电解质,C错误;
D.选项中四种物质分类正确,D正确;
故答案选D。
15.D
【详解】A.A点为碳元素的有机物,C为-4价,可能是,A项正确;
B.B点对应物质为碳单质,充分燃烧生成,为D点对应物质,B项正确;
C.为盐,对应点是F,C项正确;
D.C点对应物质为,不能与水反应,D项错误;
故选D。
16. ②③⑤ ①④⑥ ①②⑥ ③④ ⑤ ①②③ ④⑤⑥ ③⑤ ①②④⑥ ⑦⑩ ⑧ ⑨ ⑦ ⑩ ⑧ ⑧⑩ ⑦⑨
【详解】电离出的阳离子全部为氢离子的化合物属于酸,故属于酸的物质有:① ② ③ ④ ⑤ ⑥;
根据酸根离子是否含有氧元素可以将酸分为两类,含氧酸:②③⑤;无氧酸:①④⑥;
根据一定条件下能电离出的数目,可以将酸分为:一元酸:①②⑥;二元酸:③④;三元酸:⑤;
根据电离程度可以将酸分为两类,强酸:①②③;弱酸:④⑤⑥;
根据沸点高低,可以将酸分为两类,高沸点酸:③⑤;低沸点酸:①②④⑥;
阳离子含有金属阳离子或铵根离子的化合物属于盐,属于盐的物质有:⑦ ⑧ ⑨ ⑩;
根据生成盐时酸、碱中和反应进行的程度,可以将盐分为:正盐:⑦⑩;酸式盐:⑧;碱式盐:⑨;
根据生成盐的酸或碱的强弱,可以将盐分为:强酸强碱盐:⑦;强酸弱碱盐:⑩;弱酸强碱盐:⑧;
根据溶解性,可以将盐分为:易溶性盐:⑧⑩;难溶性盐:⑦⑨。
17.(1) HCl 硝酸盐 蒸馏水 碱
(2) 6HCl + Fe2O3 = 2FeCl3 +3H2O
(3) 饱和FeCl3 红褐 丁达尔 溶液和胶体
【详解】(1)A组中为无氧酸,其余三个均是含氧酸;B组中、、均属于硝酸盐,属于碳酸盐而不属于硝酸盐;C组中蒸馏水为化合物,属于纯净物,其余为分散系,属于混合物;D组中、、均属于碱,属于氧化物;
(2)A+B→气体是碳酸钠和盐酸反应,反应的化学方程式为,A和D反应是盐酸溶解氧化铁,反应的化学方程式为;
(3)取一小烧杯加入20ml蒸馏水,加热至沸腾后,向沸水中滴入几滴饱和FeCl3溶液,继续煮沸直至溶液呈红褐色,即制得Fe(OH)3胶体,将制得的胶体放置于暗处用激光笔照射,可以产生丁达尔效应,这个实验可以用来区别溶液和胶体。
18.(1) CO2 NaNO3 SO2 Fe(OH)3
(2)CO2+2KOH=K2CO3+H2O(或SO2+2NaOH=Na2SO3+H2O等)
(3)红褐色
【详解】(1)①中只有CO2是非金属氧化物,其余是金属氧化物;②中只有NaNO3是正盐,其余都是酸式盐;③中只有SO2是非电解质,其余物质都是电解质;④中只有氢氧化铁胶体属于胶体,其余物质都是溶液,故上述四种物质中与其它三种不同物质类别的化学式依次是:①CO2;②NaNO3;③SO2;④Fe(OH)3;
(2)CO2是酸性氧化物,能够与碱KOH反应产生K2CO3、H2O,该反应的化学方程式为:CO2+2KOH=K2CO3+H2O;或SO2是酸性氧化物,能够与碱NaOH反应产生Na2SO3、H2O,该反应的化学方程式为:SO2+2NaOH=Na2SO3+H2O;
(3)实验室制取氢氧化铁胶体应将饱和溶液逐滴滴入沸水中,继续加热至液体呈红褐色停止加热,就制取得到氢氧化铁胶体。
19. C 通常为固体 Si 非金属 Fe3O4 金属氧化物
【详解】1)O2、H2、N2 是气体单质,C是固体分金属单质,被选出的是C,故答案为C;通常为固体(2)Fe、Na、Al属于金属单质,Si是非金属单质,被选出的是Si,故答案为Si; 非金属 (3)NO、CO2、SO2属于分金属氧化物,Fe3O4 是金属氧化物,被选出的是Fe3O4 ,
故答案为Fe3O4;金属氧化物。
20.(1) 纯净物 化合物 无机化合物 酸 碱 盐 氧化物(或氢化物)
(2)
【解析】(1)
物质可分为纯净物和混合物,纯净物分为单质和化合物,化合物分为有机化合物和无机化合物,无机化合物又分为酸、碱、盐、氧化物(或氢化物),故答案为:纯净物;化合物;无机化合物;酸;碱;盐;氧化物(或氢化物);
(2)
Na2CO3既属于钠盐、又属于碳酸盐;Na2SO4既属于钠盐、又属于硫酸盐;K2SO4既属于钾盐、又属于硫酸盐;K2CO3既属于钾盐、又属于碳酸盐,故答案为:。
学校:___________姓名:___________班级:___________考号:___________
知识点一;化学物质的分类方法
1.下列关于物质分类的叙述中不正确的是
A.纯碱既是钠盐又是碳酸盐
B.胶体的分散剂可以是固体、液体或气体
C.能电离出的化合物不一定属于酸
D.和都属于氧化物
2.下列关于物质分类的组合正确的是
分类组合 混合物 酸 碱 盐 酸性氧化物
A 汽油
B 盐酸
C 硫酸 HClO CaO
D 漂白粉 HBr KOH CO
A.A B.B C.C D.D
3.按物质的组成进行分类,NO属于
A.碱 B.氧化物 C.盐 D.单质
知识点二:单一分类法
4.下列各组物质,按单质、化合物、混合物顺序排列的是
A.烧碱、液态氨、碘酒 B.白磷、烧碱、豆浆
C.铁、干冰、氯化氢 D.氮气、空气、胆矾
5.下列物质:①纯碱②食盐水③浓盐酸④烧碱⑤液态氧⑥氯酸钾,分类全部正确的是
A.碱——①④ B.纯净物——③④⑤
C.混合物——②⑤ D.盐——①⑥
6.牙齿的主要成分是[Ca5(PO4)3OH]。从物质的分类角度上考虑,Ca5(PO4)3OH不属于
A.碱 B.盐 C.电解质 D.化合物
知识点三:交叉分类法
7.下列有关钠的各项符合图示阴影部分条件要求的是
A B C D
溶液
A.A B.B C.C D.D
8.下图中相邻两种物质均可归属为一类,下列分类正确的是
A.甲中两种物质水溶液都呈碱性 B.乙中两种物质都是碱性氧化物
C.丙中两种物质都是钠盐 D.丁中两种物质都是硫酸盐
9.下列选项中物质的类别属于图中阴影部分的是
A.Na2SO4 B.K2SO4 C.KHSO4 D.NaCl
知识点四:树状分类法
10.下列各组物质,从物质分类的角度看,后者从属前者的一组是
A.金属氧化物、氧化物 B.含氧酸、酸
C.盐、酸式盐 D.钠盐、含钠化合物
11.下列关于物质分类的叙述中,不正确的是
A.属于酸性氧化物 B.属于酸
C.属于碱 D.属于盐
12.分类是一种重要的学习方法。物质的分类如图所示,下列说法中正确的是
A.图甲所示的分类方法属于树状分类法 B.酸性氧化物一定是非金属氧化物
C.氨水属于碱 D.甲图中“……”包含混合物
知识点五:分类方法的应用
13.下列说法正确的是
A.电离时能生成H+的化合物是酸
B.能与碱发生反应生成盐和水的化合物是酸
C.水溶液显碱性的物质是碱
D.碱电离时产生的阴离子全部是OH-
14.根据所学知识分析,下列物质分类正确的是
混合物 纯净物 单质 电解质
A 氨水 NaOH 石墨 溶液
B 空气 盐酸 铁
C 胆矾 水银 盐酸
D 胶体 晶体 NaCl
A.A B.B C.C D.D
15.构建元素化合价和物质类别的二维图是学习化学的一种重要方法。如图是碳元素的“价一类”二维图,下列说法错误的是
A.A点可能是
B.B点对应的物质充分燃烧可能得到D点对应的物质
C.某化合物的化学式为,它对应的点是F
D.C点对应的物质与水反应可能得到E点对应的物质
能力提升
16.对下列物质分类,并完善表格内容
① ② ③ ④ ⑤ ⑥ ⑦ ⑧ ⑨ ⑩
物质 分类依据 物质类型 实例
酸 根据酸根离子是否含有氧元素 含氧酸 _______
无氧酸 _______
根据一定条件下能电离出的数目 一元酸 _______
二元酸 _______
三元酸 _______
根据电离程度 强酸 _______
弱酸 _______
根据沸点高低 高沸点酸 _______
低沸点酸 _______
盐 根据生成盐时酸、碱中和反应进行的程度 正盐 _______
酸式盐 _______
碱式盐 _______
根据生成盐的酸或碱的强弱 强酸强碱盐 _______
强酸弱碱盐 _______
弱酸强碱盐 _______
根据溶解性 易溶性盐 _______
难溶性盐 _______
17.对于数以千万计的化学物质和十分丰富的化学变化,分类法的作用几乎是无可替代。某化学兴趣小组对下列四组物质进行研究:
A.HCl、H2SO4、H2CO3、HNO3 B.、NaNO3、AgNO3、Ba(NO3)2
C.FeCl3溶液、蒸馏水、CaCO3悬浊液、Fe(OH)3胶体 D.NaOH、KOH、Ba(OH)2、Fe2O3
(1)填写下列空白:
A组 B组 C组 D组
分类标准 含氧酸 ②_______ 分散系 ④_______
不属于该类别的物质 ①_______ Na2CO3 ③_______ Fe2O3
(2)写出(1)表中“不属于该类别的物质”发生反应的化学方程式。
A(足量)+B→气体:_______;
A+D:_______
(3)取一小烧杯加入20ml蒸馏水,加热至沸腾后,向沸水中滴入几滴_______溶液,继续煮沸直至溶液呈_______色,即制得Fe(OH)3胶体,将制得的胶体放置于暗处用激光笔照射,可以产生_______效应。这个实验可以用来区别_______ 。
18.下列四组物质中,均有一种物质的类别与其它三种不同。
①MgO、Na2O、CO2、CuO
②NaHCO3、NaHSO4、NaNO3、NaHS
③NaOH、Na2CO3、KOH、SO2
④氯化钠溶液、硫酸铜溶液、氢氧化铁胶体、硫酸铁溶液
(1)四种物质依次是(填化学式):① _________ , ② _________ ③ _________ ,④ _________。
(2)写出满足下列条件要求对应的化学方程式。①反应物从以上各组物质中任选两种;②要求能体现出酸性氧化物的性质_________。
(3)实验室制取氢氧化铁胶体应将饱和溶液逐滴滴入沸水中,继续加热至_________色时,停止加热。
19.下表中有三组物质,每组四种物质中有一种物质与其它三种物质属于不同的类别。请选出该物质,并把该物质及选择该物质的依据填在下表相应的空格中。
序号 物质 被选出的物质 选择依据
(1) O2、H2、C、N2
(2) Fe、Na、Al、Si
(3) NO、CO2、SO2、Fe3O4
(1)________________,___________________;
(2)_________________,______________________;
(3)_______________________,_______________________。
20.回答下列问题:
(1)(树状分类法)填写有关物质分类空格:_______、_______、_______、_______、_______、_______、_______。
(2)(交叉分类法)把“物质”与“物质类别”连接起来:_______。
物质 物质类别
Na2CO3 钠盐
Na2SO4 钾盐
K2SO4 硫酸盐
K2CO3 碳酸盐
参考答案:
1.D
【详解】A.纯碱是碳酸钠的俗称,从组成上看,碳酸钠既是钠盐又是碳酸盐,故A正确;
B.胶体种类很多,胶体的分散剂可以是液体、气体和固体,所以胶体分为液溶胶,气溶胶和固溶胶三大类,故B正确;
C.电离出的阳离子全部是氢离子的化合物属于酸,能电离出氢离子的化合物不一定属于酸,如硫酸氢钠是在溶液中能电离出氢离子的酸式盐,故C正确;
D.乙醇分子中含有氢元素、碳元素、氧元素,属于烃的衍生物,不属于氧化物,故D错误;
故选D。
2.B
【详解】A.C2H5OH为有机化合物中的醇,不属于碱,A项错误;
B.B组内物质分类都正确,B项正确;
C.酸性氧化物能与水作用生成酸或与碱作用生成盐和水,CaO和水反应生成碱Ca(OH)2,属于碱性氧化物,不属于酸性氧化物,C项错误;
D.CO既不能与酸作用生成盐和水,也不能与碱作用生成盐和水,没有相应的氢氧化物,属于中性氧化物(也称为不成盐氧化物),不属于酸性氧化物,D项错误。
答案选B。
3.B
【详解】NO由两种元素组成,其中一种元素为O元素,故NO为氧化物,综上所述故选B。
4.B
【详解】A.烧碱、液态氧、碘酒分别是化合物、单质和混合物,A错误;
B.白磷、烧碱、豆浆分别是单质、化合物和混合物,B正确;
C.铁、干冰、氯化氢分别是单质、化合物和化合物,C错误;
D.氮气、空气、胆矾分别是单质、混合物和化合物,D错误;
故选B。
5.D
【详解】A.纯碱是碳酸钠,属于盐,故A错误;
B.浓硫酸是混合物,故B错误;
C.液态氧中只含氧分子,液态氧属于纯净物,浓硫酸属于混合物,故C错误;
D.纯碱是碳酸钠,属于盐;氯酸钾由K+、构成,氯酸钾属于盐,故D正确;
故选D。
6.A
【详解】Ca5(PO4)3OH可以电离出钙离子、磷酸根离子、氢氧根离子,由金属离子和酸根离子组成,属于盐;故选:A。
7.B
【详解】A.为亚硫酸盐,钠盐,A错误;
B.是化合反应,是氧化还原反应,B正确;
C.溶液焰色试验为黄色,但不是电解质,C错误;
D.是离子反应,是置换反应,D错误;
故选B。
8.D
【详解】A.甲中NH3的水溶液呈碱性,但SO2的水溶液呈酸性,A不正确;
B.乙中Na2O为碱性氧化物,但SO2为酸性氧化物,B不正确;
C.丙中两种物质,前者是钠的氧化物,后者是钠盐,C不正确;
D.丁中两种物质都是硫酸盐,前者是硫酸的钠盐,后者是硫酸的钾盐,D正确;
故选D。
9.B
【详解】A.Na2SO4电离产生的金属阳离子是Na+,而不是K+,因此不属于钾盐,A不符合题意;
B.K2SO4电离产生的金属阳离子是K+,阴离子是SO,无其它离子产生,因此该盐属于正盐、硫酸盐、钾盐,B符合题意;
C.KHSO4电离产生的阳离子中,除了K+外,还有H+,因此属于酸式盐,而不属于正盐,C不符合题意;
D.NaCl电离产生的阴离子是Cl-,而不是SO,因此不属于硫酸盐,阳离子是Na+,不是钾盐,D不符合题意;
故合理选项是B。
10.C
【详解】A.金属氧化物属于氧化物,A错误;
B.含氧酸属于酸,B错误;
C.盐包括酸式盐,C正确;
D.钠盐属于含钠化合物,D错误;
故选C。
11.D
【详解】A.是非金属氧化物,属于酸性氧化物,故A正确;
B.属于中强酸,故B正确;
C.电离出的阴离子全部是氢氧根,属于碱,故C正确;
D.是氢化物,不属于盐,故D错误。
综上所述,答案为D。
12.A
【详解】A.树状分类法含义:对同一类事物按照某些属性进行分类的分类法,从甲图形看应属于树状分类法,故A正确;
B.酸性氧化物不一定是非金属氧化物,如金属氧化物为酸性氧化物,故B错误;
C.氨水为混合物,故C错误;
D.甲图中“……”是化合物的分类,不包含混合物,故D错误;
故答案为A。
13.D
【详解】A.电离时能生成H+的化合物不一定是酸,如NaHSO4是盐类,A错误;
B.能与碱反应生成水的化合物可能是酸、酸性氧化物等,B错误;
C.水溶液呈碱性的物质不一定是碱,如Na2CO3是盐类,C错误;
D.电离产生的阴离子全是OH-的化合物为碱,D正确;
故选D。
14.D
【详解】A.K2SO4溶液为混合物,不是电解质,A错误;
B.盐酸为混合物不是纯净物,B错误;
C.胆矾是五水硫酸铜,是纯净物不是混合物,盐酸是混合物不是电解质,C错误;
D.选项中四种物质分类正确,D正确;
故答案选D。
15.D
【详解】A.A点为碳元素的有机物,C为-4价,可能是,A项正确;
B.B点对应物质为碳单质,充分燃烧生成,为D点对应物质,B项正确;
C.为盐,对应点是F,C项正确;
D.C点对应物质为,不能与水反应,D项错误;
故选D。
16. ②③⑤ ①④⑥ ①②⑥ ③④ ⑤ ①②③ ④⑤⑥ ③⑤ ①②④⑥ ⑦⑩ ⑧ ⑨ ⑦ ⑩ ⑧ ⑧⑩ ⑦⑨
【详解】电离出的阳离子全部为氢离子的化合物属于酸,故属于酸的物质有:① ② ③ ④ ⑤ ⑥;
根据酸根离子是否含有氧元素可以将酸分为两类,含氧酸:②③⑤;无氧酸:①④⑥;
根据一定条件下能电离出的数目,可以将酸分为:一元酸:①②⑥;二元酸:③④;三元酸:⑤;
根据电离程度可以将酸分为两类,强酸:①②③;弱酸:④⑤⑥;
根据沸点高低,可以将酸分为两类,高沸点酸:③⑤;低沸点酸:①②④⑥;
阳离子含有金属阳离子或铵根离子的化合物属于盐,属于盐的物质有:⑦ ⑧ ⑨ ⑩;
根据生成盐时酸、碱中和反应进行的程度,可以将盐分为:正盐:⑦⑩;酸式盐:⑧;碱式盐:⑨;
根据生成盐的酸或碱的强弱,可以将盐分为:强酸强碱盐:⑦;强酸弱碱盐:⑩;弱酸强碱盐:⑧;
根据溶解性,可以将盐分为:易溶性盐:⑧⑩;难溶性盐:⑦⑨。
17.(1) HCl 硝酸盐 蒸馏水 碱
(2) 6HCl + Fe2O3 = 2FeCl3 +3H2O
(3) 饱和FeCl3 红褐 丁达尔 溶液和胶体
【详解】(1)A组中为无氧酸,其余三个均是含氧酸;B组中、、均属于硝酸盐,属于碳酸盐而不属于硝酸盐;C组中蒸馏水为化合物,属于纯净物,其余为分散系,属于混合物;D组中、、均属于碱,属于氧化物;
(2)A+B→气体是碳酸钠和盐酸反应,反应的化学方程式为,A和D反应是盐酸溶解氧化铁,反应的化学方程式为;
(3)取一小烧杯加入20ml蒸馏水,加热至沸腾后,向沸水中滴入几滴饱和FeCl3溶液,继续煮沸直至溶液呈红褐色,即制得Fe(OH)3胶体,将制得的胶体放置于暗处用激光笔照射,可以产生丁达尔效应,这个实验可以用来区别溶液和胶体。
18.(1) CO2 NaNO3 SO2 Fe(OH)3
(2)CO2+2KOH=K2CO3+H2O(或SO2+2NaOH=Na2SO3+H2O等)
(3)红褐色
【详解】(1)①中只有CO2是非金属氧化物,其余是金属氧化物;②中只有NaNO3是正盐,其余都是酸式盐;③中只有SO2是非电解质,其余物质都是电解质;④中只有氢氧化铁胶体属于胶体,其余物质都是溶液,故上述四种物质中与其它三种不同物质类别的化学式依次是:①CO2;②NaNO3;③SO2;④Fe(OH)3;
(2)CO2是酸性氧化物,能够与碱KOH反应产生K2CO3、H2O,该反应的化学方程式为:CO2+2KOH=K2CO3+H2O;或SO2是酸性氧化物,能够与碱NaOH反应产生Na2SO3、H2O,该反应的化学方程式为:SO2+2NaOH=Na2SO3+H2O;
(3)实验室制取氢氧化铁胶体应将饱和溶液逐滴滴入沸水中,继续加热至液体呈红褐色停止加热,就制取得到氢氧化铁胶体。
19. C 通常为固体 Si 非金属 Fe3O4 金属氧化物
【详解】1)O2、H2、N2 是气体单质,C是固体分金属单质,被选出的是C,故答案为C;通常为固体(2)Fe、Na、Al属于金属单质,Si是非金属单质,被选出的是Si,故答案为Si; 非金属 (3)NO、CO2、SO2属于分金属氧化物,Fe3O4 是金属氧化物,被选出的是Fe3O4 ,
故答案为Fe3O4;金属氧化物。
20.(1) 纯净物 化合物 无机化合物 酸 碱 盐 氧化物(或氢化物)
(2)
【解析】(1)
物质可分为纯净物和混合物,纯净物分为单质和化合物,化合物分为有机化合物和无机化合物,无机化合物又分为酸、碱、盐、氧化物(或氢化物),故答案为:纯净物;化合物;无机化合物;酸;碱;盐;氧化物(或氢化物);
(2)
Na2CO3既属于钠盐、又属于碳酸盐;Na2SO4既属于钠盐、又属于硫酸盐;K2SO4既属于钾盐、又属于硫酸盐;K2CO3既属于钾盐、又属于碳酸盐,故答案为:。
