专题6 生命活动的物质基础—糖类、油脂、蛋白质 单元检测题(含答案) 2022-2023学年高二下学期化学苏教版(2019)选择性必修3
文档属性
| 名称 | 专题6 生命活动的物质基础—糖类、油脂、蛋白质 单元检测题(含答案) 2022-2023学年高二下学期化学苏教版(2019)选择性必修3 |

|
|
| 格式 | docx | ||
| 文件大小 | 269.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-06-25 00:00:00 | ||
图片预览




文档简介
专题6《生命活动的物质基础—糖类、油脂、蛋白质》单元检测题
一、单选题(共13题)
1.新版人民币的发行,引发了人们对有关人民币中化学知识的关注。下列表述不正确的是
A.制造人民币所用的棉花、优质针叶木等原料的主要成分是纤维素
B.用于人民币票面文字等处的油墨中所含有的Fe2O3是一种磁性物质
C.防伪荧光油墨由颜料与树脂等制成,其中树脂属于有机高分子材料
D.某种验钞笔中含有碘酒溶液,遇假钞呈现蓝色,其中遇碘变蓝的是淀粉
2.蛋白质是生命的物质基础,是生命活动的主要承担者。下列有关蛋白质的说法正确的是
A.蛋白质分子能透过半透膜
B.氨基酸和蛋白质遇重金属离子均会变性
C.酶是一种高效的生物催化剂,所有的酶都属于蛋白质
D.用甘氨酸和丙氨酸缩合最多可形成四种二肽
3.有关糖类物质的叙述正确的是
A.糖类是有甜味的物质
B.由碳、氢、氧三种元素组成的有机物属于糖类
C.葡萄糖和果糖互为同系物,蔗糖和麦芽糖互为同系物
D.糖类可分为单糖、二糖和多糖
4.化学创造美好生活。下列日常活动或现象对应的化学原理分析不正确的是
选项 日常活动或现象 化学原理
A “冬月灶中所烧薪柴之灰,令人以灰淋汁,取碱浣衣。”——《 本草纲目》 “薪柴之灰”含碳酸钾,其水溶液显碱性,“浣衣”时能促进油污的水解
B 用二氧化硫漂白草帽和用臭氧漂白纸浆 二者的漂白原理相同
C 把石灰浆喷涂在树皮上,消灭过冬虫卵 碱性环境使虫卵蛋白质变性而死亡
D 春节前客家人酿制娘酒 淀粉先水解成葡萄糖等,然后在酒曲酶作用下转化为乙醇
A.A B.B C.C D.D
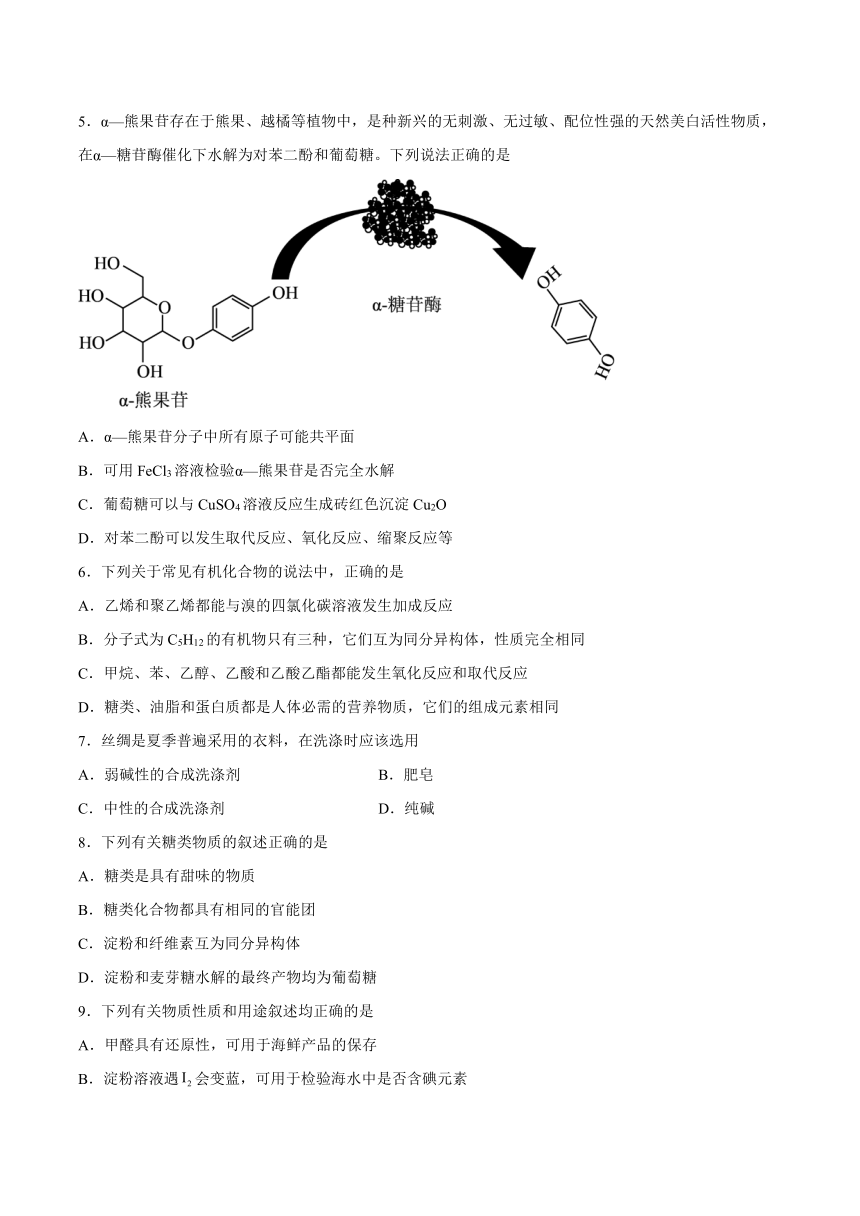
5.α—熊果苷存在于熊果、越橘等植物中,是种新兴的无刺激、无过敏、配位性强的天然美白活性物质,在α—糖苷酶催化下水解为对苯二酚和葡萄糖。下列说法正确的是
A.α—熊果苷分子中所有原子可能共平面
B.可用FeCl3溶液检验α—熊果苷是否完全水解
C.葡萄糖可以与CuSO4溶液反应生成砖红色沉淀Cu2O
D.对苯二酚可以发生取代反应、氧化反应、缩聚反应等
6.下列关于常见有机化合物的说法中,正确的是
A.乙烯和聚乙烯都能与溴的四氯化碳溶液发生加成反应
B.分子式为C5H12的有机物只有三种,它们互为同分异构体,性质完全相同
C.甲烷、苯、乙醇、乙酸和乙酸乙酯都能发生氧化反应和取代反应
D.糖类、油脂和蛋白质都是人体必需的营养物质,它们的组成元素相同
7.丝绸是夏季普遍采用的衣料,在洗涤时应该选用
A.弱碱性的合成洗涤剂 B.肥皂
C.中性的合成洗涤剂 D.纯碱
8.下列有关糖类物质的叙述正确的是
A.糖类是具有甜味的物质
B.糖类化合物都具有相同的官能团
C.淀粉和纤维素互为同分异构体
D.淀粉和麦芽糖水解的最终产物均为葡萄糖
9.下列有关物质性质和用途叙述均正确的是
A.甲醛具有还原性,可用于海鲜产品的保存
B.淀粉溶液遇会变蓝,可用于检验海水中是否含碘元素
C.蛋白质能水解,可供给人体营养
D.乙烯能被酸性高锰酸钾溶液氧化,可用浸泡过高锰酸钾溶液的硅藻土保鲜水果
10.《天工开物》中记载:“凡乌金纸由苏、杭造成,其纸用东海巨竹膜为质。用豆油点灯,闭塞周围,只留针孔通气,熏染烟光而成此纸”。下列说法错误的是
A.“乌金纸”的“乌”与豆油不完全燃烧有关
B.“巨竹膜”为造纸的原料,其主要成分是淀粉
C.豆油的主要成分油脂属于天然有机化合物
D.豆油可发生硬化、皂化等反应
11.GFP是一种能发光的荧光蛋白质,下列关于GFP的叙述合理的是
A.GFP在硫酸铜或饱和硫酸铵溶液中发生盐析,盐析是可逆过程
B.GFP在酸、碱或酶作用下发生水解,水解的最终产物氨基酸只能与碱反应
C.GFP在乙醇等作用下会凝结变性,变性是不可逆的
D.GFP与水的液态混合物可用盐析法分离,盐析法为化学方法
12.化学与人类生活、生产密切相关,下列说法中不正确的是
A.工业上利用油脂在碱性条件下水解生产肥皂
B.疫苗等生物制剂需要在低温下保存
C.淀粉、纤维素、蔗糖均属于高分子化合物且都能发生水解
D.脱氧核糖与碱基、磷酸基团共同组成脱氧核糖核苷酸
13.我国航天技术发展迅速,天宫、天和、天舟、巡天、问天、梦天、嫦娥、天问、神舟等体现了中国的强大科技力量,下列说法错误的是
A.“天问一号”火星车使用的热控保温材料纳米气凝胶可产生丁达尔效应
B.“嫦娥五号”月球车上的国旗是由优质高分子材料嵌入纤维制成的,纤维也属于高分子材料
C.“天宫二号”空间站使用了石墨烯存储器,石墨烯与金刚石互为同分异构体
D.“天和”核心舱使用了柔性三结砷化镓太阳能电池阵,砷化镓属于半导体
二、非选择题(共10题)
14.如图所示是一份体检报告,阅读后回答下列问题。
检验报告
血脂全套
项目名称 结果 参考值 单位 提示
甘油三酯 2.20 0~1.70 ↑
总胆固醇 5.50 <5.20 ↑
高密度脂蛋白胆固醇 1.56 0.9~2.0
低密度脂蛋白胆固醇 3.61 0~3.40 ↑
空腹血糖
项目名称 结果 参考值 单位 提示
空腹血糖 6.21 3.9~6.1 ↑
(1)查阅资料,了解所列检测项目对于人体生理活动产生的作用___________。
(2)针对检测结果,请对心血管系统疾病的潜在风险进行评估___________。
(3)如果这是你的体检结果,你会从饮食、运动等方面做出哪些调整___________?
15.某油脂厂废弃的油脂加氢镍催化剂主要含金属Ni、Al、Fe及其氧化物,还有少量其他不溶性物质。采用如下工艺流程回收其中的镍制备硫酸镍晶体(NiSO4·7H2O):
“碱浸”中NaOH的两个作用分别是___________
三、实验题
16.葡萄糖酸钙是一种有机钙盐,外观为白色结晶性或颗粒性粉末,无臭,无味,易溶于沸水,微溶于冷水,不溶于乙醇或乙醚等有机溶剂。葡萄糖酸钙临床上用于治疗骨质疏松症。实验室制备葡萄糖酸钙主要步骤如下:
I.葡萄糖酸溶液的制备
称取适量的葡萄糖[CH2OH(CHOH)4CHO],置于三颈烧瓶中,加入足量的溴水,在磁力搅拌器中沸水浴加热、搅拌得到无色透明的葡萄糖酸溶液。当氧化率达 80%以上时(60min),停止反应,把反应液冷却至 60-70℃待用。
Ⅱ.葡萄糖酸钙的制备
在搅拌下,分批加入足量的碳酸钙至葡萄糖酸溶液中。反应完全后,趁热用下图装置抽滤,得到澄清透明的葡萄糖酸钙溶液。将葡萄糖酸钙溶液转入 100ml 烧杯中冷却至室温,向烧杯中添加适量的无水乙醇,静置 10min 得到悬浊液,抽滤、洗涤、干燥得到白色的葡萄糖酸钙固体。
回答下列问题:
(1)步骤Ⅰ中,滴入溴水后,反应的化学方程式为_______。
(2)步骤 Ⅱ 中,判断碳酸钙已经足量的实验现象是_______。
(3)步骤Ⅱ抽滤时自来水流的作用是使瓶内与大气形成压强差,与普通过滤操作相比,抽滤的优点是_______;装置 B 的作用是_______。
(4)洗涤操作洗涤剂最合适的是________(填序号),理由是_______。
A.冷水 B.热水 C.乙醇
Ⅲ.葡萄糖酸钙中钙质量分数的测定
测定步骤:
(i)准确称取葡萄糖酸钙 m g,加入去离子水溶解,定容,配成 250mL 溶液。
(ii)用 c mol/L EDTA(H2Y2-)标准溶液润洗滴定管后,装入 EDTA 标准液,调至零刻度。
(iii)向 250mL 锥形瓶中加入 10mL 水、10mL NH3-NH4Cl 缓冲溶液和 5 mL 硫酸镁溶液。滴加 4 滴铬黑 T(HIn2-)指示剂,摇匀。用 EDTA 标准液滴定至终点。记录消耗的 EDTA 标准液的体积。
滴定过程中发生的反应如下:
Mg2+ + HIn2-(蓝色) MgIn-(酒红色)+ H+
Mg2+ + H2Y2- MgY2- + 2H+
MgIn-(酒红色)+ H2Y2- MgY2- + H+ + HIn2-(蓝色)
(iv)向上述锥形瓶中加入 25.00 mL 葡萄糖酸钙溶液,摇匀,继续用 EDTA 标准液滴定至终点,记录消耗的 EDTA 标准液的总体积。平行滴定三次,测得步骤 iii 中消耗 EDTA 标准液的平均体积为 V1 L,步骤 iv 中 EDTA 标准液的平均总体积为 V2 L。
已知:配合物的稳定常数类似于化学平衡常数,如反应 Fe3+ + 3SCN- Fe(SCN)3 的平衡常数可以看做是 Fe(SCN)3 的稳定常数 K稳,一般情况下,配合物的稳定常数越大,配合物越稳定,两种离子更容易结合。已知下列化合物稳定常数的大小顺序为 CaY2- > MgY2- > MgIn- > CaIn-,其中CaIn-的稳定常数很小,CaIn-不稳定,易导致滴定终点提前。
回答下列问题:
(5)步骤 iii 中加入硫酸镁的作用是_______。
(6)滴定终点的颜色变化为_______。
(7)步骤 iv 中,加入葡萄糖酸钙后发生反应的离子方程式为_______,_______。
(8)葡萄糖酸钙中钙的质量分数为_______。(用 V1、V2、m、c 的代数式表示)
17.为检验淀粉水解的情况,进行如下图所示的实验,试管甲和丙均用60~80 ℃的水浴加热5~6 min,试管乙不加热。待试管甲、丙中的溶液冷却后再进行后续实验。
实验1:取少量甲中溶液,加入新制氢氧化铜,加热,没有红色沉淀出现。
实验2:取少量乙中溶液,滴加几滴碘水,溶液变为蓝色,但取少量甲中溶液做此实验时,溶液不变蓝色。
实验3:取少量丙中溶液加入NaOH溶液调节至碱性,再滴加碘水,溶液颜色无明显变化。
(1)写出淀粉水解的化学方程式:___________。
(2)设计甲和乙是为了探究___________对淀粉水解的影响,设计甲和丙是为了探究___________对淀粉水解的影响。
(3)实验1失败的原因是___________。
(4)实验3中溶液的颜色无明显变化的原因是___________。
(5)下列结论合理的是___________(填字母)。
A.淀粉水解需要在催化剂和一定温度下进行
B.欲检验淀粉是否完全水解,最好在冷却后的水解液中直接加碘
C.欲检验淀粉的水解产物具有还原性,应先在水解液中加入氢氧化钠中和稀硫酸至溶液呈碱性,再加入新制氢氧化铜并加热
D.若用唾液代替稀硫酸,则实验1可能出现预期的现象
18.葡萄可用于酿酒。
(1)检验葡萄汁含葡萄糖的方法是:向其中加碱调至碱性,再加入新制备的Cu(OH)2,加热,其现象是____。
(2)葡萄在酿酒过程中,葡萄糖转化为酒精的过程如下,补充完成下列化学方程式:C6H12O6(葡萄糖)2___+2C2H5OH。
(3)葡萄酒密封储存过程中生成了有香味的酯,酯也可以通过化学实验来制备,实验室用如图所示装置制备乙酸乙酯:
①试管a中生成乙酸乙酯的化学方程式是___(请注明反应条件)。
②试管b中盛放的试剂是饱和____溶液。
③实验开始时,试管b中的导管不伸入液面下的原因是___。
④若分离出试管b中生成的乙酸乙酯,需要用到的仪器是___(填序号)。
a.漏斗 b.分液漏斗 c.长颈漏斗 d.恒压滴定漏斗
四、计算题
19.取30.0 g牛奶样品,将所含蛋白质中的氮元素全部转化为氨,用25.00 mL 1. 00 mo1/L的硫酸将其完全吸收,再加入19.00mL2.00 mol/L氢氧化钠溶液恰好生成硫酸钠和硫酸铵。请计算:
(1)样品中蛋白质转化生成的氨的物质的量为_______mo1。
(2)样品蛋白质中含氮元素的质量_______g。
(3)若蛋白质中氮元素的质量分数为14.0%,则样品中蛋白质的质量分数为_______。
20.有葡萄糖和麦芽糖的混合物90g,溶于足量的水中,在稀硫酸催化下充分反应后,用NaOH溶液中和水解液,再加入足量的Cu(OH)2悬浊液并加热煮沸,测得生成Cu2O沉淀为75.6g,求原混合物中麦芽糖的质量分数。
21.10g某天然油脂完全水解需要1.8gNaOH,1kg该油脂进行催化加氢,需消耗12g,才能进行完全。请推断1mol该油脂中平均含有碳碳双键的物质的量________。
22.某同学称取9 g淀粉溶于水,测定淀粉的水解百分率。其程序如下:
(1)各步加入的试剂为(写化学式):A________、B________、C________。
(2)若加入A溶液不加入B溶液_______(填“是”或“否”)合理,其理由是_______________。
(3)已知1 mol葡萄糖与新制Cu(OH)2悬浊液反应生成1 mol Cu2O,当生成1.44 g砖红色沉淀时,淀粉的水解率是________。
(4)某淀粉的相对分子质量为13 932,则它是由________个葡萄糖分子缩合而成的。
23.X由2种元素组成的离子化合物,阳离子与阴离子个数比为1∶2;无色气体B遇空气呈红棕色;C能使带火星的木条复燃;D为砖红色固体,E溶液呈强酸性。
(1)X的组成元素___________;X化学式___________。
(2)的离子方程式___________。
(3)反应转化过程中,生成时消耗葡萄糖的质量至少___________g。
(4)设计检验F溶液中溶质阴离子的实验方案_____。
参考答案:
1.B 2.D 3.D 4.B 5.D 6.C 7.C 8.D 9.D 10.B 11.C 12.C 13.C
14.(1)甘油三酯又称为中性脂肪,是甘油分子与脂肪酸反应所形成的脂类,为血脂的其中一种组成部分,具有为细胞代谢提供能量的功能;
总胆固醇为血液中各种脂蛋白所含胆固醇的总和,胆固醇是细胞膜的主要成分,同时也是合成肾上腺皮质激素、性激素、胆汁酸及维生素D等生理活性物质的重要原料;
高密度脂蛋白胆固醇测定为血脂检查的一项重要内容,该检查可帮助排查冠心病、动脉粥样硬化等疾病。高密度脂蛋白是由胆固醇、磷脂和蛋白质等物质组成的一种血浆脂蛋白,其主要在肝脏和小肠之中合成。具有将肝外组织内的胆固醇运送到肝脏进行分解代谢,排出体外的作用。
低密度脂蛋白是血浆中胆固醇含量占比最高的一类脂蛋白,为蛋白质、胆固醇和磷脂的复合体,是由极低密 度脂蛋白中的TG被水解代谢后转化而来,其主要功能是胆固醇存在于血液中的载体。血液中的低密度脂蛋白浓度过高、且未能被肝脏有效摄取,则可沉积于动脉内壁、促使动脉壁形成动脉粥样斑块,为动脉粥样硬化的致病性危险因素。
血糖是指血液中葡萄糖的含量,属于糖代谢检查,可用于筛查、诊断及监测糖尿病、低血糖症等多种糖代谢异常相关疾病,反映了机体对葡萄糖的吸收、代谢是否正常。血糖主要包括空腹血糖及餐后血糖两个检查指 标,检测空腹血糖时患者需要至少禁食8h以上,一般需隔夜空腹检查血糖,餐后血糖是指从进食第一口食物后开始计算时间至2h准时抽血测定血糖值。
(2)患有心血管疾病的风险较大
(3)加强体育健身锻炼,饮食以清淡低盐为主,加强果蔬、粗粮的摄入
15.除去油脂,溶解铝及其氧化物
16.(1)CH2OH(CHOH)4CHO+Br2+H2O=CH2OH(CHOH)4COOH+2HBr
(2)加入碳酸钙不再溶解且不再生成气泡
(3) 速率更快,且得到产品更干燥 起到安全瓶的作用
(4) C 葡萄糖酸钙不溶于乙醇,可减少产品的溶解损失
(5)指示滴定过程中颜色变化,确定加入EDTA 标准液的消耗量
(6)最后一滴EDTA 标准液加入后溶液酒红色褪色且半分钟内不变色
(7) Ca2++MgY2-=CaY2-+Mg2+ Mg2++ HIn2-= H++ MgIn-
(8)
17.(1)(C6H10O5)n+nH2OnC6H12O6
(2) 温度 催化剂
(3)没有加入碱中和作为催化剂的稀硫酸
(4)氢氧化钠与碘反应
(5)ABCD
18. 产生砖红色沉淀 CO2 CH3COOH+C2H5OHCH3COOC2H5+H2O Na2CO3 防止溶液倒吸 b
19.(1)
(2)0.168
(3)4%
20.95%
21.4mol
22.(1) H2SO4 NaOH Cu(OH)2
(2) 否 Cu(OH)2悬浊液与葡萄糖的反应必须在碱性条件下进行
(3)18%
(4)86
23.(1) Cu、N Cu(N3)2
(2)
(3)
(4)取少量F待测液于试管中,浓缩后加入浓与Cu片并加热,观察到红棕色气体,则待测液中含离子
一、单选题(共13题)
1.新版人民币的发行,引发了人们对有关人民币中化学知识的关注。下列表述不正确的是
A.制造人民币所用的棉花、优质针叶木等原料的主要成分是纤维素
B.用于人民币票面文字等处的油墨中所含有的Fe2O3是一种磁性物质
C.防伪荧光油墨由颜料与树脂等制成,其中树脂属于有机高分子材料
D.某种验钞笔中含有碘酒溶液,遇假钞呈现蓝色,其中遇碘变蓝的是淀粉
2.蛋白质是生命的物质基础,是生命活动的主要承担者。下列有关蛋白质的说法正确的是
A.蛋白质分子能透过半透膜
B.氨基酸和蛋白质遇重金属离子均会变性
C.酶是一种高效的生物催化剂,所有的酶都属于蛋白质
D.用甘氨酸和丙氨酸缩合最多可形成四种二肽
3.有关糖类物质的叙述正确的是
A.糖类是有甜味的物质
B.由碳、氢、氧三种元素组成的有机物属于糖类
C.葡萄糖和果糖互为同系物,蔗糖和麦芽糖互为同系物
D.糖类可分为单糖、二糖和多糖
4.化学创造美好生活。下列日常活动或现象对应的化学原理分析不正确的是
选项 日常活动或现象 化学原理
A “冬月灶中所烧薪柴之灰,令人以灰淋汁,取碱浣衣。”——《 本草纲目》 “薪柴之灰”含碳酸钾,其水溶液显碱性,“浣衣”时能促进油污的水解
B 用二氧化硫漂白草帽和用臭氧漂白纸浆 二者的漂白原理相同
C 把石灰浆喷涂在树皮上,消灭过冬虫卵 碱性环境使虫卵蛋白质变性而死亡
D 春节前客家人酿制娘酒 淀粉先水解成葡萄糖等,然后在酒曲酶作用下转化为乙醇
A.A B.B C.C D.D
5.α—熊果苷存在于熊果、越橘等植物中,是种新兴的无刺激、无过敏、配位性强的天然美白活性物质,在α—糖苷酶催化下水解为对苯二酚和葡萄糖。下列说法正确的是
A.α—熊果苷分子中所有原子可能共平面
B.可用FeCl3溶液检验α—熊果苷是否完全水解
C.葡萄糖可以与CuSO4溶液反应生成砖红色沉淀Cu2O
D.对苯二酚可以发生取代反应、氧化反应、缩聚反应等
6.下列关于常见有机化合物的说法中,正确的是
A.乙烯和聚乙烯都能与溴的四氯化碳溶液发生加成反应
B.分子式为C5H12的有机物只有三种,它们互为同分异构体,性质完全相同
C.甲烷、苯、乙醇、乙酸和乙酸乙酯都能发生氧化反应和取代反应
D.糖类、油脂和蛋白质都是人体必需的营养物质,它们的组成元素相同
7.丝绸是夏季普遍采用的衣料,在洗涤时应该选用
A.弱碱性的合成洗涤剂 B.肥皂
C.中性的合成洗涤剂 D.纯碱
8.下列有关糖类物质的叙述正确的是
A.糖类是具有甜味的物质
B.糖类化合物都具有相同的官能团
C.淀粉和纤维素互为同分异构体
D.淀粉和麦芽糖水解的最终产物均为葡萄糖
9.下列有关物质性质和用途叙述均正确的是
A.甲醛具有还原性,可用于海鲜产品的保存
B.淀粉溶液遇会变蓝,可用于检验海水中是否含碘元素
C.蛋白质能水解,可供给人体营养
D.乙烯能被酸性高锰酸钾溶液氧化,可用浸泡过高锰酸钾溶液的硅藻土保鲜水果
10.《天工开物》中记载:“凡乌金纸由苏、杭造成,其纸用东海巨竹膜为质。用豆油点灯,闭塞周围,只留针孔通气,熏染烟光而成此纸”。下列说法错误的是
A.“乌金纸”的“乌”与豆油不完全燃烧有关
B.“巨竹膜”为造纸的原料,其主要成分是淀粉
C.豆油的主要成分油脂属于天然有机化合物
D.豆油可发生硬化、皂化等反应
11.GFP是一种能发光的荧光蛋白质,下列关于GFP的叙述合理的是
A.GFP在硫酸铜或饱和硫酸铵溶液中发生盐析,盐析是可逆过程
B.GFP在酸、碱或酶作用下发生水解,水解的最终产物氨基酸只能与碱反应
C.GFP在乙醇等作用下会凝结变性,变性是不可逆的
D.GFP与水的液态混合物可用盐析法分离,盐析法为化学方法
12.化学与人类生活、生产密切相关,下列说法中不正确的是
A.工业上利用油脂在碱性条件下水解生产肥皂
B.疫苗等生物制剂需要在低温下保存
C.淀粉、纤维素、蔗糖均属于高分子化合物且都能发生水解
D.脱氧核糖与碱基、磷酸基团共同组成脱氧核糖核苷酸
13.我国航天技术发展迅速,天宫、天和、天舟、巡天、问天、梦天、嫦娥、天问、神舟等体现了中国的强大科技力量,下列说法错误的是
A.“天问一号”火星车使用的热控保温材料纳米气凝胶可产生丁达尔效应
B.“嫦娥五号”月球车上的国旗是由优质高分子材料嵌入纤维制成的,纤维也属于高分子材料
C.“天宫二号”空间站使用了石墨烯存储器,石墨烯与金刚石互为同分异构体
D.“天和”核心舱使用了柔性三结砷化镓太阳能电池阵,砷化镓属于半导体
二、非选择题(共10题)
14.如图所示是一份体检报告,阅读后回答下列问题。
检验报告
血脂全套
项目名称 结果 参考值 单位 提示
甘油三酯 2.20 0~1.70 ↑
总胆固醇 5.50 <5.20 ↑
高密度脂蛋白胆固醇 1.56 0.9~2.0
低密度脂蛋白胆固醇 3.61 0~3.40 ↑
空腹血糖
项目名称 结果 参考值 单位 提示
空腹血糖 6.21 3.9~6.1 ↑
(1)查阅资料,了解所列检测项目对于人体生理活动产生的作用___________。
(2)针对检测结果,请对心血管系统疾病的潜在风险进行评估___________。
(3)如果这是你的体检结果,你会从饮食、运动等方面做出哪些调整___________?
15.某油脂厂废弃的油脂加氢镍催化剂主要含金属Ni、Al、Fe及其氧化物,还有少量其他不溶性物质。采用如下工艺流程回收其中的镍制备硫酸镍晶体(NiSO4·7H2O):
“碱浸”中NaOH的两个作用分别是___________
三、实验题
16.葡萄糖酸钙是一种有机钙盐,外观为白色结晶性或颗粒性粉末,无臭,无味,易溶于沸水,微溶于冷水,不溶于乙醇或乙醚等有机溶剂。葡萄糖酸钙临床上用于治疗骨质疏松症。实验室制备葡萄糖酸钙主要步骤如下:
I.葡萄糖酸溶液的制备
称取适量的葡萄糖[CH2OH(CHOH)4CHO],置于三颈烧瓶中,加入足量的溴水,在磁力搅拌器中沸水浴加热、搅拌得到无色透明的葡萄糖酸溶液。当氧化率达 80%以上时(60min),停止反应,把反应液冷却至 60-70℃待用。
Ⅱ.葡萄糖酸钙的制备
在搅拌下,分批加入足量的碳酸钙至葡萄糖酸溶液中。反应完全后,趁热用下图装置抽滤,得到澄清透明的葡萄糖酸钙溶液。将葡萄糖酸钙溶液转入 100ml 烧杯中冷却至室温,向烧杯中添加适量的无水乙醇,静置 10min 得到悬浊液,抽滤、洗涤、干燥得到白色的葡萄糖酸钙固体。
回答下列问题:
(1)步骤Ⅰ中,滴入溴水后,反应的化学方程式为_______。
(2)步骤 Ⅱ 中,判断碳酸钙已经足量的实验现象是_______。
(3)步骤Ⅱ抽滤时自来水流的作用是使瓶内与大气形成压强差,与普通过滤操作相比,抽滤的优点是_______;装置 B 的作用是_______。
(4)洗涤操作洗涤剂最合适的是________(填序号),理由是_______。
A.冷水 B.热水 C.乙醇
Ⅲ.葡萄糖酸钙中钙质量分数的测定
测定步骤:
(i)准确称取葡萄糖酸钙 m g,加入去离子水溶解,定容,配成 250mL 溶液。
(ii)用 c mol/L EDTA(H2Y2-)标准溶液润洗滴定管后,装入 EDTA 标准液,调至零刻度。
(iii)向 250mL 锥形瓶中加入 10mL 水、10mL NH3-NH4Cl 缓冲溶液和 5 mL 硫酸镁溶液。滴加 4 滴铬黑 T(HIn2-)指示剂,摇匀。用 EDTA 标准液滴定至终点。记录消耗的 EDTA 标准液的体积。
滴定过程中发生的反应如下:
Mg2+ + HIn2-(蓝色) MgIn-(酒红色)+ H+
Mg2+ + H2Y2- MgY2- + 2H+
MgIn-(酒红色)+ H2Y2- MgY2- + H+ + HIn2-(蓝色)
(iv)向上述锥形瓶中加入 25.00 mL 葡萄糖酸钙溶液,摇匀,继续用 EDTA 标准液滴定至终点,记录消耗的 EDTA 标准液的总体积。平行滴定三次,测得步骤 iii 中消耗 EDTA 标准液的平均体积为 V1 L,步骤 iv 中 EDTA 标准液的平均总体积为 V2 L。
已知:配合物的稳定常数类似于化学平衡常数,如反应 Fe3+ + 3SCN- Fe(SCN)3 的平衡常数可以看做是 Fe(SCN)3 的稳定常数 K稳,一般情况下,配合物的稳定常数越大,配合物越稳定,两种离子更容易结合。已知下列化合物稳定常数的大小顺序为 CaY2- > MgY2- > MgIn- > CaIn-,其中CaIn-的稳定常数很小,CaIn-不稳定,易导致滴定终点提前。
回答下列问题:
(5)步骤 iii 中加入硫酸镁的作用是_______。
(6)滴定终点的颜色变化为_______。
(7)步骤 iv 中,加入葡萄糖酸钙后发生反应的离子方程式为_______,_______。
(8)葡萄糖酸钙中钙的质量分数为_______。(用 V1、V2、m、c 的代数式表示)
17.为检验淀粉水解的情况,进行如下图所示的实验,试管甲和丙均用60~80 ℃的水浴加热5~6 min,试管乙不加热。待试管甲、丙中的溶液冷却后再进行后续实验。
实验1:取少量甲中溶液,加入新制氢氧化铜,加热,没有红色沉淀出现。
实验2:取少量乙中溶液,滴加几滴碘水,溶液变为蓝色,但取少量甲中溶液做此实验时,溶液不变蓝色。
实验3:取少量丙中溶液加入NaOH溶液调节至碱性,再滴加碘水,溶液颜色无明显变化。
(1)写出淀粉水解的化学方程式:___________。
(2)设计甲和乙是为了探究___________对淀粉水解的影响,设计甲和丙是为了探究___________对淀粉水解的影响。
(3)实验1失败的原因是___________。
(4)实验3中溶液的颜色无明显变化的原因是___________。
(5)下列结论合理的是___________(填字母)。
A.淀粉水解需要在催化剂和一定温度下进行
B.欲检验淀粉是否完全水解,最好在冷却后的水解液中直接加碘
C.欲检验淀粉的水解产物具有还原性,应先在水解液中加入氢氧化钠中和稀硫酸至溶液呈碱性,再加入新制氢氧化铜并加热
D.若用唾液代替稀硫酸,则实验1可能出现预期的现象
18.葡萄可用于酿酒。
(1)检验葡萄汁含葡萄糖的方法是:向其中加碱调至碱性,再加入新制备的Cu(OH)2,加热,其现象是____。
(2)葡萄在酿酒过程中,葡萄糖转化为酒精的过程如下,补充完成下列化学方程式:C6H12O6(葡萄糖)2___+2C2H5OH。
(3)葡萄酒密封储存过程中生成了有香味的酯,酯也可以通过化学实验来制备,实验室用如图所示装置制备乙酸乙酯:
①试管a中生成乙酸乙酯的化学方程式是___(请注明反应条件)。
②试管b中盛放的试剂是饱和____溶液。
③实验开始时,试管b中的导管不伸入液面下的原因是___。
④若分离出试管b中生成的乙酸乙酯,需要用到的仪器是___(填序号)。
a.漏斗 b.分液漏斗 c.长颈漏斗 d.恒压滴定漏斗
四、计算题
19.取30.0 g牛奶样品,将所含蛋白质中的氮元素全部转化为氨,用25.00 mL 1. 00 mo1/L的硫酸将其完全吸收,再加入19.00mL2.00 mol/L氢氧化钠溶液恰好生成硫酸钠和硫酸铵。请计算:
(1)样品中蛋白质转化生成的氨的物质的量为_______mo1。
(2)样品蛋白质中含氮元素的质量_______g。
(3)若蛋白质中氮元素的质量分数为14.0%,则样品中蛋白质的质量分数为_______。
20.有葡萄糖和麦芽糖的混合物90g,溶于足量的水中,在稀硫酸催化下充分反应后,用NaOH溶液中和水解液,再加入足量的Cu(OH)2悬浊液并加热煮沸,测得生成Cu2O沉淀为75.6g,求原混合物中麦芽糖的质量分数。
21.10g某天然油脂完全水解需要1.8gNaOH,1kg该油脂进行催化加氢,需消耗12g,才能进行完全。请推断1mol该油脂中平均含有碳碳双键的物质的量________。
22.某同学称取9 g淀粉溶于水,测定淀粉的水解百分率。其程序如下:
(1)各步加入的试剂为(写化学式):A________、B________、C________。
(2)若加入A溶液不加入B溶液_______(填“是”或“否”)合理,其理由是_______________。
(3)已知1 mol葡萄糖与新制Cu(OH)2悬浊液反应生成1 mol Cu2O,当生成1.44 g砖红色沉淀时,淀粉的水解率是________。
(4)某淀粉的相对分子质量为13 932,则它是由________个葡萄糖分子缩合而成的。
23.X由2种元素组成的离子化合物,阳离子与阴离子个数比为1∶2;无色气体B遇空气呈红棕色;C能使带火星的木条复燃;D为砖红色固体,E溶液呈强酸性。
(1)X的组成元素___________;X化学式___________。
(2)的离子方程式___________。
(3)反应转化过程中,生成时消耗葡萄糖的质量至少___________g。
(4)设计检验F溶液中溶质阴离子的实验方案_____。
参考答案:
1.B 2.D 3.D 4.B 5.D 6.C 7.C 8.D 9.D 10.B 11.C 12.C 13.C
14.(1)甘油三酯又称为中性脂肪,是甘油分子与脂肪酸反应所形成的脂类,为血脂的其中一种组成部分,具有为细胞代谢提供能量的功能;
总胆固醇为血液中各种脂蛋白所含胆固醇的总和,胆固醇是细胞膜的主要成分,同时也是合成肾上腺皮质激素、性激素、胆汁酸及维生素D等生理活性物质的重要原料;
高密度脂蛋白胆固醇测定为血脂检查的一项重要内容,该检查可帮助排查冠心病、动脉粥样硬化等疾病。高密度脂蛋白是由胆固醇、磷脂和蛋白质等物质组成的一种血浆脂蛋白,其主要在肝脏和小肠之中合成。具有将肝外组织内的胆固醇运送到肝脏进行分解代谢,排出体外的作用。
低密度脂蛋白是血浆中胆固醇含量占比最高的一类脂蛋白,为蛋白质、胆固醇和磷脂的复合体,是由极低密 度脂蛋白中的TG被水解代谢后转化而来,其主要功能是胆固醇存在于血液中的载体。血液中的低密度脂蛋白浓度过高、且未能被肝脏有效摄取,则可沉积于动脉内壁、促使动脉壁形成动脉粥样斑块,为动脉粥样硬化的致病性危险因素。
血糖是指血液中葡萄糖的含量,属于糖代谢检查,可用于筛查、诊断及监测糖尿病、低血糖症等多种糖代谢异常相关疾病,反映了机体对葡萄糖的吸收、代谢是否正常。血糖主要包括空腹血糖及餐后血糖两个检查指 标,检测空腹血糖时患者需要至少禁食8h以上,一般需隔夜空腹检查血糖,餐后血糖是指从进食第一口食物后开始计算时间至2h准时抽血测定血糖值。
(2)患有心血管疾病的风险较大
(3)加强体育健身锻炼,饮食以清淡低盐为主,加强果蔬、粗粮的摄入
15.除去油脂,溶解铝及其氧化物
16.(1)CH2OH(CHOH)4CHO+Br2+H2O=CH2OH(CHOH)4COOH+2HBr
(2)加入碳酸钙不再溶解且不再生成气泡
(3) 速率更快,且得到产品更干燥 起到安全瓶的作用
(4) C 葡萄糖酸钙不溶于乙醇,可减少产品的溶解损失
(5)指示滴定过程中颜色变化,确定加入EDTA 标准液的消耗量
(6)最后一滴EDTA 标准液加入后溶液酒红色褪色且半分钟内不变色
(7) Ca2++MgY2-=CaY2-+Mg2+ Mg2++ HIn2-= H++ MgIn-
(8)
17.(1)(C6H10O5)n+nH2OnC6H12O6
(2) 温度 催化剂
(3)没有加入碱中和作为催化剂的稀硫酸
(4)氢氧化钠与碘反应
(5)ABCD
18. 产生砖红色沉淀 CO2 CH3COOH+C2H5OHCH3COOC2H5+H2O Na2CO3 防止溶液倒吸 b
19.(1)
(2)0.168
(3)4%
20.95%
21.4mol
22.(1) H2SO4 NaOH Cu(OH)2
(2) 否 Cu(OH)2悬浊液与葡萄糖的反应必须在碱性条件下进行
(3)18%
(4)86
23.(1) Cu、N Cu(N3)2
(2)
(3)
(4)取少量F待测液于试管中,浓缩后加入浓与Cu片并加热,观察到红棕色气体,则待测液中含离子
